氨的理化性质及对人健康的影响
液氨的化学性质

液氨的化学性质液氨,又称为无水氨,是一种无色液体。
氨作为一种重要的化工原料,应用广泛,为运输及储存便利,通常将气态的氨气通过加压或冷却得到液态氨。
氨易溶于水,溶于水后形成氢氧化铵的碱性溶液。
氨在20℃水中的溶解度为34%。
液氨在工业上应用广泛,而且具有腐蚀性,且容易挥发,所以其化学事故发生率相当高。
为了促进对液氨危害和处置措施的了解,本文特介绍液氨的理化特性、中毒处置、泄漏处置和燃烧爆炸处置4个方面的基础知识。
一、氨的理化性质分子式:NH3 气氨相对密度(空气=1):0.59分子量:17.04 液氨相对密度(水=1):0.7067(25℃) CAS编号:7664-41-7 自燃点:651.11℃熔点(℃):-77.7 爆炸极限:16%~25%沸点(℃):-33.4 1%水溶液PH值:11.7蒸气压:882kPa(20℃)二、中毒处置(一)毒性及中毒机理液氨人类经口TDLo:0.15 ml/kg 液氨人类吸入LCLo:5000 ppm/5m 氨进入人体后会阻碍三羧酸循环,降低细胞色素氧化酶的作用。
致使脑氨增加,可产生神经毒作用。
高浓度氨可引起组织溶解坏死作用。
(二)接触途径及中毒症状1.吸入吸入是接触的主要途径。
氨的刺激性是可靠的有害浓度报警信号。
但由于嗅觉疲劳,长期接触后对低浓度的氨会难以察觉。
(1)轻度吸入氨中毒表现有鼻炎、咽炎、气管炎、支气管炎。
患者有咽灼痛、咳嗽、咳痰或咯血、胸闷和胸骨后疼痛等。
(2)急性吸入氨中毒的发生多由意外事故如管道破裂、阀门爆裂等造成。
急性氨中毒主要表现为呼吸道粘膜刺激和灼伤。
其症状根据氨的浓度、吸入时间以及个人感受性等而轻重不同。
(3)严重吸入中毒可出现喉头水肿、声门狭窄以及呼吸道粘膜脱落,可造成气管阻塞,引起窒息。
吸入高浓度可直接影响肺毛细血管通透性而引起肺水肿。
2.皮肤和眼睛接触低浓度的氨对眼和潮湿的皮肤能迅速产生刺激作用。
潮湿的皮肤或眼睛接触高浓度的氨气能引起严重的化学烧伤。
氨水特性及防护知识

氨水特性及防护知识1、氨水物化特性氨气是无色、有强烈刺激性气味的气体,在标准状况下,密度小于空气,易液化,在常压下冷却至-33.5℃或在常温下加压至700~800kPa,气态氨就液化成无色液体,液氨通常用作制冷剂,属于中毒类化合物,为易溶于水的碱性物质。
氨水是氨气溶于水得到的水溶液。
它是一种重要的化工原料,为一无色透明的液体,具有特殊的强烈刺激性臭味。
(1)刺激性:因水溶液中存在着游离的氨分子;(2)挥发性:氨水易挥发出氨气,随温度升高和放置时间延长而增加挥发率,且浓度增大挥发量增加;(3)不稳定性:见光受热易分解而生成氨和水;(4)弱碱性:氨水中水和氨能电离出OH-,所以氨水显弱碱性;(5)腐蚀性:氨水有一定的腐蚀作用,对铜的腐蚀比较强,钢铁比较差。
氨的化学性质2、危险特性常温常压下,氨水是不燃烧、无爆炸危险的液体,但在温度较高时,从氨水中分离的氨气具有强烈的气味、有毒、有燃烧和爆炸危险。
氨在空气中可燃,但一般难以着火,连续接触火源,且温度要在651℃以上才可燃烧。
氨气与空气混合物的浓度在15%~28%时,遇到明火会有燃烧和爆炸的危险,如果有油脂或其他可燃性物质,则更容易着火。
氨与强酸、卤族元素(溴、碘)接触发生强烈反应,有爆炸、飞溅的危险;氨与氧化银、汞、钙、氰化汞及次氯酸钙接触,会产生爆炸物质。
氨对铜、铟、锌及合金有强烈侵蚀作用,氨区需严格杜绝上述物质。
公司脱硝系统采用质量比为20%的氨水,该物质具有比较稳定的化学和物理性质,在运输和储存过程中危险系数相对较低。
脱硝系统中,氨气分子会通过泵(离心泵、螺杆泵等)的缝隙、管道焊缝缝隙、法兰密封端面缝隙、仪表与管道连接处的缝隙等处逸出;卸氨时,氨水车的顶盖是敞开的,会逸出氨气;氨水储罐顶盖处也可能会有氨气逸出。
针对上述氨气逸出点,为防止氨气爆炸,应禁止使用火柴、打火机、电焊机等明火设施。
氨气密度比空气小,常温常压下,由于密封不严而逸出的氨气会往罐顶部流动,因此在罐顶部位应禁止使用火柴、打火机、电焊机等明火设施,若需使用明火,应在空罐条件下操作。
氨水性质、安全措施

仅供参考[整理] 安全管理文书氨水性质、安全措施日期:__________________单位:__________________第1 页共6 页氨水性质、安全措施特别警示:有强烈刺激性氨味,有毒。
理化特性:外观与性状:无色透明液体。
氨溶于水大部分形成一水合氨,是氨水的主要成分(氨水是混合物),易挥发逸出氨气,有强烈的刺激性气味。
能与乙醇混溶。
呈弱碱性,能从空气中吸收二氧化碳,与硫磺或其他强酸反应时放出热,与挥发性酸放在近处能形成烟雾。
相对密度(d25):0.90。
有毒性,半数致死量(大鼠,经口)350mG/kG。
有腐蚀性,催泪性。
主要用途:分析试剂,中和剂,生物碱浸出剂。
用于某些元素(如铜、镍)的检定和测定,用以沉淀出各种元素的氢氧化物、制备铵化合物、洗涤剂。
军事上作为一种碱性消毒剂,用于消毒沙林类毒剂。
常用的是10%浓度的稀氨水(密度0.960),冬季使用浓度则为20%。
无机工业用于制选各种铁盐。
毛纺、丝绸、印染等工业用于洗涤羊毛、呢绒、坯布,溶解和调整酸碱度,并作为助染剂等。
有机工业用作胺化剂,生产热固性酚醛树脂的催化剂。
医药上用稀氨水对呼吸和循环起反射性刺激,医治晕倒和昏厥,并作皮肤刺激药和消毒药。
托电公司主要用于配置在线仪表药和炉内处理。
危害信息:【燃烧和爆炸危险性】不燃。
易分解放出氨气,温度越高,分解速度越快,可形成爆炸性气氛。
若遇高热,容器内压增大,有开裂和爆炸的危险。
【活性反应】第 2 页共 6 页氨水具有挥发性和不稳定性,具有碱通性,易分解放出氨气,温度越高,分解速度越快,可形成爆炸性气氛。
若遇高热,容器内压增大,有开裂和爆炸的危险。
稳定性:不稳定;禁忌物:酸类;燃烧(分解)产物:氨和水。
【健康危害】吸入后对鼻、喉和肺有刺激性引起咳嗽、气短和哮喘等;可因喉头水肿而窒息死亡;可发生肺水肿,引起死亡。
氨水溅入眼内,如不采取急救措施,可造成角膜溃疡、穿孔,并进一步引起眼内炎症,最终导致眼球萎缩而失明。
氨的理化性质及危险特性表

储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。应与氧化剂、酸类、卤素、食用化学品分开存放,切忌混储。采用防爆型照明、通风设施。禁止使用易产生火花的机械设备和工具。储区应备有泄漏应急处理设备。
运输信息
危险货物编号:32061 UN№:1170 ;
运输注意事项:采用钢质气瓶包装。本品铁路运输时限使用耐压液化气企业自备罐车装运,装运前需报有关部门批准。采用刚瓶运输时必须戴好钢瓶上的安全帽。钢瓶一般平放,并应将瓶口朝同一方向,不可交叉;高度不得超过车辆的防护栏板,并用三角木垫卡牢,防止滚动。运输时运输车辆应配备相应品种和数量的消防器材。装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。严禁与氧化剂、酸类、卤素、食用化学品等混装混运。夏季应早晚运输,防止日光曝晒。中途停留时应远离火种、热源。公路运输时要按规定路线行驶,禁止在居民区和人口稠密区停留。铁路运输时要禁止溜放。
506.62kPa(4.7℃)
溶解性
易溶于水、乙醇、乙醚
主要用途
用作制冷剂及制取铵盐和氮肥
健康
危害
侵入途径
吸入
健康危害
低浓度氨对粘膜有刺激作用,高浓度可造成组织溶解坏死。
燃烧爆炸危险特性
危险特性
与空气混合能形成爆炸性混合物。遇明火、高热能引起爆炸。与氟、氯等接触会发生剧烈化学反应。遇高热,容器内压增大,有开裂和爆炸的危险。
氨的理化性质及危险特性
标识
英文名:ammonia
危险性类别:第2.3类ห้องสมุดไป่ตู้毒气体
分子式:NH3
CAS号:7664-41-7
分子量:17.03
国标编号:23003
理化性质
外观与性状
氨气的理化性质及危险特性

氨气的理化性质及危险特性
1. 理化性质
- 化学式:NH3
- 分子量:17.03 g/mol
- 物态:气体
- 密度:0.589 g/L
- 沸点:-33.34°C
- 熔点:-77.73°C
- 溶解性:易溶于水
- 颜色:无色
- 气味:刺鼻气味
2. 危险特性
- 氨气具有较强的腐蚀性,能够直接腐蚀皮肤、眼睛和呼吸道黏膜。
- 高浓度的氨气在空气中能形成爆炸性混合物,具有爆炸和燃烧危险。
- 氨气在空气中比空气重,易于聚集在低洼处,对于密闭空间
可能存在窒息和窒息危险。
- 氨气可与氧化剂和酸类物质发生剧烈反应,产生火灾和爆炸。
3. 安全措施
- 在处理氨气时,应尽量避免其接触皮肤、眼睛和呼吸道,使
用防护手套、护目镜和防护面罩等个人防护装备。
- 在储存和搬运氨气时,应选择密闭,并保持通风良好的储存
环境,避免气体泄漏。
- 避免氨气与氧化剂和酸类物质接触,以防止发生火灾和爆炸。
- 在使用氨气时,应保持操作区域通风良好,避免气体聚集。
如发现气味异常,应立即离开操作区域并寻求专业人员帮助。
以上是关于氨气的理化性质及危险特性的基本信息,请在使用
或处理氨气时务必严格遵守相关安全规定,保障人身和环境安全。
氨溶液[含氨>10%]-理化性质及危险特性表
![氨溶液[含氨>10%]-理化性质及危险特性表](https://img.taocdn.com/s3/m/a523a41791c69ec3d5bbfd0a79563c1ec5dad7e1.png)
燃烧性
易燃
燃烧分解物
一氧化碳、二氧化碳。闪点(Βιβλιοθήκη )37爆炸上限(v%)
无资料
引燃温度(℃)
无资料
爆炸下限(v%)
无资料
危险特性
蒸气与空气能形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。放出有毒气体。易分解放出氨气,温度越高分解速度越快,可形成爆炸性气氛。与酸发生放热中和反应。与强碱反应放出有毒和易燃的氨气。与硫酸二甲酯发生剧烈反应。
泄漏处理
根据液体流动和蒸气扩散的影响区域划定警戒区,无关人员从侧风、上风向撤离至安全区。建议应急处理人员戴正压自给式呼吸器,穿防酸碱服,戴橡胶手套。穿上适当的防护服前严禁接触破裂的容器和泄漏物。尽可能切断泄漏源。防止泄漏物进入水体、下水道、地下室或限制性空间。小量泄漏:用干燥的砂土或其他不燃材料吸收或覆盖,收集于容器中。大量泄漏:构筑围堤或挖坑收容。用耐腐蚀泵转移至槽车或专用收集器内。
表
标识
中文名:氨溶液[含氨>10%];氨水
危险化学品目录序号:35
英文名:Ammonium hydroxide
UN编号:2672
分子式:NH4OH
分子量:35.05
CAS号:1336-21-6
理化性质
外观与性状
无色液体,有刺激性臭味。
熔点(℃)
-77
相对密度(水=1)
0.91
相对密度(空气=1)
0.6-1.2
储运条件
储存注意事项:储存于阴凉、通风的库房。远离火种、热源。库温不宜超过30℃。保持容器密封。应与酸类、金属粉末等分开存放,切忌混储。储区应备有泄漏应急处理设备和合适的收容材料。运输注意事项:铁路运输时,钢桶包装的可用敞车运输。起运时包装要完整,装载应稳妥。运输过程中要确保容器不泄漏、不倒塌、不坠落、不损坏。严禁与酸类、金属粉末、食用化学品等混装混运。运输时运输车辆应配备泄漏应急处理设备。运输途中应防曝晒、雨淋,防高温。公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。
液氨理化性质危险有害特性及应急防护措施

接触限值:中国MAC(mg/m3)30前苏联MAC(mg/m3)20
美国TVL-TWA OSHA 50ppm,34 mg/m3;ACGIH 25ppm,17mg/m3
美国TLV-STEL ACGIH 35ppm,24mg/m3
急性毒性:LD50350mg/kg(大鼠经口)LC501390mg/m3,4小时(大鼠吸入)
贮运
包装标志:6,7 UN编号:1005包装分类:Ⅱ包装方法:钢质气瓶。
储运条件:易燃、腐蚀性压缩气体。储存于阴凉、干燥、通风良好的仓间。远离火种、热源。防止阳光直射。应与卤素(氟、氯、溴)、酸类等分开存放。罐储时要有防火防爆技术措施。配备相应品种和数量的消防器材。禁止使用易产生火花的机械设备和工具。验收时要注意品名,注意验瓶日期,先进仓的先发用。槽车运送时要灌装适量,不可超压超量运输。搬运时要轻装轻卸,防止钢瓶和附件损坏。运输按规定路线行驶,中途不得停留。
个人防护:空气中浓度超标时,建议佩戴过滤式防毒面具(半面罩)。紧急事态抢救或撤离时,佩戴空气呼吸器;戴化学安全防护眼镜;穿防静电工作服;戴橡胶手套。工作现场禁止吸烟、进食和饮水。工作毕,淋浴更衣,保持良好的卫生习惯。
泄漏处理
迅速撤离泄漏污染区人员至上风处,并立即隔离150m,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿防毒服。尽可能切断泄漏源。合理通风,加速扩散。高浓度泄漏区,喷含盐酸的雾状水中和、稀释、溶解。构筑围堤或挖坑收容产生的大量废水。如有可能,将残余气或漏出气用排风机送至水洗塔或与塔相连的通风橱内。储罐区最好设稀酸喷洒设施。漏气容器要妥善处理,修复、检验后再用。
对人体危害
侵入途径:吸入。
健康危害:低浓度氨对粘膜有刺激作用,高浓度可造成组织溶解坏死。急性中毒:轻度者出现流泪、咽痛、声音嘶哑、咳嗽、咯痰等;眼结膜、鼻粘膜、咽部充血、水肿;胸部X线征象符合支气管炎或支气管周围炎。中度中毒上述症状加剧,出现呼吸困难、紫绀;胸部X线征象符合肺炎或间质性肺炎。严重者可发生中毒性肺水肿,或有呼吸窘迫综合征,患者剧烈咳嗽、咯大量粉红色泡沫痰、呼吸窘迫、谵妄、昏迷、休克等。可发生喉头水肿或支气管粘膜坏死脱落窒息。高浓度氨可引起反射性呼吸停止。液氨或高浓度氨可致眼灼伤;液氨可致皮肤灼伤。
氨气理化性质表

迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。呼吸、心跳停止,立即进行心肺复苏术。就医。
食 入
不会通过该途径接触。
5、消防措施
危险特性
与空气混合能形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。与氟、氯等接触会发生剧烈的化学反应。若遇高热,容器内压增大,有开裂和爆炸的危险。
有害燃烧产物
分解产物
氮氧化物
11、毒理学资料
急性毒性
LD50
350mg/kg(大鼠经口)
LC50
1390mg/m3/4h(大鼠吸入);2000ppm/4h
刺激性
家兔经眼:100mg,重度刺激
亚急性与慢性毒性
大鼠,20mg/m3,24小时/天,84天,或5~6小时/天,7个月,出现神经系统功能紊乱,血胆碱酯酶活性抑制等。
PC-STEL(mg/m3):30
TLV-C(mg/m3):—
TLV-TWA(mg/m3):
TLV-STEL(mg/m3):
监测方法
纳氏试剂分光光度法。
工程控制
严加密闭,提供充分的局部排风和全面通风。提供安全淋浴和洗眼设备。
呼吸系统防护
空气中浓度超标时,建议佩戴过滤式防毒面具(半面罩)。紧急事态抢救或撤离时,必须佩戴空气呼吸器。
致突变性
微生物致突变性:大肠杆菌 1500ppm/3小时。细胞遗传学分析:大鼠吸入19800μg/m3/16周。
致畸性
大鼠经口给予最低中毒剂量(TDL0)1680 mg/kg/24W-C,按照RTECS 标准可致胃肠道肿瘤。
12、生态学资料
生态毒性
半数致死浓度LC50:>3.58mg/l/24h(彩鲑,已受精的);>3.58mg/l/24h(彩鲑,幼年的);0.068mg/l/24h(彩鲑,85天的鱼苗);0.097mg/l/24h(彩鲑,成年的);24mg/l/48h(水蚤)
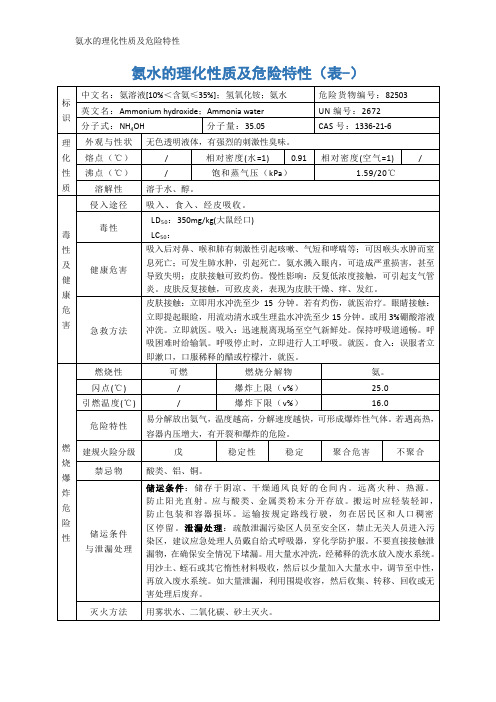
氨水的理化性质及危险特性
/
相对密度(水=1)
0.91
相对密度(空气=1)
/
沸点(℃)
/
饱和蒸气压(kPa)
1.59/20℃
溶解性
溶于水、醇。
毒性及健康危害
侵入途径
吸入、食入、经皮吸收。
毒性
LD5ห้องสมุดไป่ตู้:350mg/kg(大鼠经口)
LC50:
健康危害
吸入后对鼻、喉和肺有刺激性引起咳嗽、气短和哮喘等;可因喉头水肿而窒息死亡;可发生肺水肿,引起死亡。氨水溅入眼内,可造成严重损害,甚至导致失明;皮肤接触可致灼伤。慢性影响:反复低浓度接触,可引起支气管炎。皮肤反复接触,可致皮炎,表现为皮肤干燥、痒、发红。
氨水的理化性质及危险特性(表-)
标识
中文名:氨溶液[10%<含氨≤35%];氢氧化铵;氨水
危险货物编号:82503
英文名:Ammonium hydroxide;Ammonia water
UN编号:2672
分子式:NH4OH
分子量:35.05
CAS号:1336-21-6
理化性质
外观与性状
无色透明液体,有强烈的刺激性臭味。
燃烧爆炸危险性
燃烧性
可燃
燃烧分解物
氨。
闪点(℃)
/
爆炸上限(v%)
25.0
引燃温度(℃)
/
爆炸下限(v%)
16.0
危险特性
易分解放出氨气,温度越高,分解速度越快,可形成爆炸性气体。若遇高热,容器内压增大,有开裂和爆炸的危险。
建规火险分级
戊
稳定性
稳定
聚合危害
不聚合
禁忌物
酸类、铝、铜。
储运条件
与泄漏处理
氨的理化性质

液氨,又称为无水氨,是一种无色液体.氨作为一种重要的化工原料,应用广泛,为运输及储存便利,通常将气态的氨气通过加压或冷却得到液态氨.氨易溶于水,溶于水后形成氢氧化铵的碱性溶液.氨在20℃水中的溶解度为34%.液氨在工业上应用广泛,而且具有腐蚀性,且容易挥发,所以其化学事故发生率相当高.为了促进对液氨危害和处置措施的了解,本文特介绍液氨的理化特性、中毒处置、泄漏处置和燃烧爆炸处置4个方面的基础知识.一、氨的理化性质分子式:NH3 气氨相对密度(空气=1):0.59分子量:17.04 液氨相对密度(水=1):0.7067(25℃)CAS编号:7664-41-7 自燃点:651.11℃熔点(℃):-77.7 爆炸极限:16%~25%沸点(℃):-33.4 1%水溶液PH值:11.7蒸气压:882kPa(20℃)二、中毒处置(一)毒性及中毒机理液氨人类经口TDLo:0.15 ml/kg液氨人类吸入LCLo:5000 ppm/5m氨进入人体后会阻碍三羧酸循环,降低细胞色素氧化酶的作用.致使脑氨增加,可产生神经毒作用.高浓度氨可引起组织溶解坏死作用.(二)接触途径及中毒症状1.吸入吸入是接触的主要途径.氨的刺激性是可靠的有害浓度报警信号.但由于嗅觉疲劳,长期接触后对低浓度的氨会难以察觉. (1)轻度吸入氨中毒表现有鼻炎、咽炎、气管炎、支气管炎.患者有咽灼痛、咳嗽、咳痰或咯血、胸闷和胸骨后疼痛等. (2)急性吸入氨中毒的发生多由意外事故如管道破裂、阀门爆裂等造成.急性氨中毒主要表现为呼吸道粘膜刺激和灼伤.其症状根据氨的浓度、吸入时间以及个人感受性等而轻重不同.(3)严重吸入中毒可出现喉头水肿、声门狭窄以及呼吸道粘膜脱落,可造成气管阻塞,引起窒息.吸入高浓度可直接影响肺毛细血管通透性而引起肺水肿.2.皮肤和眼睛接触低浓度的氨对眼和潮湿的皮肤能迅速产生刺激作用.潮湿的皮肤或眼睛接触高浓度的氨气能引起严重的化学烧伤.皮肤接触可引起严重疼痛和烧伤,并能发生咖啡样着色.被腐蚀部位呈胶状并发软,可发生深度组织破坏.高浓度蒸气对眼睛有强刺激性,可引起疼痛和烧伤,导致明显的炎症并可能发生水肿、上皮组织破坏、角膜混浊和虹膜发炎.轻度病例一般会缓解,严重病例可能会长期持续,并发生持续性水肿、疤痕、永久性混浊、眼睛膨出、白内障、眼睑和眼球粘连及失明等并发症.多次或持续接触氨会导致结膜炎.(三)急救措施1.清除污染如果患者只是单纯接触氨气,并且没有皮肤和眼的刺激症状,则不需要清除污染.假如接触的是液氨,并且衣服已被污染,应将衣服脱下并放入双层塑料袋内.如果眼睛接触或眼睛有刺激感,应用大量清水或生理盐水冲洗20分钟以上.如在冲洗时发生眼睑痉挛,应慢慢滴入1~2滴0.4%奥布卡因,继续充分冲洗.如患者戴有隐形眼镜,又容易取下并且不会损伤眼睛的话,应取下隐形眼镜.应对接触的皮肤和头发用大量清水冲洗15分钟以上.冲洗皮肤和头发时要注意保护眼睛.2.病人复苏应立即将患者转移出污染区,对病人进行复苏三步法(气道、呼吸、循环):气道:保证气道不被舌头或异物阻塞.呼吸:检查病人是否呼吸,如无呼吸可用袖珍面罩等提供通气.循环:检查脉搏,如没有脉搏应施行心肺复苏.3.初步治疗氨中毒无特效解毒药,应采用支持治疗.如果接触浓度≥500ppm,并出现眼刺激、肺水肿的症状,则推荐采取以下措施:先喷5次地塞米松(用定量吸入器),然后每5分钟喷两次,直至到达医院急症室为止.如果接触浓度≥1500ppm,应建立静脉通路,并静脉注射1.0g甲基泼尼松龙(methylprednisolone)或等量类固醇.(注意:在临床对照研究中,皮质类固醇的作用尚未证实.)对氨吸入者,应给湿化空气或氧气.如有缺氧症状,应给湿化氧气.如果呼吸窘迫,应考虑进行气管插管.当病人的情况不能进行气管插管时,如条件许可,应施行环甲状软骨切开术.对有支气管痉挛的病人,可给支气管扩张剂喷雾,如叔丁喘宁.如皮肤接触氨,会引起化学烧伤,可按热烧伤处理:适当补液,给止痛剂,维持体温,用消毒垫或清洁床单覆盖伤面.如果皮肤接触高压液氨,要注意冻伤.三、泄漏处置1.少量泄漏撤退区域内所有人员.防止吸入蒸气,防止接触液体或气体.处置人员应使用呼吸器.禁止进入氨气可能汇集的局限空间,并加强通风.只能在保证安全的情况下堵漏.泄漏的容器应转移到安全地带,并且仅在确保安全的情况下才能打开阀门泄压.可用砂土、蛭石等惰性吸收材料收集和吸附泄漏物.收集的泄漏物应放在贴有相应标签的密闭容器中,以便废弃处理. 2.大量泄漏疏散场所内所有未防护人员,并向上风向转移.泄漏处置人员应穿全身防护服,戴呼吸设备.消除附近火源.向当地政府和“119”及当地环保部门、公安交警部门报警,报警内容应包括:事故单位;事故发生的时间、地点、化学品名称和泄漏量、危险程度;有无人员伤亡以及报警人姓名、电话.禁止接触或跨越泄漏的液氨,防止泄漏物进入阴沟和排水道,增强通风.场所内禁止吸烟和明火.在保证安全的情况下,要堵漏或翻转泄漏的容器以避免液氨漏出.要喷雾状水,以抑制蒸气或改变蒸气云的流向,但禁止用水直接冲击泄漏的液氨或泄漏源.防止泄漏物进入水体、下水道、地下室或密闭性空间.禁止进入氨气可能汇集的受限空间.清洗以后,在储存和再使用前要将所有的保护性服装和设备洗消.四、燃烧爆炸处置1.燃烧爆炸特性常温下氨是一种可燃气体,但较难点燃.爆炸极限为16%~25%,最易引燃浓度为17%.产生最大爆炸压力时的浓度为22.5%.2.火灾处理措施在贮存及运输使用过程中,如发生火灾应采取以下措施:(1)报警:迅速向当地119消防、政府报警.报警内容应包括:事故单位;事故发生的时间、地点、化学品名称、危险程度;有无人员伤亡以及报警人姓名、电话.(2)隔离、疏散、转移遇险人员到安全区域,建立500米左右警戒区,并在通往事故现场的主要干道上实行交通管制,除消防及应急处理人员外,其他人员禁止进入警戒区,并迅速撤离无关人员.(3)消防人员进入火场前,应穿着防化服,佩戴正压式呼吸器.氨气易穿透衣物,且易溶于水,消防人员要注意对人体排汗量大的部位,如生殖器官、腋下、肛门等部位的防护.(4)小火灾时用干粉或CO2灭火器,大火灾时用水幕、雾状水或常规泡沫.(5)储罐火灾时,尽可能远距离灭火或使用遥控水枪或水炮扑救.(6)切勿直接对泄漏口或安全阀门喷水,防止产生冻结.(7)安全阀发出声响或变色时应尽快撤离,切勿在储罐两端停留.。
氨水的理化性质及危险特性

氨水的理化性质及危险特性一、氨水的化学式和结构式氨水是一种无色、挥发性很强的液体,其化学式为NH3,结构式为:H|H-N- H|H二、氨水的理化性质1. 外观:无色、透明液体。
2. 气味:有刺激性气味。
3. 密度:0.91 g/cm³。
4. 熔点:-77.7℃。
5. 沸点:-33.34℃。
6. 溶解性:易溶于水,生成氢氧化铵,不溶于大部分有机溶剂。
7. pH值:10.8。
三、氨水的危险特性1. 有毒性:氨水能够直接对人体造成中毒,以及对鱼类、蛙类和其他生物的毒性很高。
长时间接触氨水会导致心力衰竭、中枢神经系统受损等。
2. 有刺激性:氨水具有较强的刺激性和腐蚀性,能够刺激眼睛、鼻腔和胃肠道等,引起生物反应,对人体造成伤害。
3. 燃爆性:氨水容易与空气中的氧气起反应,形成易燃的气体,因此,它具有一定的燃爆危险性。
在高温下或遇到明火、静电火花等内源火源时,就容易引发火灾。
4. 导电性:氨水具有一定的导电性,当与金属结构或其他楼道相接触时,能够导致电路短路或电气事故。
5. 化学反应:氨水与许多金属、无机酸、氧化剂等能够发生化学反应,在这些反应中所产生的气体有着很强的毒性和危险性。
6. 运输危险性:氨水属于危险品,运输时要按照有关法规进行包装、标签和处置,以防止泄漏和事故发生。
四、氨水的应用领域由于氨水在工业领域的应用广泛,因此需要注意掌握它的危险性。
以下是氨水在各个领域中的应用情况:1. 化学制品:氨水被广泛应用于生产化学品,特别是有机化合物的生产过程中,作为溶剂和催化剂使用。
2. 医药领域:氨水可以在医药领域中用作一种麻醉剂,但是由于其副作用较大很少使用。
3. 清洁剂:氨水溶液可以用作一种清洁剂,可以清洁水垢、油污、脂肪和各种污渍。
4. 食品防腐剂:氨水在食品加工领域中也能够起到一定的作用,可以用作一种防腐剂,能够延长食品的保存期限。
总之,氨水是一种广泛应用的化学品,我们需要了解它的理化性质和危险特性,并在使用中做好防范措施,保障我们的安全。
氨的理化性质

氨的理化性质、危害及应急处理知识1. 氨的理化性质和用途:分子式 NH3有毒气体沸点(℃) -33.5 易溶于水、乙醇、乙醚无色有刺激性恶臭的气体。
主要用途用做制冷剂及制取铵盐和氮肥。
储于耐压钢瓶或钢槽中由气态氨液化而得。
2. 燃烧爆炸特性:易燃、爆炸下限(%)15.7 爆炸上限(%)27.4 ,与空气混合能形成爆炸性混合物。
遇明火、高热能引起燃烧爆炸。
与氟、氯等接触会发生剧烈反应。
若遇高热,容器内压增大,有开裂和爆炸的危险。
3. 灭火方法:必须穿戴全身防火防毒服。
切断气源。
若不能立即切断气源,则不允许熄灭正在燃烧的气体。
喷水冷却容器,可能的话将容器从火场移至空旷处。
使用灭火剂:雾状水、干粉、二氧化碳、砂土。
4. 健康危害:吸入低浓度氨对粘膜有刺激作用,高浓度可造成组织溶解坏死。
高浓度氨可引起反射性呼吸停止。
5. 急救措施:皮肤接触,立即脱去被污染的衣着,应用2%硼酸液或大量清水彻底冲洗,就医。
眼睛接触,立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟,就医。
吸入迅速脱离现场至空气新鲜处,保持呼吸道通畅,如呼吸困难,给输氧,如呼吸停止,立即进行人工呼吸,就医。
6. 泄漏应急处理:迅速撤离泄漏污染区人员至上风处,并立即隔离150m ,严格限制出入。
切断火源。
建议应急处理人员戴自给正压式呼吸器,穿防毒服。
尽可能切断泄漏源。
合理通风,加速扩散。
漏气容器要妥善处理,废弃或修复、检验后再用。
爆炸下限(V%): 15.7 爆炸上限(V%): 27.4危险特性:与空气混合能形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。
与氟、氯等能发生剧烈的化学反应。
若遇高热,容器内压增大,有开裂和爆炸的危险。
燃烧(分解)产物:氧化氮、氨。
稳定性:稳定禁忌物:卤素、酰基氯、酸类、氯仿、强氧化剂。
聚合危害:不能出现灭火方法:切断气源。
若不能立即切断气源,则不允许熄灭正在燃烧的气体。
喷水冷却容器,可能的话将容器从火场移至空旷处。
氨气理化性质表
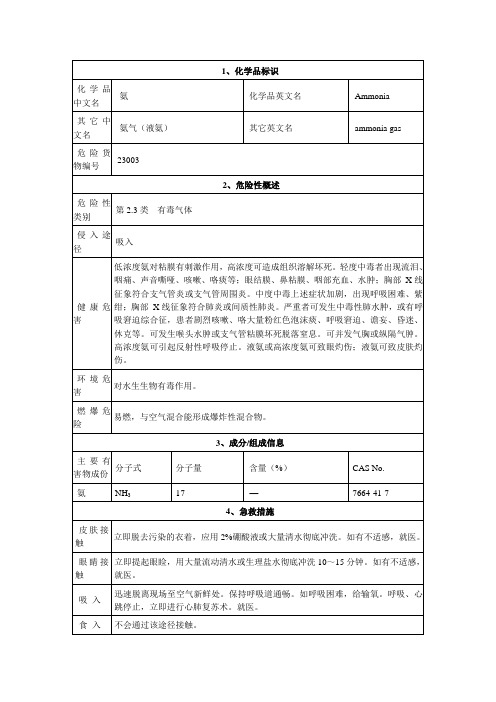
TLV-C(mg/m3):—
TLV-TWA(mg/m3):
TLV-STEL(mg/m3):
监测方法
纳氏试剂分光光度法。
工程控制
严加密闭,提供充分的局部排风和全面通风。提供安全淋浴和洗眼设备。
呼吸系统防护
空气中浓度超标时,建议佩戴过滤式防毒面具(半面罩)。紧急事态抢救或撤离时,必须佩戴空气呼吸器。
致突变性
微生物致突变性:大肠杆菌1500ppm/3小时。细胞遗传学分析:大鼠吸入19800μg/m3/16周。
致畸性
大鼠经口给予最低中毒剂量(TDL0)1680 mg/kg/24W-C,按照RTECS标准可致胃肠道肿瘤。
12、生态学资料
生态毒性
半数致死浓度LC50:>3.58mg/l/24h(彩鲑,已受精的);>3.58mg/l/24h(彩鲑,幼年的);0.068mg/l/24h(彩鲑,85天的鱼苗);0.097mg/l/24h(彩鲑,成年的);24mg/l/48h(水蚤)
506.62(4.7℃)
相对蒸汽密度(空气=1)
0.59
临界压力(MPa)
11.40
临界温度(℃)
132.5
引燃温度(℃)
651
爆炸上限%(V/V)
28
爆炸下限%(V/V)
15
溶解性
易溶于水、乙醇、乙醚。
主要用途
用作致冷剂及制取铵盐和氮肥。
10、稳定性和反应性
稳定性
稳定
聚合危害
不聚合
禁配物
卤素、酰基氯、酸类、氯仿、强氧化剂。
7、操作处置与储存
操作注意事项
严加密闭,提供充分的局部排风和全面通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴过滤式防毒面具(半面罩),戴化学安全防护眼镜,穿防静电工作服,戴橡胶手套。远离火种、热源,工作场所严禁吸烟。使用防爆型的通风系统和设备。防止气体泄漏到工作场所空气中。避免与氧化剂、酸类、卤素接触。搬运时轻装轻卸,防止钢瓶及附件破损。配备相应品种和数量的消防器材及泄漏应急处理设备。
氨的理化性质及对人健康的影响

4.1.7氨NH34.1.7.1理化性质氨,为常温、常压下具有特殊刺激性嗅味的气体,加压时易被液化为无色液体。
分子量17.032,密度0.597g/cm3,凝点-77.7℃,沸点-33.4℃,气体比重为0.596,液体比重为0.618。
易溶于水,其水溶液即为氨水,含氢氧化胺和氨,呈碱性。
1%溶液的PH值约为11.7。
与空气混合爆炸极限为15.5%~28%。
氨可由氮和氢在触媒作用下直接合成,氨与各种酸酐或酸类可直接生成铵盐。
4.1.7.2毒性氨主要作用于眼、鼻及呼吸系统,对粘膜产生刺激和腐蚀作用。
一般低浓度使眼结膜、鼻咽部和呼吸道粘膜充血、水肿等。
高浓度可使支气管粘膜坏死、脱落及损伤肺泡毛细血管壁,破坏肺泡表面活性物质,使肺泡上皮和毛细血管通透性增加,肺泡的气-血屏障破坏,使肺间质和肺泡过多渗出物,引起化学性肺炎和肺水肿。
人体对不同浓度的氨的毒性反应见表4-1表4-1人体对氨的毒性反应浓度(mg/m3)时间(mim)反应3500~700030立即死亡1750~450030危急生命70030立即咳嗽55330强烈刺激现象175~35028鼻、眼刺激、呼吸、脉搏加速140~21028有明显不适、恶心、头痛70~14030可以工作7030呼吸变慢67.245鼻咽刺激感9.845无刺激作用≥3.545可以识别气体0.745感觉到气味氨对神经系统的作用,表现为兴奋、惊厥、进而嗜睡,甚至昏迷。
4.1.7.3临床表现急性中毒为短时间内吸入高浓度氨气或直接接触液氨所致。
根据接触浓度和接触时间及个人感受性的不同,临床表现轻重不一。
1)氨气刺激反应仅有一过性眼和上呼吸道刺激症状,如流泪、咳嗽、咽痛、胸闷、气急、呕吐、头晕、头痛及咽和结膜充血等,肺部无明显阳性体征。
2)急性轻度中毒以气管、支气管损害为主,临床主要表现为支气管炎或支气管周围炎。
病人有流泪、羞明、视物模糊、咽干、咽痛、声音嘶哑、咳嗽、咳痰、胸闷及轻度头晕、头痛、乏力等,眼结膜充血,咽部充血、水肿,肺部有干性罗音或哮鸣音。
氨的理化性质及危险特性

氨的理化性质及危险特性
氨是一种常见的无机化合物,具有一系列的理化性质和危险特性。
本文将对氨的理化性质以及危险特性进行介绍。
理化性质
物理性质
- 氨是一种无色气体,具有刺激性气味。
- 氨在常温常压下是气态,熔点为-77.7摄氏度,沸点为-33.3摄氏度。
- 氨比空气轻,可以溶于水,溶液呈碱性。
化学性质
- 氨具有一定的还原性,可以与许多氧化剂反应。
- 氨与酸反应可以生成盐和水。
- 氨可以与一些金属形成配合物。
危险特性
氨具有一定的危险特性,需要注意以下几点:
1. 刺激性气味:浓度较高的氨具有刺激性气味,可能引起呼吸
道不适和眼睛刺激等问题。
在使用或工作中遇到浓度较高的氨气时,应采取适当的防护措施,避免吸入氨气。
2. 导致燃烧:氨具有较高的氧化性,与氧气或氧化剂接触时可
能引发火灾或爆炸。
在存储或处理氨气时,应避免与易燃物接触,
并保持良好的通风条件。
3. 强碱性:氨溶液具有强碱性,对皮肤和眼睛有腐蚀性。
在处
理氨溶液时,应穿戴防护手套、护目镜等个人防护装备,避免直接
与皮肤和眼睛接触。
4. 毒性:高浓度的氨气对人体有毒,可能会造成中毒症状。
因此,在接触氨气时应注意保持通风良好的环境,避免长时间暴露在
高浓度的氨气中。
结论
综上所述,氨具有一系列的理化性质和危险特性。
在使用和处理氨时,我们应当注意防护措施,避免吸入氨气、避免与易燃物接触,同时也要避免氨溶液对皮肤和眼睛造成腐蚀。
保持通风良好的环境也是避免中毒的重要措施。
氨的理化性质及危险特性
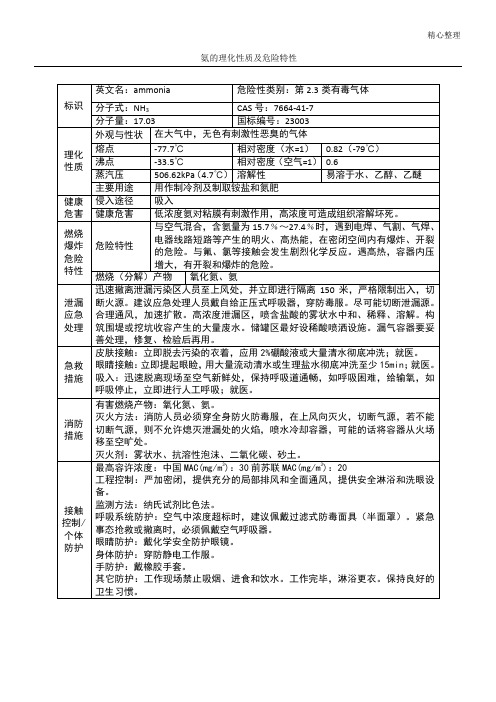
氨的理化性质及危险特性标识英文Fra bibliotek:ammonia
危险性类别:第2.3类有毒气体
分子式:NH3
CAS号:7664-41-7
分子量:17.03
国标编号:23003
理化性质
外观与性状
灭火剂:雾状水、抗溶性泡沫、二氧化碳、砂土。
接触控制/个体防护
最高容许浓度:中国MAC(mg/m3):30前苏联MAC(mg/m3):20
工程控制:严加密闭,提供充分的局部排风和全面通风,提供安全淋浴和洗眼设备。
监测方法:纳氏试剂比色法。
呼吸系统防护:空气中浓度超标时,建议佩戴过滤式防毒面具(半面罩)。紧急事态抢救或撤离时,必须佩戴空气呼吸器。
急救措施
皮肤接触:立即脱去污染的衣着,应用2%硼酸液或大量清水彻底冲洗;就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15min;就医。
吸入:迅速脱离现场至空气新鲜处,保持呼吸道通畅,如呼吸困难,给输氧,如呼吸停止,立即进行人工呼吸;就医。
消防措施
有害燃烧产物:氧化氮、氨。
灭火方法:消防人员必须穿全身防火防毒服,在上风向灭火,切断气源,若不能切断气源,则不允许熄灭泄漏处的火焰,喷水冷却容器,可能的话将容器从火场移至空旷处。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿防静电工作服。
手防护:戴橡胶手套。
其它防护:工作现场禁止吸烟、进食和饮水。工作完毕,淋浴更衣。保持良好的卫生习惯。
燃烧爆炸危险特性
危险特性
与空气混合,含氨量为15.7﹪~27.4﹪时,遇到电焊、气割、气焊、电器线路短路等产生的明火、高热能,在密闭空间内有爆炸、开裂的危险。与氟、氯等接触会发生剧烈化学反应。遇高热,容器内压增大,有开裂和爆炸的危险。
氨水的理化性质、对人体的危害、急救方法

氨水的理化性质、对人体的危害、急救方法基本性质性状:无色透明液体,有强烈的刺激性气味。
熔点:-77℃蒸汽压:1.59kPa(20℃)相对密度:氨含量越多,密度越小。
质量分数28%的氨水相对密度0.91,35%的0.88。
电离常数:K=1.8×10ˇ-5(25℃)稳定性:受热或见光易分解其它:极易挥发出氨气。
浓氨水对呼吸道和皮肤有刺激作用,并能损伤中枢神经系统。
具有弱碱性主要性质挥发性氨水易挥发出氨气,随温度升高和放置时间延长而增加挥发率,且浓度的增大挥发量增加。
腐蚀性氨水有一定的腐蚀作用,碳化氨水的腐蚀性更加严重。
对铜的腐蚀比较强,钢铁比较差,对水泥腐蚀不大。
对木材也有一定腐蚀作用。
弱碱性氨水中存在以下化学平衡:NH3+H2O=(可逆)=NH3·H2ONH3·H2O=(可逆)=NH4+ +OH-因此仅有一小部分氨分子与水反应而成铵离子NH4+和氢氧根离子OH-,故呈弱碱性。
氨水具有碱的通性:①能使无色酚酞试液变红色,能使紫色石蕊试液变蓝色,能使湿润红色石蕊试纸变蓝。
实验室中常用此法检验NH3的存在。
②能与酸反应,生成铵盐。
浓氨水与挥发性酸(如浓盐酸和浓硝酸)相遇会产生白烟。
NH3+HCl=NH4Cl (白烟)NH3+HNO3=NH4NO3 (白烟)而遇不挥发性酸(如硫酸、磷酸)无此现象。
实验室中可用此法检验NH3或氨水的存在。
工业上,利用氨水的弱碱性来吸收硫酸工业尾气,防止污染环境。
SO2+2NH3·H2O=(NH4)2SO3+H2O(NH4)2SO3+SO2+H2O= 2NH4HSO3氨极易溶于水的喷泉实验不稳定性[2]一水合氨不稳定,见光受热易分解而生成氨和水。
NH3·H2O=NH3↑+H2O实验室中,可用加热浓氨水制氨,或常温下用浓氨水与固体烧碱混合的方法制氨,其装置与操作简便,且所得到的氨气浓度较大,做“喷泉”实验效果更佳。
由于氨水具有挥发性和不稳定性,故氨水应密封保存在棕色或深色试剂瓶中,放在冷暗处。
氨的理化性质

液氨的理化性质1、液氨的理化特性外观与形状:无色有刺激性恶臭的气体熔点:-77.7℃沸点:-33.5℃相对密度:0.7714g/L 临界压力:11.40Mpa临界温度(℃):132.5溶解性:易溶于水、乙醇、乙醚2、氨的燃爆特性及健康危害燃烧性:易燃爆炸极限:15.7~27.4%引燃温度:651℃最大爆炸压力:0.580Mpa空气中最高允许浓度:30mg/m3建议火险登进:乙级危险性类别:第2.3类危险性:与空气混合能形成爆炸性混合物,遇明火高热能引起燃烧、爆炸。
与氟、氯等能发生剧烈化学反应。
若遇高热,容器内压力增大,有开裂和爆炸的危险。
灭火方法:消防人员必须穿戴全身防火防毒服。
切断气源,若不能立即切断气源,则不允许熄灭正在燃烧的气体。
喷水冷却容器,可能的话将容器从火场移至空旷处,灭火剂:雾状水、抗溶性泡沫、二氧化碳、砂土。
健康危害:低浓度氨对粘膜有刺激作用,高浓度可造成组织溶解坏死。
急性中毒:轻者出现流泪、咽痛、声音嘶哑、咳嗽、咯痰等,眼结膜、鼻粘膜、咽部充血、水肿;胸部x线征象符合支气管炎火支气管周围炎。
中度中毒上述症状加剧,出现呼吸困难、紫绀,胸部x 征象符合肺炎或间质性肺炎。
严重者可发生中毒性肺水肿,或有呼吸窘迫综合症,患者剧烈咳嗽、咯大量粉红色泡沫痰、呼吸窘迫、谵妄、昏迷、休克等。
可发生喉头水肿或支气管粘膜坏死脱落窒息。
高浓度氨可引起反射性呼吸停止。
液氨或高浓度氨可致眼灼伤,液氨可致皮肤灼伤。
3、氨的生理效应如下表所示空气中浓度(mg/m3)影响0.7 感到气味62.7 45分钟后鼻和眼有刺激感140 30分钟后眼和上呼吸道有不适,头痛175~350 20分钟呼吸和心跳加速700 咳嗽1750~4500 接触30分钟即有生命危险4500~7000 立即死亡。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4.1.7 氨NH3
4.1.7.1 理化性质
氨,为常温、常压下具有特殊刺激性嗅味的气体,加压时易被液化为无色液体。
分子量17.032,密度0.597g/cm3,凝点-77.7℃,沸点-33.4℃,气体比重为0.596,液体比重为0.618。
易溶于水,其水溶液即为氨水,含氢氧化胺和氨,呈碱性。
1%溶液的PH值约为11.7。
与空气混合爆炸极限为15.5%~28%。
氨可由氮和氢在触媒作用下直接合成,氨与各种酸酐或酸类可直接生成铵盐。
4.1.7.2 毒性
氨主要作用于眼、鼻及呼吸系统,对粘膜产生刺激和腐蚀作用。
一般低浓度使眼结膜、鼻咽部和呼吸道粘膜充血、水肿等。
高浓度可使支气管粘膜坏死、脱落及损伤肺泡毛细血管壁,破坏肺泡表面活性物质,使肺泡上皮和毛细血管通透性增加,肺泡的气-血屏障破坏,使肺间质和肺泡过多渗出物,引起化学性肺炎和肺水肿。
人体对不同浓度的氨的毒性反应见表4-1
表4-1 人体对氨的毒性反应
浓度时间反应
3500~7000 30 立即死亡
1750~4500 30 危急生命
700 30 立即咳嗽
553 30 强烈刺激现象
175~350 28 鼻、眼刺激、呼吸、脉搏加速
140~210 28 有明显不适、恶心、头痛
70~140 30 可以工作
70 30 呼吸变慢
67.2 45 鼻咽刺激感
9.8 45 无刺激作用
≥3.5 45 可以识别气体
0.7 45 感觉到气味
氨对神经系统的作用,表现为兴奋、惊厥、进而嗜睡,甚至昏迷。
4.1.7.3 临床表现
急性中毒为短时间内吸入高浓度氨气或直接接触液氨所致。
根据接触浓度和接触时间及个人感受性的不同,临床表现轻重不一。
1)氨气刺激反应仅有一过性眼和上呼吸道刺激症状,如流泪、咳嗽、咽痛、胸闷、气急、呕吐、头晕、头痛及咽和结膜充血等,肺部无明显阳性体征。
2)急性轻度中毒
以气管、支气管损害为主,临床主要表现为支气管炎或支气管周围炎。
病人有流泪、羞明、视物模糊、咽干、咽痛、声音嘶哑、咳嗽、咳痰、胸闷及轻度头晕、头痛、乏力等,眼结膜充血,咽部充血、水肿,肺部有干性罗音或哮鸣音。
3)急性中度中毒
临床表现为化学性肺炎或间质性肺水肿。
病人表现咽部烧灼痛、声音嘶哑、剧烈咳嗽、咳痰,有时痰中带血丝,胸闷、呼吸困难,伴有头晕、头痛、恶心、呕吐及乏力等。
眼结膜,咽部明显充血、水肿,甚至产生喉头水肿,呼吸快速、口唇及肢端紫绀,肺部有干、湿罗音。
4)急性重度中毒
以肺部严重损害为主,可伴有明显并发症,表现为严重的化学性
肺炎或肺泡性肺水肿。
病人表现剧烈咳嗽,咳出大量粉红色泡沫痰。
严重者甚至从鼻孔涌出大量粉红色泡沫样分泌物。
气急、胸闷、呼吸困难,心悸,明显紫钳,双肺布满干、湿罗音等。
4.1.7.4 处理
1)迅速将病人移离中毒现场,脱去被污染的衣物、注意保暖。
现场抢救时不宜用湿毛巾捂面,以免氨气遇水形成“强氨水”,而致面部皮肤灼伤。
2)合理吸氧,解除支气管痉挛,保持呼吸道畅通。
有呼吸抑制者,可给予呼吸中枢兴奋剂。
注意禁用加压呼吸。
防止肺水肿。
3)雾化吸入法:不论病情轻重,都可采用雾化吸入,常用处方为氨茶碱、地塞米松、抗生素、a糜蛋白酶等。
4.1.7.5 预防
严格执行安全操作规程,防止跑、冒、滴、漏。
