铝及铝合金
铝及铝合金分析

铝及铝合金分析铝在元素周期表中属ⅢA族,其相对原子质量为26.98154,密度2.6989g/cm3(20℃)。
纯铝呈银白色,具有良好的导电性、导热性、延展性及抗腐蚀性。
铝是典型的两性元素易,溶于盐酸和其他氢卤酸,也溶于强碱溶液不溶于冷的浓硫酸和硝酸。
铝易与氟化物、柠檬酸盐、酒石酸盐、乙二胺四乙酸二钠盐(EDTA)以及许多含氧、含氮有机试剂等生成稳定的结合物。
铝及铝合金的用途很广泛。
高纯铝抗腐蚀性强,可用来制造保存和运输硝酸、过氧化氢、甲醛、有机酸的器具,并在食品工业上用作包装材料。
纯铝可用于制造电缆、电线、电容器、整流器、汇流板等。
铝合金分为变形铝合金和铸造铝合金两大类。
变形铝合金根据其成分不同有防锈铝、硬铝、锻铝、超硬铝、特殊铝等;铸造铝合金根据成分不同有铝硅合金、铝铜合金、铝镁合金、铝锌合金等。
铝合金广泛用于航空工业、汽车工业、化工、机械制造工业以及民用建筑等。
在铝及铝合金中需要对Fe、Si、Cu、Ti、Ca、Mg、Mn、Zn、Pb、Ni、Cr、V、Sn、Zr、Ga、RE、Be、Sb、Li、B、Cd等元素进行测定。
根据上述元素含量的多少,选用不同的分析方法。
铝及铝合金中铁的测定一般采用邻菲罗啉分光光度法或原子吸收光谱法。
邻菲罗啉分光光度法是在pH2-9范围内,Fe2+与邻菲罗啉形成橙红色络合物,该方法有较高的灵敏度和良好的稳定性。
原子吸收光谱法选用较窄的通带,一般采用波长248.3nm处,在空气-乙炔氧化性火焰中进行测定。
对硅、镍、钒较高的试样,在测定时要加入一定量的锶盐消除其干扰。
铝合金中硅的含量大于1%时,一般采用重量法,近年来也采用改进的硅钼蓝分光光度法。
铝及铝合金中硅的含量小于1%的试样可采用硅钼蓝分光光度法。
溶液中,硅酸与钼酸盐形成黄色的硅钼杂多酸,它有两种形态,α-硅钼酸;β-硅钼酸。
通常分析中多采用β-硅钼酸形态,这是由于形成β-硅钼酸的酸度较高,避免某些较易水解元素的干扰,加入适当的还原剂,如抗坏血酸1-氨基-2-萘酚-4-磺酸等,由硅钼黄变成硅钼蓝。
【知识解析】铝和铝合金

铝和铝合金知识衔接◆铝是地壳中含量最多的金属元素。
根据金属活动性顺序可知,铝是一种活泼金属。
1 铝的原子结构铝的原子结构示意图为,Al-3e-===Al3+,在化学反应中表现还原性。
2 铝的物理性质3 铝和氧化铝的化学性质(1)铝与O2等非金属单质反应①常温下铝与O2的反应常温下,金属铝能被空气中的氧气氧化,表面生成一层致密的氧化铝薄膜,这层薄膜能阻止内部金属继续与氧气发生反应。
反应的化学方程式为4Al+3O2===2Al2O3。
②点燃条件下铝与O2的反应【实验操作】用镊子夹住一小团脱脂棉,蘸上一些铝粉,在酒精灯上点燃,并立即伸入盛有氧气的集气瓶中(瓶底放一些细沙),观察发生的现象。
【实验记录】点燃条件下,铝与O2可发生反应:4Al+3O22Al2O3可利用此反应制造燃烧弹、信号弹、火箭推进剂等教材延伸(1)铝箔在空气中加热不燃烧,只能熔化成液体但不滴落。
其原因是铝箔表面生成的高熔点的氧化铝包裹住内部熔化的铝,使内部的液态铝不能滴落。
熔点:2 054 ℃(2)铝与S、Cl2也能发生反应,反应的化学方程式分别为2Al+3S Al2S3和2Al+3Cl2 2AlCl3。
在Al与O2、S、Cl2的反应中,铝的化合价均由0变为+3,均作还原剂。
(2)教材P76·实验3-4氧化铝、铝与盐酸反应名师提醒(1)1 mol Al与盐酸完全反应,转移电子的物质的量是3 mol,同时生成1.5 mol H2。
(2)实验开始时不产生气泡,一段时间后产生气泡且速率由慢到快,这是因为开始时Al 表面的氧化铝薄膜参与反应但不产生H2,后来Al参与反应产生H2,随着反应的进行,温度升高,反应速率增大。
Al、Al2O3与酸的反应均放热(3)教材P76·实验3-5铝、氧化铝与NaOH溶液反应名师提醒(1)Al和Al2O3都既能与酸反应又能与碱反应。
像Al2O3这类既能与酸反应生成盐和水,又能与碱反应生成盐和水的氧化物,叫做两性氧化物。
铝及铝合金课件教学PPT

铝及铝合金的分类
01
02
铝及铝合金的牌号
铸造铝合金的牌号由3位数字组成,第一位数字表示主要合金元素,后两位数字表示合金元素的含量。
变形铝合金的牌号由1位数字和1位字母组成,数字表示主要合金元素(以265表示纯铝),字母表示加工状态(如F表示自由加工状态)。
铝的密度约为2.7g/cm³,铝合金的密度根据其成分和加工方法有所不同。
化学腐蚀
电化学腐蚀
应力腐蚀
在电解质溶液中,铝及铝合金作为阳极发生氧化反应,导致材料腐蚀。
在应力和特定环境共同作用下,铝及铝合金发生脆性断裂。
03
02
01
铝及铝合金的腐蚀机理
在铝及铝合金表面涂覆防腐蚀涂层,如油漆、清漆等,隔绝材料与外界环境的接触。
涂层保护
在铝及铝合金表面电镀一层耐腐蚀的金属,如锌、铬等,提高材料的耐腐蚀性。
密度
铝的硬度较低,可通过热处理提高其硬度。
硬度
铝是一种活泼的金属,容易与氧反应形成致密的氧化膜,具有良好的耐腐蚀性。
耐腐蚀性
铝具有良好的导电性,常用于电线、电缆等导电材料。
导电性
铝及铝合金的性能参数
04
CHAPTER
铝及铝合金的腐蚀与防护
铝及铝合金与空气中的氧气反应,生成氧化铝,导致材料表面被破坏。
铝合金
铝及铝合金的定义
铝及铝合金的特性
铝的密度约为2.7g/cm³,仅为铁的1/3,具有良好的轻量化效果。
铝具有良好的塑性变形能力,易于加工成各种形状。
铝的导电性能仅次于铜,广泛用于电线、电缆等领域。
铝表面容易形成致密的氧化膜,具有较好的耐腐蚀性。
密度小
延展性好
导电性好
铝及铝合金材料简介

铝及铝合金材料简介铝及铝合金材料简介一、铝的概述铝是一种轻质、有韧性、易于加工的金属,其密度仅为铁的三分之一。
铝的特点不仅体现在其物理性质上,而且在其化学性质上也非常稳定,不易被氧化、腐蚀甚至燃烧。
此外,铝价廉易得,是一种非常重要的工业原料,其用途广泛,特别是在航空、汽车及建筑等领域扮演着重要的角色。
二、铝的制备铝的制备有三种方法:电解法、渣法和气相法。
电解法:通过在氧化铝质量中加入氟化钠,将氧化铝溶于熔融的氟化钠中产生的电解铝的方法。
渣法:主要用于高氧化铝、重铝土矿、石墨的还原制铝。
该方法是将高氧化铝还原成铝金属的一种方法,是间接还原法。
使用低成本的能源和原料,对环境友好。
气相法:采用惰性气相还原高纯氟化铝的方法。
三、铝合金的概述铝合金是指铝与其他金属组合而成的一种金属材料,铝合金具有轻质、高强、抗腐蚀等优点,并可满足多种工业方面的需求,被广泛应用于航天、汽车、建筑等领域。
铝合金可以根据成分及应用领域被分为多种类型。
四、铝合金的种类1. 纯铝和低合金铝: 纯铝和低合金铝是最常见的铝合金,纯度为99%以上,具有良好的强度和可塑性。
2. 铝镁合金: 铝镁合金是由监金属镁和铝组成的合金,具有较高的强度和刚度,而且抗腐蚀性好,具有更好的耐腐蚀性能。
3. 铝锰合金: 铝锰合金由铝和锰组成,高强度、可塑性和抗腐蚀性强,常用于汽车结构材料。
4. 铝硅合金: 铝硅合金由铝、硅和其它杂质组成,热处理和加工性能很好,因此被广泛应用于模具、汽车零部件、建筑材料等领域。
5. 铝铜合金: 铝铜合金由铝和铜组成,具有高强度和高耐磨性,常用于制造高强度、轻量化构件。
五、铝合金的特点及优缺点铝合金主要优点:1.轻质:铝合金的密度为其他金属的三分之一,其轻量化的优点使其在燃油耗时,能够有效降低油耗,而且重量的轻量不会影响行驶的质量。
2.抗腐蚀性强:铝合金具有优异的抗腐蚀性强,这种特性使其材料在使用过程中受到自然环境和气候变化的影响也很小。
4.铝及铝合金术语

铝及铝合金术语A铝及铝合金的术语和定义由以下五个部分组成:1材料;2未压力加工产品;3压力加工产品;4工艺和处理方法;5板带箔产品缺陷(略)1 材料1.1 合金由基体金属元素(含量最大的元素)、合金元素及杂质所组成的一种金属物质。
1.2 合金元素为使金属具有某些特性,在基体金属中有意加入或保留的金属或非金属元素。
1.3 杂质存在于金属中的但并非有意加入或保留的金属或非金属元素。
1.4 变形合金主要通过塑性变形加工成产品的合金。
1.5 铸造合金主要用于生产铸件的合金。
1.6 中间合金仅作为加入料用于调节成分或控制杂质的合金。
1.7 热处理可强化合金通过适当的热处理能够强化的合金。
1.8 热处理不可强化合金仅冷加工能够强化而热处理不能明显强化的合金。
1.9 纯铝铝含量最少为99.0%并且其他任何元素的含量不超过下表规定界限值的金属。
元素 含量,%,不大于Fe+Si 1.0其他元素,每种 0.10注:①其他元素系指Cr、Cu、 Mg、 Mn、Ni、 Zn②如果铬和锰含量都不超过0.05%,铜含量允许为>0.10%~≤0.20%。
1.10 铝合金铝合金是金属物质,其铝的含量超过任何其他元素并符合下述任一条件: a.其他元素至少有一种元素的含量或铁加硅的含量超过上表规定的界限值。
b. 所有其他元素的总含量超过1.0%。
1.11 原生铝经还原或分解金属化合物所提炼的金属铝。
1.12 再生铝至少经过一次熔铸或加工并经回收和处理所获得的金属铝。
1.13 精铝用特殊冶炼方法获得的纯度不小于99.95%的金属铝。
2 未压力加工产品2.1 未压力加工产品经熔炼(或精炼)和铸造所获得的产品。
例如,轧制锭、挤压锭、锻造锭和重熔用锭。
2.2 轧制锭铸造成形并用于轧制生产的金属坯料。
2.3 重熔用锭经调节成分和(或)消除某些杂质(金属或非金属)的冶金处理,铸造成形并用于重新熔炼生产的金属坯料。
3 压力加工产品3.1 压力加工产品通过热和(或)冷塑性变形,例如:挤压、锻造、热轧、冷轧或拉伸等(这些加工方法可单独或联合采用),所获得的产品。
02铝及铝合金基础知识解析

5x52 合金牌号演化方式
52S (1933)
5052 (1954年重名命)
Si Fe Cu Mn Mg
Cr
0.25 0.40 0.10 0.10 2.2-2.8 0.15-0.35
5152 (1963) 非常用铝合金
5252 (1961) 低Fe; 不含Cr
汽车精饰镶边
5352 (1971) 不含Cr
铝及铝合金基础知识
品管培训课程
一
铝及铝合金应用
二 铝及铝合金基础知识
三
铝板带生产流程
四
铝板带产品介绍
第一章 铝和铝合金的应用
现如今铝合金在我们生活的各个方面都得到了广泛地应用
为什么用户会选择铝合金产品?
密度低
成型性好
导电性好
热传导率高
强度高
可焊接
表面光亮
抗腐蚀
隔绝气体
抗冲击性好
表面可喷漆或阳极氧化处理
合金系
区分号或纯度
从原始合金中发生了改变或 或杂质控制标准
1xxx 纯度为99.00%以上的纯铝 2xxx 以铜为主要合金元素的铝合金 3xxx 以锰为主要合金元素的铝合金 4xxx 以硅为主要合金元素的铝合金 5xxx 以镁为主要合金元素的铝合金 6xxx 以镁和硅为主要合金元素的铝合金 7xxx 以锌(和镁)为主要合金元素的铝合金 8xxx 以其它合金元素为主要合金元素的铝合金
铝及铝合金的材料特性及用途

铝及铝合金的材料特性及用途1.材料特性1.1 轻质高强:铝及铝合金的密度相对较小,大约为2.7g/cm³,仅为钢的1/3、尽管如此,铝及铝合金的强度却相当高,在常见金属中属于较高的强度。
这使得铝及铝合金在重量要求较低的应用中非常有用。
1.2良好的导电性:铝及铝合金具有优良的导电性能,仅次于铜。
这使得铝及铝合金经常被用作电导材料,如电力传输线、电力设备以及电子器件等。
1.3抗腐蚀性:铝及铝合金具有良好的抗腐蚀性。
铝表面易于与氧气发生反应生成氧化铝膜,这一薄膜可以有效地保护铝材的内部免受进一步的腐蚀侵蚀。
因此,铝及铝合金常用于需要抗腐蚀性能的应用,如飞机、汽车零部件、建筑材料等。
1.4良好可塑性:铝及铝合金具有良好的可塑性,可以通过挤压、拉伸、深成型等加工工艺将其制成各种形状的产品。
这种可塑性也使得铝及铝合金成为制造复杂零件的理想选择。
1.5可回收性:铝及铝合金是高度可回收的金属材料。
铝的回收过程不会破坏其结构和性能,因此,回收铝材所消耗的能量远低于新铝矿的提取和冶炼过程。
这使得铝及铝合金成为环保可持续发展的重要材料。
2.用途2.1建筑领域:铝及铝合金在建筑领域中具有广泛应用。
铝制窗框、门框、幕墙和屋顶覆盖等可轻松实现,且具有良好的抗腐蚀性和耐久性。
同时,铝材的轻质特性也有助于减少建筑物整体重量,减小地基压力。
2.2交通运输:铝及铝合金在交通运输行业中扮演重要角色。
铝制汽车零部件的使用可以显著减轻车辆重量,提高燃油效率。
同时,铝材的良好抗腐蚀性能也使其在航空航天工业中广泛应用,如飞机机身、翅膀、内饰等。
2.3包装行业:铝及铝合金也在包装行业中得到了广泛应用。
铝材制成的罐头盒可以有效保护食品和饮料的质量,并能延长其保质期。
此外,铝箔用于食品包装、药物包装等,具有良好的隔氧性和耐腐蚀性。
2.4电子领域:铝及铝合金在电子领域中被广泛使用。
铝制电缆、散热器和电子设备外壳具有良好的导电性和散热性能,可有效保护内部元器件的工作稳定性。
《铝及铝合金》课件

分享关于铝合金和其他材料组 合应用的案例,例如复合材料、 层叠板等。
六、铝合金的环保与回收利用
1
铝合金的可持续发展
讨论铝合金作为可持续发展材料的优势,并介绍相关的绿色生产工艺。
2
回收利用的意义和方法
探讨铝合金回收利用的重要性,以及回收利用的方法和技术。
3
铝合金回收利用的商业化前景
展望铝合金回收利用的商业化前景,如资源回收产业链和循环经济的发展。
七、结语
铝及铝合金的技术和应用发展前景
总结铝及铝合金的技术和应用现状,并展望其 未来的发展前景。
课程总结及展望
总结课程内容,以及对学生的启发和展望。
二、铝的制备
1
起源ቤተ መጻሕፍቲ ባይዱ发现
追溯铝的历史起源以及其最早被发现和应用的情况。
2
纯铝的制备方法
详细介绍通过氧化铝的还原和电解方法制备纯铝的过程和工艺。
3
工业生产中的制备方法
探讨工业生产中应用的其他铝制备方法,如焙烧法、溶剂法等。
三、铝的物理和化学性质
1
密度和熔点
介绍铝的密度和熔点,以及与其他金属相比的优势。
3
常见铝合金的组成和特点
列举常见铝合金及其具体成分与特点,如硬铝合金、耐蚀铝合金等。
五、铝合金的加工与应用
铸造、轧制、拉拔加 工
介绍铝合金常用的加工方法, 包括铸造、轧制和拉拔等,以 及各种加工方法的特点。
铝合金在航空、汽车、 铝合金异质材料的应
建筑等领域的应用
用案例
探索铝合金在航空器、汽车制 造、建筑结构等领域的广泛应 用及其优势。
《铝及铝合金》PPT课件
铝及铝合金课件,旨在分享有关铝及其合金的知识。探讨铝和铝合金的特点、 制备方法、物理和化学性质、分类、加工与应用、环保与回收利用等方面内 容。
铝及铝合金的基础知识

第一章铝及铝合金的基础知识第一节铝及铝合金的性质在有色金属中,铝是应用最广泛的一类金属。
其产量仅次于钢铁。
铝的发现,至目前还只有二百多年的历史。
但由于它具有资源丰富,生产成本低,用途广泛等特点,因此铝工业在近百年的时间内得到了迅猛的发展,随着科学技术的发展及人民生产水平的提高,铝箔应用也越来越广泛。
它已经渗透到了人们的日常生活中。
铝及铝合金的性质,概括起来,主要有以下几个方面:1比重小。
含铝量为99.5%的工业纯铝的比重为2.7克/立方厘米,只有铁和铜的三分之一左右。
2导电性好。
铝箔电阻系数(20℃)为2.67微欧毫米/米,相当于铜导电能力的60-65%。
但相同体积铝的重量只有铜的三分之一,因此按体积计算,铝的导电能力优于铜。
3良好的导热性。
铝箔导热系数(0-100℃)为0.54卡/厘米·秒·度,比铁的导热率约大三倍。
工业上许多热变换器散热材料,如目前很大的空调器散热片,都是铝及铝合金制成。
4强度高。
铝中加入少量的锰、镁、铜、铁等,具有良好的机械性能。
5良好的塑性。
适合于各种加工,可压成薄板可箔,拉成细丝,磨成细粉和挤压成复杂开头的型材。
6良好的抗腐蚀.性能。
纯铝在空气中,其表面会迅速跟氧结合,生成一层致密的氧化铝薄膜(AL2O3),此层致密的薄膜可以防止里面的铝继续氧化,对铝的内部起到保护作用。
7反射能力很强。
铝箔反射率在85%以上。
8铝具有银白色光泽、无毒、保鲜性好、防腐、防温、防干燥、不透气、不透光,因此,铝箔被广泛地用作各种食品、药用、香烟的包装上。
9焊接性能较差。
第二节铝及铝合金的牌号及状态铝及铝合金的牌号及状态以往都是采用国内统一的表示方法,即汉语拼音加顺序号,自96年起,这种表示方法已经停止使用,目前采用的是国际四位数字体系的表示方法。
1合金牌号合金牌号采用的是四位数字体系表示方法,其中:第一位代表合金的系列,如第一位数字为1,则代表为纯铝系列,第一位数字为2-8,则代表不同系列的铝合金。
铝及铝合金(2011.11.16)

• (2)除去镁粉中混有的少量铝粉,可选用 下列溶液中的( ) • A 盐酸 B 稀硝酸 • C 氨水 D 氢氧化钠溶液
• (3)铝分别与足量的稀盐酸和氢氧化钠溶 液反应,当两个反应放出的气体 相同状况 下体积相等时,反应中消耗的HCl和NaOH的 物质的量之比为( ) • A 1:1 B 2:1 C 3:1 D 1:3
观察与思考
实验1:取一块铝片,观察其表面的颜色。用镊 子将铝片的一端浸入装有稀盐酸的烧杯 中,静置一段时间后取出,观察现象。
实验2:用镊子将铝片的另一端浸入装有4 mol.L-1 氢氧化钠溶液烧杯中,静置一段时间后 取出,观察现象。
铝锅使用说明:盛放食物或水不要过夜,用后及 时洗净。酱、醋、盐、糖、酒等有酸、碱性的食 物,不宜在铝器皿内存放过久,以防腐蚀。
与某些金属氧化物反应
2Al + Fe2O3 == 2Fe + Al2O3
高温
铝热反应
用途:冶炼某些金属。
铝热反应用途
定向爆破
焊接钢轨
拓展
铝和某些盐溶液反应
根据金属活动性顺序的应用,铝能把排在它 后面的金属从它们的盐溶液中置换出来,如:
2Al+3Hg(NO3)2 =3Hg+2Al(NO3)3
铝与人体健康
*这节课你的收获是什么?
作业与思考 相关的练习
世界卫生组织提出人体每天的摄铝量不应 超过每千克体重1毫克,铝元素在人体中积累 可使人慢性中毒,1989年世界卫生组织正式将 铝确定为食品污染源之一加以控制。 试问在日常生活中有几种可能进入人体内?
铝锅使用说明:盛放食物或水不要过夜,用后及时洗净。 酱、醋、盐、糖、酒等有酸、碱性的食物, 不宜在铝器皿内存放过久,以防腐蚀。
铝及铝合金的特点

铝及铝合金的特点
铝及铝合金的特点包括:
1. 轻巧:铝的密度较低,约为钢的1/3,使其成为轻量级材料,适用于需要减重的领域,如航空航天、汽车制造等。
2. 耐腐蚀:铝具有一种紧密的氧化层,可以防止进一步的腐蚀。
因此,铝及其合金在恶劣环境中具有良好的耐腐蚀性,适用于海洋环境和化学工业等领域。
3. 导电性好:铝具有良好的导电性能,使其成为电子设备、电力输送和储存的理想材料。
4. 导热性好:铝具有优异的导热性能,使其广泛应用于散热器、汽车发动机和空调系统等领域。
5. 可塑性强:铝具有良好的可塑性,可以通过挤压、铸造、锻造等工艺加工成各种形状,满足不同应用需求。
6. 可回收利用:铝及其合金具有良好的再生性,可以重复回收利用,并且回收后的铝材质量基本不变,有助于减少资源浪费和环境污染。
7. 强度较低:与一些其他金属相比,铝的强度相对较低。
然而,通过合金化和热处理等工艺,可以显著提高铝合金的强度。
8. 容易与其他材料连接:铝可以与其他金属和非金属材料进行
连接,如焊接、铆接和粘接等,使其在多种工程应用中更易于使用。
铝及铝合金的基本特性

铝及铝合金的基本特性铝(Aluminum)是一种轻质、具有一定强度和良好的耐腐蚀性能的金属元素,是地壳中丰富的元素之一。
铝是一种可回收的金属,广泛应用于建筑、汽车、航空航天、电力等领域。
铝合金是铝和其他金属元素的化合物,其性质比纯铝更优异。
本文将介绍铝及铝合金的基本特性。
铝的物理和化学特性物理特性•质量密度:2.7 g/cm³•熔点:660.37 ℃•沸点:2519 ℃•热导率:237 W/(m·K)•热膨胀系数:2.34 × 10^-5 K^-1•电导率:37.7 × 10^6 S/m化学特性•化学符号:Al•原子序数:13•电负性:1.61•离子半径:0.053 nm•原子半径:0.143 nm其他特性铝是一种银白色的柔软金属,表面有一层致密的氧化层,可以防止进一步的氧化。
铝具有良好的可加工性、可塑性和延展性,可以通过轧制、拉伸、压铸等方式制成各种形状和尺寸的材料。
铝合金的分类铝合金是铝和其他金属元素的化合物,常用的合金元素包括铜、锌、镁、锆、硅等。
根据其成分和用途不同,铝合金可以分为多种类型,包括以下几类:系列分类•1000系列:纯铝,无添加其他合金元素。
常用于电力、建筑等领域。
•2000系列:铜为主要合金元素,也加入其他元素如镁等。
常用于航空航天、武器等领域。
•3000系列:铜和锌为主要合金元素,用于制造各种用途的容器和车身板等。
•4000系列:硅为主要合金元素,通常用于焊接应用。
•5000系列:镁为主要合金元素,强度和耐蚀性都很高。
常用于船舶、车身板等领域。
•6000系列:镁和硅是主要合金元素,具有较高的强度、耐腐蚀性和可加工性,常用于建筑、车辆等领域。
•7000系列:铝和锌为主要合金元素,常用于航空航天、运动用品等领域。
起运温度分类•非热处理型合金:起始运动温度低于不锈钢。
例如2A12、LY12等。
•热处理型合金:起始运动温度高于不锈钢。
例如7075、2024等。
铝及铝合金的材料及焊接性
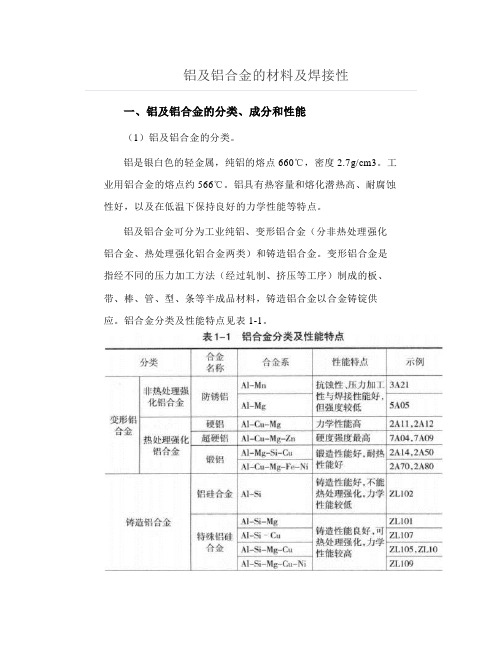
铝及铝合金的材料及焊接性一、铝及铝合金的分类、成分和性能(1)铝及铝合金的分类。
铝是银白色的轻金属,纯铝的熔点660℃,密度2.7g/cm3。
工业用铝合金的熔点约566℃。
铝具有热容量和熔化潜热高、耐腐蚀性好,以及在低温下保持良好的力学性能等特点。
铝及铝合金可分为工业纯铝、变形铝合金(分非热处理强化铝合金、热处理强化铝合金两类)和铸造铝合金。
变形铝合金是指经不同的压力加工方法(经过轧制、挤压等工序)制成的板、带、棒、管、型、条等半成品材料,铸造铝合金以合金铸锭供应。
铝合金分类及性能特点见表1-1。
按GB/T 3190—1996和GB/T 1674—1996的规定,纯铝和铝合金牌号命名的基本原则是:直接采用国际四位数字体系牌号;未命名为国际四位数字体系牌号的纯铝及其合金采用四位字符牌号。
四位字符牌号的第一位、第三位、第四位为阿拉伯数字,第二位为英文大写字母(如“A”)。
纯铝编号系统的第一位为“1”,如1xxx或1Axx,最后两位数字表示铝的纯度。
2xxx为Al-Cu 系;3xxx为Al-Mn系;4xxx为Al-Si系;5xxx为Al-Mg系;6xxx为Al-Mg-Si系;7xxx为Al-Zn系;8xxx为AI-其他元素系;9xxx为Al-备用系。
我国变形铝合金的牌号表示法与国际上的通用方法基本一致。
①工业纯铝。
工业纯铝含铝99%以上,熔点660℃,熔化时没有任何颜色变化。
表面易形成致密的氧化膜,具有良好的耐蚀性。
纯铝的导热性约为低碳钢的5倍,线胀系数约为低碳钢的2倍。
纯铝强度很低,不适合做结构材料。
退火的铝板抗拉强度为60~100MPa,伸长率为35%~40%。
②非热处理强化铝合金。
非热处理强化铝合金通过加工硬化、固溶强化提高力学性能,特点是强度中等、塑性及耐蚀性好,又称防锈铝,原代号LFxx。
Al-Mn合金和Al-Mg合金属于防锈铝合金,不能热处理强化,但强度比纯铝高,并具有优异的抗腐蚀性和良好的焊接性,是目前焊接结构中应用广泛的铝合金。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第八章铝及铝合金第一节铝的合金化及铝合金的分类铝是地壳中蕴藏量最多的金属元素,铝的总储量约占地壳总量的7.45%。
铝及铝合金的产量在金属材料中仅次于钢铁材料而居于第二位,是有色金属材料中用量最多、应用范围最广的材料。
一、纯铝的特性铝是第三周期第ⅢA族元素,原子序数为13,常见化合价为+3,原子量为26.9815,原子直径为0.286nm。
固态铝是一种具有面心立方晶格的金属,无同素异构转变。
主要物理性能参数见表8-1。
纯铝是一种具有银白色金属光泽的金属。
不仅密度低、导电性和导热性好,而且还具有塑性好、抗腐蚀性能高的特点。
铝的化学性质虽然很活泼,但在空气中易与氧结合,在金属的表面形成一层致密的稳定的氧化铝薄膜,可保护内层金属不再继续氧化,所以金属铝在大气中具有极好的稳定性。
固态纯铝的塑性极好,在室温下纯度为99.99%的纯铝的延伸率可达50%,但纯铝的强度相当低,只有45MPa。
纯铝的低温性能良好,在0℃~-253℃之间其塑性和冲击韧性均不降低。
纯铝除易于铸造和切削加工成形外,还可通过冷、热压力加工支撑不同规格的半成品。
此外,纯铝还具有很好的焊接性能,可采用气焊、氩弧焊等焊接方法进行焊接。
表8-1 纯铝的主要物理性能性能参数性能参数性能参数点阵结构fcc 热膨胀系数 2.3×10-5/K(20℃)熔点 660.4℃点阵常数 4.0496×10-10m(25℃) 导热系数 2.37W/(cm•K)(25℃)沸点 2477℃固态密度 2.72g/cm3电阻率 2.655×10-8Ω•m 熔化热10~147kJ/mol表8-2 重熔用铝锭、重熔用精铝锭的牌号及化学成分(GB/T8644-2000,GB/T1196-1993)化学成分牌号Al杂质不大于不小于Fe Si Cu Zn Ti Ca Mg 其他杂质每种总和Al99.996 99.996 0.0010 0.0010 0.0015 0.001 0.001 0.001 0.004Al99.993 99.993 0.0015 0.0013 0.0030 0.001 0.001 0.001 0.007Al99.99 99.99 0.0030 0.0030 0.0050 0.002 0.002 0.001 0.040.002 0.005 0.05 Al99.95 99.95 0.02 0.02 0.01 0.0050.080.0300.030 0.015 0.150.0050.12Al99.8599.85Al99.80 99.80 0.15 0.10 0.01 0.03 0.03 0.02 0.20 Al99.70 99.70 0.20 0.13 0.01 0.03 0.03 0.03 0.30 Al99.60 99.60 0.25 0.18 0.01 0.03 0.03 0.03 0.40 Al99.50 99.50 0.30 0.25 0.02 0.03 0.05 0.03 0.50 Al99.00 99.00 0.50 0.45 0.02 0.05 0.05 0.05 1.00 工业纯铝采用熔盐电解,即利用直流电以冰晶石为溶剂在950℃~970℃电解氧化铝的方法制取,所得到的工业电解纯铝经三层熔液电解法制得工业高纯铝。
如果再使用区域熔炼或有机溶液电解法冶炼工业高纯铝可制取纯度在99.999%以上的高纯铝,最高纯度可达99.99995%。
工业纯铝的主要用途是配制铝基合金,高纯铝则主要应用于科学试验、化学工业和其它特殊需求。
此外,纯铝还可以用来制造电线、铝箔、屏蔽壳体、反射器、包覆材料、化工容器和日用炊具等产品,是目前有色金属中应用最多的一种材料。
常用铝锭的牌号及化学成分如表8-2所示。
工业纯铝中含有少量杂质,主要为Fe 和Si ,它们在铝中的溶解度很小,形成富Fe 、Si 的脆性化合物,虽能提高铝的强度,但却严重损害铝的塑性、抗腐蚀性和导电性,除杂质元素外,纯铝的力学性能还与其加工状态有关。
二、铝的合金化工业纯铝的强度和硬度都很低,虽然可以通过冷作硬化的方式强化,但是也不能直接用于制作结构材料。
因此必须进行合金化,目前制造铝合金的常用合金元素大致可分为主加元素和辅加元素。
主加合金元素有Si 、Cu 、Mg 、Mn 、Zn 和Li 等,这些元素的单独加入或配合加入,可以获得性能各异的铝合金以满足各种工程应用的需求。
辅加元素有Cr 、Ti 、Zr 、Ni 、Ca 、B 和RE 等,其目的是进一步提高铝合金的综合性能,并改善铝合金的某些工艺性能。
由于固态铝没有同素异构转变,因此不能象钢那样借助于热处理相变强化。
合金元素对铝的强化作用主要表现为固溶强化、沉淀强化、过剩相强化及细化晶粒强化。
1.固溶强化合金元素加入铝中首先可以溶入铝中形成铝基置换固溶体。
这将导致铝的晶格发生畸变,增加了位错运动的阻力,由此提高了铝的强度。
合金元素对铝的固溶强化能力同其本身的性质及固溶度有关。
表8-3给出了一些合金元素在铝中的极限溶解度和室温溶解度数据。
其中,Zn 、Ag 、Mg 的溶解度较高,可以超过10%;其次是Cu 、Li 、Mn 、Si 等,它们的溶解度大于1%;其余各元素在铝中的溶解度则不超过1%。
表8-3一些合金元素在铝中的极限溶解度和室温溶解度由此可见,合金元素加入到铝中一般都形成有限固溶体,如Al-Cu 、Al-Mg 、Al-Si 、Al-Mn 、Al-Li 二元合金均为有限固溶体。
通常,对于同一元素而言,在铝中的固溶度越高,那么获得的固溶强化效果就越高。
但在实际应用中,也并非固溶度越高越好,因为在一些简单的二元铝合金中,如Al-Zn 、Al-Ag 系合金,由于组元间具有非常相似的物理化学和原子尺寸,因而固溶体的晶格畸变程度较低,所以提高固溶度导致固溶强化的效果并不十分显著。
这也是铝合金的强化不能单纯依靠合金元素的固溶强化的原因。
2.沉淀强化加入的合金元素除固溶在铝基体中外,就是以第二相的形式存在。
由于某些合金元素在铝中具有较大的固溶度,且固溶度随温度降低而急剧减小的特点,因此可以通过将溶有一定合金元素的铝合金加热到某一温度后快冷,得到过饱和固溶体,通常把这种工艺称为固溶处理(也称淬火)。
必须注意的是,这种过饱和固溶体和碳溶于铁中的过饱和固溶体(马氏体)不同。
因为合金元素溶于铝中形成的过饱和固溶体是置换型的过饱和固溶体,引起的晶格畸变不大,因此这种过饱和固溶体的强度不是很高,而塑性仍然很好。
碳溶于铁形成的过饱和固溶体即马氏体是间隙型过饱和固溶体,不仅引起的晶格畸变较大,而且还和位错形成柯垂耳气团;同时包含了新的强化机制(如前指出的细晶强化、位错强化等)。
溶解度(%) 溶解度(%)溶解度(%)合金元素 极限 室温 合金元素极限 室温合金元素 极限室温Zn 82.2 4.0 Cu 5.60.1Si 1.650.17Ag 55.5 0.7 Li 4.20.85Cr 0.40.002Mg 17.4 1.9 Mn 1.80.3Ca 0.60.3对于过饱和的铝基固溶体,如果将其放置在室温或加热到某一温度,则基体中过饱和的溶质原子可与基体金属铝或其它合金元素以沉淀相呈弥散状析出。
显然这个第二相的析出会合金的强度、硬度增加,塑性和韧性将下降。
这个过程通常称为时效。
铝合金的时效强化的强化效果不仅与第二相的形状、尺寸大小、数量和分布有关,而且最重要的取决于第二相的结构和特性。
因此,对铝合金进行合金化的合金元素,不仅要求能在铝中有较高的极限溶解度和明显的温度关系,而且还要求在沉淀过程中能形成均匀、弥散的共格或半共格过渡强化相,因为这类强化相在铝基体中可造成较强烈的应变场,增加对位错运动的阻力。
必须指出的是,铝合金中常用的主加元素Cu、Mg、Zn、Si、Mn等在铝中虽然都有较高的极限溶解度,并且溶解度的大小随温度的下降而急剧减小,但是除铜以外,就它们与铝的二元合金而言,沉淀相的强化作用不够明显。
这是因为它们与铝形成的沉淀相或因共格界面错配度低而使相应的应变场减弱,或因预沉淀阶段短,很快与基体丧失共格关系而形成非共格的平衡相。
如MnAl6相和Mg5Al8相就不具有沉淀强化效果。
因此为了充分发挥沉淀强化的效能,铝合金中的通常还加入第三或第四合金组元,以形成多种沉淀强化相。
如表8-4所示。
表8-4 铝合金中几种沉淀相的沉淀顺序合金系脱溶沉淀的顺序平衡沉淀相Al-Cu G.P.区(圆盘)→θ′′(圆盘)→θ′θ(CuAl2)Al-Ag G.P.区(球形)→γ′(片状)γ(Ag2Al)Al-Li G.P.区(球形)→δ′δ(AlLi)Al-Mg-Si G.P.区(棒状)→β′′→β′(杆状)β(Mg2Si)Al-Cu-Mg G.P.区(棒或球)→S′S(Al2CuMg)Al-Zn-Mg G.P.区(球)→η′(片状)η(MgZn2)3.过剩相强化当铝合金中加入的合金元素超过其溶解度极限时,合金在淬火加热时便有一部分不能溶入铝基固溶体中而以第二相的形式出现,称为过剩相。
这些过剩相多为硬而脆的金属间化合物,它们在铝合金中能够起阻碍位错滑移和运动的作用,从而提高铝合金的强度和硬度。
铝合金中的过剩相在一定限度内,数量愈多,其强化效果愈好,但合金的塑性和韧性却下降。
铸造铝合金为获得良好的铸造性能,一般希望合金成分接近共晶成分,共晶成分的铸造合金就是利用共晶中的第二相作为过剩相来强化铝合金的。
如二元铝硅合金中的过剩相即为共晶中的硅晶体。
在该合金中随着硅含量的增加,硅晶体的数量增多,合金的强度及硬度相应提高。
当合金中的硅含量超过共晶成分时,由于过剩相数量过多以及多角形的板块初晶的出现,导致合金的强度和塑性急剧下降。
因此对于二元铝硅合金,一方面要限制硅含量,一般不超过共晶成分太多;另一方面,通过采用变质处理,加入钠盐变质剂,使共晶合金中的硅晶体细化呈细粒状,获得最佳的强度、硬度和良好的塑性、韧性的配合。
此外,在铝铈合金中,也是利用过剩相Al4Ce起强化作用的,所以铝铈合金具有较高的高温强度和良好的铸造性能。
4.细晶强化细晶强化除了上述细化过剩相外,还可在铝合金中加入微量合金元素Ti、Zr、稀土等,形成难熔的金属间化合物,在合金结晶过程中起非自发形核核心的作用,细化铝基固溶体的晶粒,产生细晶强化。
如铝合金中加入加入微量的Ti 、Zr 可形成高熔点的TiAl 3、Al 3Zr 等即可作为铝基固溶体α相结晶的非自发核心而细化α相晶粒。
锰和铬加入铝合金中形成MnAl 6和Al 12Mg 2Cr ,稀土金属加入铝合金中形成金属间化合物Al 4RE 均可作为细化晶粒的第二相。
需要指出的是,稀土元素加入铝合金中,还能起到脱氧和脱硫的作用,降低铝合金中的夹杂物含量起净化作用;稀土元素与硅、铁等杂质元素形成化合物,降低这些杂质的固溶量,从而降低了铝的电阻率,对提高铝导线的质量有重要作用。
