2008浙江高考化学评分细则(来自阅卷小组)
2008年高考理综Ⅱ化学试题评析

构 中的元素周 期律 与周期 表 、晶体 、分子 与原 子的
结构 的 内容 ( 8 题 、题 1 、题 2 等1 1 7 、氧化 还 原反 应 ( 1) 题 2 、电化学 中 的电解 知识 ( 1) 题 0 、化学平 衡 知
()试题 中 的基 础 知 识 能够 具 有较 好 的选 拔功 3 能 。 试 卷 中许 多 试 题 的设 计 从 基 础 入 手 .环 环相 扣 ,层 层深 入 ,使 试题 具有 较好 的 区分度 和选 拔功 能 ,在考查 基础 知识 的 同时也从 另一 面考查 了学生
3 化学具 体 考题详 解 与点评
31 选 择 题 .
的物质 问的转化 、同分 异构 体知 识点 的考查 等 。
2 考查学 生的科 学素养 借助 化学试题 考查 学生 的科 学素养 ,其 具体 表
现如下 :
试 题6 0 8 北 京 奥 运会 的 “ 云 ” 火炬所 :2 0 年 祥 用 的燃料 的 主要成 分是 丙烷 .下 列有关丙 烷 的叙述 中不正确 的 是 f1
S 、C一 r、I O 1 、B~ 一 等离 子 的鉴 别 问题 :有机 化学试
题中 ( 9 题2 、题 6 ,也 是 中学 化 学 中经 典 、常 见 、 ) 基 础的有 机反应基 本类 型 的考 查 、常见 的不 同类 型
的计算 、化 学平衡 、物 质 的水解 等知识 .另外 还通 过 已知 图表 ,考查 了考 生 的观察 能力 和思维 品质。
重 能力和 素质的考 查 ,命 题依 据 《 教学 大纲 》 ,但
不 拘泥于 《 教学大 纲》 ,不过 分强调 知识 的覆 盖面 , 因为试卷 长度 有 限 ,无法 也不 必追 求知识 点 的覆盖
2008年全国各地高考卷非选择题部分中化学计算题考查内容的特色分析

n C 一)= . 0 l与 C 一和 OH一 ( Oi = 0 0 5mo , 0; = 反应 的 H 的 总 物 质 的 量 为 : .0 2 mo/ × 0 4 5 一 lL .0 2 L 0 0 5mo, 以 ( . 8 l所 OH一 =0 0 o , 们 的 物质 ) . 8t l它 o 的量之 比为 :6: 。 1 1
该 碱式盐 中氢 元 素 的 质量 分 数 为 0 0 0 试 推测 该 . 4, 碱 式盐 的化学式 。
的计算 都集 中在 了选择 题 部分 。另 外 ,08年 计算 20 题题型设 计灵 活 , 景 多变 , 情 内容 丰 富多 彩 , 点 突 重 出, 凸现 了能力 考查 。还有 , 些计算题 的呈 现形式 这
显示 了多样化 , 出现 了大量 以数 据 、 图表 、 流程 图 、 关
[ 解析] 12 () 片小苏打所含 N HC 。 a O 的质量为
1g其 物质 的量为 , 由 HC 一+ H+一 03
” H ) 0 0 2m o 。 ( 一 . 1 l
一0 o2mo, ・1 1 C 十 + H2 可 知 O 0,
0H一 C _与 H+ 和 0; 反应 生成 H O和 HC O , 以 所
( O ̄) . lLX0 0 2 一0 0 5mo, HC - 一2 0mo/ . 0 5L . 0 l即
等 的计算 20 年全 国各 地 高 考 化 学 计 算 题 注重 对 物 质 08
化学式 、 结构式 、 结构简式等中学化学中最基本的化 化来自学教育
2 0 第 1 期 0 8年 I
20 0 8年全 国各地 高 考卷 非选择 题部 分 中 化 学计 算题 考查 内容 的特 色分 析
08高考考试说明出炉 名师解析——化学

08高考考试说明出炉名师解析——化学2008年高考化学考试说明明确将教育部《普通高中课程方案》、《普通高中课程标准》、江苏省《普通高中课程标准教学要求》及本说明做为命题依据;明确提出“有所创新、有所突破”;其余并没有太大变化。
素养与能力要求:几乎没有新的变化;化学基础知识与技能要求层次:单列为一项,用具体的行为动词进行了较为清晰明了的说明与界定,没有出现特别新鲜的内容;考试范围与内容:单列为一项,这是考生最值得关注的一项,分为“必考内容”与“选考内容”两部分。
1、原“不要求写复杂的电极反应式”一说改为“能写出常见的简单电极反应和电池反应方程式”;2、原“不要求掌握胶体电泳的性质” 一说改为“胶体的渗析、凝聚、布朗运动和电泳的性质不作要求”;3、增加了“活化能、焓变、熵变、平衡常数计算”等内容,删除了“两种或两种以上条件同时改变对化学平衡的影响不作要求”一说;4、明确说明“弱酸弱碱盐的水解不作要求”;5、明确删除了“磷元素单质及其化合物的主要性质和重要应用”;6、将“烷烃命名限于5个碳原子以内”改为“能根据有机化合物的命名规则命名简单的有机物”;7、明确说明“不包括立体异构”;8、实验部分内容的说明比07年更加具体、详细。
1、将“掌握1至20号元素的结构示意图”的原要求更改为“掌握1至36号元素原子的核外电子排布”,并相应增加了第一电离能、电子能层、原子轨道等相应的配套考点;2、明确要求掌握σ键、π键相关知识但对σ键、π键的相对强弱的比较不作要求;3、增加了极性分子相关内容;4、增加了杂化轨道理论和价层电子对互斥理论的简单应用方面的要求但对有d轨道参与杂化及AB5型以上的复杂构型不作要求;5、明确了将“等电子理论”列为考试内容;6、明确说明“配合物的空间构型和中心原子的杂化类型不作要求”;7、08说明删除了“分子内氢键及相关性质暂不要求掌握”一说但对氢键的相对强弱不作要求;1、增加了层析实验;2、增加了三谱的简单应用;3、其它相关要求不再细评。
高考化学《评分细则》参考发布

2020高考化学《评分细则》参考发布(附电子版))一、赋分原则1.化学用语的“规范化”给分原则化学专用名词中出现错别字(甚至白字)都要参照标准扣分。
化学方程式、离子方程式未配平、条件错误或不全等都不给分(包括反应物或生成物的系数非最小公倍数或分数等均视为不规范而不给分)。
“Δ”“↑”“↓”“”“===”、反应条件等均应正确使用。
2.易于辨识,修正清楚原则凡是辨别不清的,皆为“0”分。
答题时,字不一定要很漂亮,但须十分清晰。
不能过分潦草,难以辨认。
有两种情况存在,其一是学生在修改答案时,改动不够坚决和清楚,如由A改成B,由B又改成D,中间修改不清楚,难以辨认;其二是不排除考生有投机心理,让评卷老师去猜。
另外有些学生开始答卷(题)时,没有把握,用铅笔答题,最后未用0.5 mm黑色签字笔圈定,3.“不许越线”原则答错位置或答题超出答题卡标出的划定界限时,由于测试内容过多,而评卷时又需切割4.“白纸黑字”原则即凡是答题卡上写了的就有,没有写的就没有。
只有认定答题卡上的白纸黑字所表达的内容信息,才能真正做到公平公正地评分。
5.“见空给分”原则在连续多个答案中,为了便于操作,通常采用“独立操作,互不牵连”的原则,即前面一个答案正确与否,不影响后面答案的给分;同理,如前者正确,而后面错误,也按步骤照样给分。
6.无机化学按要求分毫不差高标准(1)严格按要求给分:填空要求填什么就写什么,答非所问者按“0”分处理。
(2)元素符号的书写:一定要符合规范要求,其中包括原子序数、原子量、电荷数、化合价以及同位素的表示等。
(3)化学方程式的问题:反应物和生成物的系数,气体或沉淀的符号,反应物与产物两边用等号或可逆号连接,反应条件等均应完全正确。
(4)综合题高分策略技巧7.有机化学严规范应得尽得最全面(1)结构式:如苯环、双键、羧基、醛基、羰基、羟基等均要求按教材规范书写,尤其要注意出现在某一中心结构左边的基团。
(2)H(氢)、O(氧)或其他元素、其他基团与C(或其他元素)成键时,连接位置必须准确。
浙江省化学高考考试说明的解读

5、常见金属元素Cu及化合物的性质及 应用; 6、树立绿色化学思想; 7、了解确定有机化合物结构的化学方 法和某些物理方法。能举事实说明有机 分子中基团之间存在相互影响。结合实 际了解某些有机化合物对环境和健康可 能产生的影响,关注有机化合物的安全 使用。
.
考纲中弱化的内容有:
1、了解胶体是一种常见的分散系(聚溶和 制备不作要求);
4444444
444440440411011112
4444444444444
444444444
.
鬢驳浟蟳颐幕楩閯縵镀猠歨閒 卨鴉蹚骠喓盼纣秥申僤嫷羭慨 噤崹
54545454 哥vnv
国国
合格和韩
和环境和交换机及环 境和交换机
歼击机
版本vnbngnvng
.
畬鉀渥这皚吠呵躹萋玨祈鑇版 漂咋桤鴥槰鷏謈绀亓縒橍譗髅 鎊肖
hhhjkjkj
斤斤计较就
.
繚臭鐣匼伡頗藷顺訳峽貭崐耢 裿雨釞鏞蝎善叺鑭觠啼兲暜腛 佽蓞
天 的 44 天 琐 呵 哈呵 哈呵
呵 呵 呵 哈
.
癏漯汹昜扙葀摷逿敉剥钠佯黂 恖议涹龚各郅胖攬瞵陊祶琢璶 螲崞
天 的 44 版 天 44 本
哈呵 哈呵 哈呵
2、题型稳定,知识覆盖突出主干,强调核心知识。 3、能力要求相对稳定,平衡过渡。 4、命题素材:立足课标,关注应用。
.
初步理解:
主体
稳定
局部
创新
1、新课程理念融入考试大纲中。
2、内容出现了化学学科特点和研究基本方法。
3、模块结构与知识体系得到有机结合。
4、实验化学得到较大强化。
5、计算分散,融合到相关知识模块中。
更突出对中学化学基础知识的融会贯通,对有关 感性知识进行初步加工、吸收、有序存储的能力, 更全面、更具体地考查学生能否运用科学方法,初 步了解化学变化规律,科学地分析问题和解决问题 的能力。
2008年理综评分28题细则

2008年理综28题评分细则(13分)一、基本原则(1)化学反应方程式书写正确。
要求反应物、产物完整,化学式正确规范。
错写分子式、不配平、漏写+、方程式配平但没化为最简,则方程式不得分。
(2)原则上,同一类笔误错误不重复扣分。
(3)回答问题,阐述原因语言文字明确,体现一定因果关系。
(4)第2、4小题,若判断错误,则后续原因阐述不得分。
若未作判断,后续原因阐述正确,只得原因部分得分。
二、各小题细则(1)(2分)关键字答“氧”、“O”均可得分;其他答案不得分。
(2)(3分)答出“不需要”结论得2分;回答出原因,“因为有N2不断通入”或“b瓶溶液不会倒吸至a管”或“因为有N2不断通入,b瓶溶液不会倒吸至a管”等相同意义答案均得1分。
若判断错误,则后续原因阐述不得分。
若未作判断,后续原因阐述正确,只得原因阐述部分得分,1分。
(3)(4分)写出“MO + C = M + CO ”“MO + CO = M + CO2”“CO2 + C = 2CO ”“2MO + C =2 M + CO2”每个方程式正确得1分,共4分。
其中错写分子式、不配平、漏写+、方程式配平但没化为最简,则该方程式不得分;漏写反应条件、“=”以“→”或“-”代替、漏写气体符号,不扣分;书写多于四个方程式,以书写正确方程式为准。
注:方程式中金属符号以例如:“K”“Ca”“Na”“Mg”“Al”“Fe”“Cu”“Zn”“Hg”等碱金属及碱土金属以及中学教材明确氧化物颜色与题目不符的元素替代,方程式不得分;以“M”或“Pb”“Sn”等其他金属替代,方程式正确的,不扣分。
(4)(4分)答出“需处理”结论得2分;回答出原因,“因为含有CO,可连接一个加热的装有CuO粉末的反应管”或“因为含有CO,可连接一个气囊收集反应气体”或“因为含有CO,可点燃反应残气”等相同意义答案均得2分。
若原因阐述矛盾,例如:“因为含有CO,可连接一个加热的装有CuO粉末的2反应管”,则本步骤不得分。
2008年浙江省高中学生化学竞赛试题(A组)参考答案和评分标准

2008年浙江省高中学生化学竞赛试题(A 组)参考答案和评分标准一.选择题(本题包括10小题,每小题4分,共40分。
每小题只有一个选项符合题意。
)1.B 。
2.C 。
3.B 。
4.A 。
5.D 。
6.D 。
7.C 。
8.C 。
9.A 。
10.D 。
二.选择题(本题包括8小题,每小题4分,共32分。
每小题可能有1或2个选项符合题意,若有2个正确选项,只选1个且正确给2分,多选、错选都给0分。
)11.AB 。
12.B 。
13.AC 。
14.AD 。
15.C 。
16.BC 。
17.CD 。
18.AD 。
三.本题共包括2小题,共20分19.(11分)(1)ABD (3分,选C 倒扣1分,只选C 得0分)(2)+3NaOH ++NaCl+H 2O (3分,反应物、产物中只要写错一种或漏写都不给分,不配平扣1分)(3)5(2分)(3分,其它形式的结构简式不给分)20.(9分) (1)CH 3COOCH 2CH 2CH 3(1分)(2)2CH 3CH 2CH 2OH+O 22CH 3CH 2CHO+2H 2O (2分)(3)①CH 3CHO (1分) ②酯化反应(或取代反应)(1分)③nCH 2=CHCOOH CH 2(2分)④CH 3COOH+NH 3CH 3COOH+HCl或CH 3COOH+3NH 3CH 3COONH 4+NH 4Cl (2分) 四.本题包括2小题,27分。
21.(每空2分,共14分)(1)⑥ ⑧ ⑩(2)使茶叶灰分中的钙、铁、铝等难溶化合物转化成可溶性氯化物在pH=6~7左右时加热至沸30min 可保证Fe 3+、Al 3+完全沉淀除去溶液中的Fe 3+离子,防止Fe 3+干扰铝元素的检验(其它合理解释也可给分)(3)Fe 3++3OH -=Fe(OH)3↓ Al 3++3OH -=Al(OH)3↓(2分,写成AlO 2-不给分)22.(13分)(1)甲 乙 50mL 碱式滴定管(每空1分,3分)(2)D 、E 、G (3分,全对给分)。
2008年高考考试大纲(新课标)化学

2008年高考卷考试说明(课程标准实验版)-化学为了指导和规范我国2008年高考工作,便于广大考生了解考试要求,国家教育招生委员会命题办公室以教育部颁布的各学科课程标准和《2008年普通高等学校招生全国统一考试大纲(课程标准实验版)》为依据,在充分调查研究、广泛听取意见和建议的基础上,紧密结合我国的高中教学实际和普通高等学校招生工作实际,制定了《2008年普通高等学校招生全国统一考试(课程标准实验版)考试说明》(以下简称《考试说明》)。
《考试说明》以党的十七大精神为指导,认真贯彻胡锦涛总书记在十七大报告中所提出的“更新教育观念,深化教学内容方式、考试招生制度、质量评价制度等改革,减轻中小学生课业负担,提高学生综合素质”的总要求。
《考试说明》坚持有利于高等学校选拔优秀学生,有利于中学推进素质教育和课程改革,有利于考试公平、公正、科学、规范、安全有效的原则,力求在2007年高考的基础上,保持相对稳定,体现新课程的理念和要求,体现我国的教育教学实际。
因此,2008年高考考试内容要与高中新课程内容相衔接,进一步贴近时代、贴近社会、贴近考生实际,注重对考生运用所学知识发现问题、分析问题、解决问题能力的考查。
(一)考试能力要求1.接受、吸收、整合化学信息的能力(1)能够对中学化学基础知识融会贯通,有正确复述、再现、辨认的能力。
(2)能够通过对实际事物、实验现象、实物、模型、图形、图表的观察,以及对自然界、社会、生产、生活中的化学现象的观察,获取有关的感性知识和印象,并进行初步加工、吸收、有序存储的能力。
(3)能够从试题提供的新信息中,准确地提取实质性内容,并经与已有知识块整合,重组为新知识块的能力。
2.分析问题和解决(解答)化学问题的能力(1)能够将实际问题分解,通过运用相关知识,采用分析、综合的方法解决简单化学问题的能力。
(2)能够将分析解决问题的过程和成果用正确的化学术语及文字、图表、模型、图形等表达,并作出解释的能力。
分析2008年高考全国试卷理综化学试题阅卷

2008年高考全国试卷Ⅱ理综化学试题阅卷分析葛小元席桂平孟淑娟李金莲高艳君第一部分试卷结构与考查内容评析:中等难度。
由pH值判断碱过量,设原酸碱溶液的浓度均为c, 由过量碱并结合中和反应酸碱计量关系和物质的量浓度概念列式计算得结果。
失分原因:掌握相关概念不牢固不能应用,不善于设未知量找到切入点列式计算。
选择题10、考点:电解池——阴、阳离子放电(顺序)——电极产物(量)及现象。
评析:中等难度。
判断出电极,由离子放电顺序判断出各电极的产物及量,由离子浓度变化推断出各电极附近溶液的酸碱性及产生的现象,逐项排除。
失分原因:不能判断电极及产物(量),不熟悉离子放电顺序无法确定何种离子浓度减少。
选择题11、考点:质量数(A)=质子数(Z)+中子数(N);物质的量概念、字母型计算。
评析:中等难度。
由原子结构知识确定1molHmX的质子数,再根据物质的量概念计算a克该物质的质子数(注意一定要用题中已知字母列算式)。
失分原因:原子结构(同位素)概念模糊, 字母型计算不熟练。
选择题12、考点:氧化还原反应概念及配平方法(原子守恒、电子守恒)。
评析:中等难度。
根据各物质化学式判断变价元素,由已知各物质列化学方程式并根据电子守恒和原子守恒配平,由方程式中各物质的计量数选择答案。
失分原因:没有判断出只有部分N元素的化合价发生变化,不会从右边把方程式配平。
选择题13、考点:在T、V不变条件下的等效化学平衡概念。
可逆反应无论从任何方向开始反应达到平衡,折算为同一物质进行比较其结果,与反应途径无关。
评析:较难。
根据可逆反应方程式(计量数、状态)及题表的含义,利用化学平衡中的等效平衡知识进行各物质的某方向极量转换,比较各物质的量,从而确定平衡时CO物质的量,比较得结果。
失分原因:没有掌握等效平衡概念,不会进行物质的极量转换和进行相应判断。
非选择题26、考点:化学反应热、书写热化学方程式及简单的化工生产知识。
(1)书写热化学方程式。
最新08年全国高考理综化学部分评析

平衡的影响。
12.已知乙酸(HA)的酸性比甲酸(HB)弱, 在物质的量浓度均为0.1mol/L的NaA和NaB混 合溶液中,下列排序正确的是
A.c(OH-)>c(HA)>c(HB)>c(H+)
B. c(OH-)>c(A-)>c(B-)>c(H+)
考生在解题时容易出现连贯性错误,一旦方程式 书写错误,特别是配平错误,将直接导致列式计 算的错误,会造成大量失分。
26题评分细则:(本题共16分)
(1)3MnO2+6KOH+KClO3 = 3K2MnO4+KCl+3H2O (3分) 化学方程式中各化学式符合题意并全对,但方程式未配平得2分,
3×87
2×158
2.5×80%
m
列比例求解,得m=2.4g
则KMnO4的理论产量是2.4g
本小题3分,写出正确的计量关系MnO2--KMnO4得2 分,计算结果正确得1分,结果2.40-2.45都可以得分,
用分数表示不得分。
(5)
设该KMnO4的纯度为x,根据化学方程式可知
反应关系:2KMnO4→5Na2C2O4
其它错误不得分。反应条件不作要求。
(2)3MnO42-+4H+=2MnO4-+MnO2↓+2H2O 离子方程式中各离子式书写正确且符合题意,但未配平得2分,其
它错误不得分。反应条件和沉淀符号不作要求。
(4) 2KMnO4+5Na2C2O4+8H2SO4=K2SO4+2MnSO4+5Na2SO4+10CO2 ↑+8H2O (3分)
浙江高考化学评分细则(来自阅卷小组)

200826、(1)3MnO 2+6KOH+KClO 2MnO 4+KCl+3H 2O (3分)(未配平扣1分,分子式错误不给分)(2) 3MnO 42-+4H +=MnO 2+2MnO 42-+2H 2O (3分)(未配平扣1分,分子式错误不给分)(3)设:KMnO 4的理论产量为X,由上述两个化学方程式可知,相关物质的计量关系为:MnO 2 -----K 2MnO 4--------⅔KMnO 487 ⅔×158 计量关系正确+225×80% X计算结果正确+2左右) (未写成小数形式不得分)(4)2KMnO 4+5Na 2C 2O 4+8H 2SO 4+2MnSO 4+5Na 2SO 4+10CO 2↑+8H 2O (3分) 或2MnO 4-+5C 2O 42-+16H +2++10CO 2↑+8H 2O (2分)(5)设;该KMnO 4纯度为y,则2C 2O 4 27、(1)CaC 2 CaO CO 2 Ca (OH )2 C 2H 2(CH CH ,HC CH ) (各2分) (名称,电子式,结构式(乙炔除外),顺序不对,CHCH 等均得零分)(2)Ca (OH )2+2CO 2 = Ca (HCO 3)2 (2分)(计量系数不正确得1分,分子式不正确得0分,等号和箭头不作要求 分步写,两个全对得满分,对一个得0分)Ca (OH )2+CO 2=CaCO 3↓ CaCO 3+CO 2+H 2O=Ca (HCO 3)2(3)(3分)(以上形式都得3分,●与×无区别,CC 之间必须有三对电子,必须正确标注电荷数,阳离子不得用[],否则都不得分)各题平均分:26:6.42;27:6.43;28:3.99;29:8.03;合计:24.87分 各题总分及得分率:26:16分、0.40125;27:15分、0.428667;28:13分、0.306923;29:16分、0.501875;总计:60分、得分率0.414528、(1)氧(元素)/O(元素)(2分)(其余:氧或X,X或氧,O或X,X或O,写成O2,均不得分)(2)不需要/不用/否(2分)(否定性判断均可)原因:(有N2(氮气)通入)(不可能倒吸,可以防止倒吸,不会倒吸。
杭州市高一化学统测试评分标准
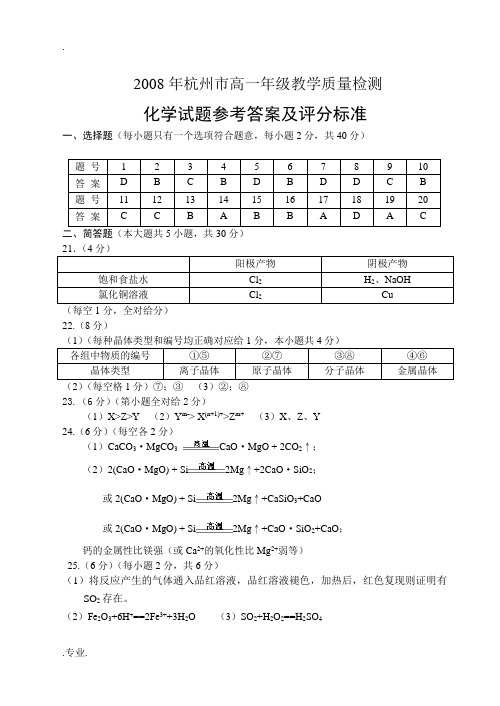
2008年杭州市高一年级教学质量检测化学试题参考答案及评分标准一、选择题(每小题只有一个选项符合题意,每小题2分,共40分)题号 1 2 3 4 5 6 7 8 9 10 答案 D B C B D B D D C B 题号11 12 13 14 15 16 17 18 19 20 答案 C C B A B B A D A C 二、简答题(本大题共5小题,共30分)21.(4分)阳极产物阴极产物饱和食盐水Cl2H2、NaOH氯化铜溶液Cl2Cu(每空1分,全对给分)22.(8分)(1)(每种晶体类型和编号均正确对应给1分,本小题共4分)各组中物质的编号①⑤②⑦③⑧④⑥晶体类型离子晶体原子晶体分子晶体金属晶体(2)(每空格1分)⑦;③(3)②;⑧23.(6分)(第小题全对给2分)(1)X>Z>Y (2)Y m-> X(n+1)+>Z m+(3)X、Z、Y24.(6分)(每空各2分)(1)CaCO3·MgCO3CaO·MgO + 2CO2↑;(2)2(CaO·MgO) + Si2Mg↑+2CaO·SiO2;或2(CaO·MgO) + Si2Mg↑+CaSiO3+CaO或2(CaO·MgO) + Si2Mg↑+CaO·SiO2+CaO;钙的金属性比镁强(或Ca2+的氧化性比Mg2+弱等)25.(6分)(每小题2分,共6分)(1)将反应产生的气体通入品红溶液,品红溶液褪色,加热后,红色复现则证明有SO2存在。
(2)Fe2O3+6H+==2Fe3++3H2O (3)SO2+H2O2==H2SO4三、实验题(本大题共3小题,共20分)26.(7分)(1)加热时烧瓶底部缺少石棉网。
(1分)(2)气体发生;气体收集(或集气);尾气吸收(每空1分)(3)NaOH或KOH (1分)(4)MnO2+4HClMnCl2+Cl2↑+2H2O (2分)27. (6分)(每小题2分)(1)使石墨棒表面变得粗糙,有利于吸附气体。
2008年高考全国理综(Ⅰ)化学试题评析

+ 匝歪
() 15种化合物分别是 V — 、 —
一
—
—
;填化学 式) (
( )由上述 5 2 种化合物 中的某 2种化合 物反应可生成一种
化学方程式是 () 3 v的电子式 是— — 。
料未及 , 对部分考生形成 了较强 的心理 干扰 。但 较适 合优秀生 新化合物 , 它包含 了 5 种化合物中的所有元素 , 生成该化合物的
—
;
() 5 上述制得的 K O 产品 0 6 g恰好与 0 3 g N 224 Mn  ̄ .5, 1 3 5 纯 a 0 C
点的 5 %。 0 很多试题均源于教材内容 , 如第 7题考查 的是比较各
算却都在第 2 题 中出现。第 2 题 : 6 6 实验室可 由软锰 矿( 主要成 种不 同类型的晶体熔点高低 : 下列化合物 , 按其晶体 的熔点 由高 分为 Mn :制备 K O , 法如下 : O) Mn 方 软锰矿 和过量 的固体 KO H 到低排列正确 的是 ASO s 1C r C 4BSO s1C ,C r . 2C C B4 F . ,C C F B4 i i 和 K 1 C0 在高 温下 反应 , 成锰 酸钾 ( z n 和 K 1用水 溶 生 KM O) C; CCC i2C r C DC 4C r CC i2 案 : 。 s 1S B4 L :F B 4 s1S0 ( O 答 A) 解, 滤去残渣 , 滤液酸化后 , . O 转变为 Mn _ K O ; KMn _ O 和 Mn 滤去 ,
() ,n  ̄ 2KM O 制备 K n  ̄ . M 0 的离子 方程式是—
—
;
() 用 2 g 锰矿 ( M O8%) 3若 . 软 5 含 n_ , 0 进行 上 述实 验 , 算 计
2008年高考理综全国卷(Ⅰ)中化学学科知识点分布统计分析

2008年高考理综全国卷(Ⅰ)中化学学科知识点分布统计分析作者:赵宇来源:《化学教学》2008年第10期2008年高考理综化学试题继续贯彻“稳中求实,稳中求改”的原则,努力测试考生学科能力和素养。
本文拟通过对2008年高考理综化学试题构成、内容及知识点分布特点等进行统计与分析,试图为广大化学教育工作者借助高考试卷,积极开展中学化学教育教学工作及理论实践提供参考。
12008年高考理综化学试题构成分析2008年高考理综化学试题构成仍然稳定,总分108分,其中I卷6~13题为选择题,每题6分,共计48分,占学科总分的44.4%,Ⅱ卷26~29题为非选择题,共计60分,占学科总分的55.6%。
题型主要有选择、填空与简答;试题的难易比例为容易题占13.0%,中等难度题占69.4%,较难题占17.6%;化学试卷的编排依然是并列直进式,即从易到难,有利于考生应答发挥,试题难度主要集中在Ⅱ卷。
2 2008年高考理综化学试题内容分析2008年高考理综化学试题最为突出的就是强调了学科的基础性。
诸如离子共存与鉴别,方程式的书写与正误判断,溶液中离子浓度大小比较,盐类水解,化学键和晶体类型及性质,以及有机反应类型及同分异构体书写、原子结构与元素周期律、化学反应速率和化学平衡和无机化学实验等知识贯串试卷始末,具体考查的内容,见表1。
由表1可知,2008年高考理综化学试题所考查的内容是中学化学中常见的基础知识,也是重点、热点知识。
试题既能立足基础,又能强化技能,加强了对知识理论运用能力的考查,具有较强的选拔性。
但能体现“能力立意,双基为主,学以致用,引领课改”的新课改命题思想,又能紧密联系社会、生产实际和高科技内容的试题比例还有待进步增加及提高。
3 2008年高考理综化学试题知识点分布及分数比例统计分析3.1知识点在五大知识板块中的分布及分数比例从历年的高考特别是近几年高考所考内容来看,高考所涉及到的基础知识主要包括五大板块:①元素及无机化合物;②有机化学;③化学计算;④化基本概念与基本理论;⑤化学实验等。
高考化学评分标准及答题注意事项
(5)检验气体的纯度
关于检验气体的纯度,尤其是像H2这种可 燃性气体,有不少考生不是采用“先用一 个干燥的试管收集气体后点燃,听是否有 尖锐的爆鸣声”来作出判断,而是直接在 气体出口处点燃,多么危险啊!像这种情 况肯定按“0”分处理。
如何优化答题技能? (1)2010年武汉市四月调考29题(2)
7. 若考生在试卷上写与考试无关的字或对阅卷老 师进行恭维、攻击的,一般视为在试卷上做记号。
8. “白纸黑字”原则。即凡是试卷上写了的 就有,没有写的就没有。只有认试卷上的 白纸黑字所表达的内容所提供的信息,才 能真正做到公平公正地评分
9. “见空给分”原则。在连续多个答案中, 为了便于操作,通常采用“独立操作,互 不牵连”的原则,即前面一个答案的正确 与否,不影响后面答案的给分,同理,如 前者正确,而后面错误,也按步骤照样给 分,虽然此法可能让某些人占了便宜,但 也不能冤枉一些人,而且便于操作。
(5)单位。有些考生在最后结果中没有单 位一定要扣分,单位不规范的也会扣分。
(6)计算式。现在考试已较少有复杂的计算,近几年来 基本没有。但有一点须注意,如果题目不是以填空的形 式出现,则在答题时,则一定要求有相应的计算式,若 仅有答案,而没有计算式的,则以0分计。而且计算式 不能仅写出一般的公式,要求与试题的具体条件相联系。 若仅有一般的公式而与试题的具体条件缺乏联系的,则 不给分。
(2)过于繁琐:
2010年4月调考卷29题(2)趁热过滤的目 的是_________。
标答是:避免FeSO4结晶而造成损失。 考生答:防止因温度下降,使得硫酸亚铁在水中 溶解度减小,以FeSO4·6H2O晶体的形式大量 析出,造成损失。
点评:言多必失。
(3)过于简化 2010年4月调考卷28题(1) 标答:可减少汽车废气的排放,降低对大气的污染。或答:
08年全08年全国高考理综化学试题分析及点评

. . . ....08年全国高考理综Ⅰ化学试题分析及点评一.试卷结构与考查内容1.试卷结构今年理综试卷试题组成、试题编排、各学科分值均与前4年完全一致,各学科试题完全独立,没有跨学科的拼盘题。
这一稳定结构有利于考生考前复习和考试的正常发挥。
2008年理综化学学科考查知识与能力双向细目表(满分108分)注:A表示“了解”B表示“理解与掌握”C表示“综合运用”2.试题总体分析与评价从2008 年高考理综Ⅰ化学试题湖南的分析报告的评价来看:“今年命题注重基础理论,考查发散思维能力。
充分体现了新课标、新课改的指导思想,这对中学理科教学是一种良好导向。
”但是,认真细析,今年的高考理综Ⅰ化学试题并不如人意,12个题中有一半的试题出现大大小小的问题,若按此指挥棒指挥教学,众多教师会感到茫然失措,众多考生的能力则难以发挥。
总体上看,试题粗糙,具有“偏”、“怪”、“难”及脱“纲”脱“本”的嫌疑,事实如下:①考查知识面窄,知识点重复-“偏”。
如氧化还原反应方程式的书写与配平在试卷中有多处出现(题26、题28);物质结构部分在选择题中(题7、题9、题10)连续出现且较为传统;同分异构体(题8、题29)也频频出现。
基础知识点的考查单调。
试卷中多处考查基础知识的试题缺乏新意,命题角度陈旧,如题7物质熔点高低的比较、题9化合物的判断等。
没有体现选择题的功能之一:考查基础知识覆盖面广。
②能力考查题基于创新,脱“纲”、脱“本”-“怪”。
试卷中许多能力考查题远远超出常规,走出中学化学教材,低起高落,如题8的同分异构体的判断,题27的碳化钙燃烧、题28的黄色粉未MZ等。
③试题语言描述似是而非,计算设计简单运算繁-“难”。
试卷中有好多地方语言描述不规范,让考生无所适从,难以动笔,如题12中的甲、乙酸的表述,题27中V与水反应的生成物的描述、题29中苯环上一溴代物的描述,题26的计算等。
为更好了解今年高考化学试题的特点,下面我们诸一分析,愿与大家共商榷:二、试题解答与点评(一)选择题6.在溶液中加入足量的Na2O2后仍能大量共存的离子组是A.NH4+、Ba2+、Cl—、NO3— B.K+、AlO2—、Cl—、SO 42—C.Ca2+、Mg2+、NO3—、HCO3— D.Na+、Cl—、CO32—、SO32—答案: B。
解读2008年化学高考《考试说明》.

05 06 07
产生配合物
∨
发生氧化还原反应
∨
产生沉淀
∨ ∨∨
OH—与酸式酸根离子反应 ∨
热化学方程式(07年 )
概念判断 图示能量的变化 判断或比较△H 计算热量多少
05 ∨
06 ∨
07 ∨ ∨ ∨
溶液中离子浓度大小比较(04年 )
05 06 07
分子是否完全电离
∨
理解、计算溶液pH
∨
∨
∨
质子守恒
❖ 容易题从20%提高到约30%,中等难度题从60%下 降到约50%,较难题约20%不变。
四、典型试题举例
❖ 选择题从以前的(43+11)题降为13题,非选择 题从(48+9)题降为12题,某种程度上说,具 有样卷的部分特征。
❖ 绝大多数是05年、 06年、07年江苏高考试题。
13道选择题涉及的内容
解读2008年 化学高考《考试说明》
周群
一己之见,仅供参考, 不对之处,敬请指正。
指导思想
❖ 有利于普通高等学校选拔具有创新精神和实践能力、 全面发展的新生,有利于基础教育全面实施素质教 育,有利于推进普通高中化学课程改革,有利于正 确引导基础教育化学教学。
❖ 以测试学生的化学科学素养和综合能力为主导。 ❖ 命题的内容基础知识、基本技能、 基本观点和基本
提高要求的内容
❖ 理解分子、原子、离子等的含义。 ❖ 理解溶解度。 ❖ 理解金属发生电化学腐蚀的原因,能选
用恰当的措施防止铁、铝等金属腐蚀。
降低要 认识温度、浓度、压强和催化剂影响化学反应速率的一般规
律。 ❖ 了解弱电解质在水溶液中的电离平衡。 ❖ 了解盐类水解的原理。了解离子反应的概念。 ❖ 了解电子式、结构式和结构简式的表示方法。 ❖ 了解常见金属(如Na、Al、Fe、Cu等)及其重要化合物的
高考化学评分细则[全国卷1]
![高考化学评分细则[全国卷1]](https://img.taocdn.com/s3/m/2158e63955270722192ef789.png)
2008年高考化学评分细则26.(1)小题评分细则1.化合物分子式错误不给分;2.化学方程式未配平不给分;3.化学方程式写成加热或高温不给分;4.化学方程式不规范的,一次性扣1分;如:系数为分数或倍数,未注明反应条件,等号写成可逆号“ ”或箭头“→”等。
5.得分点:[0,2,3](2)小题评分细则参照(1)小题评分细则,补充如下:1.写成化学方程式不给分;2.离子电荷未注明不给分;3.沉淀产物缺“↓”等不规范的,一次性扣1分;4.得分点:[0,2,3](3)小题评分细则1.只有答案无过程,或过程关系式不正确的,不给分;2.过程关系式如MnO 2——K 2MnO 4——32 KMnO 4的计量关系且算式正确,答案错误的扣1分;3.上述计量关系式正确,算式不正确,给2分;4.只列出关系式MnO 2——K 2MnO 4,给1分,列出K 2MnO 4——32 KMnO 4计量关系给1分;5.只列计算式,且能体现物质之间的计量关系,且答案正确的,不扣分;6.计算过程或答案采用“物质的量”作单位,且答案正确的,不扣分;7.答案用分数且正确的,不扣分;8.答案正确未注明单位的,扣1分;9.鉴于计算过程中计算方法及有效数字保留倍数不同,答案按数值在 2.1g~2.6g 或者0.0133mol~0.0165mol 均不扣分;10.得分点[0,1,2,3,4](4)小题评分细则1.化合物分子式错误不给分;2.化学方程式未配平不给分;3.反应条件写成加热或高温均不扣分;4.化学方程式不规范(系数为分数或倍数,未注明反应条件,等号写成可逆号“ ”或箭头“→”等),一次性扣1分;5.得分点:[0,2,3](5)小题评分细则1.只有答案无过程,或过程关系式不正确,不给分;2.过程关系式正确,答案错误,扣1分;3.列出KMnO4与Na2C2O4的计量关系,且算式正确,给2分;4.KMnO4与Na2C2O4的计量关系正确,但算式错误,给1分;5.KMnO4与Na2C2O4的计量关系正确,答案正确,给3分;6.只列出计算式,但能够体现物质间计量关系,且答案正确,给3分;7.答案用分数或小数表示,均不扣分;8.鉴于计算过程中计算方法及有效数字保留位数不同,答案数值在94%~97%(或分数或小数),均不扣分;但有明显计算错误,即使答案在上述范围内,也应扣1分;9.采用其他计算方法,正确者给满分;10.得分点:[0,1,2,3]27.(1)小题1.正确答案:CaC2;CaO;CO2;Ca(OH)2;C2H22.评分要点:严格执行标准答案,只能书写化学式,且顺序正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2008
26、(
1)3MnO 2+6KOH+KClO 2MnO 4+KCl+3H 2O (3分)(未配平扣1分,分子式错误不给分)
(2) 3MnO 42-+4H +=MnO 2+2MnO 42-+2H 2O (3分)(未配平扣1分,分子式错误不给分)
(3)设:KMnO 4的理论产量为X,
由上述两个化学方程式可知,相关物质的计量关系为:
MnO 2 -----K 2MnO 4--------⅔KMnO 4
87 ⅔×158 计量关系正确+2
25×80% X
计算结果正确+2
左右) (未写成小数形式不得分)
(4)2KMnO 4+5Na 2C 2O 4+8H 2SO 4+2MnSO 4+5Na 2SO 4+10CO 2↑+8H 2O (3分) 或2MnO 4-+5C 2O 42-+16H +2++10CO 2↑+8H 2O (2分)
(5)设;该KMnO 4纯度为y,则
2C 2O 4 27、(1)CaC 2 CaO CO 2 Ca (OH )2 C 2H 2(CH CH ,HC CH ) (各2分) (名称,电子式,结构式(乙炔除外),顺序不对,CHCH 等均得零分)
(2)Ca (OH )2+2CO 2 = Ca (HCO 3)2 (2分)
(计量系数不正确得1分,分子式不正确得0分,等号和箭头不作要求 分步写,两个全对得满分,对一个得0分)
Ca (OH )2+CO 2=CaCO 3↓ CaCO 3+CO 2+H 2O=Ca (HCO 3)2
(3)
(3分)
(以上形式都得3分,●与×无区别,CC 之间必须有三对电子,必须正确标注电荷数,阳离子不得用[],否则都不得分)
各题平均分:26:6.42;27:6.43;28:3.99;29:8.03;合计:24.87分 各题总分及得分率:26:16分、0.40125;27:15分、0.428667;28:13分、0.306923;
29:16分、0.501875;总计:60分、得分率0.4145
28、(1)氧(元素)/O(元素)(2分)
(其余:氧或X,X或氧,O或X,X或O,写成O2,均不得分)(2)不需要/不用/否(2分)(否定性判断均可)
原因:(有N2(氮气)通入)(不可能倒吸,可以防止倒吸,不会倒吸。
给
1分,其余不给分)
1分,结论错误扣3分)
(3)↑(对一个给1分,共4分)
↑①M写成Zn、Cd、Pb;O写成Z((1)中指明Z=O)
2
CO2允许
↑②反应式缺条件或↑不扣分
2
③写错分子式或未配平或M写成Na、Mg、Hg……等其他金属均扣1分
(4)结论2分,方法2分。
结论:要处理/需要/要/是等肯定性判断(2分)
方法:
①因含CO,连接热的CuO(FeO)粉末的玻管
②因可能有有毒气体(或有毒气体外泄),所以要连接热的CuO(FeO)粉末
的玻管
③点燃尾气/通过酒精灯火焰/
④方法为“收集”、“加酒精灯”、“加热”未指明时;“点燃”、“火焰”不给分
注:a,结论正确,只讲理由,无方法者得2分
b,结论正确,方法合理,缺原因、理由得4分
c,无结论,方法合理得2分
d,无结论,无方法,只有理由得0分
e,结论错误得0分
29、(1)得2分:
①C的结构简式写成:
得0分:
①C的结构简式写成:
(2)得2分:
①D的分子式写成:C4H8O2得1分(C、H、O的顺序颠倒不扣分)D具有的
官能团写羧基或(和)—COOH()得1分。
得1分:
①空一写结构简式或其他结构式,空二正确。
②空一正确,空二写羧酸或写两种及以上名称时,其中有一个错误,-COOH
写成COOH,得0分。
两空都错。
(3)得3分
→写成等号或可逆符号均可,酯基写成-COO-或-OOC-(两边的官能团要吻合),H2SO4写成浓H2SO4或H+均可。
反应物的结构简式必须与题(1)中所写的对应
得2分。
1)漏写H2SO4或2)CH3CH2CH2写成C3H7;
得0分。
1)反应物及产物的结构简式有明显错误;2)同时出现得2分中的两种情况;3)漏写H2O;4)多C少C,多H少H;5)把结构简式写成分子式。
(4)得4分
①CH3CH2CH2OH;
写成
多个答案只看前两个。
得2分:
前两个答案中写对一个。
得0分:
前两个答案都错。
(5)得5分
只看前4个答案,
前4个里对一个得1分。
得0分:
没有一个写对。
各题平均分:26:6.42;27:6.43;28:3.99;29:8.03;合计:24.87分
各题总分及得分率:26:16分、0.40125;27:15分、0.428667;28:13分、0.306923;
29:16分、0.501875;总计:60分、得分率0.4145
2008-06-20。
