(浙江选考)2019版高考化学-考前提升训练26-元素与物质推断(第27题)
浙江省2019年高考化学选考—有机化学(word版附答案)

浙江省2019 年高考化学选考——有机化学【考点解读】2015 年4 月至2018 年11 月7 次选考有机部分分值基本固定22 分,部分选择题会涉及几个有关有机化学素养的选项,总体平稳。
26、32 均是以合成框图的形式出现,26四小问6 分,32 五小问10 分。
题目的设置从易到难,简单有机物的结构简式、官能团的名称、反应类型的判断,反应方程式的书写,重要官能团性质的考查,有限制条件的同分异构体的书写,合成路线的设计,考查的知识点较广且综合性强。
虽然题目已知的信息是陌生的,给出的流程图可能也较为复杂,但是问题设置的梯度很明显,一般前面都会设置一些简单的基础题,而在后面设置中等难度的题目,往往需要根据题目所给已知信息才能解答,考查学生综合分析能力和知识迁移应用能力。
不难看出,有机化学的出题特点始终是:依据大纲,抓住课本,立足基础。
复习中要强化基础、培养思维、注重规范。
无论它怎么考,只要我们把握有机化学知识的内在联系和规律,掌握复习的技巧,就能事半功倍,达到复习的最佳效果。
【解题策略】览全题,看已知,获信息,找突破。
题目所给信息一般分为四类:条件、结构简式、分子式、特征现象。
常见的突破口有:反应条件[浓硫酸(酯化、硝化、纤维素水解等)、稀硫酸(酯、蔗糖、淀粉水解等)、O2/Cu(Ag)/△(醇氧化)、X2/FeX3(苯环上溴代)、X2/ 光照(烷基上取代等)、H2/催化剂(加成反应)];实验现象[能与Na 反应(含羟基或羧基)、能与NaOH 反应(含羧基或酚羟基)、能与NaHCO3 反应(含羧基)、能发生银镜反应(含醛基、)能与新制Cu(OH)2 共热产生砖红色沉淀(含醛基)、使酸性KMnO4 溶液褪色(含不饱和键、含醛基)]。
依据分子式及其组成的变化、官能团的衍变、原子个数的变化、特殊的转化关系、题目所给新信息等进行串联。
联系所学整合题给信息和已知,正推、逆推相结合,攻克关键中间产物,正推法的思维程序是原料→中间产物→产品,始终关注已知信息的痕迹,逆推法的思维程序是产品→中间产物→原料,在高考中往往需要正推逆推加已知相结合即从两边往中间推,在关键的中间产物上形成交集,最后全面突破,理顺合成路线。
2019年4月浙江省普通高校招生选考化学试卷和答案

2019年4月浙江省普通高校招生选考化学试卷一、选择题(本大题共25小题,每小题2分,共50分.每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)1.(2分)下列属于碱的是()A.C2H5OH B.Na2CO3C.Ca(OH)2D.Cu2(OH)2CO32.(2分)下列属于强电解质的是()A.硫酸钡B.食盐水C.二氧化硅D.醋酸3.(2分)下列图示表示过滤的是()A.B.C.D.4.(2分)下列属于置换反应的是()A.4NH2+5O24NO+6H2OB.2Na2SO3+O2═2Na2SO4C.2Na2O2+2CO2═Na2CO3+O2D.2KI+Cl2═2KCl+I25.(2分)下列溶液呈碱性的是()A.NH4NO3B.(NH4)2SO4C.KCl D.K2CO3 6.(2分)反应8NH3+3Cl2═N2+6NH4Cl,被氧化的NH3与被还原的Cl2的物质的量之比为()A.2:3B.8:3C.6:3D.3:2 7.(2分)下列表示不正确的是()A.次氯酸的电子式B.丁烷的球棍模型C.乙烯的结构简式CH2=CH2D.原子核内有8个中子的碳原子C8.(2分)下列说法不正确的是()A.液氯可以储存在钢瓶中B.天然气的主要成分是甲烷的水合物C.天然石英和水晶的主要成分都是二氧化硅D.硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等9.(2分)下列说法不正确的是()A.蒸馏时可通过加碎瓷片防暴沸B.可用精密pH试纸区分pH=5.1和pH=5.6的两种NH4Cl溶液C.用加水后再分液的方法可将苯和四氯化碳分离D.根据燃烧产生的气昧,可区分棉纤绵和蛋白质纤维10.(2分)下列说法正确的是()A.18O2和16O2互为同位素B.正己烷和2,2﹣二甲基丙烷互为同系物C.C60和C70是具有相同质子数的不同核素D.H2NCH2COOCH3和CH3CH2NO2是同分异构体11.(2分)针对下列实验现象表述不正确的是()A.用同一针筒先后抽取80 mL氯气、20mL水,振荡,气体完全溶解,溶液变为黄绿色B.在表面皿中加入少量胆矾,再加入3mL浓硫酸,搅拌,固体由蓝色变白色C.向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀D.将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成12.(2分)化学电源在日常生活和高科技领域中都有广泛应用。
(浙江选考)近年高考化学考前提升训练27化学基础实验(第28题)(2021年整理)

(浙江选考)2019版高考化学考前提升训练27 化学基础实验(第28题) 编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望((浙江选考)2019版高考化学考前提升训练27 化学基础实验(第28题))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为(浙江选考)2019版高考化学考前提升训练27 化学基础实验(第28题)的全部内容。
提升训练27 化学基础实验(第28题)1。
(2018·学军中学模拟)一定条件下,草酸铜晶体(CuC2O4· x H2O)受热分解的化学方程式为CuC2O4·x H2O·CuO+CO↑ +CO2↑ +x H2O↑.某化学兴趣小组设计如图装置,探究草酸铜晶体分解的气体产物:请回答:(1)该套实验装置的明显缺陷是。
(2)实验过程中观察到B中白色无水硫酸铜变成蓝色,C、F中澄清石灰水变浑浊,E中(填实验现象),则可证明草酸铜晶体热分解的气体产物是H2O、CO、CO2。
(3)该兴趣小组改变热分解的反应条件,完全反应后发现C中白色沉淀量明显较先前实验多,而E、F中未见明显现象,请推测A装置中固体产物成分并设计一个实验方案,用化学方法验证固体产物:(不考虑操作和药品的问题)。
2.钠与水反应的改进实验操作如下:取一张滤纸,用酚酞试液浸润并晾干,裁剪并折叠成信封状,滤纸内放一小块金属钠(约绿豆粒般大小),把含钠的滤纸信封放入水中,装置如下图所示.请回答:(1)写出金属钠与水反应的离子方程式:。
(2)实验过程中取用金属钠的操作方法是. (3)有关此实验的说法正确的是。
A.实验过程中,可能听到爆鸣声B。
浙江省学选考化学2019届高三二轮复习27题对题复习课件(15张)

2、特征反应现象 【讲义4】为探究无机盐X(仅含三种短周期元素) 的组成和性质,设计并完成如下实验:请回答:
n(SiO2)=0.03mol
n(Mg(OH)2)=0.06mol (3)高温条件下白色粉末与焦炭发生置换反应, 写出该反应的化学方程式______
高温
SiO2+2C==Si+2CO
注意几个特殊的置换反应: 1.金属 盐 金属 盐
【例3】(2018年4月)某同学用含结晶水的正盐X(四种短 周期元素组成的纯净物)进行了如下实验:
n(H2O)=0.05mol
n(HCl)=0.02mol n(MgO)=0.01mol
实验中观测到:混合气甲呈无色并被蒸馏水全部吸收; 固体乙为纯净物;在步骤③中,取1/10溶液丙,恰好中 和需消耗0.00200 mol NaOH;另取一定量的溶液丙,
n(SO3)=0.1mol
第2题和讲义第五题
n(Cu2O)=0.2mo
取一定量的浅绿色盐X进行上述实验,充分反应后得到 23.3 g白色沉淀E、28.8 g红色固体G和12.8 g红色固体H。
①浅绿色盐X在570 ℃、隔绝空气条件下受热分解为 非氧化还原反应;
②常温下B呈液态且1个B分子含有10个电子。
4KI+O2+2H2O
2I2+4KOH
。
(2)在通气良好的土壤中,土壤中NH4+的氧化途径
之一是在硝酸细菌作用下完成,写出反应的离子方程
式
NH4++2O2
硝酸细菌
NO3-+H2O+2H+。
(3)工业上一般采用电解(惰性电极)K2MnO4溶
液制KMnO4,写出电解总反应方程式
2019年4月浙江省普通高校招生选考科目考试化学试题与答案

+
D .高温高压液态水中的油脂水解,相当于常温下在体系中加入了相同 23. MgCO 3 和 CaCO 3 的能量关系如图所示 ( M = Ca 、 Mg ) : M ( g) + CO 3 ( g) ↑Δ H1 MCO 3( s)
2+ 2-
Δ H2 ———→ Δ H ———→
M ( g) + O ( g) + CO 2 ( g) ↓Δ H3 MO ( s) + CO 2( g)
+ -
... 的是
CO 2 增多、石灰石沉积 CO 2 溶解,沉积少 CO 3 浓度增大
-1 2-
CaCO 3( s) + H 2O( l) + CO 2( aq) ===Ca( HCO 3) 2( aq) NaOH 溶液。
-1
CO 2 浓度增加,会导致海水中
-1 + 2-
20 mL 0.1 mol ・ L
C.若压强不再随时间变化能说明反应 D . 1 mol N 2 和 3 mol H 2 反应达到平衡时 18.下列说法不正确 ...的是
分解为 N 2 和 H 2 的转化率为 10% 时,吸收热至
A .纯碱和烧碱熔化时克服的化学键类型相同 C. CO 2 溶于水和干冰升华都只有分子间作用力改变
B .加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
D .石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏 19.设 NA 为阿伏加德罗常数的值,下列说法不正确 ... 的是 A . 1 mol CH 2 = CH 2 分子中含有的共价键数为 6N A B . 500 mL 0.5 mol ・ L
-1
的 NaCl 溶液中微粒数大于
0.5N A
2019年4月浙江省普通高校招生选考科目考试化学试题与答案

2019 年4 月浙江省普通高校招生选考科目考试化学试题与答案前绝密★考试结束2019 年4 月浙江省普通高校招生选考科目考试化学试题姓名:____________ 准考证号:____________30 分,用分为部分,共8 页,满分100 分,考试时间90 分钟。
其中加试题部本试题卷分选择题和非选择题两出。
考生注意:【加试题】标1.答题前,请务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔分别填写在试题卷和答题纸规定的位置上。
2.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上的作答一律无效。
3.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可先使用2B 铅笔,确定后必须使用黑色字迹的签字笔或钢笔描黑,答案写在本试题卷上无效。
4.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Ca 40 Fe 56 Cu 64 Ba 137选择题部分一、选择题(本大题共25 小题,每小题 2 分,共50 分。
每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)l.下列属于碱的是A .C2H5OH B.Na2CO3 C.Ca( OH) 2 D.Cu2(OH) 2CO32.下列属于强电解质的是A .硫酸钡B.食盐水C.二氧化硅D.醋酸3.下列图示表示过滤的是A .B.C.D.4.下列属于置换反应的是催化剂A .4NH 2+5O2=======4NO+6H2O B.2Na2SO3+O2===2Na2SO4△C.2Na2O2+2CO2===2Na2CO3+O2 D.2KI +Cl 2===2KCl +I 25.下列溶液呈碱性的是A .NH4NO3 B.( NH4) 2SO4 C.KCl D.K2CO36.反应8NH3+3Cl2===N2+6NH 4Cl,被氧化的NH 3 与被还原的Cl2 的物质的量之比为A .2∶ 3 B.8∶ 3 C.6∶ 3 D.3∶ 27.下列表示不.正.确.的是?? ??A .次氯酸的电子式H ?Cl? ??O? B.丁烷的球棍模型?? ??C.乙烯的结构简式CH2=CH 2 D.原子核内有8 个中子的碳原子146C8.下列说法不.正.确.的是A .液氯可以储存在钢瓶中B.天然气的主要成分是甲烷的水合物C.天然石英和水晶的主要成分都是二氧化硅D.硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等第1 页2019 年 4 月浙江省普通高校招生选考科目考试化学试题与答案9.下列说法不正确的是A .蒸馏时可通过加碎瓷片防暴沸B .可用精密 pH 试纸区分 pH =5.1 和 pH =5.6 的两种 NH 4Cl 溶液C .用加水后再分液的方法可将苯和四氯化碳分离D .根据燃烧产生的气昧,可区分棉纤绵和蛋白质纤维 10.下列说法正确的是A .18O 2 和 16O 2互为同位素B .正己烷和 2, 2- 二甲基丙烷互为同系物C .C 60 和 C 70 是具有相同质子数的不同核素D .H 2NCH 2COOCH 3和 CH 3CH 2NO 2 是同分异构体 11.针对下列实验现象表述不正.确..的是A .用同一针筒先后抽取 80 mL 氯气、 20 mL 水,振荡,气体完全溶解,溶液变为黄绿色B .在表面皿中加入少量胆矾,再加入3 mL 浓硫酸,搅拌,固体由蓝色变白色C .向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀D .将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成 12.化学电源在日常生活和高科技领域中都有广泛应用。
2019年4月学军中学高三化学选考冲刺模拟卷答案
参考答案一、选择题(共25题,每小题只有1个选项符合题意,每小题2分,共50分)26.(6分)(1)醛基(1分)、加成反应(1分)(2)OH COONa CH C CH O Cu NaOH OH C CHO CH C CH 23222323)()u 2)(+=+→++=((2分) (3)BCD (2分)27. (6分)(1)O H O FeC 2422⋅(2分)(2)↑+CO ↑CO +O 2H +FeO O 2H O FeC 22242加热=⋅2分)(3)2FeO+CO 2=Fe 2O 3+CO (2分)28.(4分)(1)氮气保护,稀释ClO 2的浓度,防止爆炸。
(2分)(2)C D (2分)29.(4分)33.3 % 或 1/3(2分) 407~1207mm (2分) 30.【加试题】(10分) (一)(1)粗铝(2分)(2)[Al 2Br 5ArH]++6e -→2Al+5Br -+ArH (2分) (二)(1)C D(2)(3) 苄基比烷基带负电多,与MnO 4-相排斥,不利于携带KMnO 4进入有机体。
聚乙二醇再水中溶解度大,反应过程损失多,造成MnO 4-减少。
(4) (4)B C31.【加试题】(10分))Q ()()Q (44++⋅=--c MnO c MnO c kw31270(1)加热(2分)(2)KCl (1分) KH(IO 3)2+KOH=2KIO 3+H 2O (1分) (3)B D(4)223232)(Cl KCl IO KH O H KClO I ++→++.溶液中的氯气会与KOH 反应生成次氯酸钾,次氯酸钾具有强氧化性,可以将KIO 3氧化成KIO 4从而得不到碘酸钾。
(2分) (5)产生氯气,污染环境 (2分)(6)(7)4I -+4H ++O 2=2I 2+H 2O 加入的KI 过量,在酸性条件下,I -会与空气中的氧气反应,生成I 2,造成甲的实验结果偏大。
浙江省学选考化学2019届高三二轮复习27题对题复习课件(15张)

n(SO3)=0.1mol
n(Cu2O)=0.2mo 第2题和讲义第五题
取一定量的浅绿色盐X进行上述实验,充分反应后得到 23.3 g白色沉淀E、28.8 g红色固体G和12.8 g红色固体H。 ①浅绿色盐X在570 ℃、隔绝空气条件下受热分解为 非氧化还原反应; ②常温下B呈液态且1个B分子含有10个电子。
黑色粉末
红褐色沉淀 白色沉淀
MnO2、Fe3O4、 血红色溶液 CuO、C Fe(OH)3 红棕色气体 BaSO4、BaCO3、 黄绿色气体 CaCO3、AgCl、
NO2 Cl2
7
某化合物甲是制备负载型催化剂的主要原料。经 组成分析化合物甲中含有四种元素。
m(气)=3.00g n(CO)=0.06mol n(CO2)=0.03mol n(Fe2O3)=0.01mol m(K2CO3)=4.14g n(K2CO3)=0.03mol 气体混合物乙仅含两种元素,由丁和戊组成,其中丁占 总体积的2/3,密度为1.25g· L-1。戊能使澄清石灰水变 浑浊。 K3[Fe(C2O4)3]或K3FeC6O12 (1)化合物甲的化学式________ (2)加热化合物甲使其完全分解的化学方程式为 2K __________________________________________ 。 2; 3[Fe(C2O4)3]=3K2CO3+Fe2O3+6CO+3CO
【例2】(2017年11月)已知固体Na2SO3受热易 分解,实验流程和结果如下:
气体Y是一种纯净物,在标准状况下的密度为1.518g· L-1 (1)气体Y分子的电子式_______, (2)该流程中的Na2SO3受热分解的化学方程式 ____________________________________。 (3)另取固体X试样和Na2SO3混合,加水溶解后与稀盐 2-+SO 2-+6H+=3S↓+3H O 2S 3 2 酸反应,有淡黄色沉淀产生,写出产生淡黄色沉淀的 离子方程式___________________________________。
2019年4月浙江省普通高校招生选考科目考试化学试题与答案(精校版)

2019年4月浙江省普通高校招生选考科目考试化学试题可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Ca 40 Fe 56 Cu 64 Ba 137选择题部分一、选择题(本大题共25小题,每小题2分,共50分。
每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)1.下列属于碱的是A .C 2H 5OHB .Na 2CO 3C .Ca(OH)2D .Cu 2(OH)2CO 32.下列属于强电解质的是A .硫酸钡B .食盐水C .二氧化硅D .醋酸3.下列图示表示过滤的是4.下列属于置换反应的是A .324NH +5O 催化剂△24NO +6H O B .2Na 2SO 3 +O 2=2Na 2SO 4C .2Na 2O 2 +2CO 2=2Na 2CO 3 +O 2D .2KI +Cl 2=2KCl +I 25.下列溶液呈碱性的是A .NH 4NO 3B .(NH 4)2SO 4C .KClD .K 2CO 36.反应8NH 3 +3Cl 2=N 2 +6NH 4Cl ,被氧化的NH 3与被还原的Cl 2的物质的量之比为A .2:3B .8:3C .6:3D .3:27.下列表示不正确...的是 A .次氯酸的电子式Cl H O B .丁烷的球棍模型C .乙烯的结构简式CH 2=CH 2D .原子核内有8个中子的碳原子C 1468.下列说法不正确...的是 A .液氯可以储存在钢瓶中B .天然气的主要成分是甲烷的水合物C .天然石英和水晶的主要成分都是二氧化硅D .硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等9.下列说法不正确...的是 A .蒸馏时可通过加碎瓷片防暴沸B .可用精密pH 试纸区分pH=5.1和pH=5.6的两种NH 4Cl 溶液C .用加水后再分液的方法可将苯和四氯化碳分离A.18O2和16O3互为同位素B.正己烷和2,2-二甲基丙烷互为同系物C.C60和C70是具有相同质子数的不同核素D.H2NCH2COOCH3和CH3CH2NO2是同分异构体11.针对下列实验现象表述不正确...的是A.用同一针筒先后抽取80mL氯气、20mL水,振荡,气体完全溶解,溶液变为黄绿色B.在表面皿中加入少量胆矾,再加入3mL浓硫酸,搅拌,固体由蓝色变白色C.向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀D.将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成12.化学电源在日常生活和高科技领域中都有广泛应用。
2019年11月浙江省高中化学学考选考试题与答案

2019年11月浙江省普通高校招生选考科目考试选择题部分一、选择题(本大题共25小题,每小题2分,共50分。
每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分) 1.下列属于氧化物的是A .Na 2OB .Ca (OH )2C .HClOD .K 2CO 3 2.下列仪器名称为“蒸馏烧瓶”的是A .B .C .D .3.下列属于电解质的是A .镁B .酒精C .硫酸铜D .食盐水 4.下列分散系属于悬浊液的是A .牛奶B .蔗糖溶液C .泥浆水D .氢氧化铁胶体 5.下列不属于化石燃料的是A .煤B .石油C .天然气D .甲醇6.下列说法不正确...的是 A .干冰可用于人工降雨B .碘酸钾可用作加碘食盐的添加剂C .碳酸钠是发酵粉的主要成分D .次氯酸钙是漂白粉的有效成分 7.下列属于置换反应的是A .2FeCl 3+Cu===CuCl 2+2FeCl 2B .2HClO=====光照2HCl +O 2↑C .CO +CuO===△CO 2+CuD .2Mg +CO 2=====点燃2MgO +C8.下列表示不正确...的是 A .氯原子的结构示意图 B .二氧化碳的结构式O =C =O C .CH 4的球棍模型D .乙醛的官能团-CHO9.下列物质的水溶液不能使酚酞变红的是A .NaOHB .Na 2CO 3C .NaClD .NH 310.下列方法(必要时可加热)不合理的是A .用澄清石灰水鉴别CO 和CO 2B .用水鉴别苯和四氯化碳C .用Ba (OH )2溶液鉴别NH 4Cl 、(NH 4)2SO 4和K 2SO 4D .用淀粉碘化钾试纸鉴别碘水和溴水 11.下列说法正确的是A .188O 表示中子数为10的氧元素的一种核素B .金刚石和石墨互为同素异形体,两者之间不能相互转化C .CH 3COOH 和CH 3COOCH 3互为同系物8 8 +17 2D .C 6H 14的同分异构体有4种,其熔点各不相同 12.下列离子方程式不正确...的是 A .氢氧化钠溶液与二氧化硅反应SiO 2+2OH ‾===SiO 2ˉ3+H 2OB .碳酸钠溶液与氢氧化钡溶液反应CO 2ˉ3+Ba (OH )2===BaCO 3↓+2OH ‾ C .酸性硫酸亚铁溶液在空气中被氧化4Fe 2++O 2+4H +===4Fe 3++2H 2O D .氯气与氢氧化钠溶液反应Cl 2+2OH ‾===ClO ‾+Cl ‾+H 2O13.Q 、X 、Y 和Z 为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。
(浙江选考)2019高考化学二轮增分策略27题专练金属及其化合物的框图推断课件

H2SO3+H2O2===H2SO4+H2O。
解析 答案
(3)化合物X与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶
+=== Fe S + 6H 3 4 物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:________________
3Fe2++S↓+3H2S↑ 。 ____________________
解析 化合物Fe3S4与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不
溶物和一种臭鸡蛋气味气体,说明反应产物为Fe2+、S和H2S,根据得失电子守恒
和原子守恒,该反应的离子方程式为Fe3S4+6H+===3Fe2++S↓+3H2S↑。
解析 答案
以通过如下反应和相应的数据推知它的化学式。其中A~J是中学化学中的常
见物质,G是一种红褐色固体,D是一种难溶于水的含氧酸,J是一种主要的温
室气体,A为强碱,其焰色反应呈黄色,E和B分别与酸化的硝酸银溶液反应时
的实验现象相同,均有白色沉淀产生,流程中的部分生成物已略去。
回答下列问题:
(1)A的电子式:_______________。
解析 H→G的化学方程式为4Fe(OH)2+O2+2H2O===4Fe(OH)3。
解析
答案
3.(2018· 温州市高三选考适应性测试)为探究液体X[仅含两种元素,100 g· mol-1 <M(X)<200 g· mol-1]的组成和性质,设计并完成如下实验:
请回答:
S2Cl2 。 (1)化合物X的化学式为______
解析
答案
Fe2SiO4(或2FeO· SiO2) 。 (2)铁橄榄石的化学式:_____________________
解析 铁橄榄石的化学式为2FeO· SiO2。
2019届高考化学二轮复习浙江选考化学真题专项训练题组(第27题)
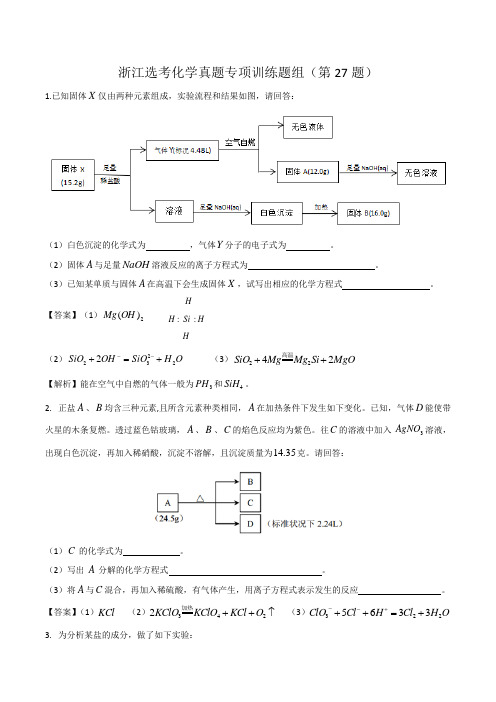
浙江选考化学真题专项训练题组(第27题)1.已知固体X 仅由两种元素组成,实验流程和结果如图,请回答:(1)白色沉淀的化学式为 ,气体Y 分子的电子式为 。
(2)固体A 与足量NaOH 溶液反应的离子方程式为 。
(3)已知某单质与固体A 在高温下会生成固体X ,试写出相应的化学方程式 。
【答案】(1)2)(OH Mg HH Si H H::....(2)O H SiO OH SiO 22322+=+-- (3)MgO Si Mg Mg SiO 2422++高温【解析】能在空气中自燃的气体一般为3PH 和4SiH 。
2. 正盐A 、B 均含三种元素,且所含元素种类相同,A 在加热条件下发生如下变化。
已知,气体D 能使带火星的木条复燃。
透过蓝色钴玻璃,A 、B 、C 的焰色反应均为紫色。
往C 的溶液中加入 3AgNO 溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解,且沉淀质量为35.14克。
请回答:(1)C 的化学式为 。
(2)写出 A 分解的化学方程式 。
(3)将A 与C 混合,再加入稀硫酸,有气体产生,用离子方程式表示发生的反应 。
【答案】(1)KCl (2)↑++2432O KCl KClO KClO 加热 (3)O H Cl H Cl ClO 2233365+=+++--3. 为分析某盐的成分,做了如下实验:请回答:(1)盐 M 的化学式是 ;(2)被NaOH 吸收的气体的电子式 ;(3)向溶液A 中通入S H 2气体,有淡黄色沉淀产生,写出反应的离子方程式 (不考虑空气的影响)。
【答案】(1)34)(ClO Fe (2)⋅⋅⋅⋅⋅⋅⋅⋅:::Cl Cl (3)↓++=++++S H Fe S H Fe 2222234. 为探究矿石样品A (仅含两种元素)的组成和性质,设计并完成如下实验:已知:溶液D 中只含一种金属阳离子,与铁粉充分反应后固体质量减少g 14。
请回答:(1)样品A 的化学式为 。
2019年4月浙江省化学选考卷(含答案)

2019年4月浙江省普通高校招生选考科目考试化学试题姓名:____________ 准考证号:____________本试题卷分选择题和非选择题两部分,共8页,满分100分,考试时间90分钟。
其中加试题部分为30分,用【加试题】标出。
考生注意:1.答题前,请务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔分别填写在试题卷和答题纸规定的位置上。
2.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上的作答一律无效。
3.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可先使用2B 铅笔,确定后必须使用黑色字迹的签字笔或钢笔描黑,答案写在本试题卷上无效。
4.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 S 32 Cl 35.5 Ca 40 Fe 56 Cu 64 Ba 137选择题部分一、选择题(本大题共25小题,每小题2分,共50分。
每个小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分) l .下列属于碱的是A .C 2H 5OHB .Na 2CO 3C .Ca(OH)2D .Cu 2(OH)2CO 32.下列属于强电解质的是A .硫酸钡B .食盐水C .二氧化硅D .醋酸3.下列图示表示过滤的是A .B .C .D .4.下列属于置换反应的是A .4NH 2+5O 2=======催化剂△4NO +6H 2O B .2Na 2SO 3+O 2===2Na 2SO 4C .2Na 2O 2+2CO 2===2Na 2CO 3+O 2D .2KI +Cl 2===2KCl +I 25.下列溶液呈碱性的是A .NH 4NO 3B .(NH 4)2SO 4C .KClD .K 2CO 36.反应8NH 3+3Cl 2===N 2+6NH 4Cl ,被氧化的NH 3与被还原的Cl 2的物质的量之比为A .2∶3B .8∶3C .6∶3D .3∶27.下列表示不正确...的是 A .次氯酸的电子式H ••Cl ••••••O ••••••B .丁烷的球棍模型C .乙烯的结构简式CH 2=CH 2D .原子核内有8个中子的碳原子146C8.下列说法不正确...的是A.液氯可以储存在钢瓶中B.天然气的主要成分是甲烷的水合物C.天然石英和水晶的主要成分都是二氧化硅D.硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等9.下列说法不正确的是A.蒸馏时可通过加碎瓷片防暴沸B.可用精密pH试纸区分pH=5.1和pH=5.6的两种NH4Cl溶液C.用加水后再分液的方法可将苯和四氯化碳分离D.根据燃烧产生的气昧,可区分棉纤绵和蛋白质纤维10.下列说法正确的是A.18O2和16O2互为同位素B.正己烷和2,2−二甲基丙烷互为同系物C.C60和C70是具有相同质子数的不同核素D.H2NCH2COOCH3和CH3CH2NO2是同分异构体11.针对下列实验现象表述不正确...的是A.用同一针筒先后抽取80 mL氯气、20 mL水,振荡,气体完全溶解,溶液变为黄绿色B.在表面皿中加入少量胆矾,再加入3 mL浓硫酸,搅拌,固体由蓝色变白色C.向二氧化硫水溶液中滴加氯化钡溶液,再滴加双氧水,产生白色沉淀D.将点燃后的镁条伸入充满二氧化碳的集气瓶,镁条剧烈燃烧,有白色、黑色固体生成12.化学电源在日常生活和高科技领域中都有广泛应用。
2019年高考化学考前提升训练26元素与物质推断(第27题)

2019年高考化学考前提升训练26元素与物质推断(第27题)1.(2018·学军中学模拟)探究无机盐X(仅含三种短周期元素)的组成和性质,设计并完成如下实验:请回答:(1)X的化学式是。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是。
(3)白色沉淀用途广泛,请列举一例: 。
2.某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期第ⅤA族。
D、E、H均为难溶于水的白色固体,化合物C、E均含A元素。
其余物质均为中学化学中的常见物质。
请回答:(1)写出H的化学式: 。
(2)化合物A3M4中含有的化学键类型为。
(3)写出反应②的离子方程式: 。
3.为了探究不溶性盐X(仅含5种元素)的组成和性质,设计并完成如下实验(所加试剂均过量,气体体积均在标准状况下测定)。
请回答:(1)X的组成元素为H、O和(用元素符号表示),气体C的电子式为。
(2)写出反应①的离子方程式: 。
4.为探究含结晶水的化合物X(含四种元素,摩尔质量为180 g·mol-1)的组成和性质,某兴趣小组设计并完成如下实验:请回答:(1)黑色固体Y的化学式为,气体C的电子式为。
(2)晶体X隔绝空气受热分解的化学方程式为。
5.某盐A是由三种元素组成的化合物,某研究小组按如图流程探究其组成:请回答:(1)写出红棕色固体C的化学式: 。
(2)写出A受热分解反应的化学方程式: 。
(3)写出检验A中阳离子的实验方案: 。
6.为探究某矿物X(仅含三种元素)的组成,设计并完成了如下实验:已知:气体A能使品红溶液褪色,固体B中仅含CuO、Fe2O3。
请回答:(1)X的化学式为。
(2)溶液C中存在的阳离子有。
参考答案提升训练26 元素与物质推断(第27题)1.答案: (1)Mg2SiO4或2MgO·SiO2(2)SiO2+2OH-Si+H2O(3)优良的阻燃剂(答案合理即可)解析: 无机盐X(仅含三种短周期元素),加入过量盐酸溶解,离心分离得到白色胶状沉淀和无色溶液,白色胶状沉淀为硅酸,硅酸充分灼烧得到白色粉末1.80 g为SiO2,其物质的量==0.03 mol,溶于氢氧化钠溶液得到无色溶液为硅酸钠溶液,说明无机盐X中含Si或Si,且物质的量为0.03 mol,若为Si,则其质量=0.03 mol×76 g·mol-1=2.28 g,金属质量=4.20 g-2.28 g=1.92 g,无色溶液中加入过量氢氧化钠溶液生成白色沉淀,则沉淀为Mg(OH)2,则无机盐X中含镁元素的物质的量==0.06 mol,质量为0.06 m ol×24 g·mol-1=1.44 g,不符合要求,则无机盐X中含Si,其物质的量为0.03 mol,质量=0.03 mol×92 g·mol-1=2.76 g,金属质量为4.20 g-2.76 g=1.44 g,其物质的量=1.44 g÷24 g·mol-1=0.06 mol,得到X为Mg2SiO4,则(1)X的化学式为Mg2SiO4或2MgO·SiO2;(2)白色粉末溶于氢氧化钠溶液的离子方程式是SiO2+2OH-Si+H2O;(3)氢氧化镁是优良的阻燃剂。
新(浙江专用)高考化学二轮复习 专题讲座二 学考第27题-元素和物质推断(含解析)-人教版高三全册化

专题讲座二 学考第27题——元素和物质推断1.(2016·浙江4月选考,27)下图中,固体A 是铁锈的主要成分。
固体A ――→足量CO 高温单质B ――→足量Cl 2加热固体C ――→SO 2/H 2O 溶液D ――→BaCl 2溶液白色沉淀E 请回答:(1)白色沉淀E 的化学式是________________。
(2)写出A→B 的化学方程式:_________________________________________________。
(3)写出C→D 在溶液中发生氧化还原反应的离子方程式:_________________________。
答案 (1)BaSO 4(2)Fe 2O 3+3CO=====高温2Fe +3CO 2(3)SO 2+2H 2O +2Fe 3+===2Fe 2++SO 2-4+4H +解析 根据题意分析出固体A 为Fe 2O 3,单质B 为Fe ,固体C 为FeCl 3,溶液D 为FeSO 4和FeCl 2的混合溶液,沉淀E 为BaSO 4。
(1)白色沉淀E 的化学式为BaSO 4。
(2)CO 还原Fe 2O 3生成Fe 和CO 2,化学方程式为Fe 2O 3+3CO=====高温2Fe +3CO 2。
(3)SO 2将Fe 3+还原为Fe 2+,自身被Fe 3+氧化为SO 2-4,离子方程式为SO 2+2H 2O +2Fe 3+===2Fe 2++SO 2-4+4H +。
2.(2015·浙江10月选考)某酸性废液中含有Fe 3+、Cu 2+、Ba 2+三种金属离子,有同学设计了下列方案对该废液进行处理(所加试剂均稍过量),以回收金属,保护环境。
请回答:(1)沉淀a 中含有的单质是________________。
(2)沉淀c 的化学式是________________。
(3)溶液A 与H 2O 2溶液在酸性条件下反应的离子方程式是____________________________。
浙江省2019年高考化学选考—有机化学(word版附答案)

浙江省2019 年高考化学选考——有机化学【考点解读】2015 年4 月至2018 年11 月7 次选考有机部分分值基本固定22 分,部分选择题会涉及几个有关有机化学素养的选项,总体平稳。
26、32 均是以合成框图的形式出现,26四小问6 分,32 五小问10 分。
题目的设置从易到难,简单有机物的结构简式、官能团的名称、反应类型的判断,反应方程式的书写,重要官能团性质的考查,有限制条件的同分异构体的书写,合成路线的设计,考查的知识点较广且综合性强。
虽然题目已知的信息是陌生的,给出的流程图可能也较为复杂,但是问题设置的梯度很明显,一般前面都会设置一些简单的基础题,而在后面设置中等难度的题目,往往需要根据题目所给已知信息才能解答,考查学生综合分析能力和知识迁移应用能力。
不难看出,有机化学的出题特点始终是:依据大纲,抓住课本,立足基础。
复习中要强化基础、培养思维、注重规范。
无论它怎么考,只要我们把握有机化学知识的内在联系和规律,掌握复习的技巧,就能事半功倍,达到复习的最佳效果。
【解题策略】览全题,看已知,获信息,找突破。
题目所给信息一般分为四类:条件、结构简式、分子式、特征现象。
常见的突破口有:反应条件[浓硫酸(酯化、硝化、纤维素水解等)、稀硫酸(酯、蔗糖、淀粉水解等)、O2/Cu(Ag)/△(醇氧化)、X2/FeX3(苯环上溴代)、X2/ 光照(烷基上取代等)、H2/催化剂(加成反应)];实验现象[能与Na 反应(含羟基或羧基)、能与NaOH 反应(含羧基或酚羟基)、能与NaHCO3 反应(含羧基)、能发生银镜反应(含醛基、)能与新制Cu(OH)2 共热产生砖红色沉淀(含醛基)、使酸性KMnO4 溶液褪色(含不饱和键、含醛基)]。
依据分子式及其组成的变化、官能团的衍变、原子个数的变化、特殊的转化关系、题目所给新信息等进行串联。
联系所学整合题给信息和已知,正推、逆推相结合,攻克关键中间产物,正推法的思维程序是原料→中间产物→产品,始终关注已知信息的痕迹,逆推法的思维程序是产品→中间产物→原料,在高考中往往需要正推逆推加已知相结合即从两边往中间推,在关键的中间产物上形成交集,最后全面突破,理顺合成路线。
浙江省名校新高考研究联盟(Z20联盟)2019届第二次联考化学含答案

浙考神墙750微信公众号提供2.下列仪器名称为oA. 分液漏斗”B.的是C. Na20D. S02C. CH^COOHD. CaC52B. H2+F2 = 2HFD. 2Na202+2H20=4Na0H+02T第26题第(3)小题中的”E十G4F”改为”E十G4H”绝密★考试结束前(高三返校联考)浙江省名校新高考研宄联盟(Z20联盟)2019届第二次联考化学试题卷命题:路桥中学陈晓與、陈玲文审校:德清高级中学陆燕海榈乡高级中学金圆林校对:林珍珍、陈秀珍本试题卷分选择题和非选择题两部分,共9页,满分100分,考试时间90分钟。
其中加试题部分为30分,用【加试题】标出。
考生注意:1.答题前,请务必将自己的姓名、准考证号用黑色字迹的签字笔或钢笔分别填写在试题卷和答题纸规定的位置上。
2.答题时,请按照答题纸上“注意事项”的要求,在答题纸相应的位置上规范作答,在本试题卷上的作答一律无效。
3.非选择题的答案必须使用黑色字迹的签字笔或钢笔写在答题纸上相应区域内,作图时可先使用2B铅笔,确定后必须使用黑色字迹的签字笔或钢笔描黑,答案写在本试题卷上无效。
4.可能用到的相对原子质量:H 1 C 12 N 14 0 16 Na 23 Mg 24 A1 27 Si 28 S 32 Cl 35.5 K 39 Ca 40 Fe 56Cu 64 Zn 65 Ag 108 Ba 137选择题部分—、选择题(本题共25小题,每小题2分,共50分。
每小题列出的四个备选项中只有一个是符合题目要求的,不选、多选、错选均不得分)1.下列属于酸性氧化物的是A. COB. KN033.下列物质属于弱电解质的是A.CuB.蔗糖4.下列反应既是氧化还原反应又是分解反应的是A.2H2O2=2H20+O21'C. 2Fe(OFT)3= Fe203+3H205.下列物质的水溶液因水解而显酸性的是A.HCIOB. CuS04C. Na2C03D. NaHS046.下列说法屮正确的是A.为了防止食品受潮,常在食品袋中放入还原性铁粉B.由于N a HC03受热笏分)»,因此常用于制胃酸中和剂C.镁合金密度小,但硬度和强度都大,被大量用子制造火箭、导弹和飞机的部件D.用Si02制造光导纤维是利用了 &02的高熔点\W 2 8 7 7. 下列化学用语表示正确的是A. CI 的结构示S 图: C. 醛基的结构简式:一COH 8.适量下列物质,能使品红溶液褪色的是A. 稀硫酸B.亚硫酸溶液B. HC1 的电子式:H'[ : Cl :]" D.甲烷的结构式:C —H 4C. 食盐水D. Na 2S04溶液9.下列有关说法不正确的是 A. 煤的气化、液化、千馏是煤综合利用的主要方法 B. 氢能的开发首先要解决由水制备氧气的能耗等问题 C. 大自然利用太阳能最成功的是植物的光合作用 D. 光一生物质能转换的本质是光一热转换10. 下列说法正确的是A. 向溴水中滴加苯,振荡,出现分层,上层橙红色,说明苯分子中不存在碳碳双键B. 在配制lOOmLOJ mol L _lNa 2C03溶液时,固体溶解、溶液转移中玻璃棒的作用相同 C.分离KC1和Mn02的固体混合物,可先加水溶解,过滤得到Mn02,蒸十滤液得到KC1 D. 在热、强酸、福尔马林等作用下,鸡蛋清溶液会发生凝聚,这种现象称为蛋白质的变性, 变性的蛋白质都不可食用11. 下列说法正确的是A. C 6H l4的同分异构体共有5种B. H 20、H 202互为同素异形体C. 氏、CHd> C2H6互为同系物CHjD.CH 3CH 2(^HCHCH 3的名称为: 3,4-二甲基戊烷 CH 312. 在一定条件下,密闭容器中发生X(g)+2Y(g)^^Z(g)△奸= 一akJ mol _l(a>0),反应过稈中速率随时间的变化如图所示, 下列说法不屯,的是A. ?i 时刻X 的正反应速率等于Z 的正反应速率 B. /2时刻可逆反应达到T-衡状态C. 时刻以后,平均反应速率为0,说明反应不再发生D.0〜t2时间内反应放出的热量可能是akJ13. 短周期元素X 、Y 、Z 、W 在元素周期表中的相对位置如图所示,W 是同周期主族元素中原子半 径最小的,下列说法正确的是 A. W 位于第3周期VII 族B. 原子半径Z>Y>XC. Y 的非金屈性比W 强,所以Y 的最高价氧化物的水化物的酸性比W 的强D.X 、Y 、Z 、W 的简单氢化物中X 的沸点最髙14.下列离子方程式不年寧的是A.实验室用过量NaOH溶液吸收二氧化硫气体: 20H_ + S02 = S0f+H20B.久置的—氧化硫水溶液滴加BaCb溶液出现&色沉淀:Ba2+ + S0r = BaS04C.小苏打溶液中加入足量的澄清石灰水:HCO3" + 0H-+Ca2+ = CaCO)i + H2OD.在淀粉碘化钾溶液中加入稀硫酸酸化,再通入C102气体,溶液变蓝:2ClO2+l0r + 8H+ = 5l2+2Cr+4H2O15.在中学化学中,下列物质间的转化不|.g—步实现的是A.HiSiCh一NasSiOjB.Mg^Mg(OH)2C.S—S03D.FeCb^FeCb16.下列说法正确的是A.乙醇、乙酸、乙酸乙酯都能发生取代反应B.相同物质的量的苯和正四面体烷(C4H4)完全燃烧消耗氧气的量也相同C.叱油、汽油、花生油含有相同的官能团,具有相似的化学性质D.淀粉和纤维素都属于糖类,但水解产物不同,前者是葡萄糖,后者是果糖17.锂硫电池是一种非常有前景的锂电池。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(浙江选考)2019版高考化学-考前提升训练26-元素与物质推断(第27题)提升训练26 元素与物质推断(第27题)1.(2018·学军中学模拟)探究无机盐X(仅含三种短周期元素)的组成和性质,设计并完成如下实验:请回答:(1)X的化学式是。
(2)白色粉末溶于氢氧化钠溶液的离子方程式是。
(3)白色沉淀用途广泛,请列举一例:。
2.某新型无机材料A3M4由两种非金属元素组成,元素M位于第二周期第ⅤA族。
D、E、H均为难溶于水的白色固体,化合物C、E均含A元素。
其余物质均为中学化学中的常见物质。
请回答:(1)写出H的化学式:。
(2)化合物A3M4中含有的化学键类型为。
(3)写出反应②的离子方程式:。
3.为了探究不溶性盐X(仅含5种元素)的组成和性质,设计并完成如下实验(所加试剂均过量,气体体积均在标准状况下测定)。
请回答:(1)X的组成元素为H、O和(用元素符号表示),气体C的电子式为。
(2)写出反应①的离子方程式:。
4.为探究含结晶水的化合物X(含四种元素,摩尔质量为180 g·mol-1)的组成和性质,某兴趣小组设计并完成如下实验:请回答:(1)黑色固体Y的化学式为,气体C的电子式为。
(2)晶体X隔绝空气受热分解的化学方程式为。
5.某盐A是由三种元素组成的化合物,某研究小组按如图流程探究其组成:请回答:(1)写出红棕色固体C的化学式:。
(2)写出A受热分解反应的化学方程式:。
(3)写出检验A中阳离子的实验方案:。
6.为探究某矿物X(仅含三种元素)的组成,设计并完成了如下实验:已知:气体A能使品红溶液褪色,固体B中仅含CuO、Fe2O3。
请回答:(1)X的化学式为。
(2)溶液C中存在的阳离子有。
参考答案提升训练26 元素与物质推断(第27题)1.答案: (1)Mg2SiO4或2MgO·SiO2(2)SiO2+2OH-Si+H2O(3)优良的阻燃剂(答案合理即可)解析: 无机盐X(仅含三种短周期元素),加入过量盐酸溶解,离心分离得到白色胶状沉淀和无色溶液,白色胶状沉淀为硅酸,硅酸充分灼烧得到白色粉末1.80 g为SiO2,其物质的量==0.03 mol,溶于氢氧化钠溶液得到无色溶液为硅酸钠溶液,说明无机盐X中含Si或Si,且物质的量为0.03 mol,若为Si,则其质量=0.03 mol×76 g·mol-1=2.28 g,金属质量=4.20 g-2.28 g=1.92 g,无色溶液中加入过量氢氧化钠溶液生成白色沉淀,则沉淀为Mg(OH)2,则无机盐X中含镁元素的物质的量==0.06 mol,质量为0.06 mol×24 g·mol-1=1.44 g,不符合要求,则无机盐X中含Si,其物质的量为0.03 mol,质量=0.03 mol×92 g·mol-1=2.76 g,金属质量为4.20 g-2.76 g=1.44 g,其物质的量=1.44 g÷24g·mol-1=0.06 mol,得到X为Mg2SiO4,则(1)X的化学式为Mg2SiO4或2MgO·SiO2;(2)白色粉末溶于氢氧化钠溶液的离子方程式是SiO2+2OH-Si+H2O;(3)氢氧化镁是优良的阻燃剂。
2.答案: (1)AgCl(2)共价键(3)SiO2+2OH-Si+H2O解析: 根据题中各物质转化关系,D受热得E,E 能与氢氧化钠溶液反应生成F,F与过量的二氧化碳反应生成D,说明D为弱酸且能受热分解;新型无机材料A3M4由两种非金属元素组成,元素M位于第2周期ⅤA族,应为氮元素,A元素在A3M4中显+4价,化合物C、E均含A元素,D、E、H均为难溶于水的白色固体,可知A3M4应为Si3N4,可以确定A为Si,E为SiO2,F为Na2SiO3,则D为H2SiO3,G与硝酸银溶液反应生成不溶于稀硝酸的沉淀H,则可知G中有Cl-,H为AgCl,故C为SiCl4,B为Cl2;由SiCl4+3H2O4HCl↑+H2SiO3↓,生成G(HCl)。
(1)H的化学式为AgCl;(2)化合物Si3N4中含有的化学键类型为共价键;(3)SiO2溶解于NaOH溶液发生反应的离子方程式为SiO2+2OH-Si+H2O。
3.答案: (1)N、S、Cu H····H(2)2NH4CuSO3+4H+Cu+Cu2++2SO2↑+2H2O+2N解析: A气体能使品红溶液褪色,应是SO2,物质的量是0.1 mol,说明X中含有亚硫酸根或亚硫酸氢根离子。
B是红色固体,应该是铜,物质的量是0.05 mol;蓝色溶液和氢氧化钠反应生成能使湿润的红色石蕊试纸变蓝的气体C和蓝色沉淀,说明C是氨气,物质的量是0.1 mol,即X中含有铵根;蓝色沉淀灼烧生成黑色固体D,D是氧化铜,物质的量是0.05 mol。
则X中铜离子、铵根和亚硫酸根(或亚硫酸氢根)的物质的量之比是1∶1∶1且均为0.1 mol,而0.1 molNH4CuSO3的质量恰好是16.2 g。
(1)根据以上分析可知X的组成元素为H、O、N、S、Cu,氨气的电子式为H····H。
(2)根据以上分析可知反应①的离子方程式为2NH4CuSO3+4H+Cu+Cu2++2SO2↑+2H2O+2N。
4.答案:(1)FeO ······C······(2)FeC2O4·2H2O FeO+CO↑+CO2↑+2H2O解析: 黑色固体Y与盐酸反应的产物遇KSCN溶液无明显现象,通入氯气后,溶液变为血红色,可知Y 为FeO,则FeO的物质的量n(FeO)==0.15 mol;混合气体与足量澄清石灰水反应生成15.0 g白色沉淀和气体B,B与足量的CuO反应生成气体C,C能与足量澄清石灰水反应生成15.0 g白色沉淀,根据原子守恒,可知混合气体中含有等物质的量的CO2和CO,即:n(CO)=n(CO2)=n(CaCO3)==0.15 mol。
结合X的物质的量n(X)==0.15 mol,X中含有H2O物质的量:n(H2O)===0.3 mol,则n(X)∶n(FeO)∶n(CO)∶n(CO2)∶n(H2O)=0.15 mol∶0.15 mol∶0.15 mol∶0.15 mol∶0.3 mol=1∶1∶1∶1∶2,推出:X的分子式为FeC2O4·2H2O。
(1)黑色固体Y的化学式为FeO,气体C(CO2)的电子式为······C······;(2)晶体X(FeC2O4·2H2O)隔绝空气受热分解的化学方程式为FeC2O4·2H2O FeO+CO↑+CO2↑+2H2O。
5.答案: (1)Fe2O3(2)2FeSO4Fe2O3+SO3↑+SO2↑(3)取少量试样配成溶液,滴入KSCN溶液,若不变色,再滴加少量氯水,出现血红色,证明有亚铁离子解析: 标准状况下448 mL气体B能与足量BaCl2溶液反应,产生2.33 g白色沉淀,则该气体中有SO3,2.33 g白色沉淀是BaSO4,物质的量为0.01mol,SO3的物质的量为0.01 mol,448 mL气体B的物质的量为0.02 mol,则气体B中还有0.01 mol SO2,红棕色固体C与盐酸反应生成黄色溶液,则红棕色固体C为Fe2O3,物质的量为1.6 g÷160 g·mol-1=0.01mol,氧化铁与盐酸反应生成氯化铁和水,氯化铁溶液呈黄色,化合物A中铁原子与硫原子的物质的量之比为1∶1,铁元素、硫元素质量和为(56+32) g·mol-1×0.02 mol=1.76 g,则盐A是由三种元素组成的化合物,另一种元素应为氧,质量为3.04 g-1.76 g=1.28 g,物质的量为0.08 mol,所以化合物中Fe、S、O的物质的量之比为1∶1∶4,A是FeSO4。
(1)根据上述分析,红棕色固体C为氧化铁,化学式为Fe2O3。
(2)根据上述分析,A为FeSO4,受热分解生成氧化铁、SO2和SO3,反应的化学方程式为2FeSO4Fe2O3+SO3↑+SO2↑。
(3)A为FeSO4,根据Fe2+的检验方法,检验FeSO4中Fe2+的实验方案是取少量试样配成溶液,滴入KSCN溶液,若不变色,再滴加少量氯水,溶液变为血红色,证明有亚铁离子。
6.答案: (1)Cu5FeS4(2)Fe3+、Cu2+、H+解析: (1)气体A能使品红溶液褪色,气体A应为SO2,固体B中仅含CuO、Fe2O3,并结合X中含有三种元素,可知X为S、Fe、Cu组成的化合物;固体B溶于足量稀盐酸生成FeCl3和CuCl2,往溶液C中加入5.0 g Cu,剩余1.8 g Cu,则溶解3.2 g Cu,其物质的量为0.05 mol,根据Cu+2Fe3+Cu2++2Fe2+,可知固体B中含有Fe3+的物质的量为0.1 mol,Fe2O3的物质的量为0.05 mol,质量为0.05 mol×160 g·mol-1=8 g,则固体B中CuO的质量为40 g,其物质的量为0.5 mol,原固体X中S的物质的量为=0.4 mol,则化合物X中n(Fe)∶n(Cu)∶n(S)=0.1 mol∶0.5 mol∶0.4mol=1∶5∶4,X的化学式为Cu5FeS4;(2)CuO、Fe2O3溶于足量稀盐酸生成FeCl3和CuCl2溶液,则所得溶液C中存在的阳离子有Fe3+、Cu2+、H+。
