PCR 常见问题集锦
PCR常见问题、原因分析及其对策

镁离子浓度不当
总结词
镁离子是PCR反应的重要成分,对PCR的效率和产物质量有 重要影响。
详细描述
镁离子浓度过高可能导致非特异性扩增和产物稳定性下降; 镁离子浓度过低则可能影响DNA聚合酶的活性,导致PCR失 败或扩增效率低下。因此,需要根据实验条件和试剂盒推荐 ,选择合适的镁离子浓度。
03
pcr问题对策
详细描述
模板质量的好坏直接影响到pcr的扩增 效果,因此需要确保模板的纯度和浓 度,避免使用降解严重的模板,以提 高pcr的产量和特异性。
优化pcr循环参数
总结词
pcr循环参数的优化可以显著提高pcr的效率和特异性。
详细描述
通过调整变性、退火、延伸等温度和时间,可以优化pcr循环参数,提高pcr的效率和特异性。同时, 合理设置预变性时间和循环数,可以有效避免非特异性扩增和产物积累。
优化引物设计
总结词
引物设计是pcr反应的关键,优化引物设计可以显著提高pcr的特异性和效率。
详细描述
引物设计时需考虑特异性、长度、GC含量、引物二聚体和发夹结构等因素,通过合理设计引物,可以避免非特 异性扩增和引物二聚体形成,提高pcr的特异性。
提高模板质量
总结词
模板质量对pcr结果的影响不容忽视, 提高模板质量可以提高pcr的产量和特 异性。
模板质量差
总结词
模板质量的好坏直接影响到PCR的效率和产物质量。
详细描述
模板中可能含有抑制剂、DNA聚合酶抑制剂或DNA聚合酶竞争性抑制剂等物质, 这些物质会影响DNA聚合酶的活性,导致PCR失败或扩增效率低下。此外,模 板的浓度过低或过高也可能影响PCR结果。
pcr循环参数不当
总结词
PCR循环参数包括变性、退火、延伸等步骤,这些步骤 的温度和时间设置对PCR结果有重要影响。
PCR实验常见问题、原因分析及其解决方案

PCR实验常见问题、原因分析及其解决方案PCR产物的电泳检测时间,一般为48h以内,有些最好于当日进行检查,大于48h后带型不规则甚至消失。
但有时仍会与到这样那样的问题,影响检测结果的判断,具体归类为以下常见的4点,描述如下:问题一:无扩增产物现象:正对照有条带,而样品则无原因:1、模板:含有抑制物,含量低2、Buffer对样品不合适3、引物设计不当或者发生降解4、反应条件:退火温度太高,延伸时间太短对策:1、纯化模板或者使用试剂盒提取模板DNA或加大模板的用量2、更换Buffer或调整浓度3、重新设计引物(避免链间二聚体和链内二级结构)或者换一管新引物4、降低退火温度、延长延伸时间问题二:非特异性扩增现象:条带与预计的大小不一致或者非特异性扩增带原因:1、引物特异性差2、模板或引物浓度过高3、酶量过多4、Mg2+浓度偏高5、退火温度偏低6、循环次数过多对策:1、重新设计引物或者使用巢式PCR2、适当降低模板或引物浓度3、适当减少酶量4、降低镁离子浓度5、适当提高退火温度或使用二阶段温度法6、减少循环次数问题三:拖尾现象:产物在凝胶上呈Smear状态原因:1、模板不纯2、Buffer不合适3、退火温度偏低4、酶量过多5、dNTP、Mg 2+浓度偏高6、循环次数过多对策:1、纯化模板2、更换Buffer3、适当提高退火温度4、适量用酶5、适当降低dNTP和镁离子的浓度6、减少循环次数问题四:假阳性现象:空白对照出现目的扩增产物原因:靶序列或扩增产物的交叉污染对策:1、操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外;2、除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3、各种试剂最好先进行分装,然后低温贮存[ 来源]:实验室之家,以及相关网络知识、转载仅为分享知识,如有侵权请联系删除。
}热文推荐:1、化学分析方法确认和验证指南PDF版全文(新版2018年4月1日实施)2、最全微生物实验室规划设计方案3、谱知识总结篇4、移液器操作六部曲,这些细节很重要化学先生(号码:chemistrysir),化学检测工作者自己的公众号。
PCR常见问题分析及对策

.PCR常见问题分析及对策(无扩增产物、非特异性扩增、拖尾、假阳性) 问题1:无扩增产物现象:正对照有条带,而样品则无原因:1.模板:含有抑制物,含量低2.Buffer对样品不合适3.引物设计不当或者发生降解4.反应条件:退火温度太高,延伸时间太短对策:1.纯化模板或者使用试剂盒提取模板DNA或加大模板的用量2.更换Buffer或调整浓度3.重新设计引物(避免链间二聚体和链内二级结构)或者换一管新引物4.降低退火温度、延长延伸时间问题2:非特异性扩增现象:条带与预计的大小不一致或者非特异性扩增带原因:1.引物特异性差2.模板或引物浓度过高3.酶量过多4.Mg2+浓度偏高5.退火温度偏低.6.循环次数过多对策:1.重新设计引物或者使用巢式PCR2.适当降低模板或引物浓度3.适当减少酶量4.降低镁离子浓度5.适当提高退火温度或使用二阶段温度法6.减少循环次数问题3:拖尾现象:产物在凝胶上呈Smear状态。
原因:1.模板不纯2.Buffer不合适3.退火温度偏低4.酶量过多5.dNTP、Mg 2+浓度偏高6.循环次数过多对策:1.纯化模板2.更换Buffer3.适当提高退火温度4.适量用酶5.适当降低dNTP和镁离子的浓度6.减少循环次数问题4:假阳性现象:空白对照出现目的扩增产物原因:靶序列或扩增产物的交*污染对策:1.操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外;2.除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3.各种试剂最好先进行分装,然后低温贮存PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。
假阴性,不出现扩增条带PCR反应的关键环节有①模板核酸的制备,②引物的质量与特异性,③酶的质量及,④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
模板:①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
PCR常见问题总汇

PCR常见问题总汇PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。
假阴性,不出现扩增条带PCR反应的关键环节有:①模板核酸的制备,②引物的质量与特异性,③酶的质量,④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
模板:①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
⑤模板核酸变性不彻底。
在酶和引物质量好时,不出现扩增带,极有可能是标本的消化处理,模板核酸提取过程出了毛病,因而要配制有效而稳定的消化处理液,其程序亦应固定不宜随意更改。
酶失活:需更换新酶,或新旧两种酶同时使用,以分析是否因酶的活性丧失或不够而导致假阴性。
需注意的是有时忘加Taq酶或溴乙锭。
引物:引物质量、引物的浓度、两条引物的浓度是否对称,是PCR失败或扩增条带不理想、容易弥散的常见原因。
有些批号的引物合成质量有问题,两条引物一条浓度高,一条浓度低,造成低效率的不对称扩增,对策为:①选定一个好的引物合成单位。
②引物的浓度不仅要看OD值,更要注重引物原液做琼脂糖凝胶电泳,一定要有引物条带出现,而且两引物带的亮度应大体一致,如一条引物有条带,一条引物无条带,此时做PCR有可能失败,应和引物合成单位协商解决。
如一条引物亮度高,一条亮度低,在稀释引物时要平衡其浓度。
③引物应高浓度小量分装保存,防止多次冻融或长期放冰箱冷藏部分,导致引物变质降解失效。
④引物设计不合理,如引物长度不够,引物之间形成二聚体等。
Mg2+浓度:Mg2+离子浓度对PCR扩增效率影响很大,浓度过高可降低PCR扩增的特异性,浓度过低则影响PCR扩增产量甚至使PCR扩增失败而不出扩增条带。
反应体积的改变:通常进行PCR扩增采用的体积为20ul、30ul、50ul。
或100ul,应用多大体积进行PCR扩增,是根据科研和临床检测不同目的而设定,在做小体积如20ul 后,再做大体积时,一定要摸索条件,否则容易失败。
PCR常见问题分析及对策
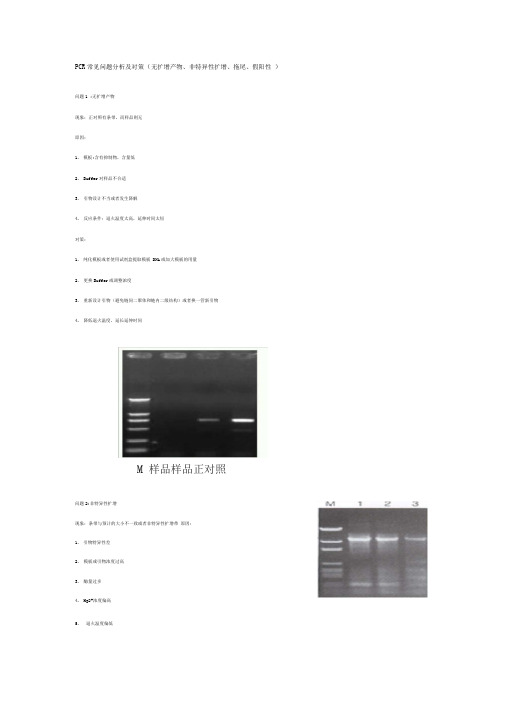
PCR常见问题分析及对策(无扩增产物、非特异性扩增、拖尾、假阳性)问题1 :无扩增产物现象:正对照有条带,而样品则无原因:1.模板:含有抑制物,含量低2.Buffer对样品不合适3.引物设计不当或者发生降解4.反应条件:退火温度太高,延伸时间太短对策:1.纯化模板或者使用试剂盒提取模板DNA或加大模板的用量2.更换Buffer或调整浓度3.重新设计引物(避免链间二聚体和链内二级结构)或者换一管新引物4.降低退火温度、延长延伸时间M 样品样品正对照问题2:非特异性扩增现象:条带与预计的大小不一致或者非特异性扩增带原因:1.引物特异性差2.模板或引物浓度过高3.酶量过多4.Mg2+浓度偏高5.退火温度偏低6.循环次数过多对策:1.重新设计引物或者使用巢式PCR2.适当降低模板或引物浓度3.适当减少酶量4.降低镁离子浓度5.适当提高退火温度或使用二阶段温度法6.减少循环次数问题3:拖尾现象:产物在凝胶上呈Smear状态原因:1.模板不纯2.Buffer不合适3.退火温度偏低4.酶量过多5.dNTP、Mg 2+浓度偏高6.循环次数过多对策:1.纯化模板2.更换Buffer3.适当提高退火温度4.适量用酶5.适当降低dNTP和镁离子的浓度6.减少循环次数问题4:假阳性现象:空白对照出现目的扩增产物原因:靶序列或扩增产物的交*污染对策:1.操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外;2.除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3.各种试剂最好先进行分装,然后低温贮存PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。
假阴性,不出现扩增条带PCR反应的关键环节有①模板核酸的制备,②引物的质量与特异性,③酶的质量及,④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
模板:①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
PCR实验常见问题、原因分析及其解决方案!

PCR实验常见问题、原因分析及其解决方案!PCR产物的电泳检测时间,一般为48h以内,有些最好于当日进行检查,大于48h后带型不规章甚至消逝。
但有时仍会与到这样那样的问题,影响检测结果的推断,详细归类为以下常见的4点,描述如下:问题一:无扩增产物现象:正对比有条带,而样品则无。
缘由:1、模板:含有抑制物,含量低。
2、Buffer对样品不合适。
3、引物设计不当或者发生降解。
4、反应条件:退火温度太高,延长时间太短。
对策:1、纯化模板或者使用试剂盒提取模板DNA或加大模板的用量。
2、更换Buffer或调整浓度。
3、重新设计引物(避开链间二聚体和链内二级结构)或者换一管新引物。
4、降低退火温度、延长延长时间。
问题二:非特异性扩增现象:条带与估计的大小不全都或者非特异性扩增带。
缘由:1、引物特异性差。
2、模板或引物浓度过高。
3、酶量过多。
4、Mg2+浓度偏高。
5、退火温度偏低。
6、循环次数过多。
对策:1、重新设计引物或者使用巢式PCR。
2、适当降低模板或引物浓度。
3、适当削减酶量。
4、降低镁离子浓度。
5、适当提高退火温度或使用二阶段温度法。
6、削减循环次数。
问题三:拖尾现象:产物在凝胶上呈Smear状态。
缘由:1、模板不纯。
2、Buffer不合适。
3、退火温度偏低。
4、酶量过多。
5、dNTP、Mg 2+浓度偏高。
6、循环次数过多。
对策:1、纯化模板。
2、更换Buffer。
3、适当提高退火温度。
4、适量用酶。
5、适当降低dNTP和镁离子的浓度。
6、削减循环次数。
问题四:假阳性现象:空白对比消失目的扩增产物。
缘由:靶序列或扩增产物的交叉污染。
对策:1、操作时应当心轻柔,防止将靶序列吸入加样枪内或溅出离心管外。
2、除酶及不能耐高温的物质外,全部试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3、各种试剂最好先进行分装,然后低温贮存。
PCR常见问题总汇

PCR常见问题总汇PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。
假阴性,不出现扩增条带PCR反应的关键环节有①模板核酸的制备,②引物的质量与特异性,③酶的质量及,④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
模板:①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
⑤模板核酸变性不彻底。
在酶和引物质量好时,不出现扩增带,极有可能是标本的消化处理,模板核酸提取过程出了毛病,因而要配制有效而稳定的消化处理液,其程序亦应固定不宜随意更改。
酶失活:需更换新酶,或新旧两种酶同时使用,以分析是否因酶的活性丧失或不够而导致假阴性。
需注意的是有时忘加Taq酶或溴乙锭。
引物:引物质量、引物的浓度、两条引物的浓度是否对称,是PCR失败或扩增条带不理想、容易弥散的常见原因。
有些批号的引物合成质量有问题,两条引物一条浓度高,一条浓度低,造成低效率的不对称扩增,对策为:①选定一个好的引物合成单位。
②引物的浓度不仅要看OD值,更要注重引物原液做琼脂糖凝胶电泳,一定要有引物条带出现,而且两引物带的亮度应大体一致,如一条引物有条带,一条引物无条带,此时做PCR有可能失败,应和引物合成单位协商解决。
如一条引物亮度高,一条亮度低,在稀释引物时要平衡其浓度。
③引物应高浓度小量分装保存,防止多次冻融或长期放冰箱冷藏部分,导致引物变质降解失效。
④引物设计不合理,如引物长度不够,引物之间形成二聚体等。
Mg2+浓度:Mg2+离子浓度对PCR扩增效率影响很大,浓度过高可降低P CR扩增的特异性,浓度过低则影响PCR扩增产量甚至使PCR扩增失败而不出扩增条带。
反应体积的改变:通常进行PCR扩增采用的体积为20ul、30ul、50ul。
或100ul,应用多大体积进行PCR扩增,是根据科研和临床检测不同目的而设定,在做小体积如20ul 后,再做大体积时,一定要模索条件,否则容易失败。
PCR常见问题及解决方法

PCR常见问题及解决方法PCR常见问题及解决方法1)、不出现扩增条带a)、引物设计有误:核对引物设计方案。
b)、扩增体系配制错误:重复实验。
c)、扩增反应条件不优化:调整Mg2+浓度、酶量、扩增程序。
d)、模板质粒质量偏差:长期放置、反复冻融会导致模板质粒断裂、开环或降解,应使用新鲜制备的质粒作为模板。
e)、模板的GC含量:GC含量过高会导致DNA的双链无法完全打开,此时加入Vazyme(诺唯赞生物)的PCR Enhancer(货号P021)可以有效降低解链温度;GC 含量过低会导致扩增效率较差,可适当延长引物长度或通过TD PCR摸索合适的反应条件。
2)、出现非特异性扩增带a)、引物设计不够优化:引物与靶序列有非特异性互补或自身聚合成二聚体,可降低引物浓度进行优化,必要时重新设计引物。
b)、模板不纯:模板被污染,需重新制备模板。
c)、试验条件不够优化:如果出现比目的条带小的杂带,可通过提高退火温度、降低循环数调整;如果出现比目的条带大的杂带,可缩短延伸时间、降低循环数;另外,可降低Mg2+及酶的浓度。
3)、条带弥散或拖尾a)、模板降解或过量:可通过电泳检查模板完整性及浓度,必要时重新纯化模板,对于简单模板(例如质粒、λDNA),每50ul反应使用1pg-10ng DNA;对于复杂模板(例如基因组、cDNA),每50ul反应使用1ng-1ug DNA。
b)、酶量加太多:如Vazyme(诺唯赞生物)的高保真系列:50ul反应体系加1U,Taq系列:50ul体系加2U。
4)、条带很暗a)、增加模板量,提高循环数。
b)、多扩几管,胶回收浓缩。
5)、产物有错配a)、检查原始模板是否原本就是突变或错配的。
b)、少量序列存在非严谨序列,有相似重组序列,导致重组错位。
PCR实验中常见问题解决方法

QuikStrip 已变干。
加入 40 μL 水,在装载前轻轻上下移液以混合均匀。
3.电泳凝胶上看不到条带、对照 DNA 和PCR 产物
凝胶未正确制备。
确保正确稀释电泳缓冲液。
融化琼脂糖时需要特别注意较高浓度 (>0.8%) 的凝胶。在倒入凝胶之前,确保溶液 没有“团块 ”和玻璃状颗粒,也可以直接使用配置好的预制胶。省时省力。
凝胶未正确染色。
染色时注意浓度,实在不行就重新染色。
电泳装置或电源出现故障。
请联系电泳仪或电泳设备供应商,帮忙排除故障
4.凝胶染色后,DNA 条带模糊。
凝胶没有染色足够长的时间。
严格按照染色流程说明进行实验操作。
5.染色后,条带可见,但不存在 PCR 产物。
PCR扩增不成功。
注意引物设计是否合理,DNA聚合酶的加入量是否适宜。
PCR实验中常见问题解决方法
PCR实验中常见问题及解决方案
PCR实验中常见问题汇总
问题,管中的液体较少。
样品挥发,损失
确保加热的盖子达到适当的温度。
吸取样本后,尽快盖上PCR 管的盖子。防止挥发。
移液不准确
确保吸取 20 µL 引物混合物和 5 µl Lambda DNA 模板到 PCR 管中。样本量少时需要采用高精度移液器。
确保PCR的正确操作,温度设计是否合理。
6.染色后,凝胶上可见条带和对照 PCR 产物,其中一部分样品不存在。
PCR 反应中添加了错误体积的 DNA 和引物。
熟练使用移液器进行精准移液定量,确保移液的准确度
PCR 常见问题及解决方案

PCR 常见问题及解决方案1没有扩展条带可能的原因及对应的解决方案如下:酶失活或在反应体系中未加入酶。
Taq DNA 聚合酶因保存或运输不当而失活,往往通过更换新酶或用另一来源的酶以获得满意的结果。
模板含有杂质。
特别是对甲醛固定及石蜡包埋的组织常含甲酸,造成DNA 脱嘌呤而影响PCR 的结果。
变性温度是否准确:PCR 仪指示温度与实际温度是否相符,过高酶在前几个循环就迅速失活;过低则模板变性不彻底。
反应系统中污染了蛋白酶及核酸酶,应在未加Taq 酶以前,将反应体系95℃加热5~10 分钟。
引物变质失效。
人工合成的引物是否正确。
是否纯化,或因储存条件不当而失活。
引物错误。
利用BLAST 检查引物特异性或重新设计引物。
DNA 凝胶电泳时加入阳性对照,确保不是DNA 凝胶和PCR 程序的问题。
2PCR 产物量过少可能的原因和对应的解决方案如下:退火温度不合适。
以 2 度为梯度设计梯度PCR 反应优化退火温度。
DNA 模板量太少。
增加DNA 模板量。
PCR 循环数不足。
增加反应循环数。
引物量不足。
增加体系中引物含量。
延伸时间太短。
以 1 kb/分钟的原则设置延伸时间。
变性时间过长。
变性时间过长会导致DNA 聚合酶失活。
DNA 模板中存在抑制剂。
确保DNA 模板干净3扩增产物跑电泳条带弥散可能的原因和对应的解决方案如下:酶量过高。
减少酶量;酶的质量差,调换另一来源的酶。
dNTP 浓度过高。
减少dNTP 的浓度。
MgCl₂浓度过高。
可适当降低其用量。
模板量过多。
质粒DNA 的用量应<50 ng,而基因组DNA 则应<200 ng。
引物浓度不够优化。
对引物进行梯度稀释重复PCR 反应。
循环次数过多;增加模板量减少循环次数至30,缩短退火时间及延伸时间,或改用二种温度的PCR 循环。
退火温度过低。
电泳体系有问题:①凝胶中缓冲液和电泳缓冲液浓度相差太大;②凝胶没有凝固好;③琼脂糖质量差。
若为PCR 试剂盒则可能:①由于运输储存不当引起试剂盒失效;②试剂盒本身质量有问题,如引物选择、循环参数等选择不当。
PCR常见问题及解决方案

一、普通PCR常见问题及解决对策PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h 后带型不规则甚致消失。
1. 假阴性,不出现扩增条带PCR反应的关键环节有①模板核酸的制备,②引物的质量与特异性,③酶的质量及活性④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
1.1 模板①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
⑤模板核酸变性不彻底。
在酶和引物质量好时,不出现扩增带,极有可能是标本的消化处理,模板核酸提取过程出了毛病,因而要配制有效而稳定的消化处理液,其程序亦应固定不宜随意更改。
1.2 酶失活需更换新酶,或新旧两种酶同时使用,以分析是否因酶的活性丧失或不够而导致假阴性。
需注意的是有时忘加Taq酶或溴乙锭。
1.3 引物引物质量、引物的浓度、两条引物的浓度是否对称,是PCR失败或扩增条带不理想、容易弥散的常见原因。
有些批号的引物合成质量有问题,两条引物一条浓度高,一条浓度低,造成低效率的不对称扩增,对策为:①选定一个好的引物合成单位。
②引物的浓度不仅要看OD值,更要注重引物原液做琼脂糖凝胶电泳,一定要有引物条带出现,而且两引物带的亮度应大体一致,如一条引物有条带,一条引物无条带,此时做PCR有可能失败,应和引物合成单位协商解决。
如一条引物亮度高,一条亮度低,在稀释引物时要平衡其浓度。
③引物应高浓度小量分装保存,防止多次冻融或长期放冰箱冷藏部分,导致引物变质降解失效。
④引物设计不合理,如引物长度不够,引物之间形成二聚体等。
1.4 Mg2+浓度Mg2+离子浓度对PCR扩增效率影响很大,浓度过高可降低PCR扩增的特异性,浓度过低则影响PCR扩增产量甚至使PCR扩增失败而不出扩增条带。
1.5 反应体积的改变通常进行PCR扩增采用的体积为20ul、30ul、50ul。
或100ul,应用多大体积进行PCR扩增,是根据科研和临床检测不同目的而设定,在做小体积如20ul后,再做大体积时,一定要模索条件,否则容易失败。
PCR常见问题

PCR常见问题PCR常见问题分析及对策(无扩增产物、非特异性扩增、拖尾、假阳性)2009-03-28 11:38问题1:无扩增产物现象:正对照有条带,而样品则无原因:1.模板:含有抑制物,含量低2.Buffer对样品不合适3.引物设计不当或者发生降解4.反应条件:退火温度太高,延伸时间太短对策:1.纯化模板或者使用试剂盒提取模板DNA或加大模板的用量2.更换Buffer或调整浓度3.重新设计引物(避免链间二聚体和链内二级结构)或者换一管新引物4.降低退火温度、延长延伸时间问题2:非特异性扩增现象:条带与预计的大小不一致或者非特异性扩增带原因:1.引物特异性差2.模板或引物浓度过高3.酶量过多4.Mg2+浓度偏高5.退火温度偏低6.循环次数过多对策:1.重新设计引物或者使用巢式PCR2.适当降低模板或引物浓度3.适当减少酶量4.降低镁离子浓度5.适当提高退火温度或使用二阶段温度法6.减少循环次数问题3:拖尾现象:产物在凝胶上呈Smear状态。
原因:1.模板不纯2.Buffer不合适3.退火温度偏低4.酶量过多5.dNTP、Mg 2+浓度偏高6.循环次数过多对策:1.纯化模板2.更换Buffer3.适当提高退火温度4.适量用酶5.适当降低dNTP和镁离子的浓度6.减少循环次数问题4:假阳性现象:空白对照出现目的扩增产物原因:靶序列或扩增产物的交*污染对策:1.操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外;2.除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3.各种试剂最好先进行分装,然后低温贮存PCR引物设计的黄金法则(转自tiangen)1.引物最好在模板cDNA的保守区内设计。
DNA序列的保守区是通过物种间相似序列的比较确定的。
在NCBI上搜索不同物种的基因,通过序列分析软件(比如DNAman)比对(Alignment),各基因相同的序列该基因的保守区2.引物长度一般在15~30碱基之间。
PCR常见问题分析及对策

PCR常见问题分析及对策(无扩增产物、非特异性扩增、拖尾、假阳性) 问题1:无扩增产物现象:正对照有条带,而样品则无原因:1.模板:含有抑制物,含量低2.Buffer对样品不合适3.引物设计不当或者发生降解4.反应条件:退火温度太高,延伸时间太短对策:1.纯化模板或者使用试剂盒提取模板DNA或加大模板的用量2.更换Buffer或调整浓度3.重新设计引物(避免链间二聚体和链内二级结构)或者换一管新引物4.降低退火温度、延长延伸时间问题2:非特异性扩增现象:条带与预计的大小不一致或者非特异性扩增带原因:1.引物特异性差2.模板或引物浓度过高3.酶量过多4.Mg2+浓度偏高5.退火温度偏低对策:1.重新设计引物或者使用巢式PCR2.适当降低模板或引物浓度3.适当减少酶量4.降低镁离子浓度5.适当提高退火温度或使用二阶段温度法6.减少循环次数问题3:拖尾现象:产物在凝胶上呈Smear状态。
原因:1.模板不纯2.Buffer不合适3.退火温度偏低4.酶量过多5.dNTP、Mg 2+浓度偏高6.循环次数过多对策:1.纯化模板2.更换Buffer3.适当提高退火温度4.适量用酶5.适当降低dNTP和镁离子的浓度6.减少循环次数问题4:假阳性现象:空白对照出现目的扩增产物原因:靶序列或扩增产物对策:1.操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外;2.除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3.各种试剂最好先进行分装,然后低温贮存PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。
假阴性,不出现扩增条带PCR反应的关键环节有①模板核酸的制备,②引物的质量与特异性,③酶的质量及,④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
模板:①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
PCR常见问题集锦

目的建议RT与PCR使用不同的引物或需要灵活选择PCR DNA聚合酶两步法RT-PCR系统高灵敏度一步法或两步法RT-PCR系统高特异性含有适当的DNA聚合酶的两步法RT-PCR系统或具有高保真Platinum Taq酶的一步法RT-PCR系统高保真度含有Pfx Taq酶的两步法RT-PCR系统长的反转录结果通常使用两步法RT-PCR系统可达到最佳结果含Elongase酶的一步法RT-PCR系统二、Generacer1. 如何针对Generacer试剂盒设计基因特异性引物(GSP)?使用5’或3’RACE试剂都需要至少一条基因特异性引物,您在设计引物时需要注意以下几点要求:*50-70%的GC含量,以提高引物熔点(Tm)*23-28个碱基长度,以提高引物特异性*降低3’端GC含量,将引物非特异性结合的可能性降至最低2. 为什么得不到RACE产物?*加入Hela对照*低质量的RNA模板*逆转录失败,SSII和SSIII非常适用于长模板cDNA的合成*目的基因丰度太低,可以通过提高PCR的循环次数来解决,建议使用巢式PCR*目的基因没有表达,可以通过使用两条GSPs来分析cDNA中是否含有目的基因*目的基因太长而不适合进行反转录,建议使用GeneRacer试剂盒中的Oligo dT来得到全长cDNA,使用随机引物或与模板的5’端尽可能近的GSP进行PCR。
*cDNA模板属于困难模板,可以通过以下方法解决:优化PCR反应参数及反应体系;降低退火温度;使用5-10%的DMSO帮助通过高GC含量区;使用高保真度和高延伸能力的酶进行PCR反应。
3. RACE的PCR结果有杂带RACE PCR杂带或非特异性PCR条带可能是由于以下原因:*GSP与其他cDNA的非特异性结合会导致在扩增目的产物时得到无关产物。
*GeneRacer引物和cDNA的非特异性结合会导致产生一端带有GeneRacer引物序列的PCR产物。
PCR实验室常见问题及经验分享

PCR实验室常见问题及经验分享一、没有ct值二、ct值过晚三、阴性对照扩增有信号四、标准曲线不佳五、熔解曲线峰不特异六、扩增曲线异常七、扩增效率低聚合酶链式反应(PCR)是一种用于放大扩增特定的DNA片段的分子生物学技术,它可看作是生物体外的特殊DNA复制,PCR的最大特点是能将微量的DNA大幅增加。
一、没有ct值检测结果遇到没有Ct值情况,排查是否有以下问题:1、循环数不够(一般不超过45循环,不仅背景值提高,定量也不准);2、PCR程序设置错误,检测荧光信号的步骤有误。
一般SG法采用72℃延伸时采集,TaqMan法则一般在退火结束时或延伸时采集信号,另外荧光采集是否选中;3、引物或探针降解。
可通过PAGE电泳检测引物和探针是否降解;4、模板量可能降解或上样量不足(不超过500ng,根据试剂盒说明书即可),对未知浓度的样本应从系列稀释样本的最高浓度做起;如果发生模板降解,应考虑样本准备中杂质的引入及反复冻融的情况,建议将模板样本小量分装储备,避免反复冻融;5、引物探针是否合适(尤其是引物跨越内含子,以确保扩增基因组DNA;上下游引物Tm值超过4℃以上也会影响扩增)。
二、ct值过晚在相对定量中,Ct值一般控制在15—25之间比较好,如果在绝对定量中,对低拷贝数的样品,Ct值会增大,但是一般不宜超过40循环,否则定量不准确。
因此,判断Ct值出现过晚是否属于非正常情况,需要根据具体实验设计和目的进行。
1、扩增效率低。
引物之间或者引物和探针的比例不合适,需要进行优化;引物或探针设计不合理,需要重新设计;2、PCR程序不合适,改用三步法进行反应,或者优化退火/延伸温度,可以适当降低退火温度;退火/延伸时间短(可以在推荐的时间条件下延长10s);3、MgCl2浓度不合适,增加镁离子浓度等。
PCR各种反应成分的降解或加样量的不足;4、PCR产物太长。
PCR产物设计超过500bp;5、模板存在抑制物。
用高纯度模板进行PCR检测或将模板进行稀释。
PCR常见问题分析及对策
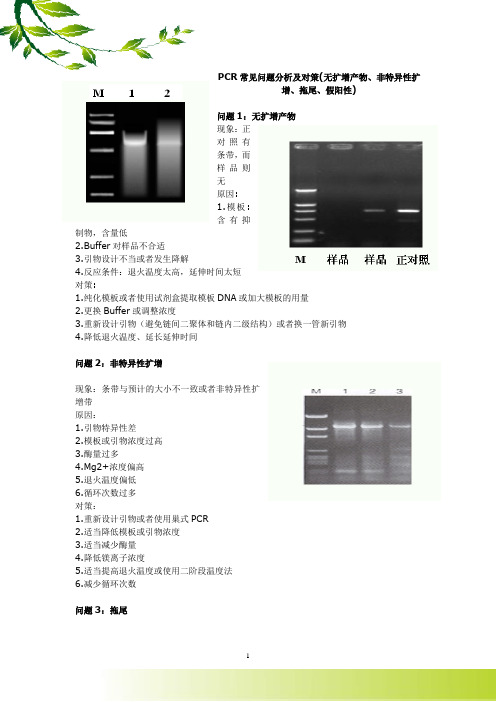
PCR常见问题分析及对策(无扩增产物、非特异性扩增、拖尾、假阳性)问题1:无扩增产物现象:正对照有条带,而样品则无原因:1.模板:含有抑制物,含量低2.Buffer对样品不合适3.引物设计不当或者发生降解4.反应条件:退火温度太高,延伸时间太短对策:1.纯化模板或者使用试剂盒提取模板DNA或加大模板的用量2.更换Buffer或调整浓度3.重新设计引物(避免链间二聚体和链内二级结构)或者换一管新引物4.降低退火温度、延长延伸时间问题2:非特异性扩增现象:条带与预计的大小不一致或者非特异性扩增带原因:1.引物特异性差2.模板或引物浓度过高3.酶量过多4.Mg2+浓度偏高5.退火温度偏低6.循环次数过多对策:1.重新设计引物或者使用巢式PCR2.适当降低模板或引物浓度3.适当减少酶量4.降低镁离子浓度5.适当提高退火温度或使用二阶段温度法6.减少循环次数问题3:拖尾现象:产物在凝胶上呈Smear状态。
原因:1.模板不纯2.Buffer不合适3.退火温度偏低4.酶量过多5.dNTP、Mg 2+浓度偏高6.循环次数过多对策:1.纯化模板2.更换Buffer3.适当提高退火温度4.适量用酶5.适当降低dNTP和镁离子的浓度6.减少循环次数问题4:假阳性现象:空白对照出现目的扩增产物原因:靶序列或扩增产物的交*污染对策:1.操作时应小心轻柔,防止将靶序列吸入加样枪内或溅出离心管外;2.除酶及不能耐高温的物质外,所有试剂或器材均应高压消毒。
所用离心管及加样枪头等均应一次性使用。
3.各种试剂最好先进行分装,然后低温贮存PCR引物设计的黄金法则(转自tiangen)1.引物最好在模板cDNA的保守区内设计。
DNA序列的保守区是通过物种间相似序列的比较确定的。
在NCBI上搜索不同物种的同一基因,通过序列分析软件(比如DNAman)比对(Alignment),各基因相同的序列就是该基因的保守区2.引物长度一般在15~30碱基之间。
PCR常见问题及解决策略

提高PCR反应特异性的策略
ห้องสมุดไป่ตู้
1.巢式PCR 2.递减PCR 3.热启动PCR 4.使用PCR增强剂
2、非特异性扩增
现象:条带 与预计的大 小不一致或 者非特异性 扩增带
原因分析及对策
原因
1. 2. 3. 4. 5. 6. 引物特异性差 模板或引物浓度过高 酶量过多 Mg2+浓度偏高 退火温度偏低 循环次数过多
对策
1. 重新设计引物或者使用巢式 PCR 2. 适当降低模板或引物浓度 3. 适当减少酶量 4. 降低镁离子浓度 5. 适当提高退火温度或使用 二阶段温度法 6. 减少循环次数
PCR常见问题及解决策略
内容
1 2 3
• PCR技术简介
• PCR常见问题、原因分析及对策
• 提高PCR反应特异性的策略
PCR三步曲
1 DNA 变性
(90℃-96℃): 双链DNA模板 在热作用下,氢 键断裂,形成单 链DNA
2 退 火
(60℃-65℃): 系统温度降低, 引物与DNA模 板结合,形成局 部双链。
现象:正对 照有条带, 而样品则无
原因分析及对策
原因
1. 模板:含有抑制物, 含量低 2. Buffer对样品不合适 3. 引物设计不当或者发 生降解 4. 反应条件:退火温度 太高,延伸时间太短
对策
1. 纯化模板或者使用试剂盒提 取模板DNA或加大模板的用 量
2. 更换Buffer或调整浓度 3. 重新设计引物(避免链间二 聚体和链内二级结构)或者 换一管新引物 4. 降低退火温度、延长延伸时 间
6. 减少循环次数
4、假阳性
M 1 2 3 4 5 6
PCR问题总汇及详细解决方案

PCR问题总汇及详细解决方案
PCR的影响因素很多的,尤其试剂的保存,人为的因素都很重要: 看看试剂是否有过期或保存不当,可能出现部分变质所以P不出来,换新的试剂看看
人为也很重要,冰上操作的时间,步骤等对P的效果很有影响,可找实验经验好点的人再试一试.
如果是怀疑仪器方面的问题,我觉得也有可能,可以去别的试验室借PCR仪看看是否能行.
别用自己的胶检测,用别人的胶检测试试,以前我P的很好,但是胶有问题老是扩散,后来用别人的胶试了试,非常赞.
本文针对PCR产物序列中引入了错误怎么办?PCR扩增有时出现涂抹带或片状带或地毯样带?如果没有回收到目的片段,还需要作什么对照实验?或者同时出现特异性扩增带与非特异性扩增带?对照实验结果好,却没有回收到目的片段,实验出了什么问题?
PCR体系是10ul的,每次PCR完了以后,管壁上有一层水气,需不需要覆盖矿务油?加多少,具体步骤应怎样?
PCR加样孔上有很亮的条带,但没有产物条带?
PCR的产量有许多因素决定他们的主次关系是什么,各因素又是怎么调节的?
PCR产物大约有900bP,哪种测序方法比较好?直接用纯化的PCR产物测序还是克隆到T载体上再测序?纯化PCR产物的方法哪种比较好?
引物间形成了比较多的二聚体,使产物很少。
这种情况该怎么处理?
为什么会产生弥散(smear)条带?如何解决?。
PCR常见问题总汇

PCR常见问题总汇PCR产物的电泳检测时间一般为48h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。
假阴性,不出现扩增条带PCR反应的关键环节有①模板核酸的制备,②引物的质量与特异性,③酶的质量及,④PCR循环条件。
寻找原因亦应针对上述环节进行分析研究。
模板:①模板中含有杂蛋白质,②模板中含有Taq酶抑制剂,③模板中蛋白质没有消化除净,特别是染色体中的组蛋白,④在提取制备模板时丢失过多,或吸入酚。
⑤模板核酸变性不彻底。
在酶和引物质量好时,不出现扩增带,极有可能是标本的消化处理,模板核酸提取过程出了毛病,因而要配制有效而稳定的消化处理液,其程序亦应固定不宜随意更改。
酶失活:需更换新酶,或新旧两种酶同时使用,以分析是否因酶的活性丧失或不够而导致假阴性。
需注意的是有时忘加Taq酶或溴乙锭。
引物:引物质量、引物的浓度、两条引物的浓度是否对称,是PCR失败或扩增条带不理想、容易弥散的常见原因。
有些批号的引物合成质量有问题,两条引物一条浓度高,一条浓度低,造成低效率的不对称扩增,对策为:①选定一个好的引物合成单位。
②引物的浓度不仅要看OD值,更要注重引物原液做琼脂糖凝胶电泳,一定要有引物条带出现,而且两引物带的亮度应大体一致,如一条引物有条带,一条引物无条带,此时做PCR有可能失败,应和引物合成单位协商解决。
如一条引物亮度高,一条亮度低,在稀释引物时要平衡其浓度。
③引物应高浓度小量分装保存,防止多次冻融或长期放冰箱冷藏部分,导致引物变质降解失效。
④引物设计不合理,如引物长度不够,引物之间形成二聚体等。
Mg2+浓度:Mg2+离子浓度对PCR扩增效率影响很大,浓度过高可降低PCR扩增的特异性,浓度过低则影响PCR扩增产量甚至使PCR扩增失败而不出扩增条带。
反应体积的改变:通常进行PCR扩增采用的体积为20ul、30ul、50ul。
或100ul,应用多大体积进行PCR扩增,是根据科研和临床检测不同目的而设定,在做小体积如20ul 后,再做大体积时,一定要模索条件,否则容易失败。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
PCR 常见问题集锦
1. cDNA产量的很低
可能的原因:
*RNA模板质量低
*对mRNA浓度估计过高
*反应体系中存在反转录酶抑制剂或反转录酶量不足
*同位素磷32过期
*反应体积过大,不应超过50μl
2. 扩增产物在电泳分析时没有条带或条带很浅
*最常见的原因在于您的反应体系是PCR的反应体系而不是RT-PCR的反应体系
*与反应起始时RNA的总量及纯度有关
*建议在试验中加入对照RNA
*第一链的反应产物在进行PCR扩增时,在总的反应体系中的含量不要超过1/10
*建议用Oligo(dT)或随机引物代替基因特异性引物(GSP)用于第一链合成。
由于RNA模板存在二级结构,如环状结果,有可能导致GSP无法与模板退火;或SSⅡ反转录酶无法从此引物进行有效延伸。
*目的mRNA中含有强的转录中止位点,可以试用以下方法解决:
a. 将第一链的反应温度提高至50℃。
b. 使用随机六聚体代替Oligo(dT)进行第一链反应。
3. 产生非特异性条带
*用RT阴性对照检测是否被基因组DNA污染。
如果RT阴性对照的PCR结果也显示同样条带,则需要用DNase I重新处理样品。
*在PCR反应中,非特异的起始扩增将导致产生非特异性结果。
在低于引物Tm 2至5℃的温度下进行退火,降低镁离子或是目的DNA的量将减少非特异性结果的产生。
*由于mRNA剪切方式的不同,根据选择引物的不同将导致产生不同的RT-PCR结果。
4. 产生弥散(smear)条带
*在PCR反应体系中第一链产物的含量过高
*减少引物的用量
*优化PCR反应条件/减少PCR的循环次数
*在用DNase处理被DNA污染的RNA样品时,其产生的寡核苷酸片段会产生非特异性扩增,一般会显示为弥散背景。
5. 产生大分子量的弥散条带
*大多数情况下是由于退火温度过低而导致的非特异性的起始及延伸产生的
*对于长片段的PCR,建议将反应体系中cDNA的浓度稀释至1:10(或1:100-1:200)
6. 在无反转录酶的情况下,对照RNA获得扩增结果
*通常是由于对照RNA中含有痕量DNA而导致的。
由于进行体外转录时不可能将所有的DNA 模板消除。
建议可将第一链cDNA稀释1:10、1:100、1:1000倍以消除DNA污染所造成的影响。
*有可能是引物二聚体的条带
7. 扩增产物滞留在加样孔中
*有可能是由于模板量过高而导致PCR结果产生了高分子量的DNA胶状物。
建议将第一链结果至少稀释100倍再进行二次扩增。
*另外,在二次PCR时使用的退火温度如果比引物的Tm值低5℃,可以将退火温度适当增高或进行热启动以提高特异性。
8. SSⅢ与SSⅡ有何不同?
*具有更高的热稳定性(达50℃)
*具有更长的半衰期(达220分钟)
*对PCR无抑制
*干冰运输
*Tdt活性更低
9. 为什么有人更喜欢用SSⅢ而不是ThermoScript?
ThermoScript如果保存不当会引起活性很快降低,SSⅢ则更稳定。
10. 为什么使用基因特异性引物(GSP)?
GSP在扩增低丰度的转录本时是最好的。
OligodT引物建议用于高质量RNA及全长转录本的逆转录;随机引物用于mRNA片段的逆转录。
11. 什么情况下需要使用RNase H?
在第一轮PCR中RNA/DNA杂合体不能正常变性时
12. 根据不同的目的选择不同的系统:
目的
建议
RT与PCR使用不同的引物
或需要灵活选择PCR DNA聚合酶
两步法RT-PCR系统
高灵敏度
一步法或两步法RT-PCR系统
高特异性
含有适当的DNA聚合酶的两步法RT-PCR系统
或具有高保真Platinum Taq酶的一步法RT-PCR系统
高保真度
含有Pfx Taq酶的两步法RT-PCR系统
长的反转录结果
通常使用两步法RT-PCR系统可达到最佳结果
含Elongase酶的一步法RT-PCR系统
二、Generacer
1. 如何针对Generacer试剂盒设计基因特异性引物(GSP)?
使用5’或3’RACE试剂都需要至少一条基因特异性引物,您在设计引物时需要注意以下几点要求:
*50-70%的GC含量,以提高引物熔点(Tm)
*23-28个碱基长度,以提高引物特异性
*降低3’端GC含量,将引物非特异性结合的可能性降至最低
2. 为什么得不到RACE产物?
*加入Hela对照
*低质量的RNA模板
*逆转录失败,SSII和SSIII非常适用于长模板cDNA的合成
*目的基因丰度太低,可以通过提高PCR的循环次数来解决,建议使用巢式PCR
*目的基因没有表达,可以通过使用两条GSPs来分析cDNA中是否含有目的基因
*目的基因太长而不适合进行反转录,建议使用GeneRacer试剂盒中的Oligo dT来得到全长cDNA,使用随机引物或与模板的5’端尽可能近的GSP进行PCR。
*cDNA模板属于困难模板,可以通过以下方法解决:优化PCR反应参数及反应体系;降低退火温度;使用5-10%的DMSO帮助通过高GC含量区;使用高保真度和高延伸能力的酶进行PCR反应。
3. RACE的PCR结果有杂带
RACE PCR杂带或非特异性PCR条带可能是由于以下原因:
*GSP与其他cDNA的非特异性结合会导致在扩增目的产物时得到无关产物。
*GeneRacer引物和cDNA的非特异性结合会导致产生一端带有GeneRacer引物序列的PCR 产物。
*RNA降解。
*PCR管或试剂污染。
注意:杂带一般是因为没有优化PCR条件,可以加入阴性对照来确定。
4. 得不到全长的5’RACE PCR产物
*CIP反应后的RNA降解产生了新的带有5’磷酸的断裂模板,可以同GeneRacer RNA Oligo连接。
一定要小心操作,保证RNA无降解。
*CIP脱磷酸不完全,可以增加反应中CIP的量或减少RNA的量。
*PCR产生了杂带,并不是真正的连接产物,可以使用上述建议优化PCR。
二、Generacer
1. 如何针对Generacer试剂盒设计基因特异性引物(GSP)?
使用5’或3’RACE试剂都需要至少一条基因特异性引物,您在设计引物时需要注意以下几点要求:
*50-70%的GC含量,以提高引物熔点(Tm)
*23-28个碱基长度,以提高引物特异性
*降低3’端GC含量,将引物非特异性结合的可能性降至最低
2. 为什么得不到RACE产物?
*加入Hela对照
*低质量的RNA模板
*逆转录失败,SSII和SSIII非常适用于长模板cDNA的合成
*目的基因丰度太低,可以通过提高PCR的循环次数来解决,建议使用巢式PCR
*目的基因没有表达,可以通过使用两条GSPs来分析cDNA中是否含有目的基因
*目的基因太长而不适合进行反转录,建议使用GeneRacer试剂盒中的Oligo dT来得到全长cDNA,使用随机引物或与模板的5’端尽可能近的GSP进行PCR。
*cDNA模板属于困难模板,可以通过以下方法解决:优化PCR反应参数及反应体系;降低退火温度;使用5-10%的DMSO帮助通过高GC含量区;使用高保真度和高延伸能力的酶进行PCR反应。
3. RACE的PCR结果有杂带
RACE PCR杂带或非特异性PCR条带可能是由于以下原因:
*GSP与其他cDNA的非特异性结合会导致在扩增目的产物时得到无关产物。
*GeneRacer引物和cDNA的非特异性结合会导致产生一端带有GeneRacer引物序列的PCR 产物。
*RNA降解。
*PCR管或试剂污染。
注意:杂带一般是因为没有优化PCR条件,可以加入阴性对照来确定。
4. 得不到全长的5’RACE PCR产物
*CIP反应后的RNA降解产生了新的带有5’磷酸的断裂模板,可以同GeneRacer RNA Oligo连接。
一定要小心操作,保证RNA无降解。
*CIP脱磷酸不完全,可以增加反应中CIP的量或减少RNA的量。
*PCR产生了杂带,并不是真正的连接产物,可以使用上述建议优化PCR。
三、PCR
在进行PCR时:
*请确保您没有使用过量的起始DNA或者过高浓度的引物,也没有加入过量的Mg++
*请确保您使用了恰当的退火温度
*请确保您没有使用过量的DNA聚合酶
四、引物
1. 应该选择哪种纯化方法?
取决于实验目的和引物的长度
2. 为什么我订购了50nmol,但是收到却只有40nmol?
50nmol是起始量
3. 怎样制备100μM的储液?
体积(μl)=质检报告上的nmol数目×10
4. 怎样设计引物?
*一般长度20-30bp;
*至少50的GC含量;
*避免引物二聚体和二级结构;
*引物对的Tm值应该接近。
5. 引物序列有插入或缺失?
*使用上游和下游引物多测几个克隆。
*请选择正确的纯化方法。
6. PCR无结果?
*请检查引物设计是否正确;
*请检测OD读数是否正确;
*做一个阳性对照和一个阴性对照。
