Suzuki_3568_001
Suzuki反应

文档经典化学合成反应标准操作Suzuki 反应编者:刘德军、武伟药明康德新药开发有限公司化学合成部目录1 前言 (3)1.1 Suzuki反应的通式 (3)1.2 Suzuki反应的机理 (3)1.3 Suzuki反应的特点及研究方向 (4)2 有机硼试剂的合成 (4)2.1 通过金属有机试剂制备单取代芳基硼酸 (4)2.1.1 通过Grinard试剂制备单取代芳基硼酸示例 (4)2.1.2 通过有机锂试剂制备单取代芳基硼酸示例 (6)2.2 通过二硼烷频哪酯制备芳基硼酸酯 (6)2.2.1 通过二硼烷频哪酯制备芳基硼酸酯示例(一) (10)2.2.2 通过二硼烷频哪酯制备芳基硼酸酯示例(二) (10)2.2.3 通过芳基硼酸转化为芳基硼酸酯 (10)2.3 烯基硼酸酯的制备 (10)2.4 烷基硼酸酯的制备 (11)3 催化剂的制备 (11)3.1 Pd(PPh3)4的制备 (11)3.2 Pd(PPh3)2Cl2的制备 (12)3.3 Pd(dppf)Cl2的制备 (13)4Suzuki偶联的应用 (13)4.1 普通的芳卤和芳基硼酸的Suzuki偶联 (14)4.1.1 Pd(PPh3)4-Na2CO3-DME-H2O 体系Suzuki偶联反应示例 (14)4.2 大位阻芳基硼酸参与Suzuki偶联反应 (15)4.3 含敏感功能团的芳基硼酸(酯)参与Suzuki偶联反应 (16)4.3.1 芳基硼酸频哪酯和芳基卤代物的Suzuki偶联 (16)4.3.2 带着酯基底物的Suzuki偶联反应示例(一) (17)4.3.3 带着酯基底物的Suzuki偶联反应示例(二) (17)4.4 杂环芳基硼酸参与Suzuki偶联反应 (18)4.5烷基硼酸参与Suzuki偶联反应 (19)4.6烯基硼酸参与Suzuki偶联反应 (20)4.7 Triflate参与Suzuki偶联反应 (20)4.7.1芳基的三氟甲基磺酸酯与芳基硼酸偶联示例 (21)4.7.2 芳基的Triflate与芳基硼酸偶联示例 (21)4.8 芳基氯参与Suzuki偶联反应 (22)4.8.1钯催化下芳基氯参与Suzuki偶联反应示例(一) (22)4.8.2钯催化下芳基氯参与Suzuki偶联反应示例(二) (23)4.9 镍催化体系用于Suzuki偶联反应 (23)(dppf)和n-BuLi催化下芳基氯参与Suzuki偶联反应示例 (23)4.9.1 NiCl24.10 其他方法 (24)4.10.1 直接Pd/C用于 Suzuki偶联反应示例 (24)用于 Suzuki偶联反应示例 (24)4.10.2 直接Pd(OAc)21 前言1.1 Suzuki 反应的通式在钯催化下,有机硼化合物与有机卤素化合物进行偶联反应,这就提供了一类常用和有效的合成碳-碳键化合物的方法,我们称之为Suzuki 偶联反应,或Suzuki-Miyaura 偶联反应。
四乙烯五胺功能化纤维素负载纳米钯催化剂的制备及其对Suzuki反应催化性能的研究

AbtatT t e y npna iefni azdcl l e C lT P w ssnhs e o px euoeadttehlnpn src :e at l ee t n tn i euo ( e —E A) a ytei d f m eoycl l n e at eee — r he m u ol e l s l z r l s r y
四 乙烯 五 胺 功 能 化 纤 维 素 负载 纳米 钯 催 化 剂 的制 备 及 其对 S zk 反 应 催 化 性 能 的研 究 uu i
杜庆 伟 , 郑长青 , 李毅群
( 暨南 大 : 学 系 , 东 学化 广 广州 5 03 ) 162
摘要 : 利用 四乙烯五胺对环氧化纤维 素进 行功能化改性 , 以其为载体 在 9 %乙醇溶液 中现场还原氯 化钯制 并 5 备 出四乙烯五胺 功能化纤 维素负载 的纳米 钯催 化剂 。利用 I XR S M,E 等分 析方法对 其进行 了表征 R, D,E T M 并用于催化 Szk 交叉偶联反应 。实 验表 明, uui 该催化剂在温和条件下能有效催 化 卤代芳烃 与芳 基硼酸 的 S - u zk 交叉偶联反应 , 化剂经 回收重 复利用 5次后 , ui 该催n ( E A)T epe a dC lT P a sda a x oimoiz aoa aim poue t yte eu tera— a ie T P . h rpr e -E A w sue am t e l s i r t m b i n np ldu rd cdi sub cv c le l ni h r d i e t no a aim cl d i 5 e ao. h s rprdct ytC IT P P 。W hrc re yI X D,E T M, i f l du ho e t 9 % t n1T ea- eae aa s e -E A.d ) a caat zdb o pl i r wh h p l ( 1 s e i R。 R S M,E
化学品英文名称

Filling material A AC 45 UBI / FR 310 5000 Acetic acid (5% at 20°C) Acetic acid (5% at 50°C) Acetic acid (at 40°C) Acetic acid (at 50°C) Acetic acid anhydride Acetoacetate, ethylAcetoacetate, methylAcetone Acetulan Acetyl chloride Acricid 40 EC Acricid liquid Acryl amide Acrylat 38092, solvent base Acrylic acid Acrylic Polymere RDZ 1263 Acrylic Polymere RDZ 2738 Acrylic Polymere RDZ 2771 Acrylic Polymere RDZ 958 Acrylic Polymere RZ 20810 Acrylic Polymere RZ 21376 Acrylic Polymere RZ 421 Activated carbon Activoll EFL Addipast 350 WD black Additol XK 391 Additol XK 406 Adhesion Promoter AMS 70 After Shave Afugan Aircraft fuel Aircraft fuel, Jet A1 Akypo RO 90 VG Akypo RO 90 VG Aldehyde C12 Aldehyde C8 Aldurol VUP 21 Aldurol VUP 51 Alkydal R 35 W Allylic heptylate
Suzuki反应铃木反应

Suzuki反应(铃木反应)铃木反应 - 简介Suzuki反应(铃木反应),也称作Suzuki偶联反应、Suzuki-Miyaura反应(铃木-宫浦反应),是一个较新的有机偶联反应,是在钯配合物催化下,芳基或烯基的硼酸或硼酸酯与氯、溴、碘代芳烃或烯烃发生交叉偶联。
通式:铃木反应 - 概述Suzuki反应对官能团的耐受性非常好,反应物可以带着-CHO、-COCH3、-COOC2H5、-OCH3、-CN、-NO2、-F等官能团进行反应而不受影响。
反应有选择性,不同卤素、以及不同位置的相同卤素进行反应的活性可能有差别,三氟甲磺酸酯、重氮盐、碘鎓盐或芳基锍盐和芳基硼酸也可以进行反应,活性顺序如下:R2-I > R2-OTf > R2-Br >> R2-Cl 另一个底物一般是芳基硼酸,由芳基锂或格氏试剂与烷基硼酸酯反应制备。
这些化合物对空气和水蒸气比较稳定,容易储存。
Suzuki反应靠一个四配位的钯催化剂催化,广泛使用的催化剂为四(三苯基膦)钯(0),其他的配体还有:AsPh3、n-Bu3P、(MeO)3P,以及双齿配体Ph2P(CH2)2PPh2(dppe)、Ph2P(CH2)3PPh2(dppp)等。
Suzuki反应中的碱也有很多选择,最常用的是碳酸钠。
碱金属碳酸盐中,活性顺序为:Cs2CO3 > K2CO3 > Na2CO3 > Li2CO3 而且,加入氟离子(F?)会与芳基硼酸形成氟硼酸盐负离子,可以促进硼酸盐中间体与钯中心的反应。
因此,氟化四丁基铵、氟化铯、氟化钾等化合物都会使反应速率加快,甚至可以代替反应中使用的碱。
铃木反应 - 机理铃木反应示意图首先卤代烃2与零价钯进行氧化加成,与碱作用生成强亲电性的有机钯中间体4。
同时芳基硼酸与碱作用生成酸根型配合物四价硼酸盐中间体6,具亲核性,与4作用生成8。
最后8经还原消除,得到目标产物9以及催化剂1。
氧化加成一步,用乙烯基卤反应时生成构型保持的产物,但用烯丙基和苄基卤反应则生成构型翻转的产物。
suzuki偶联生产实例(优化,工艺,除杂,除Pd)
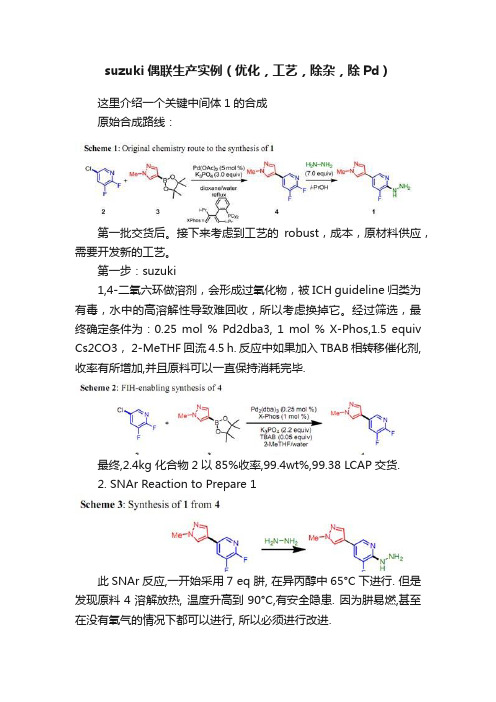
suzuki偶联生产实例(优化,工艺,除杂,除Pd)这里介绍一个关键中间体1的合成原始合成路线:第一批交货后。
接下来考虑到工艺的robust,成本,原材料供应,需要开发新的工艺。
第一步:suzuki1,4-二氧六环做溶剂,会形成过氧化物,被ICH guideline归类为有毒,水中的高溶解性导致难回收,所以考虑换掉它。
经过筛选,最终确定条件为:0.25 mol % Pd2dba3, 1 mol % X-Phos,1.5 equiv Cs2CO3, 2-MeTHF 回流4.5 h. 反应中如果加入TBAB相转移催化剂,收率有所增加,并且原料可以一直保持消耗完毕.最终,2.4kg 化合物2以85%收率,99.4wt%,99.38 LCAP交货.2. SNAr Reaction to Prepare 1此SNAr反应,一开始采用7 eq 肼, 在异丙醇中65°C下进行. 但是发现原料4溶解放热, 温度升高到90°C,有安全隐患. 因为肼易燃,甚至在没有氧气的情况下都可以进行, 所以必须进行改进.使用水做为溶剂,肼的水溶液会相对更实用,并且更安全. 反应温度需要提高到100°C才能增加原料4的溶解度, 降低到80°C虽然结果一样,但是反应时间延长(10h vs 4h).由于产品1不溶解于水,温度降低下来以后, 就可以高纯度地拿到固体. 在暴露空气的过程中,主要生成了杂质5. 大概有2%, 并且在此结晶的过程中,5可以被完全除去.改进以后, 以97%的收率, 99.6wt%, 100%LCAP的质量交货几公斤.在第二次交货以后,就开始考虑商业化进程.重新优化反应首先交货Pd残留不稳定(2-720ppm), 并且通过统计,22%生产API的费用都消耗在合成化合物1,几千美元/1kg,需要更加便宜的工艺。
继续分析发现,合成1的52%费用用在了原料3. 它的大规模制备和分离难度比较大,于是开始开发新的偶联试剂,化合物7被尝试来替代原料3.经过优化,确定条件如下:反应中发现了杂质9,原始工艺可以通过控制使用1.2eq的原料3来控制9的生成,但是使用7的时候,杂质9的生成不稳定,不同批次间含量经常变化。
