卤素
卤素在化学里的名词解释

卤素在化学里的名词解释近代化学发展的过程中,卤素一直是一个重要的研究领域。
卤素是指周期表中VIIA族的元素,包括氟(Fluorine)、氯(Chlorine)、溴(Bromine)、碘(Iodine)和磺(Astatine)。
这些元素具有一系列独特的特性和广泛的应用,我们将在本文中详细讨论它们在化学领域的意义。
1. 氟(Fluorine)首先,让我们来了解一下氟。
氟是最轻的卤素元素,常见于自然界的氟化物中。
氟具有很强的氧化能力和高反应活性,从而使其在许多应用中发挥着重要作用。
例如,氟化物经常用于牙膏和饮用水中,可以有效地预防蛀牙。
此外,氟还被广泛应用于制备氟化有机合成材料,包括药物和农药等。
2. 氯(Chlorine)接下来,我们来谈谈氯。
氯是一种常见的卤素元素,广泛存在于盐类和酸中。
氯具有强氧化性,可以有效杀死细菌和病毒。
因此,氯被广泛用作消毒剂和杀菌剂,用于净化水和消除污染。
此外,氯还在制备许多重要的化学品中发挥着关键作用,例如聚氯乙烯(PVC)和氯麦粒草(一个常见的除草剂)。
3. 溴(Bromine)溴是化学元素中的一员,是一种有毒的红褐色液体。
溴广泛应用于药物、医疗和消防等领域。
例如,一种含溴的化合物叫做溴化氢(Hydrobromic Acid),常用于制备某些药物,例如止咳药和安眠药。
此外,溴化合物还被用作阻燃剂,尤其是在建筑材料和电子产品中,以提高其耐火性。
4. 碘(Iodine)碘是一种非常重要的卤素元素,有广泛的应用。
碘在医药领域被广泛用于消毒和治疗甲状腺问题。
碘溶液可以用于皮肤消毒,碘片则可以用于皮肤伤口的消毒和预防感染。
此外,碘和碘化物还被用作食品添加剂,可以提供人体必需的碘元素。
5. 磺(Astatine)最后,我们来谈谈磺。
磺是一种人工制造的放射性元素,非常稀有。
由于其极其不稳定的性质,磺在化学领域中的应用非常有限,研究也相对较少。
然而,磺及其同位素在核能研究中扮演着重要角色,被用于放射治疗和其他核医学应用。
第十二章 卤素

§1. 卤素单质
一. 物理性质------熔、沸点和颜色
1.状态、颜色
状态原因:半径依次增大,分子量也增大,所以色散力也增大,所以分 别以气体—液体—固体状态存在。 显色原因:利用分子轨道能级图解释显色。卤素分子中π*和σ*反键轨道 能量相差较小,这个能差随着Z的增大而变小。 F2 电子数少,反键 π*、σ*轨道能差大△E大。 F2吸收可见光中能量高、波长短的那部分 光(蓝、紫光),而显示出长波段那部分光,复合色变成黄色。
HXO都不稳定,仅存在于水溶液中,从Cl到I 稳定性减 小,分解方式:
(3) 氧化性
HXO不稳定,表明HXO的氧化性很强。
XO- 盐比HXO酸稳定性高,所以经常用其盐 在酸性介质中做氧化剂。
2.HXO的制备
1)次氯酸酐Cl2O溶于水制得HClO
步骤: 将Cl2通到新制干燥的HgO表面,加热制得Cl2O
二 化学性质
从卤素在自然界中存在形式可以看出卤素单 质化学活泼性很强,价电子层结构,易获一个 电子达到8电子稳定结构。卤素单质是强氧化 剂,而F2最强,随Z增大,氧化能力变弱。碘 不仅以负一价的离子存在于自然界中,而且以 +5价态存在于碘酸钠中,说明碘具有一定的还 原性,它们的化学活泼性,从F2到I2依次减弱。
Cl、Br、I具有不同价态的含氧酸
X: 采取SP3杂化,O的2P电子与卤素3d空轨道间形成d-pπ键。 由于稳定性原因,只有常见的氯的含氧酸研究得多
一、次卤酸
1. 化学性质 (1) 酸性
因为随半径增大,分子中 H— O—X,X—O 结合力减小,X
对 H+ 斥力变小,导致酸性减小。
(2) 热稳定性
卤素元素及知识点总结

卤素元素及知识点总结卤素元素是周期表中的第17族元素,包括氟(F)、氯(Cl)、溴(Br)、碘(I)和砹(At)。
这些元素具有共同的特性,如高电负性、对金属有强烈的化学活性、易离子化等特点。
在化学和生物学领域,卤素元素的应用非常广泛,如消毒、药物制剂、化工生产等领域。
1. 氟(F)氟是周期表中最活泼的非金属元素,其电负性为3.98,是所有元素中最高的。
氟的化合物被广泛用于制造有机化合物、药物、农药和农业化肥等。
氟也是强力的腐蚀剂,能够与金属形成氟化物,并能用于制造不锈钢和铝合金。
2. 氯(Cl)氯是一种绿色有毒气体,具有刺激性气味。
氯是一种重要的工业原料,广泛用于生产塑料、橡胶、药物等化学产品。
氯化物也被用作食品加工中的脱色剂和防腐剂。
氯化合物也被广泛用于水处理、消毒等领域。
3. 溴(Br)溴是一种棕红色液体,有辛辣的气味。
溴和其化合物主要用于生产染料、消毒剂、防火剂等。
溴化银是曾经广泛用于摄影的感光材料。
4. 碘(I)碘是一种紫黑色晶体,具有金属光泽。
碘主要用于制备医药、化工原料和感光材料等。
碘也是人体必需的微量元素,对人体健康至关重要。
5. 砹(At)砹是一种放射性元素,非常不稳定。
由于其稀缺性和毒性,砹的应用非常有限。
卤素元素的化学性质主要体现在其化合物中,包括卤化物、卤氧酸盐、卤代烃等。
卤素元素可以形成离子化合物,也可以形成共价化合物。
除氟外,其他卤素元素主要以共价键的形式存在。
在生物学领域,卤素元素对生命体的作用非常重要。
如氯化物在维持体内水盐平衡、传导神经冲动和肌肉收缩等过程中起着重要作用。
碘是甲状腺激素的组成部分,对人体的新陈代谢、生长发育、心血管功能等有重要影响。
然而,卤素元素也有毒性,过量摄入会损害人体的健康。
氟过量摄入会导致骨骼矿化不良、牙齿斑点等疾病,碘过量摄入会影响甲状腺功能,导致甲亢或甲减等疾病。
卤素元素也具有重要的应用价值。
如氟化物广泛用于牙膏、口香糖等口腔护理产品中,氯化物和溴化物被用作水处理剂、消毒剂等。
卤素

At2
具有放射性 咱不讨论- - ...
1.卤素都能跟金属起反应生成卤化物。
非金属性越强,反应越易进行,生成的卤化物越稳定。
2.卤属都能跟氢气反应生成卤化氢。
F2低温下暗处就剧烈反应甚至爆炬产生HF稳定。Cl2低温下缓慢反应需光照或加热条件下进行。Br2 I2高温下才能反应,HI不稳定可分解为H2和I2 所以为可逆反应。
随着分子量的增大,卤素分子间的色散力逐渐增强,颜色变深,它们的熔点、沸点、密度、原子体积也依次递增
卤素的化学性质都很相似,它们的最外电子层上都有7个电子,有取得一个电子形成稳定的八隅体结构的卤离子的倾向
除F外,卤素的氧化态为+1、+3、+5、+7
卤素与氢结合成卤化氢,溶于水生成氢卤酸。
卤素之间形成的化合物称为互卤化物,如ClF3、ICl。
2F2+2H2O=4HF(aq)+O2 X2+H2O=HX(aq)+HXO(aq) X=表示Cl Br I (aq)代表是溶液.
4.卤素各单质的活泼性比较。
卤素各单质的活泼性顺序:F2>Cl2>Br2>I2 前者可将后者从其金属化物中置换出来.
5.碘与淀粉反应:碘+淀粉→蓝色,检验I2或淀粉的存在。
氟、氟化氢和氢氟酸对玻璃有较强的腐蚀性。
氟是氧化性最强的元素,只能呈-1价.其没有正价.
单质氟与盐溶液的反应,都是先与水反应,生成的氢氟酸再与盐的反应,通入碱中可能导致爆炸。
化学性质活泼,能与几乎所有元素发生反应(除氦、氖)。
水溶液氢氟酸是一种弱酸。但却是稳定性、腐蚀性最强的氢卤酸,如果皮肤不慎粘到,将一直腐蚀到骨髓。
卤素化学式

卤素化学式1. 引言卤素是化学元素周期表中的一组元素,包括氟(F)、氯(Cl)、溴(Br)、碘(I)和砹(At)。
它们属于同一族,具有相似的化学性质。
本文将介绍卤素的化学式及其特点。
2. 氟化学式氟是周期表中最轻的卤素,原子序数为9。
其化学式为F。
氟原子只有一个价电子,因此很容易与其他元素形成离子或共价键。
氟离子通常以F-表示,它可以与金属形成离子化合物,如氟化钠(NaF)。
在共价键中,氟通常以单质形式存在,如氯气(Cl2)中的二原子分子。
3. 氯化学式氯是周期表中第17号元素,原子序数为17。
其化学式为Cl。
与其他卤素类似,氯也具有较强的活性。
它可以与大多数金属反应形成离子化合物,例如盐酸(HCl)和氯化钠(NaCl)。
此外,氯也可以以共价键形式存在于分子中,例如二氧化二氯(Cl2O2)。
4. 溴化学式溴是周期表中第35号元素,原子序数为35。
其化学式为Br。
溴具有较高的反应活性,可以与金属形成离子化合物,如溴化钠(NaBr)。
另外,溴也可以以共价键形式存在于分子中,如四溴化碳(CBr4)。
5. 碘化学式碘是周期表中第53号元素,原子序数为53。
其化学式为I。
碘是一种重要的营养元素,在人体中起到重要的作用。
碘可以与金属形成离子化合物,如碘化钠(NaI)。
在有机化学中,碘也常用作催化剂。
6. 砹化学式砹是周期表中最重的卤素元素,原子序数为85。
其化学式为At。
砹是一种放射性元素,在自然界中非常稀少。
由于其放射性和危险性质,砹的应用范围非常有限。
7. 总结卤素是一组具有相似特性的元素,在自然界和实验室中都有广泛应用。
氟、氯、溴、碘和砹分别对应的化学式分别为F、Cl、Br、I和At。
它们可以以离子形式或共价键形式存在,具有不同的化学性质和应用领域。
了解卤素的化学式及其特点对于理解化学反应和应用具有重要意义。
以上内容介绍了卤素的化学式及其特点,希望对读者有所帮助。
参考文献: - Cotton, F. A.; Wilkinson, G.; Murillo, C. A.; Bochmann, M. (1999). Advanced Inorganic Chemistry (6th ed.). Wiley-Interscience. - Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann.附注:此文档为人工智能生成,仅供参考。
卤素

(2)物质的颜色与吸收光颜色的关系 )
物质的颜色
绿 黄 青
橙 红
白光 蓝 紫
青蓝
黄绿 黄 橙 红 紫红 紫 蓝 青蓝 青
吸收光 波长(nm) 颜色 波长(nm) 400— 紫 400—450 450— 蓝 450—480 480— 青蓝 480—490 490— 青 490—500 500— 绿 500—560 560— 黄绿 560—580 580— 黄 580—600 600— 橙 600—650 红 ) X2为非极性分子,分子间作用 为非极性分子, 力主要为┄┄ ┄┄色散力 力主要为┄┄色散力 熔沸点F 依次升高。 ∴熔沸点 2→I2 依次升高。 聚集态 F2(g)→CI2(g)→Br2(l)→I2(g) Br2:非金属中的唯一液体 I2:固体易升华,紫黑 粉红 固体易升华,紫黑→粉红
(2)与非金属作用 )
F2
反应活性 与H2反应条件 暗处 光照 Pt/350℃ 高温 ℃ F2可与所有除 O2、N2,稀有气体He和Ne外的非金属作用 稀有气体 和 外的非金属作用 直接化合成高价氟化物。 直接化合成高价氟化物。 Cl2也可与大多数非金属单质化合,但不如 2猛烈。 也可与大多数非金属单质化合,但不如F 猛烈。 2 S(s) + Cl2(g) = S2Cl2(l) 红黄色液体 S(s) + Cl2(g)(过量 = SCl2(l) 深红色发烟液体 过量) 过量 2 P(s) + 3 Cl2(g) = 2 PCl3(l) 无色发烟液体 2 P(s) + 5 Cl2(g) (过量 = 2 PCl5(l) 淡黄固体 过量) 过量 Br2和I2与许多非金属作用反应,但不如 2、Cl2激烈,不能 与许多非金属作用反应,但不如F 激烈, 氧化到最高价。 氧化到最高价。
卤素
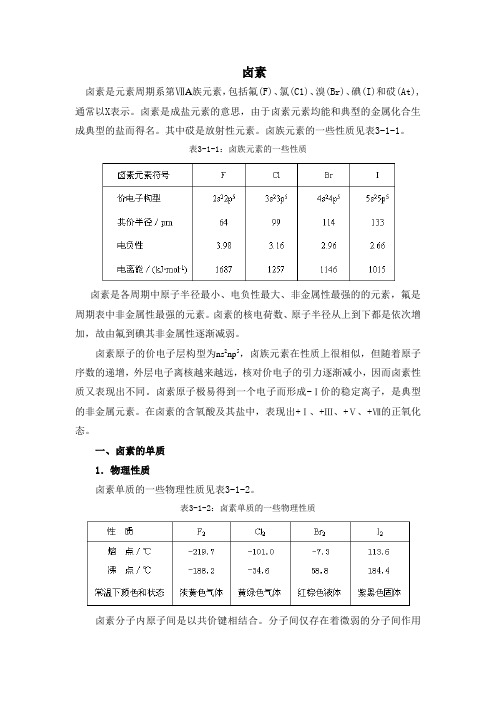
卤素卤素是元素周期系第ⅦA族元素,包括氟(F)、氯(C1)、溴(Br)、碘(I)和砹(At),通常以X表示。
卤素是成盐元素的意思,由于卤素元素均能和典型的金属化合生成典型的盐而得名。
其中砹是放射性元素。
卤族元素的一些性质见表3-1-1。
表3-1-1:卤族元素的一些性质卤素是各周期中原子半径最小、电负性最大、非金属性最强的的元素,氟是周期表中非金属性最强的元素。
卤素的核电荷数、原子半径从上到下都是依次增加,故由氟到碘其非金属性逐渐减弱。
卤素原子的价电子层构型为ns2np5,卤族元素在性质上很相似,但随着原子序数的递增,外层电子离核越来越远,核对价电子的引力逐渐减小,因而卤素性质又表现出不同。
卤素原子极易得到一个电子而形成-Ⅰ价的稳定离子,是典型的非金属元素。
在卤素的含氧酸及其盐中,表现出+Ⅰ、+Ⅲ、+Ⅴ、+Ⅶ的正氧化态。
一、卤素的单质1.物理性质卤素单质的一些物理性质见表3-1-2。
表3-1-2:卤素单质的一些物理性质卤素分子内原子间是以共价键相结合。
分子间仅存在着微弱的分子间作用力,随着相对分子质量的增大,分子的变形性逐渐增大,分子间的色散力也逐渐增强,因此,卤素单质的一些物理性质呈现规律性变化。
如卤素单质的熔点、沸点等按F—C1—Br—I的顺序依次升高。
常温下,氟和氯是气体,溴是易挥发的液体,碘为固体(易升华)。
可见卤素单质的颜色随着相对分子质量的增大而逐渐加深,这是由于从氟至碘外层电子离核越来越远,相应的外层电子更易被激发,所以外层电子被激发所需要的能量就越少,故使物质的颜色逐渐变深。
卤素单质是非极性分子,在水中的溶解度不大,易溶于有机溶剂。
氟不溶于水,它能剧烈地分解水而放出氧气。
溴在有机溶剂中的颜色随溴浓度的增加而逐渐加深,从黄色到棕红色。
碘溶于溶剂中所形成溶液的颜色随溶剂不同而有区别。
卤素单质均有刺激气味,吸人较多的蒸气会发生严重中毒,甚至造成死亡。
它们的毒性从氟到碘依次减轻。
溴易挥发,高浓度的液溴可使皮肤严重灼伤;碘的蒸气有毒,强烈刺激皮肤和眼睛;使用时要特别小心。
12-卤素

BrO4
-
BrO3
-
BrO-
Br2(l)
Br-
HI3O62- 0.65 IO3- 0.15 IO- 0.42 I2(s) 0.54 I在 0B图中,除X2/X-电对外,其余电对的电极电势虽为正值,但 均较小,即在碱性介质中,各种含氧酸盐的氧化性较含氧酸弱。
14.2.2 卤素单质物理性质
卤素单质
聚集状态 颜色 熔点/℃ 沸点/℃ 汽化热/(KJ· mol-1) 溶解度/g· (100gH2O)-1
• Cl2也可与大多数非金属化合,但不如F2猛烈。 Br2 、I2更差。 2S + Cl2 = S2Cl2 S + Cl2(过量) = SCl2
2P + 3Cl2 = 2PCl3
2P + 5Cl2(过量) = 2PCl5 2P + 3Br2 = 2PBr3 2P + 5Br2(过量) = 2PBr5
氟
气 浅黄 -219.6 -188 6.32 分解水
氯
气 黄绿 -101 -34.6 20.41 0.732
溴
液 红棕 -7.2 58.78 30.71 3.58
碘
固 紫黑 113.5 184.3 46.61 0.029
密度/(g· cm-3)
1.11(l)
1.57(l)
3.12(l)
4.93(s)
F F F I F F
Cl Cl
F F F F F I F F
I
例:ICl2 (7 + 1×2) / 2 = 4.5 (杂化轨道理论:sp3d),直线型 例:IF7 (7 + 1×7) / 2 = 7 五角双锥
对于ClF3 (7+3) 2 = 5
卤素PPT课件

05
卤素在生活生产中应用
食盐与人体健康关系探讨
食盐的化学成分及作用
主要成分为氯化钠(NaCl),是人体必需的营养元素之一,对于维持细胞内外渗透压平衡、 神经传导和肌肉收缩等生理功能具有重要作用。
食盐摄入量与健康关系
适量摄入食盐对维持人体健康至关重要,但过量摄入可能导致高血压、心血管疾病等健康问 题。世界卫生组织建议每日食盐摄入量不超过5克。
06
卤素对环境影响及治理措 施
大气中卤代烃污染现状及危害
卤代烃在大气中的来源
工业排放、汽车尾气、农药使用等。
大气中卤代烃的浓度及分布
受排放源、气象条件、地形等因素影响,浓度分布不均。
卤代烃对大气的危害
破坏臭氧层,导致紫外线辐射增强;形成光化学烟雾,危害人类健 康。
水体中卤代烃污染现状及危害
卤代烃在水体中的来源
溴和碘
物理性质
溴是一种红棕色、有刺激性气味 的液体,密度比水大,易挥发; 碘是一种紫黑色、有金属光泽的
固体,密度比水大,易升华。
化学性质
溴和碘的化学性质较为相似,都 具有氧化性,能与多种元素直接
化合生成溴化物和碘化物。
用途
溴和碘在有机合成、医药、农药 等领域有着广泛的应用。例如, 溴可用于制取溴化物、染料、灭 火剂等;碘可用于制取碘化物、
氯气可以与大多数金属直接反应,生 成相应的氯化物。
卤素性质变化规律
01
随着原子序数的增加, 卤素的非金属性逐渐减 弱,金属性逐渐增强。
02
卤素单质的颜色逐渐加 深,从氟气的浅黄绿色 到碘单质的紫黑色。
03
04
卤素单质的密度逐渐增 大,熔点和沸点也逐渐 升高。
卤素单质的氧化性逐渐 减弱,还原性逐渐增强。
卤素

溴能氧化碘离子为碘单质
Br2+2NaI I2+2NaBr
11.2.3 卤素的氢化物
1. 卤化氢的物理性质
(1)熔沸点 卤化氢的熔沸点 HF HCl HBr HI
熔点/℃ -83.57 -114.18 -86.87 -50.8 沸点/℃ 19.52 -85.05 -66.71 -35.1
例外,氢键 色散力增大,熔沸点逐渐升高
0
-2
① 氧化反应 X2 + H2O
-1 1 0
2HX + 2 O2
半反应: X2+2e- 2X-
O2+4H++4e-
2H2O E =1.23V
卤素单质的标准电极电势
卤素单质 标准电极电势 X2+2e- 2X-
F2 Cl2 Br2 I2 2.889 1.360 1.077 0.534
② 歧化反应:即水的作用导致卤素发生分解
键型:从上到下,由共价型过渡到离子型 性质:熔、沸点增高
(3)同一金属不同卤化物 的物理性质
主要 氧化数
F 2s22p5
-1,0
Cl
Br
I
3s23p5 4s24p5 5s25p5
-1,0 ,+1 -1,0 ,+1 -1,0 ,+1 +3,+5,+7 +3,+5,+7 +3,+5,+7
卤素价层电子构型为ns2np5,易得到1个电子达到8电子 稳定状态,所以都能以-1氧化态存在。
除F外,Cl、Br、I还可呈现+1、+3、+5、+7氧化态。
碘 固 紫黑 386.5 457.4 41.95 0.029* 4.93(s)
卤素

2F₂+2OH⁻→OF₂+2F⁻+H₂O
卤的氧化物中氯原子具有多种不同氧化态,可用新制得的黄色Hgo和CI₂制取
2CI₂+2Hgo=HgCI•H₂O+CI₂O
同浓度卤酸的氧化性强弱关系比较
HBrO3、HClO3和HIO3 Br与Cl相比,外层18电子的Br吸引电子的能力大于8电子的Cl; Br与I的最外层都是18电子但Br的半径r小于I,所以Br的得电子能 力也大于I。故3种卤酸氧化性顺序为:HBrO3>HClO3>HIO HBrO4、H5IO6和HClO4 稀溶液中HClO4完全解离,ClO4-为正四面体结构,对称性高, 且不受H+反极化作用的 影响,比较稳定,所以氧化能力低。 高卤酸的标准电极势数值 排列: BrO4-/BrO3- H5IO6/IO3- ClO4-/ClO3- EAθ/V 1.85 1.60 1.20 比较卤酸的标准电极电势可知氧化性:HBrO4>H5IO6>HClO4
绝大数卤素互化物是不稳定的,熔沸点低。最稳定的XY型卤素互化物是CIF, 其物理性质介于组成元素的分子性质之间。卤素互化物都是氧化剂,与大多 数金属和非金属猛烈反应生成相应的卤化物;发生水解作用生成卤离子和卤 氧离子,其分子中较大电负性较小的卤原子生成卤氧离子。 氟的卤素互化物如CIF₃、CIF₅、BrF₃通常都作为氟化剂,使金属、非金属及金 属的氧化物以及金属的卤化物、溴化物和碘化物转变为氟化物
卤化物
卤素和电负性较小的元素形成的化合物叫做卤化物。由非金属或高氧化 态金属形成的卤化物BCl₃、CCl₄、SbCl₅、SF₆、WCl₆等,不论气相、液相或 是固相,往往形成共价型卤化分子,它们有挥发性、较低的熔点和沸点, 有的不溶于水,溶于水的往往发生强烈的水解。 碱金属、碱土金属及若干镧系和锕系元素,它们的电负性小,离子半径 大,形成的卤化物主要是离子型的。它们有高的熔点和沸点,在极性溶 剂中易溶解,其溶液有导电性,熔融状态时也能导电。同一周期各元素 的卤化物,随着金属离子半径减小和氧化数增大,离子性依次降低,共 价性依次增强,熔沸点依次降低。 同一金属的卤化物随着卤离子半径的增大,变形性也增大,按氟氯溴碘 的顺序其离子性依次降低,共价性依次增加。一般来说,金属氟化物主 要是,离子型化合物其它卤化物从氯到碘共价型化合物则逐渐增多。 不同氧化物的同一金属,其高氧化态卤化物的离子性小于低氧化态卤化 物的的离子性
卤素的解释

卤素(halogen)测试|无卤检测|卤素四项(氟F/氯Cl/溴Br/碘I)/ 卤素测试报告什么是卤素(halogen)?卤素(halogen)的应用是什么?卤素(halogen)有什么危害?卤素(halogen)测试怎么做?为什么通常是卤素(halogen)四项测试?什么是卤素测试报告?卤素(halogen)的大致应用范围是哪些?什么限制卤素(halogen)使用的相关法规?本版将就一些大家关心的问题,做个简单介绍。
一、什么是卤素(halogen)?卤素(halogen)是化学周期表中第ⅦA族非金属元素。
卤素(halogen)具体来说指的是氟(Fluorine)、氯(Chlorine)、溴(Bromine)、碘(Iodine)和砹(Astatine)五种元素,合称卤素。
由于砹(Astatine)为放射性元素,因此,人们通常所指的卤素习惯上是氟F、氯CI、溴Br、碘I四种元素。
卤素化合物经常作为一种阻燃剂应用于电子零组件与材料、产品外壳、塑胶等。
此种阻燃剂无法回收使用,而且在燃烧与加热过程中会释放有害物质,威胁到人类身体的健康、环境和下一代子孙。
二、卤素(halogen)的应用卤素(halogen)(氟Fluorine/氯Chlorine/溴Bromine/碘Iodine)大多在聚合物材料中以有机物形式存在。
用于常见产品中的卤素化合物主要有PBB、PBDE、TBBP-A、PCB、六溴十二烷、三溴苯酚、短链氯化石蜡;另有用于冷冻剂、隔热材料等的臭氧破坏物质CFCs、HCFCs、HFCs等。
一般来说,卤素化合物大多是应用于阻燃剂、制冷剂、溶剂、有机化工原料、农药杀虫剂、漂白剂、羊毛脱脂剂等。
三、其它含有卤素(halogen) (F/Cl/Br/I)的各类物质有机氯化合物:用于塑料的耐燃剂、增塑剂、印刷电路格等上的耐燃剂等;聚氯乙烯(PVC):电源电缆、連接电缆、产品内連线用塑料电线、粘合剂、高压塑料电线、退磁线圈的包里、绝缘胶带;灭蚁灵(Mirex):用于树脂、橡胶、涂料、纺织物、电气产品等的阻燃剂、防锈剂等;氯化烷烃(CP):用作含有附件产品的外框(外壳)、印刷电路板(碳链长为10 -13、含氯量为50wt%以上的短链型氯化烷烃類对象);多氯化萘(PCN):润滑油、涂料等用途(氯原子数≧3以上的多氯化萘(PCN)产品);多氯联苯(PCB / PCBs):绝缘油、润滑油、塑料耐燃剂等;其它有机溴化合物:用于塑料的耐燃剂印刷电路板等上的耐燃剂等;四溴双酚-(TBBP-A):用于塑料的耐燃剂(以PS、ABS、PC/ABS、Mppe等四种塑料最常使用半导体封装材料与体积路板基材);多溴二苯醚(PBDE),用于塑料的耐燃剂;多溴联苯(PBB):用于塑料的耐燃剂;氯化石蜡Chlorinated paraffins;氯三联苯(PCT)Polychlorinated terphenyls。
卤素化学式

卤素化学式卤素是元素周期表第17族的元素,包括氟(F)、氯(Cl)、溴(Br)、碘(I)和砹(At)。
这些元素通常以分子式的形式出现,如F2、Cl2、Br2、I2和At2,表明它们是由两个原子构成的。
下面将详细介绍这些卤素的化学式及其性质。
首先是氟(F),它是元素周期表中最轻的卤素,具有原子序数9。
它的化学式为F2,表示它是由两个氟原子构成的分子。
氟是一种高度活泼的非金属元素,常以氟化物的形式存在于自然界中。
氟具有非常强的电负性,是化学中最强的氧化剂之一。
它与几乎所有的元素都能形成化合物,如氟化钠(NaF)、氟化铝(AlF3)等。
氟化物被广泛应用于铝冶炼、水处理、制药等领域。
其次是氯(Cl),它是元素周期表中第17位的元素,具有原子序数17。
氯的化学式为Cl2,表示它是由两个氯原子构成的分子。
氯是一种具有强烈刺激性气味的淡黄色气体,可以通过电解盐水或氯化物来制备。
氯在许多工业和消费品中都有广泛应用,如制造漂白剂、消毒剂、塑料等。
氯离子也是身体内重要的电解质之一,维持着酸碱平衡和正常细胞功能。
接下来是溴(Br),它是元素周期表中第35位的元素,具有原子序数35。
溴的化学式为Br2,表示它是由两个溴原子构成的分子。
溴是一种深红褐色液体,在常温下显著挥发。
溴广泛用于医药、有机合成和照相等领域。
溴离子也是现代医学中常用的造影剂之一,用于X 射线和CT扫描等检查。
之后是碘(I),它是元素周期表中第53位的元素,具有原子序数53。
碘的化学式为I2,表示它是由两个碘原子构成的分子。
碘是一种晶体,呈现出典型的紫色。
碘广泛用于消毒、制造染料和药剂、甲状腺功能检查等领域。
碘是人体必需的微量元素之一,对于身体的正常生长和发育具有重要作用。
最后是砹(At),它是元素周期表中最重的卤素,具有原子序数85。
砹的化学式为At2,表示它是由两个砹原子构成的分子。
砹是一种放射性元素,主要通过核反应制备。
卤素的化学式和性质展示了它们的独特特性和广泛用途。
卤素

卤素(ⅦA族)氟F、氯Cl、溴Br、碘I 统称为卤素。
价电子构型:ns2np5氧化态:除氟外(-1),均可呈现0、-1、+1、+3、+5、+7卤素的存在氟:是自然界中广泛分布的元素之一,在卤素中,它在地壳中的含量仅次于氯。
氟在地壳的存量为0.072%,克拉克值0.0625,存在量的排序数为12,自然界中氟主要以萤石(Fluorite)存在,其主要成分为氟化钙(CaF2)、冰晶石(3NaF.AlF3)及以氟磷酸钙[Ca5F(PO4)3]为主的矿物。
氯:氯在地壳中的含量为0.031%,自然界的氯大多以氯离子形式存在于化合物中,氯的最大来源是海水。
矿物中有光卤石(KCl ﹒MgCl6﹒6H2O)溴:以溴化物的形式存在于海水和地壳中碘:以碘化物形式存在,南美洲智利硝石含有少量的碘酸钠。
海中的植物可以富集碘。
卤素单质物理性质氟:通常情况下氟气是一种浅黄绿色的、有强烈助燃性的、刺激性毒气,是已知的最强的氧化剂之一。
熔点-219.62℃,沸点-188.14℃。
氟的电负性最高,吸引电子能力强氯:气态氯单质俗称氯气,液态氯单质俗称液氯。
在常温下,氯气是一种黄绿色、刺激性气味、有毒的气体。
压力为101.325KPa 时,氯单质的沸点为-34.4℃,熔点为-101.5℃。
氯气可溶于水和碱性溶液,易溶于CS2和CCl4等有机溶剂,饱和时1体积水溶解2体积氯气。
溴:深棕红色、易挥发、有强烈刺激性臭味、液体密度:3.119g/cm3,熔点:-7.2℃ ,沸点:58.76℃,在常温下,是唯一的液态非金属。
碘:紫黑色晶体,具有金属光泽,性脆,易升华。
有毒性和腐蚀性。
密度4.93 克/立方厘米。
熔点113.5℃,沸点184.35℃。
加热时,碘升华为紫色蒸汽,这种蒸气有刺激性气味,有毒。
易溶于乙醚、乙醇、氯仿和其他有机溶剂,形成紫色溶液,但微溶于水(但如果水中含碘离子会使其溶解度增大:I-+I2==I3-,也溶于氢碘酸和碘化钾溶液而呈深褐色。
卤素

2)通人氯把溴置换出来:
Cl2 + 2Br- = Br2 + Cl-
3)再用空气把溴吹出以碳酸钠吸收:
3Na2CO3 + 3Br2 == 5NaBr + NaBrO3 + 3CO2 4)最后用硫酸酸化,单质溴又从溶液中析出。
5HBr + HBrO3 = 3Br2 + 3H2O 用此方法,从1吨海水中可制得约0.14kg的溴。
3、除氟外,氯、溴和碘均可显正氧化态,氧化数经常是+1, +3,+5的+7。
1
2-2 卤素在自然界中的分布
卤素是最活泼的非金属元素,卤素是“成盐元素”的意思,在 自然界只能以化合态的形式存在。多数以氢卤酸盐形式存在。
氟: 萤石(CaF2)、 冰晶石(Na3AlF6)、 氟磷灰石Ca5F(PO4)3
氯和溴: 大量在海水中 NaCl、NaBr 钾石盐KCl 光卤石KCl· MgCl26H2O
碘: 智利硝石(NaNO3中含有NaIO3),富集于海带、海藻中
2-3 卤素单质
1.卤素单质的物理性质:
F2
Cl2
聚集状态
g
g
分子间力
小
颜色
浅黄 黄绿
Br2 l
红棕Leabharlann I2 s大 紫(紫黑(s))
显色原因:分子中*和*反键分子轨道能差不同,吸收的可见光 波长度不同。F2吸收能量高(波长短)的光,显示波长较长光的复 合色。
364
HI 1.49 分子极性 -50.80 熔点 -35.36 沸点 -26.5 300 稳定性 299 强
电子构型 氧化态 F [He]2s22p5 -1、0 Cl [Ne]3s23p5 -1、0、+1、+3、+4、+5、+7 Br [Ar]4s24p5 -1、0、+1、+3、+4、+5、+7 I [Ar]4s24p5 -1、0、+1、+3、+4、+5、+7
第6章 卤素

一、P区元素概述 含ⅢA~ⅦA 及零族,沿B-Si-As-Te-At为 对角线, 右上方为非金属元素区,含21种 元素;左下方为10种金属元素。 特点: 1、原子结构 :价层 ns2 np1-6 2、金属性、非金属性:同一周期从左到右、 非金属性增强 ,金属性减弱 ;同族,从上 到下,除ⅦA外,均从典型非金属元素过渡 到金属元素 。 3、氧化数:⑴除零族元素外 ,常具有多种氧 化数, 除正氧化数外,还有负氧化数。
常温
Cl2 Br2 I2 ClO
BrO 3 IO 3
-
加热
ClO 3
-
低温 ClOO
PH 4
BrO 3 IO 3
-
-
BrO (0 C) PH 6
IO 3
-
PH 9
§ 11.1 p区元素概述
ⅠA
元素周期系的分区及各区的价电 子组态
ⅡA
0
ⅢA―ⅦA
S区
ⅢB―ⅦB
Ⅷ
ⅠB ⅡB
p 区
ns1–2
第11章
卤素
氧族元素
卤素
• 一. 卤素概述: • 1.第VIIA族包括氟、氯、溴、碘 和砹五种元素,总称为卤素。卤 素希腊原文为成盐元素的意思。。 • 砹是放射性元素,在自然界中仅 以微量而短暂地存在于镭、锕或 钍的蜕变产物中。
注意价电子结构和氧化数
2np5 2.价电子层结构:ns
• 导致非单质的氧化数: • 1)最低氧化数:-1 • 2)最高氧化数:F:-1;其它:+7 • 3) 氧化数都是奇数(为什么)
• 氧化还原性 F2
-
Cl2
Br2
I2
E (X 2 /X ) /V: 2.889 1.360 1.0774 0.5345
卤素

光照
H2+Cl2=或=点==燃=2HCl
500℃
H2+Br2======2HBr
HCl稳定 较不稳定
H2+I2======2HI HI很不稳定
卤素与水的化学反应方程式
2F2+2H2O==4HF+O2 (特例)
反 应
Cl2 +H2O HCl+HClO
越
Br2+ H2O
I 2+ H2O
HBr+HBrO
单质均为双原子分子——X2
物理性质: 卤素单质都是有色物质,从上到下,其颜色
逐渐加深,密度逐渐增大,熔、沸点逐渐升高 (常温时的状态由气态经液态到固态)。
卤素与氢气的反应
名称
F2 Cl2 Br2 I2
反应条件
暗处
光照或点燃 高温
高温、持 续加热
方程式
生成氢化物的 稳定性
H2+F2====2HF
HF很稳定
元素 名称
氟
卤族 氯 元素
溴
VIIA 碘
砹
元素 符号
F Cl
Br I
At
核电 原子结构示意图 最外层电 电子层
荷数
子数
数
9
+9 2 7
7
2
17
+17
2+35 2 8 18 7
7
4
53
+53 2 8 18 18 7
7
5
85
+85 2 8 18 32 18 7
7
6
卤族元素——F Cl Br I (VIIA族)
现象
盛有NaBr溶液的试管, Cl4层变橙红色。 盛有KI溶液的试管,CCl4 层变深紫色。
卤素

常温 强光照射
Br2
常温 600C
I2
高温
爆炸、放出大量热
缓慢
爆炸
不如氯 明显
减 小
缓慢
10.2.1.3 与H2O反应
卤素与水可发生两类反应,分别是氧化作用和歧化作用:
(1)氧化作用 2X2 + 2H2O
4HX + O2↑
(2)歧化水解 X2 + H2O
H+ + X- + HXO
F2的氧化性强,只能与水发生第一类反应,且反应激烈:
主要氧化数
氟(F) 氯(Cl) 溴(Br) 碘(I)
9
17
35
53
2s22p5 3s23p5
4s24p5 5s25p5
64
99
114
133
4.0
3.0
2.8
2.5
1681 125非1 金属性1减140弱 1008
-1、0
-1、0
-1、0
-1、0 +1、+3 +5、+1、+3 +5、 +1、+3
+7
+7
力依次减弱:F2 > Cl2 > Br2 > I2
电极电势: F2/F-
Eθ (X2/X-) 2.87
Cl2/Cl1.36
Br2/Br- I2/I1.065 0.535
10.2.1.1 与金属、非金属反应
卤素
反应物质
所有金属
F2
除氮、氧外的非金属
Cl2 Br2 、I2
与上类似
活泼金属 其他金属
反应程度
10.3.2.2 还原性
卤素

单质氟的制备
1、单质氟的制备(P459图14-2) 、单质氟的制备 图
氯单质的发现
1、单质氯的发现:氯 、单质氯的发现: 是由瑞典化学家舍勒(C.W. 是由瑞典化学家舍勒 Scheele)在1774年用软锰矿 在 年用软锰矿 (MnO2)与盐酸反应而发现的, 与盐酸反应而发现的, 与盐酸反应而发现的 氯气为黄绿色, 氯气为黄绿色,所以氯一词 希腊文原意是黄绿色。 希腊文原意是黄绿色。
氟的特殊性
氟的原子半径特别小, 氟的原子半径特别小 , 其核周围电子密 度较大, 度较大 , 当它接受外来一个电子或共用 电子对成键时, 电子对成键时 , 将引起电子间较大的斥 力 , 这种斥力部分地抵消了气态氟形成 气态氟离子, 气态氟离子 , 或氟形成单质分子时所放 出的能量。所以氟的电子亲合势小于氯. 出的能量。所以氟的电子亲合势小于氯 尽管氟的电子亲合势反常 地小于氯, 但因F 地小于氯 , 但因 2 的离解 能较小, 能较小 , F- 离子的水合能 较大, 较大 , 所以氟在卤素中仍 然是个最强的氧化剂。 然是个最强的氧化剂。
单质的化学性质
2、氯(电极电势 、 电极电势=1.358V)也能与各种金属和大多 )也能与各种金属和大多
数非金属(除氮、 数非金属(除氮、氧、稀有元素外)直接化合,但有 稀有元素外)直接化合, 些反应需要加热,反应还比较剧烈。而氯与Co、 、 些反应需要加热,反应还比较剧烈。而氯与 、S、V 氧化为: 和Bi氧化为 氧化为 CoCl2,SCl4,VCl4,BiCl3(不是最高氧化态) , , , (不是最高氧化态)
卤
卤 素 通 性 卤 素 单 质 卤 化 氢 和 氢 卤 酸 卤 化 物 卤 素 互 化 物 多 卤 化 物 元 素 电 势 图
高一化学 卤素

高一化学卤素一、介绍卤素卤素是化学元素周期表第17族的元素,包括氟(F)、氯(Cl)、溴(Br)、碘(I)和砹(At)。
这些元素在自然界中广泛存在,并且常用于许多化学和生物学应用中。
在本文中,我们将对卤素的性质、用途以及相关实验进行探讨。
二、卤素的性质1. 卤素的物理性质卤素在常温下会呈现不同的物态。
氟气和氯气都是无色气体,而溴是深红色液体,碘是紫黑色固体,砹则是放射性的固体。
卤素的沸点和熔点随着原子序数的增加逐渐升高,同时密度也逐渐增加。
2. 卤素的化学性质卤素在化学反应中表现出一系列的特性。
它们可以与金属发生反应,并形成离子化合物。
例如,氯可以与钠发生反应,生成氯化钠。
另外,卤素还可以与非金属发生反应,并形成共价化合物。
例如,氟可以与氢发生反应,生成氟化氢。
三、卤素的应用1. 工业应用卤素在工业上有着广泛的应用。
氯被用于消毒水处理、漂白剂以及合成许多化合物的原料。
溴被广泛应用于制药和农业领域,用于消毒和灭虫。
碘被用于制备碘酒、碘盐和消毒剂。
砹在放射治疗中具有一定的应用价值。
2. 生物学应用卤素在生物学中也起着重要的作用。
氯化物是人体内必需的微量元素,对维持水盐平衡和神经、肌肉正常功能发挥着重要作用。
碘是甲状腺激素的重要组成部分,对身体的生长和代谢有着重要影响。
四、相关实验1. 氯离子的检测实验材料:稀盐酸(HCl)、银氨溶液(AgNO3)、氨水(NH3)实验步骤:a. 将少量的盐酸滴加到待检测的溶液中,观察是否产生气体释放。
b. 向溶液中加入几滴银氨溶液,观察是否产生白色沉淀。
c. 加入氨水后,观察沉淀是否溶解。
实验结果:a. 如果产生气体释放,可能是盐酸与氯化物反应产生氯气。
b. 如果产生白色沉淀,可能是盐酸与氯化物反应产生氯化银。
c. 沉淀溶解则表示盐酸与氯化物反应产生了可溶性的化合物。
2. 碘离子的检测实验材料:稀盐酸(HCl)、硫酸(H2SO4)、淀粉溶液实验步骤:a. 将待检测溶液加热,观察是否发生变色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2NaCl+2H2O
2NaOH + Cl2 + H2
电解
电解MgCl2熔盐制Mg的副产品
MgCl2(熔融)
Mg + Cl2
电解NaCl熔盐制Na的副产品
2NaCl(熔融)
电解
2Na + Cl2
Cl2 实验室:用MnO2、KMnO4、K2Cr2O7、KClO4
等氧化剂与浓盐酸反应 MnO2 +4HCl(浓) → MnCl2+ Cl2 +2H2O
2IO3 + 5HSO3 → 2I2 + 3HSO4 + 2SO4 + H2O
-
-
11-3 卤化氢和氢卤酸
一.制备
采用单质合成、复分解、卤化物水解等方法 1、单质合成 氢气流在氯气中燃烧,生成的氯化氢用水吸收 H2 + Cl2 → 2HCl
(1)氯分子在加热或强光照射下分解为 h 氯原子 Cl Cl + Cl (2)氯原子和氢分子反应
0 ⅥA ⅦA He 氦 O 氧 F 氟 Ne 氖 S 硫 Cl 氯 Ar 氩 Se 硒 Br 溴 Kr 氪 Te 碲 I 碘 Xe 氙 Po At 砹 氡
2 3 4 5 6
P区元素的特点(2)具有多种氧化数
因原子的价电子构型为 ns2np1-5 这种现象称为 非金属元素还具有负氧化数 ns、np电子可参与成键 惰性电子对效应 0
Cl、Br、I的价电子构型 ns 原子序数np 9 拆开1对电子 价层电子构型 2s22p5 原子半径/pm 64 ns np 电负性( xp) 4.0 拆开2对电子 I1/(kJ·mol-1) 1681
氟(F) 氯(Cl) 溴(Br) 碘(I) 氧化数为+1
nd17
35 53 3s23p5 4s24p5 5s25p5 氧化数为+3 99 114 133 nd 3.0 2.8 2.5 1251 1140 1008 氧化数为+5 ns np nd 、0 -1 -1、0 -1、0 拆开3对电子 主要氧化数 -1、0 +1、+3 +1、+3 +1、+3 氧化数为+7 +5、+7 +5、+7 +5、+7 ns np nd
氟(F2)
集聚状态 气体 熔点/℃ -219.6 沸点/℃ -188
氯(Cl2)
气体 -101 -34.6
溴(Br2)
液体 –7.2 58.76
碘(I2)
固体 113.5 184.3
颜色* 溶解度
毒性
浅黄 分解水
黄绿 红棕 紫黑 在水中溶 易溶于 解度不大 有机溶剂 具有刺激性气味,并有毒
毒性减小
具有多种氧化数 并相差2
氟(F) 氯(Cl) 溴(Br) 碘(I)
9 17 35 53 原子序数 特殊性 2 5 2 5 2 5 价层电子构型 2s22p5 3s 3p 4s 4p 5s 5p 1.F 电负性大,非金属性强 114 99 133 原子半径/pm 64 2.原子半径小,空间位阻不大,氧化能 3.0 2.8 2.5 电负性( p) 4.0 力强,与具有多种氧化数的元素化合 I1/(kJ· -1) 1681 1251 1140 1008 mol 时,该元素往往可呈现最高氧化数 -1、0 -1、0 -1、0 如 AsF5、SF6 、+1、+3 +1、+3 IF7 主要氧化数 -1、0 +1、+3 3.F-F键能小,易打开,化学性质活泼 、+7 +5、+7 +5、+7 +5
二、物理性质
HF HCl HBr HI
具有强烈刺激性气味的无色气体 在空气中易与水蒸气结合形成白色酸雾 熔点/℃ -83.1 沸点/℃ 19.54
-114.8 -8点升高
变形性 ,色散力 相对分子质量 分子极性 ,取向力 以色散力为主,分子间力 ,熔、沸点
HF
F
HCl
HBr
HI
具有强烈刺激性气味的无色气体 F F F H H H H H F F 在空气易与水蒸气结合形成白色酸雾
Br2
I2
反应条件 阴冷 常温 强光照射 常温 600C 高温
2、与水反应:分两类
(1)氧化作用 2X2 + 2H2O
(2)歧化水解 X2 + H2O
4HX + O2↑
H+ + X- + HXO
F2 只能发生(1)类反应,并反应激烈 2F2 + 2H2O →4HF + O2↑ Cl2、Br2、I2主要发生(2)类反应 反应程度越来越小 K 加碱使平衡右移 Br2 Cl2 I2 4.2×10-4 7.2×10-9 2.0×10-13
熔、沸点升高
∵ 固态为分子晶体 ∴ 熔、沸点较低
氟(F2)
集聚状态 气体 熔点/℃ -219.6 沸点/℃ -188
氯(Cl2)
气体 -101 -34.6
溴(Br2)
液体 –7.2 58.76
碘(I2)
固体 113.5 184.3
颜色*
浅黄
黄绿
红棕
紫黑
颜色加深
氟(F2)
氯(Cl2)
溴(Br2)
碘(I2)
156.6 ℃ 231.9 ℃ 630.5 ℃
Tl 铊 Pb 铅 Bi 铋 Po 6 303.5 ℃ 327.5 ℃ 271.3 ℃
At 砹 Rn 氡
P区元素的特点
(4)某些金属具有半导体性质
ⅢA ⅣA
0
2 B 硼 C 碳 N 氮 O 氧 F 氟 Ne 氖
3 Al 铝 Si 硅 P 磷 S 硫 Cl 氯 Ar 氩 4 Ga 镓 Ge 锗 As 砷 Se 硒 Br 溴 Kr 氪 5 In 铟 Sn 锡 Sb 锑 Te 碲 I 碘 Xe 氙 6 Tl 铊 Pb 铅 Bi 铋 Po At 砹 Rn 氡
沿B-Si-As-Te-At对角线,右上角为 除氢外,所有的非金属全部集中在p区 ⅢA-ⅦA和零族元素为p区元素 非金属(包括线上),左下角为金属
二、P区元素的特点 (1) 除ⅦA和零族外,均为从 典型非金属→准金属→典型金属
ⅢA 非 原 金 ⅣA 属 金 B子 硼 C 碳 半 铝 Si 硅 性 属 Al 径 增 性 Ga 镓 Ge 锗 增 强 减 大 弱 In 铟 Sn 锡 Tl 铊 Pb 铅 ⅤA N 氮 P 磷 As 砷 Sb 锑 Bi 铋
氟(F) 氯(Cl) 溴(Br) 碘(I)
9 17 35 53 原子序数 价层电子构型 2s22p5 3s23p5 4s24p5 5s25p5 与稳定的8电子构型原子相比较仅缺一 99 114 133 原子半径/pm 64 个电子,在同周期元素中核电荷是最多的, 3.0 2.8 2.5 电负性( p) 4.0 原子半径是最小的。 1251 1140 1008 I1/(kJ· -1) 1681 mol 非金属性减弱 -1、0 --1、0 + 困难 -1、0 易获得电子,是同周期中非金属性最强 I1大, X - e → X 主要氧化数 -1、0 +1、+3 +1、+3 的元素 只有碘才有这种可能 +1、+3 +5、+7 +5、+7 +5、+7
11-2 卤族单质
氟(F2)
一、物理性质
氯(Cl2) 溴(Br2) 碘(I2)
集聚状态 气体 气体 液体 固体 均为双分子 熔点/℃ -219.6 -101 –7.2 113.5 (具有稳定的8电子构型及较高的键能) 沸点/℃ -188 -34.6 58.76 184.3 在周期表中,整族是双原子分子的只有卤素
如
超纯锗
ⅤA
ⅥA
ⅦA He 氦
11-1 卤族元素通性
卤素,希腊文原意为成盐元素
ⅢA ⅣA ⅤA ⅥA
0
ⅦA He 氦
2 B 硼 C 碳 N 氮 O 氧 F 氟 Ne 氖
3 Al 铝 Si 硅 P 磷 S 硫 Cl 氯 Ar 氩 4 Ga 镓 Ge 锗 As 砷 Se 硒 Br 溴 Kr 氪 5 In 铟 Sn 锡 Sb 锑 Te 碲 I 碘 Xe 氙 6 Tl 铊 Pb 铅 Bi 铋 Po At 砹 Rn 氡
P区元素的特点 0 ⅢA ⅣA ⅤA ⅥA ⅦA He 氦 2 B 硼 C 碳 N 氮 O 氧 F 氟 Ne 氖 3 Al 铝 Si 硅 P 磷 S 硫 Cl 氯 Ar 氩 660.4℃
(3)金属的熔点较低
这些金属 Ga 镓 Ge 锗 As 砷 Se 彼此可形成氪 4 硒 Br 溴 Kr 29.78 ℃ 973.4 ℃ 低熔合金 In 铟 Sn 锡 Sb 锑 Te 碲 I 碘 Xe 氙 5
2 3 4 5 6 ⅢA B 硼 Al 铝 Ga 镓 In 铟 Tl 铊 ⅣA C 碳 Si 硅 Ge 锗 Sn 锡 Pb 铅 ⅤA N 氮 P 磷 As 砷 Sb 锑 Bi 铋 ⅥA 高 He 氦 ⅦA 低 氧 O氧氧 F 氟 Ne 氖 化稳 化稳 S 数硫 Cl 氯 Ar 氩 定 数定 Se 硒 Br 溴 Kr 氪 化性 化性 合增 减 Te 碲 I合 碘 Xe 氙 物 强At 砹 Rn 氡 物弱 Po
3、非金属卤化物水解:制备溴化氢和碘化氢
将水滴入三溴化磷或三碘化磷 PBr3+3H2O → H3PO3+ 3HBr PI3+3H2O → H3PO3+ 3HI 将溴滴入磷与少量水的混合物中 3Br2+2P+6H2O → 2H3PO3+6HBr 将水滴入碘与磷的混合物中 3I2+ 2P + 6H2O → 2H3PO3+ 6HI
2
