高中化学3.3羧酸酯教案新人教版选修5
最新人教版选修5高中化学第3章第3节 羧酸酯教学设计

第三章第三节羧酸酯一、教材分析1.教材的知识结构:本节是人教版高中《有机基础》第三章第三节《羧酸酯》,从知识结构上看,包含了两部分内容即羧酸和酯,乙酸是羧酸类物质的代表物,酯是羧酸与醇的衍生物。
本节分两课时完成,其中第一课时按教材的编排体系,包含乙酸概述、乙酸的分子结构特点、乙酸的性质研究、乙酸的用途。
第二课时包含酯的结构、性质、存在。
2.教材的地位和作用:从教材整体上看,乙酸既是很重要的烃的含氧衍生物,又是羧酸类物质的代表物,它和我们的生活生产实际密切相关,从知识内涵和乙酸的分子结构特点上看,乙酸既是醇、酚、醛知识的巩固、延续和发展,又是好酯(油脂)类合物的基础。
3.教重点:根据教大纲和以上的教材分析,乙酸和酯的结构和性质是本课的教重点,特别是酯反应的特点和过程分析即对酯反应演示实验的观察和有关问题及据分析、推又是性质教中的重点。
4.教材的处:为了使教具有更强的逻辑性,突出教重点内容,充分说明物质的性质决定于物质的结构,对教材的内容在教程序上进行了调整:(1)将乙酸的结构特点放在乙酸的性质之后去认识。
当生对乙酸的性质有了感性认识后,再提出为什么乙酸会有这些性质呢?必然使生联想到它的结构有何特点呢?这样既加深了生对结构决定性质,性质反映结构观点的认识,又能反映出思维的主要特点:由具体到抽象,由宏观到微观。
(2)为了突出酯反应的过程分析和加深对酯反应的条件解,将课本P148的演示实验做了适当的改进(祥见教过程设计),增强了生对实验过程及实验据的分析推断能力,达到了“知其然,知其所以然”的教效果。
(3)添加乙酸乙酯的水解试验,让生感受酯在不同条件下只得水解程度5.教目标:知识目标:(1)使生掌握乙酸的分子结构特点,主要物性质、性质和用途,初步掌握酯反应。
(2)根据酯的组成和结构的特点,认识酯的水解反应。
能力目标:通过实验设计、动手实验,培养生的观察能力,加强基本操作训练,培养分析、综合的思维能力和求实、创新、合作的优良品质。
2019-2020年高中化学 3.3《羧酸 酯》第一课时《羧酸》教案 新人教版选修5

2019-2020年高中化学 3.3《羧酸酯》第一课时《羧酸》教案新人教版选修5【教学目标】1、知识与技能:了解常见的羧酸及分类;了解同位素原子示踪法在探究酯化反应机理方面的应用;掌握以乙酸为重要代表物的羧酸的结构特征和性质;掌握如何通过化学实验达到研究物质性质的基本方法。
2、过程与方法:采用实验探究法,提高学生科学探究能力,训练思维的严密性、逻辑性;通过新旧知识的联系,类比归纳,培养学生分析推理、迁移扩展的能力。
3、情感态度与价值观:让学生体会科学探究的艰辛与乐趣,培养求实、严谨的优良品质。
让学生领会化学与人类生活的密切联系,激发学生学习化学的积极性。
【重点难点】1、探究重点:乙酸的酸性和乙酸的酯化反应;2、探究难点:乙酸的酯化反应;【教学方法】实验、探究、讨论【教学过程】:【创设情景】生活中,我们常常会吃到一些带有酸味的食物,同学们想一下有哪些?【投影】如食醋含有乙酸,柠檬含有柠檬酸,苹果含有苹果酸,葡萄含有酒石酸,酸奶中含有乳酸,为什么它们都有酸味呢?大家观察它们的结构,有什么共同的特征?【学生回答】羧酸类有机物的官能团是羧基,低级羧酸有酸味。
【过渡】青苹果、未熟的香蕉,吃起来什么感觉?成熟以后,会闻到香味,这种香味是什么物质?酯。
今天我们学习:羧酸酯【板书】一、羧酸:1、定义:由烃基和羧基相连组成的有机物【讲解并板书】常见羧酸,如乙酸、硬脂酸、油酸、苯甲酸、乙二酸等。
分析得出R-COOH及饱和一元羧酸的通式表示C n H2n+1COOH。
2、分类:按所含的羧基个数:一元羧酸、二元羧酸和多元羧酸根据烃基的不同:脂肪酸:如乙酸、硬脂酸(C17H35COOH)芳香酸:如苯甲酸(C6H5COOH)【过渡】羧酸在我们日常生活中广泛存在,我们今天进一步学习羧酸的代表物乙酸的性质。
【电子板书】3、乙酸物理性质:颜色:状态:气味::沸点:熔点:溶解性:【过渡】在日常生活中,我们知道食醋可以除去在水壶里的水垢,表现了乙酸什么性质?【学生】酸性。
高中化学 3.3《羧酸 酯》第二课时 酯教案 新人教版选修5-新人教版高二选修5化学教案

第三章烃的含氧衍生物第三节羧酸酯第二课时教案教学目标:【知识与技能】:1、掌握酯的概念;了解酯的通式和简单酯的命名;了解酯的物理性质及用途;掌握酯的水解反应,进一步理解可逆反应、催化作用。
2、通过酯水解实验培养学生设计实验能力、实验能力,观察、分析、对比综合推理能力;通过酯的概念和命名来培养学生抽象、概括形成规律性认识的能力。
【过程与方法】:通过酯水解的实验,培养学生实验设计方法、观察方法;通过酯的学习深化学习具体物质的科学方法。
【情感、态度与价值观】:通过硫酸和氢氧化钠在酯化或酯的水解反应中的不同作用,领悟内外因的辩证关系;结合酯化反应和酯的水解反应强化对化学反应本质的辩证认识。
通过酯水解反应的实验培养学生探索、创新品质。
教学重点:酯水解反应的机理(即断键部位);硫酸和氢氧化钠在酯化和酯的水解反应中的不同作用;教学难点:对酯化反应和酯的水解反应的化学反应本质的辩证认识。
教学方法:小组教学、实验探究教学过程:教师活动学生活动设计意图【导入新课】泗水的风光特色【板书】二、酯【展示】生活中含有酯的物质。
同时给出结构简式,通过观察引导学生分析酯的结构特点【板书】1、酯的概念官能团:-COOR【复习回顾】乙酸乙酯怎么生成的?写出乙酸、甲酸分别和乙醇的酯化反应的化学方程式。
欣赏图片观察,思考,找出共同特征聆听,强化官能团思考、回答并找两名同学到黑板上板书。
1.CH3COOH+HOCH2CH3CH3COOC2H5+H2OHCOOH+HOCH2CH3HCOOC2H5+H2O激发学生对家乡的热爱之情有个别到一般,实现总结能力上的提升回忆旧知识酯化反应,为接受新知识酯的水解反应奠定基础。
【分析理解】由以上两个方程式引导学生寻找酯命名的规律。
【板书】2、酯的命名——某酸某酯练习:给下列酯命名观察,思考,寻找规律通过语言提示,发现规律进一步“升华”,由个别认识到一般认识。
【展示】收集乙酸乙酯的试管,结合生活中含有酯的物质,总结酯的物理性质【板书】3、酯的物理性质观察,阅读由现象和生活到结论,降低难度,同时贴近学生生活。
高中化学3.3羧酸酯教案新人教版选修5

羧酸酯审核签字:中国书法艺术说课教案今天我要说课的题目是中国书法艺术,下面我将从教材分析、教学方法、教学过程、课堂评价四个方面对这堂课进行设计。
一、教材分析:本节课讲的是中国书法艺术主要是为了提高学生对书法基础知识的掌握,让学生开始对书法的入门学习有一定了解。
书法作为中国特有的一门线条艺术,在书写中与笔、墨、纸、砚相得益彰,是中国人民勤劳智慧的结晶,是举世公认的艺术奇葩。
早在5000年以前的甲骨文就初露端倪,书法从文字产生到形成文字的书写体系,几经变革创造了多种体式的书写艺术。
1、教学目标:使学生了解书法的发展史概况和特点及书法的总体情况,通过分析代表作品,获得如何欣赏书法作品的知识,并能作简单的书法练习。
2、教学重点与难点:(一)教学重点了解中国书法的基础知识,掌握其基本特点,进行大量的书法练习。
(二)教学难点:如何感受、认识书法作品中的线条美、结构美、气韵美。
3、教具准备:粉笔,钢笔,书写纸等。
4、课时:一课时二、教学方法:要让学生在教学过程中有所收获,并达到一定的教学目标,在本节课的教学中,我将采用欣赏法、讲授法、练习法来设计本节课。
(1)欣赏法:通过幻灯片让学生欣赏大量优秀的书法作品,使学生对书法产生浓厚的兴趣。
(2)讲授法:讲解书法文字的发展简史,和形式特征,让学生对书法作进一步的了解和认识,通过对书法理论的了解,更深刻的认识书法,从而为以后的书法练习作重要铺垫!(3)练习法:为了使学生充分了解、认识书法名家名作的书法功底和技巧,请学生进行局部临摹练习。
三、教学过程:(一)组织教学让学生准备好上课用的工具,如钢笔,书与纸等;做好上课准备,以便在以下的教学过程中有一个良好的学习气氛。
(二)引入新课,通过对上节课所学知识的总结,让学生认识到学习书法的意义和重要性!(三)讲授新课1、在讲授新课之前,通过大量幻灯片让学生欣赏一些优秀的书法作品,使学生对书法产生浓厚的兴趣。
2、讲解书法文字的发展简史和形式特征,让学生对书法作品进一步的了解和认识通过对书法理论的了解,更深刻的认识书法,从而为以后的书法练习作重要铺垫!A书法文字发展简史:①古文字系统甲古文——钟鼎文——篆书早在5000年以前我们中华民族的祖先就在龟甲、兽骨上刻出了许多用于记载占卜、天文历法、医术的原始文字“甲骨文”;到了夏商周时期,由于生产力的发展,人们掌握了金属的治炼技术,便在金属器皿上铸上当时的一些天文,历法等情况,这就是“钟鼎文”(又名金文);秦统一全国以后为了方便政治、经济、文化的交流,便将各国纷杂的文字统一为“秦篆”,为了有别于以前的大篆又称小篆。
人教版高中化学选修五 3.3羧酸 酯第2课时(教案1)

注课前练习]写出乙酸、甲酸分别和乙醇的酯化反应的化学方程式。
此反应中浓H2SO4的作用是什么?思考、回答并找两名同学到黑板上板书。
过渡]下面我们来学习一下羧酸和酯的通性二、羧酸1、羧酸是由烃基与羧基相连组成的有机化合物。
羧基是羧酸的官能团。
羧酸的分类:可以按烃基的种类的不同分为脂肪酸和芳香酸;可以按羧基数目的不同,可以分为一元羧酸、二元羧酸和多元羧酸;按碳原子数目不同可分为低级脂肪酸、高级脂肪酸。
一元羧酸的通式:R—COOH,饱和一元脂肪酸的分子通式为C n H2n O2或C n H2n+1—COOH。
2、羧酸的通性(1) 常见一元羧酸的酸性强弱顺序为:甲酸、苯甲酸、乙酸、碳酸(2) 酯化反应R1—COOH + R2-CH2OHR1-COO—CH2-R2 +H2O特例]无机含氧酸与醇作用也能生成酯,如 C2H5OH+HONO2C2H5-O-NO2+H2O(3) 还原反应讲]由于羟基的影响,羧基中的羰基比醛、酮分子中的羰基较难发生加成反应,但在特殊试剂如LiAlH4的作用下可将羧酸还原为醇。
3、羧酸的命名讲]选含羧基的最长的碳链作为主链,按主链碳原子数称某酸;从羧基开始给主链碳原子编号;在某酸名称之前加入取代基的位次号和名称。
4、重要的羧酸—甲酸讲]甲酸俗称蚁酸,是有刺激性气味的液体,甲酸分子中即含有羟基又有醛基,因而能表现出羧酸和醛两类物质的性质。
甲酸的性质甲酸与银氨溶液的反应:下方文件为赠送,方便学习参考第三节酯化反应教学目标知识技能:掌握酯化反应的原理、实验操作及相关问题,进一步理解可逆反应、催化作用。
能力培养:培养学生用已知条件设计实验及观察、描述、解释实验现象的能力,培养学生对知识的分析归纳、概括总结的思维能力与表达能力。
科学品质:通过设计实验、动手实验,激发学习兴趣,培养求实、探索、创新、合作的优良品质。
科学方法:介绍同位素示踪法在化学研究中的使用,通过酯化反应过程的分析、推理、研究,培养学生从现象到本质、从宏观到微观、从实践到理论的科学思维方法。
高中化学 3-3 羧酸 酯课堂教案 新人教版选修5

【课堂教案】2014年高中化学 3-3 羧酸酯新人教版选修5●课标要求认识羧酸、酯的典型代表物的组成和结构特点,知道它们的转化关系。
●课标解读1.认识乙酸、乙酸乙酯的组成和结构特点。
2.明确羧酸、酯的分子式通式、同分异构体的判断及书写。
3.掌握羧酸、酯的化学性质,明确二者转化规律。
●教学地位羧酸、酯是两种重要的烃的含氧衍生物,在日常生活中应用广泛。
羧酸和醇的酯化反应规律“酸脱羟基醇脱氢”更是高考命题的热点,尤其是羧酸和酯的相互转化,是有机合成题中的常考点。
●新课导入建议乙酸又名醋酸,它是食醋的主要成分,是日常生活经常接触的一种有机酸。
自然界的许多动植物中含有与乙酸性质相似的有机酸如蚁酸、安息香酸、草酸等。
另外,苹果和香蕉中还存在一类具有香味的酯类物质,这些有机物具有怎样的性质?这就是本节课要研究的问题。
●教学流程设计课前预习安排:看教材P60-63,填写【课前自主导学】并完成【思考交流1,2】。
⇒步骤1:导入新课,本课时教学地位分析。
⇒步骤2:对【思考交流】进行提问,反馈学生预习效果。
⇒步骤3:师生互动完成【探究1】。
可利用【问题导思】的设问作为主线。
⇓步骤7:通过【例2】的讲解研析,对“探究2 乙酸乙酯的制备方法”中注意的问题进行总结。
⇐步骤6:师生互动完成【探究2】。
可利用【问题导思】的设问作为主线。
⇐步骤5:指导学生自主完成【变式训练1】和【当堂双基达标】第4题。
⇐步骤4:通过【例1】和教材P61讲解研析,对“探究1 酯化反应的规律及类型”中注意的问题进行归纳总结。
⇓步骤8:指导学生自主完成【变式训练2】和【当堂双基达标】中第3题。
⇒步骤9:引导学生自主总结本课时主干知识,然后对照【课堂小结】,布置学生课下完成【课后知能检测】和【当堂双基检测】中剩余的习题。
1.羧酸(1)概念羧酸是由烃基与羧基相连构成的有机化合物,通式为R—COOH,官能团为羧基。
(2)分类(3)通性都具有酸性,都能发生酯化反应。
高中化学 第3章 第3节 羧酸 酯教案 新人教版选修5-新人教版高二选修5化学教案
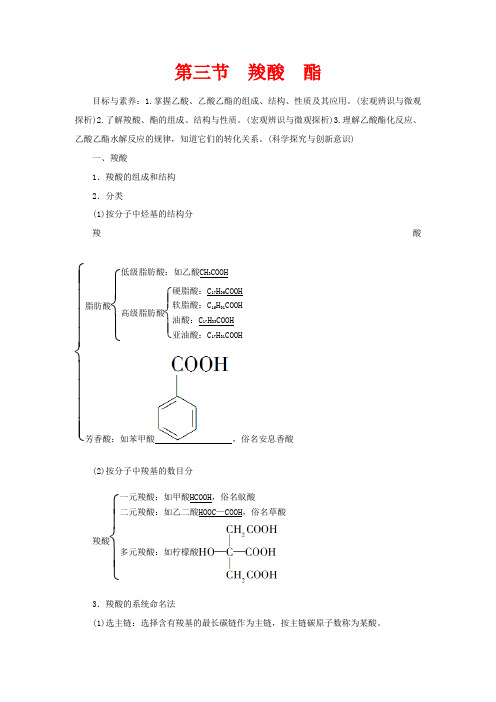
(2) 可以表现为酮和醇的性质。( )
(3)乙酸的酸性比H2CO3强,可以溶解石灰石。( )
(4)含18O的乙醇与乙酸发生酯化反应生成的H2O中含18O。
( )
[答案](1)× (2)× (3)√ (4)×
2.等浓度的下列稀溶液:①乙酸、②苯酚、③碳酸、④乙醇,它们的pH由小到大排列正确的是( )
CH3COOH+CH3CH2OH CH3COOC2H5+H2O。
②原理:
用同位素示踪法探究酯化反应中的脱水方式。用含有示踪原子的CH3CH OH与CH3COOH反应,经测定,产物 中含有示踪原子,说明酯化反应的脱水方式是“酸脱羟基醇脱氢”。
三、酯
1.组成、结构和命名
—
2.酯的性质
(1)物理性质
低级酯是具有芳香气味的液体,密度一般小于水,难溶于水,易溶于乙醇、乙醚等有机溶剂。
4.某有机物A的结构简式为 ,若取等质量的A分别与足量的Na、NaOH、新制的Cu(OH)2悬浊液充分反应,理论上消耗这三种物质的物质的量之比为( )
A.3∶2∶1B.3∶2∶2
C.6∶4∶5D.3∶2∶3
D[—COOH、—OH均与Na反应,—COOH、酚—OH与NaOH,—COOH、—CHO与新制的Cu(OH)2悬浊液均反应生成铜盐。]
(5)写出D与足量NaOH溶液共热反应的化学方程式:
__________________________________________________
__________________________________________________。
(6)写出A生成E的化学方程式:________________________
教学设计人教版选修五 第三章第三节 羧酸 酯

教学设计人教版选修五第三章第三节羧酸酯教版高中化学选修5第3章第3节《羧酸酯》第二课时《酯》教学设计一、教材分析1.教材的知识结构:本节是人教版高中《有机化学基础》第三章第三节《羧酸酯》,从知识结构上看,包含了两部分内容即羧酸和酯,乙酸是羧酸类物质的代表物,酯是羧酸与醇的衍生物。
本节分两课时完成,其中第一课时按教材的编排体系,包含乙酸概述、乙酸的分子结构特点、乙酸的性质研究、乙酸的用途。
第二课时包含酯的结构、性质、存在。
2.教材的地位和作用:从教材整体上看,乙酸既是很重要的烃的含氧衍生物,又是羧酸类物质的代表物,它和我们的生活生产实际密切相关,从知识内涵和乙酸的分子结构特点上看,乙酸既是醇、酚、醛知识的巩固、延续和发展,又是学好酯(油脂)类化合物的基础。
所以大多数老师都把重点放在了第一课时,其实酯是我们有机合成的知识链中重要环节,既是酸的酯化反应产物,也是酸和醇的来源,还是后面学习油脂的基础。
更是生活中普遍存在,又与生活息息相关的重要物质。
3.教学重点:根据教学大纲和以上的教材分析,酯的结构和性质是本课的教学重点,特别是酯的水解反应条件的探究。
二、教学目标设计:知识与技能:1. 了解酯类化合物的结构特点。
2. 掌握酯类化合物的化学性质。
过程与方法:1.培养学生用已知条件设计实验及观察、描述、解释实验现象的能力,2.培养学生对知识的分析归纳、概括总结的思维能力与表达能力。
(3)突出乙酸乙酯的水解学生实验,让学生通过对比实验,感受酯在不同条件下的水解程度,分析得出结论。
(4)介绍生活中的酯化反应和水解反应,增加兴趣,实现从生活到化学,从化学回到生活的学习理念。
四、教学过程设计为此我创建了四个教学情景问题。
教学情境1:给出资料,引出课题,扩展教学内容。
出示乙酸乙酯实物,显示图片引课:酯类化合物的存在:水果、饮料、糖类、糕点等。
问题:酯通过什么反应制得?条件?原理?酯化反应的类型活动与探究1已知乙二酸和乙二醇能形成三种酯,一种链状酯(两者物质的量之比为2∶1或1∶2)、一种环状酯和一种高分子酯,写出生成这三种酯的化学方程式:(1)_______________________________________________________________________;(2)_______________________________________________________________________;(3)_______________________________________________________________________。
2019-2020年高中化学 3.3《羧酸 酯》第一课时《羧酸》教案 新人教版选修5(II)

2019-2020年高中化学 3.3《羧酸酯》第一课时《羧酸》教案新人教版选修5(II)一、教学目标1.知识与技能知道乙酸的分子结构和主要性质,了解羧酸的结构特点和主要化学性质,理解酯化反应的反应机理。
2.过程与方法通过“乙酸的官能团——乙酸的化学性质——羧酸的官能团——羧酸的化学性质”模式的学习,提高分析能力和逻辑思维能力,强化“结构决定性质”的基本化学思想。
3.情感态度与价值观通过从羧酸结构到羧酸性质的推理,从中体会到严谨求实的科学态度;通过对生活中遇到的羧酸的了解,感受化学学科在生产生活中的重要作用;通过分子结构模型,意识到化学世界的外在美。
二、学情分析在必修2中对乙酸的物理性质、化学性质有了初步了解,知道乙酸具有酸性、能发生酯化反应。
在此基础上,本节课继续以乙酸为代表学习羧酸的结构及性质,理解酯化反应的反应机理。
三、教材分析本节位于人教版《选修5》第三章第三节,是关于羧酸类物质的内容,在有机化学学习中有承上启下的作用。
四、教学重点:乙酸的结构特点和主要化学性质。
教学难点:酯化反应机理的应用,含多官能团有机物发生酯化反应的化学方程式的书写。
五、学法指导通过知识回顾、师生互动、实验感知、实验评价、对比思考、动手操作、迁移应用、归纳总结、习题巩固等手段理解并掌握乙酸和羧酸的性质,了解羧酸类物质在生活中的应用。
六、教学用具主要仪器:表面皿、玻璃棒、试管、药匙、烧杯等。
药品:乙酸、碳酸钠粉末、滴加酚酞的氢氧化钠溶液、镁条、pH试纸、石蕊试液。
辅助用具:多媒体、球棍模型。
七、教学过程七、板书设计八、教案附件【实验感知】根据所提供的药品和仪器设计简单的实验验证乙酸的酸性药品:乙酸、碳酸钠粉末、滴加酚酞的氢氧化钠溶液、镁条、pH试纸、石蕊试液主要仪器:表面皿、玻璃棒、试管、药匙、烧杯等。
【实验设计】甲乙两实验小组利用下图所示仪器和药品,设计了两套实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱。
请对其进行评价。
(完整版)人教版高中化学选修5(教案+习题)3.3羧酸酯(2)正式版
f or s o 知识技能掌握酯化反应的原理、实验操作及相关问题,进一步理解可逆反应、催化作用。
过程方法1、培养学生用已知条件设计实验及观察、描述、解释实验现象的能力,2、培养学生对知识的分析归纳、概括总结的思维能力与表达能力。
教学目的情感价值观介绍同位素示踪法在化学研究中的使用,通过酯化反应过程的分析、推理、研究,培养学生从现象到本质、从宏观到微观、从实践到理论的科学思维方法。
重 点酯的组成和结构特点难 点酯的水解反应知识结构与板书设计二、羧酸1、羧酸是由烃基与羧基相连组成的有机化合物。
羧基是羧酸的官能团。
2、羧酸的通性(1) 常见一元羧酸的酸性强弱顺序为:甲酸、苯甲酸、乙酸、碳酸(2) 酯化反应: (3) 还原反应3、羧酸的命名4、重要的羧酸—甲酸甲酸与银氨溶液的反应: 甲酸与Cu(OH)2 的反应:三、酯1、结构简式通式:RCOOR′分子式通式:C n H 2nO 2与同碳原子羧酸同分异构体。
2、酯类化合物的存在:水果、饮料、糖类、糕点等3、化学性质 酯的水解:酯+水酸+醇教学过程备注[课前练习]写出乙酸、甲酸分别和乙醇的酯化反应的化学方程式。
此反课题3.3羧酸 酯(2)课型新授课编稿教师备课教师授课时间授课班级i n gs i n t h e i r b e i n g a r e g o o d f o r s o 应中浓H 2SO 4的作用是什么?思考、回答并找两名同学到黑板上板书。
[过渡]下面我们来学习一下羧酸和酯的通性二、羧酸1、羧酸是由烃基与羧基相连组成的有机化合物。
羧基是羧酸的官能团。
羧酸的分类:可以按烃基的种类的不同分为脂肪酸和芳香酸;可以按羧基数目的不同,可以分为一元羧酸、二元羧酸和多元羧酸;按碳原子数目不同可分为低级脂肪酸、高级脂肪酸。
一元羧酸的通式:R—COOH ,饱和一元脂肪酸的分子通式为C n H 2n O 2 或C n H 2n+1—COOH 。
2、羧酸的通性(1) 常见一元羧酸的酸性强弱顺序为:甲酸、苯甲酸、乙酸、碳酸(2) 酯化反应R 1—COOH + R 2-CH 2OHR 1-COO—CH 2-R 2 +H 2O[特例]无机含氧酸与醇作用也能生成酯,如 C 2H 5OH+HONO 2C 2H 5-O-NO 2+H 2O(3) 还原反应[讲]由于羟基的影响,羧基中的羰基比醛、酮分子中的羰基较难发生加成反应,但在特殊试剂如LiAlH 4 的作用下可将羧酸还原为醇。
高中化学 第三章 第三节 羧酸 酯教案 新人教版选修5-新人教版高中选修5化学教案

第三节 羧酸 酯[课标要求]1.了解羧酸和酯的组成和结构特点。
2.了解羧酸的分类及乙酸的物理性质、酯的物理性质及存在。
3.掌握乙酸和乙酸乙酯的结构特点和主要性质,理解乙酸的酯化反应和乙酸乙酯水解反应的基本规律。
4.掌握羧酸和酯之间的相互转化,学会其在合成与推断中的应用。
1.羧酸是由烃基与羧基相连构成的有机化合物,其官能团是羧基(—COOH)。
2.酯化反应的实质是羧酸脱羟基醇脱氢,乙酸、乙醇发生酯化反应的化学方程式为CH 3COOH +C 2H 5OH 浓H 2SO 4△CH 3COOC 2H 5+H 2O 。
3.乙酸乙酯在酸性条件下的水解是可逆的,生成乙酸和乙醇。
乙酸乙酯在碱性条件下的水解是不可逆的。
反应生成乙酸钠和乙醇,反应的化学方程式为CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH 。
4.羧酸与同碳原子的酯互为同分异构体。
如C 4H 8O 2属于羧酸的结构有2种,属于酯的结构有4种。
羧酸的概述1.羧酸的概念及分类(1)概念:由烃基和羧基相连构成的有机化合物。
(2)通式:R —COOH(或C n H 2n O 2),官能团为—COOH 。
(3)分类:①按分子中烃基的结构分类:②按分子中羧基的数目分类:2.甲酸的结构与性质(1)结构特点结构式甲酸分子结构比较特殊,不但有羧基结构,也有醛基结构,是一个具有双重官能团的化合物。
(2)化学性质①具有羧酸的性质:酸性、能发生酯化反应。
②具有醛类的某些性质:能发生银镜反应,能与新制Cu(OH)2悬浊液反应。
[特别提醒](1)能发生银镜反应的物质含有醛基,但不一定属于醛,如甲酸、甲酸酯、葡萄糖。
(2)甲酸和新制Cu(OH)2反应,加热则发生氧化反应,若不加热则发生中和反应。
(3)硬脂酸、软脂酸是乙酸的同系物,而油酸不是乙酸的同系物。
1.下列物质中,不属于羧酸类的是( )A.乙二酸B.苯甲酸C.硬脂酸 D.石炭酸解析:选D 要确定有机物是否为羧酸,关键看有机物中是否含有羧基,由于石炭酸中无羧基,故不属于羧酸。
人教版高中化学选修五3.3《羧酸酯》参考教案

第三节羧酸酯教学目标:1.认识酯典型代表物的组成和结构特点。
2.根据酯的组成和结构的特点,认识酯的水解反应。
教学重点: 酯的组成和结构特点。
教学难点: 酯的水解反应。
探究建议: ①实验:乙醇的酯化;乙酸乙酯的水解。
②实验:自制肥皂与肥皂的洗涤作用。
③阅读与讨论:乳酸、磷脂的结构、性质特点和营养作用。
课时划分:一课时教学过程:[复习提问]写出下列化学方程式:乙醛与新制的Cu(OH)2碱性悬浊液共热。
[学生活动]评判黑板上的化学方程式,检查自己书写的化学方程式。
[设计意图]对学过的知识进行查漏补缺,由有机物的衍生关系引出乙酸。
[设问]上述化学反应中有机物之间存在什么样的衍生关系?[板书][引入]这一节课我们就来学习羧酸、酯[板书]第三节羧酸、酯[自学]P60第1、2自然段,提问:1、羧酸的官能团,称为基。
2、酸的通性有哪些?作为有机含氧酸还有哪些特性?3、羧酸的分类?代表物的化学式和结构简式?4、饱和一元羧酸的通式为?[回答]CH3COOH+C2H5OH CH3COOC2H5+H2O[板书]一、羧酸1、分类:脂肪酸、芳香酸或一元酸、二元酸。
2、分子式:C2H4O2、结构式:;纯净乙酸(冰乙酸、冰醋酸)在16.6℃以下为针状晶体。
[思考]无水乙酸又称冰醋酸(熔点16.6℃)。
在室温较低时,无水乙酸就会凝结成像冰一样的晶体。
请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。
[投影][填一填]1、羧酸的官能团为:,通式为:代表物乙酸的化学式为:。
核磁共振氢谱有个吸收峰,峰的面积比为:。
说明乙酸中有种H原子,数目比为:。
所以乙酸的结构简式为:。
科学探究1:乙酸的酸性——提出问题,根据要求设计实验。
[问题] 初中化学已介绍过乙酸是一种有机弱酸,请同学们根据现有的化学药品或自己寻找合适的试剂设计实验方案①证明乙酸有酸性;②比较乙酸、碳酸、苯酚的强弱。
[提供药品] 镁粉氢氧化钠溶液氧化铜固体硫酸铜溶液碳酸钠粉末乙酸苯酚紫色石蕊试液无色酚酞试液等。
2019-2020年高中化学 3.3《羧酸 酯》第一课时《羧酸》教案 新人教版选修5(IV)

2019-2020年高中化学 3.3《羧酸酯》第一课时《羧酸》教案新人教版选修5(IV)教学目标【知识与技能】1、了解常见的羧酸及分类;2、掌握以乙酸为重要代表物的羧酸的结构特征和性质;3、掌握乙酸酸的通性,并学会运用;4、理解同位素原子示踪法在探究酯化反应机理方面的应用。
【过程与方法】采用问题探究法,提高学生科学探究能力,训练思维的严密性、逻辑性;通过新旧知识的联系,类比归纳,培养学生分析推理、迁移扩展的能力。
【情感态度与价值观】让学生体会科学探究的艰辛与乐趣,培养求实、严谨的优良品质。
让学生领会化学与人类生活的密切联系,激发学生学习化学的积极性。
通过同位素原子示踪法的方法教育,拓展学生的视野,让学生树立远大的理想。
教学环节教师活动学生活动设计意图(一)情景激学【PPT】观看视频——蜜蜂蜇人,用蜜蜂分泌物中的甲酸引入【资料卡片】介绍羧酸在我们的生活中非常常见,用途也很多,如生活中的食醋;各种水果中的羧酸;在食品包装袋的配料表上经常见到苯甲酸或山梨酸,他们是食品防腐剂;一些消炎药中也含有羧酸。
学生广泛列举,认真倾听,观看投影从生活走进化学,让学生充分感受羧酸与生活密切关联,产生浓厚兴趣质【PPT】展示一幅漫画为什么乙酸能清除水垢?这体现了乙酸的什么性质?从中比较出乙酸和碳酸酸性强弱。
【板书】羧酸的化学性质1)酸性学生写出乙酸电离反应方程式,从结构上分析官能团羧基的断键方式。
【思考】如何证明其酸性呢?酸的通性1、能使指示剂变色2、能与活泼金属反应(Na)3、能与金属氧化物反应(CaO)4、能与碱反应(Cu(OH)2)5、能与部分盐反应(Na2CO3)学生思考,按照问题要求,回答相应问题复习回顾,让学生将所学知识应用到生活中,从化学走进生活【科学探究1】比较乙酸、碳酸、苯酚的酸性强弱引导学生设计实验方案并作出评价。
【投影】合理的装置图交流合作,设计实验方案,预测现象,。
按照要求,原因分析、得出结论培养学生的思考能力和对知识的迁移能力知识总结:物质能反应的官能团Na -COOH -OHNaOH -COOH -OH(酚)Na2CO3-COOH -OH(酚)NaHCO3-COOH【学以致用】1、1mol该有机物能与 4 mol钠反应。
高中化学 3.3《羧酸 酯》第二课时 酯教案 新人教版选修5(2)

《羧酸酯》——酯一、教材分析本节课选自人教版高中化学选修5《有机化学基础》第三章中的第三节“羧酸酯”。
本章教材强调从学生生活实际和已有知识出发,尽力渗透结构分析的观点,使学生在必修2第三章《有机化合物》知识的基础上有所提高。
本节课酯的内容是以学生所学的有机化合物常识为基础的,提倡从学生的生活经验出发,在介绍了有机物——乙酸的基础上引入的。
酯在有机化学中起着承上启下的作用,酯是烃的含氧衍生物知识体系中不可或缺的部分,它建构于醇、酚和酸的知识体系之上,对学生构建一个完整的知识链条“烃——醇——醛——酸——酯”有着举足轻重的作用;同时对于学生后面掌握合成新型高分子材料的学习起到了重要的铺垫和推动作用;酯类物质在自然界中有广泛的存在,日常生活中饮料、糖果以及糕点等都含有部分酯类香料,因此,酯类物质对人类的美好生活起到了重要的影响。
二、学情分析学生通过必修2《有机化合物》以及选修5前两章内容的学习,已经基本了解了研究有机化学的方法及有机化合物结构与性质的关系,初步掌握了有机化学的学习方法。
通过对烃、卤代烃、醇、酚、醛知识的探究学习,学生初步构成了以官能团为线索的有机化合物的知识体系。
因此在本节内容的讲授过程中,基于学生目前的知识水平与认知能力,可以有效的开展探究式的教学,在原有的醇、酸的知识体系上建构羧酸酯的相关知识,利于学生的理解和掌握。
本节课的内容由生活中水果为什么会有香味,为什么会有那么多口味各异的饮料引入,从生活角度来让学生体味化学的魅力,以此来激发学生的学习兴趣,学生对本节课的学习必定有所期待。
三、教学目标(一)知识与技能目标(1)了解酯的概念、命名,同分异构体以及物理性质;(2)根据酯的组成与结构的特点,理解酯的水解反应。
(二)过程与方法目标(1)通过酯的水解反应原理的实验探究过程,学会运用观察法和实验探究法等方法研究问题;(2)通过本节课的学习,进一步体会有机物结构决定性质,性质反映结构的学习思路和方法;(3)通过本节课的学习,体会分析、归纳、推理的方法在知识学习中的作用。
人教版化学选修五教案:3-3 羧酸 酯--------

第三节羧酸酯●课标要求教学地位认识羧酸、酯的典型代表物的组成和结构特点,知道它们的转化关系。
羧酸、酯是两种重要的烃的含氧衍生物,在日常生活中应用广泛。
羧酸和醇的酯化反应规律“酸脱羟基醇脱氢”更是高考命题的热点,尤其是羧酸和酯的相互转化,是有机合成题中的常考点。
●小常识乙酸又名醋酸,它是食醋的主要成分,是日常生活经常接触的一种有机酸。
自然界的许多动植物中含有与乙酸性质相似的有机酸如甲酸(HCOOH蚁酸)、安息香酸(C6H5COOH)、草酸(HOOC-COOH 乙二酸)、苹果酸、柠檬酸等。
另外,苹果和香蕉中还存在一类具有香味的酯类物质,这些有机物具有怎样的性质?这就是本节课要研究的问题。
知识点一羧酸一、概念羧酸是由烃基与羧基相连构成的有机化合物,通式为R—COOH,官能团为羧基。
二、分类三、通性都具有酸性,都能发生酯化反应。
问题.酸的通性有哪些?【提示】(1)遇酸碱指示剂变色;(2)与活泼金属反应产生H2;(3)与碱性氧化物反应生成盐和水;(4)与碱发生中和反应;(5)与盐发生复分解反应。
、知识点二乙酸一、组成和结构乙酸又叫醋酸和冰醋酸,冰乙酸二 、物理性质 沸点117.9℃三 、化学性质 1、酸的通性乙酸的电离方程式为:CH 3COOHCH 3COO -+H +[科学探究]利用相关的仪器与药品,设计一个简单的一次性完成的实验装置,验证乙酸 、碳酸和苯酚溶液的酸性强弱:结论: 酸性:乙酸>碳酸>苯酚(1)CH 3COOH 溶液使石蕊变红(2)2CH 3COOH +2Na ―→2CH 3COONa +H 2↑ (3)2CH 3COOH +CaO ―→Ca(CH 3COO)2+H 2O (4)CH 3COOH +NaOH ―→CH 3COONa +H 2O(5)CaCO 3+2CH 3COOH ―→Ca(CH 3COO)2+CO 2↑+H 2O醇、酚、羧酸中羟基的比较2、酯化反应反应规律:羧酸脱去羟基,醇脱去羟基氢原子。
化学:3.3《羧酸 酯》教案(新人教版选修5).

第三章第三节羧酸酯第1课时曾关宝段、活动酒是越陈越香”。
你、结构式:;纯净乙酸(冰乙酸、冰醋酸在羧酸的官能团为:羧基,通式为:-COOH代表物乙酸的化学式为:C2个吸收峰,峰的面积比为:3:1 。
说明乙酸中有2种H原子,数目比为:以乙酸的结构简式为:CH3COOH、化学性质初中化学已介绍过乙酸是一种有机弱酸,合适的试剂设计实验方案①证明乙酸有酸性;②实验方案:[板书](2、酯化反应[学生实验]乙酸乙酯的制取:学生分三组做如下实验,结束后,互相比较所获得产物的量。
[投影]堂时减少乙酸乙酯在溶液中的溶解量,提高收集效率,并提高乙酸乙酯的纯度,因而收集量要多。
[讲]脱水有两种情况,(1酸脱羟基醇脱氢;(2醇脱羟基酸脱氢。
在化学上为了辨明反应第三章第三节羧酸酯第2课时曾关宝[讲]一元羧酸的通式为R—COOH,饱和一元脂肪酸的分子通式为C n H2n+1—COOH。
分子式相同的羧酸、羧酸酯、羟基醛、羟基酮等互为同分异构体。
[讲]羧酸的沸点比相应的醇的沸点高,碳原子数在4以下的羧基能与水互溶,随着分子中碳链的增长,羧酸在水中的溶解度迅速减小,直到与相对分子质量相近的烷烃的溶蚁酸(甲酸HCOOH柠檬酸HO —C —COOHCH 2—COOHCH 2—COOH未成熟的梅子、李子、杏子等含有草酸、安息香酸(苯甲酸COOHCH 2COOHCH(OHCOOH苹果酸CH 3COOH醋酸(乙酸CH 3CHCOOHOH乳酸[板书]4、重要的羧酸酯是羧酸分子中羧基上的羟基(—OH被烃氧化(-OR取代后的产物。
酯是一种羧酸衍生物,其分子是由基和烃氧基相连构成三、酯、结构简式通式:RCOOR′分子式通式:C n H 2nO 2与同碳原子羧酸同分异构体。
酯类难溶于水,易溶于乙酸和乙醚等有机溶剂,密度一般比水小。
低级酯是具有芳香气味的液体。
]2、酯类化合物的存在:水果、饮料、糖类、糕点等。
(1怎样设计酯水解的实验?(2酯在酸性、碱性、中性哪种条件易水解呢?1、(2两个问题,讨论酯水解实验的设计方案。
《羧酸酯》教案1(新人教选修5)

教案课题:第三章第三节羧酸酯(1) 授课班级课时教学目的知识与技能认识酸典型代表物的组成和结构特点,过程与方法研究探索式,辅以多媒体动画演示情感态度价值观通过设计实验、动手实验,激发学习兴趣,培养求实、探索、创新、合作的优良品质。
重点乙酸的化学性质难点乙酸的结构对性质的影响知识结构与板书设计第三节羧酸、酯一、乙酸1、分子式:C2H4O2、结构式:;纯洁乙酸〔冰乙酸、冰醋酸〕在16.6℃以下为针状晶体。
2、化学性质(1)、乙酸的酸性(2)、酯化反响○1、浓硫酸的作用:催化剂;除去生成物中的水,使反响向生成物方向进行。
○2、饱和碳酸钠溶液可以除去乙酸,溶解乙醇,减少乙酸乙酯在溶液中的溶解量。
(3)、酯化反响原理:酸脱羟基、醇脱氢原子教学过程教学步骤、内容教学方法、手段、师生活动[引入]我国是一个酒的国度,五粮液享誉海内外,国酒茅台香飘万里。
“酒是越陈越香〞。
你们知道是什么原因吗这一节课我们就来学习羧酸、酯[板书]第三节羧酸、酯[自学提问]羧酸的官能团是什么酸的通性有哪些作为有机含氧酸还有哪些特性羧酸的分类代表物的化学式和结构简式饱和一元羧酸的通式为[投影][板书]一、乙酸1、分子式:C2H4O2、结构式:;纯洁乙酸〔冰乙酸、冰醋酸〕在16.6℃以下为针状晶体。
[思考]无水乙酸又称冰醋酸〔熔点16.6℃〕。
在室温较低时,无水乙酸就会凝结成像冰一样的晶体。
请简单说明在实验中假设遇到这种情况时,你将如何从试剂瓶中取出无水乙酸。
[投影][讲]羧酸的官能团为:羧基,通式为:-COOH代表物乙酸的化学式为:C2H4O2核磁共振氢变有2个吸收峰,峰的面积比为:3:1 。
说明乙酸中有2种H原子,数目比为:3:1。
所以乙酸的结构简式为:CH3COOH [板书]2、化学性质(1)、乙酸的酸性[科学探究] 初中化学已介绍过乙酸是一种有机弱酸,请同学们根据现有的化学药品或自己寻找适宜的试剂设计实验方案① 证明乙酸有酸性;② 比较乙酸、碳酸、苯酚的强弱。
【推荐】人教版高中化学选修五-羧酸 酯第1课时(教案)

3.3 羧酸酯教學設計第1課時教學目的知識技能認識酸典型代表物的組成和結構特點,過程方法研究探索式,輔以多媒體動畫演示情感價值觀通過設計實驗、動手實驗,激發學習興趣,培養求實、探索、創新、合作的優良品質。
重點乙酸的化學性質難點乙酸的結構對性質的影響知識結構與板書設計第三節羧酸、酯一、乙酸1、分子式:C2H4O2、結構式:;純淨乙酸(冰乙酸、冰醋酸)在16.6℃以下為針狀晶體。
2、化學性質(1)、乙酸的酸性(2)、酯化反應○1、濃硫酸的作用:催化劑;除去生成物中的水,使反應向生成物方向進行。
○2、飽和碳酸鈉溶液可以除去乙酸,溶解乙醇,減少乙酸乙酯在溶液中的溶解量。
(3)、酯化反應原理:酸脫羥基、醇脫氫原子教學過程備註引入]我國是一個酒的國度,五糧液享譽海內外,國酒茅臺香飄萬裏。
“酒是越陳越香”。
你們知道是什麼原因嗎?這一節課我們就來學習羧酸、酯第三節羧酸、酯自學提問]羧酸的官能團是什麼?酸的通性有哪些?作為有機含氧酸還有哪些特性?羧酸的分類?代表物的化學式和結構簡式?飽和一元羧酸的通式為?投影]酸的通性一、乙酸1、分子式:C2H4O2、結構式:;純淨乙酸(冰乙酸、冰醋酸)在16.6℃以下為針狀晶體。
投影]乙酸的分子比例模型和核磁共振氫譜2、化學性質(1)、乙酸的酸性科學探究] p60 提供藥品]鎂粉氫氧化鈉溶液氧化銅固體硫酸銅溶液碳酸鈉粉末乙酸苯酚紫色石蕊試液無色酚酞試液等。
投影]實驗方案:(2)、酯化反應學生實驗]乙酸乙酯的制取:學生分三組做如下實驗,實驗結束後,互相比較所獲得產物的量。
第一組:在一支試管中加入3 mL乙醇和2 mL乙酸,按教材P63,圖3-21連接好裝置,用酒精燈緩慢加熱,將產生的蒸氣經導管通到盛有飽和碳酸鈉溶液的接受試管的液面上,觀察現象。
第二組:在一支試管中加入3 mL乙醇,然後邊振盪邊慢慢加入2 mL濃硫酸和2 mL乙酸,用酒精燈緩慢加熱,將產生的蒸氣經導管通到盛有水的接受試管的液面上,觀察現象。
高中化学 第三章 烃的含氧衍生物 第三节 羧酸 酯教案 新人教版选修5-新人教版高二选修5化学教案

第三节羧酸酯[明确学习目标] 1.了解羧酸和酯的组成和结构特点。
2.掌握羧酸和酯的化学性质。
3.掌握酯化反应的断键规律。
一、羧酸1.羧酸的定义及分类(1)概念由烃基和羧基相连构成的有机化合物。
(2)通式01羧基。
R—COOH,官能团是□饱和一元羧酸的通式:C n H2n+1COOH或□02C n H2n O2。
2.羧酸的化学性质(1)酸性羧酸具有酸的通性。
酸性强弱比较:羧酸>碳酸>苯酚。
(2)酯化反应浓H2SO4如丙酸与甲醇的反应□07CH3CH2COOH+CH3OH△CH3CH2COOCH3+H2O。
二、酯1.组成和结构01—OH被□02—OR′取代后的产物,(1)酯是羧酸分子羧基中的□简写为□03R—COOR′,R和R′可以相同,也可以不同。
(2)羧酸酯的官能团是□04。
2.酯的性质 酯的密度一般小于水,难溶于水,易溶于乙醇、乙醚等有机溶剂,低级酯是具有芳香气味的液体。
化学性质是易发生□05水解反应,其条件是酸催化或碱催化,有关化学方程式:(1)酸性条件:CH 3COOC 2H 5+H 2O稀硫酸△CH 3COOH +C 2H 5OH 。
(2)碱性条件:CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH 。
提示:用含有18O 的乙醇(CH 3CH 182OH)与乙酸反应,反应后18O 只存在于乙醇和乙酸乙酯中。
2.实验室制备乙酸乙酯,回答有关问题:(1)乙醇、乙酸和浓硫酸混合时,应怎样操作?(2)收集乙酸乙酯的试管内盛有的饱和碳酸钠溶液的作用是什么?(3)反应中浓硫酸的作用是什么?(4)反应中乙醇和乙酸的转化率能达到百分之百吗?(5)收集在试管内的乙酸乙酯是浮在上层,还是沉在试管底部,还是与Na 2CO 3溶为一体?为什么?(6)用什么方法将收集到的乙酸乙酯分离出来?提示:(1)混合时应向乙醇中慢慢加入浓硫酸,然后加入乙酸。
(2)吸收蒸出的乙醇,中和乙酸,降低乙酸乙酯在水中的溶解度,便于分层。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A 1种B 2种C 3种D 4种
1mol下列有机物在NaOH溶液中完全反应,所需NaOH的物质的量分别是多少?
1⑵⑶
板书设计:
教学反思:
审核签字:
在水中溶解性。
(2)化学性质
①酸的通性
练习:写出丙酸与Na、MgO、KOH、Na2CO3反应的方程式
2酯化反应
练习:丙酸与甲醇的反应
【第二课时】
三、酯
知识回顾:
书写乙酸与乙醇制取乙酸乙酯的化学方程式,指出断键位置。
书写RCOOH与R′OH发生酯化反应的化学方程式。
1.酯的结构和命名:
或RCOOR′,读做某酸某酯。
官能团:
2.乙酸的物理性质
3.乙酸的化学性质
(1)酸性
完成下列表格
CH3COOH
紫色石蕊试液
Na
CuO
NaOH
CaCO3
CH3COOH +HOCH2CH3
酯化反应的实质:酸脱去,醇脱去。
【思考】
1浓硫酸的作用
②盛反应液的试管为什么要向上倾斜45°
③导管末端能不能插入液面下?为什么?.
④饱和Na2CO3溶液的作用是什么?
4.酯的合成:分析酯的结构,找到相应的酸和醇,一般需要浓硫酸和加热。
练习:推测下列酯类化合物是由哪些相应的有机物合成的。
课堂小结:
酯的水解和酯化反应都属于取代反应,在酸性条件下二者是可逆的;酯在碱性条件下可以彻底水解得到羧酸钠和相应的醇(酚)。
(1) HCOOC2H5;(2);(3)
课后自测
1.若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用
HCOOC2H5读做
2.酯的物理性质:
3.酯的化学性质——水解反应
⑴酸性条件:
⑵碱性条件:
说明:
⑴水解速率:酯在条件下水解速率最快,其次是条件,条件下几乎不水解;升高温度,有利于增大水解速率。
⑵水解程度:在碱性条件下彻底水解,可逆;在酸性条件下部分水解可逆的。
⑶水解产物:酸性条件下得到相应,碱性条件下得到相应。
⑤能不能用NaOH溶液来代替Na2CO3溶液吗?
⑥实验中为什么要用小火加热保持微沸?
⑦如何分离出酯?
小结
二、羧酸
1.定义:
2.羧酸的分类
(1)按烃基结构分为
(2)按烃基是否饱和分为
(3)按羧基的数目分为
(4)按烃基中碳原子数的多少分为
3.羧酸通式
4.羧酸的性质
(1)物理性质
随烃基中碳原子数目增多,沸点逐渐,羧酸酯课题第三节羧酸酯
设计教师
授课教师
时间
课型
新授课
课时
2
教学
目标
1.掌握羧基的结构特点和性质特点
2.掌握酯基的结构特点和性质特点
3.掌握羧酸的化学性质
重点
难点
重点:羧基的结构特点及化学性质
难点:羧酸、酯的化学性质
教法
分析比较
教具
PPT
教材分析
师生活动
【第一课时】
一、乙酸
1.乙酸的分子结构
分子式:
结构简式:
