第十章 天然气燃料电池
燃料电池介绍

燃料电池燃料电池(FuelCell)是一种将存在于燃料与氧化剂中的化学能直接转化为电能的发电装置。
燃料和空气分别送进燃料电池,电就被奇妙地生产出来。
它从外表上看有正负极和电解质等,像一个蓄电池,但实质上它不能“储电"而是一个“发电厂"。
能源的创造和消费已经成为当今世界不可或缺的根本要素。
通过能源的生产和利用,人们的衣食住行等需求得到了满足,并极大的提高了现代社会的生活质量,推动了现代技术的快速开展。
当前,一方面我们的家居、办公和生产等所需要的大局部能源均来自化石燃料,而一方面,化石燃料的使用在造就人类文明飞速开展的同时,也造成了很大的环境问题,这些环境问题反过来成为了制约人类社会进步开展的羁绊。
此外,人类对化石燃料的无序开采和低效使用与化石燃料储量的有限产生了矛盾,如果不能及时的寻找新的可替代能源,人类在用尽化石燃料后,将面临无能源可用的危机。
幸运的是,近年来出现的一些新的能源生产技术为解决上述问题提供了可能,这些技术包括核能技术、氢能源及燃料电池技术、太阳能技术、风能和生物能技术等。
其中,以燃料电池技术为代表的氢能源受到国内外专家学者和政府机构越来越多的青睐,燃料电池技术被认为是21世纪首选的清洁高效的发电技术,美国把燃料电池技术列为仅次于基因组方案和超级材料后的第三项重要技术加以支持。
燃料电池的原理最早是由WilliamGrove在1839年提出,20世纪50年代培根(Bacon)做了一些先驱性的工作;二十世纪六十年代由通用电气公司开发的质子交换膜燃料电池被美国宇航局用于“双子星座〞航天器的动力源。
随着上世纪80年代中期电池材料和制备技术的突破性进展,使燃料电池的性能大幅度提高,本钱大大降低,民用性和实用化前景较为看好。
而质子交换膜燃料电池发电过程中只产生水作为排放物,其越来越受到电动汽车行业的重视。
美国通用公司、戴姆勒克莱斯勒公司、福特公司和本田公司,德国尼奥普兰汽车公司,日本的丰田公司及瑞典的斯堪尼亚汽车公司等相继研发出了实用的以PEMFC为电源驱动的公共汽车和混合燃料电池车。
燃料电池的应用与发展

燃料电池的应用与发展近年来,燃料电池(Fuel Cell)作为一种高效、环保的新能源技术,备受人们的关注。
燃料电池跟传统的化石燃料发电方式相比,更加环保和高效,能源利用效率可达50%以上。
目前燃料电池的应用涉及交通、能源、家庭等众多领域,已经逐步成为替代传统化石燃料的重要选择。
本文探讨燃料电池的应用和发展,以及未来的发展趋势。
一、燃料电池的基本原理及分类燃料电池是指在电化学反应中以氢气或其他可燃气体为燃料,通过催化剂催化氢气与氧气发生电化学反应,将化学能转化为电能的一种新型电源。
燃料电池按燃料类型分为直接甲醇燃料电池、质子交换膜燃料电池、固体氧化物燃料电池等几种。
质子交换膜燃料电池(PEMFC)是目前应用最为广泛的一种燃料电池,它的优势是能够高效地将氢气转化为电能,而且排放的是纯净的水,不会对环境造成污染,同时也适用于多种应用场景。
二、燃料电池在交通方面的应用交通是燃料电池应用领域的重要部分,它被认为是将燃料电池技术推向社会应用的关键一步。
图书馆吧彩票燃料电池汽车主要是通过将氢气与空气产生化学反应来产生电能,从而驱动汽车。
燃料电池汽车的优点在于其排放的物质是水,不存在传统燃料车辆产生的二氧化碳、二氧化硫、硝化物等有害气体。
同时,燃料电池汽车续航能力强,充氢时间短,而且使用寿命长,目前已经成为全球新能源汽车的主流之一。
尽管燃料电池汽车的价格和配套设施仍有待提高,但它的未来发展前景十分广阔。
三、燃料电池在能源方面的应用燃料电池除了在汽车领域的应用外,在能源领域也有广泛的应用。
燃料电池发电采用燃料电池技术进行发电,其特点是效率高、排放物质少,不受地理限制,是一种具有很大发展前景的清洁能源。
目前,燃料电池在小型应用装备、军事领域、民用发电等领域的应用也逐渐增多,展示了其在未来能源领域的广阔应用前景。
四、燃料电池在家庭方面的应用燃料电池可以成为家庭能源的备用电源,对于无电区域或者突发情况下的停电也有很好的应用前景。
燃料电池结构与工作原理

燃料电池结构与工作原理嘿,今天咱们来聊聊燃料电池的结构和工作原理,这可就像是一个神奇的能量小宇宙呢。
我有一次去参加一个科技展,在那儿看到了燃料电池的展示模型,那可真是让我大开眼界。
就像打开了一个充满神秘的宝盒一样。
咱先说说燃料电池的结构。
它就像一个精心设计的小城堡,有好多重要的部分呢。
首先是电极,电极就像城堡的大门,有阳极和阴极。
阳极就像是迎接客人的前门,它负责接收燃料,比如氢气。
那些氢气分子就像一群小客人,排着队来到阳极这个大门前。
阴极呢,就像是城堡的后门啦,氧气从这儿进来。
这两个电极可都不简单,它们是用特殊的材料做的,就像城堡的大门得用坚固又合适的材料一样,这样才能保证反应顺利进行。
在电极之间呢,有电解质。
这电解质就像城堡里的走廊,不过这个走廊很神奇哦。
它是一种能让离子通过,但不让电子通过的物质。
就像走廊有特殊的魔法,只允许特定的人(离子)走,其他人(电子)得走别的路。
这电解质的种类还不少呢,有的是质子交换膜,就像一条只允许质子通过的神秘通道。
我看着展示模型里的电解质部分,感觉它就像一个隐藏着巨大秘密的地方,那些看不见的离子就在这里面穿梭。
还有双极板,双极板就像城堡的墙壁,把一个个小单元隔开,同时还起到了导电和分配气体的作用。
它上面有一些小通道,就像墙壁上的小管道,氢气和氧气可以通过这些小通道分别到达阳极和阴极。
这双极板得设计得很精巧,要是通道太窄或者太宽,气体分布不均匀,那整个燃料电池的性能就会受到影响。
我想象着那些气体在双极板的小通道里流动,就像小蚂蚁在迷宫里找路一样,必须得走得顺畅。
再说说燃料电池的工作原理吧,这可就更有趣了。
当氢气来到阳极这个前门的时候,它就像被施了魔法一样,在催化剂的作用下,分解成了氢离子和电子。
氢离子就通过电解质这个特殊走廊向阴极走去,而电子呢,它们可不能走这条路,就像被一堵无形的墙挡住了。
于是电子就只能从外电路走,这就产生了电流,就像一群小电子在电线里奔跑,给我们提供电能。
燃料电池
电池的发展方向
• 光电池使用方便,特别是近年来 微小型半导体逆变器迅 速发展,促使其应用更加快捷.美,日,欧和发展中国家都 制定出庞大的 光伏技术发展计划,开发方向是大幅度提 高光电池转换效率和稳定性,降低成本,不断扩大产 业. 目前已有80多个国家和地区形成 • 商业化,半商业化 • 生产能力,年均增 • 长达16,市场开拓 • 从 空间转向地面 • 系统应用。
四、燃料电池
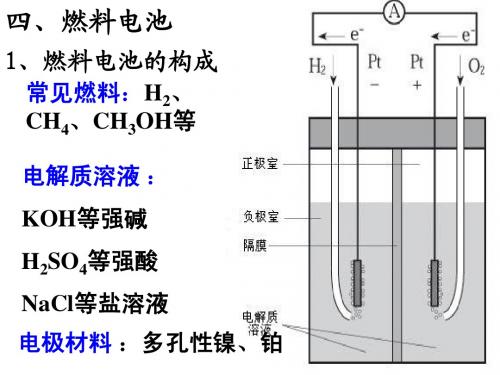
1、燃料电池的构成
常见燃料:H2、 CH4、CH3OH等
电解质溶液 :
KOH等强碱 H2SO4等强酸 NaCl等盐溶液
电极材料 :多孔性镍、铂
2、燃料电池的极反应的书写
氢氧燃料电池
电解质溶液为酸性: 负极:2H2 - 4e- = 4H+ 正极:O2 + 4H++4e- = 2H2O 总反应:2H2 + O2 = 2H2O
正极:2O2+4H2O+8e-=8OH总反应:
CH4
A
ePt (-) Pt (+) eO2
CH4+2O2+2KOH=K2CO3+3H2O
负极室 KOH 溶液
阳极室
隔膜
甲烷氧气燃料电池工作原理
学生练习:燃料:CO,CH3OH电解质为碱性
总结:
①先写总反应:燃料在氧气中的燃烧 若有CO2生成,且电解质为强碱时,
①两电极材料均为惰性电极.
②负极-可燃性气体失电子,正极-助燃性气体得
电子.
③电极反应考虑电解质溶液.
(13年新课标1)4.银质器皿日久表面会逐渐变黑, 这是生成了Ag2S的缘故。根据电化学原理可进行 如下处理:在铝质容器中加入食盐溶液,再将变 黑的银器浸入该溶液中,一段时间后发现黑色会 褪去。下列说法正确的是( ) B A.处理过程中银器一直保持恒重 B.银器为正极,Ag2S被还原生成单质银 C.该过程中总反应为2Al+3Ag2S=6Ag+Al2S3 D.黑色褪去的原因是黑色Ag2S转化为白色AgCl
燃料电池内部构造及作用

燃料电池内部构造及作用
燃料电池的内部构造包括燃料电池堆、氢气供给系统、空气供给系统、水热管理系统及电控系统。
1.燃料电池堆:由多个单电池以串联方式层叠组合构成,将双极板与膜电极三合一组件(MEA)
交替叠合,各单电池之间嵌入密封件,经前、后端板压紧后用螺杆紧固住,就组成了质子交换膜燃料电池堆。
2.氢气供给系统:的主要作用是将储氢瓶出来的氢气进行一定的处理,转化成适于燃料电池堆内
化学反应的气体(流量、压力、温度、湿度等),经过氢气供给系统的处理,让燃料电池堆处于相对舒服的条件下。
3.空气供给系统:主要是对即将进入燃料电池的空气进行过滤、加压、加湿等处理,保证燃料电
池堆阴极侧的温度、压力、湿度及流量处于比较舒适的范围内。
4.水热管理系统:在燃料电池的运行过程中起到重要作用,通过对水蒸气的控制以及对热量的管
理,确保燃料电池的正常运行。
5.电控系统:是燃料电池的控制系统,负责监控和管理燃料电池的运行状态,确保其安全、稳定
地运行。
总的来说,燃料电池的内部构造和作用是确保其高效、稳定地运行,并产生电能。
1。
天然气燃料电池原理

天然气燃料电池原理
天然气燃料电池是一种利用天然气(主要是甲烷)作为燃料,将化学能转化为电能的
装置,它采用了电化学原理,同时具备高效、环保、节能等特点。
天然气燃料电池的工作原理可分为以下三个步骤:
第一步:氧化反应
天然气燃料电池的负极为阳极(anode),正极是阴极(cathode)。
在阳极上,天然
气与水发生化学反应,生成一氧化碳(CO)、二氧化碳(CO2)、水的混合物和电子。
反应式如下:
CH4 + H2O → CO + 3H2 + 4e-
天然气燃料电池中使用的阳极通常是一种钯催化剂,它能够帮助天然气与水的反应加速,同时也能够帮助释放出反应过程中产生的电子,将它们引导到电路中。
第二步:电子传导
电子在阳极上被释放后,它们会通过外部电路传递到阴极上,从而驱动电器负载工作。
在这个过程中,电子流向阴极,同时将电量转换为势能。
最后,电子在阴极与氧气发生还原反应,生成水和热能,同时产生一个电压。
反应式
如下:
因此,天然气燃料电池产生的电能,是通过将天然气的化学能转化为电子流,并利用
电子流驱动电器负载,最后通过阴极与氧气的还原反应产生的。
总结:
天然气燃料电池利用了化学能转化为电能的原理,经过氧化、电子传导以及还原反应
等过程,将天然气的化学能转换为运动能和势能,从而驱动电器负载的工作。
它具备环保、高效、节能等优点,是未来能源发展的重要组成部分。
燃料电池讲解通用课件

04
燃料电池汽车将成为未来交通 出行的重要选择之一,具有零 排放、高效、节能等优点。
燃料电池将成为分布式发电和 储能的重要技术之一,具有环
保、灵活、高效等优点。
燃料电池在航空、航海等领域 也将得到广泛应用,如用于无
人机、船舶等。
燃料电池的技术挑战与瓶颈
01
技术挑战
02
提高燃料电池的能量密度和功率密度需要解决材料科学、制造
燃料电池的特点
高效率、低排放、低噪音、快速充电、可靠运行、方便维护等。
燃料电池的应用领域
域
作为电动汽车、船舶、航空器 的动力源,可实现零排放、高
效率的运行。
电力领域
作为电站、备用电源等,可满 足不同场合的用电需求。
工业领域
作为工业用电源,为生产设备 提供稳定可靠的电力保障。
军事领域
实际效率
由于实际运行中存在各种 损失,如反应不完全、热 能散失等,实际效率通常 略低于理论极限值。
提高效率的方法
优化催化剂设计、降低操 作温度、提高反应气体纯 度等措施可以提高燃料电 池的能量转换效率。
燃料电池的发电特点与优势
可再生能源
高效率
燃料电池使用的氢气和氧气可以由可再生 能源如太阳能、风能等提供,因此燃料电 池是一种可再生能源发电技术。
电池壳是燃料电池的外部结构,它能够保护电池不受外界 环境的影响。
燃料电池的制造设备主要包括搅拌器、涂布机、组装设备 和测试设备等。
燃料电池的使用与维护方法
使用燃料电池时,需要确保其工作在合适的温度和压力下,并定期检查其性能和安 全性。
维护燃料电池时,需要定期更换反应介质和电极材料,并保持电池壳的清洁和完好 。
工作原理:燃料电池由阳极、阴极和电解质组成。在燃料电池中,燃料(如氢气)被送到阳极,氧化 剂(如氧气)被送到阴极。阳极和阴极之间通过电解质隔开。当燃料和氧化剂在阳极和阴极上反应时 ,电子从阳极通过外部电路流向阴极,从而产生电流。
燃料电池

燃料电池简介燃料电池是一种电化学的发电装置。
因为燃料电池等温地按电化学方式直接将化学能转化为电能,不经过热机过程,因此其能量转换效率不受卡诺循环的限制,能量转化效率高(理论转化率可达100%,实际可达70%。
);它几乎不产生NOx和SOx的排放。
而且,CO2的排放量也比常规发电厂减少40%以上。
正是由于这些突出的优越性,燃料电池技术的研究和开发倍受各国政府与大公司的重视,被认为是21世纪的洁净、高效的发电技术之一。
燃料电池的基本组成有:电极、电解质、燃料和氧化剂。
燃料可以是H2、CH4、CH3OH、CO等,氧化剂一般是氧气或空气,电解质可为水溶液(H2SO4、H3PO4、NaOH等)、熔融盐(NaCO3、K2CO3)、固体聚合物、固体氧化物等。
发电时,燃料和氧化剂由电池外部分别供给电池的阳极和阴极,阳极发生燃料的氧化反应,阴极发生氧化剂的还原反应,电解质将两电极隔开,导电离子在电解质内移动,电子通过外电路做功并构成电的回路。
与普通电池不同的是,只要能保证燃料和氧化剂的供给,燃料电池就可以连续不断地产生电能。
按电解质划分,燃料电池大致上可分为五类:碱性燃料电池(AFC)、磷酸型燃料电池(PAFC)、固体氧化物燃料电池(SOFC)、熔融碳酸盐燃料电池(MCFC)和质子交换膜燃料电池(PEMFC)。
六十年代碱性燃料电池曾迅速发展并在航天领域得到应用。
七十至八十年代,熔融碳酸盐燃料电池和固体氧化物燃料电池发展起来。
九十年代以来,质子交换膜燃料电池(得到迅猛发展。
美国已确定燃料电池为经济繁荣和国家安全至关重要的27项必须发展的技术之一,PEMFC是其中的重点发展项目。
把燃料电池应用到汽车上是一个历史性的突破,它是靠燃料电池所发电来推动汽车运动的。
目前,许多大的汽车公司都在致力于燃料电池汽车的研究开发上。
这种电动汽车的最大好处是灵敏度高,不会因汽车尾气等造成环境污染。
燃料电池的众多优点吸引了广大的科技人员,各国都投入了大量的财力、人力来研制新型的燃料电池。
高二化学选择性必修课件燃料电池

PEMFC具有高效率、低噪音、零排放等优点。它可以在较低的温度下快速启动并具有较高的功率密度。 此外,PEMFC对燃料的纯度要求不高可以使用重整气或天然气等作为燃料来源。
05
实验操作演示与注意事项
实验器材准备和检查
01
02
03
04
燃料电池模型
确保模型完整无损,电极、电 解质等各部分正常。
电源和电压表
优缺点分析比较
优点总结
燃料电池具有能量转换效率高、污染小、噪音低、燃料来源广泛等优点。同时,不同类型 的燃料电池还具有各自独特的优点,如固体氧化物燃料电池(SOFC)可在高温下工作, 适用于大型电站等领域。
缺点分析
燃料电池的缺点主要包括成本高、寿命有限、对燃料和氧化剂纯度要求高等。此外,不同 类型的燃料电池还存在一些特定的缺点,如碱性燃料电池(AFC)需要使用贵金属催化剂 等。
提供稳定的电源,并配备合适 的电压表以监测电压变化。
实验气体
如氢气、氧气等,确保气体纯 度高,无杂质。
连接线路和开关
确保连接线路畅通,开关灵活 可靠。
实验步骤详细指导
组装燃料电池模型
按照模型说明书正确组装电池各部分 ,确保电极间距、电解质浓度等参数 符合要求。
气体通入与密封性检查
将实验气体通入电池模型,检查各接 口密封性,确保无气体泄漏。
气体泄漏应急处理
电源安全
如发现气体泄漏,应立即关闭气源,迅速 撤离现场,并报告老师或实验室管理员进 行处置。
确保电源稳定可靠,避免短路或过载等情 况发生。如遇电源故障,应立即切断电源 并寻求专业人员帮助。
06
环保意义及未来发展趋势 预测
环保意义阐述
清洁能源转化
燃料电池能将氢气和氧气转化为电能和水,过程中不产生温室气 体和其他有害物质,实现清洁能源的高效转化。
燃料电池范文

燃料电池范文
燃料电池
燃料电池
概述
燃料电池(Fuel Cells)是一种新型的电池,它可以将氢气(或其他
几种气体,如煤气)与氧气通过电化学反应转换为电能,是一种清洁的能
量转换技术。
燃料电池技术可以将氢和氧转换为水,并释放大量的电能。
这种技术的优点是可以替代基于化石燃料的传统能源,减少对环境的污染。
工作原理
燃料电池的工作原理是,在电解液(电解质液)中,燃料(如氢气)
与氧气发生电化学反应,生成电流和水,从而产生电能。
电解液由电解质
构成,而这些电解质使燃料电池能够更有效地转换氢气和氧气为电能。
结构
燃料电池的基本结构包括电解质层、氧化层、燃料供应层、电极和导
电支撑层。
电解质层由薄的电解质膜组成,用来引导电流和控制反应。
氧
化层由氧接受催化剂和形成氧的分子组成,它可以从外部吸收氧,并把氧
的离子传递出去。
燃料供应层由负责传输燃料的催化剂和帮助燃料输入燃
料电池的结构所组成。
电极是在燃料电池中用来收集和输出电流的电极。
最后,导电支撑层由阻断气体和电解液的导电材料组成,它可以支撑催化
剂层,并把催化剂层和外壳连接起来。
种类。
能源化工知识点--天然气生物柴油燃料电池

天然气化工一、天然气基础知识天然气与煤炭、石油并称为一次能源的三大支柱。
狭义的天然气是从能量与资源利用的角度考虑,专指天然蕴藏于底层中油田气、气井气、煤层气、泥火山气和生物生成气中,以甲烷为主的烃类混合物。
天然气是一种优质、经济、清洁的能源和化工原料,燃烧后无废渣、废水产生,是一种公认的绿色燃料。
有机成因说认为天然气主要由深埋地下的有机质经过厌氧菌分解、热分解、聚合加氢等过程而形成,主要分为生物催化、热降解、热裂解几个阶段。
生物催化:有机质在厌氧菌的作用下发生分解,被分解成CO2/CH4/NH3等简单小分子或者生物化学单体,如苯酚、氨基酸、单糖、脂肪酸等。
热降解:发生热解和聚合加氢作用,转化为气态烃类和液体烃类。
热裂解:发生热分解反应,高分子烃分解成低分子烃,液体烃裂解为气态烃,最终形成以甲烷为主的天然气。
无机成因说无机成因说认为天然气是受地球深部岩浆活动、无机盐类分解以及宇宙空间孕育而成的可燃气体。
天然气的组成及分类二.天然气的分离与净化采出气的分离重力分离可除去10~30 μm 及以上直径的颗粒,而且受气体压力和流量波动的影响较小。
重力分离通常用于分离含液量较多、液体或固体颗粒较大的天气,以及对净化要求不高的采气井口、集气站的天然气初级分离。
离心分离是将进入的液体旋转,通过调整流体的流速,可使流体所受到的离心作用力达到重力加速度的几百倍以上,在离心力的作用下,将固体及液体与气体分离。
天然气的脱水1 天然气含水量指标:绝对含水量:指单位体积天然气中所含水分的重量,(mg/m3)。
露点温度:指一定压力条件下,天然气中的水蒸气开始凝结时的温度。
2 常用的方法溶剂吸收法固体吸附法直接冷却法化学反应法(1)溶剂吸收法脱水剂的要求:必须有高的脱水性,具有化学稳定性和热稳定性,容易再生,对烃类气体溶解度小,发泡和乳化倾向性小,无腐蚀性而且廉价易得。
脱水深度(效率)-露点降常用的脱水剂:甘露醇,金属氯化物(2)固体吸附法吸附过程:流体在流经多孔固体颗粒时,其中的某些组分分子被固体内孔表面所吸着的过程。
燃料电池 原理

燃料电池原理燃料电池原理是基于氧气和氢气的化学反应来产生电能,它是一种新型的能源装置,它可以将各种氢源转化化为电能。
燃料电池是一种直接将燃料和氧气化学反应产生电能的装置,与传统的化石能源相比,它具有高能效、低排放、静音和可持续发展等优势。
近年来,燃料电池逐渐成为了能源领域的研究热点。
燃料电池的工作原理基于氢气和氧气的化学反应,通常称为氢氧化电池反应。
该反应的电化学反应可以表述为:H2 + 1/2O2 → H2O在这个反应中,氢气通过氢氧化物质作为电解质,进入阳极,以电子分离为开头的化学反应。
氧气进入阴极,这样在阴极和阳极之间形成了电势差(差异),电路就闭合了,电子从阳极流向阴极,制造出电流,电池就产生了电能。
燃料电池不仅能够使用氢气作为燃料,也可以利用其他的可再生能源,例如:太阳能、生物质等等,同时也可以采用化石燃料,例如:天然气、甲烷、甲醇等等,这样就可以提高能源利用效率,同时减少不良废气的排放。
不同类型的燃料电池有不同的特点和应用,其中最常见的几种类型包括:碱性燃料电池、酸性燃料电池、聚合物电解质燃料电池、固体氟化物燃料电池和高温氧化物燃料电池。
在实际应用中,燃料电池主要分为三个部分:氢气供给系统、燃料电池本身和电池输出系统。
氢气供给系统包括氢气的存储、氢气的输送和氢气的氧化等工艺。
燃料电池本身主要由阳极、阴极和电解质构成。
电池输出系统则是将产生的电能转换为电能输出,例如将电能用于提供电动汽车或工业设备等。
燃料电池是一种先进的能源转换装置,它具有高效、清洁、低碳、环保、持续性等多种优势,是未来替代化石能源的重要途径之一。
目前,燃料电池已经被广泛应用于许多领域,例如:交通运输、航空航天、家庭应用、工业生产等等。
在交通运输领域,燃料电池有望成为汽车燃料电池的主要驱动方式,可以替代传统燃料汽车,减少温室气体排放和空气污染,改善环境质量。
值得注意的是,与其他电池不同,燃料电池的关键是氢气的储存和输送。
燃料电池【最新精品】

固体电解质是SOFC的核心部件,这种电解 质不允许电子和氢离子通过,只允许氧负 离子自由通过。固体电解质一般由固体氧 化物构成,通过氧离子在固体氧空位中的 跃迁实现离子导电。混入了钙、镱或钇等 金属氧化物的氧化锆晶体在高温下会成为
固态良导电体。
SOFC不仅可以用H2、CO等作为燃料,而 且可以直接用天然气、煤气和其它碳氢化 合物作为燃料,以空气为氧化剂。
Membrane Fuel Cell)
碱性燃料电池(AFC)
将35~50%KOH电解液,渗透于多孔而惰 性的基质隔膜材料(如石棉)中。电池的 优点是氧在碱液中的电化学反应速度比酸 性液中的速度大;因此,可有较大的电流 密度和输出功率。
最成熟的碱性燃料电池是纯氢氧燃料电池。
碱性燃料电池有吸引力的特点是不需要 贵金属催化剂或贵金属催化剂载量低。 此外,碱性燃料电池的工作温度低,材 料的耐腐蚀问题易解决。
少,有利于隐蔽目标。PAFC是一种很好的 军用通讯电源。
熔融碳酸盐燃料电池(MCFC)
MCFC被称为第二代燃料电池,工作温度约 650℃。 MCFC以两种或多种碳酸盐的低熔 混合物为电解质,把它渗透进多孔性的基质 中,形成导电性隔膜,膜的两侧分别加上阳 极和阴极。由于工作温度高,阴极和阳极的 电化学反应速度很快,无须使用贵金属作为 催化剂。
MCFC以CO32-为导电离子,直接使用天 然气、煤气燃料,但MCFC的寿命一般 比PAFC短。
MCFC存在的主要问题是热循环过程中 由于电解质的融化和凝结,使基体的体 积发生很大的变化,导致电解质裂纹及 形貌变化。此外,高温下腐蚀严重。
固体氧化物燃料电池(SOFC)
SOFC是PAFC 、MCFC之后能量转换效率最 高的第三代燃料电池。SOFC采用CeO2稳定 的ZrO2(YSZ)陶瓷为固体电解质,Ni-YSZ复 合陶瓷为阳极,Sr掺杂的LaMnO3(LSM)为阴 极,工作温度高达1000℃。
燃料电池的工作原理

燃料电池的工作原理作者:佚名来源:不详录入:Admin更新时间:2008-8-18 10:07:07点击数:8【字体:】燃料电池的一般结构为:燃料(负极)|电解质(液态或固态)|氧化剂(正极)。
在燃料电池中,负极常称为燃料电极或氢电极,正极常称为氧化剂电极、空气电极或氧电极。
燃料有气态如氢气、一氧化碳、二氧化碳和碳氢化合物,液态如液氢、甲醇、高价碳氢化合物和液态金属,还有固态如碳等。
按电化学强弱,燃料的活性排列次序为:肼>氢>醇>一氧化碳>烃>煤。
燃料的化学结构越简单,建造燃料电池时可能出现的问题越少。
氧化剂为纯氧、空气和卤素。
电解质是离子导电而非电子导电的材料,液态电解质分为碱性和酸性电解液,固态电解质有质子交换膜和氧化锆隔膜等。
在液体电解质中应用微孔膜,0.2mm~0.5mm厚。
固体电解质为无孔膜,薄膜厚度约为20μm。
燃料电池的反应为氧化还原反应,电极的作用一方面是传递电子、形成电流;另一方面是在电极表面发生多相催化反应,反应不涉及电极材料本身,这一点与一般化学电池中电极材料参与化学反应很不相同,电极表面起催化剂表面的作用。
在氢氧燃料电池中,氢和氧在各自的电极反应。
氧电极进行氧化反应,放出电子,氢电极进行还原反应,吸收电子,总反应为:O2+2H2→2H2O反应结果是氢和氧发生电化学燃烧,生成水和产生电能。
由热力学变量可得到以下理论电动势和理论热效率公式:Eo=-(ΔG/2F)=1.23Vη=ΔG/ΔH=83.0%式中,ΔG和ΔH分别为自由能变化和热焓变化,F是法第常数。
燃料电池工作的中心问题是燃料和氧化剂在电极过程中的反应活性问题。
对于气体电极过程,必需采用多孔气体扩散电极和高效电催化剂,提高比表面,增加反应活性,提高电池比功率。
氢在负极氧化是氢原子离解为氢离子和电子的过程,若用有机化合物燃料,首先需要催化裂化或重整,生成富氢气体,必要时还要除去毒化催化剂的有害杂质。
用于天然气冷热电三联供系统的燃料电池

用于天然气冷热电三联供系统的燃料电池摘要:介绍了天然气冷热电三联供系统的技术原理,并描述了作为天然气冷热电三联供系统动力设备——燃料电池的工作机理、优点、缺点、关键材料与部件和应用领域。
1天然气冷热电三联供系统天然气冷热电三联供系统是指在动力设备通过不同形式的燃烧后,转换出三种能源产品:电力、热能(含蒸汽或者热水)以及冷水,并根据用户的不同用能特点,将其一体化的多联产、多供应的供能系统。
就天然气冷热电三联供系统供能模式较传统的分散式系统供能模式而言,其理论能源综合利用效率可在80%以上。
天然气冷热电三联供系统能源梯级利用原理见图1。
天然气冷热电三联供系统由动力设备、余热回收设备和制冷设备三个子设备系统组成,其中动力设备占据着核心主导的地位,目前国内外市场上可选择的动力设备主要有:燃气轮机、内燃机、微燃机、斯特林发动机和燃料电池,其中燃料电池在天然气冷热电三联供系统的动力设备中,最具有清洁高效技术优势和市场发展潜力。
2燃料电池2.1燃料电池的工作机理燃料电池是一种电化学装备,工作机理与一般电池非常类似,其单体电池同样是由正负两个电极(负极:燃料电极,正极:氧化剂电极)以及电解质组成,燃料电池的工作原理见图2。
相比于一般电池将活性物质贮存在电池内部的方式有所不同,燃料电池的正、负极本身不包含活性物质,仅仅是个催化转换装置而已。
燃料电池是真正把化学能转化为电能的能量转换设备,燃料和氧化剂由外部供给进行反应,只要反应物不断的进行持续输入,反应产物不断的进行持续排除,燃料电池就能够进行连续地稳定发电。
合理高效的回收燃料电池的热能,可以大大提高燃料利用的效率,并且生产出来的余热也非常清洁。
高温燃料电池的余热温度较高,可以与其他发电装置组成复合式发电循环,以提高系统的整体发电效率和燃料利用效率,中低温燃料电池可以在回热系统中将废热直接回收生产热水或蒸汽,可以运用于采暖、制冷、除湿和生活生产热水等领域。
目前,燃料电池单独发电效率可达50%,如果通过热电联供利用热能,如与燃气轮机构成联合循环,则发电效率将可能达到70%~80%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十章天然气燃料电池10—1 概论10—1—1 燃料电池概论当今能以工业规模生产的电力有火电、水电、核电等三种。
而被誉为第四种电力的燃料电池发电,也正在美、日等发达国家崛起,以急起直追的势头快步进入能以工业规模发电的行列。
燃料电池是一种化学电池,它利用物质发生化学反应时释放出的能量,直接将其变换为电能。
如图10—1所示。
从这一点看,它和其他化学电池如锰干电池、铅蓄电池等是类似的。
但是,它工作时需要连续地向其供给活物质(起反应的物质)燃料和氧化剂,这又和其他普通化学电池不大一样。
由于它是把燃料通过化学反应释出的能量直接变为电能输出,所以被称为燃料电池。
具体地说,燃料电池是利用水的电解的逆反应的“发电机”。
它由正极、负极和夹在正负极中间的电解质板所组成。
最初,电解质板是利用电解质渗入多孔的板而形成,现在正发展为直接使用固体的电解质。
工作时向负极供给燃料(氢),向正极供给氧化剂(空气)。
氢在负极分解成正离子H+和电子e-。
氢离子进入电解液中,而电子则沿外部电路移向正极。
用电的负载就接在外部电路中。
在正极上,空气中的氧同电解液中的氢离子吸收抵达正极上的电子形成水。
这正是水的电解反应的逆过程。
利用这个原理,燃料电池便可在工作时源源不断地向外部输电,所以也可称它为一种“发电机”。
与一般电池一样,燃料电池是由阴极、阳极和电解质构成。
图10—2给出了典型的(单个)燃料电池的构造。
图10—1 燃料电池直接发电与图10—2 燃料电池的构造示意传统间接发电的比较燃料电池的历史可以追溯到19世纪,确切地说是始于1839年英国人格罗夫(W.Grove)181的研究。
格罗夫使用两个铂电极电解硫酸时注意到,析出的气体(氢和氧)具有电化学活性,并在两极产生约1V的电势差。
1894年,奥斯特瓦尔德(W.Ostwald)从热力学理论上证实,燃料的低温电化学氧化优于高温燃烧,电化学电池的能量转换效率高于热机。
热机效率受卡诺(Carnot)循环限制,而燃料电池的效率不受卡诺循环限制。
20世纪初,人们就期望将化石燃料的化学能直接转变为电能。
一些杰出的物理化学家,如能斯特(Nernst)、哈伯(Harber)等,对直接碳—氧燃料电池做了许多努力,但他们的研究受到当时材料技术水平的限制。
1920年以后,由于在低温材料性能研究方面的成功,对气体扩散电极的研究重新开始。
1933年,鲍尔(Baur)设想一种电化学系统:在室温下,用碱性电解质,以氢为燃料。
英国人培根(F·Bacon)对包括多孔电极在内的碱式电极系统进行了研究。
20世纪50年代,培根成功地开发了多孔镍电极,并制造了第一个千瓦级碱性燃料电池系统。
培根的研究成果是后来美国宇航局(NASA)阿波罗(Apollo)计划中燃料电池的基础。
1958年,布劳尔斯(Broers)改进了熔融碳酸盐燃料电池系统,并取得了较长的预期寿命。
由于空间竞赛,燃料电池在50、60年代得到了广泛关注。
1968年美国宇航局完成了阿波罗登月计划。
此后对燃料电池的研究热了起来。
低催化剂载量的多孔碳基材料降低了陆地上使用的氢—空气燃料电池的成本,使人们开始热衷于电动机动车的研制。
1970年,考尔迪什(K.Kordesch)装配了以氢—空气碱性燃料电池为动力的4座位轿车,并实际运行了3年。
因为宇航项目数量上的减少,燃料电池的研究开发经历了短时期的低潮。
由于70年代初的石油危机,燃料电池的研究开发出现了新的浪潮,研究项目逐年增多,并且注重能源利用率及环境影响。
到了70年代中期,燃料电池技术的发展有了新动向。
已在空间应用方面达到最高水平的碱性燃料电池,逐步被磷酸燃料电池的广泛研究开发所取代,因为磷酸燃料电池更适用于燃料电池发电站。
与此同时,由于碳氢化合物是首选燃料,还必须开发重整技术。
磷酸燃料电池的功率已达到兆瓦级,寿命也已达到实用要求。
由于在电能和热能方面的高效率,80年代熔融碳酸盐和90年代固体氧化物燃料电池都得到了快速发展。
但寿命仍然是高温燃料电池必须解决的难题。
燃料电池在90年代最大的突破是质子交换膜燃料电池的发展。
质子交换膜燃料电池虽然早在60年代就已出现,却未被用到空间技术上,对其重视程度也不及碱性燃料电池。
随着对新型膜和催化剂的不断研究,已研制出了具有高功率密度的膜。
从历史上看,燃料电池技术的发展未能竞争过快速发展的燃烧发电技术,是因为燃料电池发展过程中相应的结构材料的发展是分阶段、时断时续进行的,未能使人们清楚地认识到对燃料电池的需求,而只醉心于使用廉价的化石燃料,大力开发火力发电技术,而中止了燃料电池的研究开发。
目前,燃料电池必须解决的问题是提高电池寿命、降低昂贵的膜及排热、排水等辅助系统的价格。
10—1—2 燃料电池的特性18210—1—2—1 燃料电池的优点燃料电池之所以受世人瞩目,是因为它具有其它能量发生装置不可比拟的优越性,主要表现在效率、安全性、可靠性、清洁度、良好的操作性能、灵活性及未来发展潜力等方面。
1.高效率从理论上讲,燃料电池可将燃料能量的90%转化为可利用的电和热。
磷酸燃料电池设计发电效率(HHV)42%,目前接近46%。
据估计,熔融碳酸盐燃料电池的发电效率可超过60%,固体氧化物燃料电池的效率更高。
这样的高效率是史无前例的。
而且,燃料电池的效率与其规模无关,因而在保持高燃料效率时,燃料电池可在其半额定功率下运行。
燃料电池发电厂可设在用户附近,这样也可大大减少传输费用及传输损失。
燃料电池的另一特点是在其发电的同时可产生热水及蒸汽。
其电热输出比约为1.0,而汽轮机为0.5。
这表明在相同电负荷下,燃料电池的热载为燃烧发电机的2倍。
2.可靠性与燃烧涡轮机循环系统或内燃机相比,燃料电池的转动部件很少,因而系统更加安全可靠。
燃料电池从未发生过像燃烧涡轮机或内燃机因转动部件失灵而发生恶性事故。
燃料电池系统发生的惟一事故就是效率降低。
3.良好的环境效益当今世界的环境问题已到了威胁人类生存和发展的程度,这并非危言耸听。
据统计,本世纪经历了两次世界大战,但因环境污染造成的死亡人数却超过了战争的死亡人数。
而环境污染的发生,多数是由于燃料的使用,尤其大气污染物绝大多数来自于各种燃料的燃烧过程。
因此,解决环境问题的关键是要从根本上解决能源结构问题,研究开发清洁能源技术。
而燃料电池正是符合这一环境需求的高效洁净能源。
普通火力发电厂排放的废弃物有颗粒物(粉尘)、硫氧化物(SO2)、氮氧化物(NO x)、碳氢化合物(HC)以及废水、废渣等。
燃料电池发电厂排放的气体污染物仅为最严格的环境标准的十分之一,温室气体CO2的排放量也远小于火力发电厂。
燃料电池中燃料的电化学反应副产物是水,其量极少,与大型蒸汽机发电厂所用大量的冷却水相比,明显少得多。
燃料电池排放的废水不仅量少,而且比一般火力发电厂排放的废水清洁得多。
因而,燃料电池不仅消除或减少了水污染问题,也无需设置废气控制系统。
由于没有像火力发电厂那样的噪声源,燃料电池发电厂的工作环境非常安静。
又由于不产生大量废弃物(如废水、废气、废渣),燃料电池发电厂的占地面积也少。
燃料电池是各种能量转换装置中危险性最小的。
这是因为它的规模小,无燃烧循环系统,污染物排放量极少。
燃料电池的环境友好性是使其具有极强生命力和长远发展潜力的主要原因。
4.良好的操作性能燃料电池具有其它技术无可比拟的优良的操作性能,这也节省了运行费用。
动态操作性能包括对负荷的响应性、发电参数的可调性、突发性停电时的快速响应能力、线电压分布及质量控制。
燃料电池发电厂的电力控制系统可以分别独立地控制有效电力和无效电力。
控制了发电参数,就可以使线电压及频率的输送损失最小化,并减少储备电量及电容、变压器等辅助设备的数量。
通常,电厂增加发电容量时,变电所的设备必须升级,否则会使整个电力系统的安全稳定性降低。
而燃料电池发电厂则不必将变电所设备升级,必要时可将燃料电池组拆分使用。
1835.灵活性灵活性是指发电厂计划与容量调节的灵活性。
这对电力公司及用户来说是最关键的因素及经济利益所在。
燃料电池发电厂可在2年内建成投产,其效率与其规模无关,可根据用户需求而增减发电容量。
6.发展潜力燃料电池在效率上的突破,使其可与所有的传统发电技术竞争。
作为正在发展中的技术,磷酸燃料电池已有了令人鼓舞的进展。
熔融碳酸盐燃料电池和固体氧化物燃料电池,将在未来15~20年内产生飞跃性进步。
相比之下,其它传统的发电技术,如汽轮机、内燃机等,由于价格、污染等问题,其发展似乎走到了尽头。
10—1—2—2 燃料电池存在的问题燃料电池有许多优点,人们对其将成为未来主要能源持肯定态度。
但就目前来看,燃料电池仍有很多不足之处,使其尚不能进入大规模的商业化应用。
主要归纳为以下几个方面:(1)市场价格昂贵;(2) 高温时寿命及稳定性不理想;(3) 燃料电池技术不够普及;(4) 没有完善的燃料供应体系。
10—1—3 燃料电池的分类燃料电池按照不同的分类标准,有不同的名称。
如以工作温度来划分,有低温、中温、高温和超高温燃料电池。
但目前最常用的方法还是以燃料电池中最重要的组成部分即电解质来划分。
电解质的类型决定了燃料电池的工作温度、电极上所采用的催化剂以及发生反应的化学物质。
按电解质划分,燃料电池大致可分为五类:碱性燃料电池(Alkaline Fuel Cell、缩写AFC)、磷酸型燃料电池(Phosphorous Acid Fuel Cell、缩写PAFC)、固体氧化物燃料电池(Solid Oxide Fuel Cell 、缩写SOFC)、熔融碳酸盐燃料电池(Molten Carbonate Fuel Cell 、缩写MCFC)和质子交换膜燃料电池(Proton Exchange Membrane Fuel Cell 、缩写PEMFC)。
下表列出了上述五种燃料电池的主要特点。
表10—1 主要燃料电池及其特性18418510—2 各类燃料电池10—2—1 碱性燃料电池碱性燃料电池(AFC )是以KOH 水溶液为电解质的燃料电池。
KOH 水溶液的质量分数一般为30% ~ 45%,最高可达85%。
在碱性电解质中,氧化还原比在酸性电解质中容易。
由于电解质是循环使用,AFC 电池堆多为单极结构(PAFC 和MCFC 的电解质是固定的,电池堆为双结构)。
在无CO 、CO 2时,阳极氧化反应为:2H 2 + 4OH - ——→ 4 H 2O + 4e阴极上氧的还原反应为:O 2 + 2H 2O + 4e ——→ 4 OH -电池反应为:2H 2 + O 2 ——→ 4 H 2O + 电能 + 热10—2—2 磷酸燃料电池磷酸燃料电池(PAFC )是以磷酸为电解质的燃料电池。
阳极通以富氢并含有CO 2的重整气体,阴极通以空气,对CO 2的承受力是PAFC 的特征之一。
