PCR检测记录表
PCR检测记录表

PCR检测记录表XXX FormXXX Date:XXX:XXX File Name:ns:1.Strictly follow the single n of the experiment。
that is。
reagent n area (Zone 1) → sample processing area (Zone 2) → n analysis area (Zone 3)。
and reverse n is strictly prohibited。
The flow of this record form also follows this process;2.Check the corresponding box before each project is executed;3.XXX 15-30℃;4.After the experiment。
refer to the "PCR Laboratory XXX and move the UV lamp the day after the experiment;5.After the experiment。
record the test results of the samples in the sample record book for future reference。
This record form is saved in the archive folder and stored in the laboratory file。
for 2 years;6.XXX are stored in the corresponding experiment date folder in the D drive。
For example。
the results of April 2004 are saved in "D:\2004\04\"。
XXX院检验科PCR实验室图表(30项)

XXXXX院检验科PCR实验室图表实验室主要负责人简历表表格编号:PCR-TAB-01实验室工作人员基本信息一览表表格编号:PCR-TAB-025XXX院检验科PCR实验室仪器设备一览表表格编号:PCR-TAB-03XXX院检验科临床PCR检验流程表表格编号:PCR-TAB-04 检验日期:检验项目:扩增仪中保存文件名:使用说明:1.本记录表需严格遵循(①试剂准备区②样本处理区③扩增及产物分析区)单一流向移动,严禁逆向移动。
2.各项工作执行后,在相应叙述签的“□”内打“√”。
XXX院检验科PCR室人员培训计划及培训记录表表格编号:PCR-TAB-058XXX院检验科PCR室仪器设备维修登记表表格编号:PCR-TAB-06XXX院检验科PCR实验室清洁消毒记录表表格编号:PCR-TAB-07XXX院检验科PCR实验室清洁消毒记录表表格编号:PCR-TAB-07注:如用10%次氯酸钠溶液、75%乙醇消毒、紫外线消毒,则在相应栏下打“√”XXX院检验科PCR实验室清洁消毒记录表表格编号:PCR-TAB-07注:如用10%次氯酸钠溶液、75%乙醇消毒、紫外线消毒,则在相应栏下打“√”XXX院检验科PCR室内温湿度记录表年月(1、2、3)区表格编号:PCR-TAB-08XXX院归档记录控制清单年表格编号:PCR-TAB-09XXX院消耗品进购记录表表格编号:PCR-TAB-10表格编号:PCR-TAB-11表格编号:PCR-TAB-12XXX院检验科PCR实验室试剂盒接收质检记录表表格编号:PCR-TAB-13检验者:审核者:说明:试剂接收外包装箱及试剂盒是否完整,完整请打“√”,如不完整,请联系供货商。
XXX院检验科PCR室室内质量控制失控报告表格编号:PCR-TAB-14XXX院检验科PCR实验室室间质评表表格编号:PCR-TAB-15表格编号:PCR-TAB-17XXX院检验科PCR实验室报告延迟处理记录表表格编号:PCR-TAB-18XXX院检验科PCR实验室标本接收及处理意见登记表表格编号:PCR-TAB-1922XXX院设备定期检定校准及核查记录表表格编号:PCR-TAB-20XXX院检验科PCR实验室仪器设备履历表表格编号:PCR-TAB-21XXX院检验科PCR实验室试剂报废申请表科室:表格编号:PCR-TAB-22XXX院检验科PCR实验室试剂报废申请表科室:表格编号:PCR-TAB-22XXX院检验科PCR实验室意外事件报告表格编号:PCR-TAB-23XXX院检验科PCR实验室意外事件报告表格编号:PCR-TAB-23XXX院检验科PCR实验室扩增仪使用维护记录年月表格编号:PCR-TAB-24XXX院检验科PCR实验室生物安全柜使用维护记录年月表格编号:PCR-TAB-25XXX院检验科离心机使用维护记录表年月型号:表格编号:PCR-TAB-26XXX院检验科PCR室传递窗使用维护记录年月表格编号:PCR-TAB-27XXX院检验科冰箱使用维护记录表年月(1、2、3)区表格编号:PCR-TAB-28XXX院检验科PCR实验室平面结构示意图编号:附图1XXX院检验科PCR实验室室内质控图编号:附图2。
PCR实验室SOP文件

前言我院是一所综合性三级医院。
近年来,随着临床医学的不断进步,检验医学也得到了迅猛的发展。
检验科为了更好的满足临床诊断的需求,根据卫生部临检中心制定的《临床基因扩增检验实验室管理暂行办法》(卫医发[2002]10号)、《临床基因扩增检验实验室工作规范》(卫检字2002第8号)文件,设立了临床基因扩增检验实验室,并于2009年6月着手编写实验室质量管理程序文件。
经过试运行,反复讨论和修改第一版已定稿。
从即日起开始实施。
1.质量方针本实验室的质量方针是:准确、及时、可靠。
2.质量目标全面贯彻质量方针,建立科学、合理的实验室质量管理体系,严格按照程序规定做好检验工作,不段提高自身素质和技术水平,为临床和患者提供准确、可靠的诊断依据。
1.目的:文件管理有序和便于资料的查用2.范围:本质量管理手册及实验室相关资料3.负责人:王宇飞4.规章4.1本质量管理手册分正副本,正本由主任保管于主任办公室;副本由实验室负责人保管于实验室;4.2本质量管理手册有电子文档,备有一份软盘,由主任保管;4.3本质量管理手册不能外借,不能复印,不能抄写,只能在本室阅读;4.4临床基因扩增实验室的每区有相应的质量管理文件副本,由实验室工作人员保管;4.5本实验室的相关资料由实验室工作人员填写,保管于相关实验室,超过一年的资料由主任保管。
4.6实验原始数据电子文档每天保存于电脑中,一年的电子文档备于光盘中,保存五年;病人原始送检单及原始资料记录本保存两年;其它实验室的记录保存两年,超过保存期可按实际情况处理。
1.目的:保证实验室工作规范而有序的进行2.范围:检验科临床基因扩增实验室3.负责人: 王宇飞4.内容:4.1基因扩增检验实验室是检验科下设的,采用实时荧光定量PCR技术对临床标本进行基因扩增诊断的专业实验室。
本实验室按《临床基因扩增检验实验室管理暂行办法》(卫医发[2002]10号)中临床基因扩增检验实验室基本设备标准结合本科实验室的条件进行配置、装修。
26!检验科PCR实验室试剂质检记录表

26!检验科PCR实验室试剂质检记录表试剂质检记录表文件编号:SYZY-PCR-BG-01版生效日期:部门:基因扩增实验室验收人:验收时间:试剂名称批号有效期规格数量1 检查试剂是否处于冻存状态:是□ 否□2 核对试剂的品种和数量:无误□ 有误□3 核对完后及时转入-18℃以下的冰箱保存:是□ 否□4 在上批试剂存量尚可维持一周时对新批号试剂进行校验实验:是□ 否□5 校验实验设置:空白对照,阴性对照,阳性对照各一;新旧试剂的对比实验同时做5个标本(选择1个阴性,2个弱阳性,2个强阳性标本)6 实验结果。
日期序号空白对照阴性对照阳性对照标本1 标本2 标本3 标本4 标本5项目校验实验采用旧批次试剂结果原始结果对比结果采用新批次试剂结果原始结果对比结果新试剂批号7 80%的测量结果相符是□ 否□8 批间有无差异:有□ 无□9 最终判断试剂是否合格:合格□ 不合格□质检结论:本批次试剂:符合质检要求□ 不符合质检要求□XXX的基因扩增实验室使用PCR室作业指导书中的试剂质检记录表。
在收到试剂后,首先要测试试剂是否处于冻存状态。
然后,核对试剂的品种和数量,核对无误后及时转入-18℃以下的冰箱保存。
在上批试剂存量尚可维持一周时,对新批号试剂进行校验实验。
校验实验设置包括空白对照、阴性对照和阳性对照各一,同时做新旧试剂的对比实验,选择1个阴性、2个弱阳性和2个强阳性标本。
实验结果需要记录在试剂质检记录表中,包括采用旧批次试剂结果、原始结果对比结果、采用新批次试剂结果和原始结果对比结果。
最终判断试剂是否合格,如果合格则标记在试剂质检记录表上。
从零开始,PCR实验室建立:PCR实验室各区表格(示例)

因文件模板不能混合上传,请大家分开下载,并根据实际情况修改使用。
总文件包括1、PCR室实验室制度,2、PCR实验质量管理程序文件,3、PCR实验SOP(示例),4、各区(样本接收区、试剂准备区、标本处理区,核酸扩增区)各区表格,5、实验室申报文件(示例)。
目录样本接收区 (3)试剂准备区 (21)样本处理区 (43)核酸扩增区 (62)样本接收区附表3、基因实验室主要仪器设备一览表PCR扩增接收标本记录表20 年月PCR扩增拒收标本记录表20 年月PCR实验室工作人员一览表PCR实验室人员培训计划及培训记录表(20 年度)PCR实验室设备校正记录表PCR实验室冰箱温度记录表****人民医院抱怨处理登记本PCR实验室抱怨记录表20 年月****人民医院PCR室垃圾处理登记表注:运送者必须将各种垃圾分理后,按垃圾规定地点放置,决不能随意丢弃。
****人民医院PCR检验实验室人员进出登记本年月仪器运行记录表20 年 月 区试剂验收记录表试剂名称:生产厂家:生产批号:使用有效期:空白对照:阴性对照:104质控品CT值:104阳性标准品CT值:105阳性标准品CT值:106阳性标准品CT值:107阳性标准品CT值:斜率:截距:相关性:验收结果:验收意见:验收人:验收时间:消耗品验收记录表耗材名称:生产厂家:生产批号:验收方法:验收结果:验收意见:验收人:验收时间:试剂准备区PCR实验室湿度、湿度记录表20 年月区PCR实验室移动紫外灯使用记录表20 年月区PCR实验室紫外灯使用记录表20 年月区PCR实验室设备校正记录表基因实验室冰箱温度记录表****人民医院PCR室垃圾处理登记表注:运送者必须将各种垃圾分理后,按垃圾规定地点放置,决不能随意丢弃。
****人民医院基因扩增检验实验室操作流程卡年月日操作人:数据处理:斜率:截距:相关系数:阳性标准品:1e7 Ct: 1e6 Ct: 1e5 Ct: 1e4 Ct:阳性质控:Ct:阴性质控:Ct:质控结果:失控原因分析及处理:****人民医院基因扩增检验实验室人员进出登记本年月仪器状态记录表20 年月区试剂使用记录表20 年月****人民医院基因扩增检验实验室清洁消毒记录卡实验区域:仪器设备维护保养登记本应急处理记录表发生时间:发生事件:报告人:应急处理方法:处理结果:处理人:处理时间:样本处理区PCR扩增标本保存记录表实验室负责人:20 年月PCR实验室湿度、湿度记录表20 年月区基因实验室移动紫外灯使用记录表20 年月区基因实验室紫外灯使用记录表20 年月区PCR实验室设备校正记录表PCR实验室冰箱温度记录表。
生物实验仪器检测报告模板

生物实验仪器检测报告模板1. 实验目的在本次实验中,我们使用生物实验仪器对特定生物样本进行检测,旨在验证仪器的准确性和可靠性。
2. 实验介绍生物实验仪器是一种用来检测和分析生物样本的设备。
它包括了各种仪器,如显微镜、离心机、光谱仪、PCR仪等。
这些仪器在生物研究和临床实验室中广泛应用,提供了精确和可靠的数据支持。
3. 实验材料与方法3.1 实验材料- 生物样本:使用xxx提供的xxx样本。
- 生物实验仪器:本次实验中使用了xxx仪器。
3.2 实验方法1. 按照仪器操作手册的指引,对仪器进行正确操作和设置,确保仪器处于适宜的工作状态。
2. 准备待测生物样本,按照仪器要求进行处理和处理,以确保样本的准确性和稳定性。
3. 将样本放入仪器中,启动实验流程,并根据仪器的提示进行操作。
4. 操作完成后,检查实验结果并记录所得数据。
4. 实验结果与分析实验结果如下表所示:样本编号检测项目1值检测项目2值检测项目3值1 xx xx xx2 xx xx xx3 xx xx xx根据实验结果分析,我们可以得出以下结论:1. 检测项目1值:样本1与样本2在检测项目1方面存在显著差异,而样本3与样本1、2相比差异不显著。
2. 检测项目2值:样本3的检测项目2值明显高于样本1和2,可推断样本3在该指标上存在异常。
3. 检测项目3值:样本2与样本3的差异最大,表明样本2的检测项目3值较高。
5. 结果讨论与建议根据实验结果分析,我们可以得出以下讨论与建议:1. 检测项目1值的差异可能是由于样本来源、处理方法等因素导致的,可以进一步分析原因,以确保实验结果的准确性。
2. 检测项目2值的异常可能表明样本3存在某种疾病变化,可以进一步对样本进行更深入的检测和分析。
3. 检测项目3值的差异可能与样本的生长环境、品种等因素有关,可以尝试不同条件下的比较实验,以确定影响因素。
6. 结论通过本次实验,我们验证了生物实验仪器的准确性和可靠性。
PCR检测记录表

基因扩增荧光定量检测记录表
实验日期:检测项目:Linegene保存文件名:
使用说明
1、严格按单一流向进行实验,即试剂准备区(1区)→样本处理区(2区)→扩增分析区(3区),严禁逆向。
本记录表的流向亦遵循此流程;
2、各项目执行后在相应项目前的方框内打√;
3、实验室内温度为15~30℃为合格范围;
4、实验后对实验室的清洁与消毒方法参见“PCR实验室清洁程序”,实验后次日关闭通风设备和移动紫外灯;
5、实验结束后,将标本的检测结果登记至标本记录本上以备查询。
本记录表保存在归档文件夹中,存放在实验室文件柜中,保存2年;
6、Linegene扩增仪中结果保存于D盘对应实验日期的文件夹中,如2004年4月的结果保存于“D:\2004\04\”中,每月底将当月资料备份于软盘中,保存2年。
DP316-全血DNA提取及检测实验记录-Tiangen-模板

微量样品基因组提取及检测实验记录-TIANGEN DP316 实验日期:注意:此实验必须在PCR前区的DNA提取室进行操作,在进入洁净区之前做好以下准备工作。
1. □核对全血样本的标记,填写如下样本信息记录表。
2. 填写此表中DNA提取试剂盒及所用关键试剂的相关资料:3. □检查所需实验仪器设备的功能是否良好和所需器材是否齐备。
4. □ 检查所需试剂是否合格。
提取操作步骤:1. □从4℃冰箱中取出全血样本,准备EP管,并做上相对应的标记编号。
2. □ 取200μL全血,转移至相应标记的EP管中。
3. □加入20μL的Proteinase K溶液。
4. □每管加200μL的缓冲液GB,充分颠倒混匀。
5. □56℃温浴10min,并不时轻摇样品。
6. □加入200μL预冷的乙醇(96%-100%),室温放置3min,短暂离心除去内壁的液滴。
7. □将上一步所得溶液和絮状沉淀都加入吸附柱CB3中(吸附柱CB3放入收集管中),12000 rpm离心30sec,倒掉收集管中的废液,将吸附柱CB3放入收集管中。
8. □向吸附柱CB3中加入500μL缓冲液GD(使用前请先检查是否已加入无水乙醇),12000 rpm离心30sec,倒掉收集管中的废液,将吸附柱CB3放入收集管中。
9. □向吸附柱CB3中加入600μL漂洗液PW(使用前请先检查是否已加入无水乙醇),12000 rpm离心30sec,倒掉收集管中的废液,将吸附柱CB3放入收集管中。
10. □重复操作步骤9。
11. □将吸附柱CB3放回收集管中,12000 rpm离心2min,倒掉废液。
将吸附柱CB3置于室温放置数分钟,以彻底晾干吸附柱材料中残余的漂洗液。
12. □将吸附柱CB3转入1.5mL离心管中,向吸附膜中间位置垂直悬空滴加()洗脱液,室温放置2-5分钟,12000 rpm离心2min,将溶液收集到离心管中。
操作者签字:特殊情况说明:检测操作步骤:2.1 □吸取1.2μL去离子水(Deionized water)至样本探测头上,轻轻合拢两端探测头,使探测头中间依靠去离子水(Deionized water)相连接,按“Blank”键,进行清零操作。
非洲猪瘟测定原始记录表
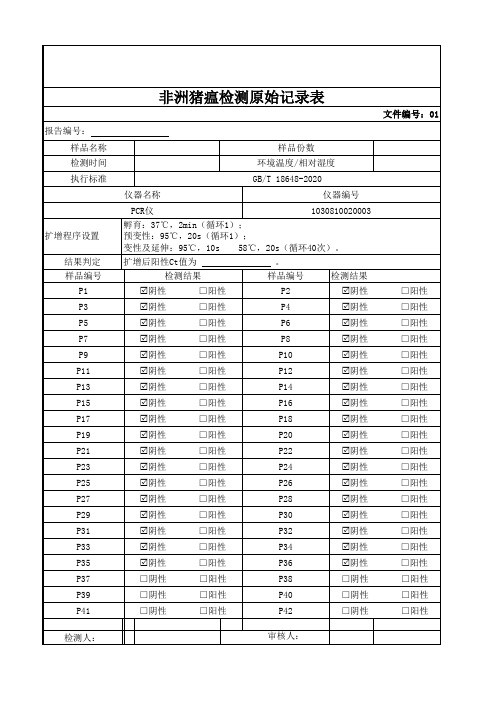
仪器名称
仪器编号
PCR仪
1030810020003
孵育:37℃,2min(循环1); 预变性:95℃,20s(循环1); 变性及延伸:95℃,10s 58℃,20s(循环40次)。
扩增后阳性Ct值为
。
检测结果
样品编号
检测结果
R阴性
□阳性
P2
R阴性
R阴性
□阳性
P4
R阴性
R阴性
□阳性
P6
R阴性
R阴性
□阳性
P8
R阴性
R阴性 R阴性 R阴性 R阴性 R阴性
□阳性 □阳性 □阳性 □阳性 □阳性
P10
R阴性
P12
R阴性
P14
R阴性
P1阴性
□阳性 □阳性 □阳性 □阳性
P20
R阴性
P22
R阴性
P24
R阴性
P26
R阴性
R阴性
□阳性
P28
R阴性
R阴性 R阴性 R阴性 R阴性
报告编号: 样品名称 检测时间 执行标准
扩增程序设置
结果判定 样品编号
P1 P3 P5 P7 P9 P11 P13 P15 P17 P19 P21 P23 P25 P27 P29 P31 P33 P35 P37 P39 P41
非洲猪瘟检测原始记录表
。
样品份数 环境温度/相对湿度
GB/T 18648-2020
□阳性 □阳性 □阳性 □阳性
P30
R阴性
P32
R阴性
P34
R阴性
P36
R阴性
□阴性
□阳性
P38
□阴性
□阴性
□阳性
检验科外送项目定期评估记录表
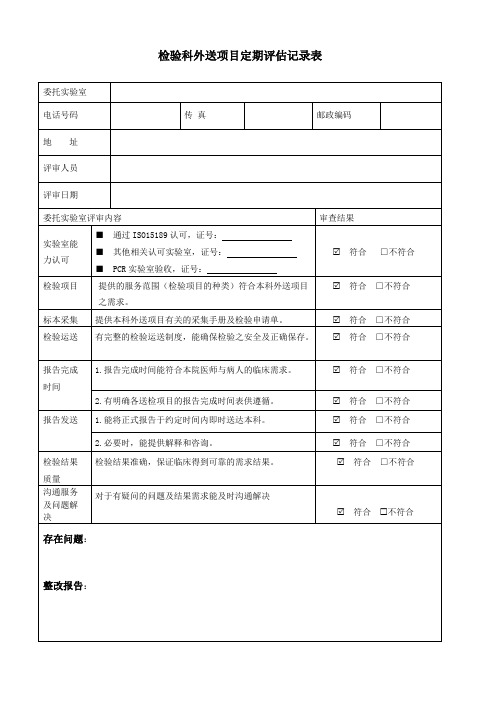
符合 □不符合
之需求。
标本采集 提供本科外送项目有关的采集手册及检验申请单。
符合 □不符合
检验运送 有完整的检验运送制度,能确保检验之安全及正确保存。 符合 □不符合
报告完成 时间
报告发送
1.报告完成时间能符合本院医师与病人的临床需求。
2.有明确各送检项目的报告完成时间表供遵循。 1.能将正式报告于约定时间内即时送达本科。
检验结果
质量 沟通服务 及问题解 决
2.必要时,能提供解释和咨询。 检验结果准确,保证临床得到可靠的需求结果。
对于有疑问的问题及结果需求能及时沟通解决
存在问题:
符合 □不符合 符合 □不符合 符合 □不符合 符合 □不符合 符合 □不符合
符合定期评估记录表
委托实验室 电话号码
传真
邮政编码
地址
评审人员
评审日期
委托实验室评审内容
审查结果
实验室能 力认可
■ 通过 ISO15189 认可,证号: ■ 其他相关认可实验室,证号: ■ PCR 实验室验收,证号:
符合 □不符合
检验项目 提供的服务范围(检验项目的种类)符合本科外送项目
PCR实验记录表

PCR实验记录表PCR实验室检验流程表检验日期:检验项目:确认试剂在有效期内。
确认生物安全柜的滤膜在使用有效期内。
确认离心管、带滤芯吸头已经经过质检合格。
实验前准备:打开通风设备。
确认扩增仪、加样器和温度计在校准的有效期内。
确认消毒溶液在有效期内。
操作者:试剂准备区(1区):实验台面清洁,用水或70%酒精擦拭。
冷冻室(-18℃±2℃)温度为:____℃,相对湿度允许范围为30%~70%。
冰箱温度:冷藏室(2~8℃)为:____℃。
实验室温度为:____℃,允许范围为10~30℃。
确认PCR试剂来源及本次试验用量。
实验后:清洁实验室台面、地面、加样器,并进行紫外线照射30分钟以上。
处理实验废弃物。
操作者:检验日期:标本制备区(2区):打开通风设备。
实验台面清洁,用水或70%酒精擦拭。
冰箱温度:冷藏室(2~8℃)为:____℃,冷冻室(-18℃±2℃)为:____℃。
实验室温度为:____℃,允许范围为10~30℃,相对湿度允许范围为30%~70%。
确认阳性室内质控物来源、浓度及批号,以及扩增位置。
确认阴性室内质控物来源、批号及扩增位置。
确认所提取的标本(对应标本接收的唯一编号)及拟扩增位置。
核酸提取及加样过程:按sop进行。
仪器设备使用:确认生物安全柜正常并使用。
确认恒温仪温度校准正常。
确认离心机正常并使用。
确认振荡器正常并使用。
试验后:清洁实验室台面、地面及仪器设备。
处理实验室废弃物。
操作者:。
PCR检测记录表

基因扩增荧光定量检测记载表
试验日期:检测项目:Linegene 保管文件名:
应用解释:
1.严厉按单一流向进行试验,即试剂预备区(1区)→样本处理区(2区)→扩增剖析区(3区),严禁逆向.本记载表的流向亦遵守此流程;
2.各项目履行后在响应项今朝的方框内打√;
3.试验室内温度为15~30℃为及格规模;
4.试验后对试验室的干净与消毒办法拜见“PCR试验室干净程序”,试验后次日封闭通风装备和移动紫外灯;
5.试验停止后,将标本的检测成果登记至标本记载本上以备查询.本记载表保管在归档文件夹中,存放在试验室文件柜中,保管2年;
6.Linegene 扩增仪中成果保管于D盘对应试验日期的文件夹中,如2004年4。
HPV分型核酸扩增 (2)

HPV分型核酸扩增标准操作规程
1.目的
规范HPV 分型的PCR 扩增操作,减少实验误差。
2.范围
使用Mx3000P扩增仪进行HPV 分型检测的核酸扩增。
3.操作人员
PCR室在岗工作人员。
4. 操作步骤
4.1 PCR 扩增
4.1.1 PCR 扩增前准备:先打开电脑,将Mx3000P电源开关打开,
4.1.2打开电脑上的Mx PRO控制软件,在里,选择需要的样本孔,在Well type中设定Standard(标准品)、NTC(阴性对照)、NPC(阳性对照)、unkown(样品);双击所选孔,自动跳出Well Information窗口,在Name框中输入样本号,在Comments 框中输入HPV,点击就能显示样品编号,编号结束选中样本孔,使之呈现浅蓝色,选择荧光通道FAM。
4.1.3 打开扩增程序:点击,点击版面右上方的,点击我的电脑,打开D盘,双击date,选择最近所做的同批号试剂的文件,打开,核对扩增程序。
4.1.3.1 HPV23分型扩增程序为:
[50℃ 3分钟,94℃ 5分钟;(94℃ 40秒→55℃ 40秒→72℃ 40秒)×40个循环;72℃ 7分钟 ];[95℃ 5分钟,4℃ 5分钟]*
*注意!下划线程序为PCR产物变性程序,程序结束后,PCR产物需要立即放于冰上用于杂交,如不及时杂交,在杂交前需要将PCR产物放入PCR仪再补充这个程序。
4.1.4 文件保存:点击界面左上角保存按钮,文件保存在D:\date中,文件名:HPV+当天日期。
4.1.5 把待测HPV23PCR反应管按照样本孔编号位置放入加热模块,核对无误后再将热盖盖紧,拉下PCR仪前方的盖子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
基因扩增荧光定量检测记录表
实验日期:检测项目:Linegene 保存文件名:
使用说明
1、严格按单一流向进行实验,即试剂准备区(1区)→样本处理区(2区)→扩增分析区(3区),严禁逆向。
本记录表的流向亦遵循此流程;
2、各项目执行后在相应项目前的方框内打√;
3、实验室内温度为15~30℃为合格范围;
4、实验后对实验室的清洁与消毒方法参见“PCR实验室清洁程序”,实验后次日关闭通风设备和移动紫外灯;
5、实验结束后,将标本的检测结果登记至标本记录本上以备查询。
本记录表保存在归档文件夹中,存放在实验室文件柜中,保存2年;
6、Linegene 扩增仪中结果保存于D盘对应实验日期的文件夹中,如2004年4月的结果保存于“D:\2004\04\”中,每月底将当月资料备份于软盘中,保存2年。
如有侵权请联系告知删除,感谢你们的配合!如有侵权请联系告知删除,感谢你们的配合!。
