重排反应整理 PPT
合集下载
2有机化学中的重排反应(上课使用)总结精品PPT课件

R C O NR N C O H 2 O R 2 NH
氮烯
异氰酸酯
氮转移一对电子与羰基成 键的时刻氮上缺电子。 紧接着R带着一对电子填补上来。
⑴霍夫曼(Hofmann)重排
酰胺与溴和碱的水溶液作用,放出CO2, 生成少一个碳 原子的胺, 称为霍夫曼重排(降解).
RCONH2 + Br2 + NaOH
RCOCHN2 + HCl
-重氮甲酮
⑵.阿恩特-埃斯特尔特(Arudt-Eistert) 反应
即,从羧酸经重氮甲酮生成高一级羧酸的方法。 (其中包含了Wolff重排。)
4. 缺电子氮重排(C→N)
• R-N:氮烯(乃春Nitrene)与卡宾类似,只是以N原子代换C原子。
可由叠氮分解得到,也可由N-卤代酰胺经-消去HX得到。 • N 原子参加的缺电子重排的基本模式:
1899 年,Baeyer 和Villiger 首次报道了利用过硫酸作氧化剂能 将环酮(如薄荷酮、香芹酮(樟脑)转化成相应的内酯,这就是 历史上最早的Baeyer-Villiger 氧化反应。现在Baeyer-Villiger 氧 化反应已成为酮或环酮转化成酯或内酯的统称。
常用的过氧酸有:H2SO5、MeCO3H、PhCO3H、HCO3H和 CF3CO3H等。现在文献报道的Baeyer-Villiger 氧化反应大多用 双氧水作为氧化剂,因双氧水还原后生成清洁的水,尽管双氧 水具有强腐蚀性,但用双氧水的拜尔-维立格反应仍不失为一 种既安全又符合现代社会绿色环保要求的好方法。
C H 3
H
H
P hC C O T s△H 3 C C C P h
C H 3 C H 3
C H 3 C H 3
苯的迁移速度为甲基的3000倍
药物合成反应 第六章 重排反应

OO Ar C C OH 慢
Ar
OO Ar C C OH
Ar
OH O Ar C C O
Ar
第二节 重排反应及其在药物 合成中的应用
2. 影响因素及反应条件 (1)底物的影响—α-二酮的结构
芳香族α-二酮的重排方向,主要受取代基的种类 和在芳环上的位置的影响。芳环的对位或间位有吸电 子基时,使反应易于进行;反之,对位或间位有给电 子基时,使重排反应速度减慢;当取代基位于芳环邻 位时,均使重排反应速率减慢。
与史蒂文斯重排相似,在强碱的作用下,发生分子内的 亲电重排
第二节 重排反应及其在药物 合成中的应用
2. 影响因素及反应条件
(1)底物的影响—季铵盐的结构
最常用的是三甲胺的季铵盐 ,否则烃基上的氢原子在反应条件 下,会发生消除反应。
(2)溶剂和温度的影响
一般情况下,温度升高,有利于发生史蒂文斯重排;而选择极 性较大的溶剂,则有利于发生萨默莱特-豪斯重排。
第二节 重排反应及其在药物 合成中的应用
2.影响因素及反应条件
(4)温度的影响
反应温度会直接影响重排反应的收率,因此,在温 度的选择上,应对催化剂、溶剂、酮肟的结构及产物的 性质进行综合考虑
3. 应用
抗高血压药胍乙啶中间体庚内酰胺的合成:
O
H2NOH
,
1 2
H2SO4
75 80
NOH
O
H2SO4
110 140
O R C N3
-N2 R N C O
物。如
HO
O
N
O
NH2OH . HCl
N
H2SO4
第二节 重排反应及其在药物 合成中的应用
2. 影响因素及反应条件
重排反应

R O C C R'
H2O R'OH O C CH R NH3 R'NH2
RCH2COOH RCH2COOR' RCH2CONH2 RCH2CONHR'
阿恩特-埃斯特尔特(Arndt-Eistert)合成
R'COOH R'COX CH2N2 R'COCH=N2 H2O R'CH2COOH
制备多一个碳的羧酸
第六章
重排反应
Rearrangement Reaction
定义:受试剂或介质的影响,同一有机分子内的一个基团
或原子从一个原子迁移到另一个原子上,使分子构架发生 改变而形成一个新的分子的反应称为重排反应。
W A B A W B
A:重排起点原子,B:重排终点原子,W:重排基团
分类: 离子型机理(亲核重排,亲电重排) 自由基重排 周环机理重排(σ-键迁移重排)
4
AlCl3
Et2O
PhCH2NHPh
2、Hofmann重排
酰胺用溴(或氯)和碱处理转变为少一个碳原子的伯胺的 反应。又叫Hofmann降解反应。
O R C NH2
NaOX
机理:
O R C NH2
or X2/NaOH O Br2 R C NH Br -HBr
RNH2
OH O R C N Br
-Br
O EtO EtONa
Cl
CH2COOEt C 所连接的取代基越少越稳定
CH3 Br H3C C EtONa C CH3 Br H3C C C O CH2 EtO Br H3C O C C OEt H3C EtOOC C CH2 CH2 Br C CH2
COOEt
高等有机化学分子重排详解演示文稿

H
CH3CH2CH2CH2OH2 H2O
CH3CH2CHCH2 CH3CH2CHCH3 H+ CH3CH=CHCH3
富电子重排:
Ph CH2 O CH3
PhLi C6H6
Ph CH O CH3 Li+
Ph
CH3 CH O-Li+
H2O
CH3 Ph CH OH
第四页,共62页。
自由基重排:
Cl
Cl C CH=CH2 Br Cl
H2O
CH3C Cl
C
CH2
Cl O CH3C C OH-
CH2
Cl O-
CH3C C OH
CH2
CH3CC O NaOH CH2 OH
RO
R2 O Cl
RO
R1 C
R2 B
C
C
A
R3 R4
O OR
R3
R1 C
C R4
SN2
R2 C Cl
O
R1 C
C R3
R2 C R4
O
R1 R3
R1 R3
A
R2 C C.. R4 ROH R2 C CHR4
OC
OC
OR
OR
第三十四页,共62页。
R1 R3
R1 R3
B
R2 C.. C R4 CO
ROH
Et O
n-Bu C H
N H
C
CH3
C
N OH
NO2
PCl5
NO2
NC OH
第二十二页,共62页。
NO2
HN C O
H N OH
H2SO4
110 ℃
H
HO HN H
CH3CH2CH2CH2OH2 H2O
CH3CH2CHCH2 CH3CH2CHCH3 H+ CH3CH=CHCH3
富电子重排:
Ph CH2 O CH3
PhLi C6H6
Ph CH O CH3 Li+
Ph
CH3 CH O-Li+
H2O
CH3 Ph CH OH
第四页,共62页。
自由基重排:
Cl
Cl C CH=CH2 Br Cl
H2O
CH3C Cl
C
CH2
Cl O CH3C C OH-
CH2
Cl O-
CH3C C OH
CH2
CH3CC O NaOH CH2 OH
RO
R2 O Cl
RO
R1 C
R2 B
C
C
A
R3 R4
O OR
R3
R1 C
C R4
SN2
R2 C Cl
O
R1 C
C R3
R2 C R4
O
R1 R3
R1 R3
A
R2 C C.. R4 ROH R2 C CHR4
OC
OC
OR
OR
第三十四页,共62页。
R1 R3
R1 R3
B
R2 C.. C R4 CO
ROH
Et O
n-Bu C H
N H
C
CH3
C
N OH
NO2
PCl5
NO2
NC OH
第二十二页,共62页。
NO2
HN C O
H N OH
H2SO4
110 ℃
H
HO HN H
第二部分 第四章 重排反应

H+
H2O
CH3CH2CHCH2
CH3CH2CH+CH3
CH3CH=CHCH3
亲电重排: 亲电重排:
Ph CH2 O CH3 PhLi C6H6
Ph CH O CH3
Li+
CH3 - + H2O Ph CH O Li
自由基重排
Cl Cl C CH=CH2 Cl Br
CH3 Ph CH OH
Cl Cl C CH CH2Br Cl
本课程按照活泼中间体或机理进行分类讲解, 本课程按照活泼中间体或机理进行分类讲解, 着重介绍以下几类型反应: 着重介绍以下几类型反应: 1、经过正离子重排 、 2、经过负离子重排 、 3、经过卡宾Carbene 、氮宾 、经过卡宾 氮宾Nitrene重排 重排 4、σ-迁移反应(属于周环重排) 、 迁移反应 属于周环重排) 迁移反应(
H2O
R C N R' OH2
-H+
R C N R' OH
互变 异构
R C NH R' O
脱羟、重排、夺羟、 脱羟、重排、夺羟、互变
举例
Et 例 1 n-Bu C C Me H N OH
H2SO4 乙醚
Et O n-Bu C N C CH3 H H
例2 C N OH
NO2
PCl5
NO2 N C OH HN C O
NH2 HNO2 OH
CHO
试分析
CH2NH2 OH
HNO2
O
• 通常经过三元环碳正离子历程,迁移基团从离去基 通常经过三元环碳正离子历程, 三元环碳正离子历程 团背后迁移。 团背后迁移。
CH3 H ph NH2 OH HO Me NH2 H OCH3
H2O
CH3CH2CHCH2
CH3CH2CH+CH3
CH3CH=CHCH3
亲电重排: 亲电重排:
Ph CH2 O CH3 PhLi C6H6
Ph CH O CH3
Li+
CH3 - + H2O Ph CH O Li
自由基重排
Cl Cl C CH=CH2 Cl Br
CH3 Ph CH OH
Cl Cl C CH CH2Br Cl
本课程按照活泼中间体或机理进行分类讲解, 本课程按照活泼中间体或机理进行分类讲解, 着重介绍以下几类型反应: 着重介绍以下几类型反应: 1、经过正离子重排 、 2、经过负离子重排 、 3、经过卡宾Carbene 、氮宾 、经过卡宾 氮宾Nitrene重排 重排 4、σ-迁移反应(属于周环重排) 、 迁移反应 属于周环重排) 迁移反应(
H2O
R C N R' OH2
-H+
R C N R' OH
互变 异构
R C NH R' O
脱羟、重排、夺羟、 脱羟、重排、夺羟、互变
举例
Et 例 1 n-Bu C C Me H N OH
H2SO4 乙醚
Et O n-Bu C N C CH3 H H
例2 C N OH
NO2
PCl5
NO2 N C OH HN C O
NH2 HNO2 OH
CHO
试分析
CH2NH2 OH
HNO2
O
• 通常经过三元环碳正离子历程,迁移基团从离去基 通常经过三元环碳正离子历程, 三元环碳正离子历程 团背后迁移。 团背后迁移。
CH3 H ph NH2 OH HO Me NH2 H OCH3
《重排反应》PPT课件

P C H3OC 6H5 Ph
H 2S O 4
P C H3OC 6H5 C C Ph
OH OH
P C H3OC 6H5
P C H3OC 6H5 C C Ph Ph O
72%
+ Ph
P C H3OC 6H5 C C Ph
28%
O整理课件C 6 H 5 O C H 3 P
9
Ph Ph C
CH3 C CH3
第四章 重排反应
定义:受试剂或介质的影响,同一有机分子内的一个基团 或原子从一个原子迁移到另一个原子上,使分子构架发生 改变而形成一个新的分子的反应称为重排反应。
重排反应类型(按终点原子电荷分) 缺电子重排 富电子重排 自由基重排
• 从碳原子到碳原子的重排 • 从碳原子到杂原子的重排 • 从杂原子到碳原子的重排 • -键迁移重排
关注1,2重排 烯丙基结构 构型保留
R
碱B R
机理
YC H
BH
YC
R YC
整理课件
51
一、Stevens重排
季铵盐分子中连于氮原子的碳原子上具有吸电子的 基团取代时,在强碱性条件下,可重排生成叔胺的 反应称为Stevens重排反应。
RC H C O H2O RC H2C O O H
COCl
1. C H 2 N 2 2. P h C O O A g /E tO H /T E A
C H2C O O C 2H5
84~92%
整理课件
28
Arndt-Eistert同系列羧酸的合成反应
Arndt-Eistert合成是将一个酸变成它的高一级同系 物或转变成同系列酸的衍生物,(如酯或酰胺)的反 应。该反应可应用于脂肪族酸和芳香族酸的制备。
有机化学:第十五章 - 重排反应

5、弗里斯(Fries)重排--分子间重排
酚酯催化加热,酰基迁移到邻位或对位
O
O C CH3 AlCL3
OH COCH3
OH
heat
COCH3
25oC H3COC
OH
OOCCH3
H3C
H3C
165oC H3C
COCH3
OH
O OCR
+ AlCl3
AlCl3 O COR
Cl3Al O
+R C O
Cl3Al O
C6H5 > (CH3)3C >(CH3)2CH >C2H5 >CH3
H3CO
CC OH OH
H+
OCH3
1,2-二苯基-1,2-二(对甲氧基苯基)乙二醇
CC O
OCH3
OCH3
主要产物
分析
C6H5
C6H5 C6H5 C1 C2 CH3
OH OH
形成C+离子稳定性C1>C2 C2上取代基迁移苯基>甲基
O
(C6H5)3C C CH3
分析
H3C
CH3
CH CH3
H3C
C 1
C
2
CH2 CH3
OH OH
• 形成C+离子稳定性C1>C2 • C2上取代基迁移乙基>甲基
H3C
CH3
CH CH3
H3C C C O
C2H5
HO OH
(d)
R 羟基位于脂环上的连乙二醇
R
OH Ph
Ph
O Ph Ph
2、蒂芬欧-捷姆扬诺夫(Tiffeneau-Demjanov)重排
质子化
五章节重排反应
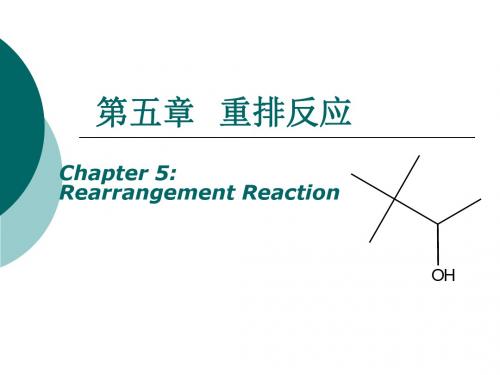
H2O(-H+)
R1 R2
OH C
R4 C R5 R3
第一节 从碳原子到碳原子的重排一Wangner-Meerwein重排
1 形成C+ 形式
(a)卤代烃 Ag+ AlCl3
(CH3)3C-CH2Cl
Ag (AgNO3) (CH3)3C-CH2+AgCl
(b)含-NH2,重氮化放氮
(CH3)3C-CH3NH2
O R C NH2
NaOX or X2/NaOH
RNH2
第二节 由碳原子到杂原子的重排 2 Hofmann重排
机理:
O R C NH2 Br2
-HBr
O
H
OH
R C N Br
O R C N Br
O
-Br
RC N
O CNR
H2O HO C N R HO
HO CH OH
H N R △ CO2 + NH2R
2 迁移基团迁移顺序
OCH3
>
Cl
>
> R3C- > R2CH-
> RCH3- > CH3- > H-
第一节 从碳原子到碳原子的重排一Wangner-Meerwein重排
Ag+
H3C C CH2Cl CH3
∨ ∨ CH3
H3C C CH2Cl
CH3
H3C
C
C H
CH3
Ag+ H3C C CH2CH3
OO CC
G
OH
第一节 从碳原子到碳原子的重排
三、二苯基乙二酮-二苯乙醇酸型重排
应用实例:
OCH3
CC OO
OCH3 KOH/n-BuOH/H2O
第五章-重排反应

12
二、 Pinacol重排
(邻二醇或邻二官能团合成醛酮的方法)
药 学 院 药 物 合 成 反 应
定义:在酸催化下,邻二叔醇失去一分子水, 重排成醛或酮的反应称Pinacol重排。
R1发生1,2-迁移
1
2
1
2
邻二醇
羰基类化合物
13
二、 Pinacol重排
反应机理:
(☆☆☆☆☆)
邻二醇
不对称的质子化酮
RCONH2 + NaOBr R N C O H2O RNH2
机理:
R C NH2 O OH Br2 R C NHBr O R N C O
R C N Br O
• 供电性R速度快于 吸电性R • 重排后R保留原来 手性
40
H2O/OH
RNH2 + CO3
2
36
15
二、 Pinacol重排 2、影响因素
i. 碳正离子稳定性的影响
ii. 立体化学因素的影响
iii.迁移基团迁移能力的影响
iv.反应条件的影响
16
i. 碳正离子稳定性的影响
关键:不对称连二醇类化合物重排的方向决定于羟基失去后,所 生成碳正离子的稳定性,通常与基团迁移能力的大小无关 。
不对称的邻二醇
OH COOH O
29
4)Favorski 卤化酮重排 法沃尔斯基重排
(☆☆☆)
定义: -卤代酮在亲核碱(NaOH, RONa等)条件下,发生重排,α-基团迁移到 卤素位置,得到羧酸盐、酯或酰胺的反应称为Favorski卤化酮重排反应。
R EtONa/EtOH O C X C CH3 NaOH R R C COOEt α-卤代酮的反应 COOH
二、 Pinacol重排
(邻二醇或邻二官能团合成醛酮的方法)
药 学 院 药 物 合 成 反 应
定义:在酸催化下,邻二叔醇失去一分子水, 重排成醛或酮的反应称Pinacol重排。
R1发生1,2-迁移
1
2
1
2
邻二醇
羰基类化合物
13
二、 Pinacol重排
反应机理:
(☆☆☆☆☆)
邻二醇
不对称的质子化酮
RCONH2 + NaOBr R N C O H2O RNH2
机理:
R C NH2 O OH Br2 R C NHBr O R N C O
R C N Br O
• 供电性R速度快于 吸电性R • 重排后R保留原来 手性
40
H2O/OH
RNH2 + CO3
2
36
15
二、 Pinacol重排 2、影响因素
i. 碳正离子稳定性的影响
ii. 立体化学因素的影响
iii.迁移基团迁移能力的影响
iv.反应条件的影响
16
i. 碳正离子稳定性的影响
关键:不对称连二醇类化合物重排的方向决定于羟基失去后,所 生成碳正离子的稳定性,通常与基团迁移能力的大小无关 。
不对称的邻二醇
OH COOH O
29
4)Favorski 卤化酮重排 法沃尔斯基重排
(☆☆☆)
定义: -卤代酮在亲核碱(NaOH, RONa等)条件下,发生重排,α-基团迁移到 卤素位置,得到羧酸盐、酯或酰胺的反应称为Favorski卤化酮重排反应。
R EtONa/EtOH O C X C CH3 NaOH R R C COOEt α-卤代酮的反应 COOH
第五章重排反应
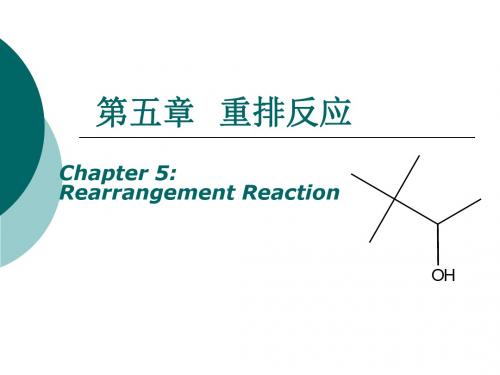
冷却 OH OH
CH3O
迁移基团电荷密度越高越有利于迁移
第一节 从碳原子到碳原子的重排二 频纳醇重排(Pinacol)
(C)
R' R
R' C C R
OH OH
Ph CH3
Ph CH3
H2SO4
Ph C C CH3 冷 却 Ph C C CH3
OH OH
Байду номын сангаас
OH
Ph CH3
Ac2O/ZnCl2 Ph C C CH3 OH OAc
O R C NH2
NaOX or X2/NaOH
RNH2
第二节 由碳原子到杂原子的重排 2 Hofmann重排
机理:
O R C NH2 Br2
-HBr
O
H
OH
R C N Br
O R C N Br
O
-Br
RC N
O CNR
H2O HO C N R HO
HO CH OH
H N R △ CO2 + NH2R
第五章 重排反应
Chapter 5: Rearrangement Reaction
OH
第五章 重排反应
定义:同一分子内部一个原子重排到另一个原子,形
成新分子。
W
W
AB
AB
A:重排起点原子,B:重排终点原子,W:重排基团
分类: 离子型机理(亲核重排,亲电重排)
自由基重排
周环机理重排(σ-键迁移重排)
RR R C CR
OH
R R CCR
OH R
R
H+
RCCR OH R
-H+
R
第五章 重排反应(Rearrangement reaction)
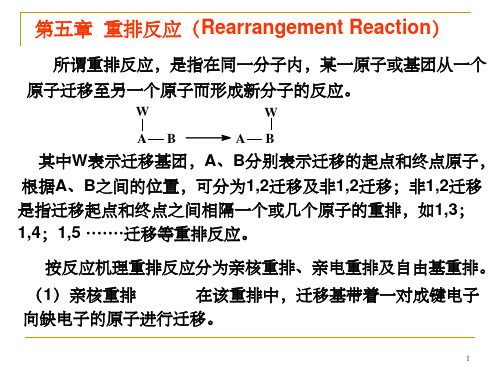
CH3
+
C CH2
CH3
C CH2 CH3
1,2-烷基迁移
CH3
+
C CH2 CH3 CH3
CH3
H+
CH3 C CH CH3
CH3
转变成更稳定的正离子是重排的一个动力,另外,转变成中 性化合物也是重排的一种动力,有时为促进重排,常在离去基或
其β-位上引入活性基团。如庚醇(heptanol)在三苯基膦的作用
原子或基团发生迁移。如下列化合物在酸催化下重排,得氢迁
移产物醛或酮。
H Ph Ph C C
OH OH
CH3(CH2)4 O
HCl(g) CH3 25 。C ,3h
CH3 CH2CCH2OH O OH
TsOH/C6H6
Ph Ph C C
OH
CH3(CH2)4 O
CH3
CH3 CH2CHCHO O
(90%) (80%)
5
下,经重排、水解得双环[2.2.1]庚醇:
OH NHTs Ph3P/DEAD
OPPh3
NHTs Ph3P=O
+
NHTs H
Ar O ArCO2
O
NHTs
(80%)
除此之外,碳正离子也可通过其他方式形成,如烯烃的卤加成, 氨基的重氮化等形式。
Br2 50。C Br
+ Br Br
+
Br Br
6
苯基迁移
HO
OH
HO
O
在脂环系统中,若两个羟基均处于同一脂环上,且呈顺式,
此时,离去基团(⊕OH2)与迁移基团互成反式,经重排得相 应的酮;若两个羟基呈反式,发生σ键迁移,得缩环产物。
第七章-重排反应PPT课件

1、史帝文斯重排(Stevens)
——季铵盐在碱作用下,烃基从氮迁移到邻近 的负碳离子上得到胺。
例如:
CH3 NCH+ C2PHh2CBHr- CH2 CH3
C4H9OK
CH2Ph
+-
CH3 N CH CH CH2
CH3
CH2ph
CH3 N CH CH CH2
CH3
.
形成叔胺 型化合物
22
C H 2R CH3 N+ R'
X
两处的碳负离子谁易形成?
容易
但后者除了进行分子内取代外,另有变化
.
30
✓分子内取代:
O
-OR
R
CH3
O
-
O
R
R
CH3
这个结构 不予成立
以原先与卤素 相连处断开
问题二 如果该结构式成立的话,就有二个分离 可能,但事实上只有一种。
O C OR R CH CH CH3
ROH
.
O C OR R CH CH2 CH3
1
重排反应的分类:
➢(1)以重排范围分类
分子内重排:(以此为主) 分子间重排:(是以后发展的方向)
➢(2)以重排发生的距离分类
1,2-重排:邻位重排(*) 1,3-重排:间位重排 各种位置之间的重排
重排反应的特点:
➢(1)剧烈性:与上述所说的不稳定性有关, 瞬间性
.
2
➢(2)复杂性:不可测性
许多重排的产物复杂; 许多重排的机理尚不十分明了,尚无定论
CH2N2 重氮甲烷
RO O C CH R
可用于生成 酯、酸、酰胺
+-
ROH, H2O, NH3
第三章 重排反应

O C
O C H
+使用酚盐(ArOM) ,因为其碱性弱,不足以发生重排
本重排反应物虽以α-芳二酮为主,但脂肪族、脂环族、杂环 族的α-二酮也能反应
O O OH HO COO H3O HO COOH
1,2-环己二酮
KOH/EtOH H3O
2-羟基-1-环己烷甲酸
1. 2.
O
O
HO
OH O Ar C CH Ar CN
OH
Ar C CH Ar CN
OH CH Ar
Benzil重排机理:
O Ar C O Ar C Ar O OH C Ar fast O fast C OH O Ar C O C Ar O Ar C O slow C OH Ar
OH OH O Ar C C O Ar
Benzil重排动力:生成稳定的羧酸盐
若用醇盐(ROM)代替NaOH,则重排产物为相应的酯。
O C O C (CH3)3COK (CH3)3COH C COOC(CH3)3 OH 93% 二苯基羟基乙酸叔丁酯
用醇盐(ROM)时注意:
(1) 醇盐不能有α-H,否则发生氧化还原反应
O C O C
+
H R2C O
(4) 脂肪族伯胺经亚硝酸处理,重氮化失氮
R NH2 HNO2 R N N R + N2
(5) 烯的质子化
R CH CH2 H R CH CH3
亲核重排的两种过程:
分子内的SN1 过程 Z C L C L Z C C C Z C
分子内的SN2 过程(邻基参与过程) Z C C L Z L C C
邻基参与又称邻基促进,迁移基就在离去基附近,有效浓 度高,所以有邻基参与的重排常比没有邻基参与的容易使 离去基离去,重排的速率也大。
高等有机化学课件第十三章
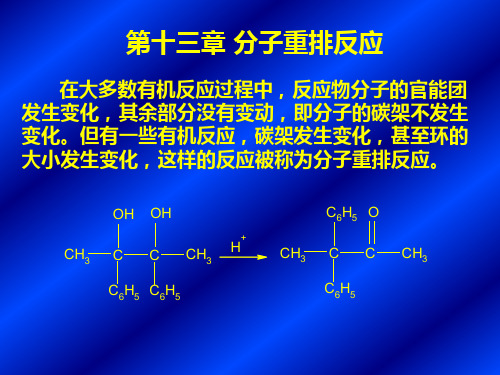
CHO KOH CHO
CH2OH COOK
五、碳-氮重排
1、贝克曼重排
R
R'
R
R'
C
+
H
C
N
N
HO
O+H2
2、霍夫曼重排
O R C NH2
O R C NHBr
R
R
O
C+ OH2
C
N R'
NH R'
O RC N
RNC O
六、碳-氧重排 Baeyer-Villiger重排
酮在过氧酸的存在下,氧原子插入到酮和迁移基 团之间,生成酯的重排反应。常用过氧酸是三氟过氧 乙酸。
CH3 CH3
C6H5 C
+
C C6H5 H
OH OH
O CH3 C6H5 C C C6H5
CH3 C6H5
C6H5 C C CH3 O
CH3
3、反式迁移 迁移基团与离去基团处于反式位置时,迁移速率
较快。例如 顺-1,2-二甲基-1,2-环己二醇在稀硫酸作用 下能迅速重排;而反- -1,2-二甲基-1,2-环己二醇在相 同条件下,由于迁移基团与离去基团不处于反式位置, 反应很慢,并导致环缩小反应。
三、按迁移的相对位置分类 按迁移基团的相对位置,可分为[1,2]迁移、[1,3]
迁移等等,大多数的重排反应都是[1,2]迁移。
第二节 亲核重排
亲核重排是迁移基团带着一对电子转移到缺电子 的迁移终点。亲核重排一般包括三步:第一步是缺电 子中心的创建;第二步是迁移基团带着一对电子迁移
到缺电子中心,使迁移起点成为缺电子中心;第三步
C C C6H5
C6H5
第五章 重排反应ppt课件

酯;
30
• (2)环状二酮生成环状羟基酸
31
四、Favorski重排 • 1. 反应通式
32
• 2. 反应机理
33
• 3. 影响因素
催化剂的影响
34
• 4. 应用特点 • 由卤代酮制备羧酸衍生物
35
五、 Wolff重排及Arndt-Eistert反应 • 1. 反应通式 Wolff rearrangement
C H 3O > >C l
> C H 2=C H
> R 3C > R 2C H> C H 3 > H
2020/1/14
17
• (3)胺类化合物的Wagner-Meerwein重排
CH3
CH3 C CH2NH2 CH3
HNO2 - N2
CH3 CH3 C CH2
CH3
CH3 C CH2CH3 CH3
36
• 2. 反应机理
37
38
• 3. 影响因素
Ph CH2 OCH3 PhLi C6H6
PhCHOCH3 Li+
CH3 PhCH
O-Li+
H2O
CH3 Ph CH OH
2020/1/14 8
3. Radical rearrangement
Cl
Cl CCH=CH2 Br Cl
Cl
Cl C CH CH2Br Cl
Cl
C
Cl CH
CH2Br
Br2
Cl
2. 碳原子到杂原子重排
(1)Beckmann重排 (2)Hoffman重排 (3)Curtius重排 (4)Schmidt重排 (5)Bayer-Villiger反应
3
重排反应
30
• (2)环状二酮生成环状羟基酸
31
四、Favorski重排 • 1. 反应通式
32
• 2. 反应机理
33
• 3. 影响因素
催化剂的影响
34
• 4. 应用特点 • 由卤代酮制备羧酸衍生物
35
五、 Wolff重排及Arndt-Eistert反应 • 1. 反应通式 Wolff rearrangement
C H 3O > >C l
> C H 2=C H
> R 3C > R 2C H> C H 3 > H
2020/1/14
17
• (3)胺类化合物的Wagner-Meerwein重排
CH3
CH3 C CH2NH2 CH3
HNO2 - N2
CH3 CH3 C CH2
CH3
CH3 C CH2CH3 CH3
36
• 2. 反应机理
37
38
• 3. 影响因素
Ph CH2 OCH3 PhLi C6H6
PhCHOCH3 Li+
CH3 PhCH
O-Li+
H2O
CH3 Ph CH OH
2020/1/14 8
3. Radical rearrangement
Cl
Cl CCH=CH2 Br Cl
Cl
Cl C CH CH2Br Cl
Cl
C
Cl CH
CH2Br
Br2
Cl
2. 碳原子到杂原子重排
(1)Beckmann重排 (2)Hoffman重排 (3)Curtius重排 (4)Schmidt重排 (5)Bayer-Villiger反应
3
重排反应
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Wagner-Meerwein重排 Pinacol重排 苯偶酰-二苯乙醇酸型重排 Favorski重排 Wolff重排
一、Wagner-Meerwein 重排
终点碳原子上羟基、卤原子或重氮基等,在质子 酸或Lewis酸催化下离去形成碳正离子,其邻近 的基团作1,2-迁移至该碳原子,同时形成更稳定 的起点碳正离子,后经亲核取代或质子消除而生 成新化合物的反应
O H
R RC C R
O R
Y=NH2,X,OSO2R, 酯基,环氧基等
C l
O H C H C P h H N O 2 C l P h N H 2
O H H
C C P h P h
C l
O H
C C P h P h
三、Wolff重排
-重氮酮 在银、银盐或铜等金属存在下,或 光照、加热分解条件下,发生消除氮分子而重 排为烯酮的反应。
OHOH
若两个羟基处于同一个脂环上, 顺式和反式的重排结果不同
OH H3C H3C
OH
H3C H3C
OH
OH2
H
H3C
H3C
OH
CH3 H
CH3C
O
实例:
(3)、
OH H
OH
O
(4)、
HO
O
H OHOHFra bibliotekH HO
O H
O
Semipinacol重排
R R R C C R
O H Y
R R R C C R
ONN RCCR
N ON RCCR
R RCCO
R RCCO
H2O
R RCH CO2H
R'OH
R RCH CO2R'
R'NH2
R RCH CO2NHR'
R
hv, -CO2
CO R
举例:
1、 O N2
Ph HNCO2Et
UV
Ph NCO2Et O
N 2
2、
OC O 2 B u - tR h ( O A c ) 2 2 5 /C o C H 2 C l2 /M e O H
H
1、 H 3 CCCC H 3
O H O H
OP h
OP h
H 3 CCCC H 3+ P hCCC H 3
P h
C H 3
主 要 产 物
PhPh
H
2、p-H3CO C6H4
CCC6H4O CH3-p O H O H
OPh PhCCC6H4O CH3-p
C6H4O CH3-p 主 要 产 物
+
OPh
OHOH
Ac2O/ZnCl2
CH3 Ph H3CCCPh
O H
Ph CH3 Ph CCCH3
HO OAc
_H
OPh H3CCCPh
CH3
OPh Ph CCCH3
CH3
(2)、
PhC 6H 4O C H 3-p PhCCC 6H 4O C H 3-p
H 2SO 4
O H O H
O Ph Ph C C C6H4OCH3-p
L
z
A + B
z
+ A B
z AB Nu
反应中间体的稳定性 迁移基团的迁移能力 立体位阻
分类:
z AB
L
z
A + B
z
+ A B
z AB N u
反应机理:亲核重排、亲电重排、自由基重排、 -迁移重排等。
迁移起点和终点的原子种类:C-C、C-X、XC的重排。
第一节 从碳原子到碳原子的重排
R2R2
H+
R1CCR1
OHOH
R2 R1CCR2
OR1
反应机理:
R2R2 R1 CCR1
OHOH
H+
R2R2
_H2O
R1 CCR1 OH
R2 R1 CCR1
OHR2
R2 R1 CCR1
OHR2
-H+
R2 R1 CCR1
OR2
反应的影响因素:
碳正离子中间体的稳定性 基团的迁移能力 立体位阻
C6H4OCH3-p
2、三取代的邻二醇重排:
产物复杂,分离困难,无制备价值 主要考虑碳正离子的稳定性
HP h P hC C
H OO H
H C l
O P h
P hC C
H
3、羟基位于脂环上 --扩环或缩环
(1)、
OH H2SO4/Et2O
OH r.t.2h C
Ph Ph
Ph
O Ph
(2)、
O H
1、四取代的邻二叔醇重排:
1)、四个取代基相同,产物单一。
RR RCCR
O HO H
2)、对称的邻二叔醇, 重排结果主要取 决于R1 、R2的迁移能力。
迁移能力: 芳基>烷基,H 不确定。 含给电子取代基的芳基>含 吸电子取代基的芳基
R2 R2 R1 C C R1
OHOH
应用实例:
P hP h
N2
3、
M eO H
O
r.t., hv
CO 2M e
C O 2 B u - t C O 2 M e
Arndt-Eistert Reaction
C O 2 H S O C l2
C O C l C H 2 N 2
C O C H N 2 A g 2 O /H 2 O
C H 2 C O 2 H
四、二苯基乙二酮-二苯乙醇酸型重排
重排反应整理
定义:
有机反应中,同一有机分子内的一个基团或原 子从一个原子迁移到另一个原子上,使分子构架 发生改变而形成一个新的分子的反应
重排反应三步骤:
z AB
L
z
A + B
z
+ A B
z AB N u
1)生成活性中间体
2)重排→生成更稳定的中间体
3)生成消去和取代产物
反应的影响因素:
z AB
OH H
OH H
CH2 -H
莰烯
CH2
应用实例:
CH2
CH3
CH3 CH3
1、
TsOH
CH3 C6H5
CH3
H3C
CH3
2、
H3CO
NH2 NaNO2/HOAc
H3CO
H3C OH H
H
二、Pinacol 重排
邻二叔醇类化合物 在酸催化下,失去一分子 水重排生成醛或酮的反应,称为Pinacol重 排反应。
二苯基乙二酮(苯偶酰)类化合物用碱处理, 生成二苯基-羟基酸(二苯乙醇酸) 。
OO CC
KO H /EtO H
O H CC O 2
O O O H O O
O O
O H O
A rC C A r
A rC C O H A rC C O H A rC C O
p-H3CO C6H4 CCC6H4O CH3-p Ph
3)、不对称的邻二叔醇
重排方向主要取决于:羟基失去后形成的碳 正离子的稳定性
一般,叔碳>仲碳>伯碳
通常与基团的迁移能力无关。
R1 R2 R1 C C R2
OH OH
R2 R3 R1 C C R4
OHOH
实例:
(1)、
CH3Ph
H
H3C C C Ph
C H 3B r H 3 CCC H 2
A lB r3H 3 CC C H 3 C H 2
C H 3 -A lB r4
C H 3
B r H 3 CCC H 2 C H 3 A lB r4H 3 CCC H 2 C H 3
C H 3
_ H
C H 3 H 3 CCC H C H 3
C H 3
实例:
异冰片
一、Wagner-Meerwein 重排
终点碳原子上羟基、卤原子或重氮基等,在质子 酸或Lewis酸催化下离去形成碳正离子,其邻近 的基团作1,2-迁移至该碳原子,同时形成更稳定 的起点碳正离子,后经亲核取代或质子消除而生 成新化合物的反应
O H
R RC C R
O R
Y=NH2,X,OSO2R, 酯基,环氧基等
C l
O H C H C P h H N O 2 C l P h N H 2
O H H
C C P h P h
C l
O H
C C P h P h
三、Wolff重排
-重氮酮 在银、银盐或铜等金属存在下,或 光照、加热分解条件下,发生消除氮分子而重 排为烯酮的反应。
OHOH
若两个羟基处于同一个脂环上, 顺式和反式的重排结果不同
OH H3C H3C
OH
H3C H3C
OH
OH2
H
H3C
H3C
OH
CH3 H
CH3C
O
实例:
(3)、
OH H
OH
O
(4)、
HO
O
H OHOHFra bibliotekH HO
O H
O
Semipinacol重排
R R R C C R
O H Y
R R R C C R
ONN RCCR
N ON RCCR
R RCCO
R RCCO
H2O
R RCH CO2H
R'OH
R RCH CO2R'
R'NH2
R RCH CO2NHR'
R
hv, -CO2
CO R
举例:
1、 O N2
Ph HNCO2Et
UV
Ph NCO2Et O
N 2
2、
OC O 2 B u - tR h ( O A c ) 2 2 5 /C o C H 2 C l2 /M e O H
H
1、 H 3 CCCC H 3
O H O H
OP h
OP h
H 3 CCCC H 3+ P hCCC H 3
P h
C H 3
主 要 产 物
PhPh
H
2、p-H3CO C6H4
CCC6H4O CH3-p O H O H
OPh PhCCC6H4O CH3-p
C6H4O CH3-p 主 要 产 物
+
OPh
OHOH
Ac2O/ZnCl2
CH3 Ph H3CCCPh
O H
Ph CH3 Ph CCCH3
HO OAc
_H
OPh H3CCCPh
CH3
OPh Ph CCCH3
CH3
(2)、
PhC 6H 4O C H 3-p PhCCC 6H 4O C H 3-p
H 2SO 4
O H O H
O Ph Ph C C C6H4OCH3-p
L
z
A + B
z
+ A B
z AB Nu
反应中间体的稳定性 迁移基团的迁移能力 立体位阻
分类:
z AB
L
z
A + B
z
+ A B
z AB N u
反应机理:亲核重排、亲电重排、自由基重排、 -迁移重排等。
迁移起点和终点的原子种类:C-C、C-X、XC的重排。
第一节 从碳原子到碳原子的重排
R2R2
H+
R1CCR1
OHOH
R2 R1CCR2
OR1
反应机理:
R2R2 R1 CCR1
OHOH
H+
R2R2
_H2O
R1 CCR1 OH
R2 R1 CCR1
OHR2
R2 R1 CCR1
OHR2
-H+
R2 R1 CCR1
OR2
反应的影响因素:
碳正离子中间体的稳定性 基团的迁移能力 立体位阻
C6H4OCH3-p
2、三取代的邻二醇重排:
产物复杂,分离困难,无制备价值 主要考虑碳正离子的稳定性
HP h P hC C
H OO H
H C l
O P h
P hC C
H
3、羟基位于脂环上 --扩环或缩环
(1)、
OH H2SO4/Et2O
OH r.t.2h C
Ph Ph
Ph
O Ph
(2)、
O H
1、四取代的邻二叔醇重排:
1)、四个取代基相同,产物单一。
RR RCCR
O HO H
2)、对称的邻二叔醇, 重排结果主要取 决于R1 、R2的迁移能力。
迁移能力: 芳基>烷基,H 不确定。 含给电子取代基的芳基>含 吸电子取代基的芳基
R2 R2 R1 C C R1
OHOH
应用实例:
P hP h
N2
3、
M eO H
O
r.t., hv
CO 2M e
C O 2 B u - t C O 2 M e
Arndt-Eistert Reaction
C O 2 H S O C l2
C O C l C H 2 N 2
C O C H N 2 A g 2 O /H 2 O
C H 2 C O 2 H
四、二苯基乙二酮-二苯乙醇酸型重排
重排反应整理
定义:
有机反应中,同一有机分子内的一个基团或原 子从一个原子迁移到另一个原子上,使分子构架 发生改变而形成一个新的分子的反应
重排反应三步骤:
z AB
L
z
A + B
z
+ A B
z AB N u
1)生成活性中间体
2)重排→生成更稳定的中间体
3)生成消去和取代产物
反应的影响因素:
z AB
OH H
OH H
CH2 -H
莰烯
CH2
应用实例:
CH2
CH3
CH3 CH3
1、
TsOH
CH3 C6H5
CH3
H3C
CH3
2、
H3CO
NH2 NaNO2/HOAc
H3CO
H3C OH H
H
二、Pinacol 重排
邻二叔醇类化合物 在酸催化下,失去一分子 水重排生成醛或酮的反应,称为Pinacol重 排反应。
二苯基乙二酮(苯偶酰)类化合物用碱处理, 生成二苯基-羟基酸(二苯乙醇酸) 。
OO CC
KO H /EtO H
O H CC O 2
O O O H O O
O O
O H O
A rC C A r
A rC C O H A rC C O H A rC C O
p-H3CO C6H4 CCC6H4O CH3-p Ph
3)、不对称的邻二叔醇
重排方向主要取决于:羟基失去后形成的碳 正离子的稳定性
一般,叔碳>仲碳>伯碳
通常与基团的迁移能力无关。
R1 R2 R1 C C R2
OH OH
R2 R3 R1 C C R4
OHOH
实例:
(1)、
CH3Ph
H
H3C C C Ph
C H 3B r H 3 CCC H 2
A lB r3H 3 CC C H 3 C H 2
C H 3 -A lB r4
C H 3
B r H 3 CCC H 2 C H 3 A lB r4H 3 CCC H 2 C H 3
C H 3
_ H
C H 3 H 3 CCC H C H 3
C H 3
实例:
异冰片
