医用化学_第十一章_羧酸和羧酸衍生物
合集下载
有机化学第十一章羧酸衍生物

O CB r+H N N aO H
O CN +N ar B +H 2O
( C H 3 C O ) 2 O + C 6 H 5 N H 2 C 6 H 5 N H C O C H 3 + C H 3 C O O H
O C CO+ HN O
O CN
COOH
编辑ppt
25
(2)环状酸酐与氨反应,开环后得到单酰 胺酸的铵盐,酸化后得到单酰胺酸。如 在加热时,可得到酰亚胺。
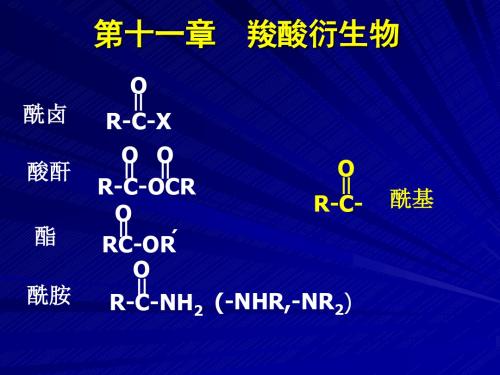
第十一章 羧酸衍生物
编辑ppt
1
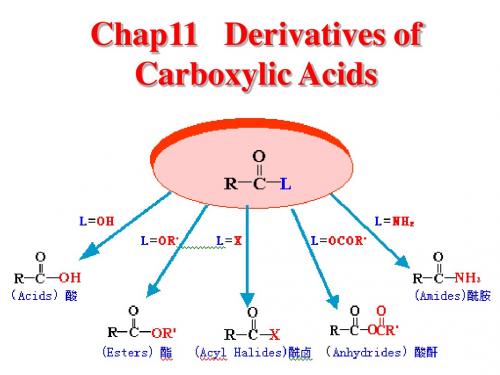
羧基中的羟基被取代,生成酰卤、酸酐、 酯或酰胺等化合物,统称为羧酸衍生物。
编辑ppt
2
一、羧酸衍生物的制法
(教材P.166~168)
1.生成酰卤
可由羧酸与三氯化磷、五氯化磷或氯化 亚砜直接反应制得。
RCOOH+ PCl5
RCOCl
RCOOH+ PCl3 RCOOH+ SOCl
C 6 H 5 C O O H + C 2 H 5 S HC 6 H 5 C O S C 2 H 5 + H 2 O
编辑ppt
9
二、羧酸衍生物的命名
1.酰基的命名
O OO
羧酸中的羧基去掉羟基后剩余的部分称为
CR HC3 CC
酰基。酰基的名称根据相应的酸命名,
即将“某酸”改为“某酰基”即可。例
如:
编辑ppt
22
3. 氨解
酰卤、酸酐、酯都能与氨或胺反应生成 酰胺。(板书)另一产物分别为:HX、 羧酸、醇(交换)。
编辑ppt
23
(1) 酰卤或酸酐与氨在较低温度下与氨反 应,可缓慢地生成酰胺,是有机合成中 常用的方法。该反应又称为氨(或胺) 的酰化反应。 例如:
第十一章羧酸衍生物
三、酯的命名
一元醇与一元酸生成的酯称某酸某(醇
或酚)酯;多元醇酯称为某醇某酸酯;内酯 用希腊字母标明原羟基的位置,称某内酯。
O
COOCH3
CH2-O-Cll -CH3 l
COOH CH2-O-Cll-CH3
H3C
O
O
O
邻苯二甲酸甲酯 乙二醇二乙酸酯 γ-戊内酯
四、酰胺的命名
简单的酰胺是在酰基名称后加“胺”或
(三)酯缩合反应
具有α-H的酯,在醇钠的作用下能发生类 似醇醛缩合反应。——Claisen缩合反应
CH3COOCH2CH3CH3CH2ONa -CH2COOCH2CH3
OCH3C CH2COOCH2CH3
OCH2CH3
CH3CO CH2COOCH2CH3 + CH3CH2O-
COOC2H5 + CH3COOC2H5NaOC2H5 COCH2COOC2H5 + C2H5OH
第十一章 羧酸衍生物
酰卤 酸酐 酯 酰胺
O ll R-C-X
R-OCll -OOlCl R O
RCll -ORˊ
O ll R-C-
O R-Cll -NH2 (-NHR,-NR2)
酰基
第一节 羧酸衍生物的命名
酰基的名称是将其羧酸的名称的“酸” 字改成“酰基”。
O
CH3C OH 乙酸
O
CH3C 乙酰基
交叉Claisen酯缩合反应
三、碳酸衍生物
氨基甲酸酯 脲(尿素) 胍 丙二酰脲
四、尼龙和聚酯
CH3CONH2 + NH2CH3 CH3CONHCH3 + NH3
(二)酰基亲核取代反应的机制
O R-lCl —L+:Nu
羧酸及羧酸衍生物

O C OCH3
甲氧甲酰基
O O C CH3
O C NH2
氨甲酰基
O C X
卤甲酰基
乙酰氧基
二、物理性质
bp:酰卤和酯较相应的羧酸低;酰胺比相应的 羧酸高,氨基上的氢被取代后,bp降低; 酸酐比分子量相当的羧酸低,但常较相应 的羧酸高。
O R C O H
H O C R O
O R C NH H
H NH C O R
O + H H R'C O CR3
+
属于SN1机制。
3º 醇的酯化动力学上是一级反应。
c 酰基正离子机制
CH 3 O C-OH CH 3
H2SO4(浓)
CH 3
O + C-OH2 CH 3
CH 3
O +C CH 3
+O
CH 3
C CH 3
CH 3
CH 3
CH 3
CH 3
CH 3
O H C-OCH3 + CH 3
O O + H2O O
O O RCOONa + R'COCl Δ RCOCR' + NaCl
4.成酰胺反应
CH3COOH + NH3
CH3COONH4
CH3COONH4
Δ
CH3CONH2 + H2O
(四) α-氢原子的取代反应
R CH2 COOH
Br2 ,红磷
R CH C OOH
Br 赫尔-佛尔哈德-泽林斯基反应
(四)亲核取代和结构的关系
O R C L + Nu
-
slow
OR C Nu L
fast
甲氧甲酰基
O O C CH3
O C NH2
氨甲酰基
O C X
卤甲酰基
乙酰氧基
二、物理性质
bp:酰卤和酯较相应的羧酸低;酰胺比相应的 羧酸高,氨基上的氢被取代后,bp降低; 酸酐比分子量相当的羧酸低,但常较相应 的羧酸高。
O R C O H
H O C R O
O R C NH H
H NH C O R
O + H H R'C O CR3
+
属于SN1机制。
3º 醇的酯化动力学上是一级反应。
c 酰基正离子机制
CH 3 O C-OH CH 3
H2SO4(浓)
CH 3
O + C-OH2 CH 3
CH 3
O +C CH 3
+O
CH 3
C CH 3
CH 3
CH 3
CH 3
CH 3
CH 3
O H C-OCH3 + CH 3
O O + H2O O
O O RCOONa + R'COCl Δ RCOCR' + NaCl
4.成酰胺反应
CH3COOH + NH3
CH3COONH4
CH3COONH4
Δ
CH3CONH2 + H2O
(四) α-氢原子的取代反应
R CH2 COOH
Br2 ,红磷
R CH C OOH
Br 赫尔-佛尔哈德-泽林斯基反应
(四)亲核取代和结构的关系
O R C L + Nu
-
slow
OR C Nu L
fast
8.5 羧酸及羧酸衍生物

第五节
羧酸及羧酸衍生物
分子中含有羧基(-COOH)的化合物,叫羧酸。 羧酸在自然界中广泛存在,而且对人类生活非 常重要,如食醋,是2%的乙酸;日常使用的肥皂, 是高级脂肪酸的钠盐;食用油,是高级不饱和脂肪 酸的甘油酯。羧酸也是许多合成纤维(如尼龙、的 确良等)的原料之一。
1
目录
25
小 结
+I效应使RCOOH酸性减弱,-I效应使RCOOH酸性增强。 -I效应强弱次序: NH3+>NO2>CN>COOH>F>Cl>Br +I效应强弱次序: O->COO->(CH3)3C>CH3CH2>CH3>H
26
B.芳香酸
①酸性:HCOOH > C6H5COOH > CH3COOH pk a 3.37 4.20 4.73 ②芳环上有吸电子基时,ArCOOH酸性增加。
¡¡ ¡¡
H+
COOH OH
H3C
OH ¡¡
H3C
羧酸盐是离子化合物,易溶于水,高级脂肪酸的钠盐(硬脂 酸钠)可用于制皂,苯甲酸钠、乙酸钙、山梨酸钾是常用的 食品防腐剂。
23
(2) 影响酸性的因素 羧酸根负离子愈稳定,愈容易生成,酸性就愈强。 任何使酸根负离子稳定的因素都将增加其酸性。
A. 脂肪酸
O
O2N COOH
PCl5
O2N
O CH3CCl
CCl
CH3COOH
SOCl2
(100%)
33
2. 酸酐的生成
O R-C O H OH R-C O
¡¡¡
O R-C O + H2O R-C O
¡ £ Ã Ñ ® Á ¹ P2O5¡Al2O3¡¨H 2SO4 ³ Ó Í Ë » £
羧酸及羧酸衍生物
分子中含有羧基(-COOH)的化合物,叫羧酸。 羧酸在自然界中广泛存在,而且对人类生活非 常重要,如食醋,是2%的乙酸;日常使用的肥皂, 是高级脂肪酸的钠盐;食用油,是高级不饱和脂肪 酸的甘油酯。羧酸也是许多合成纤维(如尼龙、的 确良等)的原料之一。
1
目录
25
小 结
+I效应使RCOOH酸性减弱,-I效应使RCOOH酸性增强。 -I效应强弱次序: NH3+>NO2>CN>COOH>F>Cl>Br +I效应强弱次序: O->COO->(CH3)3C>CH3CH2>CH3>H
26
B.芳香酸
①酸性:HCOOH > C6H5COOH > CH3COOH pk a 3.37 4.20 4.73 ②芳环上有吸电子基时,ArCOOH酸性增加。
¡¡ ¡¡
H+
COOH OH
H3C
OH ¡¡
H3C
羧酸盐是离子化合物,易溶于水,高级脂肪酸的钠盐(硬脂 酸钠)可用于制皂,苯甲酸钠、乙酸钙、山梨酸钾是常用的 食品防腐剂。
23
(2) 影响酸性的因素 羧酸根负离子愈稳定,愈容易生成,酸性就愈强。 任何使酸根负离子稳定的因素都将增加其酸性。
A. 脂肪酸
O
O2N COOH
PCl5
O2N
O CH3CCl
CCl
CH3COOH
SOCl2
(100%)
33
2. 酸酐的生成
O R-C O H OH R-C O
¡¡¡
O R-C O + H2O R-C O
¡ £ Ã Ñ ® Á ¹ P2O5¡Al2O3¡¨H 2SO4 ³ Ó Í Ë » £
第十一、十二章 羧酸及其衍生物

> C9 蜡状固体,无气味。
2. 溶解性(solubility) 低级羧酸与水混溶;高级羧酸不溶;一般二元和 多元酸易溶。
第18页,共109页。
羧酸的物理性质
3.熔点(melting point)
有一定规律,随着分子中碳原子数目的增加呈锯齿状的 变化。
乙酸熔点16.6℃,当室温低于此温度时,立即凝成冰状 结晶,故纯乙酸又称为冰醋酸。
COOH
CHCO2H OH
羧基 连在Ar或R
上都可
羟基酸
C CO2H O
羰基酸
CH COOH NH2
氨基酸
取代羧酸
第1页,共109页。
羧酸分子中烃基上的氢被取代后的产物称取代羧酸。
R CH COOH X
R CH COOH OH
R C COOH O
R CH COOH NH2
取代羧酸
R
O
R
R C OH
R
R
O CX O C OCOR O C OR O C NH2
羧酸衍生物
第2页,共109页。
DHA怎么补?
DHA
DHA,二十二碳六烯酸(docosahexenoic acid ),俗称脑 黄金,是一种对人体非常重要的多不饱和脂肪酸,属于 Omega-3不饱和脂肪酸家族中的重要成员。DHA是神经系统
细胞生长及维持的一种主要元素,是大脑和视网膜的重要
136pm
O···· H
羰基和羟基通过 p-π共轭 构成一个整 体, 故羧基不是羰基和羟基的简单加合。
第15页,共109页。
123pm
127pm
R
136pm 游离羧酸分子中的 p-π 共轭
R
H
127pm 羧酸根负离子的 p-π 共轭
2. 溶解性(solubility) 低级羧酸与水混溶;高级羧酸不溶;一般二元和 多元酸易溶。
第18页,共109页。
羧酸的物理性质
3.熔点(melting point)
有一定规律,随着分子中碳原子数目的增加呈锯齿状的 变化。
乙酸熔点16.6℃,当室温低于此温度时,立即凝成冰状 结晶,故纯乙酸又称为冰醋酸。
COOH
CHCO2H OH
羧基 连在Ar或R
上都可
羟基酸
C CO2H O
羰基酸
CH COOH NH2
氨基酸
取代羧酸
第1页,共109页。
羧酸分子中烃基上的氢被取代后的产物称取代羧酸。
R CH COOH X
R CH COOH OH
R C COOH O
R CH COOH NH2
取代羧酸
R
O
R
R C OH
R
R
O CX O C OCOR O C OR O C NH2
羧酸衍生物
第2页,共109页。
DHA怎么补?
DHA
DHA,二十二碳六烯酸(docosahexenoic acid ),俗称脑 黄金,是一种对人体非常重要的多不饱和脂肪酸,属于 Omega-3不饱和脂肪酸家族中的重要成员。DHA是神经系统
细胞生长及维持的一种主要元素,是大脑和视网膜的重要
136pm
O···· H
羰基和羟基通过 p-π共轭 构成一个整 体, 故羧基不是羰基和羟基的简单加合。
第15页,共109页。
123pm
127pm
R
136pm 游离羧酸分子中的 p-π 共轭
R
H
127pm 羧酸根负离子的 p-π 共轭
羧酸及羧酸衍生物

R'OH
水解
(1)反应特点:
+ RCOOR' H2O
① 反应可逆(酯化和水解都不能进行完全)。
② 反应速度慢,催化剂同时加速酯化和水解反应。
增大产率:① 增加反应物; ② 减少生成物。
(2)反应历程: ① 伯、仲醇:亲核加成—消除历程 醇中羟基上的氢与羧酸中的羟基结合脱水生成 酯,反应中羧酸的酰氧键断裂。
沸点(162℃)
O
+ R C OH SOCl2
沸点(79℃)
O
+ R C Cl POCl3 制备高沸点酰氯
沸点(107℃)
O
+ + R C Cl SO2 HCl
两种情况均适用
生成酰卤的反应历程
R
O
-HCl
C OH + PCl3
R
O CO
PCl2
Cl- R
O C
O PCl2
b.p. 75℃
Cl
O R C Cl + HO PCl2
攻酰基碳而发生酯化。
O
O
O
+O
+
C-OH
C-OH2
+C
C
CH3
CH3 H2SO4(浓) CH3
CH3 CH3
CH3 CH3
CH3
CH3
CH3OH CH3
CH3
OH C-O+ CCHH33
-H+ CH3
CH3
O C-OCH3
CH3
CH3
78%
CH3
CH3
(3)羧酸和醇的结构对酯化反应速率的影响 ① 羧酸α-C上支链愈多,基团愈大,酯化反应 速率愈慢。
水解
(1)反应特点:
+ RCOOR' H2O
① 反应可逆(酯化和水解都不能进行完全)。
② 反应速度慢,催化剂同时加速酯化和水解反应。
增大产率:① 增加反应物; ② 减少生成物。
(2)反应历程: ① 伯、仲醇:亲核加成—消除历程 醇中羟基上的氢与羧酸中的羟基结合脱水生成 酯,反应中羧酸的酰氧键断裂。
沸点(162℃)
O
+ R C OH SOCl2
沸点(79℃)
O
+ R C Cl POCl3 制备高沸点酰氯
沸点(107℃)
O
+ + R C Cl SO2 HCl
两种情况均适用
生成酰卤的反应历程
R
O
-HCl
C OH + PCl3
R
O CO
PCl2
Cl- R
O C
O PCl2
b.p. 75℃
Cl
O R C Cl + HO PCl2
攻酰基碳而发生酯化。
O
O
O
+O
+
C-OH
C-OH2
+C
C
CH3
CH3 H2SO4(浓) CH3
CH3 CH3
CH3 CH3
CH3
CH3
CH3OH CH3
CH3
OH C-O+ CCHH33
-H+ CH3
CH3
O C-OCH3
CH3
CH3
78%
CH3
CH3
(3)羧酸和醇的结构对酯化反应速率的影响 ① 羧酸α-C上支链愈多,基团愈大,酯化反应 速率愈慢。
第十一章_羧酸衍生物

例:
n-BuOH
H2C
CH COOCH3
TsOH
H2C
CH COOBun
+
CH3OH 蒸除
O CH3O C
O O CCH3
HOCH3 NaOCH3
O CH3O C OH + CH3COOCH3
选择性酯交换
CH
CH2 CH OAc
n
CH2
CH3OH OH
CH
CH2 CH OH
聚乙烯醇
n
CH2
OAc
OH
不溶于水, 不能直接水解
(4)酰胺的醇解反应
O
R
R"OH
O
R
C
NHR'
H+ or R"O
C
OR"
+
R'NH2
* 反应相对不易进行 (因为
NHR' 的离去能力比 OR' 差)
* 合成上意义不大(合成酯类化合物的方法有更好的方法)
3、羧酸衍生物的胺解反应
(1)酰氯的胺(氨)解
O
R R'NH2
O
R
C
Cl
O
+
HOR'
碱用量 > 化学计量,反应可进行完全。
(4)酰胺的水解
O
R
C
NHR'
H2O H+
O
R
C
OH
+
H3NR'
O
R
C
NHR'
H2O OH
O
R
C
O
+
H2NR'
H+ or OH
第十一章 羧酸衍生物
乙酰苯胺
N-甲基苯甲酰胺
§2 Properties
一、 结构分析
-L为卤素、酰氧基、烷氧基和氨(胺)基,均为吸 电子基,卤素和酰氧基以-I效应为主,羰基碳带有 更多的正电荷,更易发生亲核加成反应;烷氧基和 氨(胺)基以+C效应为主,较难发生亲电加成。 L基团的总效应(-I/+C): 吸电子能力越强(相对
C NH2 + H N O O
H2N
C NH C NH2
缩二脲反应: 分子中含两个以上酰胺键结构的 化合物, 其碱溶液遇硫酸铜显紫红色(紫色)的 反应(多肽等).
( 三) 胍
1.强碱性: pKa =13.8,与KOH相当
胍为何具有强碱性?
2. 游离胍易水解
(四) 丙二酰脲
制备方法
O CH 2 C OC 2H 5 + C OC 2H 5 O H H N H N H O C CH 2 C O N H H N C = O + 2C2H5OH C =O C2H5ONa
CH3 CH2= CCOOCH3
CH2OOCCH3 CHOOCCH3 CH2OOCCH3
COOCH2CH3 COOH
a-甲基丙烯
酸甲酯
丙三醇三乙 草酸氢乙酯 酸酯
酰胺:
酰基+胺或某胺, 酰胺氮原子有取代 基, 取代基前+”N” , -线隔开.
O CH3 C NH2
O CH3 C NH
乙酰胺
O C NH CH3
CONH(CH2)3CH3 苯 菌灵(杀 菌剂)
(二) 脲(尿素)
弱碱性
O H 2N C O H 2N C NH 2 + NH 2 + HNO3 H 2N O HNO3 C NH 2 · O H 2N
有机化学第十一章羧酸衍生物

肪 硬脂酸(十八碳酸)Fra bibliotek酸 花生四烯酸(二十碳酸)
棕榈油酸(9-十六碳烯酸)
结构式 CH3(CH2)10COOH CH3(CH2)12COOH CH3(CH2)14COOH CH3(CH2)16COOH CH3(CH2)18COOH
CH3(CH2)5CH=CH(CH2)7COOH
不 油酸(9-十八碳烯酸)
② 酸酐的氨(胺)解 酸酐与胺反应,除产生酰胺外,还有一分子羧 酸,因此反应中经常加入三级胺,以中和反应产生的酸。
③ 酯的氨(胺)解 酯可以与氨或胺反应形成酰胺。氨或胺本身作 为亲核试剂,进攻酯羰基碳。
④ 酰胺的氨(胺)解 酰胺与氨(胺)反应是一个胺的交换反应。
2.异羟肟酸铁盐反应 除酰卤外,酸酐、酯和酰伯胺均能与羟胺反应生成异羟肟酸,异 羟肟酸与三氯化铁作用,得到紫红色的异羟肟酸铁盐,这一反应常用 来鉴别酸酐、酯和酰胺,称为异羟肟酸铁盐反应。
有机化学
第十一章 羧酸衍生物
学习目标
1. 掌握羧酸衍生物的结构特征、分类、命名方法及主要化学性质; 2. 理解不同羧酸衍生物在化学性质上的异同; 3. 了解常见羧酸衍生物的性质和用途; 4. 学会油脂和类脂化合物的鉴别方法。
第十一章 羧酸衍生物
羧酸分子中的羟基被其它原子或基团取代所生成的化合物,主要 有酰卤、酸酐、酯、酰胺,其分子结构中均含有酰基,因而也被称为 酰基化合物。
1.水解反应
在酸、碱或酶的作用下,油脂可发生水解反应。在酸性条件下,
油脂水解生成高级脂肪酸和甘油,该反应为可逆反应。
在碱性条件(如NaOH或KOH)下,油脂水解生成甘油和高级脂肪
酸钠(钾)盐。高级脂肪酸钠盐俗称肥皂。因此,把油脂在碱性溶液
中的水解反应称为皂化反应。
《羧酸及羧酸衍生物》课件

酰胺
由羧酸和胺反应得到,广泛应用于药物和化妆品制 备。
应是羧酸与醇反应,通过酸催化发生。
2
步骤一
酸催化下,羧酸与醇发生酯化反应,生成酯和水。
3
步骤二
反应达到平衡状态,酯与水分子间形成酯水平衡。
美拉德反应的原理和应用
1
反应机制
美拉德反应是羧酸与胺或胺盐反应,形成酰
原理
2
步骤一
羧酸经过羰基化反应,碳氧化物离子(COX)作为中间体。
3
步骤二
COX中间体与亲电试剂反应,形成酰化产物。
羧酸衍生物在医学上的应用
药物
羧酸衍生物广泛应用于药物制备中,如酰胺类和酯 类药物。
缓控释技术
羧酸衍生物可以用于缓慢释放药物的技术。
抗生素
许多抗生素中含有羧酸结构,用于治疗细菌感染。
抗氧化剂
医药行业
羧酸被用于制药中的药物合成和 酯化反应。
农业领域
羧酸作为农药、杀菌剂等的主要 成分,用于作物保护。
食品工业
羧酸用作食品添加剂、防腐剂等, 延长食品的保鲜期。
羧酸衍生物的分类
酯
由羧酸和醇反应得到,广泛应用于溶剂、香精等领 域。
酸酐
羧酸的缩合物,常用于有机合成中的酯化反应。
酰氯
由羧酸和PCl5反应得到,用于有机合成和涂料制备。
溶解性
羧酸在水中可溶,其溶解度受羧基 和碳链长度的影响。
酸性
羧酸具有酸性,可通过释放H+离子 作为酸的一种。
羧酸的命名方法
1 系统命名法
2 常规命名法
3 官能团命名法
根据羧基的碳数和包含的取 代基,使用规则命名。
根据常用名称给予命名,如 乙酸、苹果酸等。
由羧酸和胺反应得到,广泛应用于药物和化妆品制 备。
应是羧酸与醇反应,通过酸催化发生。
2
步骤一
酸催化下,羧酸与醇发生酯化反应,生成酯和水。
3
步骤二
反应达到平衡状态,酯与水分子间形成酯水平衡。
美拉德反应的原理和应用
1
反应机制
美拉德反应是羧酸与胺或胺盐反应,形成酰
原理
2
步骤一
羧酸经过羰基化反应,碳氧化物离子(COX)作为中间体。
3
步骤二
COX中间体与亲电试剂反应,形成酰化产物。
羧酸衍生物在医学上的应用
药物
羧酸衍生物广泛应用于药物制备中,如酰胺类和酯 类药物。
缓控释技术
羧酸衍生物可以用于缓慢释放药物的技术。
抗生素
许多抗生素中含有羧酸结构,用于治疗细菌感染。
抗氧化剂
医药行业
羧酸被用于制药中的药物合成和 酯化反应。
农业领域
羧酸作为农药、杀菌剂等的主要 成分,用于作物保护。
食品工业
羧酸用作食品添加剂、防腐剂等, 延长食品的保鲜期。
羧酸衍生物的分类
酯
由羧酸和醇反应得到,广泛应用于溶剂、香精等领 域。
酸酐
羧酸的缩合物,常用于有机合成中的酯化反应。
酰氯
由羧酸和PCl5反应得到,用于有机合成和涂料制备。
溶解性
羧酸在水中可溶,其溶解度受羧基 和碳链长度的影响。
酸性
羧酸具有酸性,可通过释放H+离子 作为酸的一种。
羧酸的命名方法
1 系统命名法
2 常规命名法
3 官能团命名法
根据羧基的碳数和包含的取 代基,使用规则命名。
根据常用名称给予命名,如 乙酸、苹果酸等。
第十章羧酸第十一章羧酸衍生物
二 羧基中氢的反应
1 酸碱反应 强无机酸 > 羧酸 > 碳酸 > 酚
p Ka
4~5 6.35 10
RCOOH + NaHCO 3 羧酸可以和碳酸氢钠反应
RCOO -Na+ + CO 2 + H2O
ArONa + CO 2 + H2O
ArOH + NaHCO 3 酚不能和碳酸氢钠反应
2 羧酸盐的若干性质
诱导吸电子作用中、
共轭给电子作用小。
诱导吸电子作用小、 共轭给电子作用大。
pka 2.98
pka 4.08
pka 4.57
苯甲酸的pka 4.20
第四节 羧酸的制备 一 氧化法
醇、醛、芳烃、炔、烯、酮(卤仿反应)的氧化
二 羧酸衍生物的水解反应(参见十三章)
O
OO
O
O
R-C-X R-C-O-C-R' R-C-OR' R-C-NH 2
HCOOH pka 3.37
C 6H5-COOH 4.20
CH 3COOH 4.73
(2)空间效应: 利于H+离解的空间结构 酸性强,不利于H+离解的空 间结构酸性弱.
O
OH H O
(3)分子内的氢键也能 使羧酸的酸性增强。
4 芳香羧酸的情况分析
取代基具有吸电子共轭效应时,酸性强弱顺序为: 邻>对>间
*1. 羧酸盐是固体 *2. 羧酸盐的溶解度
钠、钾、銨 盐可溶于水,重金属盐不溶于水。 *3. 羧酸根具有碱性和亲核性
羧酸盐能与活泼卤代烷反应(见下页)
三 羧酸α-H的反应 —— 赫尔 -乌尔哈 -泽林斯基反应
医用有机化学课件:羧酸及衍生物

2,3- 二甲基戊酸 (α,β-二甲基戊酸)
(2)不飽和羧酸
2 -甲基-3-戊烯酸
5 -甲基-4 -乙基己酸 (δ -甲基- γ -乙基己酸)
2,4 -戊二烯有酸 机化学
(3)脂肪族二元酸或多元酸:主鏈含兩羧基,稱 “某二酸”。
3 - 羧基 -3- 羥基戊二酸
有机化学
(4)脂環族和芳香族羧酸:環作為取代基
親核取代反應 親核試劑:水、醇和氨
活性:醯鹵 > 酸酐 > 酯 > 醯胺
有机化学
羧酸衍生物親核取代反應機理
❖ 親核取代反應 ❖ 不是SN1,SN2,而是親核加成—消除機理
❖活性由親核加成活性和消去活性共同決定的。 ❖活性:醯鹵 > 酸酐 > 酯> 醯胺(為什麼?)
有机化学
(補充):親核取代活性的原因
丙烯酸
HOOC-COOH 乙二酸(草酸) HOOCCH=CHCOOH
丁烯二酸
脂環族羧 酸
芳香族羧 酸
COOH
環已基甲酸 (環己烷羧酸)
COOH
苯甲酸
COOH COOH
1,2-環戊基二甲酸 (1,2-環戊烷二羧酸)
COOH
COOH
鄰苯二甲有酸机化学
(2)命名(與醛相似)
(1)簡單羧酸(可用希臘字母αβγδ標位)
(1)一元羧酸的脫羧反應較困難,低級羧酸的鈉鹽及 芳香族羧酸的鈉鹽與堿石灰(NaOH-CaO)加熱,發生 脫羧反應。(瞭解)
CH3COONa 碱石灰
CH4 + Na2CO3
(2)一元羧酸很難直接脫羧, 若α-C上連有強吸電子 基,即A= (-COOH, -CN, -C=O, -NO2, -X) 時, 加熱即可脫羧。
大学有机化学 羧酸衍生物

O CH3CNH NH2 O - + H O-C H OH, KOH CH3C O K + Br 2 2 5 95% △, Br
上页 下页 首页
第十一章 羧酸衍生物 第三节 羧酸衍生物的性质(二、化学性质)
酯在碱溶液中的水解反应机制 —— 酰氧键断裂:
O C R OR'
O C R
O-
OH
-
R'O
C
上页 下页 首页
第十一章 羧酸衍生物 第三节 羧酸衍生物的性质(二、化学性质)
一般来说,高活性的羧酸衍生物易转化为低活性的羧酸 衍生物。酰卤很容易转化为酸酐、酯和酰胺;酸酐很容易转 化为酯和酰胺;酯能转化为酰胺;而酰胺仅能被水解成羧酸。
高活性
O C Cl R O C O O C R R O C OR' R O C
L
酰基是含氧酸分子中去掉 -OH 后余下的 基团。分羧酸的酰基、磺酰基、无机含氧酸的 酰基三类。
上页 下页 首页
第十一章 羧酸衍生物
根据相应的酸命名酰基:“某酸”
“某酰基”
O S OH O
O CH3C OH
乙酸
acetic acid
O CH3C
乙酰基(acetyl)
O C
苯磺酸
O S O
O C OH
+
R-C=L
+
-Cl, Br
酰卤 酸酐 酯类 酰胺
首页
L=
-OCOR -OR
-NH2,-NHR,-NR2
上页 下页
第十一章 羧酸衍生物 第二节 羧酸衍生物的结构
O
苯甲酰氯
酰氯键
Cl
酸酐键
O O 乙酸酐 CH3-C—O—C-CH3
上页 下页 首页
第十一章 羧酸衍生物 第三节 羧酸衍生物的性质(二、化学性质)
酯在碱溶液中的水解反应机制 —— 酰氧键断裂:
O C R OR'
O C R
O-
OH
-
R'O
C
上页 下页 首页
第十一章 羧酸衍生物 第三节 羧酸衍生物的性质(二、化学性质)
一般来说,高活性的羧酸衍生物易转化为低活性的羧酸 衍生物。酰卤很容易转化为酸酐、酯和酰胺;酸酐很容易转 化为酯和酰胺;酯能转化为酰胺;而酰胺仅能被水解成羧酸。
高活性
O C Cl R O C O O C R R O C OR' R O C
L
酰基是含氧酸分子中去掉 -OH 后余下的 基团。分羧酸的酰基、磺酰基、无机含氧酸的 酰基三类。
上页 下页 首页
第十一章 羧酸衍生物
根据相应的酸命名酰基:“某酸”
“某酰基”
O S OH O
O CH3C OH
乙酸
acetic acid
O CH3C
乙酰基(acetyl)
O C
苯磺酸
O S O
O C OH
+
R-C=L
+
-Cl, Br
酰卤 酸酐 酯类 酰胺
首页
L=
-OCOR -OR
-NH2,-NHR,-NR2
上页 下页
第十一章 羧酸衍生物 第二节 羧酸衍生物的结构
O
苯甲酰氯
酰氯键
Cl
酸酐键
O O 乙酸酐 CH3-C—O—C-CH3
