初中化学各单元课标要求及思维导图
初中化学各单元知识思维导图

初中化学各单元知识思维导图物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱Na2C O3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3.10H2O;氨水NH3。
H2O;3、物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱Na2C O3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水NH3.H2O。
金属活动性1、金属活动性顺序:K>Ca〉Na>M g>Al>Zn>Fe〉Sn>P b(H)C u〉H g〉A g>Pt〉Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强.3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、C a、N a除外)。
酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐).碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:C a(OH)2(石灰水注明“澄清”的原因)、C a SO4(实验室制二氧化碳时不用稀硫酸的原因)A g2S O4(鉴别S O42—和Cl-时,不用硝酸银的原因)、M g CO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、K NO3、N aN O3、A g NO3、B aS O4不能做复分解反应的反应物。
初中化学各单元知识思维导图

初中化学各单元知识思维导图物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱N a2CO3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3.10H2O;氨水NH3。
H2O;3、物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱N a2CO3;烧碱、火碱、苛性钠N a OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水NH3。
H2O。
金属活动性1、金属活动性顺序:K〉C a〉N a〉M g〉Al>Zn〉Fe〉Sn>P b(H)C u〉H g>Ag>Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强.3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素).(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、C a、Na除外)。
酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶.2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:C a(OH)2(石灰水注明“澄清"的原因)、C a SO4(实验室制二氧化碳时不用稀硫酸的原因)A g2S O4(鉴别SO42—和C l-时,不用硝酸银的原因)、M g CO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、K NO3、N aN O3、A g NO3、B aS O4不能做复分解反应的反应物。
初中化学思维导图

第一单元走进化学世界思维导图
编辑版word
第二单元我们周围的空气思维导图
编辑版word
第三单元物质构成的奥秘思维导图
编辑版word
编辑版word
第四单元自然界的水思维导图
编辑版word
第五单元化学方程式思维导图
编辑版word
第六单元碳与碳的氧化物思维导图
编辑版word
第七单元燃料及其利用思维导图
编辑版word
第八单元金属和金属材料思维导图
编辑版word
第九单元溶液思维导图
编辑版word
编辑版word
第十单元酸和碱思维导图
编辑版word
第十一单元盐化肥思维导图
编辑版word
编辑版word
第十二单元化学与生活思维导图
编辑版word
编辑版word
编辑版word
1、征服畏惧、建立自信的最快最确实的方法,就是去做你害怕的事,直到你获得成功的经验。
2、忍别人所不能忍的痛,吃别人所别人所不能吃的苦,是为了收获得不到的收获。
就像驴子面前吊着个萝卜就会往前走。
正因为有那个目标,你才有劲儿往前走。
编辑版word
编辑版word
(此文档部分内容来源于网络,如有侵权请告知删除,文档可自行编辑修改内容,供参考,感谢您的配合和支持)
编辑版word。
最新初中化学各单元考纲要求及思维导图
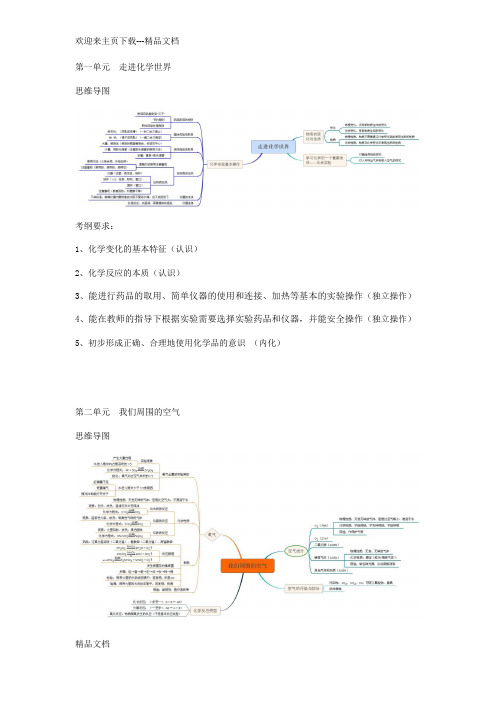
考纲要求: 1、化学变化的基本特征(认识) 2、化学反应的本质(认识) 3、能进行药品的取用、简单仪器的使用和连接、加热等基本的实验操作(独立操作) 4、能在教师的指导下根据实验需要选择实验药品和仪器,并能安全操作(独立操作) 5、初步形成正确、合理地使用化学品的意识 (内化)
第四单元 自然界的水 思文档
欢迎来主页下载---精品文档 2、硬水与软水的区别( 知道) 3、吸附、沉淀、过滤和蒸馏等净化水的常用方法 (认识) 4、水对生命活动的重大意义 (认识) 5、水是宝贵的自然资源 (认识) 6、树立保护水资源和节约用水的意识 (内化) 7、处理“三废”(废水、废气和废渣)的必要性以及处理的一般性原则 (认识) 8、典型的大气、水、土壤污染物的来源及危害 (认识) 9、化学在环境监测与环境保护中的重要作用 (认识) 10、纯净物和混合物、单质和化合物、有机化合物和无机化合物 (理解) 11、能从元素组成上认识氧化物 (认识) 12、能说出几种常见元素的化合物 (知道) 13、能用化学式表示某些常见物质的组成 (认识) 14、利用相对原子质量、相对分子质量进行物质组成的简单计算 (理解) 15、能看懂某些商品标签上标示的组成元素及其含量 (认识) 16、初步学习使用过滤、蒸发的方法对混合物进行分离 (独立操作) 17、熟记常见元素化合价,根据化合价写出常见元素化合物的化学式 (理解)
精品文档
欢迎来主页下载---精品文档 第九单元 溶液 思维导图
考纲要求: 1、溶解现象 (认识) 2、溶液是由溶质和溶剂组成的 (知道) 3、水是重要的溶剂,酒精、汽油也是常见的溶剂 (知道) 4、饱和溶液和溶解度的含义 (认识) 5、溶质质量分数的简单计算( 理解) 6、配制一定溶质质量分数的溶液 (独立操作) 7、结晶现象 (知道) 8、一些常见的乳化现象 (知道) 9、溶液在生产、生活中的重要意义 (认识)
(人教版)初中化学全册思维导图(知识点版)+初中化学知识点总结
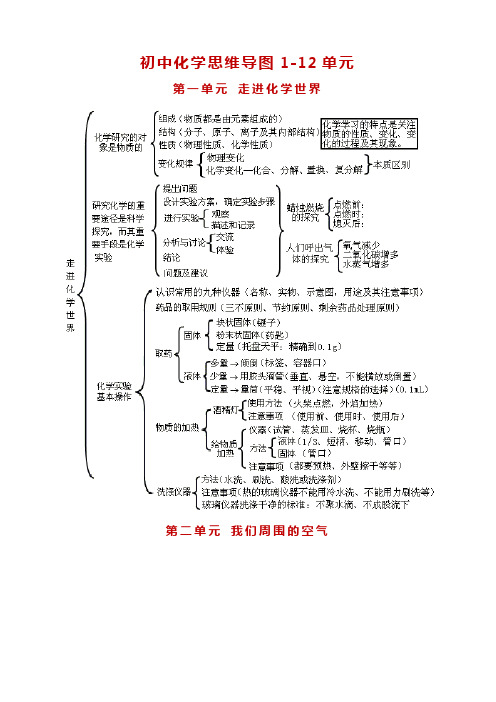
初中化学思维导图1-12单元第一单元走进化学世界第二单元我们周围的空气第三单元自然界的水第四单元物质构成的奥秘第五单元化学方程式第六单元碳和碳的氧化物第七单元燃料及其利用第八单元金属和金属材料第九单元溶液第十单元酸碱第十一单元盐化肥第十二单元化学与生活初中化学知识点总结1、单质:非惰性气体一般由两个原子组成:F2,O2,H2,Cl22、惰性气体:一般由一个原子组成:He,Ne,Ar,Kr,Xe3、化合物:氢化物居多:H2S,HCl,H3P,HF,HBr,HI(一)、固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,干冰,金刚石7、银白色固体:银,铁,镁,铝,汞等金属8、黑色固体:铁粉,木炭,氧化铜,二氧化锰,四氧化三铁,(碳黑,活性炭)9、红褐色固体:氢氧化铁10、白色固体:氯化钠,碳酸钠,氢氧化钠,氢氧化钙,碳酸钙,氧化钙,硫酸铜,五氧化二磷,氧化镁(二)、液体的颜色11、无色液体:水,双氧水12、蓝色溶液:硫酸铜溶液,氯化铜溶液,硝酸铜溶液13、浅绿色溶液:硫酸亚铁溶液,氯化亚铁溶液,硝酸亚铁溶液14、黄色溶液:硫酸铁溶液,氯化铁溶液,硝酸铁溶液15、紫红色溶液:高锰酸钾溶液16、紫色溶液:石蕊溶液(三)、气体的颜色17、红棕色气体:二氧化氮18、黄绿色气体:氯气19、无色气体:氧气,氮气,氢气,二氧化碳,一氧化碳,二氧化硫,氯化氢等气体。
(一)质量增加的1、由于吸水而增加的:氢氧化钠固体,氯化钙,氯化镁,浓硫酸;2、由于跟水反应而增加的:氧化钙、氧化钡、氧化钾、氧化钠,硫酸铜;3、由于跟二氧化碳反应而增加的:氢氧化钠,氢氧化钾,氢氧化钡,氢氧化钙;(二)质量减少的1、由于挥发而减少的:浓盐酸,浓硝酸,酒精,汽油,浓氨水;2、由于风化而减少的:碳酸钠晶体。
(一)、气体的检验1、氧气:带火星的木条放入瓶中,若木条复燃,则是氧气.2、氢气:在玻璃尖嘴点燃气体,罩一干冷小烧杯,观察杯壁是否有水滴,往烧杯中倒入澄清的石灰水,若不变浑浊,则是氢气.3、二氧化碳:通入澄清的石灰水,若变浑浊则是二氧化碳.4、氨气:湿润的紫红色石蕊试纸,若试纸变蓝,则是氨气.5、水蒸气:通过无水硫酸铜,若白色固体变蓝,则含水蒸气.(二)、离子的检验.。
初中化学各单元知识思维导图

初中化学各单元知识思维导图物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C aCO3;食盐的主要成分Na C l ;纯碱、口碱N a2C O3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4.5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水NH3。
H2O;3、物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl;纯碱、口碱N a2CO3;烧碱、火碱、苛性钠N a OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3.10H2O;氨水NH3。
H2O。
金属活动性1、金属活动性顺序:K〉C a>Na〉Mg〉Al>Z n〉F e〉S n〉P b(H)C u>Hg>A g〉Pt〉A u2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强.3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素).(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、C a、Na除外).酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐).碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:C a(O H)2(石灰水注明“澄清"的原因)、C a SO4(实验室制二氧化碳时不用稀硫酸的原因)A g2S O4(鉴别SO42—和C l—时,不用硝酸银的原因)、M g CO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、K NO3、N aN O3、A g NO3、B aS O4不能做复分解反应的反应物.溶液的酸碱性与酸碱度的测定1、指示剂———溶液的酸碱性紫色的石蕊试液遇酸性溶液变红;遇碱性溶液变蓝无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作用;碱性溶液不一定是碱的溶液(特例:碳酸钠的水溶液显碱性)2、p H值-—-溶液的酸碱度:pH<7溶液为酸性(越小酸性越强);pH=7溶液为中性;pH〉7溶液为碱性(越大碱性越强)离子的检验C l-(在溶液中)---在被测溶液中加入硝酸银溶液,如果生成不溶于硝酸的白色沉淀,则原被测液中含氯离子.S O42—(在溶液中)—--在被测溶液中加入氯化钡(或硝酸钡、或氢氧化钡)溶液,如果生成不溶于硝酸(或盐酸)的白色沉淀,则原被测液中含硫酸根离子。
初中化学思维导图
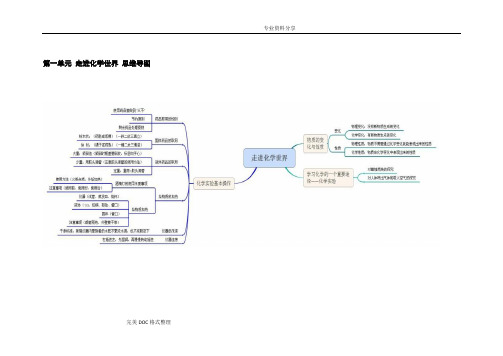
第一单元走进化学世界思维导图
完美DOC格式整理
第二单元我们周围的空气思维导图
完美DOC格式整理
第三单元物质构成的奥秘思维导图
完美DOC格式整理
完美DOC格式整理
第四单元自然界的水思维导图
完美DOC格式整理
第五单元化学方程式思维导图
完美DOC格式整理
第六单元碳与碳的氧化物思维导图
完美DOC格式整理
第七单元燃料及其利用思维导图
完美DOC格式整理
第八单元金属和金属材料思维导图
完美DOC格式整理
第九单元溶液思维导图
完美DOC格式整理
完美DOC格式整理
完美DOC 格式整理
第十单元 酸和碱 思维导图
第十一单元盐化肥思维导图
完美DOC格式整理
完美DOC格式整理
第十二单元化学与生活思维导图
完美DOC格式整理
完美DOC格式整理。
初中化学思维导图(精讲版)

第一单元走进化学世界a 学研究的领域:①制造新物质②合成新药物③开发新能源④防止环境污染。
「物理变化:没有生成其他物质的变化。
如:水的沸腾、汽物质的1油挥发、铁水铸成锅、湿衣服晾干。
变化]化学变化:生成其他物质的变化。
如:燃烧反应、铁生、锈、酒的酿制、食物腐败。
'物理性质:物质不需要发生化学变化就表现出来的性质。
如: 物质的 <色、态、味、沸点、熔点、硬度、密度、导电性、导热性。
性京 I 化学性质:物质在化学变化中表现出来的性质。
如:可燃【性、助燃性、氧化性、还原性、酸碱性、稳定性、毒性。
保存:广口瓶固体,取用:药匙、纸槽(粉末状)<一斜二送三直立〉 镶子(块状、金属颗粒)<一横二放三直立)〃保存:细口瓶取用:量多f 倾倒(瓶塞、瓶口、标签)量少一►胶头(垂直、悬空、不能横放或倒置) 定量一量简(平视)7吏用方法:火柴点燃,外焰加热。
注意事项:绝对禁止向燃着的酒精灯里添加酒精, 以免失火;绝对禁止用酒精灯引燃另一只酒精灯; 、用完酒精灯后,必须用灯帽盖灭,不可用嘴吹。
可直接加热的:试管、蒸发皿、燃烧匙 可间接加热的:烧杯、烧瓶方法:保持试管干燥,先预热再用酒精灯的外焰均 匀加热,试管口不可对着人。
液体体积不超过试管<容积的1/3o仪器干净的标准:玻璃仪器内壁附着的水既不聚成水滴,也不成股 、流下。
物质的 变化和《 性质走进化学世界化学是 一门以 实验为《 基础的 科学蜡烛燃 烧的探< 究’点燃前:白色固体,略有气味,质软,不溶于水,密度 不水小。
燃着时:石蜡熔化并发光发热,火焰分三层:外焰、内 焰、焰心,外层最明亮,里层最暗,火柒从中间到两端 逐渐变黑,烧杯内壁出现水珠,石灰水变浑浊。
I 熄灭后:产生白烟,用火柴点燃白烟,蜡烛重新被点燃。
人体呼出气体的探究:与空气中的气体相比,人体呼出的气体中含 有较多的二氧化碳和水蒸气,较少的氧气。
药品的取用规则(三不准原则、节约原则、处理原则、保护原贝D化学实 验的基 以操作仪器]给物质J 加热第二单元我们周囹的空军物理性质:无色无味的气体,密度比空气大,不易溶于水。
初中化学各单元知识思维导图

初中化学各单元知识思维导图物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱N a2CO3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水NH3.H2O;3、物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱Na2C O3;烧碱、火碱、苛性钠N a OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水NH3.H2O。
金属活动性1、金属活动性顺序:K>Ca〉Na〉Mg〉A l〉Zn>F e〉S n〉P b(H)C u>Hg>A g〉Pt>Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强.3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、C a、Na除外)。
酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪.硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐).碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:C a(O H)2(石灰水注明“澄清”的原因)、C a SO4(实验室制二氧化碳时不用稀硫酸的原因)A g2S O4(鉴别S O42-和C l—时,不用硝酸银的原因)、M g CO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、K NO3、N aN O3、A g NO3、B aS O4不能做复分解反应的反应物。
(完整版)初中化学各单元知识框架图
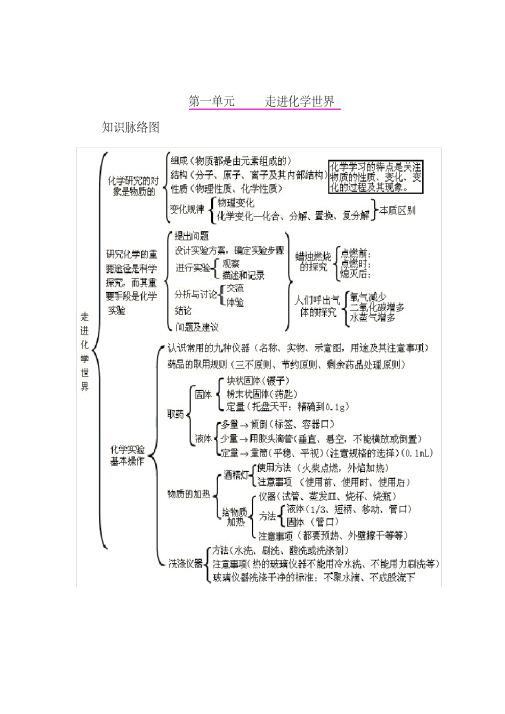
2 、溶液 ( 多为无色 ) 浅绿色溶液 ---( 亚铁盐溶液 )FeCl2
溶液、 FeSO4 溶液黄色溶液 --- ( 铁盐溶液 )FeCl3
溶液、 Fe2(SO4)3 溶液、 Fe(NO3)3
溶液蓝色溶液 ---( 铜盐溶液 )CuCl2
溶液、 CuSO4 溶液、 Cu(NO3)2 溶液蓝绿色溶液 -CuCl2
溶质的 质量分数
不饱和溶液
饱和溶液 结晶
溶解度
十、酸 碱 盐 氧化物、酸、碱和盐的知识点可以从以下十个方面掌握: 一、化学用语 1、电离方程式
H 2 SO4 2 H SO42 ; NaOH Na OH ; Al 2 ( SO4 ) 3 2Al 3 3SO42
2、物质的俗称和主要成分生石灰 ??CaO熟石灰、消石灰、 石灰水的主要成分 ??Ca(OH)2石灰石、大理石 ??CaCO3食盐的主 要成分 ??NaCl 纯碱、口碱 ??Na2CO3烧碱、火碱、苛性钠 ??NaOH 胆矾、蓝矾 ??CuSO4.5H2O碳酸钠晶体 ??Na2CO3.10H2O氨 水 ??NH3.H2O
(2) 碱能与酸性氧化物反应生成盐和水 (3) 碱能与酸反应生成盐和水 (4) 某些碱能与某些盐反应生成新的盐和新的碱 3、盐的性质 (1) 某些盐能与较活泼的金属反应生成新的盐和金属 (2) 某些盐能与酸反应生成新的盐和新的酸 (3) 某些盐能与某些碱反应生成新的盐和新的碱 (4) 有些不同的盐之间能反应生成两种新的盐
六、溶液的酸碱性与酸碱度的测定 1、指示剂 --- 溶液的酸碱性紫色的石蕊试液遇酸性溶液变 红;遇碱性溶液变蓝 无色的酚酞试液只遇碱溶液变红注:不溶性碱与指示剂无作 用碱性溶液不一定是碱的溶液 ( 特例:碳酸钠的水溶液显碱性 ) 2、pH值 --- 溶液的酸碱度 pH>7溶液为酸性 ( 越小酸性越 强)pH=7 溶液为中性 pH<7溶液为碱性 ( 越大碱性越强 ) 七、离子的检验 Cl-( 在溶液中 )--- 在被测溶液中加入硝酸银溶液 , 如果生成 不溶于硝酸的白色沉淀,则原被测液中含氯离子。 SO42-(在溶液中 )--- 在被测溶液中加入氯化钡 ( 或硝酸钡、 或氢氧化钡 ) 溶液,如果生成不溶于硝酸 ( 或盐酸 ) 的白色沉淀, 则原被测液中含硫酸根离子。 CO32-(1)( 固体或溶液 )--- 在被测物质中加入稀酸溶液,如 果产生能使澄清石灰水变浑浊的气体,则原被测物质中含碳酸 根离子。
初中化学各单元知识思维导图

初中化学各单元知识思维导图物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(OH)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱Na2C O3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4.5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水N H3.H2O;3、物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱N a2CO3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水N H3.H2O。
金属活动性1、金属活动性顺序:K>Ca〉Na〉Mg>A l〉Zn>F e>Sn〉P b(H)Cu〉H g〉Ag〉Pt>A u2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、C a、N a除外)。
酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:C a(OH)2(石灰水注明“澄清”的原因)、C a SO4(实验室制二氧化碳时不用稀硫酸的原因)A g2S O4(鉴别S O42—和Cl—时,不用硝酸银的原因)、M g CO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、K NO3、N aN O3、A g NO3、B aS O4不能做复分解反应的反应物。
初中化学各单元知识思维导图

初中化学各单元知识思维导图物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl ;纯碱、口碱N a2CO3;烧碱、火碱、苛性钠Na OH;胆矾、蓝矾Cu SO4.5H2O;碳酸钠晶体Na2C O3.10H2O;氨水NH3。
H2O;3、物质的俗称和主要成分:生石灰Ca O;熟石灰、消石灰、石灰水的主要成分Ca(O H)2;石灰石、大理石C a CO3;食盐的主要成分Na Cl;纯碱、口碱Na2C O3;烧碱、火碱、苛性钠N a OH;胆矾、蓝矾Cu SO4。
5H2O;碳酸钠晶体Na2C O3。
10H2O;氨水NH3.H2O.金属活动性1、金属活动性顺序:K〉C a〉N a〉M g>Al>Z n〉F e>Sn〉Pb(H)C u>Hg>A g〉P t〉Au2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素).(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、C a、N a除外).酸、碱、盐的溶解性1、常见盐与碱的溶解性:钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶.2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙、氢氧化镁、氢氧化铜、氢氧化铁3、四微溶物:C a(OH)2(石灰水注明“澄清”的原因)、C a SO4(实验室制二氧化碳时不用稀硫酸的原因)A g2S O4(鉴别SO42—和C l—时,不用硝酸银的原因)、M g CO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:氢氧化银、碳酸铝、碳酸铁复分解反应发生的条件反应有气体、水或沉淀生成(即有不在溶液中存在或在水溶液中不易电离的物质)1、不溶性碱只能与酸性发生中和反应;2、不溶性盐,只有碳酸盐能与酸反应;3、K NO3、N aN O3、A g NO3、B aS O4不能做复分解反应的反应物。
初中化学全册思维导图
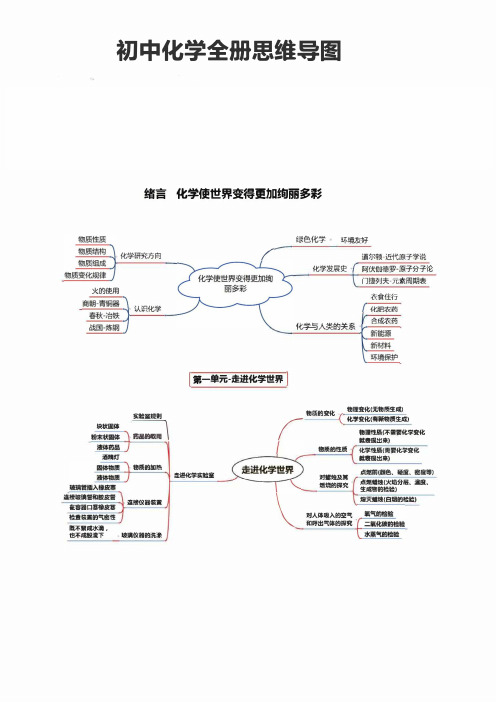
初中化学全册思维导图火的使用块状固体酒精灯连接玻璃宦和胶皮琶在容器口塞橡皮宴检查装重的气密性既不聚成水滴,也不成股流下“绪言化学使世界变得更加绚丽多彩绿色化学环境友好{-!'; 学研究方向/ 道尔顿近代原子学说认识化学:::l心崔押啊物质的加热连接仪器装盂玻璃仪罹的洗涤1第一单元-走进化学世界I化学发展史。
(阿伏伽德罗-原子分子论化学与人类的关系<I门捷列夫-元素周期表衣食住行合成农药物质的变化物理变化(无物质生成)r c归__妇物理性质吓需要化学变化就表现出来)物质的性质化学性质(需要化学变化就表现出来)走进化学实脸室对蜡烛及其点燃前(颜色、硬度、密度等)燃烧的探究点燃蠕烛(火焰分层.温度、\ 生成物的检验)熄灭蟠烛(臼烟的检迄)对人体吸入的空气和呼出气体的探究组成人体蛋臼质尿素、水、二氧化碳和能量水、二氧化碳水解生成和能量蒲萄糖淀粉人体供能的60-70%固态一脂肪;液态油水、二氧化碳和能量• 甘油和脂肪酸,油脂人体供能的20-25%胡萝卜、动物肝脏夜盲症.. VA缺乏蔬菜水果坏血病。
v c缺乏一氧化碳、二氧化碳、碳酸钙、高猛酸钾等·无机化合物甲烧乙醇、磕酸、蛋白质、油尽维生素等六大基本詈养素第十二单元化学与生活骨质疏松、钙骨骼·侚搂膺(奶、豆类虾皮钠钾,水分和pH贫血铁/'肝脏芹菜,瘦肉、蛋锌发育不良—勺肝脏甲状腺肿大、呆小症旦{海产品、加磺盐引起憩症、硒·表皮角质化氝·产生祸(qu)齿热塑性塑料、塑料·热固性塑料有机合成材料濠纶、锦纶等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一单元走进化学世界
思维导图
考纲要求:
1、化学变化的基本特征(认识)
2、化学反应的本质(认识)
3、能进行药品的取用、简单仪器的使用和连接、加热等基本的实验操作(独立操作)
4、能在教师的指导下根据实验需要选择实验药品和仪器,并能安全操作(独立操作)
5、初步形成正确、合理地使用化学品的意识(内化)
第二单元我们周围的空气
思维导图
考纲要求:
1、空气的主要成分(知道)
2、空气对人类生活的重要作用(认识)
3、氧气能跟许多物质发生氧化反应(知道)
4、结合实例说明氧气的主要性质和用途(理解)
5、氧气的实验室制取方法(模仿操作)
6、自然界中的氧循环(认识)
7、催化剂对化学反应的重要作用(知道)
8、常见的化合反应、分解反应、置换反应和复分解反应(认识)
9、利用常见的化合反应、分解反应、置换反应和复分解反应解释日常生活中的一些化学现象(理解)
10、典型的大气、水、土壤污染物的来源及危害(认识)
11、化学在环境监测与环境保护中的重要作用(认识)
12、初步形成“在一定条件下物质可以转化”的观点(内化)
第三单元物质构成的奥秘
思维导图
考纲要求:
1、物质的微粒性(认识)
2、分子、原子、离子等都是构成物质的微粒(知道)
3、能用微粒的观点解释某些常见的现象(理解)
4、原子是由原子核和核外电子构成的(知道)
5、原子可以结合成分子、同一元素的原子和离子可以互相转化(知道)
6、核外电子在化学反应中的作用(认识)
7、氢、碳、氧、氮等与人类关系密切的常见元素(认识)
8、一些常见元素的名称和符号(理解)
9、元素的简单分类(知道)
10、能根据原子序数在元素周期表中找到指定的元素(知道)
11、形成“化学变化过程中元素不变”的观念(内化)
第四单元自然界的水
思维导图
考纲要求:
1、水的组成(认识)
2、硬水与软水的区别(知道)
3、吸附、沉淀、过滤和蒸馏等净化水的常用方法(认识)
4、水对生命活动的重大意义(认识)
5、水是宝贵的自然资源(认识)
6、树立保护水资源和节约用水的意识(内化)
7、处理“三废”(废水、废气和废渣)的必要性以及处理的一般性原则(认识)
8、典型的大气、水、土壤污染物的来源及危害(认识)
9、化学在环境监测与环境保护中的重要作用(认识)
10、纯净物和混合物、单质和化合物、有机化合物和无机化合物(理解)
11、能从元素组成上认识氧化物(认识)
12、能说出几种常见元素的化合物(知道)
13、能用化学式表示某些常见物质的组成(认识)
14、利用相对原子质量、相对分子质量进行物质组成的简单计算(理解)
15、能看懂某些商品标签上标示的组成元素及其含量(认识)
16、初步学习使用过滤、蒸发的方法对混合物进行分离(独立操作)
17、熟记常见元素化合价,根据化合价写出常见元素化合物的化学式(理解)
第五单元化学方程式
思维导图
考纲要求:
1、质量守恒定律(认识)
2、说明化学反应中的质量关系(理解)
3、正确书写简单的化学反应方程式(理解)
4、根据化学反应方程式进行简单的计算(理解)
5、定量研究对化学科学发展的重大作用(认识)
思维导图
考纲要求:
1、结合实例说明二氧化碳的主要性质和用途(理解)
2、二氧化碳的实验室制取方法(模仿操作)
3、自然界中的碳循环(认识)
第七单元燃烧及其利用
思维导图
考纲要求:
1、物质发生化学变化时伴随有能量变化(知道)
2、通过化学反应实现能量转化的重要性(认识)
3、燃料完全燃烧的重要性(认识)
4、使用氢气、天然气(或沼气)、液化石油气、酒精、汽油和煤等燃料对环境的影响(认识)
5、选择对环境污染较小的燃料(认识)
6、燃烧、缓慢氧化和爆炸发生的条件(认识)
7、防火灭火、防范爆炸的措施(认识)
8、化石燃料(煤、石油、天然气)是人类社会重要的自然资源(知道)
9、海洋中蕴藏着丰富的资源(认识)
10、石油是由多种有机物组成的混合物(知道)
11、石油通过炼制可以得到液化石油气、汽油、煤油等产品(认识)
12、我国能源与资源短缺的国情(认识)
13、资源综合利用和新能源开发的重要意义(认识)
14、化学在环境监测与环境保护中的重要作用(认识)
15、燃烧的条件(独立操作)
思维导图
考纲要求:
1、金属的物理特征(认识)
2、常见金属的主要化学性质(认识)
3、防止金属腐蚀的简单方法(认识)
4、一些常见金属(铁、铝等)矿物(知道)
5、可用铁矿石炼铁(知道)
6、在金属中加入其他元素可以改变金属材料的性能(知道)
7、生铁和钢等重要的合金(知道)
8、金属材料在生产、生活和社会发展中的重要作用(认识)
9、废弃金属对环境的影响和回收金属的重要性(认识)
10、常见的化合反应、分解反应、置换反应和复分解反应(认识)
11、利用常见的化合反应、分解反应、置换反应和复分解反应解释日常生活中的一些化学现象(理解)
12、用金属活动顺序对有关置换反应进行判断(理解)
13、用金属活动顺序解释日常生活中的一些化学现象(理解)
第九单元溶液
思维导图
考纲要求:
1、溶解现象(认识)
2、溶液是由溶质和溶剂组成的(知道)
3、水是重要的溶剂,酒精、汽油也是常见的溶剂(知道)
4、饱和溶液和溶解度的含义(认识)
5、溶质质量分数的简单计算(理解)
6、配制一定溶质质量分数的溶液(独立操作)
7、结晶现象(知道)
8、一些常见的乳化现象(知道)
9、溶液在生产、生活中的重要意义(认识)
第十单元常见的酸和碱
思维导图
考纲要求:
1、常见酸碱的主要性质和用途(认识)
2、酸碱的腐蚀性(知道)
3、常见酸碱溶液的稀释方法(独立操作)
4、用酸碱指示剂(酚酞、石蕊)和pH试纸检验溶液酸碱性的方法(独立操作)
5、酸碱性对人体健康和农作物生长的影响(知道)
6、溶液酸碱性的检验(独立操作)
7、酸、碱的化学性质(独立操作)
第十一单元盐化肥
思维导图
考纲要求:
1、食盐、纯碱、小苏打、碳酸钙等盐在日常生活中的用途(认识)
2、一些常用化肥的名称和作用(知道)
3、常见的化合反应、分解反应、置换反应和复分解反应(认识)
4、利用常见的化合反应、分解反应、置换反应和复分解反应解释日常生活中的一些化学现象(理解)
5、合理使用化肥、农药对保护环境的重要意义(认识)
6、粗盐中难溶性杂质的去除(独立操作)
第十二单元化学与生活
思维导图
考纲要求:
1、生活中一些常见的有机物(知道)
2、有机物对人类生活的重要性(认识)
3、常见的合成纤维、塑料、合成橡胶及其应用(知道)
4、使用合成材料对人和环境的影响(认识)
5、新材料的开发与社会发展的密切关系(认识)
6、某些元素(如:钙、锌、铁等)元素对人体健康的重要作用(认识)
7、一些对生命活动具有意义的有机物(如:葡萄糖、淀粉、油脂、蛋白质、维生素等)(知道)
8、某些物质(如:一氧化碳、甲醛、黄曲霉素等)对人体健康的影响(知道)
9、掌握化学知识能帮助人们提高自我保护意识(认识)
10、化学科学发展在帮助人类营养保健与战胜疾病方面的重大贡献(认识)
11、化学在环境监测与环境保护中的重要作用(认识)
12、无机化合物可以分成氧化物、酸、碱、盐(知道)。
