南京航空航天大学考研历年真题之813无机化学2002--2015年真题
南京航空航天大学2015年《811普通物理》考研专业课真题试卷

16. 两偏振片的偏振化方向成 600 角, 自然光透射过两偏振片, 如偏振片的偏振化方向有 10%
的吸收,则透射光与入射光强度之比为(16) 。
科目代码:811 科目名称:普通物理 第 2 页 共 4 页
二、计算题(每题 10 分,共 70 分) 17. 长为 l,质量为 m 的均质细杆 AB 悬挂于 A 点,且可绕过 A 点的 定轴在竖直平面内自由转动,一块质量也为 m 的油灰以水平速度打 在静止杆下端 B 点,并粘在一起。要使细杆能绕 A 转圈,求油灰碰
南京航空航天大学 2015 年硕士研究生入学考试初试试题
科目代码: 科目名称: 811 普通物理
A卷
分
满分: 150
注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无
效;③本试题纸须随答题纸一起装入试题袋中交回!
一、填空题(每题 5 分,共 80 分) 1. 一物体质量为 m,从地球表面高度为 H 处由静止下落,受空气的阻力 f=kυ2(k 为大于 零的常数) ,则物体落到地面瞬间的速率 (1) 。 (设重力加速度 g 为已知)
θ
mq
第 8 题图
9. 如图所示,有一接地导体球,半径为 R,距球心为 d 处有一
点电荷 Q。则导体球面上的感应电荷的电量是(9) 。
R d 第 9 题图
Q •
10.一半径为 R1 的金属球带有正电荷 Q ,球外包围着一层同心的相对电容率(相对介电常
数)为 ε r 的均匀电介质球壳层,其内半径为 R1 ,外半径为 R2 ,在电介质内有一点 a 距离 球心距离为 ra (ra < R2 ) ,则 a 点的电势为(10) 。 (设真空电容率ε0 为已知) 11. 真空中有电荷线密度为λ、半径为 R 的均匀带电圆环,则当圆环绕过圆心且与圆环平面 垂直的轴以角速度ω转动时,运动电荷在环心处产生的磁感应强度的大小为(11) 。 (设 真空磁导率率µ0 为已知)
南京航空航天大学2015年硕士研究生入学考试初试试题A卷

南京航空航天⼤学2015年硕⼠研究⽣⼊学考试初试试题A 卷南京航空航天⼤学2015年硕⼠研究⽣⼊学考试初试试题 A卷科⽬代码:830满分:150 分科⽬名称:⾦属材料学注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均⽆效;③本试题纸须随答题纸⼀起装⼊试题袋中交回!⼀、名词解释(20分,每个5分)1. α-Fe与α-Ti2. 渗碳体与合⾦渗碳体3. 第⼀类回⽕脆性和第⼆类回⽕脆性4. 孕育处理与球化处理⼆、填空题(20分,每空1分)1. 在⼀般钢中,要严格控制杂质元素S、P的含量,其中硫只能溶于钢液中,在固态铁中⼏乎不能溶解,⽽是以的形式存于固态钢中。
在热加⼯时容易导致开裂,这种现象叫。
2. 合⾦钢按⽤途可分为、及三⼤类。
⼤多数合⾦元素溶于奥⽒体后,能增加的稳定性,能使C曲线位置,减⼩了钢的,提⾼了钢的。
3. 过冷奥⽒体等温转变动⼒学曲线是表⽰不同温度下与关系的曲线。
共析碳钢的连续冷却转变只发⽣转变和转变,不发⽣转变。
4. 贝⽒体转变产物由铁素体(α相)与组成的两相机械混合物;贝⽒体中铁素体的碳含量⼀般也是过饱和的,随着贝⽒体形成温度的,铁素体中碳的过饱和程度。
5. 按腐蚀机理的不同,⾦属腐蚀可分为和两种,其中腐蚀危害更⼤。
三、选择题(20分,每个1分)1. 在钢内部形成细⼩的裂纹,⼜称⽩点的元素是(a)P (b)N (c)S (d)H2.⾦属材料学科中,Q275表⽰(a)球墨铸铁,强度为275MPa (b)球墨铸铁,含碳量为2.75%(c)含碳量为0.275%的⼯程结构钢(d)屈服强度为275 MPa的⼯程结构钢3. 下⾯哪⼀组合⾦元素提⾼了Ms温度?(a)C和Ti (b)Ni和V (c)Mn 和W (d)Co和Al4. 引起⾼温回⽕脆性的主要原因是(a)含碳量太⾼(b)温度太⾼引起晶粒长⼤⽽引起的脆性(c)在⾼温区保温时间太长引起的脆性(d)钢中杂质元素磷、锡、锑等在原奥⽒体晶界的平衡偏聚引起的晶界脆化5. 20CrMnTi钢中Ti元素的主要作⽤是(a)提⾼淬透性(b)防⽌晶间腐蚀(c)强化铁素体(d)细化晶粒6. 抗腐蚀性能最差的不锈钢钢种是(a)马⽒体(b)铁素体(c)奥⽒体(d)奥⽒体-马⽒体型7. 下列适⽤于氮化处理以提⾼表⾯硬度的钢种是(a)45 (b)40Mn (c)35CrMo (d)30SiMn8. 可⽤于制造⼤型重要渗碳齿轮,如航空发动机齿轮的渗碳合⾦钢是(a)20Mn2 (b)20CrMnTi (c)18Cr2Ni4WA (d)20SiMnVB9. 低合⾦⾼强度钢的耐⼤⽓腐蚀性能随合⾦元素的种类和含量⽽改变。
无机化学2017年南京航空航天大学硕士研究生考试真题

南京航空航天大学2017年硕士研究生入学考试初试试题(A卷)科目代码:813满分:150 分科目名称:无机化学注意:①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无效;③本试题纸须随答题纸一起装入试题袋中交回!一、判断题(填写√或╳,20分)1. 隔离系统的热力学能恒定不变。
()2. 温度不变时,系统既不吸热也不放热。
()3. 冰在室温下自动溶化成水,是熵增起了主要作用。
()4. H2S溶液中,c(H+) = 2 c(s2-) ()5. 在氧化还原反应中,若两个电对的θE值相关越大,则反应进行得越快。
()6. 共价键的键长等于成键原子共价半径之和。
()7. 离子晶体具有脆性,是由于阳离子和阴离子交替排列,不能错位的缘故。
()8. I-可被F e3+氧化,但加入F-后就不被Fe3+氧化。
()9. 用浓氨水可检测氯气管道是否漏气。
()10. 加热CuCl2・2H2O时得不到无水的CuCl2。
()11. 焊接金属时,常用浓ZnCl2溶液处理金属表面。
()12. 镧系元素的原子核都是稳定的,锕系都是放射性的。
()13. 日常生活中,衣服上沾的铁锈可用高锰酸钾清洗。
()14. Cr2(SO4)3和Na2S溶液反应的主要产物是Cr(OH)3和H2S。
()15. 氨和空气的混合物在800 o C下通过铂铑丝网后,其主要产物为NO2。
()16. 溶液与沉淀分离的方法常用过滤法、离心分离法、蒸发法。
()17. 实验室常用的干燥剂变色硅胶失效后呈现红色。
()18. 白色的NH4VO3加热后变成棕色,是因为生成了V2O5。
()19. PCl4+的空间构型是正八面体。
()20. Fe(OH)3、Al(OH)3、Cr(OH)3均是难溶的氢氧化物,分离它们必须利用它们的溶解性和氧化还原性。
()二、填空题(20分)1. 滴定时如酸溶液滴在锥形瓶内壁上,应用少量蒸馏水把酸溶液洗下,否则会导致实验结果 。
无机化学2013年南京航空航天大学硕士研究生考试真题

南京航空航天大学2013年硕士研究生入学考试初试试题A 卷科目代码: 813科目名称:无机化学满分: 150分注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无效;③本试题纸须随答题纸一起装入试题袋中交回!一、填空题(共20分,每空0.5分)1. 已知反应 2N 2O 5(g)4NO 2(g)+ O 2(g)的m r H ∆﹤0,则增加总压反应速率_____,平衡移动方向 ________,升高温度反应速率_____。
2. 对于电极反应Cr 2O 72- + 14H + + 6e = 2Cr 3+ + 7H 2O ,其他条件不变,随着氢离子浓度的降低,Cr 2O 72-的氧化性将 (增强,减弱,不变)。
3. 在配合物[CoCl 2(en)2]Cl 中,形成体是________,其配位原子是________,配位数是______,配位化合物应该读作________________。
4. 实验测得[Cr(NH 3)6]3+配离子的磁矩为 3.9 B.M.,则该配合的空间构型为______,属于____型配合物(填内轨或外轨),中心离子的杂化类型为_____。
5. 最难溶的硫化物是____,它可溶于_____和_____。
6. 已知 Mn 的元素电势图如下图所示:Mn Mn Mn MnO MnO MnO V V V V V ⎯⎯→⎯⎯⎯→⎯⎯⎯→⎯⎯⎯→⎯⎯⎯→⎯−+++++−+−18.1250.1396.0227.22456.04从该电势图判断在水中可以稳定存在的离子是 和 。
7. 用H 2O 2溶液漂白已变黑的古画,其原理是(化学方程式) 。
8. 三氯化铁蒸汽中含有的分子化学式为 ,其结构与金属 的氯化物相似。
9. 在AgNO 3溶液中,加入K 2CrO 4溶液,生成 色的 沉淀,将该沉淀加入氨水生成 ,再加入KBr 溶液,生成 色的 沉淀,将沉淀加入Na 2S 2O 3溶液,有 配离子生成。
2014年南京航空航天大学813无机化学考研初试真题(A卷)

南京航空航天大学2014年硕士研究生入学考试初试试题A 卷 科目代码813 科目名称无机化学 满分150 分注意:①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无效;③本试题纸须随答题纸一起装入试题袋中交回!一、填空题(共20分,每空0.5分)1. 某反应的速率常数为0.462 min -1,其初始浓度为1.00 × 10-3 mol·L -1,反应的半衰期为 。
2. 如题例反应)()(2/1)(222l O H g O g H =+在298.15 K 温度下,Q p 和Q v 的数值差为 kJ·mol -1。
3. 已知氯仿(三氯甲烷)的\m vap H ∆= 29.4 kJ·mol -1,沸点为61℃,则氯仿的\m vap S ∆为 J·mol -1·K -1。
4. 有下列几种物种:I −、NH 3·H 2O 、CN −和 S 2-(1) 当________________存在时,Ag + 的氧化能力最强;(2) 当________________存在时,Ag 的还原能力最强。
(1710518)(−×=AgI K sp θ50210696)(−×=S Ag K sp θ721011)((×=+NH Ag K θ稳2121031)((×=−CN Ag K θ稳 )5. 根据酸碱质子理论,硫酸在水中的酸性比它在醋酸中的酸性________;氢氟酸在液态醋酸中的酸性比它在液氨中的酸性____________;氨在水中的碱性比它在氢氟酸中的碱性________;相同浓度的高氯酸和硝酸在水中的酸性实际无法比较,这是因为存在____________________效应。
6. 反应2A + B 2D 的K p =B D p p /2,升高温度和增大压力都使平衡逆向移动,则正反应是_______ 热反应,K c 的表达式是_____________。
南京航空航天大学2013年研究生考试813无机化学真题试卷

a 南京航空航天大学2013 年硕士研究生入学考试初试试题(A 卷 )科目代码:813科目名称:无机化学满分: 150分注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无效;③本试题纸须随答题纸一起装入试题袋中交回!一、填空题(共 20 分,每空 0.5 分)1. 已知反应 2N 2O 5(g) 4NO 2(g)+ O 2(g)的∆r H m ﹤0,则增加总压反应速率,平衡移动方向,升高温度反应速率。
2. 对于电极反应 Cr 2O 72- + 14H + + 6e = 2Cr 3+ + 7H 2O ,其他条件不变,随着氢离子浓度的降低,Cr 2O 72-的氧化性将 (增强,减弱,不变)。
3. 在配合物[CoCl 2(en)2]Cl 中,形成体是,其配位原子是 ,配位数是,配位化合物应该读作。
4. 实验测得[Cr(NH 3)6]3+配离子的磁矩为 3.9 B.M.,则该配合的空间构型为,属于型配合物(填内轨或外轨),中心离子的杂化类型为。
5. 最难溶的硫化物是,它可溶于和。
6.已知 Mn 的元素电势图如下图所示:MnO - ↓+↓0.5↓6V → MnO 2- ↓+↓2.2↓7V→MnO↓+↓0.9↓6V → Mn 3+ ↓+↓1.5↓0V → Mn 2+ ↓-↓1.1↓8V→ Mn442从该电势图判断在水中可以稳定存在的离子是 和 。
7. 用 H 2O 2 溶液漂白已变黑的古画,其原理是(化学方程式)。
8. 三氯化铁蒸汽中含有的分子化学式为 ,其结构与金属的氯化物相似。
9.在 AgNO 3 溶液中,加入 K 2CrO 4 溶液,生成 色的 沉淀,将该沉淀加入氨水生成,再加入 KBr 溶液,生成色的 沉淀,将沉淀加入 Na 2S 2O 3 溶液,有 配离子生成。
10. 写出下列物质的化学组成式:海波,原硅酸,硼砂,立德粉,碳酸羟铜。
11. 已知 A(g)→B(g)+D(g)为一级反应,在 400℃时,经过三小时有 20%分解,在 900℃时反应的 t 1/2 为 9 秒,这个反应的活化能 kJ·mol -1。
专业技法与理论2015年南京航空航天大学硕士研究生考试真题

科目代码:995科目名称:专业技法与理论 第1页 共1页 南京航空航天大学
2015年硕士研究生入学考试初试试题
A 卷 科目代码: 995 科目名称: 专业技法与理论 满分: 150 分 注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无
效;③本试题纸须随答题纸一起装入试题袋中交回!
美术史论综合部分(50分)
一、简述题(30分,每题10分,所有方向考生必答)
1、新造型主义或风格派
2、用明暗表现形体
3、清初“四王”山水是指那四位画家?并简述其绘画特色及影响。
二、论述题(20分,2题任选其1)
1、《开国大典》——“油画民族论”的创作观念及审美追求
2、试论颜真卿作为与王羲之相提并论的大书家其在楷书、行草书上的艺
术成就及其在历史上对后世书家的影响
专业技法部分(100分)
一、默画室外有人物的场景画(100分,默画有两个以上人物组合的有室外场
景的单色画一幅。
限定为01油画创作、03数字媒体美术图形图象、04壁画创作、05素描造型技法、06中国画创作方向考生的考题)
二、书法专业理论(100分,不得少于1500字,限定为02书法创作方向考生
的考题)
根据你对当前书法界个方面情况的了解,请论证一下你心目中最理想的书法家应该具备哪些修养、能力?
梦想不会辜负每一个努力的人。
2015-2018年南京航空航天大学考研试题813无机化学

其原因是为了增大液体压力。 11. 在实验操作中,蒸发皿和启普发生器都可以用来加热液体。 12. 用 NaOH 标准溶液滴定 HCl 溶液至终点时,酚酞变红,放置一会后红色消失,原因是
溶液吸收了空气中的 CO2,碱性减弱。 13. 实验操作中,不慎把苯酚溅到手上,应立即用 70℃以上的热水冲洗。 14. 酸度计长期不用时,复合电极应如何保存 3mol/l KCl 溶液中。 15. 在符合朗伯一比尔定律的范围内,有色物质的浓度,最大吸收波长,吸光度三者的关系
H3PO4
的
K
θ a1
=
6.7 ×10−3
K
θ a2
=
6.2 ×10−8
K
θ a3
=
4.5 ×10−13
2. 某溶液中含 Cl-和 CrO42-,它们的浓度分别是 0.10 mol·L-1 和 0.0010 mol·L-1,通过计算证
明,逐滴加入 AgNO3 试剂,哪一种沉淀先析出。当第二种沉淀析出时,第一种离子是否被
南京航空航天大学
科目代码: 科目名称:
2015 年硕士研究生入学考试初试试题ď A 卷 Đ
813 无机化学
满分: 150 分
注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无
效;③本试题纸须随答题纸一起装入试题袋中交回!
一、填空题(20 分)
1. 按 试 剂 所 含 杂 质 的 多 少 , 我 国 通 用 试 剂 纯 度 的 等 级 标 准 分 为 四 级 , 分 别 为 优 质
纯、
、
、实验试剂。
南京航空航天大学真题下载索引
钢结构理论2003 飞机性能工程2002 马克思主义哲学原理 马克思主义哲学原理 高分子材料2001 高分子材料2002 高分子物理2005 高等代数1999 高等代数2000 高等代数2001 高等代数2002 高等代数2003 高等代数2004 高等代数2005 高等教育管理学2004 高等教育管理学2005
学校 南京航空航天大学
科目及年份 CAD和CAM技术基础2001 CAD和CAM技术基础2002 世界近现代史1999 世界近现代史2000 世界近现代史2001 中国共产党党史2002 中国美术史2004 中国美术史综合-2005 中国革命史1999 中国革命史2000 中国革命史2001 中外音乐史和曲式作品分析 产品设计2004 产品设计2005 会计学2002 传热学1999 传热学2000 传热学2001 传热学2002 俄语-2005 信号与系统1999 信号与系统2000 信号与系统2001 信号与系统2002 信号系统与数字信号处理 信号系统与数字信号处理 信息检索-2004 信息资源管理基础信息资源管理基础发展经济学2002 发展经济学2003 国民经济管理学2004 国民经济管理学2005 土质土力学2002 基础英语2004 基础英语2005 基础英语2006 复变函数2002 大学物理1999(普通物理 宏观经济学-2004 宏观经济学-2005 工业工程基础2002 工业设计史2004 工程热力学1999 工程热力学2000 工程热力学2001
工程热力学2002 工程热力学2003 工程热力学2004 工程热力学2005 工程结构设计原理工程结构设计原理2004 工程结构设计原理2005 市场营销学2002 常微分方程1999 常微分方程2000 常微分方程2002 弹性力学2002 微分几何1999 微机原理及应用1997 微机原理及应用1998 微机原理及应用1999 微机原理及应用2000 微机原理及应用2001 微机原理及应用2002 微观经济学2002 微观经济学2002答案 微观经济学2003 微观经济学2003答案 微观经济学2004 微观经济学2005 思想政治教育学2005 技术经济学2004 技术经济学2005 振动基础2001 振动基础2002 操作系统2001 操作系统2002 政治学2001 政治学原理2005 政治经济学2001 教育学2004 教育学2005 数字电路1999 数字电路2000 数字电路2001 数字电路2002 数学分析-1999 数据库原理及应用2004 数据库原理及应用2005 数据结构与操作系统 数据结构与操作系统 数据结构与操作系统
南京航空航天大学-2018年-硕士研究生入学考试初试试题(A卷)-813无机化学

科目代码:813科目名称:无机化学 第1页 共3页 南京航空航天大学 2018年硕士研究生入学考试初试试题( A 卷 ) 科目代码:813 满分: 150分 科目名称: 无机化学 注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无效;③本试题纸须随答题纸一起装入试题袋中交回!一、填空题(30分)1. 镧系与锕系元素水合离子的颜色是由________引起的。
2. 根据酸碱质子理论,HNO 3的共轭酸是 ,NH 2-的共轭碱是 。
3. 硫的同素异形体中,室温稳定态是________,每个硫原子以________杂化轨道成键。
4. 按离子极化作用大小排列 FeCl 3,FeCl 2,KCl ,CaCl 2____________________________。
5. 既可以用来鉴定Fe 3+,也可以用来鉴定Co 2+的试剂是________,既可以用来鉴定Fe 3+,也可以用来鉴定Cu 2+的试剂是________。
6. 在配离子[Fe(CN)6]3-中,中心离子以d 2sp 3杂化与配体形成配位键,那么配离子的空间构型为 。
7. 溶液与沉淀分离的方法常用 、 、 。
8. 化学元素中,第一电离能最小的是 ,最大的是 。
9. 已知反应 2N 2O 5(g) 4NO 2(g)+ O 2(g)的m r H ∆﹤0,则增加总压反应速率_____,平衡移动方向________,升高温度反应速率_____。
(填增大或减小;正向或逆向)10. 在ⅢA--Ⅴ A 各族中,第四到第六周期元素最高氧化态氧化物的水合物,酸性最强的是________,碱性最强的是________。
11. 白色的NH 4VO 3加热后变成棕色,是因为生成了 。
12. 金在王水中溶解的反应方程式为 。
13. 第81号元素的离子在水中较稳定的氧化态是 ,原因是 。
14. 320o C 下,一级反应)()()(2222g Cl g SO g Cl SO +→的半衰期为s 4105.4⨯,则16.2 h 后,剩余的SO 2Cl 2的质量分数是 。
南京航空航天大学813无机化学2012-2018年考研专业课真题试卷

17. 对于电极反应 Cr2O72- + 14H+ + 7e = 2Cr3+ + 7H2O,其他条件不变,随着氢离子浓度的降低,Cr2O72-
的氧化性将
(填增强,减弱,不变)。
18. 用 H2O2 溶液漂白已变黑的古画,其原理是(化学方程式)
。
科目代码:813 科目名称:无机化学 第 1 页 共 3 页
5. 已知 E (HCN / H2 ) 0.545V ,试计算 ka (HCN) 。
6. 已知反应:
N2
g
2H
2
g
N2
H4
l
r
H
m,1
298.15K
50.63kJ
mol
1
H2
g
1 2
O2
g
H2O l
r
Hm ,2
298.15K
精都教育——全国 100000 考生的选择
我们的梦想,为成就更多人的梦想
南 京 航 空 航 天 大 学 研 究 生 入 学 考 试 试 题
原版考研真题试卷
更多考研真题、笔记、模拟、题库、讲义资料就上精都考研网 /
南京航空航天大学2018年考研专业课真题试卷(原版)
3. 试求 300 mL 0.50 mol·L-1 H3PO4 和 500 mL 0. 50 mol·L-1 NaOH 的混合溶液的 pH 值。已知 H3PO4 的 pKθa1=2.12;pKθa2=7.21;pKθa3=12.67。
4. 25℃时,晴纶纤维生产的某种溶液中,c(SO42-)为 6. 0×10-4 mol·L-1。若在 40.0 L 该溶液中,加入 0.010 mol·L-1BaCl2 溶液 10.0 L,问是否能生成 BaSO4 沉淀?如果有沉淀生成,问能生成 BaSO4 多少克?最 后溶液中 c(SO42-)是多少?已知 ksp (BaSO4 ) 1.11010
2015江苏南京航空航天大学材料科学基础考研真题

2015江苏南京航空航天大学材料科学基础考研真题一、(15 分)下图为 fcc 点阵 Cu 晶体 X 射线衍射图,图中三条峰对应的 2值分别为,已知 Cu 的晶格常数为3.615Å;布拉格公式:,其中波长λ=1.5406 Å,d 为晶面间距。
(1)三条峰对应的晶面(一般为低指数面)分别是什么?请写出具体计算分析步骤。
(2)画出其它两种具有 fcc 点阵的典型晶体结构(fcc 结构纯金属除外),并指出其结构基元。
二、(15 分)超细晶粒的制备已成为提高材料强韧性的主要手段之一。
通过凝固的快冷(即增加过冷度)是获得细晶铸件的重要方法。
已知铜的凝固温度,溶化热,比表面能,(1)试求欲在均匀形核条件下获得半径为 2nm 晶粒所需的过冷度(2)试写出其它两种可能获得细晶的方法,并说出其理由。
三、(15 分)根据 A‐B 二元相图(下图)回答:(1)写出图中的液相线、固相线、α和β相的溶解度曲线、所有两相区及三相恒温转变线(2)平衡凝固时,计算 A‐25%(wt%)合金(yy’线)凝固后初晶β相在铸锭中的相对量(3)画出上述合金的冷却曲线及室温组织示意图四、(10 分)下图所示的含 Pb 为 15%的 Sn-Sb-Pb 三元相图的垂直截面中,温度为 200℃的水平线上发生什么样的平衡反应?写出反应式。
在水平线的上方和下方各有几个三相区?写出每个三相区的组成相。
五、(20 分)根据材料的原子键合方式及结构特点回答下述问题:(1)高分子涂料在配置时一般采用分子量较低的化合物,涂覆完成后再进行固化处理,这样做的理由是什么?(2)硅酸盐晶体的断裂一般为脆性断裂,为什么?六、(12 分)柏氏矢量为的全位错可以在面心立方晶体的哪些{111}面上存在?若分解为 Shockley 分位错,试分别写出位错反应式;已知点阵常数 a=0.3nm,切变模量 G=7×,层错能γ=0.01J/m2,求扩展位错的宽度;层错能的高低对层错的形成、扩展位错的宽度和扩展位错运动有何影响?层错能对金属材料冷、热加工行为的影响如何?七、(12 分)由于钼丝的强度和韧性都比较好,不易断丝,价格低廉,被广泛用于快走丝电火花线切割领域,钼丝的常用直径为∅0.20~0.25mm。
南京航空航天大学考研历年真题之815理论力学2002--2015年真题
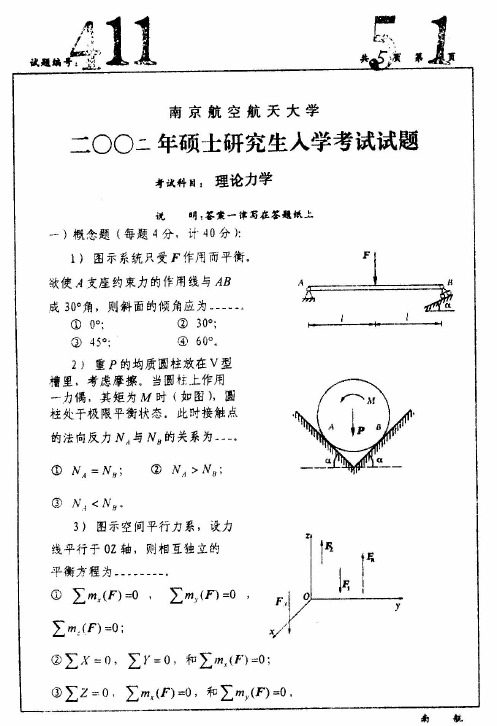
第 1 题 (25 分) 图示平面结构由杆 AEB、DC 和 BC 组成,尺寸如图,长度 a 为已知。在杆 AEB 的 AE 段受到均布载荷作用,载荷 集度为 q, 在杆 DC 上作用一力偶矩为 M 的力偶,且 M = qa2。各杆自重及各处摩 擦均不计。试求:支座 A、D 和 E 处的 约束力。 第 2 题 (15 分) 图示边长分别为 a、b、c 的长方体 受到由三个力构成的力系的作用,已知 F1 = Fi,F2 = 2Fj,F3= 3Fk, ,其中 i, j, k
A
第 4 题图
ϕ
O R r
第 5 题图
第 6 题(20 分) 如图所示,长为 l、质量为 m 的均质杆 AB,左端 A 为固定铰支座, 另一端用绳子 OB 拉住使其静止于水平位 置。已知:θ=60°,不计各处摩擦及绳子的质量。用达朗 贝尔原理求突然撤去支座 A 的瞬时: (1)杆 AB 的角加速 度; (2)绳子 OB 的拉力。 第 7 题(15 分) 在图示平面机构中,杆 CD 上作用一力偶矩为 M 的力偶,滑块 E 可在铅垂槽中运动,其上作用一铅垂 方向的力 F, AD 连线铅直。 在图示位置机构处于平衡, 此时,杆 AB 水平,AC = CB = l,角度如图,不计各 构件和滑块的自重与各处摩擦。试用虚位移原理求此 时力偶矩 M 与力 F 之间的关系。
FP G1
R C
B G2 D
第 2 题图
第 3 题 (25 分) 图示平面机构,半径为 R 的圆环 C 固定,圆心 C 与 铰链 A 连线处于铅垂位置,杆 AB 绕定轴 A 转动,小圆环 M 套在杆 AB 和大圆环 C 上,已知杆 AB 的角速度和角加 速度分别为 ω 和 α 。试用点的合成运动方法,求杆 AB 与 水平线间的夹角ϕ =60 的瞬时,小环 M 的绝对速度和绝
2012年南京航空航天大学考研试题813无机化学(试题)

南京航空航天大学2012年硕士研究生入学考试初试试题( A 卷) 科目代码: 813 科目名称: 无机化学 满分: 150 分注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无效;③本试题纸须随答题纸一起装入试题袋中交回! 一、填空题(20分)1. 根据酸碱质子理论,PO 43-的共轭酸是 ;NH 4+的共轭碱是 。
2. 已知()()()32CaCO s CaO s CO g Δ⎯⎯→+的1m(298K) 178.32r H kJ mol θ−Δ=⋅,-11m (298K) =160.6r S J mol K θ−Δ⋅⋅,则反应的分解温度为 K 。
3. 已知某化学反应的速率常数为6.29×10-41s −,则此反应为 级反应,半衰期为 s 。
4. 放热反应的E a (正) E a (逆)(填大于,小于或等于)。
5. 某封闭系统从环境吸收100 J 的热量,并对外做功200 J ,则此系统热力学能的变化为 。
6. 已知12sp 24(Ag CrO ) 1.110K θ−=×,则该温度下该物质的溶解度为 mol ·L -1。
7. 根据E θ(PbO 2/PbSO 4) >E θ(MnO 4-/Mn 2+) >E θ(Sn 4+/Sn 2+),则六种物质中还原性最强的是 。
8. 第26号元素原子的电子排布是 。
9. 根据杂化轨道理论,N 与F 形成NF 3 时,采取 杂化,其分子构型为 。
10. H 3BO 3是 元弱酸,请写出相应的化学方程式 。
11. H 2S 在充足的空气中燃烧的化学方程式为 。
813无机化学第 1 页 共 4 页12. 在酸性的K 2Cr 2O 7溶液中,加入Pb 2+离子,可生成的沉淀物质是 。
13. 某溶液和Cl -离子作用,生成白色沉淀,加氨水后变黑,则该溶液可能存在的离子是 。
14. K 4[Fe(CN)6]的系统命名是______________________,中心离子采取的杂化方式为 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3. 已知 KI 的晶格能(U)为 631.9KJ/mol,钾的升华热 S(K)为 90.0KJ/mol,钾的电离能(I)为 418.9KJ/mol,碘的升华热 S(I2)为 62.4KJ/mol,碘的离解能(D)为 151KJ/mol,碘的电子亲合 θ 能(E)为 310.5KJ/mol,求碘化钾的生成热(△fH )
θ −1 (1) 2 NH 3 ( g ) + 3 N 2O( g ) → 4 N 2 ( g ) + 3H 2O(l ) ∆ r H m ,1 = −1010kJ .mol
(2) N 2O( g ) + 3H 2 ( g ) → N 2 H 4 (l ) + H 2O(l ) 1 (3) 2 NH 3 ( g ) + O2 ( g ) → N 2 H 4 (l ) + H 2O(l ) 2 1 (4) H 2 ( g ) + O2 ( g ) → H 2O(l ) 2
θ θ 已知 K spa ( FeS ) = 6 × 10 2 , K spa (CuS ) = 6 × 10 −16
2.今有 2.00 L 的 0.500 mol/L NH3 (aq)和 2.00 L 的 0.500 mol/LHCl 溶液,若配制 pH=9.00 的缓冲溶液, 不允许再加水, 最多能配制多少升缓冲溶液?其中 c(NH3), c(NH4+)各为多少?
8. Hg 与过量稀硝酸反应的方程式为 9. 金属钠与液氨反应的方程式为 10. (NH4)2Cr2O7 受热分解的产物为
时 N2O4 的 α=50%,则反应的 K θ 为 。 。 。
11. 一密闭容器中含 1.0molN2O4,反应:N2O4(g)→2NO2(g) 在 25℃、100 kPa 下达到平衡
813 无机化学
第 1 页 共 4 页
2. 0.10 mol/L H2S 溶 液 中 S2- 的 浓 度 为
θ −19 ) Ka 2( H 2 S ) = 7.1× 10
θ −8 mol/L 。 ( 已 知 Ka , 1( H 2 S ) = 8.9 × 10
3. 命名下列配合物[Cr(OH)(H2O)5](OH)2
南京航空航天大学 2011 年硕士研究生入学考试初试试题
科目代码: 科目名称: 813 无机化学
A卷
分
满分: 150
注意: ①认真阅读答题纸上的注意事项;②所有答案必须写在答题纸上,写在本试题纸或草稿纸上均无
813 无机化学 第 2 页 共 4 页
4. 反应 HgO(s) U Hg(g)+1/2O2(g) ,于 693K 达平衡时总压为 5.16×104Pa,于 723K
达平衡时总压为 1.08×105Pa 。①求反应的
∆rHmθ。
5. 在298.15K、恒压条件下,已知下列各反应及其热效应为
。
θ 4. 已知 E θ (Zn 2+ /Zn) = −0.7621V ,则 ∆ f Gm (Zn 2+ , aq) 为
。
5. 已知某副族元素 A 原子,最后一个电子填入 3d 轨道,族号=3,请写出其核外电子排布
式 。 。 。
6. 请写出 CH3OH-H2O 之间存在的分子间力类型为
7. 已知[Fe(CN)6]3−的 µ = 2.0 B.M . ,则 Fe3+的杂化轨道类型为
效;③本试题纸须随答题纸一起装入试题袋中交回!
一、判断题(15 分) 1. 一个反应的△G 数值越负,其正反应自发进行的倾向越大,反应进行得越快。 ( ) 2. 酸碱质子理论认为: 酸是任何可以接受电子对的物种, 碱是任何可以提供电子对的物种。 ( ) 3. H3BO3 是一种一元酸,而不是三元酸。 ( ) 4. 原子形成共价键的数目,等于气态原子的未成对的电子数。 ( ) 5. 相同原子间双键的键能等于其单键键能的两倍。 ( ) 6. 在 2SO 2 (g)+O 2 (g) U 2SO3 (g) 的反应中,在一定温度和浓度的条件下,不论使用催化剂 或不是有催化剂,只要反应达到平衡时,产物的浓度总是相同的。 ( ) 7. 配位数为 5 的配合物的空间构型是四方锥。 ( ) 8. 叠氮酸根离子 N3‐是直线型离子, 除形成两个σ键外, 还形成 2 个三中心四电子键大π键。 ( ) 9. 0.10mol/L 的 HAc 溶液稀释时,解离度增大,H+离子浓度也增大。 ( ) 10. H2 + I2 反应。 ( ) 11. 磷的同素异形体常见的有白磷、 红磷、 黑磷, 其中最活泼的是白磷, 它在空气中易自燃, 应在煤油中保存。 ( ) 12. CaCO3 在常温下不分解,是因为其分解反应是吸热反应;在高温(T>1173K)下分解,是 因为此时分解放热。 ( ) 13. 对偶极矩为零的多原子分子,其组成分子的原子的电负性必定相等。 ( 面体。 ( ) 15. 配制 SnCl2 溶液,常在溶液中放入少量固体 Sn 粒,其原因是防止 Sn2+水解。 ( ) 二、填空题(15 分) 1. 已知 K spθ (Ag 2 CrO 4 ) = 1.1×10−12 ,则同温下 S (Ag 2 CrO 4 ) 为 mol/L。 ) 14. 在 CCl4、CHCl3 和 CH2Cl2 分子中,碳原子都是采用 sp3 杂化,因此这些分子都呈正四 2HI 的反应,实验测定的动力学方程表明是二级反应,因此它是一个双分子
。 。 。
12. 已知 226Ra 的半衰期为 1590 年,则此一级反应的速率常数为 13. 环境对系统做功时 W 0(填写“<、>或=”) 。
。
14. 超氧化钾常用做防毒面具的供氧剂,其反应方程式为 15. 写出 PbO2 和浓盐酸反应的方程式
三、计算题 (30 分) 1. (1)在 0.1mol/LFeCl2 溶液中,不断通入 H2S (g),若不生成 FeS 沉淀,溶液的 pH 最高不 应超过多少? (2) 在 pH 为 1.00 的某溶液中含有 FeCl2 与 CuCl2,两者的浓度均为 0.10mol/L,不断通 入 H2S (g)时,能有哪些沉淀生成?各种离子浓度分别是多少?
