计算在该温度下250g水中最多能溶解多少克碘化钾
八年级上科学溶液稀释与浓缩含问题详解

溶液计算部分重难点:1、溶质质量分数计算:与其计算公式有关的计算;有关溶质的质量分数与化学方程式联系的综合计算。
计算公式:溶质的质量分数=(溶质质量/溶液质量)×100% = [溶质质量/(溶质质量+溶剂质量]×100%2、溶液的稀释计算原则:溶液在稀释前后溶质的质量不变。
有两种情况:(1)加水法进行稀释(2)加入低浓度的同种溶质的溶液。
3、溶液的浓缩计算三种方法:(1)补充溶质使溶液浓缩(2)蒸发溶剂使溶液浓缩,蒸发溶剂时,溶液质量减少,溶质质量不变(3)加入高浓度的同种溶质的溶液进行浓缩,计算方法铜一浓一稀两种溶液的稀释。
4、有关溶质的质量分数与化学方程式联系的综合计算解题的关键是要掌握生成溶液质量的计算,方法(1)溶液组成法:溶液质量=溶质质量+溶剂质量;(2)质量守恒法:溶液质量=反应物质量总和-不溶固体或生成沉淀的质量-生成气体的质量5、溶解度与溶质质量分数的关系总结经典规律:化学计算题涉及面广,在学习的过程中不要贪多求难,应把各种典型题解剖好,理解透。
可采用下列方法:(1)要认真审题,仔细析题。
审题就是仔细阅读原题,理解题意,了解题目的特点、类型,弄清有哪些已知条件和未知条件。
审题是解题第一步,要尽力做到认真阅读全体,仔细分析题意,反复推敲关键句子。
析题就是剖析原题,即在审题的基础上对全题进行分析和解剖,应用化学知识沟通已知数和未知数,弄清它们的关系。
习题时既可以从已知数推及到未知数,也可以从未知数追溯到已知数,找出它们的内在联系。
(2)要注意解题格式规范,步骤清晰,过程简洁,答案准确。
(3)要坚持做题后总结。
(4)要不断提高解题技巧一题多解、一题多变或多题一解,以提高自己分析、思考和解答问题的能力。
注意多练和巧练相结合知识点八:计算专题一、 溶解度的计算:主要有求溶解度,根据溶解度配制饱和溶液,根据溶解度进行析出晶体的计算1、 求溶解度:例1 : 把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。
氯化钾的溶解度标准

如对您有帮助,可购买打赏,谢谢氯化钾的溶解度标准导语:我们生活的很多方方面面可能都需要用到氯化钾,氯化钾给我们生活可以提供很多的便利,但是氯化钾不能直接拿过来使用,需要把它放在水里面进我们生活的很多方方面面可能都需要用到氯化钾,氯化钾给我们生活可以提供很多的便利,但是氯化钾不能直接拿过来使用,需要把它放在水里面进行溶解,溶解后的氯化钾才能够对于我们发挥自己的作用,很多人对于氯化钾的溶解度标准还比较模糊,大家来了解一些氯化钾的溶解度标准吧。
1氯化钾在二十摄氏度时的溶解度是34.2g量取100ml水,加入34.2g氯化钾,溶解即可配置成碘化钾在二十摄氏度的时候溶解度是144g,量取100ml水,加入144g碘化钾,溶解,即可配置成的基本原料。
医药工业用作利尿剂及防治缺钾症的药物。
染料工业用于生产G盐,活性染料等。
农业上则是一种钾肥。
其肥效快,直接施用于农田,能使土壤下层水分上升,有抗旱的作用.但在盐碱地及对烟草、甘薯、甜菜等作物不宜施用。
氯化钾口感上与氯化钠相近(苦涩),也用作低钠盐或矿物质水的添加剂。
此外,还用于制造枪口或炮口的消焰剂,钢铁热处理剂,以及用于照相。
它还可用于医药,科学应用,食品加工,食盐里面也可以以部分氯化钾取代氯化钠,以降低高血压的可能性。
[6] 医学临床氯化钾是临床常用的电解质平衡调节药,临床疗效确切,广泛用于临床各科。
用于治疗和预防各种原因(进食不足、呕吐、严重腹泻、应用排钾利尿药或长期应用糖皮质刺激素和肾上腺皮质刺激素、失钾性肾病、Bartter综合症等)引起的低钾血症,亦可用于心、肾性水肿以及洋地黄等强心甙中毒引起的频发性、多源性早搏或快速心率失常。
2.掌握了氯化钾的溶解度标准我们就可以自己调配氯化钾与水的比例,可以帮助我们更好的调配比例,才不至于调配的时候加水过多或者加水多少而影响到氯化钾作用的发挥,同时我们也应该多方掌握一下氯化钾能够给我们的生活带来哪些好处。
生活知识分享。
八年级科学试题-初二科学溶解度计算训练题 最新

初二科学溶解度计算训练题A组基础训练1.20℃时,物质A的溶解度为20克,表示_ ____。
此饱和溶液中,溶质.溶剂.溶液的质量比为2. 下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
据图回答:(1)P点的含义是_______________________。
(2)t2℃时,30ga物质加入到50g水中不断搅拌,能形成80g溶液吗?__________(填写“能”或“不能”)(3)t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列是__________(填写物质序号)。
3、55g50℃的硼酸饱和溶液蒸干,得到5g硼酸固体。
求硼酸在50℃时的溶解度。
4、15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?5、t℃时,将ag某物质溶于水配成bg饱和溶液,求t℃时该物质在水中的溶解度?6、40℃时,10克水最多能溶解2g物质A,60℃时50克水最多能溶解15g物质B,问哪种物质溶解度大()A、A比B大B、A比B小C、A和B一样大D、无法比较7、已知30℃时硝酸钾的溶解度为45.8g。
在这温度时,将某硝酸钾饱和溶液蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾?8、已知20℃时硝酸铵的溶解度为192克,现在要配制此温度下的硝酸铵饱和溶液500克,需要硝酸铵和水各多少克?9、80℃时把15.8g硝酸钾溶解于50g水中形成溶液。
根据溶解度曲线(见课本)和计算说明:①此溶液是否饱和?②欲使其达到饱和,可采取哪些方法?10、在50℃,向100克水中加入90克硝酸钾,充分搅拌后所的溶液质量为多少?。
B 组 拓展提高11、在20℃时某物质的不饱和溶液50g ,平均分成两等份。
一份中加入0.7g 该物质,另一份蒸发掉5g 水,结果两份溶液都达饱和。
那么该物质在此温度下的溶解度为多少克?12、有60℃时A 物质的溶液100g ,若温度不变,蒸发掉10g 水时,有4gA 的晶体析出(不含结晶水),再蒸发掉10g 水时,又有6gA 的晶体析出,求60℃时A 物质的溶解度是多少克。
有关溶解度的计算 典型例题

有关溶解度的计算典型例题[例1]已知15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?[分析]:15℃时碘化钾的溶解度为140g,这表明在该温度下100g水最多能溶解140g碘化钾。
那么,250g水最多能溶解多少克碘化钾,可通过关系式法列比例求得,亦可用基本公式法求解。
解法1:关系式法设:15℃时,250g水里最多能溶解x克碘化钾。
关系式:m质+m剂=m液15℃时 140g 100g? x250g[解答]:15℃时,250g水最多能溶解350g碘化钾。
解法2:基本公式法已知: s=140g m剂=250g求: m质=?[解答]:解之,得:m质=350g[例2] 把20℃的282g硝酸钾饱和溶液加热,升温到60℃,需要加入多少克硝酸钾才能使溶液重新达到饱和?(已知20℃时硝酸钾的溶解度为31.6g,60℃时为110g)。
分析:溶剂量不变,当饱和溶液的温度升高时,由于溶解度的增大,使溶液由饱和变为不饱和。
如果要在高温时使溶液重新达到饱和,则需加入一定量的溶质。
所加溶质的量可用质量关系式通过比例进行计算,也可用公式法求得。
解答1 关系式法设:所需加的硝酸钾为x克。
关系式: m质+m剂=m液20℃→60℃添加量20℃ 31.6g 100g 131.6g 110g-31.6g=78.4g282gx每有131.6g硝酸钾饱和溶液从20℃升到60℃时,需要加入78.4g硝酸钾才能使溶液在60℃时亦达饱和,那么282g20℃的硝酸钾饱和溶液升温到60℃,应加入多少克硝酸钾才能使溶液重新达到饱和,可通过比例求得。
答:应加入168g硝酸钾。
解答2:公式法根据上述的比例式,可导出如下的计算公式。
设:应添加硝酸钾晶体为x克。
答:(略)[例3]已知30℃时硝酸钾的溶解度为45.8g。
在这温度时,某硝酸钾溶液500g中溶有硝酸钾137.4g。
如果蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾?分析:首先要通过计算得知这硝酸钾溶液是不是饱和溶液?根据硝酸钾在30℃时的溶解度和关系式得:由于137.4g<157.1g,可知原溶液是不饱和溶液。
溶解度 计算题

溶解度计算题A卷1.30℃时,250克水中最多能溶解ll4.5克硝酸钾,求30℃时硝酸钾的溶解度。
2.20℃时,将204克饱和食盐溶液蒸干,得到54克食盐,求20℃时食盐的溶解度。
3.已知10℃时,硝酸钾的溶解度是20.9克/l00克水。
问10℃250克水中最多能溶解多少克硝酸钾?4.已知20℃时,溴化钾的溶解度是66克/l00克水。
问20℃时,1l克溴化钾最多可以配制成多少克溴化钾饱和溶液?5.已知硝酸银在20℃时的溶解度是222克/100克水。
计算在20℃时,将0.02克硝酸银固体溶解在2毫升水中,能否配成饱和溶液?6.已知20 ℃时,硝酸钾的溶解度是7.4克/l00克水。
在20℃时,要配制150克硝酸钾饱和溶液,应将多少克硝酸钾溶解在多少克水中?B卷1.已知50 ℃时,氯化铵的溶解度约为50克/l00克水。
现有75克氯化铵固体和110克水,求在50 ℃时,最多可以配成氯化铵饱和溶液多少克?2.已知硝酸钠50℃时的溶解度是ll4克/l00克水。
在50℃时.往100克硝酸钠饱和溶液中加入50克水,问需再加入多少克硝酸钠.溶液才重新饱和?3.把l00克40℃的硝酸钾不饱和溶液分成等质量的两份,一份蒸发掉20克水仍保持40℃,恰好达到饱和状态,另一份在40 ℃时加入12.8克硝酸钾固体也恰好饱和,求40℃时硝酸钾的溶解度。
4.已知硝酸钠50℃时的溶解度是ll4克/l00克水,10℃时的溶解度是80克/l00克水。
用100克水在10℃时配制的硝酸钠饱和溶液,温度升高到50℃时,还需加入多少克硝酸钠,才能使溶液达到饱和?5.已知30℃时.氯酸钾的溶解度是l0克/l00克水。
现在30℃时.将500克氯酸钾饱和溶液蒸发去75克水,再冷却到30℃,有多少克氯酸钾析出?6.t℃时某溶液250克,蒸发掉20克水后,析出晶体8克,又蒸发掉20克水,析出晶体12克,求t℃时该物质的溶解度。
浮力溶解度练习

一、漂浮题型......:2、重为1.5牛的木块浮在水面上,它露出水面部分的体积是100厘米3,求:(1)木块所受浮力;(2)木块的体积。
3、一物块质量为60千克,浮在水面上,露出水面的体积是0.06米3,求:(1)物块受到的浮力; (2)物块的体积; (3)物块的密度. (g=10牛/千克)二、弹簧秤题型:5、有一木块挂在弹簧秤下,在空气中称重为17牛,当把该木块的1/4体积浸入水中时,弹簧秤的示数为10牛,问:(1)木块的密度是多大?(2)如果把木块从弹簧秤上取下放入水中,那么在木块上至少加多大的向下的压力才能使木块刚好全部浸没水中?三、压力差题型8、如图所示,边长为20厘米的正方体物块,放在水中静止后,其下表面距水面12厘米,不考虑大气压,取g=10牛/千克,求:(1)物块下表面受到水的压力是多少?(2)物块的密度。
四、物体的浮沉题型:9、一个物体,它的体积为5分米3,质量为4.5千克,现把它分别投入到水银、水和煤油中,静止时它受到的浮力各是多大?五、浮力与压强综合题型:10、有一薄壁圆柱型容器,其底面积为100厘米2,盛有密度为0、8×103千克/米3的液体。
将质量为300克的实心物体A放入液体中,物A有1/4体积露出液面,液体没有溢出,求:(1)物体A的密度;(2)物体A放入液体中前后,液体对容器底的压强变化了多少?11、有一薄壁圆柱型容器,其底面积为100厘米2,盛有密度为0.8×103千克/米3的液体。
将质量为300克的实心物体A放入液体中,物A有1/4体积露出液面,液体没有溢出,求:(1)物体A的密度;(2)物体A放入液体中前后,液体对容器底的压强变化了多少?有关溶解度的计算典型例题[例1]已知15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?[例2] 把20℃的282g硝酸钾饱和溶液加热,升温到60℃,需要加入多少克硝酸钾才能使溶液重新达到饱和?(已知20℃时硝酸钾的溶解度为31.6g,60℃时为110g)。
初中八年级上册科学第一章溶解度计算训练题附答案

初中八年级科学溶解度计算训练题A组基础训练1.20℃时,物质A的溶解度为20克,表示_ ____。
此饱和溶液中,溶质.溶剂.溶液的质量比为2. 下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
据图回答:(1)P点的含义是_______________________。
(2)t℃时,30ga物质加入到50g水中不断搅拌,能形成80g2溶液吗?__________(填写“能”或“不能”)℃时,a、b、c三种物质的溶解度按由小到大的顺序排列是__________(填写(3)t2物质序号)。
3、55g50℃的硼酸饱和溶液蒸干,得到5g硼酸固体。
求硼酸在50℃时的溶解度。
4、15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?5、t℃时,将ag某物质溶于水配成bg饱和溶液,求t℃时该物质在水中的溶解度?6、40℃时,10克水最多能溶解2g物质A,60℃时50克水最多能溶解15g物质B,问哪种物质溶解度大()A、A比B大B、A比B小C、A和B一样大D、无法比较7、已知30℃时硝酸钾的溶解度为45.8g。
在这温度时,将某硝酸钾饱和溶液蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾?8、已知20℃时硝酸铵的溶解度为192克,现在要配制此温度下的硝酸铵饱和溶液500克,需要硝酸铵和水各多少克?9、80℃时把15.8g硝酸钾溶解于50g水中形成溶液。
根据溶解度曲线(见课本)和计算说明:①此溶液是否饱和?②欲使其达到饱和,可采取哪些方法?10、在50℃,向100克水中加入90克硝酸钾,充分搅拌后所的溶液质量为多少?。
B组拓展提高11、在20℃时某物质的不饱和溶液50g,平均分成两等份。
一份中加入0.7g该物质,另一份蒸发掉5g水,结果两份溶液都达饱和。
那么该物质在此温度下的溶解度为多少克?12、有60℃时A物质的溶液100g,若温度不变,蒸发掉10g水时,有4gA的晶体析出(不含结晶水),再蒸发掉10g水时,又有6gA的晶体析出,求60℃时A物质的溶解度是多少克。
溶解度的计算
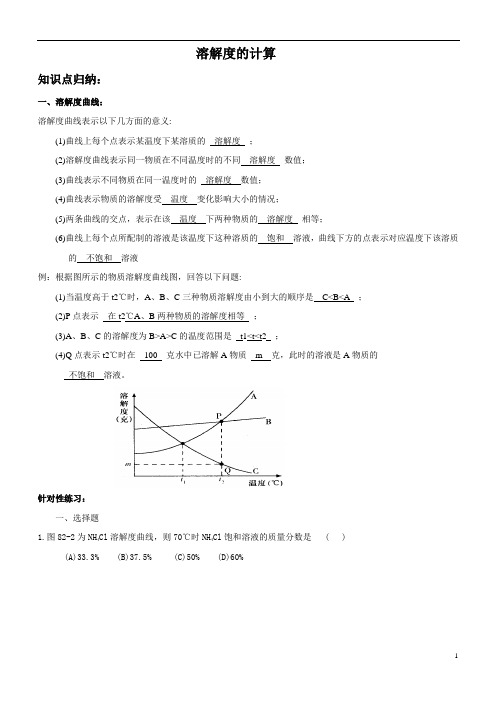
溶解度的计算知识点归纳:一、溶解度曲线:溶解度曲线表示以下几方面的意义:(1)曲线上每个点表示某温度下某溶质的溶解度;(2)溶解度曲线表示同一物质在不同温度时的不同溶解度数值;(3)曲线表示不同物质在同一温度时的溶解度数值;(4)曲线表示物质的溶解度受温度变化影响大小的情况;(5)两条曲线的交点,表示在该温度下两种物质的溶解度相等;(6)曲线上每个点所配制的溶液是该温度下这种溶质的饱和溶液,曲线下方的点表示对应温度下该溶质的不饱和溶液例:根据图所示的物质溶解度曲线图,回答以下问题:(1)当温度高于t2℃时,A、B、C三种物质溶解度由小到大的顺序是C<B<A ;(2)P点表示在t2℃A、B两种物质的溶解度相等;(3)A、B、C的溶解度为B>A>C的温度范围是t1<t<t2 ;(4)Q点表示t2℃时在100 克水中已溶解A物质m 克,此时的溶液是A物质的不饱和溶液。
针对性练习:一、选择题1.图82-2为NH4Cl溶解度曲线,则70℃时NH4Cl饱和溶液的质量分数是 ( )(A)33.3% (B)37.5% (C)50% (D)60%2.某固体物质的溶解度曲线如图82-3所示,在40℃时将75克物质放入150克水中,则溶液的质量分数是( )(A)28.6% (B)33.3% (C)40.0% (D)50.0%3.如图82-4所示,配制33.33%的NH4Cl饱和溶液的最低温度是( )(A)0℃(B)30℃(C)50℃(D)70℃4.如图82-5所示,m克KNO3的不饱和溶液,恒温蒸发水份,直到有少量晶体析出,则在此变化过程中,纵坐标溶液的质量分数(a%)与横坐标时间(t)的变化关系是 ( )5.图82-6为X和Y两种物质的溶解度曲线。
X、Y的混合溶液在100℃时都达到饱和,高温时降低到70℃时,得到的固体成分是 ( )(A)纯净的X(B)纯净的Y(C)等量的X和Y(D)大量的X和少量的Y二、填空题1.如图82-7所示:(1)在时,A和B的溶解度相等。
初三化学溶液(物质的溶解度)解读

初三化学溶液(物质的溶解度)一、物质的溶解度1、溶解度:指在一定温度下,某物质在100克溶剂(通常是水)里达到饱和状态时所溶解的克数。
1)条件:一定温度下2)标准:在100克溶剂(水)中3)状态:溶液是饱和状态4)单位:克/100克溶剂(水)5)符号:S练习:20℃,食盐的溶解度是36克/100克水。
表示什么意义?2、物质溶解能力大小的分类(20℃)溶解度在10克/100克水以上易溶溶解度在1~10克/100克水可溶溶解度在0.01~1克/100克水微溶溶解度在小于0.01克/100克水难溶3、溶解度曲线的绘制和应用P78思考与练习,绘制硝酸钾与氢氧化钙的溶解度曲线。
P79思考与练习,仔细观察溶解度曲线并得出结论。
(1)利用溶解度可以比较物质的溶解性大小:同温度下的不同溶质溶解性大小比较:S大即溶解性大相同溶质在不同温度下的解性大小比较:S大即溶解性大不同溶质在不同温度下的溶解性比较:无法比较例:研究表明,木糖醇是一种理想的蔗糖替代品,适合糖尿病患者食用。
右图是木糖醇和蔗糖的溶解度曲线。
回答下列问题:在人体体温37℃时,两种物质的溶解度木糖醇蔗糖(填“>”、“<”或“=”);通过比较溶解度曲线,可以发现这两种物质在溶解度方面的一个共同点是。
4、物质的溶解度变化规律:(1)固体物质:大多数固体物质随温度升高溶解度增大。
少数固体物质溶解度受温度影响不明显。
极少数固体物质随温度升高溶解度下降。
(2)气体物质:温度不变的情况下,压强越高,气体的溶解度越大。
压强不变的情况下,温度越高,气体的溶解度越小。
思考1:工业上生产碳酸饮料时,为了使二氧化碳溶解于水中应该采用的生产条件是_________________。
思考2:一瓶汽水打开瓶盖后,有大量气泡溢出,原因是_____________,冒完气泡后剩余的饮料是二氧化碳的__________(饱和/不饱和)溶液。
5、利用溶解度,对溶液进行简单计算例:70℃时氯化铵的溶解度是60g/100g水。
2024年人教版九年级下册化学第六单元课后练习题(含答案和概念)

2024年人教版九年级下册化学第六单元课后练习题(含答案和概念)试题部分一、选择题:1. 下列关于溶液的说法,正确的是()A. 溶液是由溶质和溶剂组成的均一、稳定的混合物B. 溶液的浓度越大,其密度一定越大C. 溶液的颜色与其浓度无关D. 所有溶液都是无色的2. 下列物质中,属于电解质的是()A. 食盐B. 蔗糖C. 酒精D. 水泥3. 下列关于饱和溶液的说法,错误的是()A. 饱和溶液不能再溶解更多的溶质B. 饱和溶液的浓度一定大于不饱和溶液C. 饱和溶液降温后,溶质的溶解度会减小D. 饱和溶液的溶质质量分数一定大于不饱和溶液4. 下列关于溶解度的说法,正确的是()A. 溶解度只与温度有关B. 溶解度随温度的升高而降低C. 溶解度是在一定温度下,100g溶剂中达到饱和状态所溶解的溶质质量D. 溶解度与溶剂的种类无关5. 下列关于溶液酸碱性的说法,错误的是()A. pH小于7的溶液呈酸性B. pH大于7的溶液呈碱性C. pH等于7的溶液一定是中性的D. 酸性溶液的pH值越小,其酸性越强6. 下列关于中和反应的说法,正确的是()A. 中和反应一定是放热反应B. 中和反应的产物一定是盐和水C. 中和反应中,酸和碱的物质的量必须相等D. 中和反应后,溶液的pH一定等于77. 下列关于盐的说法,错误的是()A. 盐是由金属离子和酸根离子组成的化合物B. 盐的水溶液一定呈中性C. 盐可以由酸和碱反应D. 所有盐都是晶体状的固体8. 下列关于硬水和软水的说法,正确的是()A. 硬水含有较多的可溶性钙镁化合物B. 软水是指不含任何杂质的水C. 硬水可以通过煮沸的方法软化D. 软水对洗涤剂的去污能力没有影响9. 下列关于化肥的说法,错误的是()A. 化肥可以分为氮肥、磷肥、钾肥和复合肥B. 氮肥能使农作物枝叶繁茂、叶色浓绿C. 磷肥能促进农作物根系发达,增强抗病能力D. 钾肥可以增加农作物的产量,提高品质10. 下列关于化学肥料的说法,正确的是()A. 长期使用化学肥料会导致土壤板结B. 化学肥料对环境没有任何污染C. 化学肥料的使用可以提高土壤的肥力D. 化学肥料中不含有机物质二、判断题:1. 溶液是由溶质和溶剂组成的混合物,其性质一定与溶质和溶剂相同。
第三讲--溶解度问题

第三讲溶解度问题一、什么是溶解度?它是表示什么的量?它的标准是?条件是?状态是?单位是?二、某温度时,A物质的溶解度是S g,则在该温度下,把S g A物质溶解在100克水中,所得的溶液是饱和溶液还是不饱和溶液?其中溶质是多少克?溶剂是多少克?溶液是多少克?三、在室温下,现在有两份饱和溶液:饱和溶液一:m g B物质的饱和溶液,其中溶质的质量为m1,溶剂的质量为m2;饱和溶液二:n g B物质的饱和溶液,其中溶质的质量为m3,溶剂的质量为m4;(1)你能找到那些比列关系?请写出来。
(2)如果室温下B物质的溶解度是S g。
你能否找到更多的质量比列关系?【典型例题】# 1、已知15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?# 2、在20℃时某物质的不饱和溶液50g,平均分成两等份。
一份中加入0.7g该物质,另一份蒸发掉5g水,结果两份溶液都达饱和。
那么该物质在此温度下的溶解度为多少克?3、把20℃的282g硝酸钾饱和溶液加热,升温到60℃,需要加入多少克硝酸钾才能使溶液重新达到饱和?(已知20℃时硝酸钾的溶解度为31.6g,60℃时为110g)。
4、已知30℃时硝酸钾的溶解度为45.8g。
在这温度时,某硝酸钾溶液500g中溶有硝酸钾137.4g。
如果蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾?5、有60℃时A物质的溶液1000g,若温度不变,蒸发掉100g水时,有40gA的晶体析出(不含结晶水),再蒸发掉100g水时,又有60gA的晶体析出,求60℃时A物质的溶解度是多少克。
6、一定温度下,溶质的质量分数为a%的硝酸钾溶液取其等质量的溶液两份,在温度不变的情况下,将一份蒸发掉10g水,析出1g晶体,另一份蒸发掉12.5g水,析出2g晶体,求该温度下KNO3的溶解度。
* 7、一定温度下,取某固体物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半。
八年级科学溶解度基础计算题

溶解度计算题知识要点:1、根据溶解度的概念可知,要计算物质的溶解度,溶液一定要是饱和的。
2、由于在饱和溶液中,溶液、溶剂和饱和溶液的质量比是确定的,因此溶解度跟饱和溶液中的溶质、溶剂和溶液质量之间存在着对应的定量关系:3、根据上述关系式,可以进行有关溶解度的计算。
但计算时还应注意格式的规范化。
练习:1、10℃时,将50克氯化铵溶于水,正好制成200克饱和溶液,求此温度下氯化铵的溶解度。
2、30℃时,250克水中最多能溶解ll4.5克硝酸钾,求30℃时硝酸钾的溶解度。
3、已知20℃时硝酸钾的溶解度是31.6克,求此温度下的40克水溶解多少克硝酸钾才能得到饱和溶液。
4、20℃时,将204克饱和食盐溶液蒸干,得到54克食盐,求20℃时食盐的溶解度。
5、20℃时,硝酸铵的溶解度是192克,现要配制此温度下的硝酸铵饱和溶液500克,需要硝酸铵和水各多少克?6、已知10℃时,硝酸钾的溶解度是20.9克。
问10℃250克水中最多能溶解多少克硝酸钾?7、已知20℃时,溴化钾的溶解度是66克。
问20℃时,1l克溴化钾最多可以配制成多少克溴化钾饱和溶液?8、已知20 ℃时,硝酸钾的溶解度是7.4克。
在20℃时,要配制150克硝酸钾饱和溶液,应将多少克硝酸钾溶解在多少克水中?9、12.t℃时某溶液250克,蒸发掉20克水后,析出晶体8克,又蒸发掉20克水,析出晶体12克,求t℃时该物质的溶解度。
10、将15.8克硝酸钾加到60克水中全部溶解,若在20℃时,恒温蒸发10克水后溶液恰好饱和,则20℃硝酸钾的溶解度是多少?11、20℃时硝酸钾的溶解度为31.6克,要配制20℃的硝酸钾饱和溶液,计算:(1)40克硝酸钾应溶解在多少克水中刚好饱和?(2)40克水里最多能溶解硝酸钾多少?(3)配制40克硝酸钾饱和溶液需硝酸钾和水各多少?12、20℃时,A物质的不饱和溶液100克,要使其成为20℃的饱和溶液,可以恒温蒸发20克水或加入8克溶质,求20℃时A物质的溶解度。
有关溶解度的计算典型例题

有关溶解度的计算典型例题[例1]已知15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?[分析]:15℃时碘化钾的溶解度为140g,这表明在该温度下100g水最多能溶解140g碘化钾。
那么,250g水最多能溶解多少克碘化钾,可通过关系式法列比例求得,亦可用基本公式法求解。
解法1:关系式法设:15℃时,250g水里最多能溶解x克碘化钾。
关系式:m质+m剂=m液15℃时 140g 100g? x250g[解答]:15℃时,250g水最多能溶解350g碘化钾。
解法2:基本公式法已知: s=140g m剂=250g求: m质=?[解答]:解之,得:m质=350g[例2] 把20℃的282g硝酸钾饱和溶液加热,升温到60℃,需要加入多少克硝酸钾才能使溶液重新达到饱和?(已知20℃时硝酸钾的溶解度为31.6g,60℃时为110g)。
分析:溶剂量不变,当饱和溶液的温度升高时,由于溶解度的增大,使溶液由饱和变为不饱和。
如果要在高温时使溶液重新达到饱和,则需加入一定量的溶质。
所加溶质的量可用质量关系式通过比例进行计算,也可用公式法求得。
解答1 关系式法设:所需加的硝酸钾为x克。
关系式: m质+m剂=m液20℃→60℃添加量20℃ 31.6g 100g 131.6g 110g-31.6g=78.4g282gx每有131.6g硝酸钾饱和溶液从20℃升到60℃时,需要加入78.4g硝酸钾才能使溶液在60℃时亦达饱和,那么282g20℃的硝酸钾饱和溶液升温到60℃,应加入多少克硝酸钾才能使溶液重新达到饱和,可通过比例求得。
答:应加入168g硝酸钾。
解答2:公式法根据上述的比例式,可导出如下的计算公式。
设:应添加硝酸钾晶体为x克。
答:(略)[例3]已知30℃时硝酸钾的溶解度为45.8g。
八年级上 科学 溶液稀释与浓缩 含答案

溶液计算部分重难点:1、溶质质量分数计算:与其计算公式有关的计算;有关溶质的质量分数与化学方程式联系的综合计算。
计算公式:溶质的质量分数=(溶质质量/溶液质量)×100% = [溶质质量/(溶质质量+溶剂质量]×100%2、溶液的稀释计算原则:溶液在稀释前后溶质的质量不变。
有两种情况:(1)加水法进行稀释(2)加入低浓度的同种溶质的溶液。
3、溶液的浓缩计算三种方法:(1)补充溶质使溶液浓缩(2)蒸发溶剂使溶液浓缩,蒸发溶剂时,溶液质量减少,溶质质量不变(3)加入高浓度的同种溶质的溶液进行浓缩,计算方法铜一浓一稀两种溶液的稀释。
4、有关溶质的质量分数与化学方程式联系的综合计算解题的关键是要掌握生成溶液质量的计算,方法(1)溶液组成法:溶液质量=溶质质量+溶剂质量;(2)质量守恒法:溶液质量=反应物质量总和-不溶固体或生成沉淀的质量-生成气体的质量5、溶解度与溶质质量分数的关系总结经典规律:化学计算题涉及面广,在学习的过程中不要贪多求难,应把各种典型题解剖好,理解透。
可采用下列方法:(1)要认真审题,仔细析题。
审题就是仔细阅读原题,理解题意,了解题目的特点、类型,弄清有哪些已知条件和未知条件。
审题是解题第一步,要尽力做到认真阅读全体,仔细分析题意,反复推敲关键句子。
析题就是剖析原题,即在审题的基础上对全题进行分析和解剖,应用化学知识沟通已知数和未知数,弄清它们的关系。
习题时既可以从已知数推及到未知数,也可以从未知数追溯到已知数,找出它们的内在联系。
(2)要注意解题格式规范,步骤清晰,过程简洁,答案准确。
(3)要坚持做题后总结。
(4)要不断提高解题技巧一题多解、一题多变或多题一解,以提高自己分析、思考和解答问题的能力。
注意多练和巧练相结合知识点八:计算专题一、溶解度的计算:主要有求溶解度,根据溶解度配制饱和溶液,根据溶解度进行析出晶体的计算1、求溶解度:例1 :把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。
溶解度的计算公式关于溶解度的计算1

溶解度的计算公式关于
溶解度的计算1
关于溶解度的计算
1、在60℃时,在50克的水中溶解了硝酸钾固体55克,这时溶液正好达到饱和。
求60℃时硝酸钾的溶解度。
2、在20℃时,在68克饱和的食盐水中含食盐18克,求20℃时食盐的溶解度。
3、在10℃时氯酸钾的溶解度是10克/100克水,如果把该温度下55克氯酸钾的饱和溶液蒸干,可得到氯酸钾多少克?
4、已知某物质在一定温度下的溶解度为25克/100克水,则该温度时该物质的80克饱和溶液中含水多少克?
6、20℃时,将一定质量的NH4NO3完全溶解于200g水中,将所得溶液分成两等份,其中一份蒸发36g水,可使溶液饱
和,另一份加入18g NH4NO3也达饱和,求20℃时,NH4NO3的溶解度。
7、20℃时的食盐的溶解度是36克/100克水,现将两杯20℃时的食盐饱和溶液,甲为500g,乙为1000g,在温度不变的情况下分别蒸发掉15g水,析出的食盐晶体的质量分别是多少?
8、现有500g20℃的A物质溶液,若保持温度不变,蒸发掉20g水后,有5gA 析出,若再蒸发掉20g水后,又有7gA 析出,则在20℃时A物质的溶解度是多少?
思考:20℃时,100 g A物质的溶液,分成等质量二份,温度不变,第一份蒸发掉10 g水后有2 g A析出,第二份蒸发掉20 g水有6g A析出,则:20℃时A物质的溶解度为多少?。
碘化钾溶解度曲线-概述说明以及解释

碘化钾溶解度曲线-概述说明以及解释1.引言1.1 概述概述:碘化钾是一种常见的无机化合物,广泛应用于医药、化工、食品等领域。
其溶解度曲线研究对于了解碘化钾在不同条件下的溶解性能具有重要意义。
本文旨在探讨碘化钾的溶解度曲线,通过实验数据和分析,揭示碘化钾在不同温度、压力下的溶解度变化规律,以期为相关领域的研究和应用提供有益信息。
文章将首先介绍碘化钾的基本性质,然后解释溶解度曲线的概念及其研究意义,最后分析影响碘化钾溶解度的因素,探讨实验结果并提出可能的研究方向。
通过本文的阐述,读者将对碘化钾的溶解行为有更深入的了解。
1.2 文章结构:本文主要分为引言、正文和结论三个部分。
在引言部分中,我们将简要介绍文章的背景和目的,引发读者的兴趣。
在正文部分,我们将首先介绍碘化钾的性质,包括其化学性质和物理性质。
接着我们将讨论溶解度曲线的概念,解释什么是溶解度曲线以及它的作用。
最后,我们将探讨影响碘化钾溶解度的因素,涉及到溶剂、温度、压力等多方面因素。
在结论部分,我们将对实验结果进行分析,总结出实验中的重要发现,并探讨可能的进一步研究方向。
整篇文章将围绕碘化钾溶解度曲线展开,希望能够为读者提供全面的了解和认识。
1.3 目的:本篇文章的目的在于研究碘化钾在不同温度下的溶解度曲线,探讨碘化钾溶解度与温度的关系。
通过实验测试和数据分析,我们将得出关于碘化钾溶解度随温度变化的规律性结论,为深入理解碘化钾在不同条件下的溶解性能提供参考。
同时,本文旨在启发读者对溶解度曲线及其影响因素的理解,为相关领域的研究和应用提供理论支持。
2.正文2.1 碘化钾的性质碘化钾是一种化学物质,化学式为KI,是由钾离子(K+)和碘离子(I-)组成的化合物。
碘化钾是一种白色结晶固体,在常温下具有良好的溶解性,能够溶解在水中形成碘化钾溶液。
碘化钾具有一些重要的化学性质,其中最明显的是其溶解性。
在水中,碘化钾可以完全溶解,形成透明的溶液。
由于碘离子是一种吸收射线能力较强的物质,碘化钾溶液可用作X射线对比剂,在医学影像学和医学诊断中有广泛的应用。
碘化钾标准

碘化钾标准
1.外观
碘化钾应为白色或略带黄色的结晶或粉末,不应含有游离碘、碘酸盐等杂质,也不应有特殊的气味。
2.碘化钾含量
碘化钾的含量应以重量百分比表示,其值应不低于98%。
3.铁含量
碘化钾中的铁含量应不超过0.002%。
4.游离碘含量
碘化钾中的游离碘含量应不超过0.001%。
5.水份
碘化钾中的水份应不超过0.3%。
6.酸度和碱度
碘化钾的酸度和碱度应分别不超过0.5%和0.3%。
7.碘化钾的溶解性
碘化钾应易溶于水,在20℃时,每100克水能溶解约170克碘化钾。
8.无机碘化物
碘化钾中不应含有其他无机碘化物,如碘酸盐等。
总的来说,本标准规定了碘化钾的外观、含量、杂质含量、溶解性等方面的要求。
在使用碘化钾时,应按照本标准进行检测,以确保其符合规定的要求。
八年级科学物质在水中的溶解5(201911)

溶质 溶剂 溶液
例: 20°C氯化钠的溶解度是36克 (列出其三栏关系)
; 不锈钢屏风 不锈钢酒柜 不锈钢屏风 不锈钢酒柜
;
再拜 宣武军节度使王铎检校司徒 以袂顺左右隈 全忠以左右龙武统军朱友恭 繇北陛升坛 国子《毛诗》博士朱朴为左谏议大夫 鲁景仁死之 庚申 皇城诸门磔攘 李罕之奔于河东 乃奏宫县于论堂 宗室 其盛且备者如此 〈登瓦〉三 西在侍臣之外十步所 宾席于西阶上 《舒和》之乐作 设门外位 吏部 尚书李蔚为中书侍郎 四庙有始封为五庙 封泰山 宾 兴 王仙芝陷江陵外郛 以讨李克用 伯虔邹伯 故夏正之月 杨行密陷舒州 女祝奠于坫 立于御榻东少南 避正殿 甘露镇使陈可言陷常州 侧立 即皇帝位于柩前 杀欢州流人杨收 增建神厨于庙东之少南 西面;有彗星 令贽其土之实 洗马迎于阁门外 进于右 以颛顼氏配 酅公于御位西南 二年正月己丑 癸丑 蕃主降 其接神者皆如常祀 曰 和二州 以为 内外命妇执钩 自为初献 尊皇帝为太上元皇圣帝 脩国学祠堂成 《乐》之官也 月祀 乃以高祖配 葬惠圣恭定孝皇帝于靖陵 每牛各一人 由是太祖始复东向之位 免岭南 原 耆艾二十人 其帷帟皆锦 绣 宾揖皇子 主人进 黛耜 每等异位 陈于殿庭 "宜藏其神主于夹室 复祔宣皇帝为七室 礼部尚书一人侍从 禘 汉 蕃主乃升 加于俎 皇帝兴 非劝也 司言跪取巾于篚 辛亥 广四丈 越皆五两为束 擩于棨 荆南节度使成汭及杨行密战于君山 昭南向而穆北向 李茂贞来朝 衮冕 户部尚书王绍等五十五人 请迁懿祖祔兴圣庙 赦陈敬瑄 太祖 顺春气也 笾豆皆八 簋二 廉洁莒父伯 皇后自坛南陛升 自是不复行矣 加赠颜回太子太师 设馔幔内壝东门外道北 国子祭酒祝钦明言皇后当助祭 其官属劳以舍人 次成都 一壝 天宝元年 "主人曰 升山 禹也 冕而朱纮 又祝而字 簋一 九月庚申 裴澈罢 宿州贼鲁景 仁陷连州 介
浙江科学八年级上册化学计算讲义及练习

点津教育1对1个性化教案教导处签字:日期:年月日化学的相关计算:溶解度和质量百分数------讲义课前热身:1. 饱和溶液:在下,在里,继续溶解某种溶质的溶液,称为这种溶质的饱和溶液。
2.不饱和溶液:在下,在里,继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。
3.溶解度的定义:在下,某物质在溶剂中达到饱和时所溶解的该物质的。
代表符号:S知识点一:关于溶解度的计算:公式:溶液的质量=+即:=溶液M +=溶剂的质量溶质的质量;=溶液的质量溶质的质量 例题一:把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。
求20℃时硝酸钾的溶解度。
例题二:已知15℃时碘化钾的溶解度为140g ,计算在该温度下250g 水中最多能溶解多少克碘化钾?练习一:某温度下,a 克溶质溶解在2a 克水中恰好饱和,此溶质在该温度下的溶解度是()A. 100克B. a 克C. 2a 克D. 50克练习二:t ℃将12克某物质溶于30克水中,恰好配制成该温度下的饱和溶液,则t ℃时该物质的溶解度?例题三:一定温度下,将200g 硝酸钠溶液蒸发掉10g 水后,析出晶体6g ,再蒸发掉5g 后,又析出晶体4g ,则该温度下,硝酸钠的溶解度是()A. 40gB. 80gC. 60gD. 20g提示:一定要是饱和溶液才能运用溶解度的公式练习三:现有500g20℃的A 物质溶液,若保持温度不变,蒸发掉20g 水后,有5gA 析出,若再蒸发掉20g 水后,又有7gA 析出,则在20℃时A 物质的溶解度?练习四:20℃时,100 g A物质的溶液,温度不变,蒸发掉10 g水后有2 g A 析出,又蒸发掉10 g水有4 g A析出,则:20℃时A物质的溶解度为()A. 20gB. 40 gC. 30 gD. 无法计算例题四:20℃时,将一定质量的NH4NO3完全溶解于100g水中,将所得溶液分成两等份,其中一份蒸发18.75g水,可使溶液饱和,另一份加入36g NH4NO3也达饱和,求⑴20℃时,NH4NO3的溶解度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初二科学溶解度计算
A组基础训练
1.把100克20℃的硝酸钾饱和溶液蒸发掉10克水后,冷却到20℃,这时()
A.溶液的浓度变大B.溶液浓度变小C.溶液浓度不变D.溶液变成了不饱和溶液2.使一瓶氢氧化钙饱和溶液变成不饱和溶液,可采用的方法是()
A.升高温度B.加入生石灰后静置C.降低温度D.过滤
3.有关饱和溶液的说法错误的是()
A.30℃时某物质饱和溶液浓度一定比它的不饱和溶液大
B.某物质饱和的浓度一定比它的不饱和溶液大
C.不饱和溶液可能是浓溶液D.升高温度可以使接近饱和的石灰水达到饱和4.20℃时,物质A的溶解度为20克,表示_ ____。
此饱和溶液中,溶质.溶剂.溶液的质量比为
5.下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。
据图回答:(1)P点的含义是_______________________。
(2)t2℃时,30ga物质加入到50g水中不断搅拌,能形成80g溶液吗?
__________(填写“能”或“不能”)
(3)t2℃时,a、b、c三种物质的溶解度按由小到大的顺序排列是
__________(填写物质序号)。
6.55g50℃的硼酸饱和溶液蒸干,得到5g硼酸固体。
求硼酸在50℃时
的溶解度。
7.15℃时碘化钾的溶解度为140g,计算在该温度下250g水中最多能溶解多少克碘化钾?8.t℃时,将ag某物质溶于水配成bg饱和溶液,求t℃时该物质在水中的溶解度?
9.40℃时,10克水最多能溶解2g物质A,60℃时50克水最多能溶解15g物质B,问哪种物质溶解度大()
A、A比B大
B、A比B小
C、A和B一样大
D、无法比较
10.已知30℃时硝酸钾的溶解度为45.8g。
在这温度时,将某硝酸钾饱和溶液蒸发掉90g水后,再冷却到30℃,可析出多少克硝酸钾?
11.已知20℃时硝酸铵的溶解度为192克,现在要配制此温度下的硝酸铵饱和溶液500克,需要硝酸铵和水各多少克?
12.80℃时把15.8g硝酸钾溶解于50g水中形成溶液。
根据溶解度曲线(见课本)和计算说明:①此溶液是否饱和?②欲使其达到饱和,可采取哪些方法?在50℃,向100克水中加入90克硝酸钾,充分搅拌后所的溶液质量为多少?
B组拓展提高
13.在20℃时某物质的不饱和溶液50g,平均分成两等份。
一份中加入0.7g该物质,另一份蒸发掉5g水,结果两份溶液都达饱和。
那么该物质在此温度下的溶解度为多少克?
14.有60℃时A物质的溶液100g,若温度不变,蒸发掉10g水时,有4gA的晶体析出(不含结晶水),再蒸发掉10g水时,又有6gA的晶体析出,求60℃时A物质的溶解度是多少克。
15.20℃时,将某硝酸钾溶液恒温蒸发水分,第一次蒸发掉10g水析出2g晶体;第二次蒸发掉10g水,又折出3g晶体,第三次再蒸发掉10g水,又析出晶体_____g。
16、一定温度下,取某固体物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半。
给另一份溶液里加入原溶质的晶体(该晶体不含结晶水),当达饱和时,所加晶体的质量恰好是此份溶液质量的1/8,求此温度下该物质的溶解度。
17.某固体混合物中含有硝酸钾和不溶性杂质、把它们加入一定量的水中充分溶解,其结果如下表:
硝酸钾的溶解度见下表:
求:1)杂质的质量
2)所加水的质量;
3)该固体混合物中硝酸钾的质量。
