酸碱盐溶解度表
常见酸碱盐溶解表℃

21.5
+溶K
溶112
31.6
溶
11.1
溶
34.7
溶
111.5
+溶Rb
117溶
53
溶
48
溶
91
溶
450
+溶Cs
330溶
23
溶
179
溶
186
溶
﹥500
2+难Be
溶
107
溶
39
溶
﹥500
2+难Mg
0.009溶
70
溶
33
溶
54.2
微
2+微Ca
0.165溶
129
微
0.21
溶
74.5
难
2+微Sr
溶0.8
71
3+In
微
0.04
溶
500﹥
——
——
+Tl
溶
18.6
微
0.05
难
0.0006
3+Tl
——
——
溶
溶
2+Ge
微
0.24
溶
——
——
溶
4+Ge
——
——
——
——
——
——
2+Sn
难
溶
溶
微
0.98
4+Sn
溶
500﹥
——
——
——
——
2+Pb
难
微
0.064
微
0.084
微
0.063
3+As
常见酸碱盐溶解度表℃

0.013
溶
53.8
难
Ba2+
溶
3.9
溶
8.7
难
0.00024
溶
36
难
Al3+
难
0.0001
溶
69
溶
38
溶
70
——
——
Ga3+
微
溶
﹥500
溶
﹥500
In3+
微
溶
﹥500
Tl+
25.9(0℃)
溶
9.55
溶
微
0.33
溶
4
Tl3+
溶
溶
溶
4.87
溶
﹥500
Ge2+
——
——
——
——
Ge4+
——
——
——
——
Sn2+
微
0.04
溶
﹥500
——
——
Tl+
溶
18.6
微
0.05
难
0.0006
Tl3+
——
——
溶
溶
Ge2+
微
0.24
溶
——
——
溶
Ge4+
——
——
——
——
——
——
Sn2+
难
溶
溶
微
0.98
Sn4+
溶
﹥500
——
——
——
——
Pb2+
难
微
0.064
微
(完整word)高中阶段常见酸碱盐溶解性表

NO3ˉ
Clˉ
SO42ˉ
S2ˉ
SO32ˉ
CO32ˉ
SiO32ˉ
PO43ˉ
H+
溶、挥
溶、挥
溶Байду номын сангаас
溶、挥
溶、挥
溶、挥
难
溶
NH4+
溶、挥
溶
溶
溶
溶
溶
溶
—
溶
K+
溶
溶
溶
溶
溶
溶
溶
溶
溶
Na+
溶
溶
溶
溶
溶
溶
溶
溶
溶
Ba2+
溶
溶
溶
难
—
微
难
难
难
Ca2+
微
溶
溶
微
—
难
难
难
难
Mg2+
难
溶
溶
溶
—
微
微
难
难
Al3+
难
溶
溶
溶
—
—
—
难
难
Mn2+
难
溶
溶
溶
难
难
难
难
难
Zn2+
难
溶
溶
溶
难
难
难
难
难
Cr3+
难
溶
溶
溶
—
—
—
难
难
Fe2+
难
溶
溶
溶
难
难
难
难
难
Fe3+
高中化学酸、碱和盐的溶解性表大全
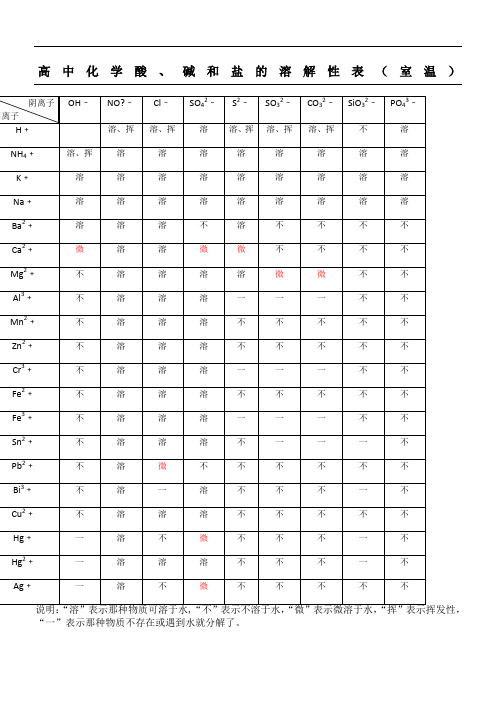
溶
溶
溶
溶
微
微
不
不
Al3﹢
不
溶
溶
溶
一
一
一
不
不
Mn2﹢
不
溶
溶
溶
不
不
不
不
不
Zn2﹢
不
溶
溶
溶
不
不
不
不
不
Cr3﹢
不
溶
溶
溶
一
一
一
不
不
Fe2﹢
不
溶
溶
溶
不
不
不
不
不
Fe3﹢
不
溶
溶
溶
一
一
一
不
不
Sn2﹢
不
溶
溶
溶
不
一
一
一
不
Pb2﹢
不
溶
微
不
不
不
不
不
不
Bi3﹢
不
溶
一
溶
不
不
不
一
不
Cu2﹢
不
溶
溶
溶
不
不
不
不
不
Hg﹢
一
溶
不
微
不
不
不
一
不
Hg2﹢
一
溶
溶
溶
不
不
不
一
不
Ag﹢
一
溶
不
微
不
不
不
不
不
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“一”表示那种物质不存在或遇到水就分解了。
酸碱盐的溶解性表

①指20℃时在水中的溶解性;
②“溶”表示那种物质可溶于水,“难”表示难溶于水,“微”表示微溶于水,“挥”表示那种物质具有挥发性,“—”表示那种物质不存在或遇到水就分解了。
常见沉淀
白色:BaSO4、BaCO3、CaCO3、AgCl、Mg(OH)2、Fe(OH)2、Al(OH)3、ZnCO3、MnCO3、Zn(OH)2
蓝色:Cu(OH)2、CuCO3
浅黄色:AgBr、Ag2CO3
红褐色:Fe(OH)3
钾钠铵硝都能溶,盐酸不溶只有银;
硫酸不溶只有钡,微溶还有钙和银;
碳酸大多都不溶,铵溶钾钠微溶银;
碱类大多都不溶,只溶铵钾钠和钡,
石灰水儿属微溶。
注:“钾钠铵硝”分别指钾盐、钠盐、铵盐、硝酸盐,“盐酸不溶只有银”中的“银”指氯化银,其他语句中的元素指某物质。
酸碱盐溶解性表和口诀(精华版)
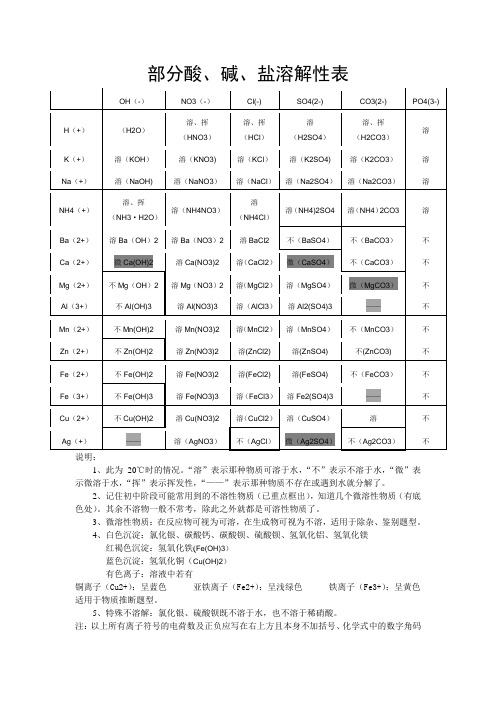
说明:
1、此为20℃时的情况。
“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“——”表示那种物质不存在或遇到水就分解了。
2、记住初中阶段可能常用到的不溶性物质(已重点框出),知道几个微溶性物质(有底色处)。
其余不溶物一般不常考,除此之外就都是可溶性物质了。
3、微溶性物质:在反应物可视为可溶,在生成物可视为不溶,适用于除杂、鉴别题型。
4、白色沉淀:氯化银、碳酸钙、碳酸钡、硫酸钡、氢氧化铝、氢氧化镁
红褐色沉淀:氢氧化铁(Fe(OH)3)
蓝色沉淀:氢氧化铜(Cu(OH)2)
有色离子:溶液中若有
铜离子(Cu2+):呈蓝色亚铁离子(Fe2+):呈浅绿色铁离子(Fe3+):呈黄色适用于物质推断题型。
5、特殊不溶解:氯化银、硫酸钡既不溶于水,也不溶于稀硝酸。
注:以上所有离子符号的电荷数及正负应写在右上方且本身不加括号、化学式中的数字角码
应写在右下方,这里是为了方便打字,请谅解。
部分酸碱盐溶解性背诵口诀
①钾钠铵盐硝酸盐,
完全溶解不困难。
②硫酸盐中钡不溶,
盐酸盐中只银难,
硫酸钡和氯化银,
两种沉淀记心间。
③碳酸盐溶钾钠铵,
碳酸铝铁银碱无。
④硫酸钙银盐微溶,
微溶还有碳酸镁。
⑤碱有钾钠铵钡溶,
氢氧化钙是微溶,
其他全都不能溶。
⑥常见诸酸皆可溶,
记住挥酸盐硝碳。
注:口诀仅供参考,本身并不完全准确,但是能促进记忆。
(完整版)初中化学酸碱盐溶解性表以及口诀(最新整理)

碳酸盐
CO32-
H2CO3 溶、挥 (NH4)2CO3
溶 K2CO3 溶 Na2CO3 溶 BaCO3 ☆不 CaCO3 ☆不 MgCO3 微 —— —— MnCO3 不 ZnCO3 不 FeCO3 不 —— —— CuCO3 不 Ag2CO3 不 碳酸某
不
Zn2+
不
溶
溶
溶
不
Fe2+
不
溶
溶
溶
不
Fe3+
不
溶
溶
溶
-
Cu2+
不
溶
溶
溶
不
Ag+
-
溶
不
微
不
部分酸碱盐溶解性表(20℃)
℃
记忆口诀:钾钠铵硝酸盐全溶,
盐酸盐只有 AgCl 不容,硫酸盐只有 BaSO4 不容, 碳酸盐只溶 K+、Na+、NH4+,碱类只溶 K+、Na+、NH4+和 Ba2+ Ca(OH)2、CaSO4、Ag2SO4 微溶.
3
Ca(NO3) CaCO3
3
CaSO4
阳离子 阴离子
OH-
NO3-
Cl-
SO42-
CO32-
Commented [eke1]:
H+
溶、挥 溶、挥 溶 溶、挥
NH4
溶、挥 溶
溶
溶
溶
K+
溶
溶
溶
溶
溶
Na+
溶
溶
溶
溶
溶
Ba2+
溶
溶
溶
不
不
Ca2+
酸碱盐溶解性表
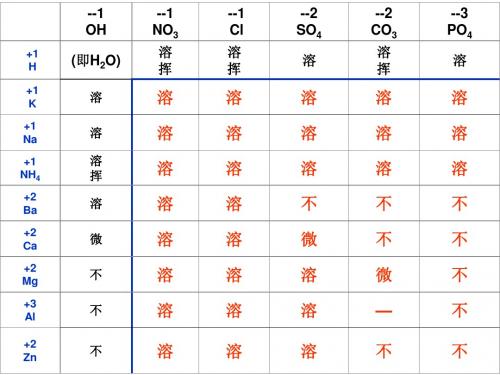
溶 溶 溶 不 微 溶 溶 溶
溶 溶 溶 不 不 微 — 不
溶 溶 溶 不 不 不 不 不
--1 OH
--1 NO3
--1 Cl
--2 SO4
--2 CO3
--3 PO4
+2 Fe +3 Fe +2 Cu +1 Ag +2 Pb
不
不 不
溶
溶 溶
溶
溶 溶
溶
溶 溶
不
— 不
不
不 不
—
不
溶
溶
不
微
微
不
不
不
不
例1:AgNO3、Na2SO4
(B)H2 SO4、NaCl、Na2CO3 (C)Na2SO4、KNO3、Ba(OH)2 (D)BaCl2、NaCl、KOH
(物质共存不反应, 反应不共存.)
解释: A.是银离子与氯离子不能共存 , Ag+ 和 Cl-- 结合 ,得到 AgCl沉淀 B. 是氢离子与碳酸根离子不能共存 , H+ 和 CO32– 结 合得到H2CO3, H2CO3 不稳定分解得到 H2O和CO2 H2 SO4 + Na2CO3 == Na2SO4 + H2O + CO2↑ C. 是硫酸根离子 与 钡离子不能共存 , Ba2+和SO42- 结合, 得到 BaSO4 沉淀
不
说明:“溶”表示那种物质可溶于水, “不”表示不溶于, “微”表示微溶于水,“挥”表示挥发性, “——”表示 那种物质不存在或在遇到水就分解了
3. 酸碱盐的溶解性表-----口决: (1)(钾、钠、铵、硝酸)盐溶 (2) 盐酸盐不溶银(例:AgCl ) (3) 硫酸盐不溶钡和铅 (例:BaSO4 PbSO4 ) (4) 碳酸盐,磷酸盐只溶钾,钠,铵 备注:①Ag2SO4 ,CaSO4 MgCO3 微溶于水; ②AgCl与BaSO4 不仅不溶于水,也不溶于酸
高中化学盐溶解性表及元素周期表
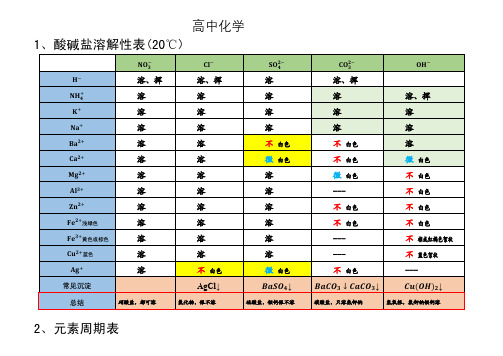
高中化学盐溶解性表及元素周期表
1、酸碱盐溶解性表(20℃)
−
−
−
−
−
−
溶、挥
溶、挥
溶
溶、挥
+
溶
溶
溶
溶
溶、挥
+
溶
溶
溶
溶
溶
+
溶
溶
溶
溶
溶
+
溶
溶
不
白色
不
白色
溶
&色
不
白色
微
白色
+
溶
溶
溶
微
白色
不
白色
+
溶
溶
溶
---
不
白色
+
溶
溶
溶
不
白色
不
白色
+ 浅绿色
溶
溶
溶
不
白色
不
白色
+ 黄色或棕色
溶
溶
溶
---
不
棕或红褐色絮状
+ 蓝色
溶
溶
溶
---
不
蓝色絮状
溶
不
不
---
+
AgCl↓
常见沉淀
总结
白色
硝酸盐,都可溶
2、元素周期表
氯化物,银不溶
微
白色
↓
酸碱盐可溶性表及口诀
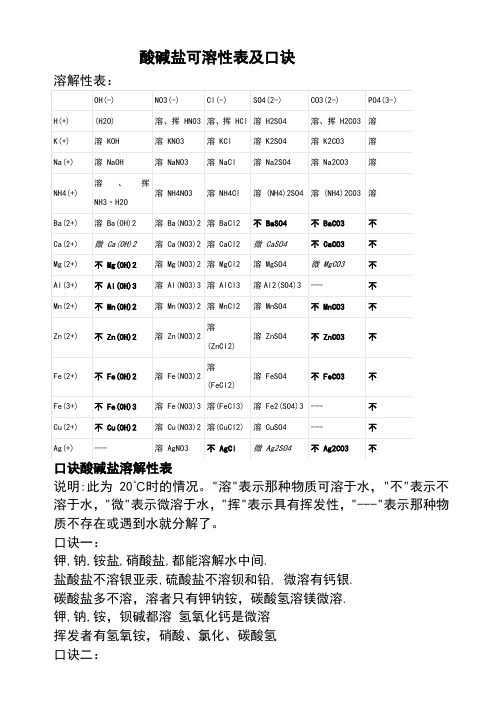
酸碱盐可溶性表及口诀溶解性表:口诀酸碱盐溶解性表说明:此为20℃时的情况。
"溶"表示那种物质可溶于水,"不"表示不溶于水,"微"表示微溶于水,"挥"表示具有挥发性,"---"表示那种物质不存在或遇到水就分解了。
口诀一:钾,钠,铵盐,硝酸盐,都能溶解水中间.盐酸盐不溶银亚汞,硫酸盐不溶钡和铅, 微溶有钙银.碳酸盐多不溶,溶者只有钾钠铵,碳酸氢溶镁微溶.钾,钠,铵,钡碱都溶氢氧化钙是微溶挥发者有氢氧铵,硝酸、氯化、碳酸氢口诀二:钾钠铵硝酸盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④注: ①钾钠铵盐都溶于水; ②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶; ③硝酸盐都溶于水; ④口诀中没有涉及的盐类都不溶于水;口诀三:钾、钠、铵盐、硝酸盐; (钾盐、钠盐、铵盐、硝酸盐均可溶于水) 氯化物除银、亚汞; (氯化物除氯化银、氯化亚汞外均可溶于水)硫酸盐除钡和铅; (硫酸盐除硫酸钡、硫酸铅外均可溶于水)碳酸、磷酸盐,只溶钾、钠、铵。
说明:以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
口诀四:钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶。
口诀五:钾、钠、硝酸溶, (钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞, (盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅, (硫酸盐中不溶的是硫酸钡和硫酸铅。
) 其余几类盐, (碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵, (只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
口诀六:钾钠铵盐硝酸盐,完全溶解不困难。
氯化亚汞氯化银,硫酸钡和硫酸铅。
生成沉淀记心间,氢硫酸盐和碱类。
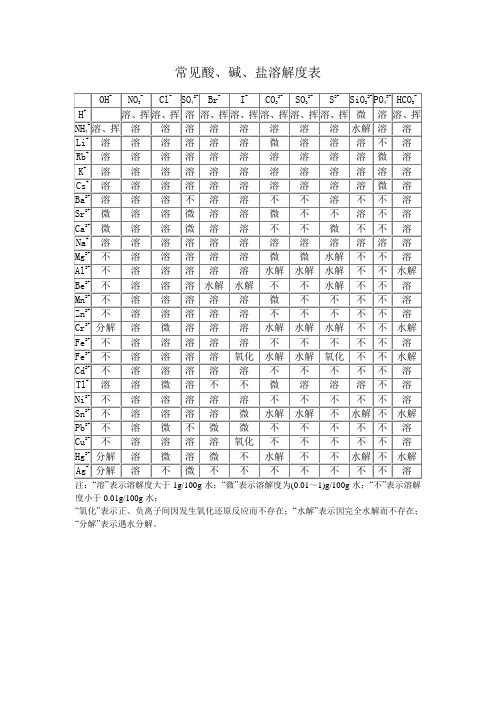
常见酸碱盐溶解度表
溶
溶
溶
溶
氧化
不
不
不
不
不
溶
Hg2+
分解
溶
微
溶
微
不
水解
不
不
水解
不
水解
Ag+
分解
溶
不
微
不
不
不
不
不
不
不
溶
常见酸、碱、盐溶解度表
注:“溶”表示溶解度大于1g/100g水;“微”表示溶解.01g/100g水;
“氧化”表示正、负离子间因发生氧化还原反应而不存在;“水解”表示因完全水解而不存在;“分解”表示遇水分解。
溶
溶
溶
溶
微
溶
Ba2+
溶
溶
溶
不
溶
溶
不
不
溶
不
不
溶
Sr2+
微
溶
溶
微
溶
溶
微
不
不
溶
不
溶
Ca2+
微
溶
溶
微
溶
溶
不
不
微
不
不
溶
Na+
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
溶
Mg2+
不
溶
溶
溶
溶
溶
微
微
水解
不
不
溶
Al3+
不
溶
溶
溶
溶
溶
水解
水解
水解
不
不
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2+
Ag+
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水, “挥”表示挥发性,“—”表示那种物质不存在或遇到水就分解了。
PO4 溶 溶 溶 溶 不 不 不 不 不 不 不 不 不 不 不 不 不 不 不 不
3-
部分酸、碱和盐的溶解性表(20℃)
OHH K
+ +
NO3 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶
-
Cl溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 微 - 溶 不 溶 不
SO4 溶 溶 溶 溶 不 微 溶 溶 溶 溶 溶 溶 溶 溶 不 溶 溶 微 溶 微
2-
2-
SiO3 微 溶 溶 溶 不 不 不 不 不 不 不 不 不 - 不 - 不 - - 不
2-
溶、挥 溶 溶 溶 微 不 不 不 不 不 不 不 不 不 不 不 - - -
溶、挥 溶、挥
溶、挥 溶、挥 溶、挥
NH4
+
Na Ca
+
Ba2+
2+
Mg2+ Al3+ Mn Cr Fe
2+
Zn2+
3+
Fe2+
I溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 溶 - 溶 溶 不 - 不 不 不
S2溶 溶 溶 - - - - 不 不 - 不 - 不 不 不 不 不 不 不
SO3 溶 溶 溶 不 不 微 - 不 不 - 不 - - 不 不 不 不 不 不
2-
CO3 溶 溶 溶 不 不 微 - 不 不 - 不 - - 不 不 不 不 不 不
