金属活动性顺序表及酸性排名
金属性顺序表
金属性顺序表
金属顺序表为:k钾、Ca钙、Na钠、Mg镁、Al铝、Zn锌、Fe铁、Sn 锡、pb铅、H氢、Cu铜、Hg汞、Ag银、pt铂、Au金,这是最常用的金属,需要背过的,位于H氢前的金属是较活泼的金属,能和盐酸硫酸反应,氢后面的是不活泼金属。
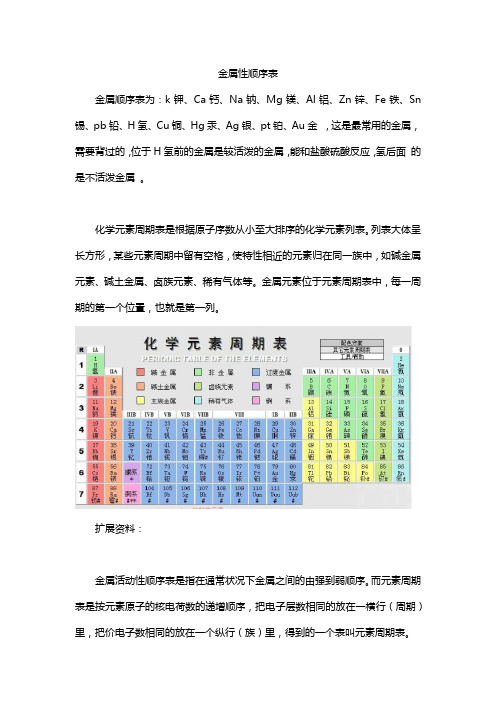
化学元素周期表是根据原子序数从小至大排序的化学元素列表。
列表大体呈长方形,某些元素周期中留有空格,使特性相近的元素归在同一族中,如碱金属元素、碱土金属、卤族元素、稀有气体等。
金属元素位于元素周期表中,每一周期的第一个位置,也就是第一列。
扩展资料:
金属活动性顺序表是指在通常状况下金属之间的由强到弱顺序。
而元素周期表是按元素原子的核电荷数的递增顺序,把电子层数相同的放在一横行(周期)里,把价电子数相同的放在一个纵行(族)里,得到的一个表叫元素周期表。
联系:在元素周期表中,同一周期里核电荷数的递增,金属性逐渐减弱;在同一族里,核电荷数的递增,金属性逐渐增强。
2021年中考化学知识点之金属活动性顺序-七三课堂整理

2021年中考化学知识点之金属活动性顺序
金属活动性顺序
金属活动性顺序由强至弱:KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu
(按顺序背诵)钾钙钠镁铝锌铁锡铅(氢)铜汞银铂金
② 属位置越靠前的活动性越强,越易失去电子变为离子,反应速率越快
②排在氢前面的金属能置换酸里的氢,排在氢后的金属不能置换酸里的氢,跟酸不反应;
③排在前面的金属,能把排在后面的金属从它们的盐溶液里置换出来。
排在后面的金属跟排在前面的金属的盐溶液不反应。
④混合盐溶液与一种金属发生置换反应的顺序是“先远”“后近”
注意:*单质铁在置换反应中总是变为+2价的亚铁。
常用金属活动性顺序表

常用金属活动性顺序表K Ba Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn (H) Cu Hg Pb Ag Pt Au即:钾钡钙钠镁铝锰锌铬铁钴锡铅氢铜汞银铂金各种金属的金属性从左到右递减,对应金属的简单的,一般正价的离子氧化性从左到右递增(特殊:Hg2+<Fe3+<Ag+). 还有Cu(+1);Mn有+2;+4;+7价金属大概是这样:由强到弱铯最强然后是稀土、钡、铷、再然后是钾〉钙〉钠〉镁〉锂〉铝〉铍〉锰〉锌〉铁〉钴〉镍〉锡〉铅〉铜〉汞〉银〉铂〉金。
非金属是这样:因为非金属一般都是若干原子构成的分子,而分子是非金属常见形态,所以这里排的是分子顺序表,比较实用:氟〉氯〉氧〉溴〉氮、硫〉氢〉红磷〉碘、碳、砷、硒、硼、硅惰性气体:Xe>Kr>Ar>Ne>He总之元素周期表里越是左下方,越是右上方越强。
惰性气体不算。
金属活动性顺序表的应用金属活动性顺序是历年来中考命题的热点,题目的难易不同,题型各异。
因此对金属活动性顺序表的正确理解和灵活运用十分重要。
我们主要从以下几个方面对其进行理解。
1. 金属与酸发生反应(1)金属应是在金属活动性顺序中排在(H)前面的金属。
(2)单质铁与酸发生置换反应时生成亚铁盐。
(3)K、Ca、Na除与酸反应外,还能与水在常温下发生置换反应生成,其余金属则不能。
2. 金属与盐发生置换反应(1)在金属活动性顺序中只有排在前面的金属才能把排在后面的金属从其盐溶液中置换出来,而与H的位置无关。
但K、Ca、Na等金属例外,由于它们过于活泼,与盐溶液不发生置换反应,而是先与溶液中的水发生反应。
(2)铁与盐溶液发生置换反应时,只生成二价亚铁盐。
(3)用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来。
用不同的金属置换同种盐溶液,盐中金属排在金属活动性顺序中较前的金属先被置换出来。
金属活动性顺序表及酸性排名
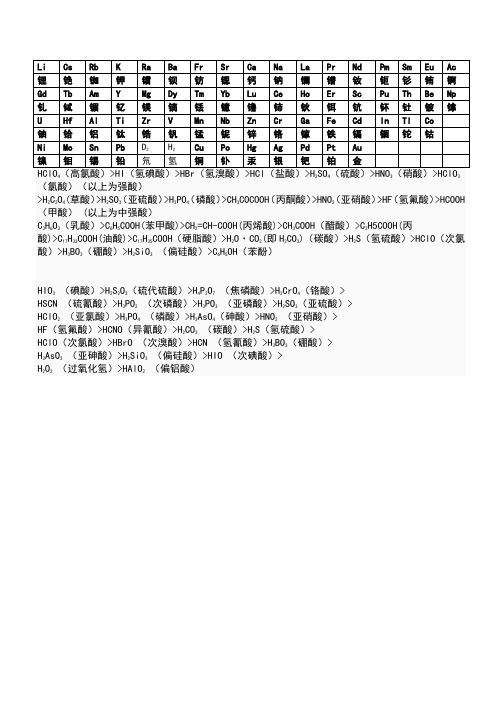
HIO3(碘酸)>H2S2O3(硫代硫酸)>H4P2O7(焦磷酸)>H2CrO4(铬酸)>
HSCN (硫氰酸)>H3PO2(次磷酸)>H3PO3(亚磷酸)>H2SO3(亚硫酸)>
HClO2(亚氯酸)>H3PO4(磷酸)>H3AsO4(砷酸)>HNO2(亚硝酸)>
HF(氢氟酸)>HCNO(异氰酸)>H2CO3(碳酸)>H2S(氢硫酸)>
HClO(次氯酸)>HBrO (次溴酸)>HCN (氢氰酸)>H3BO3(硼酸)>
H3AsO3(亚砷酸)>H2SiO3(偏硅酸)>HIO (次碘酸)>
H2O2(过氧化氢)>HAlO2(偏铝酸)
Sn
Pb
D2
H2
Cu
Po
Hg
Ag
Pd
Pt
Au
镍
钼
锡
铅
氘
氢
铜
钋
汞
银
钯
铂
金
HClO4(高氯酸)>HI(氢碘酸)>HBr(氢溴酸)>HCl(盐酸)>H2SO4(硫酸)>HNO3(硝酸)>HClO3(氯酸)(以上为强酸)
金属活动性顺序表

金属活动性顺序表常见金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au金属活动性顺序表的意义(1)金属的位置越靠前,它的活动性越强(2)位于氢前面的金属能置换出酸中的氢(强氧化酸除外)。
(3)位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(K,Ca,Na除外)。
(4)很活泼的金属,如K、Ca、Na与盐溶液反应,先与溶液中的水反应生成碱,碱再与盐溶液反应,没有金属单质生成。
如:2Na+CuSO4+2H2O==Cu(OH)2↓+Na2SO4+H2↑(5)不能用金属活动性顺序去说明非水溶液中的置换反应,如氢气在加热条件下置换氧化铁中的铁:Fe2O3+3H22Fe+3H2O金属原子与金属离子得失电子能力的比较金属活动性顺序表的应用(1)判断某些置换反应能否发生a.判断金属与酸能否反应:条件:①金属必须排在氢前面②酸一般指盐酸或稀硫酸b.判断金属与盐溶液能否反应:条件:①单质必须排在盐中金属的前面②盐必须可溶于水③金属不包含K、Ca、Na(2)根据金属与盐溶液的反应判断滤液、滤渣的成分。
如向CuSO4,AgNO3混合液中加铁粉,反应后过滤,判断滤液和滤渣成分。
铁与CuSO4和AgNO3溶液反应有先后顺序,如果铁足量,先将AgNO3中的Ag完全置换后再置换CuSO4中的Cu,那么溶液中只有FeSO4;如果铁的量不足,应按照“先后原则”分别讨论滤液和滤渣的成分。
(3)根据金属活动性顺序表判断金属与酸反应的速率或根据反应速率判断金属的活动性顺序。
如镁、锌、铁三种金属与同浓度的稀H2SO4反应产生氢气的速率:Mg>Zn>Fe,则可判断金属活动性Mg>Zn>Fe, (4)利用金属活动性顺序表研究金属冶炼的历史。
金属活动性越弱,从其矿物中还原出金属单质越容易; 金属活动性越强,从其矿物中还原出金属单质越难。
所以越活泼的金属越不易冶炼,难于冶炼的金属开发利用的时间就越迟。
(完整版)金属活动性顺序表

金属活动性顺序表常见金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au金属活动性顺序表的意义(1)金属的位置越靠前,它的活动性越强(2)位于氢前面的金属能置换出酸中的氢(强氧化酸除外)。
(3)位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来(K,Ca,Na除外)。
(4)很活泼的金属,如K、Ca、Na与盐溶液反应,先与溶液中的水反应生成碱,碱再与盐溶液反应,没有金属单质生成。
如:2Na+CuSO4+2H2O==Cu(OH)2↓+Na2SO4+H2↑(5)不能用金属活动性顺序去说明非水溶液中的置换反应,如氢气在加热条件下置换氧化铁中的铁:Fe2O3+3H22Fe+3H2O金属原子与金属离子得失电子能力的比较金属活动性顺序表的应用(1)判断某些置换反应能否发生a.判断金属与酸能否反应:条件:①金属必须排在氢前面②酸一般指盐酸或稀硫酸b.判断金属与盐溶液能否反应:条件:①单质必须排在盐中金属的前面②盐必须可溶于水③金属不包含K、Ca、Na(2)根据金属与盐溶液的反应判断滤液、滤渣的成分。
如向CuSO4,AgNO3混合液中加铁粉,反应后过滤,判断滤液和滤渣成分。
铁与CuSO4和AgNO3溶液反应有先后顺序,如果铁足量,先将AgNO3中的Ag完全置换后再置换CuSO4中的Cu,那么溶液中只有FeSO4;如果铁的量不足,应按照“先后原则”分别讨论滤液和滤渣的成分。
(3)根据金属活动性顺序表判断金属与酸反应的速率或根据反应速率判断金属的活动性顺序。
如镁、锌、铁三种金属与同浓度的稀H2SO4反应产生氢气的速率:Mg>Zn>Fe,则可判断金属活动性Mg>Zn>Fe,(4)利用金属活动性顺序表研究金属冶炼的历史。
金属活动性越弱,从其矿物中还原出金属单质越容易;金属活动性越强,从其矿物中还原出金属单质越难。
所以越活泼的金属越不易冶炼,难于冶炼的金属开发利用的时间就越迟。
(完整版)金属活动性顺序表知识点及专题复习

金属活动性顺序表的应用金属活动顺序大概是:由强到弱铯最强然后是稀土、钡、铷、再然后是钾〉钙〉钠〉镁〉铝〉铍〉锰〉锌〉铁〉钴〉镍〉锡〉铅〉(氢)〉铜〉汞〉银〉铂〉金。
符号式为(从钾至金):K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au(初中生应该掌握的··)。
1.金属与酸发生反应(1)金属应是在金属活动性顺序中排在(H)前面的金属。
(2)单质铁与酸发生置换反应时生成亚铁盐。
(3)K、Ca、Na除与酸反应外,还能与水在常温下发生置换反应生成对应的碱和H2,其余金属则不能。
2. 金属与盐发生置换反应(1)在金属活动性顺序中只有排在前面的金属才能把排在后面的金属从其盐溶液中置换出来,而与H的位置无关。
但K、Ca、Na等金属例外,由于它们过于活泼,与盐溶液不发生置换反应,而是先与溶液中的水发生反应。
如把钠放入硫酸铜溶液中[2Na+2H2O===2NaOH+H2↑,CuSO4+2NaOH===Cu(OH)2↓+Na2SO4]最终没有单质铜生成(2)铁与盐溶液发生置换反应时,只生成二价亚铁盐。
(3)用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来。
用不同的金属置换同种盐溶液,盐中金属排在金属活动性顺序中较前的金属先被置换出来。
还有要知道:金属只与溶液发生置换反应,而且若有一种金属和多种混合盐溶液反应,最先反应的是最不活泼的那个金属的盐溶液,如:锌粒与氯化亚铁和硫酸铜和硝酸汞的混合溶液反应,最先反应的是硝酸汞,当硝酸汞被消耗完时,硫酸铜才与锌粒反应,同理,硫酸铜反应完后,锌才会和氯化亚铁反应。
还有,当多种金属与一种盐溶液反应时,最活泼的金属先反应,如:把打磨光亮的镁带,铝丝,铜丝一起放入硝酸银溶液中,镁被消耗完后,铝才和硝酸银反应,铝反应完后,铜跟硝酸银反应注意:必须是一种金属单质和一种溶液,其他不可以反应,如:Cu+AgCO3≠ (Cu>Ag,但AgCO3不溶于水)金属活动性顺序表专题复习一、选择题1、下列化学方程式中,正确的是()A、Cu + 2AgCl == 2Ag + CuCl2B、Zn + 2AgNO3 == 2Ag +Zn(NO3)2C、2Na + CuSO4== Cu + Na2SO4D、2Fe +3CuCl2==2FeCl3 + 3Cu2、将锌片投入下列盐溶液中,充分反应后,使溶液质量减轻的是( )A、MgCl2B、CuCl2C、Ag(NO3)2D、KCl3、下列物质可以由相应的金属和酸发生置换反应而制得的是( )A、Fe2(SO4)3B、CuCl2C、AgNO3D、Al2(SO4)34、将一定质量的铁粉放入到足量的Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,测得滤渣中只含有一种金属,则该金属是( )A、Fe B、Cu C、Ag5、向CuCl2、ZnCl2、HCl的混合溶液中加入过量的Fe粉,反应后的溶液中一定含有()A、ZnCl2、HClB、FeCl2、CuCl2C、CuCl2、HClD、ZnCl2、FeCl26、下列金属中,金属活动性最强的是()。
常见金属活动性顺序

常见金属活动性顺序k\ueca\uena\uemg\ueal\uezn\uefe\uesn\uepb\ue(h)\uecu\uehg\ueag\uept\ueau 。
钾、钙、钠、镁、铝、锌、铁、锡、铅、(氢)、铜、汞、银、铂、金。
k\ueca\uena\uemg\ueal\uezn\uefe\uesn\uepb\ue(h)\uecu\uehg\ueag\uept\ueau 。
钾、钙、钠、镁、铝、锌、铁、锡、铅、(氢)、铜、汞、银、铂、金。
元素的金属性是指元素的原子失电子能力,判断元素金属性强弱,主要可从以下几方面来判断。
一、依金属活动顺序表中推论。
金属活动顺序表中,一般位置越后的金属,金属性越弱,原子的还原性越弱。
完全相同:金属活动性:sn\uepb,但元素的金属性: pb \ue sn。
二、依元素周期表判断1.同一周期,从左到右:原子的还原性逐渐弱化,水解性逐渐进一步增强;其对应的离子的水解性逐渐进一步增强,还原性逐渐弱化。
2.同一主族,从上到下:原子的还原性逐渐增强,氧化性逐渐减弱;其对应的离子的氧化性逐渐减弱,还原性逐渐增强。
金属活动性的辨认出:年,贝开托夫在实验的基础上,根据金属和金属离子间相互置换能力的大小,以及金属跟酸、跟水等反应的剧烈程度,首先确定了金属活动性顺序,在这个顺序里已包括了氢。
因为氢可以被位于它前面的金属从稀酸里置换出来,而氢后面的金属不能从酸中置换出氢。
在电化学获得发展后,金属活动性的来衡量尺度变成金属的标准电极电势,电势越负者还原性越弱,金属活动性也越弱。
由此可以看出,金属活动性与金属性是不同的概念,不可混为一谈。
金属在水中的活动性也不能体现金属在所有情况下的性质,例如钾的金属活动性强于钠,但钠可以置换出熔融氯化钾中的钾。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
D2
H2
Cu
Po
Hg
Ag
Pd
Pt
Au
镍
钼
锡
铅
氘
氢
铜ห้องสมุดไป่ตู้
钋
汞
银
钯
铂
金
HClO4(高氯酸)>HI(氢碘酸)>HBr(氢溴酸)>HCl(盐酸)>H2SO4(硫酸)>HNO3(硝酸)>HClO3(氯酸)(以上为强酸)
>H2C2O4(草酸)>H2SO3(亚硫酸)>H3PO4(磷酸)>CH3COCOOH(丙酮酸)>HNO2(亚硝酸)>HF(氢氟酸)>HCOOH(甲酸)(以上为中强酸)
HIO3(碘酸)>H2S2O3(硫代硫酸)>H4P2O7(焦磷酸)>H2CrO4(铬酸)>
HSCN (硫氰酸)>H3PO2(次磷酸)>H3PO3(亚磷酸)>H2SO3(亚硫酸)>
HClO2(亚氯酸)>H3PO4(磷酸)>H3AsO4(砷酸)>HNO2(亚硝酸)>
HF(氢氟酸)>HCNO(异氰酸)>H2CO3(碳酸)>H2S(氢硫酸)>
HClO(次氯酸)>HBrO (次溴酸)>HCN (氢氰酸)>H3BO3(硼酸)>
H3AsO3(亚砷酸)>H2SiO3(偏硅酸)>HIO (次碘酸)>
H2O2(过氧化氢)>HAlO2(偏铝酸)
Cs
Rb
K
Ra
Ba
Fr
Sr
Ca
Na
La
Pr
Nd
Pm
Sm
Eu
Ac
锂
铯
铷
钾
镭
钡
钫
锶
钙
钠
镧
镨
钕
钷
钐
铕
锕
Gd
Tb
Am
Y
Mg
Dy
Tm
Yb
Lu
Ce
Ho
Er
Sc
Pu
Th
Be
Np
钆
铽
镅
钇
镁
镝
铥
镱
镥
铈
钬
铒
钪
钚
钍
铍
镎
U
Hf
Al
Ti
Zr
V
Mn
Nb
Zn
Cr
Ga
Fe
Cd
In
Tl
Co
铀
铪
铝
钛
锆
钒
锰
铌
锌
铬
镓
铁
镉
铟
铊
钴
Ni
Mo
Sn
C3H6O3(乳酸)>C6H5COOH(苯甲酸)>CH2=CH-COOH(丙烯酸)>CH3COOH(醋酸)>C2H5COOH(丙酸)>C17H33COOH(油酸)>C17H35COOH(硬脂酸)>H2O·CO2(即H2CO3)(碳酸)>H2S(氢硫酸)>HClO(次氯酸)>H3BO3(硼酸)>H2SiO3(偏硅酸)>C6H5OH(苯酚)
