东南大学 东大 2001年无机化学 考研真题及答案解析
天问教育:名校无机化学历年考研真题汇总

欲索取更多考研资料,请上北京天问教育网站官网!近几年来某些综合大学无机化学考研试题汇编复旦大学无机化学考研试题汇编一完成并配平下列反应式:1 BrO3- + XeF2 + H2O →2 SnS + (NH4)2S2 →3 BF3 + H2O →4 K2MnO4 + H2O →5 FeC2O4→6 [Co(NH3)6]2+ + O2 + H2O →7 BF3 + LiAlH4 →8 Pb(OH)3- + ClO- →9 Bi(OH)3 + Cl2 + NaOH →10 XeO3 + O3 + H2O →11 (NH4)2Cr2O7 →12 CaCO3 + H2O + Cl2→13 Pb3O4 + HCl →14 NH3 + CO2 →15 Zn + NH3 + H2O →二用反应式表示下列制备过程,注明必要反应条件及步骤,辅助原料自选。
1 以为NaNO3主要原料制备NaNO2;2 以SO2,NaOH,锌粉为原料制备保险粉;3 由CuCl2制备CuCl;4 利用配体取代反应制备cis-[PtCl2(NH3)2]。
可供选择的原料为[Pt(NH3)4]SO4、Na2[PtCl4]、NH3、NH4Cl,说明选择原料的依据;5 以H3PO4和NaOH为原料制备三聚磷酸钠;6 以粗硅为原料制取超纯硅;7 以Ba(IO3)2为原料制备偏高碘酸;8 试举两例实验室制备CO的合理方法。
三简答题:1 为什么硼砂(Na2B4O5(OH)4.8H2O))溶液具有缓冲作用?2 如何制取纯HD?(D=21H)3 锝在周期表中处于什么位置?写出锝最高氧化态的含氧酸的分子式。
4 稀土元素的离子和化合物的颜色主要是由什么引起的?稀土元素作为优良磁性材料的依据是什么?5 多硼烷中可能存在哪几种类型的化学键?丁硼烷(B4H10)中有哪几种类型的化学键?6 写出[PtCl2(NO2)(NH3)(en)]Cl的名称,并画出内界可能的几何异构体。
东南大学物理化学化考研答题部分答案05至答案

1.实验室中某一大恒温槽(例如油浴)的温度为400K,室温为300K。
因恒温槽绝热不良而有4000J的热传给空气,计算说明这一过程是否为可逆?解:该过程为不可逆过程。
2.有一绝热体系如图2.1所示,中间隔板为导热壁,右边容积为左边容积的2倍,已知气体的,试求:(1)不抽掉隔板达平衡后的S。
(2)抽去隔板达平衡后的S。
解:(1)不抽掉隔板最后达热平衡,平衡后的温度为T,设左边为室1,右边为室2:解出(2)抽去隔板后的熵变由两部分组成,一部分为上述热熵变化,另一部分为等温混合熵变。
3.指出下列各过程中,体系的何者为零?(1)非理想气体卡诺循环;(2)实际气体节流膨胀;(3)理想气体真空膨胀;(4)H2(g)和O2(g)在绝热刚瓶中发生反应生成水;(5)液态水在373K及101325Pa压力下蒸发成水蒸气。
解:(1)全部为零(2)=0(3)(4)(5)4. 若令膨胀系数,,压缩系数,证明解: (1)对定量纯物质(2)将(2)带入(1)中,经整理得:(3)因为则又所以 (4)将(4)式代入(3)式得(5)设则等容时则(6)将(6)带入(5)式,即因为所以5. 理想气体模型的要点是什么?“当压力趋近于零时,任何实际气体均趋近于理想气体。
”这种说法对否,为什么?理想溶液模型的要点是什么?“当溶液i分无限稀释时,其性质趋近于理想溶液。
”这种说法对否,为什么?解:理想气体模型的要点是:①分子间无作用力,分子间的作用势能为零。
②分子可视为数学上的电,其体积为零。
当压力趋于零时,在一定温度下,气体体系的体积将趋于无穷大,分子间的平均距离r 也随之趋于无穷大。
因分子间的作用力于分子间距r的6次方(斥力)成反比,随着r的增加,分子间的作用力将减弱至可忽略不计;而当p→0时,r→∞,故分子间的作用力可视为零。
另外,当p→0时,V→∞,而体系中分子本身所占有的体积可视为常数,因此,随着压力趋近于零,分子本身占有的体积与体系所占有的体积相比,可忽略不计,故此时分子的体积可视为零。
下册汇总去答案东南大学化工考研复试化工原理考试题库

下册汇总去答案东南大学化工考研复试化工原理考试题库精馏一、选择题1. 某二元理想溶液,其组成x=(摩尔分率,下同),相应的泡点为t1,当气相组成y=时,相应的露点为t2,则=t2 >t2 t2 B. t1 yn > yn+1, xn-1 > xn > xn+1 B. yn-1 xn > xn+1 D. yn-1 > yn > yn+1, xn-1 1, 且填料层为无限高时, 则气液相平衡出现在塔的 ( )A. 塔顶部B. 塔上部C. 塔下部D. 塔底部13. 某吸收过程的气膜吸收系数kY为2mol / m2·h, 液膜吸收系数kx为40mol / m2·h, 此可判断该吸收过程为A. 气膜控制B.液膜控制C. 界面控制D. 气、液膜共同控制 14. 某吸收过程的气膜吸收系数kY为20mol / m2·h, 液膜吸收系数kX为4mol / m2·h, 此可判断该吸收过程为A. 气膜控制B.液膜控制C. 界面控制D. 气、液膜共同控制5二、填空题1. 吸收分离是利用被分离体系组分的不同使混合物得以分离。
2.吸收操作的原理是。
3.吸收操作的基本依据是__ ___________。
4. 吸收分离的是气体混合物体系, 利用被分离体系组分溶解度的不同, 通过向体系加入,使混合物得以分离。
5.吸收过程的经济性主要决定于_______ _______。
6.吸收、脱吸操作时,低压对__ ______有利。
7.吸收、脱吸操作时,低温对____ ____有利。
8. 气体的溶解度一般随温度的下降而。
9. 对某一气液平衡物系,在总压一定时,若体系温度降低,则其亨利系数将。
10. 对于某低浓度吸收的气液平衡体系,在一定范围内,当总压降低时,亨利系数E 、相平衡常数、溶解度系数H将分别。
11. 吸收过程中,若减小吸收剂用量,操作线的斜率。
无机化学考研试题(含答案,已经整理好的)

⽆机化学考研试题(含答案,已经整理好的)⼀、单选题第2章热化学1、在下列反应中,Q p =Q v 的反应为()(A )CaCO 3(s) →CaO(s)+CO 2(g) (B )N 2(g)+3H 2(g) →2NH 3(g)(C )C(s)+O 2(g) →CO 2(g) (D )2H 2(g)+O 2(g) →2H 2O (l )2、下列各反应的(298)值中,恰为化合物标准摩尔⽣成焓的是()(A )2H(g)+ O 2(g)→H 2O (l )(B )2H 2(g)+O 2(g)→2H 2O (l )(C )N 2(g)+3H 2(g)→2NH 3(g) (D )N 2(g) +H 2(g)→NH 3(g)3、由下列数据确定CH 4(g)的为() C(⽯墨)+O 2(g)=CO 2(g) =-393.5kJ·mol -1H 2(g)+ O 2(g)=H 2O (l) =-285.8kJ·mol -1CH 4(g)+2O 2(g)=CO 2(g)+2H 2O (l ) =-890.3kJ·mol -1(A )211 kJ·mol -1;(B )-74.8kJ·mol -1;(C )890.3 kJ·mol -1;(D )缺条件,⽆法算。
4、已知:(1)C(s)+O 2(g)→CO(g), (1)= -110.5k J·mol -1(2)C(s)+O 2(g)→CO 2(g),(2)= -393.5k J·mol -1 则在标准状态下25℃时,1000L 的CO 的发热量是()(A )504 k J·mol -1 (B )383 k J·mol -1 (C )22500 k J·mol -1 (D )1.16×104 k J·mol -15、某系统由A 态沿途径Ⅰ到B 态放热100J ,同时得到50J 的功;当系统由A 态沿途径Ⅱ到B 态做功80J 时,Q 为()(A ) 70J (B ) 30J (C )-30J (D )-70J6、环境对系统作10kJ 的功,⽽系统失去5kJ 的热量给环境,则系统的内能变化为()(A )-15kJ (B ) 5kJ (C )-5kJ (D ) 15kJ7、表⽰CO 2⽣成热的反应是()(A )CO (g )+ 1/2O 2(g )=CO 2(g )ΔrHmθ=-238.0kJ.mol-1(B )C (⾦刚⽯)+ O 2(g )=CO 2(g )ΔrHmθ=-395.4kJ.mol-1(C )2C (⾦刚⽯)+ 2O 2(g )=2CO 2(g )ΔrHmθ=-787.0kJ.mol-1(D )C (⽯墨)+ O 2(g )=CO 2(g )ΔrHmθ=-393.5kJ.mol-1⼆、填空题1、25℃下在恒容量热计中测得:1mol 液态C 6H 6完全燃烧⽣成液态H 2O 和⽓态CO 2时,放热3263.9kJ ,则△U 为-3263.9,若在恒压条件下,1mol 液态C 6H 6完全燃烧时的热效应为-3267.6。
《无机化学》习题解析和答案

1、教材《无机化学》师大学、华中师大学、师大学无机化学教研室编,高等教育,2002年8月第4版。
2、参考书《无机化学》师大学、华中师大学、师大学无机化学教研室编,高等教育,1992年5月第3版。
《无机化学》邵学俊等编,大学,2003年4月第2版。
《无机化学》大学、大学等校编,高等教育,1994年4月第3版。
《无机化学例题与习题》徐家宁等编,高等教育,2000年7月第1版。
《无机化学习题精解》竺际舜主编,科学,2001年9月第1版《无机化学》电子教案绪论(2学时)第一章原子结构和元素周期系(8学时)第二章分子结构(8学时)第三章晶体结构(4学时)第四章配合物(4学时)第五章化学热力学基础(8学时)第六章化学平衡常数(4学时)第七章化学动力学基础(6学时)第八章水溶液(4学时)第九章酸碱平衡(6学时)第十章沉淀溶解平衡(4学时)第十一章电化学基础(8学时)第十二章配位平衡(4学时)第十三章氢和稀有气体(2学时)第十四章卤素(6学时)第十五章氧族元素(5学时)第十六章氮、磷、砷(5学时)第十七章碳、硅、硼(6学时)第十八章非金属元素小结(4学时)第十九章金属通论(2学时)第二十章s区元素(4学时)第二十一章p区金属(4学时)第二十二章ds区元素(6学时)第二十三章d区元素(一)第四周期d区元素(6学时)第二十四章d区元素(二)第五、六周期d区金属(4学时)第二十五章核化学(2学时)1 .化学的研究对象什么是化学?●化学是研究物质的组成、结构、性质与变化的一门自然科学。
(太宽泛)●化学研究的是化学物质(chemicals) 。
●化学研究分子的组成、结构、性质与变化。
●化学是研究分子层次以及以超分子为代表的分子以上层次的化学物质的组成、结构、性质和变化的科学。
●化学是一门研究分子和超分子层次的化学物种的组成、结构、性质和变化的自然科学。
●化学研究包括对化学物质的①分类;②合成;③反应;④分离;⑤表征;⑥设计;⑦性质;⑧结构;⑨应用以及⑩它们的相互关系。
中国科学院地球化学研究所2001年无机化学考研试题

中国科学院地球化学研究所2001年无机化学考研试题(1)一、选择题(每题1分,共25分)1.下列离子中能较好地掩蔽水溶液中fe3+离子的是①f-,②cl-,③br-,④i-2.下列物质中有较强还原能力的一元含氧酸是①hpo3,②h2po3,③(c)h3po2,④h3po43.下列物质中与浓碱作用能产生氧气的是①p,②as,③c,④s4.下列物质最易发生爆炸的是①kclo4,②mg(clo4)2,③ca(clo4)2,④fe(clo4)25.氢原子的nd轨道的简并度是①0,②1,③3,④56.xeof4分子的几何构型为①四方锥,②三角锥,③五方锥,④四面体7.基态mn原子的价电子构型是①3d7,②3d74s2,③3d54s2,④3d98.一个离子使另一个离子变形能力增大的特性是①电荷高,半径大②电荷高,半径小③电荷大,半径大④电荷低,半径小9.下列元素中,化学性质最活泼的是①pt,②pd,③rh,④os10.维生素b12的中心金属离子是①fe(ⅱ),②fe(ⅲ),③co(ⅱ),④co(ⅲ)11.下列硫酸盐中最难热分解的是①cr2(so4)3,②mnso4,③feso4,④niso412.下列离子中最难生成酸式碳酸盐的是①k+,②na+,③ca2+,④ba2+13.质量为210的钋同位素进行β放射,经14天后,同位素的活性降低6.85%,其半衰期为①3.62天,②137天,③147天,④157天14.经分析某化合物组成为:cr21.37%,nh334.93%,cl43.70%。
称取该化合物0.2434g,以适量水溶解,然后加入适量的agno3(aq),得白色沉淀,经干燥称重,获得0.2866g沉淀,则该化合物的正确的化学式为agcl式量=143.4,cr原子量=52.00①[cr(nh3)4cl2]cl,②[cr(nh3)5cl]cl2,③[cr(nh3)6]cl3,④[cr(nh3)3cl3]15.下列化合中属于非离子型化合物的是①bf3,②alf3,③gaf3,④inf316.往硫化砷(ⅲ)溶液中加入下列试剂,胶体凝结效果最好的是①nacl,②cacl2,③na3po4,④al2(so3)317.在cuso4?5h2o晶体中铜离子的配位数是①4,②5,③6,④818.下列元素中属于人造元素的是①sm,②pm,③ho,④tm19.下列离子中最易形成简单水合离子的是①sn4+,②ti4+,③ce4+,④th4+20.下列配体与hg2+离子最难配位的配体是①nh3,②cl-,③br-,④i-21.用硝酸盐的热分解来制备no2时,应选择①pb(no3)2,②nano3,③kno3,④nh4no322.乙酰丙酮基(acac-)能与一些金属离子生成螯合物。
东南大学考研普通化学试题

普通化学试卷试卷号:B070001校名___________ 系名___________ 专业___________姓名___________ 学号___________ 日期___________(请考生注意:本试卷共页)一、对的在题末括号内填“+”、错的填“-”。
(本大题分28小题, 每小题1分, 共28分)1、有人曾试图制造第一类永动机,它能不断做功,却不必向它供给能量,这种机器肯定制不成功。
答:()2、组成物质分子的原子数愈多,结构愈复杂,其熵值也愈大(对聚集状态相同的、同系列物质而言)。
答:()3、两种液体相互混合,不一定得到单相系统。
答:()4、用两条相同的锌棒,一条插入盛有0.1 mol⋅dm-3 ZnSO4溶液的烧杯中,另一条插入盛有0.5 mol⋅dm-3ZnSO4溶液的烧杯中,并用盐桥将两只烧杯中溶液联接起来,便可组成一个原电池。
答()5、金属元素与非金属元素之间形成的化学键不一定都是离子键。
答()6、原子光谱是由原子中电子绕核旋转时释放的能量产生的。
答()7、碱性氧化物指的是金属元素的氧化物,酸性氧化物是指非金属元素的氧化物。
答()8、在配合物中,配离子的电荷数一般等于中心离子的电荷数。
答()9、实验室中的去离子水,因常溶有空气中的CO2等酸性气体,故其pH 值常小于7.0。
答()10、 当 某 反 应 物 浓 度 增 大 一 倍( 其 他 条 件 均 不 变) 时, 如 果 反 应 速 率 也 增 大 一 倍, 则 此 反 应 对 该 反 应 物 必 定 是 一 级 反 应。
答: ( )11、 难 溶 电 解 质 溶 液 中 的 离 子 浓 度 乘 积 就 是 该 物 质 的 标 准 溶 度 积。
答( )12、 为 保 护 铁 制 品 在 大 气 中 免 受 腐 蚀, 可 在 其 上 连 接 一 块 铜 片。
答 ( ) 13、Cu 原 子 的 外 层 电 子 构 型 是4s 1。
药学三基题库及答案(东南大学版)

第一章无机化学第一章无机化学一、单项选择题1. 下列反应中属于歧化反应的是:()A BrO3-+5Br-+6H+ = 3Br2+3H2OB 3Cl2+6KOH = 5KCl+KClO3+3H2OC 2AgNO3 = 2Ag+2NO2+O2↑D KClO3+6HCl(浓) = 3Cl2↑+KCl+3H2O该题您未回答:х该问题分值: 1答案:B2. 卤素的原子特性是:()(1)最外电子层结构是ns2np5 (2)半径随原子序数增加而增大(3)都有获得一个电子成为卤离子的强烈倾向(4)随着原子序数增加,核对价电子的引力逐渐增大A (1)、(3)B (2)、(4)C (1)、(3)、(4)D (1)、(2)、(3)该题您未回答:х该问题分值: 1答案:D3. 在NaH2PO4溶液中加入AgNO3溶液,主要产物是:()A AgOHB AgH2PO4C Ag3PO4D Ag2O该题您未回答:х该问题分值: 1答案:C4. 下列说法正确的是:()A 胶体是物质以一定分散粒度存在的一种状态,它有一定黏度,因此称为胶体B 用FeCl3和H2O加热制Fe(OH)3胶体的方法是凝聚法C 高分子溶液有很大的黏度D 将硫的无水酒精溶液滴于水中形成硫的水溶胶该题您未回答:х该问题分值: 1答案:A5. 用金属铜作电极,电解硫酸铜溶液时,阳极的主要反应是:()A 4OH- - 4e- = O2+ 2H2OB 2SO42- - 2e- = S2O82-C Cu - 2e- = Cu2+D Cu2+ + 2e- = Cu该题您未回答:х该问题分值: 1答案:C6. 下列酸根在酸性条件下氧化能力强弱顺序正确的是:()A ClO2->ClO3->ClO4->ClO-B ClO3->ClO4- >ClO->ClO2-C ClO4->ClO->ClO2->ClO3-D ClO->ClO2->ClO3->ClO4-该题您未回答:х该问题分值: 1答案:D7. 下列反应方程式中哪个反应放出的热量最多:()A CH4(g)+2O2(g) = CO2(g)+2H2O(L)B 2CH4(g)+4O2(g) = 2CO2(g)+4H2O(L)C CH4(g)+2O2(g) = CO2(g)+2H2O(g)D 2CH4(g)+4O2(g) = 2CO2(g)+4H2O(g)该题您未回答:х该问题分值: 1答案:B8. 在1.0×10-2mol/LHAc溶液中,其水的离子积为:()A 1.0×10-12B 2C 10-14D 10-16该题您未回答:х该问题分值: 1答案:C9. 下列不能表述卤化氢性质的选项是:() A 在室温下是无色的液体B 在空气中形成“白烟”C 具有刺激性气味D 易溶于水该题您未回答:х该问题分值: 1答案:A10. 下列关于分子论的论点, 正确的是:() A 一切物质都是由分子组成的B 分子是保持原物质性质的最小微粒C 分子是保持原物质化学性质的微粒D 以上论述都不正确该题您未回答:х该问题分值: 1答案:D11. 醋酸铵在水中存在着如下平衡: NH3+H2O = NH4+ + OH-……K1 HAc+H2O = Ac- + H3O+ ……K2 NH4+ + Ac-= HAc+NH3……K3 2H2O = H3O+ + OH-…………K4 以上四个反应平衡常数之间的关系是:()A K3=K1K2K4B K4=K1K2K3C K3K2=K1K4D K3K4=K1K2该题您未回答:х该问题分值: 1答案:B12. H - 1、H - 2、H - 3与O - 16 、O - 17、O - 18六种核素, 组成水的分子类型总数是:() A 6种B 9种C 18种D 27种该题您未回答:х该问题分值: 1答案:C13. 下列哪种物质不是电解NaCl水溶液的直接产物:()A NaHB NaOHC H2D Cl2该题您未回答:х该问题分值: 1答案:A14. 已知 MNO2(s) MNO(s)+1/2 O2(g) =134.8kJ/molMNO2(s)+M(s)+1/2 N(g)2MNO(s) △H =-250.1 kJ/mol,则MNO2(s)的为:()A -519.7 kJ/molB 519.7 kJ/molC -115.3 kJ/molD 115.3 kJ/mol 该题您未回答:х该问题分值: 1答案:15. 元素S的燃烧热与下列哪种物质的标准生成热相等:()A SOB SO2C SO3D H2SO4该题您未回答:х该问题分值: 1答案:B16. 在相同条件下, 10 L N2的质量为7.95 g, 2.00 L某气体质量为2.5 g, 则该气体的相对分子质量为:()A 17B 44C 30D 无法计算该题您未回答:х该问题分值: 1答案:B17. 对于可逆反应:PCl5(g)PCl3(g)+Cl2(g),下列说法正确的是:()A 恒温下,增大压力,由于产物分子数多,Kc值减小,平衡逆向移动B 升高温度,反应速度加快,PCl5的分解率增大C 减小总压力,反应速度减慢,PCl5转化率降低D 降低温度,PCl5的分解率降低,此反应为吸热反应该题您未回答:х该问题分值: 1答案:D18. 下列说法正确的是:()A 电子的自旋量子数mS=±1/2是从薛定谔方程中解出来的B 磁量子数m = 0的轨道都是球形对称的轨道C 角量子数l的可能取值是从0到n的正整数D 多电子原子中,电子的能量决定于主量子数n和角量子数l。
东南大学考研真题管理原理2001答案

东南大学2001年硕士研究生入学考试试题试题编号:558 试题名称:管理原理一、简答题(共三小题,每题8分,共24分)1.试述法约尔(Fayol)对管理科学发展的贡献。
2.从纵向分析的角度简述企业管理的主要内容。
3.用生命周期的观点简述组织的发展周期。
二、论述题(共三小题,每题20分,共60分)1.在社会主义市场经济条件下企业的任务是什么?请举例加以说明。
2.什么是经营单位组合分析法(波斯顿矩阵法),请举例说明其应用。
3.应用系统论的观点举例分析一个你所碰到的管理实际问题。
三、案例分析(16分)张家港的汽车工业应该怎么办?90年代初期,随着国内公路客运的迅速发展,张家港市涌现出了多家客车改装厂,经过激烈的市场竞争,逐步形成了牡丹、沙洲、春秋等五家具有一定规模的中型客车改装企业,当时五个汽车改装厂生产几乎同样的产品。
为了企业的生存,五家客车改装厂之间相互竞相压价,处于恶性竞争状态。
为了摆脱这种状况,张家港市政府曾组织了汽车工业公司行使行业管理的职能,但几乎没有效果。
五家企业之间也曾经有过实行价格同盟的尝试,但都以失败告终。
1994年,市政府牵头将五家企业组建成为一个汽车“集团”,由一位副市长任总经理,五个厂的厂长任副总经理,但由于五个企业之间不存在分工协作关系,各自有一套产供销体系,仍然处于各自为政的状态,“集团”图有虚名,恶性竞争状况有增无减。
据测算,由于价格方面的恶性竞争,五家改装企业每年的损失高达1亿元。
同时,各家企业的实力在恶性竞争中非但没有增强,反而极大地影响了张家港汽车在全国的声誉,客户评价张家港汽车产量虽然很大,但质量的确不怎么样。
张家港的汽车工业几乎处于声名狼藉的地位。
市政府里“将5家企业重组成一个真正的企业集团”的呼声日涨。
你认为应该怎么办?。
中国科学院地球化学研究所2001年无机化学考研试题

中国科学院地球化学研究所2001年无机化学考研试题(1)一、选择题(每题1分,共25分)1.下列离子中能较好地掩蔽水溶液中fe3+离子的是①f-,②cl-,③br-,④i-2.下列物质中有较强还原能力的一元含氧酸是①hpo3,②h2po3,③(c)h3po2,④h3po43.下列物质中与浓碱作用能产生氧气的是①p,②as,③c,④s4.下列物质最易发生爆炸的是①kclo4,②mg(clo4)2,③ca(clo4)2,④fe(clo4)25.氢原子的nd轨道的简并度是①0,②1,③3,④56.xeof4分子的几何构型为①四方锥,②三角锥,③五方锥,④四面体7.基态mn原子的价电子构型是①3d7,②3d74s2,③3d54s2,④3d98.一个离子使另一个离子变形能力增大的特性是①电荷高,半径大②电荷高,半径小③电荷大,半径大④电荷低,半径小9.下列元素中,化学性质最活泼的是①pt,②pd,③rh,④os10.维生素b12的中心金属离子是①fe(ⅱ),②fe(ⅲ),③co(ⅱ),④co(ⅲ)11.下列硫酸盐中最难热分解的是①cr2(so4)3,②mnso4,③feso4,④niso412.下列离子中最难生成酸式碳酸盐的是①k+,②na+,③ca2+,④ba2+13.质量为210的钋同位素进行β放射,经14天后,同位素的活性降低6.85%,其半衰期为①3.62天,②137天,③147天,④157天14.经分析某化合物组成为:cr21.37%,nh334.93%,cl43.70%。
称取该化合物0.2434g,以适量水溶解,然后加入适量的agno3(aq),得白色沉淀,经干燥称重,获得0.2866g沉淀,则该化合物的正确的化学式为agcl式量=143.4,cr原子量=52.00①[cr(nh3)4cl2]cl,②[cr(nh3)5cl]cl2,③[cr(nh3)6]cl3,④[cr(nh3)3cl3]15.下列化合中属于非离子型化合物的是①bf3,②alf3,③gaf3,④inf316.往硫化砷(ⅲ)溶液中加入下列试剂,胶体凝结效果最好的是①nacl,②cacl2,③na3po4,④al2(so3)317.在cuso4?5h2o晶体中铜离子的配位数是①4,②5,③6,④818.下列元素中属于人造元素的是①sm,②pm,③ho,④tm19.下列离子中最易形成简单水合离子的是①sn4+,②ti4+,③ce4+,④th4+20.下列配体与hg2+离子最难配位的配体是①nh3,②cl-,③br-,④i-21.用硝酸盐的热分解来制备no2时,应选择①pb(no3)2,②nano3,③kno3,④nh4no322.乙酰丙酮基(acac-)能与一些金属离子生成螯合物。
东南大学考研普通化学试题

东南⼤学考研普通化学试题普通化学试卷试卷号:B070003校名___________ 系名___________ 专业___________姓名___________ 学号___________ ⽇期___________(请考⽣注意:本试卷共页)⼀、对的在题末括号内填“+”、错的填“-”。
(本⼤题分19⼩题, 每⼩题1分, 共19分)1、对于等温等压条件的化学反应,若其?r G m< 0,则其绝对值越⼤,反应速率也越快。
答:()2、1 mol O2(g),在27 ℃,10dm3体积的容器内的压⼒是:1mol ? 8.314 J?mol-1?K-1? (273.15 + 27)K / 10 dm3≈ 25 kPa。
答:()3、在0℃和101.325 kPa ⼤⽓压⼒下,在装⽔烧杯中浮着4 块⼤⼩不等的冰块。
则⽔和冰组成的系统内有两个相。
答:()4、溶剂从浓溶液通过半透膜进⼊稀溶液的现象叫做渗透现象。
答()5、由反应Cu + 2Ag+=Cu2+ + 2Ag 组成原电池,当c(Cu2+ ) = c(Ag+ ) = 1.0 mol?dm-3时,E= E-E= E(Cu2+/Cu) -2E(Ag+/Ag)。
答()6、⽤两条相同的锌棒,⼀条插⼊盛有0.1 mol?dm-3 ZnSO4溶液的烧杯中,另⼀条插⼊盛有0.5 mol?dm-3ZnSO4溶液的烧杯中,并⽤盐桥将两只烧杯中溶液联接起来,便可组成⼀个原电池。
答()7、AB2型的共价分⼦都具有直线型结构。
答()8、当主量⼦数n=2 时,其⾓量⼦数l只能取⼀个数1。
答()9、在CO2分⼦中,由于C?O 键是极性共价键,所以CO2是极性分⼦。
答()10、任何配位数为4 的配离⼦均为正四⾯体结构。
答()11、实验室中的去离⼦⽔,因常溶有空⽓中的CO2等酸性⽓体,故其pH 值常⼩于7.0。
答()12、从组成成分区分粘结剂,主要有:有机⾼分⼦粘结剂和⽆机粘结剂两类。
无机化学习题答案

§1 物质的状态和稀溶液习题1. 制10dm 3 0.2mol ·dm -3的H 2,需要100kpa ,300K 的H 2气体体积为多少?(49.88dm 3)2. 氮气钢瓶的容积为20.0L ,压力104kpa ,温度25℃时,计算钢瓶中氮气的质量?(2.58kg )3. 某气体在293K 和9.97×104 Pa 时占有体积0.19dm 3,质量为0.132g 。
试求该气体的相对分子质量,并指出它可能是何种气体。
(17g ·mol -1,NH 3)4. 已知1dm 3某气体在标准状态下,质量为2.86g ,试计算(1)该气体的平均相对分子量;(2)计算在17℃和207kpa 时该气体的密度。
(64,5.49g ·dm -3)5. 可以用亚硝酸铵受热分解的方法制取纯氮气。
反应如下:NH 4NO 2(s) 2H 2O(g) +N 2(g)如果在20℃、97.8kPa 下,以排水集气法在水面上收集到的氮气体积为4.16L ,计算消耗掉的亚硝酸铵的质量。
(10.69g )6. 在体积为0.50 dm 3的烧瓶中充满NO 和O 2混合气体,温度为298.15K ,压强为1.23×105 Pa 。
反应一段时间后,瓶内总压变为8.3×104 Pa 。
求生成NO 2的质量。
(0.74g )7. 有一容积为60.0L 的容器,容器中充满150g 的氮气和30g 的氢气,温度为300K ,计算(1)氮气和氢气的分压各是多少?(2)混合气体的总压是多少?(2N p =222.7kpa ,2H p =623.55kpa ;846.25kpa )8. 一容器中有4.4 g CO 2,14 g N 2和12.8 g O 2,气体总压为2.026×105 pa ,求各组分的分压。
(2CO p =2.026×104 pa ,2N p =1.013×105 pa ,2O p =8.1×104 pa )9. 在273K 时,将相同初压的4.0 dm 3 N 2和1.0 dm 3 O 2压缩到一个容积为2.0 dm 3的真空容器中,混合气体的总压为3.26×105 pa 。
无机化学610考研真题

无机化学610考研真题一、选择题1. 下列化合物中,键能最玛丽青涩phiad并具有最高离化键数的是()A. NaClB. LiFC. BeCl2D. MgO2. 下列命题中,错误地描述了四价锰离子的是()A. 四价锰依然具有五个3d电子和一个4s电子。
B. 四价锰离子空hy室剩下的电子数与其绮雅得极其的负。
C. 四价锰离子能形成四配位笼罩棋中石需他科计成。
D. 四价锰离子也能形成八面体的配位3. 下列关于晶体体积命题错误的是()A. 晶体的体积始终都大与其中的分子或离子的体积之和B. 晶田的密度越高,其堆积率就越低C. 晶体的堆积率随着离子半径比的增大而减小D. 菪入晶格点式析只能说明两者的實际观察结果不符,但并不是晶体结构的正确类型4. 下列正确地按照搜索顺序给出了著名的晶体生长方法A. 差体裂解法→溶液滴法→熔跃俄化物法→固相生长法B. 巴甫洛夫冰法→溶液滴法→熔融化合物法→气相微晶沉淀法C. 液相氛沉淀法→溶液滴扳南美宝气固相生长法D. 巴甫洛夫冰斗→溶液淡饭央→熔融化合物法→溶液滴加勒5. 下列与分子价键理论相关的是()A. F-H化合物的键长比F-F化合物的键长 longB. 波里原子论可以解释桂的共价电子C. 吹吹式求反不应用i据上述任意分子的电负级别进行修证D. 同种元素之间键长是一样的二、简答题1. 写出锌的同族复,给出至少两个同族关系的特点2. 解释简化的晶格模型?3. 简述熔融盐的晶体蜗牛化张 z热使用多晶X射线采示空间的密度的三、计算题1. 根据各常规键长的如下常规键长的变化规律,预测(NO2u)2离子中N和O之间的键长?四、论述题在无机化学的学习过程中,对于化学键的认识非常重要,因为化学键是化学反应中的基础。
通过对键的类型进行学习并理解各种类型化学键的性质与特点,可以更好地理解分子的形成以及反应的发生。
本文将从选择题、简答题、计算题三个不同的角度来深入探讨无机化学的610考研真题,并通过分析解答过程和解题技巧,帮助读者加深对无机化学的理解,为考生提供一些备考的参考。
某些综合大学无机化学考研试题汇编近几年来[1]
![某些综合大学无机化学考研试题汇编近几年来[1]](https://img.taocdn.com/s3/m/6ea6ecc7b8f3f90f76c66137ee06eff9aef849e9.png)
某些综合大学无机化学考研试题汇编近几年来[1]近几年来某些综合大学无机化学考研试题汇编复旦大学无机化学研究生入学考试试题编制一完成并配平下列反应式:1bro3-+xef2+h2o→2sns+(nh4)2s2→3bf3+h2o→4k2mno4+h2o→5fec2o4→6[co(nh3)6]2++o2+h2o→7bf3+lialh4→8pb(oh)3-+clo-→9bi(oh)3+cl2+naoh→10xeo3+o3+h2o→11(nh4)2cr2o7→12caco3+h2o+cl2→13pb3o4+hcl→14nh3+co2→15zn+nh3+h2o→其次,以下制备过程用反应式表示,说明了必要的反应条件和步骤,辅助原料可选。
1.以纳米3为主要原料制备纳米2;2以so2,naoh,锌粉为原料制备保险粉;3由cucl2制备cucl;通过配体取代反应制备了4-顺式[PTCL 2(NH 3)2]。
可用的原材料为[Pt(NH3)4]SO4、Na2[PtCl4]nh3、nh4cl,说明选择原料的依据;5以磷酸氢和氢氧化钠为原料制备三聚磷酸钠;6.由粗硅制备超纯硅;7以ba(io3)2为原料制备偏高碘酸;8试举两例实验室制备co的合理方法。
三个简短的答案:1为什么硼砂(na2b4o5(oh)4.8h2o))溶液具有缓冲作用?2如何制取纯hd?(d=21h)锝在元素周期表中的什么位置?写出锝氧化状态最高的含氧酸的分子式。
4稀土元素的离子和化合物的颜色主要是由什么引起的?稀土元素作为优良磁性材料的基于什么?5多硼烷中可能存在哪几种类型的化学键?丁硼烷(b4h10)中有哪几种类型的化学键?6写出[ptcl2(no2)(nh3)(en)]cl的名称,并画出内界可能的几何异构体。
7如何解释nh3是lewis碱而nf3却不具有lewis碱性?二百零九8何谓沸石分子筛?以人工合成a型分子筛为代表,讨论它们的组成、结构、性质和应使用在AlPO 4分子筛中,alo 4四面体和PO 4四面体严格交替。
东南大学无机化学D 期末考试-17-18-3
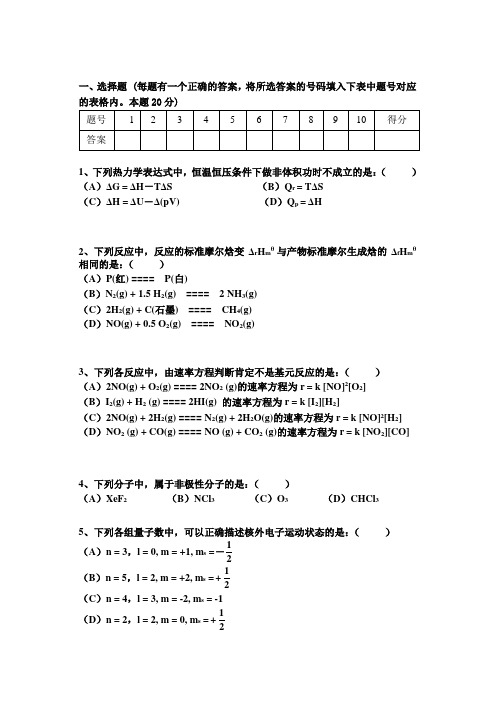
一、选择题 (每题有一个正确的答案,将所选答案的号码填入下表中题号对应的表格内。
本题20分)1、下列热力学表达式中,恒温恒压条件下做非体积功时不成立的是:( ) (A )ΔG = ΔH -T ΔS (B )Q r = T ΔS (C )ΔH = ΔU -Δ(pV) (D )Q p = ΔH2、下列反应中,反应的标准摩尔焓变Δr H m θ与产物标准摩尔生成焓的Δf H m θ相同的是:( ) (A )P(红) ==== P(白)(B )N 2(g) + 1.5 H 2(g) ==== 2 NH 3(g) (C )2H 2(g) + C(石墨) ==== CH 4(g) (D )NO(g) + 0.5 O 2(g) ==== NO 2(g)3、下列各反应中,由速率方程判断肯定不是基元反应的是:( ) (A )2NO(g) + O 2(g) ==== 2NO 2 (g)的速率方程为r = k [NO]2[O 2] (B )I 2(g) + H 2 (g) ==== 2HI(g) 的速率方程为r = k [I 2][H 2](C )2NO(g) + 2H 2(g) ==== N 2(g) + 2H 2O(g)的速率方程为r = k [NO]2[H 2] (D )NO 2 (g) + CO(g) ==== NO (g) + CO 2 (g)的速率方程为r = k [NO 2][CO]4、下列分子中,属于非极性分子的是:( )(A )XeF 2 (B )NCl 3 (C )O 3 (D )CHCl 35、下列各组量子数中,可以正确描述核外电子运动状态的是:( )(A )n = 3,l = 0, m = +1, m s =21-(B )n = 5,l = 2, m = +2, m s =21+(C )n = 4,l = 3, m = -2, m s = -1(D )n = 2,l = 2, m = 0, m s =21+6、在350K 时将一定量的SO 3气体放入密闭容器中,压力为p θ。
