有机合成方法大全目录(部分)
有机合成新方法

有机合成新方法化工05-1 李光06052550摘要:本文先简单得介绍了有机化学的发展,然后花大篇幅介绍了有机合成方法的新方法及新进展。
关键词:有机化学新方法有机合成前言: (4)1有机化学的发展 (4)2有机合成方法的一些新方法新进展 (4)2.1组合合成 (5)2.2不对称合成 (5)2.3绿色合成 (6)2.4金属参与的有机合成反应 (6)2.5金参与的有机合成反应 (6)2.6微波技术在液相有机合成中的应用 (6)结语 (7)参考文献 (8)前言:随着人类社会进入二十一世纪,科学技术高速发展,与此同时,化工合成行业已经形成一个比较完善,有一定系统的行业,特别是有机合成的发展很大程度上促进了人类社会的发展。
随着人们对生活质量要求的越来越高,有机合成行业一直在不断根新,新的合成方法不断出现。
1有机化学的发展虽然纪年历法仅是一个人为约定的相对时间标记,但人们还是对纪年中的十、百、千年不惜以大量的笔墨去回顾和展望。
8年前,我们经历了公元纪年的新世纪,正好又是千年的转换,所以很热闹了一阵。
自然科学也正好经历了发展中最快速的100 年,化学及其最丰富多彩的有机化学也同样经历了一个日新月异的世纪。
因此我们不难在报章杂志上看到众多名家借此机会总结化学的辉煌百年,并预言更辉煌的新世纪。
现在,进入新世纪已8年了,8年在历史长河中只是一个极短暂的瞬间,即使就近代自然科学的发展来讲也不是一段很长的时间,但人们还是会问这8年中有些什么过去曾预料到的或者不曾料到的发展动向和迹象。
下面是自己从很小的角度观察的有机化学的进展以及记录下来的一些看法。
一段时期以来,有机化学界都注意到了生命科学、材料科学以及环境科学等是今后有机化学大有发展的领域,而这些领域中对有机化学提出的要求又正是有机合成、有机分析和物理有机化学最具挑战性的课题。
生命科学在这8年中的大事件是完成了人类基因组的测定,从而也开始了后基因组、蛋白质组研究的新时期。
有机合成方法

NaOH
R OCH2
苄基醚
H3+O
R OH +
CH2OH
H2 Pd
R OH +
CH3
-OH
C6H5COCl OH-, H2O
-OCOC6H5
BACK
基团的保护和去保护
• 羟基的保护
HOH2C O Base H H + MeO H H OH OH
吡啶
C Cl
MeO
20℃
C OCH2
O Base H H
(2)性质
COOC 2H5 CH 2 COOC 2H5 COOC 2H5 Na CH COOC 2H5 pKa = 13
NaOC 2H5
丙二酸二乙酯在有机合成中的应用 丙二酸二乙酯的上述性质在有机合成上广泛用于合成各 种类型的羧酸(一取代乙酸,二取代乙酸,环烷基甲酸,
二元羧酸等)。
用丙二酸二乙酯法合成下列化合物,其结构分析如下:
C OR C N
,
C , SH C P C R ,
C N+ C H C C
,
, C C CR
官能团的引入与转化
• 官能团的转化:
CH2COOH CONR2
LiAlH4 LiAlH4
官能团的去除
OH H CH2OH
Cr6+
O
H
H
Cr6+ NaBH4
CH2OH CH2NR2
CHO
LiAlH4
Cr6+
OH (4)
H2SO4
OH
SO3H O
(5)
H2/Pt
OH
BACK
基团的保护和去保护
• 请判断下列转化是否能实现,请简述理由。
有机合成方法

540
还原和加氢
不饱和键的加氢 硝基的还原
常用的还原剂: 催化氢化:
O (Ph3P)3RhCl H2, C6H6 O
催化剂的选择性可以通过配体来调节
化学还原法
有两种主要形式: 其一是电子,对不饱和化合物进行加成,继而 质子转移,该方法中金属作为电子的来源,水、 醇、酸作为质子的供给体
NaX
三烷基锍盐 (锍叶立徳) [H]
RSO2Cl
RSO2H (亚磺酸)
一定条件下产生的硫自由基,可以和卤代烷进行反应 生成硫醚,产物的收率较高
Br R
78.C BuLi S R
S
S RCH2Br Lett., 2002,43:2145
胺(伯胺)
R C N RNO2 [H] [H] NH3
HBr
H2O
O R NH C OH
CO2
RNH2
芳香族化合物的重排反应
Fries重排
R N NO HX NHR NO NHR
NO
联苯胺重排
NHNH
H2N
NH2
环化反应
电环反应
多烯烃化合物的π体系的末端可以闭合成环状化合物
heat
light
环加成反应
Diels-Alder反应
CHCOOC2H5 CHCOOC2H5 COOC2H5 COOC2H5
N N N N CH2 Ph Cl
SO2
PhCH2NHCH2OSO2H 亚磺酸苄氨基甲酯
HCl KOH
PhCH2NH2
胺(仲胺)
R NH2 1HC(OR)3 2H2O, H+ RX RNH2
R NH R
现代有机合成第4章

第四章 潜在官能团
现代有机合成化学
第四章 潜在官能团
近年来,关于烯烃的反应层出不穷,其中一个代表性的反应称为RCM (Ring Closi ng Metathesis) 反应.这一反应利用催化量的Ru络合物即可完成关环,因此分子 内如果存在两个烯烃单元,就可以经RCM反应转化为一个环状化合物.这样,如 果我们将前体中的两个烯烃单元作为潜在基团,那么RCM反应就是一种展示方 式,而生成的环状产物就是目标.这类反应在许多敏感的底物上应用越来越多.
第四章 潜在官能团
复杂分子合成中,多官能团分子反应时如果存在反应活性重叠,将 出现给定的试剂不能按计划只进攻某一部位或官能团的情况.为解决 这一问题,通常采纳三种策略:
①选择性反应. ②可逆性去活化.包括保护(protecting)、堵塞(blocking)和掩蔽(mas king). ③潜在官能团(latent functionality). 我们在前面已经讨论了第一和第二种策略.当前两者都达不到效果 时,更多的会使用第三种方式,即潜在官能团方法.本章我们将就此作 一些论,潜在官能团是一条完全不同的途径,这一名词最初是由Ledni
上述选择性氧化苯环作为潜在官能团的展示反应显然是十分出色的,但是使用 还原方法使苯酚醚去芳香化则更具有普遍意义.
1944年Birch发现苯酚醚在液氨中并在质子供体如醇或铵盐的存在下可以被碱 金属,最好为金属锂还原为非共轭的1-烷氧基-1,4-环己二烯.由这一化合物可以转 化为许多合成的中间体,从而使苯酚醚广泛用于天然产物的合成,特别是含六员 环化合物的全合成.如甾体的A、B和D环都曾以苯酚醚为前体而获得.
t-BuOK在t-BuOH中 70℃,2h,86%
烯丙基醇就氧化态而论相当于1,3-二醇,它们的烯醇醚可以通过加热引发Σ (3, 3)Claisen重排[18]转化为 γ,β-不饱和羰基化合物,视羰基α-位碳原子上的取代基情况 可得不同氧化态的不饱和羰基化合物.
有机合成方法大全

第一章卤化与卤置换反应向有机化合物分子引入卤素的方法有三种,即取代卤化、加成卤化和置换卤化。
得到卤化物的目的有两个:一个是为了得到性能更优异的产品;另一目的是可以通过进一步转换,制备其它中间体产品。
根据引入卤原子的不同,可分为氟化、氯化、溴化和碘化。
1.1醇羟基的卤化1.1.1用DAST制备氟化物5-bromo-2-(4-chloro-2-fluorophenyl)-6-fluoro-4,5,6,7-tetrahydro-2H-isoindole-1,3-dione分子式C14H9BrClF2NO2摩尔质量376.58合成反应式操作过程向250mL反应瓶内,加入原料1g,加入20mL的DMSO使固体溶解,用冰浴降温至0℃,搅拌下滴加入0.4mL的DAST,于0℃反应2小时,缓慢升温至室温反应1小时,向反应液内加入50g冰水。
用EA萃取,减压浓缩干,过硅胶柱分离得白色固体0.8g,收率:80%参考文献1.W.Ros enbrook,D.A.Riley,vley;T etrahedron Lett.,1985,36,3-42.K.C.Nicolaou,J.L.Randall,G.T.Furst;J.Am.Chem.Soc.,1985,107,5556-5558 1.1.2用氟化氢制备氟化物2-(4-fluoro-1-methylpyrrolidin-3-yl)pyridine分子式C10H13FN2摩尔质量180.22合成反应式操作过程向100mL反应瓶内,加入原料0.5g,用液氮降温至-70℃,加入无水氟化氢5g,搅拌下加下2g四氟化硫,于-70℃反应3小时,缓慢升温至室温使低沸物逸出,将反应液倾倒入100g冰水中。
用2mol/L的NaOH水溶液调到碱性,用DCM萃取,油层再用2mol/L的盐酸反萃取。
酸水溶液减压浓缩干后得黄色固体0.7g,将此粗品溶于饱和碳酸钠水溶液,用EA萃取3遍。
过硅胶柱分离得无色固体0.4g,收率:89%参考文献1.WO1998/25924,PCT/GB97/03054.1998.6.181.1.3用氯化亚砜制备ethyl2-chloro-3-(3-chloropropylcarbamoyl)-4-(methylsulfonyl)benzoate分子式C14H17Cl2NO5S摩尔质量382.26合成反应式操作过程向100mL反应瓶内,加入7g原料,搅拌下滴加入10mL氯化亚砜。
《有机合成方法》PPT课件

所有的起始原料确定后,再设计全合成路
线。在实施合成时,可以采用逐步合成法或
片段组合法进行合成。
(3)计算机辅助有机合成路线设计
a. 化学信息学和化学信息数据库
与有机合成有关常用数据库: * 现有化学品数据库 * 有机化学反应数据库 * 合成方法和转化数据库 * 合成方法参考文献库 * 保护基团数据库 * 杂环合成数据库
相合成所应用的活化单体。
DMT
OCH 2 O B
H H
O
CH3O P
H H
H
+
C H(C H3)2
NH
C H(C H3)2
Protonated phosphoramidite
氯甲基酮衍生物:
R-COCH2Cl 是良好的烷基化活性中间体,
容易与氨基和巯基等发生烷基化反应。
O
R 1
+
RC C H 2 C l R 2
HH
H
H
OH OH
* 在温和条件下, 仅有极少量的第二醇羟基或碱 基上的氨基与单甲氧基三苯甲基氯作用。 * 用 80% 的乙酸或吡啶-乙酸处理, 即可以除去 这类保护基。
取代的γ-酮酰基 (γ-keto acyl) 保护醇羟基: * 在中性条件下, 用水合肼处理可以方便地除去。
O RC
O
(CH2)2 C OCH2 O Base
a. 氨基保护
O H2 Ph C O C Cl
benzylchloroformate base
+
H2N
H C
CO-O
R
amino acid
O H2 Ph C O C
H HN C
CO-O
R
CBz-amino acid
高中化学之有机合成方法归纳

高中化学之有机合成方法归纳.有机合成【知识构建】一、有机合成的关键是、碳链的减短、成:一()、碳骨架的构建碳链的增长环或开环1、碳链增长的途径: Br + NaCN → CHCH23CHO + HCN →CH 3CHCHCHCHO + CHCHO →2323烯烃、炔烃的加聚、加成反应、碳链缩短的途径:2由醋酸钠制备甲烷:3、成环与开环的途径:)成环:如羟基酸分子内酯化1( HOCHCH COOH →22 (2)开环:如环酯的水解反应O → +2H COOCH 22COOCH2结合已学知识,小结以下(二)官能团的引入与转化官能团引入的方法。
的方法:C=C、至少列出三种引入1页 11 共页 2 第有机合成.;如(1)(2) ;如(3) ;如2、至少列出四种引入卤素原子的方法:(1) ;如;如(2);如(3);如 (4) (—OH)的方法:3、至少列出四种引入羟基(1) ;如(2) ;如(3) ;如;如(4)、在碳链上引入羰基(醛基、酮羰基)的方法:4 5、在碳链上引入羧基的方法:(1) ;如;如(2)(3) ;如二、中学常用的合成路线 1.烃、卤代烃、烃的含氧衍生物之间的转化关系页 11 共页 3 第有机合成.2.一元合成路线HX――→CH—CH=一元卤代烃―→一元醇―→R一定条件2一元羧酸―→酯醛―→ 3.二元合成路线X二元→→二元醇―→二元醛――→CH=CH222)羧酸―→酯(链酯、环酯、聚酯 4.芳香族化合物合成路线:应特别注意条件的Cl的反应,特别提醒和2做催化剂取代苯环邻、Fe变化;光照只取代甲基上的氢,对位上的氢。
三、有机合成题的解题思路典型例题:等其他试剂制取为原料,并以Br1例.以2页 11 共页 4 第有机合成.,用反应流程图表示合成路线,并注明反应条件。
1练习.用苯作原料,不能经一步化学反应制得1)(的是苯C..A硝基苯B.环己烷.溴苯 D 酚.在有机物分子中,不能引入羟基的反2) (应是.消 C B.水解反应 A.氧化反应.加成反应 D去反应年诺贝尔化概括了2005”3.“绿色、高效()学奖成就的特点。
有机合成的常规方法PPT教学课件

2020/12/10
7
★官能团的衍变
♣不同官能团间的转换 R—X R—C=C—R’
R—OH RCOH
RCOH ♣通过某种途径使一个官能团变为两个
CH3CH2OH
HOCH2CH2OH
ห้องสมุดไป่ตู้
♣通过某种途径使官能团的位置改变
CH2=CHCH2CH3 CH2=CHCH2CH3
[思] CH2=CHCH2CH3 CH2=CHCH=CH2
有机合成的常规方法
2020/12/10
2001.3.19
1
例
以CH3CH2Cl为原料合成
O C C=O
C C=O O
其它无机原料自选,写出有关化学方程式。
2020/12/10
2
一.有机合成的必备知识 ➢官能团的引入 ➢官能团的消除 ➢官能团的衍变
2020/12/10
3
1.羟基的引入
加热加压
♣烯烃加水 CH2=CH2+H2O催化剂 CH3CH2OH
11
例
醛酮中α-H的醛能自身加成生成β-羟基醛
R-CH2-CHO+R’-CH2-CHO
R-CH2-CH-CH-CHO OH R’
巴豆酸(CH3-CH=CH-COOH)主要用于合成 树脂,现用乙醇及无机原料合成巴豆酸?
写出有关反应方程式。
2020/12/10
12
PPT精品课件
谢谢观看
Thank You For Watching
13
♣醇与HX的取代
C2H5OH+HBr
2020/12/10
5
3.双键的引入
♣醇与卤代烃的消去反应 CH3CH2OH
♣醇的氧化 CH3CH2OH
第十一章 近代有机合成方法
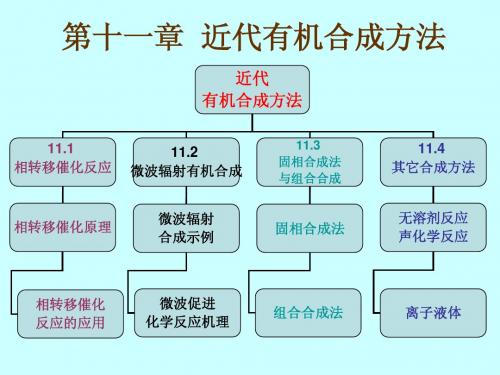
R R'
N H
N H
苯/50%NaOH,5%TBAB + RX 30 ℃,搅拌,6~22h
RX=Me2SO4,Et2SO4,C2H5Br,PhCH2Br等
N 78%~98% R 78%~98%
◆硫的烃基化:
2 4 2 PhCH2Br +KHS
RX=Me SO ,Et SO 聚乙醇二甲醚 4,C2H5Br,PhCH2Br等 PhCH2SH 0.5h, r.t
PhOH + O PhOCH 2 O O CH 2 O C C CH 2 CH 3 + CH2=CCH3COOH
TEBA 85℃,4h
OH Ph O
O
CH 2 CH CH 2 O C C CH 2 CH 3
◆ 例如,双酚A与对苯二甲酰氯在TEBA催化作用下生成双酚A型聚芳酯,
与非相转移催化相比,速率快、条件温和、产物相对分子量大。
O
R2
R1 C CH CH CH2 CHO COOEt 44%~64%
R1=OEt,CH3;R2=H,CH3,Ph等
◆相转移催化剂能够使醇醛缩合反应条件改善,提高反应收率。
例如,苯甲醛的安息香缩合,使用PTC可使反应时间从20h缩短至1h。
CHO 2 + KCN O
Bu4N+ClH2O,r.t
CH C OH 70%
式中R1=烷基,芳基;R2=R3=H,烷基,芳基;X=Cl, Br, I。
◆α,β-不饱和醛(酮、酯)与活泼亚甲基化合物的Michael 加成,一般方法易发生树脂化,采用液-液相转移催化法可
以避免。
R1COCH2COOEt + R2CH=CHCHO
Na2CO3(液)/TEBA/苯 40~50℃,1~4h
有机合成方法大全(第二章p1-12)
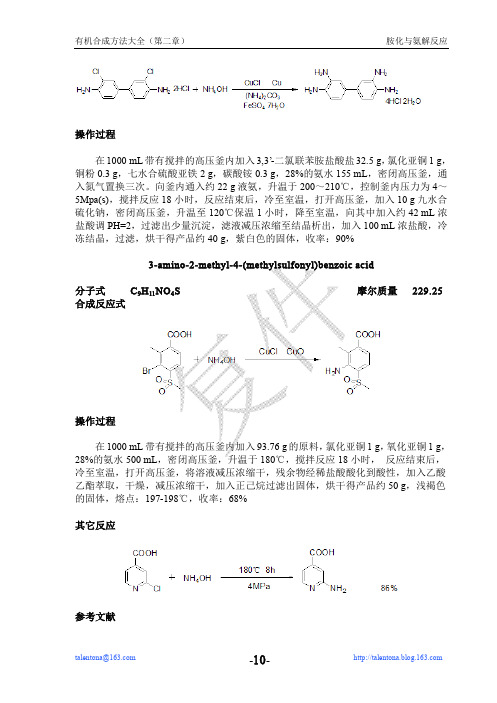
操作过程在1000mL带有搅拌的高压釜内加入3,3’-二氯联苯胺盐酸盐32.5g,氯化亚铜1g,铜粉0.3g,七水合硫酸亚铁2g,碳酸铵0.3g,28%的氨水155mL,密闭高压釜,通入氮气置换三次。
向釜内通入约22g液氨,升温于200~210℃,控制釜内压力为4~5Mpa(s),搅拌反应18小时,反应结束后,冷至室温,打开高压釜,加入10g九水合硫化钠,密闭高压釜,升温至120℃保温1小时,降至室温,向其中加入约42mL浓盐酸调PH=2,过滤出少量沉淀,滤液减压浓缩至结晶析出,加入100mL浓盐酸,冷冻结晶,过滤,烘干得产品约40g,紫白色的固体,收率:90%3-amino-2-methyl-4-(methylsulfonyl)benzoic acid分子式C9H11NO4S摩尔质量229.25合成反应式操作过程在1000mL带有搅拌的高压釜内加入93.76g的原料,氯化亚铜1g,氧化亚铜1g,28%的氨水500mL,密闭高压釜,升温于180℃,搅拌反应18小时,反应结束后,冷至室温,打开高压釜,将溶液减压浓缩干,残余物经稀盐酸酸化到酸性,加入乙酸乙酯萃取,干燥,减压浓缩干,加入正己烷过滤出固体,烘干得产品约50g,浅褐色的固体,熔点:197-198℃,收率:68%其它反应参考文献参考文献[1]Jack(Jianhua)Cao unpublished result[2]Chand,Pooran;Kotian,Pravin L.;Morris,Philip E.;Bantia,Shanta;Walsh,David A.;Babu,Yarlagadda S.;Bioorganic&Medicinal chemistry,13(7),2005,2665-26782.1.8用六亚甲基四胺(乌络托品)制备(4-bromophenyl)methanamine分子式C7H8BrN摩尔质量186.05合成反应式操作过程向500mL反应瓶内加入15.4g乌络托品和120mL的氯仿,油浴升温于50℃,开始滴加25g的对溴溴苄,搅拌反应24小时后,反应结束后,冷至室温,过滤,得中间体,将中间体加入250mL反应瓶内,搅拌下加入73mL的浓盐酸,升温回流并蒸出,收集馏出物,向其中加入约50mL的40%氢氧化钠水溶液,分出油层,水层用THF 萃取,合并干燥,减压浓缩干,得产品约15.8g,黄色的油状物,收率:85%2.1.9二苄基胺为胺化试剂N,N-dibenzyl-2-chloro-5H-pyrrolo[3,2-d]pyrimidin-4-amine分子式C20H17ClN4摩尔质量348.83合成反应式操作过程第二章胺化与氨解反应用氨或伯胺、仲胺与有机物作用生成胺的过程称为氨解胺化反应。
第二十一章 有机合成简介

选择性不大,甚至希望起作用的恰巧是活性较小的基团
时,为了使反应能在指定位置进行,往往用引入导向基
的办法解决。
Br
Br
Br
溴是邻对位定位基,本身的定位效应不能引入间位
取代。可通过引入导向基——氨基。
混酸
NO2
Fe 稀盐酸
NH2 NaNO2 H2SO4, 0 ~ 5℃
N2HSO4H3PO2
NH2
氨基
是强邻对
★ 合成等价物(synthetic equivalents):能起到合成子作 用的相应的真实化合物。
★ 化学反应逆推过程:“ ”逆推符号。
2. 官能团的转换、引入和消除
① 官能团的转换:将一个官能团转换成另一个官能团。 (functional group interconversion,FGI)。
② 卤素加成 R-CH=CH-R/
X2
R-CH—CH-R/
Zn
XX
卤代烃:对碱、氧化剂、还原剂然增 加合成步骤,导致总产率降低。
同时,若分子中有相似反应性的基团时,要保护 某一基团也有困难。因此,不仅需注意探求高选择 性的保护基,更应以极大的兴趣去从事发展高选择 性反应试剂的研究。
CH2OH
(Cannizarro 反应)
OH
HNO3
CH2CH2COOH
CH2CH2COOH
(氧化反应)
过氧酸氧化
O
3. 通过周环反应
R
R
+
(氧化反应) (Diels-Alder反应)
OCH2 CH CH2
OH CH2 CH CH2
(Claisen重排)
+
(2 + 2 环加成)
4. 通过重排反应
有机合成
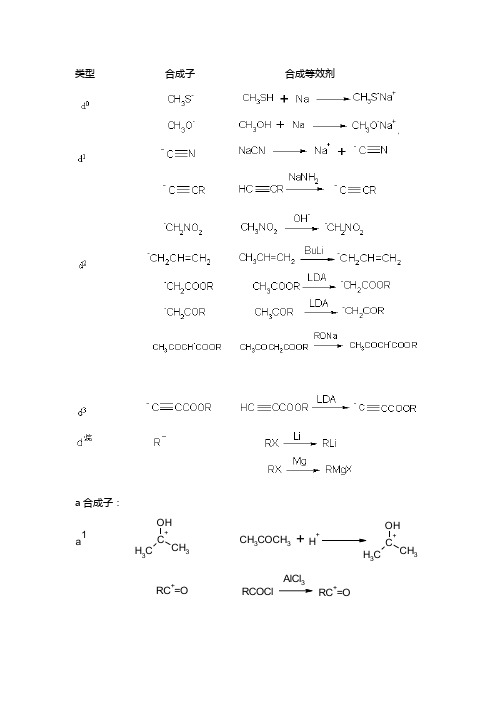
类型 合成子 合成等效剂a 合成子:C+OH CH 3CH 3CH 3COCH 3H +C+OHCH3CH 3RC+=ORCOClAlCl 3RC +=O+CH 2COCH 3BrCH 2COCH 3BrC -HCOCH 3+CH 2CHOHCH 3OCH 3H++CH 2CHOHCH3R(H)OCNXX=Cl,Br,IR+RXR 2SO 48.1.2.2合成子的作用规律一个d 合成子与一个a 合成子在适当的条件下化合,得到一个加合的C -C 键(d 0合成子除外)。
下述的一些规律,可以用来设计产物(目标分子)中的官能团的位臵。
d 烷+a 烷,反应产物是无官能团产物 a 烷+d 1,a 1+d 烷,反应产物是单官能团化合物 a 1+d 1, 反应产物是1,2-双官能团化合物 a 1+d 2,a 2+d 1,反应产物为1,3-双官能团化合物等等。
例如:烷基a +烷基d :CH 3LiCH 3Br CH 3-CH 3a 1+d 1:RC=OHHCNRCH OHCNa 1+d 2:CH 3COCH 3CH 3CHOC OHCH 2CHOCH 3C H 3a2+d2:OCOOCH3BrO COOCH3OCOOCH3O COOCH3a3+d2:OOHO注意:目标分子是合成子就必须由一个以上官能团。
如果在开链化合物分子中,含有一个电子接受体部位和一个供电子中心,则这两个原子间可进行分子内键合。
相应地生成单环化合物。
例如:O OMeO8.2供电子合成子8.2.1烷基(烃基)d合成子碳负离子是带一对电子的有机负离子,电荷主要集中在碳原子上。
烷基、烯基、炔基负离子中,非键合的电子总是定域在碳原子上,它们具有高度的反应活性。
形成碳负离子的难易程度:与碳氢键中的S成分有关,S成分增加,则越易形成碳负离子。
C CH C CH C CH当碳原子上的取代基数目不同时,饱和烷基负离子的稳定性顺序为3o<2o<1o,但他们的稳定性都很小。
合成有机化合物的方法与机理

消去反应
定义:消去反应是一种有机化学反应,通过消除一个或两个小分子(如水、卤化氢等),将不饱和键转化为不饱和 键。
条件:通常在加热和催化剂存在下进行。
类型:包括分子内消去反应和分子间消去反应。
应用:在有机合成中,消去反应是一种重要的制备有机化合物的途径。
聚合反应
定义:由单体合成聚合物的反应 分类:加聚反应和缩聚反应 聚合反应的特点:高分子化合物的生成,反应过程中有聚合度增长的变化 聚合反应的应用:合成高分子化合物,如塑料、纤维、橡胶等
自由基取代反应机理
添加 标题
定义:自由基取代反应是一种有机化学反应,其中自由基作为反应中间体,通过与底物分子发生取代反应生 成新的化合物。
添加 标题
反应机理:自由基取代反应通常包括引发、增长和终止三个阶段。引发阶段是产生自由基活性种的过程,增长阶段是自由基 与底物分子发生取代反应的过程,终止阶段是自由基之间或自由基与其它物种之间发生反应,使自由基消失的过程。
反应条件控制:通过调节温度、压力、溶剂等反应条件,选择性地进行有机合成反应。
催化剂选择:使用特定性质的催化剂,促进所需反应的选择性进行。 底物控制:选择具有特定结构的底物,通过其结构特点实现选择性合成。
反应步骤控制:通过控制合成步骤的顺序和条件,选择性地进行有机合成反应。
选择性控制的实例
反应条件控制:通过调节温度、压力、溶剂等反应条件,实现对有机合成反应的选择性控制。 催化剂选择:选用不同类型的催化剂,可以实现对有机合成反应路径和产物选择性的控制。
绿色氧化剂:利用过氧化氢、过氧化羧酸等环保型氧化剂进行有机合成,具有条 件温和、产物纯净、无毒或低毒等优点。
绿色溶剂:利用水、离子液体等代替传统有机溶剂进行有机合成,具有条件温和、 产物纯净、无X
有机合成

有机合成 有机合成技巧 第一节概述有机化学的内容一般可以分成三部分,即有机合成、有机理论和有机分析。
虽然这三部分对于生产实际都有联系,可是有机合成和生产实际得更加密切一些。
不论在工业或农业上,都迫切期望我们能不断合成出更好的化合物,以满足各方面的需要,所以有机合成是一项非常重要的工作。
有机合成通常是指从元素、简单无机化合物通过化学反应制取比较复杂的有机物质的过程。
它通常经过一系列反应,反应步骤的多少视所欲合成的分子(目标分子)的复杂性而定。
任何有机合成都应尽可能符合如下前提:(1) 应采用尽可能有效(产率高)的反应和方便的步骤,要力求采用只生成一种或主要生成一种产物的可靠的反应,避免生成各种产物的混合物。
(2) 要尽可能压缩反应以避免合成周期过长和总产率过低;一个每步产率为80%的十步合成的全过程产率仅为10.7%,而每步产率为40%的二合成的全过程产率可达到16%。
(3) 原料应是易得和价廉的。
通常,含有五个或少于五个碳原子的单官能团化合物和单取代苯等大多是较容易购得的。
第二节反向合成分析在我们学习有机化学的时,一直是沿着由起始原料经过有机化学反应生成特定结构的化合物这种思维路线进行的。
即反应物反应产物这种学习的顺序已经逐渐变成了我们思考问题的习惯,但是,当开始制定一项有机合成计划时,最初提供的信息只是需要合成的目标分子,这时就要求合成有机化学家应用化学反应作为工具,寻找合适的起始原料。
这也就是应用与过去学习有机化学时相反的思维路线去考虑问题。
即产物结构起始原料反应这种分析目标分子的结构,找出起始原料,制定出合成计划的思维方法就是反向合成(antithetic synthesis )即使对于一个较简单的合成,应用反向合成法也往往可导出许多不同的中间体,组成许多不同的合成程序,结果得到一个所谓的“合成树”:从合成树可得出一个结论,那就是:有机合成并非只有唯一答案。
究竟哪条路线好,要结合实际情况加以判断。
高等有机化工工艺学-烯烃的合成方法

八、邻位二羧酸的氧化脱羧
R1 R2
R3 R4 COOH COOH
Pb(OAc)4/O2
R1 R2
R3 R4
在氧气存在下.邻位二羧酸化合物与四乙酸铅在吡啶中共热,发生氧化脱羧, 生成烯烃。由于许多环状邻位二羧酸极易由Diels-Alder反应或环加成反应制得。因 此本法特别适用于制备环烯烃。 1,4-环己二烯的合成。
HMPA
Br(CH2)4CH
CH2
49%
二、醇的脱水
RCH2CHR' OH RCH CHR'
+
H2O
虽然卤代烃脱卤代氢是烯烃常用的合成方法,但合成简单的烯烃时, 醇往往是更易获得的原料。 醇的酸催化脱水法应用最为普通,脱水速度是叔醇>仲醇>伯醇。 醇的脱水和卤代烃消除类似,不能获得单一的烯烃。 常用的酸性脱水剂有硫酸、磷酸、草酸、五氧化二磷等,而新的试 剂不断出现。
+
CH3SOH
在氢化钠存在下,1,1-二苯乙烯与二甲基亚砜进行烃化反应,继而在减压 150-200℃热解,生成3,3-二苯基丙烯。
NaH
(C6H5)2C=CH2
+
CH3SOCH3
(C6H5)2CHCH2CH2SOCH3
(C6H5)2CHCH=CH2
96%
亚砜可以从硫醚氧化而得。因此,在分子的某一位置,若能引入一经硫基,则 通过氧化、继而热解,可在该处形成一个碳碳双键。
醇在三氟化硼-乙醚作用下,能在十分温和的条件下脱水,如2-甲基-2-十九醇的脱水。
CH3(CH2)15
OH
BF3Et2O CH2Cl2
CH3(CH2)15 95
+
CH3(CH2)15 5
有机合成方法大全(第五章 P1-P5)

第五章氧化反应氧化既是失去电子,氧化的一种情况是脱氢;氧化反应关键是选择合适的氧化剂,另外也要看被氧化的基团是烷烃还是杂原子,以防止其它的基团被破坏,比较常用的氧化剂有:硝酸,二氧化锰,双氧水,高锰酸钾,重铬酸盐,四醋酸铅,次卤酸及其盐,过氧有机酸,过硫酸钾,四氧化锇,高价金属化合物,铬酸及其盐等。
5.1羟基的氧化5.1.1用PCC氧化羟基为醛或酮(2S,5a R,7R,91S)-2-((tert-butyldimethylsilyloxy)methyl)-7-methyl-3-(trimethylsilyl)-4,5,5a,6,7,8-hexahydro-1H-cyclopenta[c]inden-9(2H)-one操作过程向50mL反应瓶内,投入400mg的原料和5mL的DCM,搅拌溶解后,加入422 mg的PCC,并于室温反应2小时,加入10mL的乙醚,过滤,滤液减压浓缩干,残余物经硅胶柱分离纯化,得产品323mg,黄色液体,收率:88%PCC的制备:向184mL的6M稀盐酸内,冰盐浴降温到0℃,分批加入100g的三氧化铬,搅拌5分钟成均匀溶液,控温在10℃以下滴加入79.1g的吡啶,重新冷却至0℃,有橙黄色结晶析出,过滤,真空干燥,得产品180.8g,收率:84%,在室温下稳定保存。
其它反应参考文献[1]Chin-Kang Sha,Fang-Kun Lee and Ching-Jung Chang;J.Am.Chem.Soc.,1999,121,9875-9876[2]Omar Farooq,Mike Marcelli,G.K.Surya Prakash,and George A.Olah;J.Am.Chem.Soc.,1988,V ol.110,3,864-8675.1.2用PDC氧化羟基为醛或酮N-(4-([1,2,4]triazolo[4,3-a]pyridin-6-ylamino)phenyl)-3-hydroxybenzamide操作过程向50mL反应瓶内,投入50mg的原料,加入20mL的DCM,室温下加入520 mg的PDC,室温搅拌反应1小时,过滤,滤液减压浓缩干,经硅胶柱分离纯化,得产品35mg,白色固体,收率:70%注:PCC对许多官能团来说是一个通用的氧化试剂,常用于把一级醇或二级醇氧化为醛或酮,而且几乎没有过氧化;对于含有酸敏感基团的化合物,应采用更为温和的PDC 氧化剂,在这一点上它比PCC更有优势。
有机合成方法大全目录(部分)

有机合成方法大全
——Jack Cao
2008 年于北京
目
第一章 卤化与卤置换反应
录
1. 醇羟基的卤化----------------------------------------------------------1-12 2. 苯环及稠环上的卤化-----------------------------------------------12-23 3. 杂环的卤化-----------------------------------------------------------23-29 4. 芳香环侧链的卤化--------------------------------------------------29-33 5. 脂肪烃的卤化--------------------------------------------------------33-42 6. 加成卤化--------------------------------------------------------------42-55 7. 卤置换反应-----------------------------------------------------------55-67
第二章 胺化与氨解反应
1. 卤代物的胺化----------------------------------------------------------1-19 2. 羟基和亚甲基的胺化-----------------------------------------------20-28 3. 芳香环的胺化--------------------------------------------------------28-30 4. 羧基和羰基的胺化--------------------------------------------------30-38 5. 其它的胺化反应-----------------------------------------------------38-42
高中化学之有机合成方法归纳

有机合成【知识构建】一、有机合成的关键是(一)、碳骨架的构建:碳链的增长、碳链的减短、成环或开环1、碳链增长的途径:CH3CH2Br + NaCN →CH3CHO + HCN →CH3CH2CHO + CH3CH2CHO →烯烃、炔烃的加聚、加成反应2、碳链缩短的途径:由醋酸钠制备甲烷:3、成环与开环的途径:(1)成环:如羟基酸分子内酯化HOCH2CH2COOH →(2)开环:如环酯的水解反应COOCH2 +2H2O →COOCH2(二)官能团的引入与转化结合已学知识,小结以下官能团引入的方法。
1、至少列出三种引入C=C的方法:(1) ;如(2) ;如(3) ;如2、至少列出四种引入卤素原子的方法:(1) ;如(2) ;如(3) ;如(4) ;如3、至少列出四种引入羟基(—OH)的方法:(1) ;如(2) ;如(3) ;如(4) ;如4、在碳链上引入羰基(醛基、酮羰基)的方法:5、在碳链上引入羧基的方法:(1) ;如(2) ;如(3) ;如二、中学常用的合成路线1.烃、卤代烃、烃的含氧衍生物之间的转化关系2.一元合成路线R —CH =CH 2――→HX 一定条件卤代烃―→一元醇―→一元醛―→一元羧酸―→酯3.二元合成路线CH 2=CH 2――→X 2→二元醇―→二元醛→二元羧酸―→酯(链酯、环酯、聚酯)4.芳香族化合物合成路线:特别提醒 和Cl 2的反应,应特别注意条件的变化;光照只取代甲基上的氢,Fe 做催化剂取代苯环邻、对位上的氢。
三、有机合成题的解题思路典型例题:例1.以为原料,并以Br 2等其他试剂制取,用反应流程图表示合成路线,并注明反应条件。
练习1( ) 1.用苯作原料,不能经一步化学反应制得的是A .硝基苯B .环己烷C .苯酚D .溴苯( ) 2.在有机物分子中,不能引入羟基的反应是A .氧化反应B .水解反应C .消去反应D .加成反应( ) 3.“绿色、高效”概括了2005年诺贝尔化学奖成就的特点。
