2019-2020学年高中化学 第一章 物质结构元素周期律 第一节 元素周期表第2课时教案4 新人教版必修2.doc
第一章第1节元素周期表

二、元素周期表的结构
不同横行中最外层电子数相同的 2、族: 元素按电子层数递增的顺序由上 到下排成纵行。
共 18 个纵行, 16 个族
七 共7个主族 主族序数=最外层电子数 主 (A族)表示为罗马数字加A 七 副族: ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB ,ⅠB , ⅡB 副 族 共7个副族 零 (B族)表示为罗马数字加B 八 包含三列(8、9、10) 第VIII 族: 族 最外层稳定结构的稀有气体元素 零族:
元素金属性强弱判断依据:
1、根据金属单质与水或者与酸反应置换出氢的 难易程度。置换出氢越容易,则金属性越强。
已知金属A可与冷水反应, 金属B和热水才能反应,金属 C和水不能反应,判断金属A、 B、C金属性强弱如何?
金属性 A〉 B〉 C
元素金属性强弱判断依据:
1、根据金属单质与水或者与酸反应置换出氢的
碱金属与氧气反应比较
单质 Li Na K Rb Cs 与O2反应 Li2O Na2O、Na2O2 K2O、K2O2、KO2 更为复杂 更为复杂 反应程度
越 来 越 剧 烈
(1)碱金属元素原子的最外层都有 1个电子,它们的化学性质相似 ①与O2的反应
Δ Δ 4Li + O2 = 2Li2O
Li、Rb、Cs 又如何呢?
二、元素周期表的结构
具有相同电子层数的元素,按 1、周期: 照原子序数递增顺序由左往右 排成横行。 共 7 横行— 7 个周期
周期数 = 电子层数
短周期 三 短 周期 四 长周期 长 (横向)
第1周期: 2种元素 第2周期:
第3周期:
第4周期:
8种元素 18种元素
第5周期:
第6周期: 32种元素 第7周期: 26种元素
高一化学物质结构元素周期律

3.元素、核素、同位素 书P4 元素: 具有相同质子数(核电荷数)的同一类原子的总称。 质子数(或核电荷数) 决定元素种类的是_______________
核素: 具有一定数目的质子和一定数目的中子 的一种原子。 决定核素(原子)种类的是质子数和中子数 _______________
同位素: 质子数相同而中子数不同的同一元素的 不同核素互称为同位素。(对于原子来说) 判断条件:①质子数相同 ②中子数不同 ③同一元素的原子
根据以根据以上数据,磷原子的半径可能是( B
)
A. 0.080nm B. 0.110nm C. 0.120nm D. 0.070nm 第四 2、 34号元素是第__________ 周期元素;族序数是
ⅥA +6价 。 _______; 最高正价是________
H2A 若用A表示该元素,其气态氢化物的化学式是________ 。
练:
下列各组物质中,互为同位素的是(ห้องสมุดไป่ตู้(A)O2、、O3 、O4 ) D
40 42 (C)H2O、D2O、 T2O (D) 20Ca 和20 Ca
(B)H2、D2、T2
下列各组中属于同位素关系的是( A ) 39 A. 40 K 与 19 B.T2O与H2O K
19
C.
40 19 K
与
40 20 Ca
元素周期表的结构
短 周 期
周 期
长 周 期
第1周期:2 种元素 第2周期:8 种元素 第3周期:8 种元素 第4周期:18 种元素 第5周期:18 种元素 第6周期:32 种元素
镧系元素:共15 种元素 锕系元素:共15 种元素
不完全周期 第7周期
周期序数 = 电子层数
必修二第一章物质结构元素周期律知识点总结
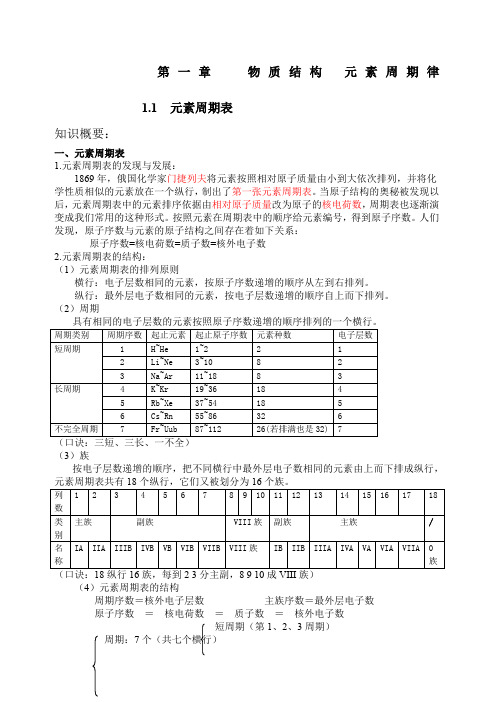
第一章物质结构元素周期律1.1 元素周期表知识概要:一、元素周期表1.元素周期表的发现与发展:1869年,俄国化学家门捷列夫将元素按照相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵行,制出了第一张元素周期表。
当原子结构的奥秘被发现以后,元素周期表中的元素排序依据由相对原子质量改为原子的核电荷数,周期表也逐渐演变成我们常用的这种形式。
按照元素在周期表中的顺序给元素编号,得到原子序数。
人们发现,原子序数与元素的原子结构之间存在着如下关系:原子序数=核电荷数=质子数=核外电子数2.元素周期表的结构:(1)元素周期表的排列原则横行:电子层数相同的元素,按原子序数递增的顺序从左到右排列。
纵行:最外层电子数相同的元素,按电子层数递增的顺序自上而下排列。
(2)周期(3)族按电子层数递增的顺序,把不同横行中最外层电子数相同的元素由上而下排成纵行,(4)元素周期表的结构周期序数=核外电子层数主族序数=最外层电子数原子序数=核电荷数=质子数=核外电子数短周期(第1、2、3周期)周期:7个(共七个横行)周期表长周期(第4、5、6、7周期)主族7个:ⅠA-ⅦA族:16个(共18个纵行)副族7个:IB-ⅦB第Ⅷ族1个(3个纵行)零族(1个)稀有气体元素(5)认识周期表中元素相关信息随堂检测(一)1.已知某主族元素的原子结构示意图如下,判断其位于第几周期?第几族?2.主族元素在周期表中的位置取决于该元素的()A.相对原子质量和核外电子数B.电子层数和最外层电子数C.相对原子质量和最外层电子数D.电子层数和次外层电子数3.下列各表为周期表的一部分(表中为原子序数),其中正确的是()A.B.C.D.4.,同一周期ⅡA、ⅢA的两种元素的原子序数差可能为几?5.已知元素的原子序数,可以推断元素原子的()①质子数②核电荷数③核外电子数④离子所带电荷数A.①③B.②③C.①②③D.②③④6.由长周期元素和短周期元素共同构成的族是()①0族②主族③副族④第Ⅷ族A.①②B.①③C.②③D.③④7.下列说法中正确的是()A.现行元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的B.最外层电子数相同的元素一定属于同一族C.非金属元素的最外层电子数都≥4D.同周期元素的电子层数相同二、元素的性质与原子结构1.碱金属元素:从原子结构上看:相同点:最外层都只有一个电子。
2020学年新教材高中化学第1章原子结构元素周期表本章核心素养聚集课件鲁科版必修第二册

一、宏观辨识与微观探析
化学研究的重点是在原子、分子水平上认识物质的结构、组成、性质和变化 规律,并据此改造或创造物质。本章是从原子结构的角度认识元素及其物质 的性质与变化规律,建立原子结构与元素性质、元素性质与物质性质的关系, 会用原子结构的知识解释元素性质及其变化规律,能从元素周期表的构成、 元素周期律的递变认知上,形成“结构决定性质”的观念,从宏观和微观相 结合的视角分析解决实际问题。
(2)Z在周期表中的位置__第__5_周__期__Ⅶ__A_族__。 (3)判断非金属性:X__<___Y。 (4)判断非金属性:Y__>___Z,试从原子结构上分析其原因:_二__者__最__外__层__电__子__ _数__相__同__,__但__I_的__电__子__层__数__多__,__原__子__半__径__大__,__得__电__子__能__力__弱___。
离子方程式 甲_2_B__r-__+__C_l_2=_=_=__B_r_2+__2_C__l-_ 乙_2_I_-_+__C_l_2_=_=_=_I_2+__2_C__l-____ 结论:卤素单质的氧化性由强到 弱的顺序为Cl2>Br2>I2
解析 氯气氧化性大于溴和碘,所以氯气能置换出溴和碘;
②[评价]甲同学设计的实验方案的合理性是__B___(填字母)。 A.非常合理 B.部分合理 C.完全不合理
二、证据推理与模型认知
“证据推理与模型认知”在本章的具体体现:利用元素在元素周期表中的 位置和原子结构分析、预测、比较元素及其化合物的性质,能用原子结构 解释元素性质及其变化规律,并能结合实验及事实进行说明。在此基础上, 建立相关知识应用的思维方法模型,如10电子、18电子微粒识别与判断, 微粒半径大小比较,元素金属性、非金属性强弱比较,元素“位—构—性” 关系的应用、化学键类型的判断等。
第一章 物质结构元素周期律(知识点总结)

Z 第一章物质结构元素周期律班级姓名一、原子结构质子(Z个)原子核注意:中子(N个)质量数(A)=质子数(Z)+中子数(N) 1.原子(A X)原子序数=质子数= 核电荷数=原子的核外电子数核外电子(Z个)2.原子核外电子的排布规律:①电子总是尽先排布在能量最低的电子层里;②各电子层最多容纳的电子数是2n2;③最外层电子数不超过8个(K层为最外层不超过2个),次外层不超过18个,倒数第三层电子数不超过32个。
电子层:一(能量最低)二三四五六七对应表示符号: K L M N O P Q3.元素、核素、同位素元素:具有相同核电荷(质子)数的同一类原子的总称。
核素:具有一定数目质子和一定数目中子的一种原子。
同位素:质子数相同而中子数不同的同一元素的不同原子互称为同位素(对于原子来说)二、元素周期表1.编排原则:①按原子序数递增的顺序从左到右排列;②将电子层数相同......的各元素从左到右排成一横行..③把最外层电子数相同........的元素按电子层数递增的顺序从上到下排成一纵行..(注意:周期序数=原子的电子层数;主族序数=原子最外层电子数)2.结构特点:核外电子层数元素种类第一周期 1 2种元素短周期第二周期 2 8种元素周期第三周期 3 8种元素元(7个横行)第四周期 4 18种元素素(7个周期)长周期第五周期 5 18种元素周第六周期 6 32种元素期不完全周期:第七周期 7 未填满(已有26种元素)表主族:7个主族族副族:7个副族(18个纵行)第Ⅷ族:三个纵行(16个族)零族:稀有气体三、元素周期律1.元素周期律:元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着核电荷数的递增而呈周期性变化的规律。
元素性质的周期性变化实质是元素原子核外电..........子排布的周期性变化.........的必然结果。
2.同周期元素性质递变规律(从左到右):电子层数相同,最外层电子数依次增加,原子半径依次减小,金属性减弱,非金属性增强,与H2的化合由难到易,氢化物的稳定性由弱到强。
第一节元素周期表

【解析】选C。本题考查对元素周期表的认识,第1周期只有两
种元素,故A项错。2号元素位于元素周期表中的最后一列,故B
项错。10号元素为稀有气体元素,其下面必为18号稀有气体元
素,故D项错。
类型 二
元素周期表的应用 )
【典例】(2013·聊城高一检测)下列说法正确的是( A.原子序数之差为2的两种元素不可能位于同一主族 B.D-核外有36个电子,则元素D位于第4周期第ⅦA族
二、现行元素周期表的编排原则
周期表 中的顺序给元素编号。 1.原子序数:按照元素在_______ 2.原子序数与原子结构之间的关系: 核电荷数 质子数 核外电子数 。 原子序数=_________=_______=___________
电子层数 原子序数
最外层电子数
电子层数
三、元素周期表的结构 1.周期(横行): 7 个横行,即有__ 7 个周期。 (1)数目:元素周期表有__
C.位于同一主族相邻的甲乙两种元素,甲的原子序数为x,则乙 的原子序数可能为x+4
D.位于同一周期的甲乙两种元素,甲位于ⅠA族,原子序数为x,
乙位于ⅢA族,则乙原子序数可能为x+19
【解题指南】解答本题要注意以下3点: (1)第1~7周期分别含有2、8、8、18、18、32、32种元素,同 一主族两种元素的原子序数的差值为上列数值或连续几个数值 之和。 (2)不同周期ⅠA族与ⅢA族之间相隔的元素数量不一定相同。
(3)简单阴离子的核外电子与同周期的稀有气体相同。
【解析】选B。氢和锂两种元素的原子序数之差为2,却同位于 第ⅠA族,A错误;简单阴离子的核外电子与同周期的稀有气体相 同,D-核外有36个电子,即与第4周期的0族元素Kr处于同一周期, 且D比Kr少一个电子,即在第ⅦA族,B正确;甲乙同主族,根据元
第一章 物质结构 元素周期律快速复习法

(一)离子键
1.离子键:
(1)离子键形成的一般条件:
,特殊:。
(2)形成离子键的微粒:;相互作用:;
2.原子电子式:在元素符号周围用“·”(或“×”)标出最外层电子
(二)共价键
1.共价键:
(1)共价键形成的一般条件:。
(2)形成共价键的微粒:;相互作用:;
2.复杂粒子电子式
(1)阳离子电子式:单核阳离子直接用离子符号表示,多原子阳离子要标出最外层电子,再括
(6)在阳离子( )中:核外电子数=Z-n
(7)在阴离子( )中:核外电子数=Z+m
2.核外电子排布的规律
(1)电子运动的特征:高速,空间小,无确定轨迹。
电子运动的描述:电子云:小黑点的多少表示电子出现机率的多少
(2)分层排布:
①编号:KLMNOPQ……
②层序:1234567……
(3)原子核外电子的排布规律:
上“[ ]”,且“[ ]”右上方标上所带的正电荷。
(2)阴离子电子式:要标出最外层电子,再括上“[ ]”,且“[ ]”右上方标上所带的负电荷。
(3)离子化合物:共价化合:3.极性键和非极性键
(2)极性键形成的一般条件:。
(3)非极性键形成的一般条件:。
4.化学键是。
(三)化学反应的本质是______________________________________________________________________
(4)同主族元素性质的递变
同一主族的元素从上到下,随着核电荷数的,电子层数依次,原子半径逐渐,原子失电子能力逐渐,得电子能力逐渐,所以,元素的金属性逐渐,非金属性逐渐。
表现在:最高价氧化物对应水化物的酸性逐渐,碱性逐渐,非金属单质与氢气化合的能力逐渐,气态氢化物的稳定性逐渐;金属单质与水或酸反应的剧烈程度越来越。
人教版高中化学必修二 第一章 物质结构 元素周期律第一章复习和总结(含答案)

本章重点掌握以下几点:1.元素周期表的结构;2.元素、核素、同位素的辨别;3.核外电子排布规律;4.原子、离子、分子中基本构成微粒间的关系;5.元素周期律及其实质;6.化学键中的相关概念;7.电子式的书写。
要点一、元素周期表1.元素周期表的结构(“七横十八纵”)2.几种关系(1)电子层数=周期数(2)最外层电子数=主族序数=最高正化合价(除F、O)(3)质子数=原子序数(4)∣最高正价∣+∣最低负价∣=8(对非金属元素而言,但对H不适用)注意:O无最高正价(+6),F无正价例题:原子序数为x的元素位于周期表中的ⅡA族,则原子序数为x+1的元素不可能为() A.ⅢA族B.IA族C.镧系元素D.ⅢB族要点二、元素、核素、同位素例题: 是( ) A .氢的五种同位素 B .五种氢元素C .氢的五种同素异形体D .氢元素的五种不同微粒 要点三、原子核外电子排布规律 1.在含有多个电子的原子里,电子依能量的不同是分层排布的,其主要规律是:核外电子总是尽先排布在能量较低的电子层,然后由里向外,依次排布在能量逐步升高的电子层。
2.原子核外各电子层最多容纳2n 2个电子。
3.原子最外层电子数目不超过8个(K 层为最外层时不能超过2个电子)。
4.次外层电子数目不能超过18个(K 层为次外层时不能超过2个),倒数第三层电子数目不能超过32个。
注意:以上规律既相互联系,又互相制约,不能孤立片面的理解。
如M 层为最外层的时候,最多为8个,而不是18个。
H 2H +H 112H 13H 1、、、、要点四、核外电子数相等的微粒例题:两种微粒的质子数和电子数均相等,下列关于两种微粒间关系的说法错误的是( ) A .它们可能是不同的分子 B .它们可能是不同的离子 C .它们可能互为同位素D .它们可能是分子和离子 要点五、元素周期律元素周期表中主族元素性质的递变规律要点六、比较元素的金属性强弱和非金属性强弱的一般方法金属性比较本质原子越易失电子、金属性越强判断依据1.在金属活动顺序表中越靠前,金属性越强。
高中化学 第一章 物质结构元素周期律 1.1 元素周期表(核素)化学教案

第一章第一节元素周期表(核素)
电性和电量
1个电子带1个
单位负电荷1个质子带1个单
位正电荷
不显电性
质量/kg 9.109×10-31 1.673×10-27 1.675×10-27
相对质量1/1836(电子 1.007 1.008
二、从表格得出原子的质量主要取决于哪种微粒?质子和中子的质量
原子的质量主要集中在原子核,质子和中子的相对质量都近似为1,如果忽略电子的质量,将核内所有质子和中子的相对质量取近似值相加起来,所得的数值叫做质量数。
质量数(A)=质子数(Z)+中子数(N)
在化学上,我们为了方便地表示某一原子。
在元素符号的左下角表出其质子数,
左上角标出质量数A
Z
X。
粒子符号质子数(Z)中子数(N)质量数(N)用A
Z
X表示为
①O 8 18
②Al 24 27
③Ar 18 22
④Cl 35
17
Cl
⑤H 1
1
H
科学研究证明,同种元素原子的原子核中,中子数不一定相同。
如组成氢元素的氢原子,就有以下三种:我们把具有一定数目的质子和一定数目的中子的
原子叫核素。
三种不同的氢原子
原子
符号
质了数中子数氢原子名称和简称
①1
1
H 氕(H)
②2
1
H 氘(D)。
高中化学:第一章物质结构 元素周期律 精品教、学案新人教版

第一节元素周期表(第一课时)【学习目标】1、了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系2、初步掌握元素周期表的结构,能根据提供的原子序数判断其在周期表中的位置3、知道元素、核素的含义,了解同位素的概念及相关知识4、通过化学史的学习,养成勇于创新的的品质【重点难点】1、元素周期表的结构2、原子结构与元素周期表的位置相互推断;元素、核素、同位素之间的关系【课前预习】1、1869年,俄国化学家将已知的元素通过分类、归纳,制出了第一张元素周期表,成为化学发展史上的重要里程碑之一。
在周期表中,把相同的元素,按的顺序从左到右排成横行,叫做;把相同的元素,按的顺序排成纵行,称为。
2、原子序数= = = 原子。
3、在周期表中,有些族还有一些特别的名称。
如:第ⅠA族(除氢),又称;第ⅦA族,又称;0族,又称。
X代表一个原子。
4、原子符号Az【思考】元素、核素、同位素的不同和联系。
在周期表中收入了112种元素,是不是就只有112种原子呢?【学习探究】一、元素周期表【阅读思考】请同学们阅读教材P4—P5页,思考回答下面的问题:1、现行的元素周期表编排的依据是什么?如何进行编排的?2、周期表中周期和族划分的依据是什么?【小结】原子序数=核电荷数=质子数=核外电子数周期:电子层数相同的元素,按原子序数递增的顺序从左到右排成横行,称为周期;族:最外层电子数相同的元素,按电子层数递增的顺序由上到下排成纵行,称为族。
【思考】观察元素周期表,回答下列问题:1、周期表中有多少周期?每周期有多少种元素?2、在周期表中共有多少列?分为哪些族?3、在所有族中,元素最多的族是哪一族?共有多少种元素?4、在周期表中的第18列(稀有气体元素)为何称为0族?【小结】横行叫周期,共有七周期;一~三短周期,其余长周期;竖行称作族,总共十六族;Ⅷ族最特殊,三行是一族;一、八依次现,一、零再一遍;二、三分主副;先主后副族;镧、锕各十五,均属ⅢB族。
高中化学必修2第一章第一节元素周期表

高中化学必修2《高中新课标优秀教案》第一章物质结构、元素周期律从容说课物质结构,元素周期律是中学化学重要理论组成部分,是中学化学教学的重点,也是难点。
新教材把本章内容作为必修2的第一章,足以体现了它的重要性。
本章包括三节内容:第一节:元素周期律;第二节:元素周期律;第三章:化学健。
根据新课标要求及新课改精神,必修内容只要学生具备化学学科的基本知识,具备必需的学科素养,新教材的安排,正好体现了这一要求。
三节内容,都属于结构理论的基础知识,学生只有具备这些知识,对该结构理论才能有初步的了解,也才有可能进一步继续学习选修内容。
新教材在这部分内容的编排上,打乱了原有的知识体系,首先介绍周期表,给学生以感性认识,然后简略地介绍了周期表的形成过程,逐步引入主题:现行的周期表。
既让学生了解了科学家探索的过程,也有利于学生掌握这些知识。
其间穿插碱金属元素,卤族元素等知识,使抽象的内容具体化,便于学生归纳总结,形成规律,为第二节元素周期律打下基础。
第二节:元素周期律。
新教材在初中学习的基础上,直接给出了1-20号元素核外电子排布,删去“电子云”等一些抽象的概念,大大降低了学习难度,然后,以第三周期为例,或以实验,或以给出的图表,让学生动手推出结论,体现了学生的参与意识。
第三节:化学键,以NaCl、HCl为例介绍了离子键,共价键的知识,简明扼要,学生理解难度并不大。
教学时,可以多举典型实例,使抽象问题具体化,以帮助学生巩固概念。
教学时要充分利用教材上所提供的图表,引导学生归纳、总结推理、探究,切忌教师照本宣科,给出现成的结论,这样,学生不经过分析、观察,生吞活剥教师所讲授的内容,实践证明,既不利于掌握知识,更不利于培养能力。
通过本章学习,力求让学生体会理论对实践的指导作用,使学生在结构理论的指导下,更好地为以后学习服务。
本章教学重点:元素周期表的结构,元素周期建;离子键、共价健,元素在周期表中的位置、原子结构、元素性质的关系。
2019高考化学(物质结构元素周期律)第1节原子结构考点(2)原子核外电子排布讲与练(含解析)

物质结构元素周期律李仕才第一节原子结构考点二原子核外电子排布1.电子层的表示方法及能量变化2.原子核外电子排布规律(1)核外电子一般总是尽可能地先排布在能量较低的电子层里。
(2)每个电子层最多容纳的电子数为2n2个。
①最外层最多容纳电子数不超过8个(K层为最外层时不超过2个)。
②次外层最多容纳的电子数不超过18个,倒数第三层最多容纳的电子数不超过32个。
3.核外电子排布的表示方法(1)原子结构示意图(以Na为例)(2)离子结构示意图主族中的金属元素的原子失去最外层电子形成与稀有气体元素原子电子层结构相同的阳离子,非金属元素的原子得到电子形成与稀有气体元素原子电子层结构相同的阴离子:4.常见“10电子”“18电子”微粒(1)“10电子”的微粒:(2)常见的“18电子”的微粒:判断正误(正确的打“√”,错误的打“×”)1.硫离子的结构示意图:。
( ×)2.最外层电子数为8的粒子一定是稀有气体元素原子。
( ×)3.非金属元素原子的核外电子数一般大于或等于4。
( √)4.核外电子首先占据能量较高的电子层。
( ×)5.某原子M层上电子数为L层上电子数的4倍。
( ×)6.NH+4与Na+的质子数与电子数均相同。
( √)7.16O和18O是氧元素的两种核素,16O与18O核外电子排布方式不同。
( ×)8.M层是最外层时,最多能容纳18个电子。
( ×)9.某元素原子的最外层电子数是次外层的a倍(a>1),则该原子核外电子排布只有两层。
( √)10.最外层电子数相同的元素,其化学性质一定相同。
( ×)11.核外电子排布相同的微粒化学性质也相同。
( ×)12.1.00 mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023。
( √)13.多电子原子中,在离核较近的区域内运动的电子能量较高。
人教版高中化学必修 化学2 第一章 第一节 元素周期表(第1课时)

6
55
56
5771
72
73
74
75 76
77 78 79
80 81
82
83
84 85 86
7
87
88
89103
104
105
106
107
108
109
110
111
112
过渡元素
镧系
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
锕系
89
90
91
92
93
94
95
96
97
98
99
100
101
102
VIII
IB
IIB
Sc
Ti
21 钪 22钛
V 23钒
1
2
IA H 1氢 Li 3锂 Na 11钠 K 19钾
IIA Be 4铍 Mg 12镁 Ca 20钙
3
4
2020/4/25
Cr 24铬
Mn 25锰
Fe 26铁
Co 27钴
Ni 28镍
Cu 29铜
A:主族
B:副族
IIIA B 5硼 Al 13铝
IVA C 6碳 Si 14硅
另外,特别族名称:第ⅦA 族—卤族元素
第 0 族—稀有气体元素
2020/4/25
江西省鹰潭市第一中学 桂耀荣
18
一、元素周期表
课堂小结: 1、元素周期表的结构:
七主七副七周期,Ⅷ族零族镧锕系。
2、元素原子结构与其在周期表中位置的关系:
元素周期表(第一课时)

二、编排原则 1、按照原子序数(核电荷数)递增的顺序从左到右排列。 2、将电子层数相同的元素,按原子序数递增的顺序从 左到右排成一横行—周期。 3、把最外层电子数相同的元素,按电子层数递增的顺 序由上而下排成一纵行—族。
三、元素周期表的结构
1、周期 周期序数 = 电子层数
①元素周期表中具有相同的电子层数的元素,
N : +7 2 5
O : +8 2 6
F : +9 2 7 Ne : +10 2 8
Na : +11 2 8 1 Mg :+12 2 8 2 Al : +13 2 8 3 Si : +14 2 8 4
P : +15 2 8 5 S : +16 2 8 6 Cl : +17 2 8 7 Ar : +18 2 8 8
57
6 55 56 - 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
71
18 32
7 87
88
89103
104
105
106
107
108
109
110
111
112
【小结】对于ⅢA到ⅦA族, 同主族相邻元素的原子序数相差下一周期所容纳元素种。类
2、同主族相邻元素的原子序数之差:
8 5 6 7 8 9 10
III IV V VI VII
3 11 12 B B B B B
VIII
8 IB
II B
13 14 15 16 17 18
M L k
18 4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
第一节元素周期表

归纳:碱金属的主要物理性质
相似性: 1) 银白色有金属光泽(铯略带金色) 2) 较柔软,有延展性 3) 密度小 4) 熔点低(均小于200℃) 5) 导电、导热
递变性: 随着核电荷数的增加:
• 密度增大 (但K 反常) • 熔、沸点逐渐降低
2、卤族元素
(1)物理性质
物理性质
随原子序数的递增: 1.颜 色: 颜色逐渐加深 2.状 态: 气态~液态~固态 3.熔沸点: 逐渐升高 4.密 度: 逐渐增大
(2)原子结构
(3)化学性质
①卤素单质与氢气反应
卤素单质与氢气反应 剧烈程度:F2>Cl2>Br2>I2 生成氢化物稳定性:
HF>HCl>HBr>HI
②卤素单质间的置换反应
颜色
溶于水
溶于CCl4
Cl2
黄绿色
黄绿色
黄绿色
Br2
深红棕色 橙黄色
橙红色
I2
紫黑色
褐色
紫红色
实验1—1
实验
现象
化学方程式
57
6 55 56 - 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
71
7 87 88 89103
104
105
106
107
108
109
110
111
112
过渡元素
镧 系 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71
碳有两个电子层,位于第二周期,镁有三个电子层, 位于第三周期;溴有四个电子层,位于第四周期。
(2)族(16个) 七个主族 七个副族 一个第Ⅷ族(3个纵行) 一个0族
2019-2020学年人教版高中化学必修二(全册)

价值观
2.锻炼团结协作的精神
3.了解内因与外因的关系
2019/10/9
思维激活
纵观化学史,在元素周期律的发现过程中,不论是拉瓦 锡的最初尝试,还是德贝莱纳、纽兰兹、门捷列夫等人的具 体探索,无不浸透着科学家对化学的探究。这些探究不仅表 现在元素周期律的外部形式之上,而且深入到了它的内部联 系之中。科学家的探究途径中化学实验贡献甚大,化学实验 是化学基石,是检验化学理论的标准。那么,如何通过实验 来探究元素结构与性质的关系呢?
结论 ―F―2――C―l2――B―r2――I→2 a.剧烈程度:逐渐减弱 b.生成 HX 的稳定性:逐渐减弱
化学方程式
H2+F2=2HF
H2+
光照
Cl2=====2HCl
H2+Br2==△===2HBr
H2+I2 △ 2HI
2019/10/9
(2)卤素间的置换反应实验
实验
现象
化学方程式
a.将少量新制的饱和氯水加 入盛有 NaBr 溶液的试管中, 振荡后加 CCl4,振荡,静置
____________________________________。
答案 (1)2Li+2H+=2Li++H2↑ (2)2Rb+2H2O=2Rb++2OH-+H2↑
2019/10/9
②差异性:随着核电荷数的增加,碱金属元素原子的电 子层数逐渐增多,原子半径逐渐增大。碱金属元素的性质也 有差异,从锂到铯,单质还原性逐渐增强,如钾与氧气或水 反应比钠的反应剧烈,铷、铯的反应更剧烈。
答案 不正确;0族中的He元素和某些副族元素(如Zn)原 子的最外层电子数也为2。
名师解惑
一、元素周期表(长式)的结构
2019/10/9
2019/10/9
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
元素性质的递变规律与元素组成微粒结构的联系
课型
讲授:习题:复习:讨论:其他:
集体备课教案
个人备课教案
复习原子结构示意图:
我们把ⅠA称为碱金属族,我们为什么要把他们编在一个族呢?请同学们观察碱金属的原子结构示意图,分析碱金属原子结构的共同之处。
1、下面我们通过实验来探讨同一族元素的性质。
[实验1]将一干燥的坩埚加热,同时取一小块钾,擦干表面的煤油后,迅速的投入到热坩埚中,观察现象。同钠与氧气的反应比较。
相
似
点
颜色
均
较小
熔沸点
较低
导电导热性
强
递变性
密度变化
逐渐增大(K特殊)
熔沸点变化
单质的熔沸点逐渐降低
有上表可见,碱金属在物理性质上也表现出一些相似性和规律性。
刚才我们以典型的金属一族为例,下面我们以典型的非金属为例。看看他们的性质有原子结构间是否存在联系?
3、补充习题
1、下列说法中错误的是
A.原子及其离子的核外电子层数等于该元素所在周期数
B.元素周期表中从ⅢB族到ⅡB族10列的元素都是金属元素
C.除氦外的稀有气体原子的最外层电子数都是8个
D.同一元素的各种同位素的物理性质和化学性质完全相同
2.鉴别Cl-、Br-、I-可以选用的试剂是
A.碘水,淀粉溶液B.氯水,四氯化碳
A.FeCl3B.K2SO3C.KNO3D.Na2S
教学回顾与反思
[实验2]在培养皿中放入一些水,然后取绿豆大的钾,吸干表面的煤油,投入到培养皿中,观察现象。同钠与水的反应进比较
根据实验讨论钠与钾的性质有什么相似性和不同。你认为元素的性质与他们的原子结构有关系吗?
同一主族元素化学性质相似。且
Li Na K Rb
还原性增加
2、
碱金属的物理性质的比较
Li Na k Rb Cs
C.淀粉,KI溶液D.硝酸银溶液,稀HNO3
3.砹(At)是卤族元素中位于碘后面的元素,试推测砹和砹的化合物最不可能具备的性质是
A.砹易溶于某些有机溶剂B.砹化氢很稳定不易分解
C.砹是有色气体D.砹化银不溶于水或稀HNO3
4、在HI溶液中滴加淀粉溶液无明显变化,但加入某种物质后,溶液立即变蓝。该物质可能是。
过程
与
方法
1、培养学生的抽象思维能力和逻辑思维能力;通过对元素原子结构、位置间的关系的推导,培养学生的分析和推理能力。
2、通过对元素周期律和元素周期表的关系的认识,渗透运用辩证唯物主义观点分析现象和本质的关系。
情感
态度
价值观
培养学生的求实、严谨和创新的优良品质;提高学生的学习兴趣
重点
同周期、同主族性质的递变规律
2019-2020学年高中化学第一章物质结构元素周期律第一节元素周期表第2课时教案4新人教版必修2
教
学
目
的
知识
与
技能
1、了解原子结构与元素性质的关系。
2、能初步学会总结元素递变规律的能力,具有把元素的性质、元素周期表的位置与元素组成微粒的结构初步联系起来并在一定条件下相互转化的运用能力
3、通过对元素性质的递变规律与元素组成微粒结构的联系。从而认识事物变化过程中量变引起质变的规律性,接受辨证唯物主义观点的教育。
