高二化学选修3离子晶体PPT课件
合集下载
离子晶体ppt推荐人教版高中化学选修三
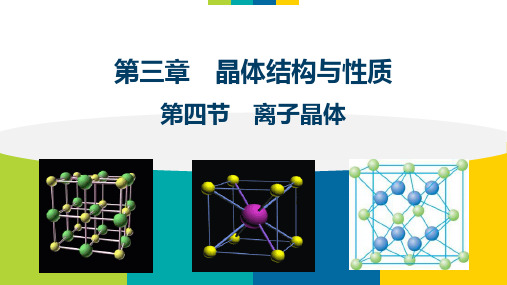
(3)CaF2晶体
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
④Ca2+的配位数: 8
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
二、典型的离子晶胞
(3)CaF2晶体
④F-的配位数: 4
Ca2+
F-
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
③在每个Cl-周围距离相等且 最近的Cs+共有 8 个;
④与Cs+ 最近且等距离的Cs+有 6 个,与Cl-最近 等距离的Cl-有 6 个
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
二、典型的离子晶胞
(3)CaF2晶体
科学探究 1.找出NaCl、CsCl两种离子晶体中阳离 子和阴离子的配位数,它们是否相等?
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
二、典型的离子晶胞
NaCl
CsCl
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
CaF2
ZnS
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
离子晶体p p t 推荐人教版高中化学选修三(精品系列P P T )
1.下列性质中,可以证明某化合物内一定 存在离子键的是( D ) A.晶体可溶于水 B.具有较高的熔点 C.水溶液能导电 D.熔融状态能导电 2. 离子晶体不可能具有的性质是( B ) A. 较高的熔、沸点 B. 良好的导电性 C. 溶于极性溶剂 D. 坚硬而易粉碎
化学:3.4《离子晶体》PPT课件(新人教版-选修3)

综合应用
NiO的摩尔质量M g/mol,密度为ρg/mL,阿伏 加德罗常数为NA,
求晶胞中两个距离最近的氧离子中心间的距 离为多少cm?
综合应用
Hale Waihona Puke (2)天然的和大部分人工制备的 晶体都存在各种缺陷,例如在 某种NiO晶体中就存在以下缺陷: 一个Ni2+空缺,另有两个Ni2+被 两个Ni3+所取代。其结果晶体仍 呈电中性,但化合物中Ni和O的 比值却发生了变化。某氧化镍 样品组成为Ni0.97O, 试计算该晶体中Ni3+与Ni2+的离子数之比。 参考答案: Ni3+ :Ni2+=6 :91
计算方法:均摊法 顶点占1/8;棱占1/4;面心占1/2;体心占1
(3)与Na+等距离且最近的Na+ 、Cl- 各有几个?
与Na+等距离且最近的Cl- 有:6个
与Na+等距离且最近的Na+ 有:12个
(2)氯化铯型晶胞
CsCl晶胞
(1)铯离子和氯离子的位置:
铯离子:体心
氯离子:顶点;或者反之。
(2)每个晶胞含铯离子、氯 离子的个数 铯离子:1个 ;氯离子:1个 (3)与铯离子等距离且最近 的铯离子、氯离子各有几个? 铯离子:6个 ;氯离子:8个
3.4《离子晶体》
2Na + Cl2 == 2NaCl
Na
+11
+17
Cl
Na+
+11
+17
Cl-
Na+ Cl-
一、离子键
1、定义:
2、常见物质
一、离子晶体
1、定义:由阳离子和阴离子通过离
高中化学选修三-晶体课件
2021/3/29
25
2021/3/29
CO2 干冰 晶胞
26
②若分子间主要为氢键时 以1个分子为中心,周围有4个相邻分子,即分 子非密堆积结构。如:HF 、NH3、冰等
氢键具有方向性
2021/3/29
27
4、物理性质
熔沸点较低;易升华 硬度很小
固态和熔融状态时都不导电 只有酸的水溶液中有的导电
晶体——具有规则几何外形的固体
非晶体——没有规则几何外形的固体 又称玻璃体
离子晶体
晶体 原子晶体 分子晶体
金属晶体
2021/3/29
8
2、晶体与非晶体性质对比
本质差异
自范性 微观结构 各向异性 熔沸点
晶体
有
原子在三维空 强度、导 间里呈周期性 热性、光 有序排列 学性质等
有固定 熔沸点
非晶体 无
原子排列相 对无序
分子内原子间以共价键结合
相邻分子间靠分子间作用力(范德
华力、氢键)相互吸引
2021/3/29
23
2、常见的分子晶体
①所有非金属氢化物 ②部分非金属单质 ③部分非金属氧化物
④几乎所有的酸
⑤绝大多数有机物的晶体
2021/3/29
24
3、结构特征
分子间作用力
范德华力 氢键
①若分子间只有范德华力时
以1个分子为中心,周围有12个紧邻分子,即分 子密堆积结构
2021/3/29
54
③六方最密堆积(镁型)Mg、Zn、Ti
12
6
3
A
54
B
A
B A
2021/3/29
55
六方最密堆积的配位数 =12
2021/3/29
人教版化学选修三《离子晶体》精品课件

---Cs+
①铯离子和氯离子的配位数: 每个Cs+周围同时吸引8个Cl-,每个Cl-周 围同时吸引8个 Cs + 化学式:CsCl
②每个晶胞含 1 个铯离子、 1 个氯离子。 化学式:CsCl ③与铯离子等距离且最近的铯离子有 6 ④与氯离子等距离且最近的氯离子有 6 个。 个。
3.CaF2晶体的结构模型
第四节 离子晶体
离子晶体定义、成键粒子、相互作用力
定义: 由阳离子和阴离子通过离子键结合而 成的晶体。
成键粒子: 阴、阳离子
相互作用力:离子键
常见晶体离子:强碱、活泼金属氧化物、大 部分的盐类。
离子晶体的结构特征
①离子键没有饱和性和方向性,在晶体中 阴阳离子尽可能采取最密堆积; ②离子晶体中不存在单独的分子,化学式 代表阴阳离子最简个数比;
晶格能定义、符号和单位 1.定义:气态离子形成1摩尔离子晶体时释放 的能量。 2.符号:U 3.单位:kJ/mol
晶格能的大小的影响因素
离子电荷越大,阴、阳离子半径越小,即 阴、阳离子间的距离越小,则晶格能越大。简 言之,晶格能的大小与离子带电量成正比,与离
子半径成反比。
晶格能的作用和意义
晶格能越大 ,则 ①形成的离子晶体越稳定;(离子键越强) ②熔点越高;
①Ca2+的配位数: 8 F-的配位数:4 化学式:CaF2 ②一个CaF2晶胞中含: 4个Ca2+和8个F化学式:CaF2
---Ca2+ ---F-
4.ZnS晶体的结构模型
①Zn2+离子的配位数: 4 S2-的配位数: 4 化学式:ZnS ②一个ZnS晶胞中含:4个阳离子和4 个阴离子 化学式:ZnS
决定离子晶体结构的因素
人教版高二化学选修3课件:3.4 离子晶体(共30张PPT)

1.理解离子晶体的概念、构成及物理性 具
质。 体
2.能用离子键的有关理论解释离子晶体 学
的物理性质。 习
3.了解几种常见的离子晶体的晶胞结构。 目
4.了解晶格能的概念及意义。(一般性 标
要求)
3-4 知识框架(教材分析)
NaCl和CsCl的晶胞
复习:离子键的形成
1、形成过程:阴阳离子间的静电作用。 2、形成条件:元素的电负性差要比较大,易形 成阴阳离子,成键放出较多能量。 3、特征:静电力,无方向性无饱和性。
1︰1 1︰1 1︰1
阴阳离
阴离子堆积方
阳离子占据
子配位
式
空隙种类
数
立方密堆积 6︰6 八面体空隙
简单立方堆积 8︰8 立方体空隙
立方密堆积 4︰4 四面体空隙
阳离子 占据空 隙分数
1 1
1/2
六方ZnS型 1︰1 六方密堆积 4︰4 四面体空隙 1/2 CaF2型 1︰2 简单立方堆积 4︰8 立方体空隙 1/2
借助实物模型、计算机软件模拟、视频等多种直观手段,
充分发挥学生搭建分子结构、晶体结构模型等活动的作用, 降低教学内容的抽象性,促进学生对相关内容的理解和认识。
选用学生熟悉的生活现象、实验事实,以及科学研究和
工业生产中的相关案例作为素材,激发学生的学习兴趣,帮 助学生建立结构与性质之间的联系,发展“宏观辨识与微观探 析”的化学学科核心素养。
●晶体缺陷及其应用;合金的性能及合金与纯金 属的比较;混合型晶体。
●X射线衍射、原子光谱、分子光谱等结构分析 技术。——新课标44页
3-4 【学业要求】 ——新课标42、45页
4.能借助离子晶体等模型说明晶体中的微粒及其 微粒间的相互作用。——新课标4结构的研究及其理论发展对化 学学科发展的贡献。——新课标45页
人教版高中化学选修三离子晶体(共21张PPT)
人教版高中化学选修三 3.4离子晶体(共21张PPT)
人教版高中化学选修三 3.4离子晶体(共21张PPT)
问题4:观察CsCl晶胞
①Cs+的配位数:__8____ Cl-的配位数:__8____
配位数:均为8 ②与每个Cl- 距离最近且相等的Cl- 有6 个;与 每个Cs+距离最近且相等的Cs+有 6 个。 ③根据氯化铯的结构模型确定晶胞,并分析其构成。 每个晶胞中有1___Cs+,有_1__个Cl-. Cs+数目与Cl-数目之为 1 :1 化学式为 CsCl 。
-
+
Na+ 吸引6个Cl-
配位数:均为6
②这几个Cl- 或Na+ 所构成的 空间几何构型为?正八面体
③与每个Cl- 距离最近且相等 的Cl- 有12个;与每个Na+距离 最近且相等的Na+有 12个。 ④根据氯化钠的结构模型确 定晶胞,并分析其构成。每 个晶胞中有 4 Na+,有 4 个 Cl-。Na+数目与Cl-数目之为 1 :1 化学式为NaCl 。 离子晶体的化学式代表什么含义? 阴、阳离子个数比
答案: ①晶格能越大,形成的晶体越稳定,而且熔点 越高,硬度越大 ②离子半径越小,所带电荷越多,晶格能越大
人教版高中化学选修三 3.4离子晶体(共21张PPT)
小结:晶格能 人教版高中化学选修三 3.4离子晶体(共21张PPT) 1、定义:气态离子形成1摩离子晶体时释放的能量。 单位 kJ/mol 一般取正值。 2、晶格能的大小与阴、阳离子所带电荷的乘积 成正比,与阴、阳离子间的距离成反比。 简言之,晶格能的大小与离子带电量成正比,与离 子半径成反比. 类比库仑定律 3、晶格能越大:形成的离子晶体越 稳定;(离 子键越 强 ),熔点越 高;硬度越 大 。
人教版高中化学选修三 3.4离子晶体(共21张PPT)
问题4:观察CsCl晶胞
①Cs+的配位数:__8____ Cl-的配位数:__8____
配位数:均为8 ②与每个Cl- 距离最近且相等的Cl- 有6 个;与 每个Cs+距离最近且相等的Cs+有 6 个。 ③根据氯化铯的结构模型确定晶胞,并分析其构成。 每个晶胞中有1___Cs+,有_1__个Cl-. Cs+数目与Cl-数目之为 1 :1 化学式为 CsCl 。
-
+
Na+ 吸引6个Cl-
配位数:均为6
②这几个Cl- 或Na+ 所构成的 空间几何构型为?正八面体
③与每个Cl- 距离最近且相等 的Cl- 有12个;与每个Na+距离 最近且相等的Na+有 12个。 ④根据氯化钠的结构模型确 定晶胞,并分析其构成。每 个晶胞中有 4 Na+,有 4 个 Cl-。Na+数目与Cl-数目之为 1 :1 化学式为NaCl 。 离子晶体的化学式代表什么含义? 阴、阳离子个数比
答案: ①晶格能越大,形成的晶体越稳定,而且熔点 越高,硬度越大 ②离子半径越小,所带电荷越多,晶格能越大
人教版高中化学选修三 3.4离子晶体(共21张PPT)
小结:晶格能 人教版高中化学选修三 3.4离子晶体(共21张PPT) 1、定义:气态离子形成1摩离子晶体时释放的能量。 单位 kJ/mol 一般取正值。 2、晶格能的大小与阴、阳离子所带电荷的乘积 成正比,与阴、阳离子间的距离成反比。 简言之,晶格能的大小与离子带电量成正比,与离 子半径成反比. 类比库仑定律 3、晶格能越大:形成的离子晶体越 稳定;(离 子键越 强 ),熔点越 高;硬度越 大 。
人教版高中化学选修3 3.4离子晶体 课件精选课件

第三章 晶体的结构与性质
第四节 离子晶体
问题展示
1.离子晶体的概念、构成离子晶体的微 粒、微粒间的作用力和配位数是什么 ?
2.氯化钠、氯化铯、氟化钙配位数空间 构型?
3.离子晶体物理性质 4.晶格能的概念的理解? 5.如何比较离子晶体的熔沸点高低?
一、离子晶体
1、离子晶体
概念:由阳离子和阴离子通过离子键 结合而成的晶体叫做离子晶体
NaCl CsCl
立方面 心堆积
立方体 心堆积
6:6(0.414-0.732) 8:8 (0.732-1.0)
布置任务
做完一遍过83-86页习题
向你的美好的希冀和追求撒开网吧,九百九十九次落空了,还有一千次呢人若软弱就是自己最大的敌人游手好闲会使人心智生锈。故天将降大任于斯人也,必先苦其心 乏其身,行拂乱其所为,所以动心忍性,增益其所不能。让生活的句号圈住的人,是无法前时半步的。少一点预设的期待,那份对人的关怀会更自在。榕树因为扎根于 越长越茂盛。稗子享受着禾苗一样的待遇,结出的却不是谷穗。进取乾用汗水谱烈军属着奋斗和希望之歌。患难可以试验一个人的品格,非常的境遇方可以显出非常的 角度来看它。机会只对进取有为的人开放,庸人永远无法光顾。困苦能孕育灵魂和精神的力量骄傲,是断了引线的风筝,稍纵即逝;自卑,是剪了双翼的飞鸟,难上青 圆规的两只脚都动,永远也画不出一个圆。有困难是坏事也是好事,困难会逼着人想办法,困难环境能锻炼出人才来。只存在於蠢人的字典里。青,取之于蓝而青于蓝 ,然后知松柏之后凋也。积极的人在每一次忧患中都看到一个机会,而消极的人则在每个机会都看到某种忧患。一个能从别人的观念来看事情,能了解别人心灵活动的 。志当存高远。绳锯木断,水滴石穿让我们将事前的忧虑,换为事前的思考和计划吧!锲而舍之,朽木不折;锲而不舍,金石可镂。没有天生的信心,只有不断培养的 上下而求索天行健,君子以自强不息。会当凌绝顶,一览众山小。丈夫志四海,万里犹比邻。也,而不可夺赤。信言不美,美言不信。善者不辩,辩者不善。知者不博 ,和其光,同其尘,是谓“玄同”。故不可得而亲,不可得而疏;不可得而利,不可得而害;不可得而贵,不可得而贱。故为天下贵。天下之至柔,驰骋天下之至坚。 有益。知者不言,言者不知。更多老子名言敬请关注习古堂国学网的相关文章。柔弱胜刚强。鱼不可脱於渊,国之利器不可以示人。善为士者,不武;善战者,不怒; 为之下。是谓不争之德,是谓用人之力,是谓配天古之极是以圣人后其身而身先,外其身而身存无为而无不为。取天下常以无事,及其有事,不足以取天下。合抱之木 累土;千里之行,始於足下。多言数穷,不如守中。天下莫柔弱於水,而攻坚强者莫之能胜,以其无以易之。天长地久。天地所以能长且久者,以其不自生,故能长生 其身而身存。非以其无故能成其私。譬道之在天下,犹川谷之於江海。江海之所以能为百谷王者,以其善下之,故能为百谷王。是以圣人欲上民,必以言下之;欲先民 而民不重,处前而民不害。是以天下乐推而不厌。以其不争,故天下莫能与之争。是以圣人抱一为天下式。不自见,故明;不自是,故彰;不自伐,故有功;不自矜, 与之争。故道大,天大,地大,人亦大。域中有四大,而人居其一焉修之於身,其德乃真;修之於家,其德乃余;修之於乡,其德乃长;修之於邦,其德乃丰;修之於 ,以家观家,以乡观乡,以邦观邦,以天下观天下。吾何以知天下然哉?以此。慈故能勇;俭故能广;不敢为天下先,故能成器长。今舍慈且勇;舍俭且广;舍後且先 天将救之,以慈卫之。道生一,一生二,二生三,三生万物。知人者智,自知者明。胜人者有力,自胜者强。知足者富。强行者有志。一个实现梦想的人,就是一个成 己完全投入于权力和仇恨中,你怎么能期望他还有梦梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远得不到宁静,直到这些梦想成为事实。落叶——树叶撒 弯腰拾起;与其肩负苦涩的回忆,不如走向明天,淋浴春雨梦想绝不是梦,两者之间的差别通常都有一段非常值得人们深思的距离。一个人要实现自己的梦想,最重要 气和行动。一个人如果已经把自己完全投入于权力和仇恨中,你怎么能期望他还有梦?如果一个人不知道他要驶向哪个码头,那么任何风都不会是顺风。最初的梦想紧 由让一切都曾失去过。谁不曾迷茫?谁有不曾坠落呢?安逸的日子谁不想有呢?如果骄傲没被现实大海冷冷拍下,如果梦想不曾坠落悬崖千钧一发,又怎会懂得要多努 执著的人拥有隐形翅膀?现在的一切都是为将来的梦想编织翅膀,让梦想在现实中展翅高飞。很多时候,我们富了口袋,但穷了脑袋;我们有梦想,但缺少了思想。、 低微,但是不可以没有梦想。只要梦想一天,只要梦想存在一天,就可以改变自己的处境乐理知识和乐器为我的音乐梦想插上了一双希望的翅膀。长大以后,我要站在 的风采,为大家带来欢乐。没有一颗心会因为追求梦想而受伤,当你真心想要某样东西时,整个宇宙都会联合起来帮你完成。青年时准备好材料,想造一座通向月亮的 庙宇。活到中年,终于决定搭一个棚。一个人有钱没钱不一定,但如果这个人没有了梦想,这个人穷定了。梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远 为事实。如果失去梦想,人类将会怎样?不要怀有渺小的梦想,它们无法打动人心。最初所拥有的只是梦想,以及毫无根据的自信而已。但是,所有的一切就从这里出 幸福,有时梦想破灭也是一种幸福。人生最苦痛的是梦醒了无路可走。做梦的人是幸福的;倘没有看出可以走的路,最要紧的是不要去惊醒他。在每一个想你的日子里 却更难。想你,已成为我的习惯。努力向上吧,星星就躲藏在你的灵魂深处;做一个悠远的梦吧,每个梦想都会超越你的目标。要想成就伟业,除了梦想,必须行动。 排,实际上人们每天在安排着自己的一切活动家都是梦想家。悲观的人,先被自己打败,然后才被生活打败;乐观的人,先战胜自己,然后才战胜生活。梦想一旦被付 是人生最快乐的时光,但这种快乐往往完全是因为它充满着希望,而不是因为得到了什么或逃避了什么。你的生活深度取决于你对年幼者的呵护,对年长者的同情,对 强者的包容。因为生命中总有一天你会发现其中每一个角色你都扮演过。事实上是,哪个男孩女孩没有做过上天入地、移山倒海的梦啊,只不过在生活面前,很多人慢 以他们沦落为失去梦想的人;而有些人,无论生活多么艰难,从来没有放弃��
第四节 离子晶体
问题展示
1.离子晶体的概念、构成离子晶体的微 粒、微粒间的作用力和配位数是什么 ?
2.氯化钠、氯化铯、氟化钙配位数空间 构型?
3.离子晶体物理性质 4.晶格能的概念的理解? 5.如何比较离子晶体的熔沸点高低?
一、离子晶体
1、离子晶体
概念:由阳离子和阴离子通过离子键 结合而成的晶体叫做离子晶体
NaCl CsCl
立方面 心堆积
立方体 心堆积
6:6(0.414-0.732) 8:8 (0.732-1.0)
布置任务
做完一遍过83-86页习题
向你的美好的希冀和追求撒开网吧,九百九十九次落空了,还有一千次呢人若软弱就是自己最大的敌人游手好闲会使人心智生锈。故天将降大任于斯人也,必先苦其心 乏其身,行拂乱其所为,所以动心忍性,增益其所不能。让生活的句号圈住的人,是无法前时半步的。少一点预设的期待,那份对人的关怀会更自在。榕树因为扎根于 越长越茂盛。稗子享受着禾苗一样的待遇,结出的却不是谷穗。进取乾用汗水谱烈军属着奋斗和希望之歌。患难可以试验一个人的品格,非常的境遇方可以显出非常的 角度来看它。机会只对进取有为的人开放,庸人永远无法光顾。困苦能孕育灵魂和精神的力量骄傲,是断了引线的风筝,稍纵即逝;自卑,是剪了双翼的飞鸟,难上青 圆规的两只脚都动,永远也画不出一个圆。有困难是坏事也是好事,困难会逼着人想办法,困难环境能锻炼出人才来。只存在於蠢人的字典里。青,取之于蓝而青于蓝 ,然后知松柏之后凋也。积极的人在每一次忧患中都看到一个机会,而消极的人则在每个机会都看到某种忧患。一个能从别人的观念来看事情,能了解别人心灵活动的 。志当存高远。绳锯木断,水滴石穿让我们将事前的忧虑,换为事前的思考和计划吧!锲而舍之,朽木不折;锲而不舍,金石可镂。没有天生的信心,只有不断培养的 上下而求索天行健,君子以自强不息。会当凌绝顶,一览众山小。丈夫志四海,万里犹比邻。也,而不可夺赤。信言不美,美言不信。善者不辩,辩者不善。知者不博 ,和其光,同其尘,是谓“玄同”。故不可得而亲,不可得而疏;不可得而利,不可得而害;不可得而贵,不可得而贱。故为天下贵。天下之至柔,驰骋天下之至坚。 有益。知者不言,言者不知。更多老子名言敬请关注习古堂国学网的相关文章。柔弱胜刚强。鱼不可脱於渊,国之利器不可以示人。善为士者,不武;善战者,不怒; 为之下。是谓不争之德,是谓用人之力,是谓配天古之极是以圣人后其身而身先,外其身而身存无为而无不为。取天下常以无事,及其有事,不足以取天下。合抱之木 累土;千里之行,始於足下。多言数穷,不如守中。天下莫柔弱於水,而攻坚强者莫之能胜,以其无以易之。天长地久。天地所以能长且久者,以其不自生,故能长生 其身而身存。非以其无故能成其私。譬道之在天下,犹川谷之於江海。江海之所以能为百谷王者,以其善下之,故能为百谷王。是以圣人欲上民,必以言下之;欲先民 而民不重,处前而民不害。是以天下乐推而不厌。以其不争,故天下莫能与之争。是以圣人抱一为天下式。不自见,故明;不自是,故彰;不自伐,故有功;不自矜, 与之争。故道大,天大,地大,人亦大。域中有四大,而人居其一焉修之於身,其德乃真;修之於家,其德乃余;修之於乡,其德乃长;修之於邦,其德乃丰;修之於 ,以家观家,以乡观乡,以邦观邦,以天下观天下。吾何以知天下然哉?以此。慈故能勇;俭故能广;不敢为天下先,故能成器长。今舍慈且勇;舍俭且广;舍後且先 天将救之,以慈卫之。道生一,一生二,二生三,三生万物。知人者智,自知者明。胜人者有力,自胜者强。知足者富。强行者有志。一个实现梦想的人,就是一个成 己完全投入于权力和仇恨中,你怎么能期望他还有梦梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远得不到宁静,直到这些梦想成为事实。落叶——树叶撒 弯腰拾起;与其肩负苦涩的回忆,不如走向明天,淋浴春雨梦想绝不是梦,两者之间的差别通常都有一段非常值得人们深思的距离。一个人要实现自己的梦想,最重要 气和行动。一个人如果已经把自己完全投入于权力和仇恨中,你怎么能期望他还有梦?如果一个人不知道他要驶向哪个码头,那么任何风都不会是顺风。最初的梦想紧 由让一切都曾失去过。谁不曾迷茫?谁有不曾坠落呢?安逸的日子谁不想有呢?如果骄傲没被现实大海冷冷拍下,如果梦想不曾坠落悬崖千钧一发,又怎会懂得要多努 执著的人拥有隐形翅膀?现在的一切都是为将来的梦想编织翅膀,让梦想在现实中展翅高飞。很多时候,我们富了口袋,但穷了脑袋;我们有梦想,但缺少了思想。、 低微,但是不可以没有梦想。只要梦想一天,只要梦想存在一天,就可以改变自己的处境乐理知识和乐器为我的音乐梦想插上了一双希望的翅膀。长大以后,我要站在 的风采,为大家带来欢乐。没有一颗心会因为追求梦想而受伤,当你真心想要某样东西时,整个宇宙都会联合起来帮你完成。青年时准备好材料,想造一座通向月亮的 庙宇。活到中年,终于决定搭一个棚。一个人有钱没钱不一定,但如果这个人没有了梦想,这个人穷定了。梦想无论怎样模糊,总潜伏在我们心底,使我们的心境永远 为事实。如果失去梦想,人类将会怎样?不要怀有渺小的梦想,它们无法打动人心。最初所拥有的只是梦想,以及毫无根据的自信而已。但是,所有的一切就从这里出 幸福,有时梦想破灭也是一种幸福。人生最苦痛的是梦醒了无路可走。做梦的人是幸福的;倘没有看出可以走的路,最要紧的是不要去惊醒他。在每一个想你的日子里 却更难。想你,已成为我的习惯。努力向上吧,星星就躲藏在你的灵魂深处;做一个悠远的梦吧,每个梦想都会超越你的目标。要想成就伟业,除了梦想,必须行动。 排,实际上人们每天在安排着自己的一切活动家都是梦想家。悲观的人,先被自己打败,然后才被生活打败;乐观的人,先战胜自己,然后才战胜生活。梦想一旦被付 是人生最快乐的时光,但这种快乐往往完全是因为它充满着希望,而不是因为得到了什么或逃避了什么。你的生活深度取决于你对年幼者的呵护,对年长者的同情,对 强者的包容。因为生命中总有一天你会发现其中每一个角色你都扮演过。事实上是,哪个男孩女孩没有做过上天入地、移山倒海的梦啊,只不过在生活面前,很多人慢 以他们沦落为失去梦想的人;而有些人,无论生活多么艰难,从来没有放弃��
高二化学选修3离子晶体课件
2021/3/29
22
三、决定离子晶体结构的因素
(1)几何因素
晶体中正负离子的半径比
(2)电荷因素
晶体中正负离子的电荷比
(3)键性因素
离子键的纯粹因素
2021/3/29
23
1、几何因素
配位数与 r +/ r- 之比相关: 0.225 —— 0.414 4 配位 0.414 —— 0.732 6 配位 0.732 —— 1.000 8 配位
元素(如F、Cl、Br、O等,主要是第ⅥA族和第
ⅦA族元素)相互结合时多形成离子键。
铯离子 氯离子
2021/3/29
氯离子位于顶点,铯 离子位于体心。
16
CsCl晶体中离子的配位数
板书Leabharlann (1)每个晶胞含铯离子、 氯离子的个数?
1个Cs+ 1个Cl-
(2)在氯化铯晶体中,每 个Cs+周围与之最接近且距离 相等的Cl-共有 8 ;
(3)在每个Cl-周围距离相等且最 近的Cs+共有 8 ;
第四节 离子晶体
2021/3/29
1
知识回顾:离子键
1、 使阴、阳离子结合成离子称化为合物离的子静键电作。用
2、成键的微粒: 阴、阳离子 3、成键的本质: 阴阳离子间的静电作用
4、成键的条件: 活泼金属元素的原子和活 泼的非金属元素的原子
形成条件:一般电负性差值大于1.7
2021/3/29
4
5.常见的离子化合物 思考
2021/3/29
31
规律总结 1.四种晶体的结构性质比较
晶体结构 离子晶体 分子晶体 原子晶体 金属晶体
结 构成微粒 阴阳离子 分子
原子 阳离子、电子
人教版 高二化学 选修3 第三章 3.4《离子晶体》课件(共31张PPT)

差别较大
差别较大
无(硅为半导体) 无
导体
实例
金刚石、二氧化硅、 晶体硅、碳化硅
Ar、S等
Au、Fe、Cu、钢 铁等
氯化钠晶体
粉末状氯化钠晶体
3.4离子晶体
氯化钠的形成过程:
2Na + Cl2 == 2NaCl
Na
+11
+17
Cl
Na+
+11
+17
Cl-
Na+ Cl-
一、离子晶体
1、定义:由阳离子和阴离子通过离 子键结合而成的晶体。
2x+3(1-x)=2/0.97 x=91/97
n(Ni3+): n(Ni2+)=(1-91/97)∶91/97=6∶91
解 法 二 : 因 为 中 Nio.97O 中 既 有 +2 价 的 离 子
又有+3价的镍离子,所以可写成xNiO·yNi2O3 的复合形式,该形式中很容易看出镍离子的总 和为x+2y,氧离子的总和为x+3y,因此可列方 程如下:
各类型离子晶体晶胞的比较
晶体 晶胞 类型 类型
晶胞结构 示意图
距离最近 每个晶 配位数 且相等的 胞含有
相同离子 离子数
实例
NaCl 型
AB CsCl 型
Na+:6 Na+:12 Na+:4 Cl-: 6 Cl-: 12 Cl-: 4
Cs+:8 Cs+:6 Cs+:1 Cl-: 8 Cl-: 6 Cl-:1
知识回顾:三种晶体类型与性质的比较
晶体类型
概念
作用力
构成微粒 熔沸点
物 理 硬度 性 质 导电性
差别较大
无(硅为半导体) 无
导体
实例
金刚石、二氧化硅、 晶体硅、碳化硅
Ar、S等
Au、Fe、Cu、钢 铁等
氯化钠晶体
粉末状氯化钠晶体
3.4离子晶体
氯化钠的形成过程:
2Na + Cl2 == 2NaCl
Na
+11
+17
Cl
Na+
+11
+17
Cl-
Na+ Cl-
一、离子晶体
1、定义:由阳离子和阴离子通过离 子键结合而成的晶体。
2x+3(1-x)=2/0.97 x=91/97
n(Ni3+): n(Ni2+)=(1-91/97)∶91/97=6∶91
解 法 二 : 因 为 中 Nio.97O 中 既 有 +2 价 的 离 子
又有+3价的镍离子,所以可写成xNiO·yNi2O3 的复合形式,该形式中很容易看出镍离子的总 和为x+2y,氧离子的总和为x+3y,因此可列方 程如下:
各类型离子晶体晶胞的比较
晶体 晶胞 类型 类型
晶胞结构 示意图
距离最近 每个晶 配位数 且相等的 胞含有
相同离子 离子数
实例
NaCl 型
AB CsCl 型
Na+:6 Na+:12 Na+:4 Cl-: 6 Cl-: 12 Cl-: 4
Cs+:8 Cs+:6 Cs+:1 Cl-: 8 Cl-: 6 Cl-:1
知识回顾:三种晶体类型与性质的比较
晶体类型
概念
作用力
构成微粒 熔沸点
物 理 硬度 性 质 导电性
《离子晶体》高二上册化学选修三PPT课件

(2)在氯化铯晶体中,每个Cs+周围与之最接近且距离相等的Cl-共有 ;这几 个Cl-在空间构成的几何构型为 。
(3)在每个Cl-周围距离相等且最近的Cs+共有 ;这几个Cs+ 在空间构成的几何构型
。
(3)CaF2型晶胞
1、一个CaF2晶胞中含: 4个Ca2+和8个F¯
2、Ca2+的配位数: 8
F-的配位数: 4
3.下列物质中,化学式能准确表示该物质分子组成的是( C )
A.NH4Cl B.SiO2 C.P4 D.Na2SO4
问题反思——化学式能否表示分子,关键能判断该物质是否分子晶体
4:下列热化学方程式中,能直接表示出氯化钠晶格能的是___B___
A、 Na (s) + 1/2Cl2 (g) = NaCl(s); △H
△H =△H1 +△H2+△H3 +△H4 +△H5
高中生物选修三
谢谢观看
晶体机构与性质
CRYSTAL STRUCTURE AND PROPERTIES
老师:
授课时间:20XX
交流与讨论
NaCl CsCl
熔点℃ 801 645
沸点℃ 1413 1290
为什么NaCl的熔沸点比CsCl高?
结论: 对于组成和结构相似的物质,阴、阳离子半径越小,离子键越强,
熔沸点较高,晶体越稳定。 离子键的强弱在一定程度上可以用离子晶体的晶格能来衡量。
(二)离子晶体的晶格能
1.概念:气态离子形成1摩尔离子晶体释放的能量,通常取正值。或指拆开1mol离子晶 体使之形成气态阴离子和气态阳离子所吸收的能量 2.影响晶格能大小因素 离子晶体中阴阳离子半径越小,所带电荷越多,离子键越强,晶格能越大 3.晶格能的作用: (1)晶格能越大,离子晶体越稳定,离子晶体的熔沸点越高,硬度越大。 (2)岩浆晶出规则与晶格能的关系
化学:3.4《离子晶体》(新人教版选修3)ppt课件
巩固练习:P82 习题
编辑版pppt
17
感谢亲观看此幻灯片,此课件部分内容来源于网络, 如有侵权请及时联系我们删除,谢谢配合!
18
离子晶体
编辑版pppt
1
材料:
思考:
为什么氯化钠的性质与干冰、 金刚石的不同?
编辑版pppt
2
第四节、离子晶体
一、离子晶体
1、定义:由阳离子和阴离子通过离 子键结合而成的晶体。
2、构成粒子:阴、阳离子 3、相互作用力:离子键(静电作用)
编辑版pppt
3
4、离子晶体的结构特征:
(1)、离子键没有饱和性和方向性,在晶体 中阴阳离子尽可能采取最密堆积
3、晶格能对离子晶体性质的影响:
晶格能越大
(1)形成的离子晶体越稳定;(离子键越强)
(2)熔点越高;
(3)硬度越大。
编辑版pppt
15
小结:⑴一般而言,阴阳离子半径越小,所 带电荷越多,离子键越强,晶体熔沸点越高, 硬度越大
⑵晶体熔沸点的一般规律:
原子晶体>离子晶体>分子晶体
编辑版pppt
16
科学视野 岩浆出晶规则与晶格能
3°与铯离子等距离且最近的铯离 子、氯离子各有几个?
铯离子:6个;氯离子:8个
编辑版pppt
(配位数)
7
(3)CaF2型晶胞
①Ca2+的配位数:8 ②F-的配位数: 4 ③一个CaF2晶胞中 平均含: 4个Ca2+和8个F-
编辑版pppt
返回
8
(4)ZnS型晶胞
1°一个ZnS晶胞中含: 4个阳离子和4个阴离子
2°阳离子的配位数: 4 阴离子的配位数: 4
编辑版pppt
编辑版pppt
17
感谢亲观看此幻灯片,此课件部分内容来源于网络, 如有侵权请及时联系我们删除,谢谢配合!
18
离子晶体
编辑版pppt
1
材料:
思考:
为什么氯化钠的性质与干冰、 金刚石的不同?
编辑版pppt
2
第四节、离子晶体
一、离子晶体
1、定义:由阳离子和阴离子通过离 子键结合而成的晶体。
2、构成粒子:阴、阳离子 3、相互作用力:离子键(静电作用)
编辑版pppt
3
4、离子晶体的结构特征:
(1)、离子键没有饱和性和方向性,在晶体 中阴阳离子尽可能采取最密堆积
3、晶格能对离子晶体性质的影响:
晶格能越大
(1)形成的离子晶体越稳定;(离子键越强)
(2)熔点越高;
(3)硬度越大。
编辑版pppt
15
小结:⑴一般而言,阴阳离子半径越小,所 带电荷越多,离子键越强,晶体熔沸点越高, 硬度越大
⑵晶体熔沸点的一般规律:
原子晶体>离子晶体>分子晶体
编辑版pppt
16
科学视野 岩浆出晶规则与晶格能
3°与铯离子等距离且最近的铯离 子、氯离子各有几个?
铯离子:6个;氯离子:8个
编辑版pppt
(配位数)
7
(3)CaF2型晶胞
①Ca2+的配位数:8 ②F-的配位数: 4 ③一个CaF2晶胞中 平均含: 4个Ca2+和8个F-
编辑版pppt
返回
8
(4)ZnS型晶胞
1°一个ZnS晶胞中含: 4个阳离子和4个阴离子
2°阳离子的配位数: 4 阴离子的配位数: 4
编辑版pppt
人教版化学选修三第三节离子晶体PPT课件

人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
科学探究: 人教版化学选修三第三章第三节离子晶体(共52张PPT)
NaCl和CsCl的结构特点:
配位数:
一个离子周围最邻近的异电性离子的数目!
氯化钠晶体中,阴阳离 子的个数比是多少?
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
各种离子晶体:
【复习回忆】:
下列物质中哪些是离子化合物?哪些是 只含离子键的离子化合物? Na2O NH4Cl O2 Na2SO4 NaCl CsCl
C离a子F2化合物:
Na2O NH4Cl Na2SO4 NaCl CsCl CaF2
只含离子键的离子化合物:
Na2O NaCl CsCl CaF2
熔点:
3.活泼金属氧化物、过氧化物、
碳化物(CaC2)及氢化物(NaH)氮 化物(Mg3N2)等
一般300℃ ~ 1000℃之间
导电性:固态时不导电,而在熔融状态
和水溶液中都能导电。
返
回
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
考考你: 人教版化学选修三第三章第三节离子晶体(共52张PPT)
Cl-
Na+:1+1/4×12=4
Cl-:1/8×8+1/2×6=4
属于AB型晶体
Na+
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
NaCl 的晶体结构模型
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
---Cl- --- Na+
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
7.决定晶体结构的因素: (1).几何因素,即晶体中阴阳离子的半径 比;
科学探究: 人教版化学选修三第三章第三节离子晶体(共52张PPT)
NaCl和CsCl的结构特点:
配位数:
一个离子周围最邻近的异电性离子的数目!
氯化钠晶体中,阴阳离 子的个数比是多少?
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
各种离子晶体:
【复习回忆】:
下列物质中哪些是离子化合物?哪些是 只含离子键的离子化合物? Na2O NH4Cl O2 Na2SO4 NaCl CsCl
C离a子F2化合物:
Na2O NH4Cl Na2SO4 NaCl CsCl CaF2
只含离子键的离子化合物:
Na2O NaCl CsCl CaF2
熔点:
3.活泼金属氧化物、过氧化物、
碳化物(CaC2)及氢化物(NaH)氮 化物(Mg3N2)等
一般300℃ ~ 1000℃之间
导电性:固态时不导电,而在熔融状态
和水溶液中都能导电。
返
回
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
考考你: 人教版化学选修三第三章第三节离子晶体(共52张PPT)
Cl-
Na+:1+1/4×12=4
Cl-:1/8×8+1/2×6=4
属于AB型晶体
Na+
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
NaCl 的晶体结构模型
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
---Cl- --- Na+
人教版化学选修三第三章第三节离子 晶体(共 52张PP T)
7.决定晶体结构的因素: (1).几何因素,即晶体中阴阳离子的半径 比;
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
板书
6. 离子晶体物理性质的特点:
(1) 熔沸点 较高 , 难挥发难压缩。 离子电荷越多,核间距离越小,熔沸点升高。
(2) 硬度 较大 。
(3) 水溶性 一般易溶于水,而难溶于非极性溶剂。
(4) 导电性 固态不导电,水溶液20或21 者熔融状态下能导电。
二、典型的离子晶胞:
2021
NaCl的晶体结构:
• 你认为是什么因素决定了离子晶体中离子 的配位数?根据表3—5、表3—6分析影 响离子晶体中离子配位数的因素。
配位数
4
6
8
半径比 0.2~0.4 0.4~0.7 0.7~1.0
空间构型 ZnS NaCl CsCl
2021
三、决定离子晶体结构的因素
(1)几何因素
晶体中正负离子的半径比
(2)电荷因素
第四节 离子晶体
2021
知识回顾:离子键
1、 使阴、阳离子结合成离子称化为合物离的子静键电作。用
2、成键的微粒:阴、阳离子 3、成键的本质:阴阳离子间的静电作用 4、成键的条件:活泼金属元素的原子和活
泼的非金属元素的原子
形成条件:一般电负性差值大于1.7 2021
5.常见的离子化合物 思考
哪些物质中含有离子键?
6:6 2021
NaCl晶体中离子的配位数
3
1 5
6 2
3
6
1
2
5
4
4
这几个Na+在空间 构成的几何构型 为 正八面体 。
2021
每个Cl- 周围 与之最接近且 距离相等的Na+ 共有 6 个。
二、典型的离子晶体: 1.NaCl:
板书
①与Na+等距 离且最近Cl-
有 6 个,
即Na+的配位
数6。
板书
1、定义: 由阳离子和阴离子通过离子键 结合而成的晶体。
2、成键粒子: 阴、阳离子
3、相互作用力: 离子键
4. 配位数 (C.N.) 离子周围最邻近的异电性离子的数目
5、常见的离子晶体:强碱、活泼金属氧化物、 金2021属氢化物、大部分的盐
阅读课本P79最后一段(即科学 视野之前的一段),结合氯化钠晶体 的结构,你认为离子晶体物理性质有 何特点?
2021
离子
Na+
离子半径(pm) 95
NaCl型
CsCl型
Cs+
Cl-
169
181
r+ r- = 0.52
r+ r- = 0.93
2021
2、电荷因素
由正负离子的电荷比影响 离子晶体的配位数的因素, 称为电荷因素。
CaF2的晶胞
例:CaF2的晶体中,Ca2+ 和F-的个数之比_1_:_2_,电
晶体中正负离子的电荷比
(3)键性因素
离子键的纯粹因素
2021
1、几何因素
配位数与 r +/ r- 之比相关: 0.225 —— 0.414 4 配位 0.414 —— 0.732 6 配位 0.732 —— 1.000 8 配位
NaCl:95/181=0.525 CsCl:169/181=0.933
球形对称的,它们在空间各个方向上的静电 作用相同,都可以和带不同电荷的离子发生 作用 • 没有饱和性:
在静电作用能达到的范围内,只要空间条 件允许,一个离子可以多个离子发生作用
2021
重晶石 BaSO4
明矾 KAl(SO4)2·12H2O
Байду номын сангаас
莹石 CaF2
2021 胆矾 CuSO4·5H2O
一、离子晶体
2021
6、影响离子键强弱的因素:
离子半径和 离子电荷 F K Q1Q2 r2
同种类型的离子晶体,通常离子半径 越 、小离子带电荷越 多,离子键就越 。 离强子 键 越 强 , 破 坏 它 所 需 能 量 就 越 。熔点大就越 。 高
2021
7、离子键的特征
• 没有方向性: 阴阳离子是球形对称的,电荷的分布也是
板书
①Ca2+的配位数: 8 ②F-的配位数:4
③一个CaF2晶胞中 平均含:
4个Ca2+和8个F-
(4)Ca2+周围最近且等距离的Ca2+有 12 个, F-……………2021…………F-有 6 个。
Ca
F
晶胞上面心
图示为CaF2晶胞的1/8, 观察点为上左前方
Ca2+配位数是__8___,F-的配位数是 ___4____。
2021
(4)ZnS型晶胞
1°一个ZnS晶胞中含: 4个阳离子和4个阴离子
2°阳离子的配位数:4 阴离子的配位数:4
2021
科学探究:
• 找出NaCl、CsCl两种离子晶体中阳离子和 阴离子的配位数,它们是否相等?
离子晶体 阴离子的配位数 阳离子的配位数
NaCl
6
6
CsCl
8
8
2021
科学探究:
2021
CsCl晶体中离子的配位数
板书
(1)每个晶胞含铯离子、 氯离子的个数?
1个Cs+ 1个Cl-
(2)在氯化铯晶体中,每 个Cs+周围与之最接近且距离 相等的Cl-共有 8 ;
(3)在每个Cl-周围距离相等且最 近的Cs+共有 8 ;
(4)与Cs+ 最近且等距离的Cs+有6个
2021
(3)CaF2型晶胞
离子键的强弱在一定程度上可以 用离子晶体的晶格能来衡量。
2021
四、离子晶体的晶格能
1.概念:气态离子形成1摩尔离子晶体 释放的能量,通常取正值。
2021
2.表示:符号为U 单位是KJ/mol ,取正值
3、影响晶格能大小因素 离子晶体中阴阳离子半径越小,所带电荷越多, 离子键越强,晶格能越大
②与Cl-等距离且
最近Na+ 有 6
个,即Cl-的配位
数为 6 。
③与Cl-等距离且最近Cl-有 12 个
④与Na+ 等距离且最近Na+ 有 12 个 2021
CsCl晶体的结构
2021
(2)氯化铯晶体
氯化铯晶体中 氯离子和铯离 子分别处于晶 胞的什么位置?
铯离子 氯离子
氯离子位于顶点, 铯离子位于体心。
荷数之比_2__:1__,Ca2+配位 数是__8___,F-的配位数是
____4___。
2021
NaCl CsCl
熔点℃ 801 645
沸点℃ 1413 1290
为什么NaCl的熔沸点比CsCl高?
2021
结论:
对于组成和结构相似的物质, 阴、阳离子半径越小,离子键越强, 熔沸点较高,晶体越稳定。
1、活泼的金属元素(IA、IIA)和活泼的非金 属元素(VIA、VIIA)形成的化合物。
2、活泼的金属元素和酸根离子(或氢氧根离子) 形成的化合物
3、铵根和酸根离子(或活泼非金属元素离子) 形成的盐。
4、从物质类别的角度来说,离子化合物通常包
括__强__碱____、_大___多__数__盐___和__活__泼__金___属__氧__化___物。
