最新2020版高考化学总复习热门考点分解透析:考点2_元素周期律与元素周期表_含解析
2020年全国卷化学高考真题考点分布汇总

2020年全国卷化学高考真题考点分布汇总养成良好的答题习惯,是决定成败的决定性因素之一。
做题前,要认真阅读题目要求、题干和选项,并对答案内容作出合理预测;答题时,切忌跟着感觉走,最好按照题目序号来做,不会的或存在疑问的,要做好标记,要善于发现,找到题目的题眼所在,规范答题,书写工整;答题完毕时,要认真检查,查漏补缺,纠正错误。
总之,在最后的复习阶段,学生们不要加大练习量。
在这个时候,学生要尽快找到适合自己的答题方式,最重要的是以平常心去面对考试。
高考质量提升是一项系统工程,涉及到多个方面、各个维度,关键是要抓住重点、以点带面、全面突破,收到事半功倍的效果。
一、备考策略务必精准高三备考的不同阶段,目标和任务各不相同,就像打仗一样,攻克不同的山头有不同的打法,只有抓住要领,才能打赢主动仗。
一是细化“作战地图”。
从现在到一模考试前,主要任务是过课本、串教材,把基础知识再夯实,为专题复习奠定坚实基础。
各学科组教师要认真学习新课程、新课标、《中国考试评价体系及说明》和近三年高考原题,把高考考点和试题变化点做成“作战地图”,平时考试、练习要对照“作战地图”进行选题,并在“作战地图”上一一标注,确保考点训练无死角、考点覆盖无遗漏。
二是组织集体攻坚。
发挥学科组集体备考的优势,学科组内任务分解、责任到人,每次考试变式训练的预测由组长把关。
学科组坚持“一课一研”、“一考一研”,新老教师步调一致,节奏有序,充分发挥分工协作的集体教研智慧。
三是找准学科增分点。
认真研究本省、本市、本校近年来的高考数据,细化到每一个知识点的得失分情况,找准突破点和增分点,有目的进行专项训练和突破提升。
英语的阅读理解和小作文、语文的古文分析和作文、理科的做题速度、文科的答题思路等,都要制定详细的训练方案和突破的方法策略,在实践中调整提升,打破制约瓶颈,找到质量提升的突破口。
二、课堂教学务必高效。
课堂是教育教学是主阵地。
高三年级教学时间紧,教学任务重,更要切实发挥课堂40分钟的作用。
高考化学二轮复习元素周期律和元素周期表专题总结

高考化学二轮复习元素周期律和元素周期
表专题总结
1.元素周期表的结构
掌握元素周期表的结构中各族的排列顺序,结合惰性气体的原子序数,我们可以推断任意一种元素在周期表中的位置。
记住各周期元素数目,我们可以快速确定惰性气体的原子序数。
各周期元素数目依次为2、8、8、18、18、32、32(如果第七周期排满),则惰性气体原子序数依次为2、2+8=10、10+8=18、18+18=36、36+18=54、54+32=86、86+32=108。
2.元素周期律
3.同周期、同主族元素性质的递变规律
4.简单微粒半径的比较方法
5.元素金属性和非金属性强弱的判断
1。
高考化学复习考点知识专题讲解20 元素周期表、元素周期律

高考化学复习考点知识专题讲解专题二十、元素周期表、元素周期律考点知识本高考化学复习考点知识专题讲解专题重要知识有元素周期表的结构、核素、同位素的概念核外电子排布规律、元素周期律、粒子半径大小比较,主要考查元素周期表的结构及应用,原子结构中各离子数之间的关系,核素、同位素的概念,原子结构中各离子“量”之间的关系,原子核外电子排布规律,判断元素“位、构、性”的关系,元素的金属性、非金属性强弱的比较,粒子半径大小的比较。
预测今年的高考以新元素的发现或元素的新应用为载体,考查同周期、同主族元素性质的递变规律及其与原子结构的关系。
同时,以元素性质及其化合物在工业生产的应用为背景,考查元素周期律的指导作用,如半导体材料、制造农药材料、催化剂和耐高温、耐腐蚀材料等也是高考命题的一大趋势。
重点、难点探源一、元素周期表1、原子序数按照元素在周期表中的由小到大的顺序给元素所编的序号,叫原子序数。
原子序数=核电荷数=核内质子数=核外电子数。
2、元素周期表(1)1869年.俄国化学家门捷列夫制出了第一张元素周期表。
(2)编排原则①横行:把电子层数相同的元素按原子序数递增的顺序从左向右排列的一系列元素,称为周期。
②纵行:把不同横行中最外层电子数相同的元素按电子层数递增的顺序从上到下排列的一系列元素,称为族。
(3)结构①周期(七个横行,七个周期)②族(18个纵行,16个族)二、元素的性质与原子结构1、碱金属元素2、卤族元素三、元素周期律1.定义:元素的性质随着原子序数的递增而呈周期性变化的规律。
2.实质:元素原子核外电子排布的周期性变化。
3.主族元素的变化规律四、元素周期表和元素周期律的应用1、元素的分区:2、元素周期表和元素周期律的应用(1)寻找未知元素。
(2)预测元素的性质①比较同周期、同主族元素的性质。
②预测未知元素的性质。
(3)寻找新材料①在分界线附近的元素中寻找半导体材料;②在过渡元素中寻找优良的催化剂和耐高温、耐腐蚀的合金材料;③在周期表中的氟、氯、硫、磷附近探索研制农药的材料。
2020年高考化学考点 元素周期表

应用元素周期表,以典型金属元素族(碱金属)和典型非金属元素族(卤族元素)为例,运用理论探究和
实验探究的方法,达到掌握元素的性质与原子结构关系的目的。重点掌握元素周期表中同一主族元素的相似性和
递变性。
1.碱金属元素 查阅元素周期表和课本,我们可得到碱金属元素的有关信息如下表:
学性质上表现出的相似性和递变性。 6.知道核素和同位素的涵义。
【要点梳理】 要点一、元素周期表的编排 1.门捷列夫制作第一张元素周期表的依据
(1)将元素按照相对原子质量由小到大依次排列。 (2)将化学性质相似的元素放在一个纵行。 要点诠释: ①门捷列夫(1834—1907,俄国化学家)是元素周期表的创始人。它所制作的元素周期表,揭示了化学元素 间的内在联系,使其构成了一个完整的体系,成为化学发展史上的重要里程碑之一。 ②随着科学发展,人们逐渐认识到门捷列夫给周期表中元素排序的依据存在缺陷,真正科学的依据是元素原 子的核电荷数(即质子数)。
(6)第六周期的镧系元素、第七周期的锕系元素分别包含 15 种元素,为了使元素周期表的结构紧凑,放在 第ⅢB 族;但实际上每种元素都占有元素周期表的一格,所以另外列出,放在元素周期表的下方。
3.周期表与原子结构的关系 (1)周期序数=电子层数 (2)族序数=最外层电子数(对主族而言) (3)原子序数=质子数
4Li+O2 2Li2O
2Na+O2
Na2O2
2Na+2H2O==2NaOH+H2↑ 2K+2H2O==2KOH+H2↑ 实验探究:对比钾、钠与氧气、水的反应
实验内容
现象
与 氧 气 反 钠在空气中燃烧 钠开始熔化成闪亮的小球,着火燃
2020版高考化学一轮复习专题一第六讲元素周期表和元素周期律讲义(含解析).doc

2020版高考化学一轮复习专题一第六讲元素周期表和元素周期律讲义(含解析)元素周期表和元素周期律[江苏考纲要求] 1.了解元素周期表长式的结构周期、族及其应用,掌握同一周期、同一主族元素的原子结构与元素性质的递变规律。
元素周期表2.理解元素主族和零族原子结构、在周期表中的位置、性质及其它们之间的关系。
[教材基础自热身] 1.编排原则2.元素周期表的结构1周期7个横行,7个周期短周期长周期序号 1 2 3 4 5 6 7 元素种数18 32 32 0族元素原子序数36 54 86 118 2族18个纵行,16个族主族列 1 2 13 14 15 16 17 族ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 副族列 3 4 5 6 7 11 12 族ⅢB ⅣB ⅤB ⅥB ⅦB ⅠB ⅡB Ⅷ族第8、9、10,共3个纵行0族第18纵行3元素周期表中元素的分区①分界线如图所示,沿着元素周期表中铝、锗、锑、钋与硼、硅、砷、碲、砹的交界处画一条斜线,即为金属元素区和非金属元素区分界线氢元素除外。
②各区位置分界线左下方为金属元素区,分界线右上方为非金属元素区。
③分界线附近元素的性质既表现金属元素的性质,又表现非金属元素的性质。
[注意] ①从元素周期表的分区中可以看出,非金属性最强的是F,金属性最强的是Cs放射性元素除外。
②金属元素和非金属元素分界线右侧都是非金属,但左侧的并不都是金属元素,如氢元素。
③过渡元素都是金属元素,金属元素只有正价,没有负价。
④处在金属元素和非金属元素分界线上下的元素单质并不一定是半导体,如Al是导体,B硼不导电。
3.元素周期表的三大应用1科学预测为新元素的发现及预测他们的原子结构和性质提供了线索。
2寻找新材料3用于工农业生产对探矿有指导意义的是地球化学元素的分布与它们在元素周期表中的位置关系,研制农药材料等。
[知能深化扫盲点] 提能点一元素周期表中的4个关系1常见的四组等量关系①核电荷数=质子数=原子序数。
2020届全国新高考化学核心考点 元素周期律和元素周期表

2020届全国新高考化学核心考点考点07 元素周期律和元素周期表2020届高考化学复习精准预测1、立德树人,弘扬中华传统文化“要全面贯彻党的教育方针,落实立德树人的根本任务,发展素质教育,推进教育公平,培养德智体美全面发展的社会主义建设者和接班人”。
近年来的高考化学命题,特别重视传统文化对于立德树人的独特功能,弘扬和考查优秀的中国传统文化。
例如,在选择题中通过成语、诗词等考查物理变化和化学变化,通过古代的化学生产工艺考查物质的分离与提纯,通过古文或谚语考查化学知识在生产生活中的应用,这类考查优秀中华传统文化的试题会一直成为今后高考的热点题型。
2、图表信息,考查知识获取能力考试大纲明确指出,考生应能通过对自然界、生产和生活中的化学现象的观察,以及对实验现象、实物、模型的观察,对图形、图表的阅读,获取有关的感性知识和印象,并进行初步加工、吸收和有序存储。
与之对应,高考化学试题中经常出现图表题。
这类试题以图像、统计图、表格、模型等为信息,以化学中的基本概念、基本理论、元素化合物和化学实验等知识为载体,反映一组或多组内容相关的数据或信息,主要考查考生对图表数据的读取、分析与处理能力。
图表可以采用多种形式呈现(无机化工生产流程图、有机推断与合成图、实验流程图等也属于图表),这种考查方式是化学学科素养中“证据推理与模型认知”的具体体现,是高考化学的主流题型。
3、原理综合,考查知识运用能力在高考化学试卷中,有一道化学反应原理的综合题。
随着科学技术的日新月异,化学原理综合题的命制具有广阔的空间。
这道试题通常以新材料或新能源的开发利用、环境保护或对污染的治理、重要物质的制备或性质等问题为切入点,将热化学、电化学、化学反应速率及三大平衡知识融合在一起命题,有时还会涉及图象或图表,题目的设问较多,考查的内容较多,对思维能力的要求较高。
“变化观点与平衡思想”是化学学科素养的重要组成部分,化学反应原理综合题以真实的情景为依托,要求考生能够多角度、动态地分析化学变化,通过化学的视角分析解决实际问题。
高三一轮复习元素周期律元素周期表和化学键知识点总结

(2)化合物
离子化合物: 共价化合物:
(3)用电子式表示形成过程
离子化合物: 共价化合物:
4、极性分子和非极性分子
共价化合物 (空间结构是否对称)
极性分子 例如:CO、NO、H2O、SO2、H2S、NH3、PCl3等
非极性分子 例如:He、Ne、Ar、CO2、CS2、SO3、CH4、CCl4等
二、分子间作用力和氢键
第1周期:2 种元素 第2周期:8 种元素 第3周期:8 种元素
长周期
第4周期:18 种元素 第5周期:18 种元素
第6周期:32 种元素
镧57La – 镥71Lu 共15 种元素称镧系元素
不完全周期
第7周期:现有26种元素
锕89Ac – 铹103Lr 共15 种元素称锕系元素 周期序数 = 电子层数
谢谢观赏
3、具体表现如下
金属性、非金属性的周期性变化
金属性逐渐增强
H
金 属 性 逐 渐 增 强
非
Li
Be
B
C
N
O
F
金 属
性
逐
Mg
Al
Si
P
S
Cl
渐
增
强
K
Ca
Ga
Ge
As
Se
Br
Rb
Sr
In
Sn
Sb
Te
I
Cs
Ba
Tl
Pb
Bi
Po
At
非金属性逐渐增强
4、元素金属性、非金属性强弱的比较 (1)元素金属性、非金属性强弱:取决于元素原子得失电子的难易程度(能力),与得失电子数目无关。
如NaOH 如He、Ne等 如NH4Cl等 如AlCl3 如溶解
2024年高考化学元素周期表知识点总结(2篇)

2024年高考化学元素周期表知识点总结2024年高考化学考试中,元素周期表是一个重要的考点。
掌握元素周期表的基本知识,理解元素周期表的结构和规律,对于解答选择题和计算题等各类试题都至关重要。
下面是2024年高考化学考试的元素周期表知识点总结。
一、元素周期表的分类元素周期表是按照元素的原子序数(即核外电子的数目)和相似性等规律排列的。
在2024年高考中,会考察以下几个方面的分类:1. 元素的主族和副族:元素周期表分为A族(主族)和B族(副族)两大类。
主族元素是周期表的第1A至8A组,副族元素是周期表的1B至8B组。
2. 元素的金属、非金属和类金属:元素周期表中,大多数元素为金属,少数元素为非金属,还有一部分元素是类金属(也称过渡元素)。
3. 元素的周期和组:元素的周期是指横向排列的行数,而元素的组则是指纵向排列的列数。
在元素周期表中,周期从1至7,组从1到18。
二、元素周期表的结构和规律1. 周期表的横向趋势规律:元素周期表的每个周期代表了一层电子壳,周期数越大,电子壳层数越多。
同时,周期表中,原子半径逐渐增大,离原子核越远,电子云也相应扩大。
2. 周期表的纵向趋势规律:元素周期表的每个主族代表了一个电子云中最外层电子的主要能级。
向下排列的元素,原子半径逐渐增大,电子云扩大;而向上排列的元素,原子半径逐渐减小,电子云缩小。
3. 元素周期表的原子半径和电离能规律:元素周期表中,原子半径随着周期数的增加而减小,原子半径随着组数的增加而增大。
电离能则是指原子失去一个电子所需要的能量,电离能随着周期数的增加而增大,电离能随着组数的增加而减小。
4. 元素周期表的化合价规律:元素的化合价一般是由元素的主族和副族决定的。
主族元素的化合价通常等于它们在周期表上的组数;而副族元素的化合价通常等于它们在周期表上的组数减去10。
三、常见元素和其特点以下是一些常见元素和其特点的简要总结:1. 氢(H):最轻的元素,原子量为1。
高中化学一轮复习:元素周期律和元素周期表知识点总结
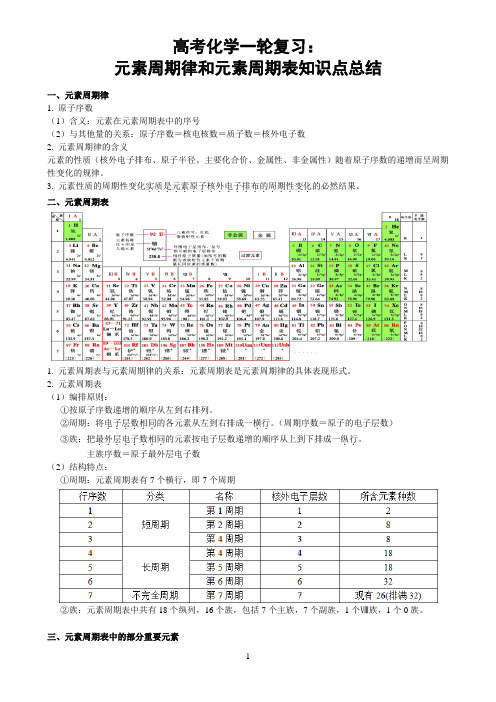
高考化学一轮复习:元素周期律和元素周期表知识点总结一、元素周期律1. 原子序数(1)含义:元素在元素周期表中的序号(2)与其他量的关系:原子序数=核电核数=质子数=核外电子数2. 元素周期律的含义元素的性质(核外电子排布、原子半径、主要化合价、金属性、非金属性)随着原子序数的递增而呈周期性变化的规律。
3. 元素性质的周期性变化实质是元素原子核外电子排布的周期性变化...................的必然结果。
二、元素周期表1. 元素周期表与元素周期律的关系:元素周期表是元素周期律的具体表现形式。
2. 元素周期表(1)编排原则:①按原子序数递增的顺序从左到右排列。
②周期:将电子层数相同..。
(周期序数=原子的电子层数)......的各元素从左到右排成一横行③族:把最外层电子数相同..。
........的元素按电子层数递增的顺序从上到下排成一纵行主族序数=原子最外层电子数(2)结构特点:①周期:元素周期表有7个横行,即7个周期②族:元素周期表中共有18个纵列,16个族,包括7个主族,7个副族,1个Ⅷ族,1个0族。
三、元素周期表中的部分重要元素四、焰色反应1、Na 黄Li 紫红K 浅紫(透过蓝色钴玻璃观察,因为钾里面常混有钠,黄色掩盖了浅紫色)2、Rb 紫Ca 砖红色Sr 洋红Rb 紫Cu 绿Ba 黄绿Co 淡蓝五、微粒半径的大小与比较(1)一看“电子层数”:当电子层数不同时,电子层数越多,半径越大。
如:同一主族元素,电子层数越多,半径越大如:r(Cl)>r(F)、r(O2-)>r(S2-)、r(Na)>r(Na+)。
(2)二看“核电荷数”:当电子层数相同时,核电荷数越大,半径越小。
如:同一周期元素,电子层数相同时核电荷数越大,半径越小。
如r(Na)>r(Cl)、r(O2-)>r(F-)>r(Na+)。
(3)三看“核外电子数”:当电子层数和核电荷数均相同时,核外电子数越多,半径越大。
如:r(Cl-)>r(Cl) 、r(Fe2+)>r(Fe3+)。
高考化学元素周期律和元素周期表(精练)一轮复习(解析版)

元素周期律和元素周期表(精练)完卷时间:50分钟一、选择题(每小题只有一个正确选项,共12*5分)1.(2020年全国统一考试化学试题(新课标Ⅲ))W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物XW3与WZ相遇会产生白烟。
下列叙述正确的是A.非金属性:W> X>Y> Z B.原子半径:Z>Y>X>WC.元素X的含氧酸均为强酸D.Y的氧化物水化物为强碱【答案】D【解析】根据题干信息可知,W、X、Y、Z为原子序数依次增大的短周期元素,化合物XW3与WZ相遇会产生白烟,则WX3为NH3,WZ为HCl,所以W为H元素,X为N元素,Z为Cl元素,又四种元素的核外电子总数满足X+Y=W+Z,则Y的核外电子总数为11,Y为Na元素。
根据上述分析可知,W为H元素,X为N元素,Y 为Na元素,Z为Cl元素,则A.Na为金属元素,非金属性最弱,非金属性Y<Z,A选项错误;B.同周期元素从左至右原子半径依次减小,同主族元素至上而下原子半径依次增大,则原子半径:Na>Cl>N>H,B 选项错误;C.N元素的含氧酸不一定全是强酸,如HNO2为弱酸,C选项错误;D.Y的氧化物水化物为NaOH,属于强碱,D选项正确;答案选D。
2.(北京市2020年普通高中学业水平等级性考试)已知:33As(砷)与P为同族元素。
下列说法不正确的是A.As原子核外最外层有5个电子B.AsH3的电子式是C.热稳定性:AsH3<PH3D.非金属性:As<Cl【答案】B【解析】A.As与P为同族元素,为VA族元素,则其原子核外最外层有5个电子,A说法正确;B.AsH3属于共价化合物,电子式与氨气相似,为,B说法不正确;C.非金属的非金属性越强,其气体氢化物越稳定,非金属性As<P,热稳定性:AsH3<PH3,C说法正确;D.同周期元素,原子序数越小,非金属性越强,非金属性:As<Cl,D说法正确;答案为B。
化学高考必背知识点2020版

化学高考必背知识点2020版近年来,随着高考竞争的加剧,对于高中化学的学习也变得愈发重要。
高考中化学占据了相当大的比重,因此掌握高考必背的知识点成为了考生们的当务之急。
本文将为大家总结2020年高考化学的必背知识点,帮助考生们在备考中更好地掌握重点。
一、化学中的基础知识1. 化学基本概念:原子,元素,化合物,分子,离子,原子价,原子量等。
2. 元素周期表:包括元素的周期性规律、主族元素、副族元素等。
3. 锐化学反应:如原子核衰变、化学键的形成和断裂、氧化还原反应等。
二、化学方程式和化学计算1. 化学方程式的写法:包括物质的化学式、反应物和生成物的量比、反应物和生成物的状态符号等。
2. 化学方程式的计算:包括摩尔比、摩尔质量、反应物转化率等相关概念和计算方法。
3. 氧化还原反应的简化表示:如氧化剂、还原剂、氧化态、还原态等。
三、化学反应的原理与应用1. 杂质对化学反应的影响:包括杂质的种类、性质和浓度对反应速率、平衡等的影响。
2. 化学反应的速率与反应机理:包括反应速率的求解、反应级数、反应速率与温度的关系等。
3. 化学反应的平衡:包括平衡常数、平衡常数与温度的关系、Le Chatelier原理等。
四、物质的组成与结构1. 原子的结构和电子排布:包括原子的亚壳层、轨道、轨道能量等。
2. 共价键的形成和特点:包括简并轨道、杂化轨道的概念及其应用。
3. 有机化合物的基本结构:包括烷烃、烯烃和炔烃的结构、命名规则等。
五、化学反应的能量变化1. 化学能和反应焓的概念:包括化学能、内能、焓变等。
2. 化学反应与能量变化的计算:包括焓变计算、反应焓与反应熵的关系等。
3. 燃烧反应的能量变化:包括燃烧热、热值等燃烧反应的计算和应用。
六、酸碱性质和溶液1. 酸碱指示剂:包括中性、酸性和碱性指示剂的种类和应用。
2. 溶液的准备和化学计算:包括溶液浓度的表示和计算、溶液制备的原理和方法等。
3. 酸碱滴定和滴定曲线:包括滴定的基本原理、滴定剂的选择、滴定点的判断等。
2020年高考化学(人教版)总复习-原子结构、元素周期律和周期表和化学键(含解析)

⨯ 1.设某元素某核素内质子数为 m ,中子数为 n ,则下列叙述中正确的是( )(A ) 不能由此确定该元素的相对原子质量 (B ) 这种元素的相对原子质量为 m+n(C ) 若碳原子质量为Wg ,此原子质量为(m+n )Wg(D ) 核内中子总质量小于质子总质量2.一种微粒的质子数和电子数分别与另一种微粒的质子数和电子数相同,则下列说法中错误的是( ) (A )可能是不同分子 (B )可能是不同离子(C ) 可能是一种分子和一种离子 (D ) 可 能 是 同 位 素3.下列各项中表达正确的是( )A .F -的结构示意图:B .CO 2 的分子模型示意图:C .NaCl 的电子式:Na ∙ClD .N 2 的结构式:N = N:4.短周期元素 X 、Y 能形成 XY 4 化合物,若X 原子序数为m ,Y 原子序数为n ,则m 和n 关系不可能是( )(A )m -13=n (B )n +5=m (C )m +8=n(D )n -11=m5.下列排列顺序正确的是()①热稳定性:H 2O>HF>H 2S ②原子半径:Na>Mg>O③酸性:H 3PO 4>H 2SO 4>HClO 4 ④结合质子能力:OH ->CH 3COO ->Cl - A .①③B .②④C .①④D .②③6. 短周期元素 X 、Y 的原子序数相差 7,下列有关判断错误的是()A .X 和Y 可能处于同一周期B .X 和Y 可能处于相邻周期C .X 和Y 可能处于同一主族 D.X 和Y 可能处于相邻主族7. 已知 1~18 号元素的离子。
a W 3+、b X +、c Y 2-、d Z -都具有相同的电子层结构,则下列关系正确的是( )A .四种元素位于同一周期B .离子的氧化性:a W 3+>b X +C .氢化物的稳定性:H 2Y>HZD .a+3=c-28.已知 A、B、C、D 是中学化学常见的四种不同微粒.它们之间存在如下转化关系:(1)如果 A、B、C、D 均是 10 电子的微粒,请写出:A 的结构式;D 的电子式.(2)如果A 和C 是 18 电子的微粒,B 和D 是 10 电子的微粒,请写出:①A与B 在溶液中反应的离子方程式②根据上述离子方程式,可以判断C 与B 结合质子的能力大小是(用化学式或离子符号表示):> .(3)已知肼(H2N-NH2)和甲胺(CH3-NH2)都是含 18 电子的分子.分析肼和甲胺的结构特点并从中受到启发,写出与其具有相同电子数的有机化合物的结构简式(至少写两个) .1.有两短周期元素 X 和Y,可组成化合物 XY3,当Y 原子序数为m 时,X 原子序数为① m-4 ② m+4 ③ m+8 ④ m-2 ⑤ m+6,其中正确的组合是()(A)①②④ (B)①②⑤ (C)①②③⑤ (D)①②③④⑤2.X、Y、Z 是 3 种短周期元素,其中 X、Y 位于同一主族,Y、Z 处于同一周期。
元素周期表 元素周期律-巅峰冲刺山东省2020年高考化学一轮考点扫描(原卷版)

专题2 元素周期表元素周期律【名师预测】本专题是高考命题的重点内容,主要以元素推断为主体的“位—构—性”关系的考查。
从几种常见的短周期元素出发,设置相关问题情境,考查元素及其化合物的性质、元素在周期表中的位置与性质的关系等知识。
通过图表、文字或相关数据分析等推断同主族、同周期元素性质的递变规律,或以陌生元素在元素周期表中的位置,推断其可能具有的性质等,常以选择题、推断题形式出现。
主要考查方式是以元素化合物知识为载体,结合物质的性质、性质的递变规律、定性推断、规律总结与运用等,对考生的化学素养、知识与能力水平进行考查,而联系元素周期律、元素周期表与元素化合物之间的桥梁就是“位—构—性”的三角关系。
【知识精讲】一、体系构建二、元素周期表的结构1.原子序数:按照元素在周期表中的顺序给元素编号,称之为原子序数,原子序数=核电荷数=质子数=核外电子数。
2.编排原则(1)周期:把电子层数相同的元素,按原子序数递增的顺序,从左至右排成的横行。
(2)族:把最外层电子数相同的元素,按电子层数递增的顺序,从上至下排成的纵行。
3.元素周期表的结构总结元素周期表⎩⎪⎪⎨⎪⎪⎧周期7个⎩⎨⎧短周期⎩⎪⎨⎪⎧ 第一、二、三周期元素种数分别为2、8、8种长周期⎩⎪⎨⎪⎧第四、五、六、七周期元素种数分别为18、18、32、32排满时种族16个⎩⎪⎨⎪⎧主族:由短周期和长周期共同构成,共7个副族:完全由长周期元素构成,共7个第Ⅷ族:第8、9、10共3个纵行0族:第18纵行三、 元素周期律及应用 1.元素周期律2.主族元素的周期性变化规律项目同周期(左→右) 同主族(上→下) 原子结构核电荷数逐渐增大 逐渐增大 电子层数 相同 逐渐增多 原子半径逐渐减小 逐渐增大离子半径 阳离子逐渐减小 阴离子逐渐减小 r (阴离子)>r (阳离子)逐渐增大性质化合价最高正化合价由+1→+7(O 、F 除外)负化合价=-(8-主族序数)相同,最高正化合价=主族序数(O 、F 除外)。
高考化学三轮复习回归教材重难点 05 元素周期律再熟悉 Word版含解析
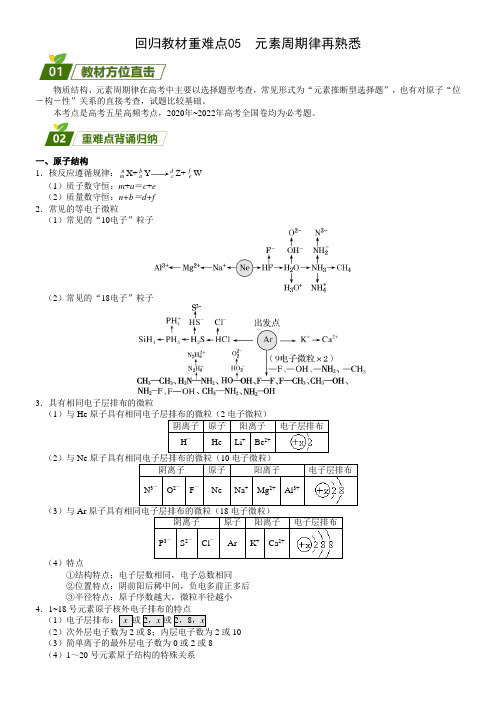
回归教材重难点05 元素周期律再熟悉物质结构、元素周期律在高考中主要以选择题型考查,常见形式为“元素推断型选择题”,也有对原子“位-构-性”关系的直接考查,试题比较基础。
本考点是高考五星高频考点,2020年~2022年高考全国卷均为必考题。
一、原子结构1.核反应遵循规律:nm X+baY dcZ+feW(1)质子数守恒:m+a=c+e(2)质量数守恒:n+b=d+f2.常见的等电子微粒(1)常见的“10电子”粒子(2)常见的“18电子”粒子3.具有相同电子层排布的微粒(1)与He原子具有相同电子层排布的微粒(2电子微粒)阴离子原子阳离子电子层排布H-He Li+Be2+(2)与Ne原子具有相同电子层排布的微粒(10电子微粒)阴离子原子阳离子电子层排布N3-O2-F-Ne Na+Mg2+Al3+(3)与Ar原子具有相同电子层排布的微粒(18电子微粒)阴离子原子阳离子电子层排布P3-S2-Cl-Ar K+Ca2+(4)特点①结构特点:电子层数相同,电子总数相同②位置特点:阴前阳后稀中间,负电多前正多后③半径特点:原子序数越大,微粒半径越小4.1~18号元素原子核外电子排布的特点(1)电子层排布:x 或2,x或2,8,x(22或10(3)简单离子的最外层电子数为0或2或8(4)1~20号元素原子结构的特殊关系特殊关系元素最外层电子数等于次外层电子数的一半Li、Si最外层电子数等于次外层电子数Be、Ar最外层电子数等于次外层电子数的2倍 C最外层电子数等于次外层电子数的3倍O最外层电子数等于次外层电子数的4倍Ne最外层电子数等于电子层数H、Be、Al最外层有1个电子H、Li、Na、K最外层有2个电子He、Be、Mg、Ca内层电子数之和是最外层电子数2倍的元素Li、P电子总数为最外层电子数2倍的元素Be二、元素周期表1.元素周期表的结构2.族序数与列数的关系(1)2、3周期IIA和IIIA相邻,原子序数相差1(2)4、5周期IIA和IIIA之间有副族和VIII族,原子序数相差11(3)6、7周期IIA和IIIA之间有副族和VIII族,还额外多出镧系和锕系,原子序数相差25 3.元素周期表的实际应用4.周期表中的元素(1)元素种类最多的族:ⅢB族,共32种元素(2)元素种类最多的主族:ⅠA族,共7种元素(3)元素种类最多的周期:7周期,共32种元素(4)在短周期中非金属元素多,在周期表中金属元素多。
第29讲元素周期表元素周期律-2024年高考化学一轮复习高频考点精讲(新教材新高考)

价层电子排布 ns1~2
ns2np1~6(除He外) (n-1)d1~9ns1~2(除钯外)
(n-1)d10ns1~2 (n-2)f0~14(n-1)d0~2ns2
(4)元素的金属性、非金属性与元素周期表的分区
①分界线:沿着元素周期表中___铝__、_锗__、_锑__、_钋______与_硼__、_硅__、_砷__、__碲_、__砹____的 交界处画一条虚线,即为金属元素和非金属元素的分界线。
[名师点拨] 微粒半径大小的比较方法
一看电子层数:最外层电子数相同时,电子层数越多,半径越大。 二看核电荷数:当电子层结构相同时,核电荷数越大,半径越小。 三看核外电子数:当电子层数和核电荷数均相同时,核外电子数越多,半径 越大。
2.根据元素周期律比较下列各组性质(用“>”或“<”填空): (1)金属性:K____>____Na____>____Mg; 非金属性:F_____>___O_____>___S。 (2)碱性:Mg(OH)2____<____Ca(OH)2____<____KOH。 (3)酸性:HClO4____>____H2SO4____>____HClO。 (4)热稳定性:CH4___<_____NH3____<____H2O。 (5)还原性:HBr_____>___HCl,I-___<_____S2-。 (6)氧化性:Fe3+____>____Cu2+_____>___Fe2+。
[名师点拨] (1)判断元素非金属性或金属性的强弱,依据的是元素原子在化学反应中得失 电子的难易而不是得失电子的多少。 (2)金属性是指金属气态原子失电子能力的性质,金属活动性是指单质在水溶 液中,金属原子失去电子能力的性质,二者顺序基本一致,仅极少数例外。如金 属性 Pb>Sn,而金属活动性 Sn>Pb。 (3)根据元素氧化物对应水化物的酸碱性的强弱判断元素非金属性或金属性的 强弱时,必须是其最高价氧化物对应的水化物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考对物质结构和元素周期律的考查点主要有原子结构、元素周期表、元素周期律和化学键等。
原子结构和元素周期表是新课标高考中的热点之一,而元素周期律是每年高考中的重点内容,化学键的考查层次较低,多放在对概念的理解上。
原子结构与元素周期表的具体考查形式主要有:(1)考查原子结构中各粒子数之间的关系,核素、同位素的概念;(2)考查元素周期表的结构及应用。
该考点以选择题的考查形式为主,同时也会在非选择题中渗透考查。
元素周期律主要是对元素金属性和非金属性的比较方法、微粒半径大小比较的常用规律、“位一构一性”的综合判断与应用的考查,以选择题的考查形式为主。
高考对化学键的考查主要是围绕电子式书写或正误判断、化学键与物质类别和性质的关系等方面进行,题目基础性较强,一般不独立命题,通常为选择题的一个选项。
由以上分析可知,复习该考点时要抓住原子序数、核电荷数、质子数、中子数、核外电子数及其数量之间的关系;总结元素周期表中元素的电子排布和化合价规律、元素周期表的结构规律;熟练掌握“位一构一性”之间的关系,即熟练掌握原子结构与元素在周期表中的位置关系,根据原子序数会推断元素在周期表中的位置,并能根据元素在周期表中的位置推断元素的性质。
例3 (2016年高考新课标Ⅰ卷)短周期元素W、X、Y、Z的原子序数依次增加。
m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L–1r溶液的pH为2,s通常是难溶于水的混合物。
上述物质的转化关系如图所示。
下列说法正确的是()
A.原子半径的大小W<X<Y B.元素的非金属性Z>X>Y
C.Y的氢化物常温常压下为液态 D.X的最高价氧化物的水化物为强酸
解析:短周期元素W、X、Y、Z的原子序数依次增加。
m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,则Z是氯元素,n是Cl2;0.01 mol·L–1 r溶液的pH为2,说明r 是一元强酸,Cl2与两种元素组成的化合物反应会产生两种化合物,其中一种r是HCl,另一种物质q的水溶液具有漂白性,则说明W是H元素;m是H2O,q是HClO;两种元素组成的化合物p与Cl2光照反应产生HCl,同时产生s,s通常是难溶于水的混合物,根据转化关系图可知p是甲烷,则s可能是CH3Cl、CH2Cl2、CHCl3、CCl4中的几种物质。
因此X是碳元素,Y是氧元素。
A.根据元素周期律的原子半径变化规律:同一周期的元素,原子序数越大原子半径越小,同一主族的元素,原子核外电子层数越多,原子半径越大,则原子半径的大小W<Y<X,错误;B.同周期元素,随着原子序数的增大,自左向右元素的非金属性逐渐增
强,则非金属性Y>X,最高价氧化物对应的水化物酸性越强,相应元素的非金属性越弱,高氯酸的酸性大于碳酸的酸性,则非金属性Z>X,氯元素与氧元素组成的常见化合物如次氯酸等,氯元素显正价,氧元素显负价,由此可判断非金属性Y>Z,因此元素的非金属性Y>Z>X,错误;C.Y元素的氢化物有H2O和H2O2,二者在常温常压下都为液态,正确;D.X的最高价氧化物的水化物是碳酸,该物质是二元弱酸,不是强酸,错误。
答案:C
例4( 2016年高考新课标Ⅱ卷)a、b、c、d为短周期元素,a的原子中只有1个电子,b2-和C+离子的电子层结构相同,d与b同族。
下列叙述错误的是()
A.a与其他三种元素形成的二元化合物中其化合价均为+1
B.b与其他三种元素均可形成至少两种二元化合物
C.c的原子半径是这些元素中最大的
D.d和a形成的化合物的溶液呈弱酸性
【适应练习】
1.(2015山东理综化学)短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。
已知YW的原子充数之和是Z的3倍,下列说法正确的是()
A.原子半径:X<Y<Z B.气态氢化物的稳定性:X>Z
C.Z、W均可与Mg形成离子化合物 D.最高价氧化物对应水化物的酸性:Y>W
2.(2016年高考上海卷)已知W、X、Y、Z为短周期元素,原子序数依次增大。
W、Z同主族,X、Y、Z同周期,其中只有X为金属元素。
下列说法一定正确的是()
A.原子半径:X>Y>Z>W
B.W的含氧酸的酸性比Z的含氧酸的酸性强
C.W的气态氢化物的稳定性小于Y的气态氢化物的稳定性
D.若W与X原子序数差为5,则形成化合物的化学式为X3W2
3.(2014年高考广东卷)甲~辛等元素在周期表中的相对位置如下表。
甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。
下列判断正确的是()
A.金属性:甲>乙>丁 B.原子半径:辛>己>戊
C.丙和庚的原子核外电子数相差13 D.乙的单质在空气中燃烧生成只含离子键的化合物
2.解析:由于原子序数按W、X、Y、Z依次增大,W与Z是同一主族的元素,而X、Y、Z是同一周期的元素,
且只有X是金属元素,则这四种元素在元素周期表中的相对位置为
W
X Y Z。
A.同一周期的元素原子序
数越大,原子半径越小;同一主族的元素,原子核外电子层数越多,原子半径越大。
所以原子半径:X>Y>Z>W,正确;B.W的最高价氧化物对应的水化物的酸性一定比Z的强,但含氧酸的酸性不一定比Z的强,如B的含氧酸可能是HNO2,Z的含氧酸是H3PO4,酸性HNO2< H3PO4,错误;C.元素的非金属性W>Y,所以气态氢化物的稳定性W>Y,错误;D.若W、X原子序数相差5,当W为N,X为Mg时,满足X3W2,当W为O,X为Al 时,满足X2W3,当W为F,X为Si时,满足XW4,错误。
答案:A
3.解析:元素推断题需把握题目中的相关信息,寻找突破口,如本题中的戊的一种单质是自然界硬度最大的物质,就是本题的突破口,根据所学知识判断戊的元素的种类,然后再根据题目中所给的元素周期表的相对位置以及甲和戊的原子序数相差3,判断其他元素,从而进行解答。
分析如下:戊的一种单质是自然界硬度最大的物质,所以戊是C元素;则己、庚分别是Si、Ge元素;甲和戊的原子序数相差3,所以甲是Li 元素,则乙、丙分别是Na、K元素;则丁是Ca元素,辛是Ga元素。
A、根据元素周期律,同主族元素的金属性从上到下逐渐增强,所以金属性:甲<乙<丙,错误;B、电子层数越多,原子半径越大,所以原子半径:辛>己>戊,正确;C、丙的原子序数是19,庚的原子序数是32,所以原子的核外电子数的差值也即原子序
数的差值,丙与庚的原子核外电子数相差13,正确;D、Na在空气中燃烧生成过氧化钠,既含离子键又含共价键,错误。
答案:BC。
