金属与酸反应的图像专题
2020-2021中考化学复习金属与酸反应的图像专项易错题含答案

一、中考初中化学金属与酸反应的图像1.下列图像能正确反应其对应关系的是()A.向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液B.向足量的镁和铁中加入等质量、等质量分数的稀硫酸C.向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液D.某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】B【解析】【详解】A、向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液,pH应该是由小于7逐渐升高,直至等于或大于7,该选项对应关系不正确;B、向足量的镁和铁中加入等质量、等质量分数的稀硫酸,最终生成氢气质量相等,由于镁比铁活泼,反应需要时间短,该选项对应关系正确;C、向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液,氢氧化钠先和硫酸反应生成硫酸钠和水,后和硫酸镁反应生成氢氧化镁沉淀和硫酸钠,该选项对应关系不正确;D、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,硝酸钾不能溶解,溶质质量分数不变,该选项对应关系不正确。
故选B。
2.如图所示四个图像,分别对应四个过程,其中不正确的是 A .向一定量的锌中加入足量的稀盐酸B .向一定量硫酸铜溶液中加入足量的铁C .足量锌、铁中分别加入等质量、等质量分数的稀硫酸D .等质量的锌和铁中分别加入足量等质量分数的稀硫酸【答案】B【解析】【分析】【详解】A 、向一定量的锌中加入足量的稀盐酸,锌完全反应后质量为0,不符合题意;B 、向一定量硫酸铜溶液中加入足量的铁,铁和硫酸铜反应生成硫酸亚铁和铜,44=Fe+CuSO FeSO +Cu ,每56g 固体铁加入置换出64g 铜单质,反应后固体质量增加,溶液的质量减小,反应完后不再减小,符合题意;C 、足量锌、铁中分别加入等质量、等质量分数的稀硫酸,锌的活动性强,在相同的时间内生成的氢气多,稀硫酸的质量相同,完全反应后生成的氢气相同,不符合题意;D 、等质量的锌和铁中分别加入足量等质量分数的稀硫酸,相同的酸反应,生成的氢气质量相同,根据反应方程式:22Zn+2HCl=ZnCl +H ↑22Fe+2HCl=FeCl +H ↑每生成2g 氢气需要锌的质量为65g ,需要铁的质量为56g ,等质量的锌和铁中分别加入足量等质量分数的稀硫酸,完全反应后,铁生成的氢气多,不符合题意。
人教版化学高考复习:金属与酸反应图像PPT

图5
19
人教版化学高考复习:金属与酸反应 图像ppt 【公开 课课件 】
专项训练
2.将质量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应,反应情况如 图5所示。反应结束时,下列可能情况分析正确的是 ( D )
A.铝粉、铁粉和硫酸均有剩余 B.铝粉、铁粉均反应完,硫酸有剩余 C.硫酸、铝粉均反应完,铁粉有剩余 D.硫酸、铁粉均反应完,铝粉有剩余
图2
7
人教版化学高考复习:金属与酸反应 图像ppt 【公开 课课件 】
考点突破
(2)归纳
三个量
原理
结论
金属越活泼,与酸反应速率
反应速率
越快,反应时间越短
Mg>Al>Zn>Fe
产生氢 气质量
生成氢气质量由酸的质量 决定,酸质量相等,生成氢气 质量相等
Al=Mg=Fe=Zn
消耗金 相对原子质量越小,化合价
属质量 越高,消耗金属质量越小 Al<Mg<Fe<Zn
人教版化学高考复习:金属与酸反应 图像ppt 【公开 课课件 】
图1
8
人教版化学高考复习:金属与酸反应 图像ppt 【公开 课课件 】
考点突破
3.金属与盐溶液反应图像 • 金属与盐溶液反应遵循“远距离先置换”的规律。反应结束后,固体中的成
分不与溶液的成分反应,能共存。
16
人教版化学高考复习:金属与酸反应 图像ppt 【公开 课课件 】
专项训练
1.向一定量的铁粉中逐滴加入稀硫酸至过量,图4是反应过程中某种物质的质量
y随加入稀硫酸的质量变化的关系,则y不可能表示
()
A.消耗铁粉的质量 B.生成硫酸亚铁的质量 C.溶液的总质量 D.生成氢气的质量
(完整版)金属与酸反应图像问题

金属与酸反应的图像问题1、将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.(1)写出锌与稀硫酸反应的化学方程式________________________________,该反应的基本类型为__________反应.(2)对于该图象的理解,下列说法正确的是( ) (填序号).①A表示锌和稀硫酸的反应曲线②反应结束后两种金属一定都有剩余③反应结束后稀硫酸都没有剩余④反应结束后消耗两种金属的质量相等2、金属,与我们生活息息相关.(1)在空气中________制品(填“铝”或“铁”)更耐腐蚀.(2)人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度_______(填“大”或“小”).(3)用下列试剂验证铝、铁、铜这三种金属的活动性顺序,能达到目的是( )(填序号).A.硫酸铝溶液B.硫酸亚铁溶液C.硫酸铜溶液(4)将等质量的锌粉和铁粉分别于溶质质量分数相同且等质量的稀硫酸充分反应,产生氢气的质量与时间的关系如图所示.请回答下列问题:①表示铁粉与稀硫酸反应的曲线是:________(填 a 或b)②对于曲线a表示的反应,__________(填化学式)有剩余.3、等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是_________A.M、N两种金属中较活泼的是NB.生成H2的质量M<NC.相对原子质量较大的是ND.D产生的H2速率M>N4、等质量的三种不同的金属X、Y、M,分别和足量的溶质质量分数相同的稀硫酸反应,生成XSO4、YSO4、MSO4,产生氢气的质量与反应时间的关系如图所示。
回答:(1)三种金属的活动顺序由强到弱的是________________。
(2)三种金属的相对原子质量由大到小的是______________。
金属与酸的反应不同横坐标的图像

金属与酸的反应图像一、质量与m 的金属与足量的酸反应(1)质量为m 的铁粉与足量的稀硫酸反应,求产生氢气的质量? 设:产生氢气的质量为X H 2SO 4 + Fe = FeSO 4 + H 2↑ 98 56 152 2 m x256 = xm得:X =562m 答:产生氢气的质量为562m。
(2)质量为m 的锌粉与足量的稀硫酸反应,求产生氢气的质量? 设:产生氢气的质量为X H 2SO 4 + Zn = ZnSO 4 + H 2↑ 98 65 161 2 m x265 = x m 得:X =652m 答:产生氢气的质量为652m。
(3)质量为m 的镁粉与足量的稀硫酸反应,求产生氢气的质量? 设:产生氢气的质量为X H 2SO 4 + Mg = MgSO 4 + H 2↑ 98 24 120 2 m x224 = x m 得:X =242m 答:产生氢气的质量为242m。
(4)质量为m 的铝粉与足量的稀硫酸反应,求产生氢气的质量? 设:产生氢气的质量为X 3H 2SO 4 + 2Al = Al 2(SO 4)3 + 3H 2↑ 294 54 342 6m x654 = x m 得:X =546m =273m 答:产生氢气的质量为273m。
总结:当足量的酸与一定质量m 的金属反应时,产生氢气的质量要通过金属来求。
且产生的氢气的质量为金属的相对原子质量化合价M×,(M 为金属的实际质量)。
在同一坐标图中(横坐标是时间,纵坐标是产生氢气的质量)表示反应情况:单独比较Mg 、Fe 、Zn 三种等质量m 的金属与足量的稀硫酸反应,发现规律: ①金属越活跃,曲线越陡;②金属的相对原子质量越大产生的氢气越少,消耗的酸越少在同一坐标图中(横坐标是稀硫酸质量,纵坐标是产生氢气质量)表示反应情况:求四种金属消耗的硫酸的质量Fe +H 2SO 4 = FeSO 4 + H 2↑ Zn + H 2SO 4= ZnSO 4 + H 2↑ 56 98 65 98 m X m X9856 = x m 得: X =5698m 9865=x m 得:X =6598mMg + H 2SO 4= MgSO 4 + H 2↑ 2Al +3H 2SO 4= Al 2(SO 4)3 + 3H 2↑ 24 98 54 294 m X m X9824=x m 得: X =2498m 29454=x m 得: X =54294m =1898m由此可见等质量的金属消耗的酸的量不一样。
2020人教版化学高考复习:金属与酸(盐)反应图像 (共32张PPT)

• 步骤2:涉及的化学反应方程式
• 先:
;
• 后:
。
11
考点突破
• (1)反应过程中溶液中溶质成分、固体成分变化
• 步骤1:判断金属的活动性顺序为Zn>Cu>Ag。
• 步骤2:涉及的化学反应方程式
• 先:
;
• 后:
。
12
考点突破
步骤3:分析反应过程
反应 顺序
①
②
金属锌 质量
少量 (用完)
少量 (用完)
图4
18
专项训练
2.将质量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应,反应情况如 图5所示。反应结束时,下列可能情况分析正确的是 ( )
A.铝粉、铁粉和硫酸均有剩余 B.铝粉、铁粉均反应完,硫酸有剩余 C.硫酸、铝粉均反应完,铁粉有剩余 D.硫酸、铁粉均反应完,铝粉有剩余
图5
19
专项训练
2.将质量相等的铝粉和铁粉分别与同体积、同浓度的稀硫酸反应,反应情况如 图5所示。反应结束时,下列可能情况分析正确的是 ( D )
32
1.生活在新时代的我们,除了认真学 习,提 高自己 的知识 水平之 外,社 会上的 一些热 点问题 也不容 忽视, 这是我 们应该 思考探 究的。 2.在钓鱼岛问题上,中国政府一直奉 行尽量 和平交 谈,但 不放弃 武力保 护的主 张,表 现出了 对历史 遗留问 题有理 有利有 节的策 略。 3.这种新研制的牙膏香气浓郁,清新 爽口, 去污洁 齿力强 ,而且 不损伤 牙釉质 ,能保 持牙齿 洁白光 亮,深 受消费 者所喜 爱。 4.我们只有在重大集会、节日庆典与 外交场 合穿具 有中国 范儿的 “国服”,才能 有利于 在世界 上树立 充满文 化自信 的中国 形象。 5.人类利用自然资源,其实就是利用 自然地 理系统 中的某 些要素 ,从而 对自然 地理环 境产生 影响。 6.不可更新资源的利用,需要其他资 源的配 合,也 影响其 他环境 要素。
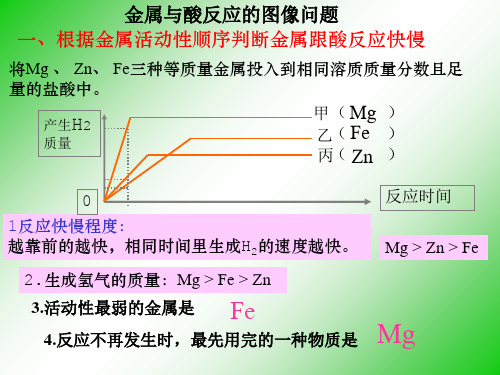
金属与酸反应的图像问题
消耗金属的质量= 金属金相属对化原合子价质量×氢气质量 制取等质量的氢气消耗金属的质量
相对原子质量 ———————-(比值越大),消耗的金属越多。 化合价绝对值
相对原子质量
*制取1克氢气消耗金属的质量= ———————-
金属化合价绝对值
制取1克氢气消耗金属的质量 Mg:12g Al:9g Fe :28g
应生成H2的质量与反应时间的关系如图所示。根据图中
所提供的信息,得出的结论正确的是
( AD )
(已知:A、B、C在生成物中均为+2价)
A.放出H2的质量是A>B>C B.金属活动性顺序是A>B>C
C.反相同质量的Mg、Zn、Fe和足量的稀硫酸反 应,产生氢气的总质量(m)随时间(t)变化的 关系如下图,则下图中a、b、c表示的金属分 别为:a Mg 、 b Fe 、c Zn 。
y1
n
Mg 24
+2HCl=MgCl2+H22↑
y2 Fe 56
+2HCl=FeCl2 +H2n2↑
y3
n
y1= y2= y3=
27n
3
24n 2 56n 2
Zn +2HCl=ZnCl2 +H2↑
65
2
65n
y4
n y4= 2
27n×2 6
y1=
27n 3
y2=
24n 2
y3=
56n 2
65n y4= 2
2、等质量的金属A、B与相同质量的稀硫酸反 应,在反应中A、B均显+2价,产生氢气的质 量随时间变化的情况如右图。则: ⑴金属A、B的活动性:A__>__B__ ⑵金属A、B的相对原子质量_A_>__B_。 ⑶对于曲线A表示的反应,物质_稀__硫__酸__ 有剩余。 ⑷请你写出符合此图像的两种金属:A: _锌____B:__铁____,并分别写出它们与稀硫酸 反应的方程式。
中考化学——金属与酸反应的图像的综合压轴题专题复习附详细答案

中考化学——金属与酸反应的图像的综合压轴题专题复习附详细答案-CAL-FENGHAI.-(YICAI)-Company One1一、中考初中化学金属与酸反应的图像1.向一定量的稀盐酸中,分别加入足量的水、金属铁、氢氧化钙溶液、硝酸银溶液,下列图示正确的是A.B.C.D.【答案】D【解析】【分析】铁和稀盐酸反应生成氯化亚铁和氢气,稀盐酸和氢氧化钙反应生成氯化钙和水,稀盐酸和硝酸银反应生成氯化银和硝酸。
【详解】A、向一定量的稀盐酸中加入足量的水时,酸性减弱,pH升高,但不会变成中性或碱性,pH只会接近7,故A不正确;B、活泼金属和酸接触就会放出氢气,铁和稀盐酸反应生成氯化亚铁和氢气,起点应该从零开始,故B不正确;C、一定量的稀盐酸和氢氧化钙反应生成氯化钙和水,随着反应的进行,溶液的质量增加,反应完全后溶液质量不变,故C不正确;D、稀盐酸和硝酸银反应生成氯化银和硝酸,随着反应的进行,沉淀的质量增加,反应完全,质量不变,故D正确。
故选D。
2.下列图像能正确反应其对应关系的是()A.向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液B.向足量的镁和铁中加入等质量、等质量分数的稀硫酸C.向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液D.某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】B【解析】【详解】A、向一定体积的稀硫酸中逐滴加入足量的氢氧化钠溶液,pH应该是由小于7逐渐升高,直至等于或大于7,该选项对应关系不正确;B、向足量的镁和铁中加入等质量、等质量分数的稀硫酸,最终生成氢气质量相等,由于镁比铁活泼,反应需要时间短,该选项对应关系正确;C、向硫酸镁和硫酸的混合溶液中逐渐加入氢氧化钠溶液,氢氧化钠先和硫酸反应生成硫酸钠和水,后和硫酸镁反应生成氢氧化镁沉淀和硫酸钠,该选项对应关系不正确;D、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,硝酸钾不能溶解,溶质质量分数不变,该选项对应关系不正确。
故选B。
2020-2021中考化学压轴题专题金属与酸反应的图像的经典综合题附详细答案(1)

一、中考初中化学金属与酸反应的图像1.如图表所示4个图象中,能正确反映变化关系的是A .足量镁和铝分别放入等质量、等浓度的稀盐酸中B .镁在空气中加热C .加热一定质量的高锰酸钾固体D .向一定质量的二氧化锰中加入过氧化氢溶液【答案】B【解析】【分析】【详解】A 、根据反应的化学方程式及其质量关系:22Mg+2HCl=24MgCl +3H 72↑,325421961872Al +6HCl =2AlCl +3H 32↑可知 ,足量的镁和铝分别放入等质量、等浓度的稀盐酸中,酸能完全反应,因此反应生成的氢气质量相同,产生相同质量的氢气,消耗镁的质量大于 铝的质量,图像不能正确反映变化关系,不符合题意;B 、镁与空气中的氧气反应生成氧化镁,根据质量守恒定律,反应物质量应该等于生成物质量,因此固体的质量不断增加,图像能正确反映变化关系,符合题意;C 、高锰酸钾受热分解生成了锰酸钾、二氧化锰和氧气,固体的质量减小,锰元素的质量不变,因此固体中锰元素的质量分数应当增加,图像不能正确反映变化关系,不符合题意;D 、向一定质量的二氧化锰中加入过氧化氢溶液,二氧化锰是该反应的催化剂,质量不变,图像不能正确反映变化关系,不符合题意。
故选B 。
2.下列图像能正确反映其对应实验操作的是A .①等质量的镁、铁分别加入到足量的同浓度的稀盐酸中B .②用等质量、等浓度的双氧水分别制取氧气C .③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液D .④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体【答案】C【解析】【分析】【详解】A 、等质量的镁、铁分别加入到足量的同浓度的稀盐酸中,镁与稀盐酸反应:22Mg+2HCl=MgCl +H ↑,铁与稀盐酸反应:22Fe+2HCl=FeCl +H ↑,镁比铁活泼,反应速率快,镁的相对原子质量小,相同质量的镁、铁与足量同浓度的稀盐酸反应,最后,镁生成氢气的质量大,不符合题意;B 、用等质量、等浓度的双氧水分别制取氧气,加催化剂的反应速率快,但是最后生成氧气的质量一样,不符合题意;C 、向一定体积的稀盐酸中逐滴加入氢氧化钠溶液,一开始,pH <7,随着反应的进行,pH 逐渐增大至大于7,符合题意;D 、某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体,由于溶液已经达到饱和,故硝酸钾不再溶解,溶质质量分数不变,不符合题意。
2020人教版化学高考复习-金属与酸(盐)反应图像(共32张PPT)

Al=Mg=Fe=Zn
消耗金 相对原子质量越小,化合价
属质量 越高,消耗金属质量越小 Al<Mg<Fe<Zn
精编优质课PPT2020人教版化学高考复 习:金 属与酸 (盐)反 应图像 (共32张PPT)(获奖课件推荐下载)
图1
8
精编优质课PPT2020人教版化学高考复 习:金 属与酸 (盐)反 应图像 (共32张PPT)(获奖课件推荐下载)
考点突破
步骤3:分析反应过程
反应 顺序
①
②
金属锌 质量
少量 (用完)
少量 (用完)
得到固体 银(部分) 银(全部)
溶液中溶质 AgNO3(部分)和Cu(NO3)2、Zn(NO3)2(生成少量) Cu(NO3)2、Zn(NO3)2(生成量增多)
精编优质课PPT2020人教版化学高考复 习:金 属与酸 (盐)反 应图像 (共32张PPT)(获奖课件推荐下载)
氢,生成氢气,根据质量守恒定律,反应前后元素质量守恒,酸质量相等,生成氢气
质量相等,曲线拐点相平。图2乙中产生相等质量氢气时,消耗金属的质量关系
为
。
精编优质课PPT2020人教版化学高考复 习:金 属与酸 (盐)反 应图像 (共32张PPT)(获奖课件推荐下载)
图2
6
精编优质课PPT2020人教版化学高考复 习:金 属与酸 (盐)反 应图像 (共32张PPT)(获奖课件推荐下载)
精编优质课PPT2020人教版化学高考复习:金属与酸(盐)反应图像 (共32张PPT)(获奖课件推荐下载)
则曲线A对应的金属与稀盐酸反应的化学方程式为Fe+2HCl===FeCl2+H2↑。
若向溶液中插入铝丝,铝丝表面有红色固体析出,
中考化学一轮复习:金属与酸的反应图像问题

中考化学一轮复习专题:金属与酸反应的图像问题金属与酸反应的图像问题是近年来各省市中考试卷中高频率出现,这类试题综合性较强,对学生的思维能力要求较高,涉及到金属的化学活动性、金属的相对原子质量、氢气的质量、溶液的质量、溶质质量分数等知识点。
中考中常考的金属与酸反应的图像问题可以分为两类 :①等量的金属分别和足量的酸反应:即酸过量(足量)②等量的酸分别和足量的金属反应:酸不足(金属过量)在初中化学中常考察的金属只有四个:镁(Mg)、铁(Fe)、锌(Zn)、铝(Al)解题技巧:①首先要判断金属和酸的过量少量情况,一般通过题干中“少量”,“足量”,“过量”等字眼。
而反应中最终产生氢气的多少是由反应物中少量的那个量决定的。
②在讨论金属与酸反应的图像问题时,一定要分清图像中横坐标和纵坐标所表示的具体含义,一般纵坐标是产生氢气的量;而横坐标通常会出现两种情况:(1)时间/s;(2)消耗酸的质量/g 或消耗金属的质量/g.③两种或多种金属与稀酸反应时,反应的快慢(即相同时间内产生氢气的多少)由金属的活动性决定,在温度、金属颗粒大小和稀酸溶液溶质质量分数一定的条件下,金属的活动性越强,生成氢气就越快;生成氢气越快,说明金属的活动性就越强。
④等质量的金属与足量的稀酸反应时,产生氢气的最大量由金属决定,通过化学方程式可以得出:当金属的化合价相同时,对于相同质量的金属,金属的相对原子质量越大,生成的氢气越少;生成的氢气越多,金属的相对原子质量越小。
⑤两种或多种等质量的金属与足量的稀酸反应时,当有部分金属过量时,一定是相对原子质量小的(化合价相等时,这里Al 可以等效成18)金属过量,而相对原子质量大的金属先反应完。
(1)横坐标为反应时间相同质量的Mg,Al,Zn,Fe分别跟足量的等质量等浓度的同种酸反应:①反应速率关系是:Mg>Al>Zn>Fe②最终产生氢气的质量关系是:Al>Mg>Fe>Zn(2)横坐标为酸的质量相同质量的Mg,Al,Zn,Fe分别跟足量的等质量等浓度盐酸反应:金属均完全反应后,最终产生氢气的质量关系是:Al>Mg>Fe>Zn(1)横坐标为反应时间等质量等浓度的同种酸和足量的Mg,Al,Zn,Fe分别充分反应:①产生氢气的反应速率关系:Mg>Al>Zn>Fe②最终产生氢气的质量关系是:Mg=Al=Zn=Fe(2)横坐标为金属的质量等质量等浓度的同种酸和足量的Mg,Al,Zn,Fe分别充分反应:最终产生氢气的质量关系是:Mg=Al=Zn=Fe中考化学一轮复习专题:金属与酸反应的图像问题1.(2020.济宁)在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系如图。
化学干货金属与酸反应的图象问题

化学⼲货⾦属与酸反应的图象问题⾦属与酸溶液反应这⼀知识点的出现,通常是考查同学们对⽣成氢⽓的快慢和多少的掌握情况,往往还会与图象联系在⼀起,因此,图象题的学习是第⼋章的重点。
我们来分析⼀下Mg、Al、Zn、Fe四种⾦属与酸反应的图象问题。
//⾸先,复习⼀下常见⾦属在溶液中的活动性顺序在⾦属活动性顺序⾥,⾦属的位置越靠前,它的活动性就越强。
在⾦属活动性顺序⾥,位于氢前⾯的⾦属能置换出盐酸、稀硫酸中的氢。
在⾦属活动性顺序⾥,位于前⾯的⾦属能把位于后⾯的⾦属从它们化合物的溶液⾥置换出来。
//我们在做图象题时要注意的⼏点内容:⾸先要注意横坐标和纵坐标的物理意义。
其次要注意特殊点的含义,例如起始点、转折点。
最后要注意曲线的趋势的含义。
1等量⾦属和⾜量酸的反应(1)横坐标表⽰时间,纵坐标表⽰⽣成氢⽓的质量图1如图1所⽰,当⾦属与稀盐酸溶液反应时,随着反应的进⾏,⽣成氢⽓的质量越来越多,此时在图象上表现为从O发出的⼀条上升的直线,且⽣成氢⽓越快,这条直线的倾斜程度越⼤。
横坐标表⽰时间,直线的倾斜程度只需看⾦属活动性,倾斜程度即坡陡坡缓,“坡越陡”表⽰⽣成氢⽓越快,“坡越缓”表⽰⽣成氢⽓越慢。
当⾦属与稀酸溶液充分反应后,⽣成氢⽓的质量将不再发⽣变化,此后在图象上表现为⼀条⽔平直线。
⽣成氢⽓越多,⽔平直线在图像上就越⾼。
因此,从图象上看⽣成氢⽓的多少,只需看直线的⾼度,即线⾼线低,“线越⾼”表⽰⽣成的氢⽓越多,“线越低”表⽰⽣成的氢⽓越少。
通过上图,我们可以得出的结论是:产⽣H₂由快到慢的顺序为:Mg>Al>Zn>Fe产⽣H₂由多到少的顺序为:Al>Mg>Fe>Zn//(2)横坐标表⽰⾦属的质量,纵坐标表⽰⽣成氢⽓的质量向⾜量的酸中逐渐加⼊⾦属,所加的⾦属能够完全反应,所以得到的图象为从O发出的射线。
由以上分析可知,等质量的⾦属产⽣的氢⽓由多到少的顺序为Al、Mg、Fe、Zn,因此⽣成氢⽓质量随加⼊⾦属质量的变化图象如图2所⽰。
专题复习 金属与酸、盐溶液反应的图像分析

( B)
6.下列图像中有关量的变化趋势与对应叙述关系正确的是( D )
A.向一定量的铁粉和铜粉的混合物中加入足量稀盐酸 B.向一定量的稀硫酸中加入铁粉至过量 C.向一定量的硫酸铜溶液中不断加入锌粉 D.向铁片(足量)中加入一定量的硫酸铜溶液
7.下列图像与对应叙述不相符的是( B )
A.将等质量的镁片和锌片分别加入溶质质量分数相同的足量稀硫酸中 B.分别向等质量且足量的锌中加入等质量、不同浓度的稀硫酸 C.向等质量、等质量分数的稀硫酸中分别加入铁粉和锌粉至过量 D.铁和硝酸银溶液反应
氢气的质量与反应时间的关系如图。关于甲、乙两金属判断
合理的
(C )
A.铁、镁 C.铁、锌
B.锌、铁 D.锌、镁
4.取一定量打磨后的铝片于某容器中,再逐渐加入稀盐酸。 加入稀盐酸的质量与有关量的变化关系图错误的是 ( B )
5.向一定质量AgNO3和Cu(NO3)2的混合溶液中逐渐加入足量
的锌粒,下列图像不能正确反映对应关系的是
注意 从上述两个图中不能判断金属的活动性强弱!
二、金属与盐溶液的反应图像
图1
图2
金属与盐溶液反应后溶液及固体质量的变化与两种金属的相对原子质量和化学计量数有关。
举例:
固体+ 溶液 —→溶液 + 固体
2Al + 3CuCl2═══2AlCl3+ 3Cu
54
405
267
192
反应后溶液质量减小,变化趋势如图1所示,固体质量增大,变化
等量金属,足量酸 (等金不等氢)
足量金属,等量酸 (等酸等氢)
图像
酸足量,生成氢气的质量由参加反应的金属的质量决定,由化学方
分
反应后金属的化合价
析 程式可知,生成氢气的质量=金属的质量×金属的相对原子质量;
2024年中考化学二轮复习---金属与酸反应的图像分析

1.0~m1阶段,酸过量,产生氢气的质量由金属决定。对于Mg、Fe、Zn三种 金属,生成等质量的氢气,金属的相对原子质量越小,消耗的金属越少(有铝 时,铝的消耗量最少)。 2.金属的质量大于m2之后,金属足量,酸不足,产生氢气的质量由酸决定。
专题精练
1.(2021·日照)现将等质量且形状相同的甲、乙、丙三种金属,分别放入三份 溶质质量分数相同的足量稀硫酸中,产生氢气的质量随反应时间的关系如图 所示(已知甲、乙、丙在生成物中化合价均为+2)。下列说法正确的是( B )
7.(2022·重庆)学会识图能发展科学思维,一小块未打磨的铝片和一定质量的
稀盐酸反应,产生气泡的快慢和反应时间的关系如下图。下列猜想正确的有
( D)
①0~t1阶段,可能是铝表面有层氧化膜
②t1~t2阶段,可能是铝和稀盐酸反应放出热量
③t3时刻,可能是稀盐酸过量
④t3时刻,可能是稀盐酸不足
A.1项
横坐标是时间时,曲线的倾斜程度越大,反应速率越___大_______,金属活动 性越___强_______。等量的金属与足量酸反应生成氢气的质量由金属的质量决
定,计算公式:氢气的质量=参加反应的金属的质量
×
金属在生成盐中的化合价 金属的相对原子质量
。所以当金属元素的化合价相同时,相对原子质
量越小,生成氢气的质量越___大_____。
4.(2023·广西)向三个烧杯中分别放入足量的Mg、Al、Fe粉末,同时加入质 量分数相同的100 g稀盐酸,充分反应。反应的有关图像错误的是( D )
5.(2022·怀化)现有质量相等的X、Y、Z三种金属,分别放入三份溶质质量分 数相等的足量稀硫酸中,X不发生反应,Y、Z在生成物中均显+2价,Y、Z 反应生成氢气的质量与反应时间的关系如图所示,则下列说法正确的是( D )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
A、只有Zn
B、只有Cu
C、有Cu和Na
D、有Cu和Zn
7.如图所示,容器中盛有蓝色硫酸铜溶液,液
面上漂浮这一塑料块,若向溶液中投入一铁片,
则塑料块将会( B )
A.向上浮一些
B.向下沉一些
C.保持原位不动
D.无法确定
2Al+6HCl=2AlCl3+3H2↑
27×2
2×3
x1
m
Mg 24
+2HCl=MgCl2+H2↑ 2
x2
m
Fe 56 x3
+2HCl=FeCl2 +H22↑ m
Zn +2HCl=ZnCl2 +H2↑
65
2
x4
m
x1=
27m 3
x2=
24m 2
56m x3= 2
x4=
65m 2
不同金属与足量的某酸反应制得等量的氢气 时,所消耗的金属质量:Zn>Fe>Mg>Al
●
反应中完全消耗
●
图2
t1
酸等量、金属足量,生成氢气质量相等,
①反应时间越短,说明产生氢气的速度越快, 性质越活泼.活动性:Mg > Al > Zn > Fe 最先被消耗完 ②同一时间,产生氢气的质量: Mg > Al > Zn > Fe
计算:镁、铝、锌、铁与足量的稀盐酸反应制得m克的 氢气时,所消耗的金属质量分别是多少?
36.5×2
2
Zn + 2HCl = ZnCl2 + H2↑
36.5×2
2
36.5×2 36.5×2 36.5×2 36.5×2
酸均因量不足而在反应中完全消耗,H守恒
都生成2g氢气,镁、铝、铁、锌需要HCl的质量相等 如果是质量相等HCl ,产生氢气的质量相等
酸等量、金属足量,生成氢气一样多
●
●
酸均因量不足而在
m
x3
x3=
2m 56
Zn +2HCl=ZnCl2 +H2↑
65 m
2 x4
x4= 26m5
等质量的不同金属与足量的酸反应产生氢气的质量:
Al > Mg > Fe > Zn
等质量的不同金属与足量的酸反应产生氢气的质量: Al > Mg > Fe > Zn
●
等质量的不同金属
●
酸足量
● ●
图1 t1 t2 t3
t4
其他信息:活动性:Mg > Al > Zn > Fe ①反应时间越短,线越陡,说明产生氢气的速度越快,越活泼. ②同一时间,产生氢气的质量: Mg > Al > Zn > Fe
讨论:等质量的金属、足量的酸,当金属元素 化合价相同时,有什么规律?
氢气的质量=
金属元素的化合价×金属的质量 金属的相对原子质量
金属质量比等于金属元素的相对原子质量与其化合价的比。
金属用量的求算公式:
金属的质量=
金属的相对原子质量×氢气的质量 金属元素的化合价
氢气的质量=
金属元素的化合价×金属的质量 金属的相对原子质量
金属的质量=
金属的相对原子质量×氢气的质量 金属元素的化合价
练一练:
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量 的稀盐酸中,反应生成H2的质量与反应时间的关系如图8所示。根据图中所提 供的信息,得出的结论正确的是( )(A、B、C在生成物中均为+2价)
2Al+6HCl=2AlCl3+3H2↑
27×2
2×3
x1
m
Mg 24
+2HCl=MgCl2+H2↑ 2
x2
m
Fe 56 x3
+2HCl=FeCl2 +H22↑ m
Zn +2HCl=ZnCl2 +H2↑
65
2
x4
m
x1=
27m 3
x2=
24m 2
56m x3= 2
x4=
65m 2
不同金属与足量的某酸反应制得等量的氢气时,所消耗的
A.X表示反应所用时间,Y表示生成氢气的质量
B.X表示滴加稀硫酸的质量,Y表示生成氢气的质 量
学习总结
1.等质量的不同金属与足量的酸反应,生成氢气的质 量用价量比
2.足量金属与等量的酸生成氢气质量相等 3.不同金属与足量的酸反应,参加反应的金属的质量
用量价比
6.在CuCl2和NaCl的混合溶液中加入过量的Zn粉,
金属与酸反应 图像专题
计算:(相同质量)m克镁、铝、锌、铁,分别与足量 的稀盐酸反应,产生氢气的质量分别是多少并排序?
2Al+6HCl=2AlCl3+3H2↑
27×2 m
2×3 x1
x1=
3m 27
Mg 24
+2HCl=MgCl2+H22↑
m
x2
x2=
2m 24
Fe 56
+2HCl=FeCl2 +H22↑
产生氢气的质量关系为 相等
。
5.相同质量的Mg、Zn、Fe和足量的稀硫酸反应, 产生氢气的总质量(m)随时间(t)变化的关系 如下图,则下图中a、b、c表示的金属分别为: a Mg 、 b Fe 、c Zn 。
m a
b c
0 t1 t2 t3
t
表示等质量的金属Mg和Al分别
A.放出H2的质量是A>B>C
B.金属活动性顺序是A>B>C
C.反应速率最大的是A
D.相对原子质量是C>B>A
4、相同质量的镁、锌、铁分别与足量的稀硫酸反应,
产生氢气的质量关系为 镁﹥铁﹥锌 ,
足量的镁、锌、铁与相同质量的酸反应,产生氢气的质
量关系为 镁=铁=锌 ,
两份质量相等的锌分别与足量的稀盐酸和稀硫酸反应,
等质量的金属、足量的酸,当金属元素化合价相同 时,金属的相对原子质量越小,产生氢气越多。
讨论:足量的镁、铝、锌、铁分别与等量的 酸反应,产生氢气的质量有什么关系?
2Al + 6HCl = 36.5×6
2AlCl3 + 32H×2↑3
Mg + 2HCl = 36.5×2
MgCl2
+
H2↑ 2
Fe + 2HCl = FeCl2 + H2↑
