第十八章 杂环化合物
第十八章 杂环化合物

O
(3)羟醛缩合反应
CHO + CH3CHO 稀碱 O CH=CHCHO
O
(4)安息香缩合反应
CHO KOH 醇溶液 O O CH C OH O
O
3)糠醛的用途 糠醛是良好的溶剂,常用作精练石油的溶剂,以 溶解含硫物质及环烷烃等。可用于精制松香,脱出色 素,溶解硝酸纤维素等。糠醛广泛用于油漆及树脂工 业。
第十八章
杂环化合物
学习要求
1、掌握杂环化合物的分类和命名; 2、掌握五元杂环化合物的结构和化学性质,了解 它们的制法; 3、掌握糠醛的性质,了解一些含五元杂环化合物 的用途; 4、掌握吡啶的结构和化学性质,了解一些含六元 杂环化合物的用途; 5、了解生物碱的一般性质和提取方法。
第一节
杂环化合物的分类和命名
HCON(CH3)2
DMF
RCOCl
POCl3
N H (1) pKa≈ 17.5 Na 或 K 或浓NaOH N K+ (2)
C6H5N2+XC2H5OH-H2O AcONa
N=N-C 6H5
RX
N R
Hale Waihona Puke 或K+NH2-CO2
加热 加压
N H
RMgX
N H
COOH
N COOH
1 CO2 2 H2O
N MgX
三、六元杂环化合物的命名:
六元杂环:
γ 4 5 6 N 1 3β 2α
5 6 O 1 γ 4 3β 2α
5 6 O 1 O 4 3 2
4 5 6 O 1 3 2 O
吡啶(pyridine)
4 5 6 N 1 3 N2
吡喃(pyran)
4 5 6 N 1 N3 2
杂环化合物

第十八章杂环化合物教学要求1.了解杂环化合物的分类、命名。
2.掌握重要的五元、六元及稠环杂环化合物的结构和性质。
如:呋喃、噻吩、吡咯、喹啉(斯克奥浦合成)。
3.了解嘧啶及嘌呤的结构。
4.了解生物碱的一般概念。
杂环化合物是指组成环的原子中含有除碳以外的原子(杂原子——常见的是N、O、S等)的环状化合物。
杂环化合物不包括极易开环的含杂原子的环状化合物,例如:本章我们只讨论芳香族杂环化合物。
杂环化合物是一大类有机物,占已知有机物的三分之一。
杂环化合物在自然界分布很广、功用很多。
例如,中草药的有效成分生物碱大多是杂环化合物;动植物体内起重要生理作用的血红素、叶绿素、核酸的碱基都是含氮杂环;部分维生素,抗菌素;一些植物色素、植物染料、合成染料都含有杂环。
第一节杂环化合物的分类和命名一、分类二、命名杂环的命名常用音译法,是按外文名词音译成带“口”字旁的同音汉字。
当环上有取代基时,取代基的位次从杂原子算起依次用1,2,3,… (或α,β,γ…)编号。
如杂环上不止一个杂原子时,则从O、S、N顺序依次编号。
编号时杂原子的位次数字之和应最小。
第二节五元杂环化合物含一个杂原子的典型五元杂环化合物是呋喃、噻吩和吡咯。
含两个杂原子的有噻唑、咪唑和吡唑。
本节重点讨论呋喃、噻吩和吡咯,简单介绍一下噻唑、咪唑和吡唑。
一、呋喃、噻吩、吡咯杂环的结构呋喃、噻吩、吡咯在结构上具有共同点,即构成环的五个原子都为sp2杂化,故成环的五个原子处在同一平面,杂原子上的孤对电子参与共轭形成共轭体系,其π电子数符合休克尔规则(π电子数 = 4n+2),所以,它们都具有芳香性。
二、呋喃、噻吩、吡咯的性质1、存在与物理性质2、光谱性质3、化学性质(1)亲电取代反应从结构上分析,五元杂环为∏56共轭体系,电荷密度比苯大,如以苯环上碳原子的电荷密度为标准(作为0),则五元杂环化合物的有效电荷分布为:五元杂环有芳香性,但其芳香性不如苯环,因环上的π电子云密度比苯环大,且分布不匀,它们在亲电取代反应中的速率也比要苯快得多。
杂环化合物

吡咯 —无色液体,b.p. 130~131℃,有弱的苯胺气味 —松木片反应:遇盐酸浸湿的松木片呈红色
二、吡啶的物理性质
▪ 吡啶为具有特殊臭味的无色液体, b.p. 115.5℃, 密度 0.982, 可与水、乙醇、乙醚任意混合
▪ 化学性质稳定 可作溶剂(碱性)
三、五员杂环化合物的化学性质
1.亲电取代反应 反应活性顺序:吡咯>呋喃>噻吩>苯
(1) 卤化 呋喃、噻吩在温和条件下(如溶剂稀释及低温)反应 可得一卤代产物;
Br2, 0℃
O Br O O
Cl2
O
-40℃
+ O Cl Cl O Cl
80%
吡咯卤化常得四卤化物,唯有2-氯吡咯可直接卤化制
得。
Br
Br
Br N Br H
Br2, 0℃
AcONO2
O
-5~-30℃
HNO3/(CH3CO)2O
N H
H O NO2
N NO2 H
AcOPyridine
S
H
H
AcO O NO2
O NO2 35%
混酸
S NO2
(3)磺化
呋喃、噻吩和吡咯常用较温和的磺化试剂-吡 啶与三氧化硫加合物进行反应
SO3, CH2Cl2
N
r. t.
综上所述,五元、六元杂环化合物虽然都具有芳香性,
但其环上的电子云的密度是不同的,其电子云密度由高到 低的顺序是:
S
N
O
N
H
§16-4 杂环化合物的性质
一、呋喃、噻吩、吡咯的物理性质
▪ 呋喃 ▪ —无色液体,b.p. 31.36℃,有氯仿气味 —松木片反应:遇盐酸浸湿松木片呈绿色
第十八章 杂环化合物 Heterocyclic compounds
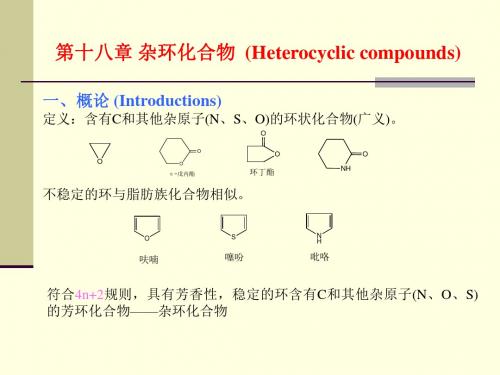
N
异喹啉 isoquinoline
NN
喋啶
第二节 五元杂环化合物
一杂五环
O
Furan
S
thiophene
一、结构特点:
N H
pyrrole
p sp2
O
sp2 NH
p sp2
S
呋喃:π6 5 有一对孤电子参与π-π共轭,有另一对孤对电子参与环上π-π共轭 吡咯:π6 5 N上有一对孤对电子参与环上π-π共轭 噻吩:π 6 5 S上有一对孤对电子参与环上π -π 共轭,另一对孤对电子未共轭
N N
O
吡喃 pyriane
N
嘧啶 pyrimidine
N
吡嗪 pyrozine
N N
哒嗪 pyridazine
按环的形成
单杂环
五杂环
一杂五环 二杂五环
O
S
N
H
Furan thiophene pyrrole
N
N
N N H
吡唑 pyrazole
N H
咪唑 imidazole
S
噻唑 thiazole
一杂六环
Cl2
Cl
Cl
Cl
Cl
S
S
ROOC-C C-COOR
△ (Diels-Alder)
COOR
S
COOR
COOR COOR
[H]
[H]
Ni
H
H
Ni
N H
N H
CHCl3 KOH
N H N H
Cl
Cl
N H
CHCl2
N H
CHO
HN
4.吡咯弱碱性和弱酸性
弱碱性:
有机化学Chap18~21-周环杂环糖脂类氨基酸复习重点资料

D. 油脂易酸败
7. 维生素 A 为动物生长发育所必须,人体缺乏它,会导致夜盲症。它属于( )
A. 单萜
B. 倍半萜
C. 双萜
D. 三萜
8. 下列属于甾族化合物的是( )
有机化学
第4页
有机化学习题集
Chap20、21-杂环、脂类、氨基酸
Chap18-杂环化合物 参考答案
Chap19-杂环化合物 参考答案
A. 葡萄糖
B. 蔗糖
5. α-D-吡喃葡萄糖的 Haworth 式为()
C. 糖原
D. 麦芽糖
6. 下列糖与 HNO3 反应后,产生内消旋体的是()
7. D-吡喃葡萄糖与 1mol 无水乙醇和干燥 HCl 反应得到的产物属于()
A. 醚
B. 酯
C. 缩醛
D. 半缩醛
8. 下列叙述正确的是()
A. 糖类又称为碳水化合物,都符合 Cm(H2O)n 通式
一、选择题 1. D 2. A
二、是非题 1. × 2. √
3. C 4. C 5. A 6. A 3. √ 4. × 5. √
参考答案
7. C 8. B
Chap21 脂类、氨基酸 参考答案
一、选择题 1. C 2. C 3. A 4. B 5. B 6. C 7. C 8. A
有机化学
第5页
3. 由于β-D-葡萄糖的构象为优势构象,所以在葡萄糖水溶液中,其含量大于α-D-
葡萄糖。( )
有机化学
第3页
有机化学习题集
Chap20、21-杂环、脂类、氨基酸
4. 葡萄糖、果糖、甘露糖三者既为同分异构体,又互为差向异构体。( ) 5. β-D-甲基吡喃葡萄糖苷在酸性水溶液中会产生变旋光现象。( )
第十八章 杂环化合物

NH : 供 电 子
2、溶解性: 是与水、油均能混溶的良好溶剂。 烃基R:易溶于有机溶剂
N
孤对电子:与水成氢键,易溶于水。
3、化学性质
(1)N原子的性质 碱性
N
+ HCl
HCl N
盐酸吡啶
含 孤 对 电 子 : 弱 碱
叔胺
N + RX
N R X-
+
(2) 亲电取代:吡啶环看作苯环,N看作NO2。
机化学、有机化学、生理学乃至物理学多学科共同配合,共同努 力的结果。
CH 2OH
维生素 B12
-
H H O O CH 2 HN O=C (CH 2)2 H H2C H C=O H2N N CH 3 CH 3 O P O
H OH
O N N
H CH 3 CH 3 CO-NH 2 CH 2 CH 3 CH 2
芳香性强弱的次序 • 苯 > 噻吩 117 > 吡咯 88 > 呋喃 67 KJ/mol
离域能: 152
取代反应活性的次序 • 吡咯 > 呋喃 > 噻吩 > 苯
如:
+ 4 I2
N H
I I N H
I I
四碘吡咯(伤口消毒剂)
+ H2SO4
S
室 温 S SO3H
α-噻吩磺酸
(CH 3CO) 2O
O
SnCl 2
叶绿素
叶绿素是含于植物的叶和茎中的绿色素,它与蛋白质
结合存在于叶绿体中,是植物进行光合作用所必需的催化 剂,通过叶绿素吸收了太阳能才能进行光合作用。 叶绿素是叶绿素a和叶绿素b的混合物(a:b=3:1),叶 绿素a是蓝色结晶,m.p.150-153℃,其乙醇溶液为蓝绿色, 并有深红色荧光。叶绿素b是深绿色粉末, m.p.120-130℃, 其乙醇溶液为黄色或蓝绿色,并有红色荧光。二者都有旋 光性。
第十八章杂环化合物

5 6
4
3 CH3
7 8
H3C
N2
1
N HO
3,8-二甲基喹啉 8-羟基喹啉
如果环内含有不止一种杂原子时,编号的 先后顺序是 O、S、N、C。4-甲基-5-(-羟乙基)噻唑
第二节 五元杂环化合物
代表化合物:呋喃、噻吩、吡咯。
呋喃(furan) 吡咯(pyrrol)
苯噻吩吡咯呋喃
亲电取代反应(α-位取代): 硝化、磺化、卤化、F-C酰基化、F-C烷基化 活性次序:吡咯>呋喃>噻吩>苯
(1)溴代反应:
(2)硝化反应
(3)磺化反应
噻吩因很容易磺化而溶于 H2SO4,比苯 容易磺化,利用这一性质可以除去苯或 汽油中的噻吩.
(4)酰化反应
2、加成反应
3 吡咯的弱碱性和弱酸性(酸性较醇强较 酚弱)
吡啶能发生亲核取代反应,且主要发 生在 2-位。
+ NaNH2 N
N(CH3)2
NH2 N
2-氨基吡啶
4. 吡啶对氧化剂的稳定性 酸性氧化剂中比苯环稳定:
过氧化物氧化:
5. 还原反应 吡啶环对还原剂比苯环活泼:
嘧啶及其衍生物
嘧啶
有三种嘧啶的衍生物存在于核酸的碱基中, 它们是胞嘧啶、胸腺嘧啶、脲嘧啶
光谱数据
呋喃:δ:α-H 7.42 吡咯:δ:α-H 6.68 噻吩:δ:α-H 7.68 偶极矩:呋喃0.70D
噻吩0.51D 吡咯1.81D
β-H 6.37 β-H 6.22 β-H 7.10
三、五元杂环化合物的化学性质
能发生 SE 反应,且反应主要发生在-位。 其反应活性顺序:
吡咯呋喃噻吩苯 化合物的稳定性顺序:
噻吩(thiophene)
有机化学答案下册

第十二章 羧酸习题解答1、解:(1)3-甲基丁酸 (2)3-(4-氯苯基)丁酸 (3)1,3-苯二酸 (4)9,12-十八碳二烯酸(5)CO 2H(6)HO 2CCO 2HOH(7)CO 2HCl(8)CO 2H2、解:(1) CH 3COOH + CH 3CH 2OHH +CH 3C OOC 2H 5(2) CH 3COOH + PCl 3CH3C O Cl + H 3PO 3(3) CH 3COOH + PCl 5CH 3C O Cl + POCl 3 + HCl(4) CH 3COOH + NH 3CH 3COONH 4(5) CH 3COOHCH 4NaOH,CaO+ Na 2CO 33、解:¼×ËáÒÒËáÒÒÈ©+ CO+ CO -(1)ÒÒ´¼ÒÒÃÑÒÒËá£-£- £« CO(2)乙酸草酸丙二酸-+CO 2+CO 2KMnO 4溶液+褪色-(3)丙二酸丁二酸己二酸CO 2CO 2CO (4)4、解:(1)C 6H 5CH 2MgCl ,C 6H 5CH 2COOH ,C 6H 5CH 2COClNC CH 2Cl CH 2ClOHHOOC CH 2Cl CH 2Cl OH HOOC CH 2CN CH 2CN OH HOOC CH 2COOHCH 2COOHOH(2)5、解:H 2C CH 23C CH 2NaCN3CH 2H 3O +3CH 2COOH(1)CH 3CH 2CH 2H +∆H 3CHC CH 2HBr¹ýÑõ»¯ÎïCH 3CHCH 3BrNaCNCH 3CHCH 3CNH 3O +CH 3CHCH 3COOH(2)CH 3CH 2COOH P + BrCH 3Br OH -CH 3CHCOOHOH (3)CH 3CH 2COOH +(4)CH 3CH 2COOH P 2O5∆(CH 3CH 2CO)2OBrEt 2OMgBr CO 2H 2OCOOH 2C 2H 5(5)6三个碳原子,只能是CH 3CH 2COOH 。
杂环化合物和生物碱-有机化学

溶解1份吡咯、呋喃及噻吩,分别需要17、 35、700份的水。 当五元杂环上连有羟基时,溶解度增大。
如: O
H3C O OH
S
S
OH
(1:35)
(1:20)
(1:700)
(1:16)
3. 杂环化合物的化学性质 (1)、亲电取代反 应
N H O S
HNO3
I2 NaOH
吡咯、呋喃、噻吩 α位取代
I
第四节 稠杂环化合物
稠杂环化合物是指苯环与杂环稠合或杂环与杂环稠合在一起的化 合物。常见的有喹啉、吲哚和嘌呤。
泳衣品牌
3 2 d ★ c
N
a b
N
1
N
★ b 2 a 3
N1
S
N
吡啶并[2,3-d]嘧啶
咪唑并[2,1-b] 噻唑
第二节
五元杂环化合物
五元杂环化合物包括含有1个杂原子的五元杂 环和含2个杂原子的五元杂环。 一、含1个杂原子的五元杂环化合物 1.结构
4 5 1N 3 2
4 5 3 2 4 5 3 2
OH
2.亲电取代反应
Cl2, AlCl 3 100 ℃ Br2, 浮石催化 300 ℃ 气相
Cl
3 氯吡啶
N
Br
3 溴吡啶
N
NO2
N
浓 H2SO4 HgSO4 催化, ℃ 220 混酸 300 ℃
3 硝基吡啶
N
SO3H
吡啶 3 磺酸
N
3.氧化还原反应
(1)氧化反应
COOH N β 吡啶甲酸(烟酸) HNO 3 N COOH N α 吡啶甲酸
由于吡啶环的N上在环外有一孤对电子,故吡啶环上的电荷分布不均。
曾昭琼《有机化学》(第4版)章节题库(杂环化合物)【圣才出品】

(2)
(3)
10 / 26
圣才电子书
十万种考研考证电子书、题库视频学习平 台
(4)
8.完成下列反应,写出主要有机产物。
11 / 26
圣才电子书
十万种考研考证电子书、题库视频学习平 台
答:
12 / 26
圣才电子书
5.为什么五元杂环的芳香性顺序是噻吩>吡咯>呋喃? 答:这三个化合物环上的杂原子电负性顺序为 O>N>S,与其相应的呋喃、吡咯、噻 吩分子中,O、N、S 的未共用电子对向芳环的给电子能力正好相反,S 最强,O 最差,因
8 / 26
圣才电子书
十万种考研考证电子书、题库视频学习平
9 / 26
圣才电子书
十万种考研考证电子书、题库视频学习平 台
7.分离和鉴别: (1)试用化学方法区别 2-氯丙酸和丙酰氯。 (2)试用化学方法区别丙酸乙酯和丙酰胺。 (3)用简单的化学方法分离丁醚和 2-庚酮。 (4)试用化学方法分离喹啉和 8-羟基喹啉。 答:(1)
8.不能用于从水相中萃取呋喃甲醇的试剂是( )。 A.乙醚 B.乙酸乙酯 C.乙醇 D.二氯甲烷 【答案】C
9.下列化合物中酸性最大的是( )。
3 / 26
圣才电子书
【答案】D
十万种考研考证电子书、题库视频学习平 台
二、填空题
1.将下列化合物按亲电取代反应活性高低排列成序:
6 / 26
圣才电子书
十万种考研考证电子书、题库视频学习平
台
4.(1)呋喃甲醛在浓 NaOH 作用下能发生歧化反应生成呋喃甲醇和呋喃甲酸,呋喃
甲醛在使用前需要减压蒸馏进行钝化,请画出减压蒸馏装置图。简述反应结束后,将采取
十八杂环化合物

吡啶用过氧羧酸氧化(或30%的H2O2和CH3COOH作用) 时,生成吡啶N-氧化物或称氧化吡啶:
• 吡啶经催化氢化或用乙醇和钠还原,可得六氢吡啶:
第35页/共43页
湿AgOH,Δ ?
吡啶和哌啶的衍生物
尼古丁
第36页/共43页
二、 喹啉和异喹啉
喹啉的制备
Q. Liu
October 13, 2024
Q. Liu
October 13, 2024
第40页/共43页
罂粟花
三、 嘧啶、嘌呤及其衍生物
(1)嘧啶的衍生物——广泛存在于生物体内。
•是核酸的重要组成部分
Q. Liu
October 13, 2024
第41页/共43页
(2)嘌呤及其衍生物
• 嘌呤的结构
• 嘌呤的衍生物(1)
Q. Liu
October 13, 2024
强的亲核试剂
亲核取代 取代产物
与硝基苯相似:吡啶与强的亲核试剂起亲核取代反 应,主要生成取代产物(齐齐巴宾反应):
• 与2-硝基氯苯相似,2-氯吡啶与碱或氨等亲核试剂 作用,可生成相应的羟基吡啶或氨基吡啶:
第33页/共43页
(C)氧化与还原——吡啶比苯稳定,不易被氧化剂氧 化。吡啶的同系物被氧化时总是侧链先氧化而芳杂环 不破坏,生成相应的吡啶甲酸:
• 命名2:位,其次为位,再次为位:
第4页/共43页
含有两个或以上的相同杂原子的单杂环衍生物,编 号从连有取代基(或氢原子)的那个杂原子开始,顺 序定位,使另一个杂原子的位次保持最小:
第5页/共43页
命名3:根据相应的碳环来命名。把杂环看作相应碳环 中的碳原子被杂原子取代而形成的化合物,命名时在 相应的碳环名称前加上杂原子的名称:
杂环化合物

吡嗪 (pyrazine)
8 7 6 5 9
吡喃 (pyran)
1 2 3 1 6
稠 杂
6 7 8
N
N
3
5
N N
7
N
1
N
2
N1 H
N
2
4
8
10
4
环
喹啉 (quinoline)
异喹啉
(isoquinoline)
吲哚 ( indole )
吖啶 (acridine)
嘌呤 (purine)
2、命名: 采用IUPAC原则,以45个杂环化合 物的俗名为基础作为命名的依据 ,英文 译音,汉字加“口”旁。
苯环与杂环稠合
稠杂环 杂环与杂环稠合
杂环种类 五
4 5 3 4 5 3
重
4 5 1
要
3
杂
4 5
环
N S
1 2 3 4 5 1 3 4 5 1
N N H
2
3
单
元 杂 环
元 杂 环
O
1
2
S
1
2
N H
2
N H
N2
呋喃 (furan)
4 5 3
噻吩 (thilphene)
4 5 3
吡咯 (pyrrole)
NH2 N N N H N
5、鸟嘌呤(guanine) 2-氨基-6-氧嘌呤称为鸟嘌呤(G)
O H N H2N N N H N H2N N N N H OH N
小 结 杂环化合物的分类 杂环化合物的命名 作 业
6 7 8
N-甲基-2-巯基咪唑 5-乙基噻唑 2,4-二羟基嘧
(3)、特定名称的稠杂环,有其固定的编号顺序 5 4
第十八章 杂环化合物

呋喃: 存在于松木焦油中,无色液体,bp.31.36℃ 噻吩: 存在于煤焦油中, 无色液体, bp. 84.16℃ 吡咯: 存在于煤焦油和骨焦油中,无色液体
bp.130~131℃
2、松木片反应——呋喃、吡咯、噻吩的鉴定反应: 呋喃: 其蒸气遇到盐酸浸湿的松木片——呈绿色 吡咯: 其蒸气遇到盐酸浸湿的松木片——呈红色 噻吩: 在浓H2SO4作用下与松木片反应——呈蓝色 (噻吩最好用如下反应鉴定)
乙酰化和烷基化反应:
呋喃和吡咯的烷基化 反应大多生成聚合物
吡咯、呋喃、噻吩的亲电取代反应说明:
取代基主要进入α-位 对试剂及反应条件必须有所选择和控制: 卤代反应: 不需要催化剂,要在较低温度下进行;
硝化反应: 不能用混酸硝化,一般是用乙酰基硝酸酯 (CH3COONO2)作硝化试剂,在低温下进行
• 环上只有一个杂 原子时,有时也把 靠近杂原子的位置 叫位,其次为位 ,再次为位:
特殊编号!
• 含有两个或以上的相同杂原子的单杂环衍生物,编 号从连有取代基(或氢原子)的那个杂原子开始, 顺序定位,使另一个杂原子的位次保持最小:
异噁唑
噁唑
第二节 五元杂环化合物
一、呋喃、噻吩、吡咯杂环的结构: 芳香性:苯 > 噻吩 > 吡咯 > 呋喃
二、呋喃、噻吩、吡咯的性质 松木片反应; 亲电取代反应活性: 吡咯 > 呋喃 > 噻吩 > 苯 取代基主要进入α-位 卤代、硝化、磺化时试剂要求; 加成反应;吡咯的弱碱性和弱酸性; 了解——糠醛、噻唑、咪唑和吲哚、卟啉化合物
返回教学内容
第二节 五元杂环化合物
重点讨论呋喃、噻吩、吡咯 一、呋喃、噻吩、吡咯杂环的结构 :
杂环芳烃讲解

种p-π共轭体系属于π56 的多π电子环系。且X射线衍射测得
呋喃、噻吩、吡咯的键长如下:
0.1421nm 0.1361nm
0.1429nm 0.1371nm
0.1423nm 0.1370nm
O
0.1362nm
N
0.1380nm
S
0.1724nm
与典型的键长数据相比较,可知呋喃、噻吩、吡咯分子中的 C=C比典型的双键长,而碳与杂原子形成的单键缩短,分子中键
> N H O
> S
>
在呋喃、噻吩、吡咯分子中都有大π键,说明它们有一定程 度的不饱和性。因此,在一定条件下能发生加成反应,例如,发 生加氢反应,生成饱和的杂环化合物,同时还能像1,3-丁二烯一 样发生D-A反应等。
(2)呋喃、噻吩、吡咯的性质:呋喃、噻吩、吡咯环系,广泛存在
于各种生物体中,可以从天然物中提取制得,例如从稻草,玉米棒
杂环化合物广泛存在于自然界中。如植物的叶绿素和动物的 血色素分子中;石油,煤焦油中含有含硫、含氮及含氧的杂环化 合物;许多药物如治疟疾的双磷酸伯氢喹,止痛的吗啡,抗结核 的异菸肼。抗癌的喜树碱,抗菌素如青霉素,染料如靛蓝等都是 杂环化合物。此外在工业上用作抽提芳烃,分离丁二烯的环丁砜 和精制润滑油的糠醛以及高分子化学中出现的一些含有杂环结构 耐高温的高聚物如聚苯并噻唑,聚苯并咪唑均属杂环化合物。
等植物茎中制取呋喃衍生物糠醛,糠酸等。工业上分馏煤焦油可得
到噻吩和吡咯,但更常用的方法是人工合成这些杂环化合物。
①物理性质 :呋喃存在于松木焦油中,无色液体,有氯仿的气味, 难溶于水,易溶于乙醇、乙醚等有机溶剂,将它的蒸汽通过被盐酸 浸饱过的松木时呈绿色,此反应叫木片反应,可以用来鉴定呋喃的 存在。
李景宁《有机化学》(第五版)笔记和课后习题(含考研真题)详解-杂环化合物【圣才出品】

(2)物理性质 ①噻唑是无色、有吡啶臭味的液体,沸点 117℃,易与水互溶,有弱碱性。 ②咪唑是无色固体,熔点 90℃,易溶于水。 (3)酸碱性 噻唑具有弱碱性,咪唑同时具有酸碱性,且其碱性较噻唑强。 (4)亲电反应 咪唑环比噻唑环较容易发生亲电取代反应,如卤代、硝化和磺化等。
(2)噻吩的制法 从 C4 馏分制备:丁烷与硫、丁烯与二氧化硫,在高温下反应得噻吩,如:
6 / 34
圣才电子书 十万种考研考证电子书、题库视频学习平台
(3)吡咯的制法 ①呋喃与氨在高温下反应得吡咯,如:
②吡咯还可从乙炔与甲醛经由丁炔二醇合成,如:
5.噻唑和咪唑 (1)定义 ①噻唑是含有一个硫原子和一个氮原子的五元杂环化合物。
2 / 34
圣才电子书 十万种考研考证电子书、题库视频学习平台
吡咯、呋喃和噻吩在 3077~3003cm-1 区域出现 C—H 键伸缩振动吸收峰。 b.N—H 键伸缩振动 含有 N—H 基团的杂环在 3500~3200cm-1 区域出现 N-H 键伸缩振动吸收。 吡咯在非极性溶剂的稀溶液中于近 3495cm-1 处出现一条尖锐的峰,而在浓溶液中则于 近 3400cml-1 处出现一条宽峰,在浓和稀的中间浓度时两种峰都有。 c.环伸缩振动(骨架谱带) 环伸缩振动出现于 1600~1300cml-1 区域。 呋喃、吡咯和噻吩在这一区域里出现 2~4 个峰。 ②1HNMR 在吡咯的 1H NMR 中,α-H 的化学位移(δ值)为 6.68,而β-H 为 6.22,约在 8.0 出现 N —H 键的信号。 (4)亲电取代反应 ①亲电取代活性 a.反应速率 呋喃、吡咯、噻吩的反应速率比苯快得多,主要在于环上的五个原子共有 6 个π电子, 其π电子云密度比苯大。 b.反应活性 吡咯和呋喃比较活泼,与苯胺或苯酚相当,而噻吩则是三者中活性最差的。 ②亲电取代的定位原则 呋喃进行亲电取代反应时,亲电基团进入呋喃环的 2 位(即α位)上,若 2、5(即α及α') 两个位置已有基团存在,则进入 3 位。 ③亲电取代的条件
第18章 杂环化合物

N Pyridine
O Pyran
吡啶
吡喃
六元 环
N N
含两个杂原子:
N
N
N Pyrimidine
N Pyrazine
Pyridazine
哒嗪
嘧啶
吡嗪
N N Quinoline N Isoquinoline N
N N N
稠杂 环
喹啉
异喹啉
N N N H Purine N
蝶啶
吖啶
N H Indole
+E
N
+
E
进攻β 位
N
+
H
+
E H N
+
E H
N
吡啶的亲电取代反应示例 (a )磺化
SO3
H2SO4, HgSO4
N
70% 230 C ,
o
N H
+
(b )硝化
H2SO4, KNO3
NO2 N
N
Fe, C ,22% 330
o
(c )卤化
Br2 N 300 C
o
Br + N
Br
Br
N
吡啶可被催化加氢为六氢吡啶(哌啶)。 吡啶可被催化加氢为六氢吡啶(哌啶)。 六氢吡啶的碱性( =2.7) 六氢吡啶的碱性(pKb=2.7)比一般脂肪族仲 胺略强
单环 含一个杂原子
O Furan N H Pyrrole S Thiophene
呋喃
N
吡咯
N N H Imidazole
噻吩
N S Thiazole
五元环
O Oxazole
噁唑
咪唑
N H Pyrazole N
第十八章 杂环化合物

六. 吲哚
吲哚的亲电取代反应在3位发生:
七、 卟啉化合物 四个吡咯环和四个次甲基(一CH=)交替相联组成的大环叫卟啉 环,含卟啉环的化合物称为卟啉族化合物。
第三节 六元杂环化合物
六元杂环最重要的有吡啶和嘧啶,它们的衍生物广泛存在于自 然界,不少合成药物也含有吡啶环或嘧啶环。 一、吡啶 1.吡啶的来源和制法 氧化法: 工业上从煤 焦油提取甲 基吡啶氧化。
3. 酸碱性
大多数生物碱具碱性反应,能使红色石蕊试纸变蓝。碱性的强弱与分子中 氮原子存在的状态有密切关系,一般是季胺碱>叔胺碱>仲胺碱。若氮原 子呈酰胺状态,则碱性极弱甚至消失,如胡椒碱、秋水仙碱等。有的生物 碱分子具有酚羟基或羧基,因而具酸碱两性,如槟榔次碱 和吗啡等。 生物碱分子中的氮原子有一对未用电子对,对质子有一定的吸引力,一般 能与无机酸或有机酸结合成盐。
为了使提取更完全,也常常对上述方法进行组合如冷浸-超声 波,冷浸-索氏提取,冷浸-热回流提取,因冷浸、冷浸-超声 波提取操作简便,故使用较多,必要时,要对上述方法作比 较,以优选出最佳提取方法。
第五节 改变人行为的药物
一、兴奋剂 以中枢兴奋作用为主,代表物质如尼古丁、可卡因、咖啡因、 冰毒等。 二、致幻剂 代表物质如大麻、氯胺酮等。 三、抑制剂 以中枢抑制作用为主,代表物质如海洛因、吗啡、 γ-羟丁酸等。 四、兼具兴奋和致幻作用,代表物质如摇头丸。
(2)
吡啶环对氧化剂的稳定性
(3)还原反应
吡啶环对还原剂则比苯环活泼。
例如,钠加乙醇使吡啶还原为六氢吡啶,而苯不受还原剂作用。
催化加氢也使吡啶还原为六氢吡啶。
(4) 亲核取代反应 在-上发生,若两个 -被占据,则在-上发生。
二、嘧啶
三. 喹啉
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
本章内容
杂环化合物的分类与命名 五元杂环化合物 六元杂环化合物 生物碱
广义定义:除碳原子外还含有其他原子(N、S、O)的环状化合物。 狭义定义:构成环的原子除碳原子外还有其它原子,并具有芳香结 构的环状有机化合物。 杂原子:组成杂环的原子除碳以外都叫杂原子。
杂环化合物在自然界中分布很广,功用很多。
CH CH OH
H CH C H O H OH CHO
2. 性质和用途 无-氢的醛;具不饱和呋喃杂环:
O
CHO
四. 呋喃、噻吩、吡咯的制法
1. 呋喃的制法 (1)由糠醛经催化脱羰基;
(2)1,4-二酮经五氧化二磷反应(帕尔-诺尔Paal-Knorr合成法)
CH2 C6H5 C O CH2 C CH2COOH O
N H 1H-吡咯
N
2H-吡咯
O
2H-吡喃
O
4H-吡喃
(三)取代杂环化合物的命名 当杂环上连有取代基时,先确定杂环母体的名称和编号,然后将取 代基的名称连同位置编号以词头或词尾形式写在母体名称前或后, 构成取代杂环化合物的名称。
2-氨基咪唑
8-羟基喹啉
COOH
SO3H
O
CHO
N OH
N
2-呋喃甲醛
Penicillin G
维生素B1
青霉素
2.咪唑
含有两个氮原子的五元杂环, 无色固体,熔点90℃,易溶于水,碱 性较噻唑强。它也有微弱的酸性,NH 上的氢原子可被碱金属原子置换而成 盐。
N
N
N H
NHCl-
HCl
N H N H
N
N
NaNH2
N H N
Na+
咪唑环的互变异构 咪唑环有互变异构体,当环上无取代基时, 这一现象不易辨别,当环上有取代基时则很明显。
CH CH2
CH3 N CH CH2 CH3
HO2CCH2CH2
Heme
Sedative( 镇痛药): Phenobarbital(镇静安眠药)
H O H N O N O CH2CH3
Phenobarbital
Antibiotic(抗生素): Penicillin (青霉素)
O C6H5CH2 C NH H O N H H S CH3 CH3 CO2H
嘌呤 Purine
(二)杂环母环的编号规则 杂环母体的编号原则是: 1.含一个杂原子的杂环 含一个杂原子的杂环从杂原子开始编号。 2.含两个或多个杂原子的杂环 含两个或多个杂原子的杂环编号时应使杂原子位次尽可能小, 并按O、S、NH、N的优先顺序决定优先的杂原子,见咪唑、噻唑 的编号。 3.有特定名称的稠杂环的编号有其特定的顺序 如异喹啉、嘌呤的编号。 4.标氢 用其编号加H(大写斜体)表示。例如:
3.喹啉及其衍生物的合成 合成喹啉及其衍生物的常用方法是斯克劳普(Skraup)合成法。 用苯胺(或其它芳胺)、甘油(或α,β不饱和醛酮)、硫酸、硝基苯 (相应于所用芳胺)共热,即可得到喹啉及其衍生物。
NH2 CH2OH CHOH CH2OH NO2 H2SO4 N NH2
反应过程包括以下步骤: (1)甘油在浓硫酸作用下脱水生成丙烯醛;
CH2 OH CH OH CH2OH H2SO4 CH2 CHCHO H2O
(2)苯胺与丙烯醛经麦克尔加成生成β-苯胺基丙醛;
NH2 δ δ CH2 CH Oδ C δ H CHO H N
(3)醛经过烯醇式在酸催化下脱水关环得到二氢喹啉;
H N CHO HO H H N C H OH H N H H2O H N
苯并咪唑 Benzimdazole
咔唑 Carbazole
含一个杂原子的六元杂环
γ
4 5 6 1 3 2
γ β α
5 6 4 3 1 2
γ β α
4 5 6 1 3 2
β α
N
O
O
吡啶 Pyridine 含两个杂原子的六元杂环
43 5 6 1 2N 5 6
2H-吡喃 2H-Pyran
4H-吡喃 4H-Pyran
N H
O
1
O
1
2 Nα
S
1
α
吡唑 Pyrazole
咪唑 Imidazole
噁唑 Oxazole
异噁唑 Isoxazole
噻唑 Thiazole
五元稠杂环
4 5 2 6 7 1 3 5 4 3 5 1 7 2 6 7 4
N
2
3
5 6 7 8 9
4 3 2 1
N H
6
O
N H
1
N H
吲哚 Indole
苯并呋喃 Benzofuran
含一个杂原子的五元杂环
β
4
β
5 1 3 2
β α α
4 5
3
β α α
β
5
β
4 3
α
N H
O
1
2
S
1
2
α
吡咯 Pyrrole
呋喃 Furan
噻吩 Thiophene
含两个杂原子的五元杂环
β
4 3
β α
β
5
4
3 1
Nβ
2
β α α
5
α
4
3
Nβ
2
β α α
5
β
4 3
β α
5
4
3
Nβ
2
5 1
2 Nα
N H
六、吲哚
存在与物理性质
5 6 7
3
N1 H
2
存在于煤焦油中,为白色片状结晶,熔点52.5℃,沸点254 C。
CH2CHCOOH NH2 N H
CH2COOH N
色氨酸
HO N H NH2
β-吲哚乙酸
H3CO N H
H
NHCOCH3
5-HT
褪黑素
取代反应 吲哚的化学性质与吡咯相似,也有松木片反应呈红色,亲 电取代主要发生在3位。
O CHO O NH3 500 o C CH2OH
N
实验室合成法为汉茨施(Hantzsch)合成法:
H C ROOC C C CH3 OH H N H H O
H ROOC
H
C C
COOR
COOR N H
HO H
CH3
H3C
CH3
ROOC
COOR N H CH3
HNO 3/H2SO 4 H3C
2.电子结构及芳香性
Penicillin G
第一节 分类和命名
1 按环的个数分:单环和稠环(单环与芳香环或其它杂环稠并而成)
三 杂环 四 杂环 S O N N S
单杂环
五 杂环 六 杂环
O N
O N H
七 杂环 N H
2 按是否具有芳香性分: 芳香杂环化合物和普通杂环化合物
杂环化合物的命名
(一)有特定名称的杂环
按照英文名称的读音,选用同音汉字加“口”旁组成音译名,其中 “口”代表环的结构。
注意:
硝化反应:不能用硝酸或混酸进行硝化反应,只能用较温和的 非质子性的硝乙酐作为硝化试剂,并且在低温条件下进行反应。 磺化反应:吡咯和呋喃的磺化反应也需要使用比较温和的非质 子性的磺化试剂,常用吡啶三氧化硫作为磺化试剂。 由于噻吩比较稳定,可直接用硫酸进行磺化反应。
4. 加成反应
(1) 呋喃的加成反应
3-吡啶甲酸
8-羟基喹啉-5-磺酸
第二节 五元杂环化合物
含一个杂原子的五元杂环化合物
O Furan 呋喃
N H Pyrrole 吡咯
S Thiophene 噻吩
一、呋喃、噻吩、吡咯杂环的结构
物理方法证明:
吡咯、呋喃和噻吩这三个化合物都是平面型分子。 碳原子与杂原子均以sp2杂化轨道与相邻的原子彼此以σ键构成 五元环,每个原子都有一个未参与杂化的 p轨道与环平面垂直, 碳原子的p轨道中有一个电子,而杂原子的p轨道中有两个电子。 这些p轨道相互侧面垂直重叠形成封闭的大 π键,大π键的π电 子数是6个,符合4n+2规则,因此,这些杂环具有芳香性特征。
P2O5 C6H5 O
CH2COOH
2. 噻吩的制法 (1)煤焦油中提取; (2)1,4-二酮经五硫化二磷反应(帕尔-诺尔Paal-Knorr合成法)
3. 吡咯的制法 (1)呋喃与氨在高温下反应:
Al2O3 o 430 C
+
NH3
O
N H
(2)丁炔二醇与氨在压力下反应:
HOCH2
CH2OH
+
NH3
N
N
尿嘧啶(Uracil)
胞嘧啶(Cytosine)
胸腺嘧啶
嘧啶衍生物广泛存在于动植物中。
H3C HN + N NH2 CH3 + N S OH 2Cl
-
维生素B1
三、喹啉与异喹啉
5 6 7 8 4 3 6 7 8 1 5 4 3
N
1
2
N2
1.结构 2.化学性质
亲电取代反应、亲核取代反应有以下规律: (1)亲电取代反应发生在苯环上,其反应活性比萘低,比吡 啶高,取代基主要进入5位和8位。 (2)亲核取代反应发生在吡啶环上,反应活性比吡啶高。喹 啉取代主要发生在2位上,异喹啉取代主要发生在1位上。
七、卟啉类化合物
NH N
CH3 CH2 CH N CH3 CH3 H N Mg N H N O CO2CH3 H O O CH3 H CH3 H CH2CH3
N HN
CH3
Chlorophyll a
第三节 六元杂环化合物
一、吡啶
1. 来源和制法 吡啶是从煤焦油中分离出来的具有特殊臭味的无色液体,沸点为 115.3℃,比重为0.982,是性能良好的溶剂和脱酸剂。 工业上可从糠醛制备:
