山东省济宁市实验中学2020届高三上学期期中考试化学试卷Word版含答案
2020届高三化学精准培优专练:十六 弱电解质电离平衡及电离平衡常数 Word版含答案

1.影响电离平衡的因素典例1.常温下,在pH =5的CH 3COOH 溶液中存在如下电离平衡:CH 3COOH CH 3COO −+H +,对于该平衡,下列叙述正确的是( )A .加入水时,平衡向右移动,CH 3COOH 电离常数增大B .加入少量CH 3COONa 固体,平衡向右移动C .加入少量NaOH 固体,平衡向右移动,c (H +)减小D .加入少量pH =5的硫酸,溶液中c (H +)增大 2.电离平衡常数的应用典例2.分析下表,下列选项错误的是( )弱酸 CH 3COOH HCN H 2CO 3 电离常数 (25℃)1.8×10-54.9×10-10K a1=4.3×10-7 K a2=5.6×10-11A .CH 3COO -、HCO -3、CN -在溶液中可以大量共存B .向食醋中加入水可使CH 3COOH 的电离平衡向电离方向移动C .相同物质的量浓度的Na 2CO 3和NaCN 溶液,后者pH 较大D .pH =a 的上述3种酸溶液,加水后溶液的pH 仍相同,则醋酸中加入水的体积最小 3.强弱电解质的比较典例3.某温度下,相同体积、相同pH 的氨水和氢氧化钠溶液加水稀释时的pH 变化曲线如图所示,下列判断正确的是( )A .a 点导电能力比b 点强B .b 点的K w 值大于c 点C .与盐酸完全反应时,消耗盐酸体积V a >V c培优点十六 弱电解质电离平衡及电离平衡常数一.弱电解质电离平衡及电离平衡常数的应用D .a 、c 两点的c (H +)相等 4.实验探究典例4.25℃时,0.1 mol·L -1 HA 溶液中c (H +)c (O H -)=108,0.01 mol·L -1 BOH 溶液pH=12。
请回答下列问题:(1)0.1 mol·L -1 HA 溶液pH= ,HA 的电离常数K a 为 ,BOH 是 (填“强电解质”或“弱电解质”)。
山东省济南第一中学2020┄2021届高三上学期期中考试化学试题 Word版含答案

济南一中2020┄2021学年度第一学期期中考试高三化学试题(理科)本试卷分第I卷(选择题)和第II卷(非选择题)两部分,满分100分.考试时间90分钟.考试结束后,将本试卷和答题卡一并收回.注意事项:1.答第I卷前,考生务必将自己的姓名、准考证号、考试科目涂写在答题卡上.2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案,不能答在试卷上.可能用到的相对原子质量:H 1 C 12 O 16 S 32 K 39 Mn 55 Cu 64 Ba 137第I卷(选择题共48分)一、选择题(本大题共16小题,每题仅有一个选项符合题意,每小题3分,共48分.)1.化学与人类生产、生活、社会可持续发展密切相关。
下列有关说法正确的是()A.MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al B.水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质C.医疗上用的“钡餐”其成分是碳酸钡,漂白粉的成分为次氯酸钙;D.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化2.分类是化学学习与研究的常用方法,下列分类正确的是()①硫酸、烧碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;③Na2O、Fe2O3、A12O3属于碱性氧化物④根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;⑤根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;⑥CO2、SO2、NO2都能和碱溶液发生反应,因此它们都属于酸性氧化物⑦根据溶液导电能力强弱,将电解质分为强电解质、弱电解质A.只有②④⑥⑦ B.只有①③⑤⑦C.只有③④⑥ D.只有①②⑤3.下列有关实验的说法正确的是()A.除去铁粉中混有少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤B.光照氯水有气泡冒出,该气体主要为Cl2C.制备Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中D.Na溶液和盐酸可以通过相互滴加的方法来鉴别, NaHCO3溶液和Ca(OH)2溶液也可以通过相互滴加的方法来鉴别4. 用下列装置不能达到有关实验目的的是()A.用甲图装置证明ρ(煤油)<ρ(钠)<ρ(水)B.用乙图装置制备Fe(OH)2C.用丙图装置制取金属锰D.用丁图装置比较NaHCO3和Na2CO3的热稳定性5.能正确表示下列反应的离子方程式的是()A.氢氧化钡溶液中加入少量稀硫酸:Ba2++OH—+H++SO42—=== BaSO4+H2OB.NaClO(aq)中通入过量 SO2:C1O- + SO2 + H2O = HClO +HSO3-C.氯气通入水中:Cl2+H2O=2H++Cl-+ ClO-D.次氯酸钙溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2=CaCO3↓+2 HClO6.N A表示阿伏加德罗常数的值。
山东省济宁市2020┄2021届高考化学二模试卷Word版 含解析

2021年山东省济宁市高考化学二模试卷一、选择题(共7小题,每小题6分,满分42分)1.化学与生活、社会发展息息相关,下列说法不正确的是()A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应C.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金2.用N A表示阿伏伽德罗常数的值,下列说法正确的是()A.1molNa2O2固体中含离子总数为4N AB.用双氧水分解制取0.1mol氧气,转移的电子总数为0.4×6.02×1023C.0.1molAlCl3完全水解转化为氢氧化铝胶体,生成0.1N A个胶粒D.VL amol•L﹣1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl﹣的数目大于3×6.02×10233.分子式为C5H10O3并能使新制Cu(OH)2悬浊液溶解,继续加热会出现砖红色沉淀的有机物有(不含立体异构)()A.3种B.4种C.5种D.6种4.用下列实验方案及所选玻璃容器(非玻璃容器任选)就能实现相应实验目的是()实验目的实验方案所选玻璃仪器A除去KNO3中少量NaCl将混合物制成热的饱和溶液,冷却结晶,过滤酒精灯、烧杯、玻璃棒B证明HClO和CH3COOH的酸性强弱同温下用pH试纸测定浓度为0.1mol•L﹣1NaClO溶液和0.1mol•L﹣1CH3COONa溶液的玻璃棒、玻璃片pHC检验蔗糖水解产物具有还原性向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热试管、烧杯、酒精灯、滴管D配制1L 1.6%的CuSO4溶液(溶液密度近似为1g/mL)将25g CuSO4•5H2O溶解在975水中烧杯、量筒、玻璃棒A.A B.B C.C D.D5.X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素.下列说法正确的是()A.五种元素的原子半径从大到小的顺序是:M>W>Z>Y>XB.X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物C.化合物YW2、ZW2都是酸性氧化物D.用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀6.高能糖电池是一种新型的电池,该电池解决了环境污染问题,有望在未来代替传统电池.该电池的工作原理为C6H12O6(葡萄糖)+6O 26CO2+6H2O,下列有关说法正确的是()A.该电池的工作环境应在高温条件下B.正极反应:O2+2H2O+4e﹣═4OH﹣C.电池工作时葡萄糖在负极上失去电子发生还原反应D.电池工作时H+由负极移向正极,电解质溶液的pH增大7.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k•c m(NO)•c n(H2)(k、m、n待测),其反应包含下下列两步:①2NO+H2═N2+H2O2(慢)②H2O2+H2═2H2O(快)T℃时测得有关实验数据如下:序号 c(NO)/mol•L﹣1 c(H2)/mol•L﹣1速率/mol•L﹣1•min﹣1Ⅰ 0.0060 0.0010 1.8×10﹣4Ⅱ 0.0060 0.0020 3.6×10﹣4Ⅲ 0.0010 0.0060 3.0×10﹣5Ⅳ 0.0020 0.0060 1.2×10﹣4下列说法错误的是()A.整个反应速度由第①步反应决定B.正反应的活化能一定是①<②C.该反应速率表达式:v=5000c2(NO)•c(H2)D.该反应的热化学方程式为2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=﹣664kJ•mol﹣1二、解答题(共3小题,满分43分)8.联苄()是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:(一)催化剂的制备:图1是实验室制取少量无水AlCl3的相关实验装置的仪器和药品:(1)将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e,接,接,接.(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3.你认为这样做是否可行(填“可行”或“不可行”),你的理由是.(3)装置A中隐藏着一种安全隐患,请提出一种改进方案:.(二)联苄的制备联苄的制取原理为:反应最佳条件为n(苯):n(1,2﹣二氯乙烷)=10:1,反应温度在60﹣65℃之间.实验室制取联苄的装置如图2所示(加热和加持仪器略去):实验步骤:在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7mL1,2﹣二氯乙烷,控制反应温度在60﹣65℃,反应约60min.将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g.相关物理常数和物理性质如下表名称相对分子质量密度/(g•cm﹣3)熔点/℃沸点/℃溶解性苯780.88 5.580.1难溶水,易溶乙醇1,2一二氯乙烷99 1.27﹣35.383.5难溶水,可溶苯无水氯化铝133.5 2.44190178(升华)遇水水解,微溶苯联苄1820.9852284难溶水,易溶苯(4)仪器a的名称为,和普通分液漏斗相比,使用滴液漏斗的优点是.(5)洗涤操作中,水洗的目的是;无水硫酸镁的作用是.(6)常压蒸馏时,最低控制温度是.(7)该实验的产率约为.(小数点后保留两位有效数字)9.铜陵有色金属集团公司是电解铜产量全国第一的大型企业.其冶炼工艺中铜、硫回收率达到97%、87%.图表示其冶炼加工的流程:冶炼中的主要反应为:Cu2S+O22Cu+SO2.(1)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图:①用离子方程式表示反应器中发生的反应.②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是.③用吸收H2后的稀土储氢合金作为电池负极材料(用MH)表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量、长寿命的镍氢电池.电池充放电时的总反应为:Ni(OH)2+M═NiO(OH)+MH,电池放电时,负极电极反应式为;充电完成时,全部转化为NiO(OH),若继续充电,将在一个电极产生O2,O2扩散到另一个电极发生电极反应被消耗,从而避免产生的气体引起电池爆炸,此时,阴极电极反应式为.(2)在精炼铜的过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解.几种物质的溶度积常数(K sp)物质Fe(OH)2Fe(OH)3Zn(OH)2Cu(OH)2K sp8.0×10﹣16 4.0×10﹣38 3.0×10﹣17 2.2×10﹣20①调节电解液的pH是除去杂质离子的常用方法.根据上表中溶度积数据判断,含有等物质的量浓度Fe2+、Zn2+、Fe3+、Cu2+的溶液,随pH升高最先沉淀下来的离子是.②一种方案是先加入过量的H2O2,再调节pH到4左右,加入H2O2的目的是.加入H2O2后发生反应的离子方程式为.10.汽车尾气是造成雾霾天气的重要原因之一,尾气中的主要污染物为C x H y、NO、CO、SO2及固体颗粒物等.研究汽车尾气的成分及其发生的反应,可以为更好的治理汽车尾气提供技术支持.请回答下列问题:(1)治理尾气中NO和CO的一种方法是:在汽车排气管上装一个催化转化装置,使二者发生反应转化成无毒无污染气体,该反应的化学方程式是.(2)活性炭也可用于处理汽车尾气中的NO.在1L恒容密闭容器中加入0.1000molNO和2.030mol固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量以及容器内压强如下表:活性炭/mol NO/mol A/mol B/mol P/MPa200℃ 2.0000.04000.03000.0300 3.93335℃ 2.0050.05000.02500.250P根据上表数据,写出容器中发生反应的化学方程式并判断p 3.93MPa (用“>”、“<“或“=”填空).计算反应体系在200℃时的平衡常数Kp (用平衡分压代替平衡浓度计算,分压=总压×体积分数).(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液.常温下,测得某纯CaSO3与水形成的浊液pH为9,已知K al(H2SO3)=1.8×10﹣2,K a2(H2SO3)=6.0×10﹣9,忽略SO32﹣的第二步水解,则Ksp(CaSO3)= .(4)尾气中的碳氢化合物含有甲烷,其在排气管的催化转化器中可发生如下反应CH4(g)+H2O (1)⇌CO(g)+3H2(g)△H=+250.1kJ.mol﹣l.已知CO(g)、H2(g)的燃烧热依次为283.0kJ.mol﹣1、285.8kJ.mol﹣1,请写出表示甲烷燃烧热的热化学方程式.以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,其负极电极反应式为,已知该电池的能量转换效率为86.4%,则该电池的比能量为kW.h.kg﹣1(结果保留1位小数,比能量=,lkW•h=3.6×1 06J).三、【化学--选修3物质结构与性质】11.第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.(1)①H、C、N、O四种元素的电负性由小到大的顺序为.②下列叙述不正确的是.(填字母)a.因为HCHO与水分子间能形成氢键,所以HCHO易溶于水b.HCHO和CO2分子中的中心原子均采用sp2杂化c.C6H6分子中含有6个σ键和1个大π键,C2H2是非极性分子d.CO2晶体的熔点、沸点都比二氧化硅晶体的低③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式.(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是②六氰合亚铁离子[Fe(CN)6]4﹣中不存在.A、共价键B、非极性键C、配位键D、σ键E、π键写出一种与 CN﹣互为等电子体的单质分子式.(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于区.(4)一种Al﹣Fe合金的立体晶胞如图所示.请据此回答下列问题:①确定该合金的化学式.②若晶体的密度=ρg/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为cm.2021年山东省济宁市高考化学二模试卷参考答案与试题解析一、选择题(共7小题,每小题6分,满分42分)1.化学与生活、社会发展息息相关,下列说法不正确的是()A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应C.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金【考点】绿色化学.【专题】化学应用.【分析】A.气溶胶属于胶体,有丁达尔效应;B.依据湿法炼铜原理解答;C.青蒿素的提取用的是低温萃取,属于物理方法;D.合金是指金属与非金属或者金属融合而成具有金属性质的材料.【解答】解:A.雾霾所形成的气溶胶属于胶体,胶体都具有丁达尔效应,故A正确;B.铁活泼性强于铜,铁置换铜属于湿法炼铜,该过程发生了置换反应,故B正确;C.青蒿素的提取用的是低温萃取,没有新物质生成,属于物理方法,故C错误;D.铁中含碳量越高,硬度越大,含碳量越少,韧性越强,剂钢是铁与碳的合金,故D正确;故选:C.【点评】本题考查了化学与生活、社会关系,涉及胶体的性质、物理变化与化学变化的判断、合金的性质,题目难度不大,掌握基础是解题关键.2.用N A表示阿伏伽德罗常数的值,下列说法正确的是()A.1molNa2O2固体中含离子总数为4N AB.用双氧水分解制取0.1mol氧气,转移的电子总数为0.4×6.02×1023C.0.1molAlCl3完全水解转化为氢氧化铝胶体,生成0.1N A个胶粒D.VL amol•L﹣1的氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl﹣的数目大于3×6.02×1023【考点】阿伏加德罗常数.【专题】阿伏加德罗常数和阿伏加德罗定律.【分析】A、过氧化钠由2个钠离子和1个过氧根构成;B、用双氧水分解制氧气,氧元素的价态由﹣1价变为0价;C、一个氢氧化铝胶粒是多个氢氧化铝的聚集体;D、铁离子是弱碱阳离子,在溶液中会水解.【解答】解:A、过氧化钠由2个钠离子和1个过氧根构成,故1mol过氧化钠中含3mol离子即3N A个,故A错误;B、用双氧水分解制氧气,氧元素的价态由﹣1价变为0价,故当生成0.1mol氧气时,转移0.2mol电子即0.2N A个,故B错误;C、一个氢氧化铝胶粒是多个氢氧化铝的聚集体,故0.1mol氯化铝所形成的胶粒的个数小于0.1N A个,故C错误;D、铁离子是弱碱阳离子,在溶液中会水解,故当铁离子为1mol时,则溶液中的氯离子大于3mol即3N A个,故D正确.故选D.【点评】本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.3.分子式为C5H10O3并能使新制Cu(OH)2悬浊液溶解,继续加热会出现砖红色沉淀的有机物有(不含立体异构)()A.3种B.4种C.5种D.6种【考点】有机化合物的异构现象.【专题】同分异构体的类型及其判定.【分析】分子式为C5H10O3并能使新制Cu(OH)2悬浊液溶解,继续加热会出现砖红色沉淀,说明有机物中含有1个羧基、醛基,相当于丁酸的一元取代产物来解答.【解答】解:分子式为C5H10O3并能使新制Cu(OH)2悬浊液溶解,继续加热会出现砖红色沉淀,说明有机物中含有1个羧基、醛基,丁酸有2种同分异构体:CH3CH2CH2COOH、(CH3)2CHCOOH;当丁酸为CH3CH2CH2COOH时,一元取代产物有3种;当丁酸为(CH3)2CHCOOH时,一元取代产物有2种;当所以共有5种结构,故选C.【点评】本题考查同分异构体的书写,难度中等,根据等效氢判断同分异构体数目,利用对称性确定分子中等效氢原子数目是解题的关键.4.用下列实验方案及所选玻璃容器(非玻璃容器任选)就能实现相应实验目的是()实验目的实验方案所选玻璃仪器A除去KNO3中少量NaCl将混合物制成热的饱和溶液,冷却结晶,过滤酒精灯、烧杯、玻璃棒B证明HClO和CH3COOH的酸性强弱同温下用pH试纸测定浓度为0.1mol•L﹣1NaClO溶液和0.1mol•L﹣1CH3COONa溶液的pH玻璃棒、玻璃片C检验蔗糖水解产物具有还原性向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热试管、烧杯、酒精灯、滴管D配制1L 1.6%的CuSO4溶液(溶液密度近似为1g/mL)将25g CuSO4•5H2O溶解在975水中烧杯、量筒、玻璃棒A.A B.B C.C D.D【考点】化学实验方案的评价.【专题】实验评价题.【分析】A.过滤时还需要用漏斗;B.NaClO具有强氧化性,不能用pH试纸测定浓度为0.1mol•L﹣1 NaClO溶液的pH;C.银镜反应需要在碱性条件下进行;D.1L 1.6%的CuSO4溶液(溶液密度近似为1g/mL)中溶质的物质的量是0.1mol.【解答】解:A.过滤时还需要用漏斗,该实验中没有漏斗,故A错误;B.NaClO具有强氧化性,不能用pH试纸测定浓度为0.1mol•L﹣1 NaClO溶液的pH,则不能确定pH大小,不能比较酸性的强弱,故B错误;C.银镜反应需要在碱性条件下进行,所以在加入银氨溶液之前需要加入NaOH溶液中和未反应的酸,故C错误;D.1L 1.6%的CuSO4溶液(溶液密度近似为1g/mL)中溶质的物质的量是0.1mol,溶液的质量是1000g,25g CuSO4•5H2O中硫酸铜的物质的量是0.1mol,故D正确;故选D.【点评】本题考查了实验方案评价,明确实验原理是解本题关键,题目难度不大,注意不能用pH 试纸检验次氯酸钠溶液的pH大小,因为次氯酸具有漂白性,易错选项是B.5.X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素.下列说法正确的是()A.五种元素的原子半径从大到小的顺序是:M>W>Z>Y>XB.X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物C.化合物YW2、ZW2都是酸性氧化物D.用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀【考点】原子结构与元素周期律的关系.【专题】元素周期律与元素周期表专题.【分析】X元素的原子形成的离子就是一个质子,应为H元素,Y原子的最外层电子数是内层电子数的2倍,应为C元素;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,则Z为N元素、W为O元素;M是地壳中含量最高的金属元素,应为Al元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.【解答】解:X元素的原子形成的离子就是一个质子,应为H元素,Y原子的最外层电子数是内层电子数的2倍,应为C元素;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,则Z为N元素、W为O元素;M是地壳中含量最高的金属元素,应为Al元素,A.H原子半径最小,同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径Al>C>N>O>H,即M>Y>Z>W>X,故A错误;B.N、H两元素能形成NH3、N2H4,故B正确;C.NO2与水反应生成硝酸和NO,不是酸性氧化物,故C错误;D.用Al单质作阳极,石墨作阴极电解NaHCO3溶液,阴极生成氢气,不会生成沉淀,故D错误.故选B.【点评】本题考查结构位置性质关系应用,为高频考点,侧重于学生的分析能力的考查,难度中等,推断元素是解题关键,注意理解根据最外层电子数关系确定元素,对学生的逻辑推理有一定的要求.6.高能糖电池是一种新型的电池,该电池解决了环境污染问题,有望在未来代替传统电池.该电池的工作原理为C6H12O6(葡萄糖)+6O26CO2+6H2O,下列有关说法正确的是()A.该电池的工作环境应在高温条件下B.正极反应:O2+2H2O+4e﹣═4OH﹣C.电池工作时葡萄糖在负极上失去电子发生还原反应D.电池工作时H+由负极移向正极,电解质溶液的pH增大【考点】化学电源新型电池.【专题】电化学专题.【分析】A.该电池是燃料原电池,反应条件温和;B.在正极上发生得电子的还原反应;C.葡萄糖在负极上失去电子被氧化,发生氧化反应;D.原电池中阳离子移向正极,根据电池反应判断酸碱性的变化.【解答】解:A.该电池是燃料原电池,电池中没有发生燃烧反应,反应条件温和,所以不是高温条件,故A错误;B.在电池正极上发生得电子的还原反应,即O2+4H++4e﹣═2H2O,故B错误;C.葡萄糖在负极上失去电子被氧化,发生氧化反应,故C错误;D.电池工作时H+由负极移向正极,已知C6H12O6(葡萄糖)+6O26CO2+6H2O产生水将溶液稀释,电解液的pH变大,故D正确;故选:D.【点评】本题考查化学电源新型电池,明确原电池原理解答本题的关键,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力.7.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,该反应的速率表达式为v=k•c m(NO)•c n(H2)(k、m、n待测),其反应包含下下列两步:①2NO+H2═N2+H2O2(慢)②H2O2+H2═2H2O(快)T℃时测得有关实验数据如下:序号 c(NO)/mol•L﹣1 c(H2)/mol•L﹣1速率/mol•L﹣1•min﹣1Ⅰ 0.0060 0.0010 1.8×10﹣4Ⅱ 0.0060 0.0020 3.6×10﹣4Ⅲ 0.0010 0.0060 3.0×10﹣5Ⅳ 0.0020 0.0060 1.2×10﹣4下列说法错误的是()A.整个反应速度由第①步反应决定B.正反应的活化能一定是①<②C.该反应速率表达式:v=5000c2(NO)•c(H2)D.该反应的热化学方程式为2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=﹣664kJ•mol﹣1【考点】反应热和焓变;热化学方程式.【专题】化学反应中的能量变化.【分析】A.依据反应过程中的两步反应可知,反应慢的决定整个反应速率;B.反应①难以进行,说明反应的活化能高;C.比较图表数据ⅠⅡ数据NO浓度不变,氢气浓度增大一倍,反应速率增大一倍,ⅢⅣ数据分析,H2浓度不变,NO浓度增大一倍,反应速率增大到4倍,据此得到速率方程,代入数值计算得到K分析判断方程正误;D.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,生成28gN2放热664KJ,结合热化学方程式书写分析判断,标注物质聚集状态和对应反应的焓变;【解答】解:A.①2NO+H2═N2+H2O2(慢),②H2O2+H2═2H2O(快),反应历程中反应慢的决定反应速率,整个反应速度由第①步反应决定,故A正确;B.反应①难以进行,说明反应的活化能高,正反应的活化能一定是①>②,故B错误;C.比较图表数据ⅠⅡ数据NO浓度不变,氢气浓度增大一倍,反应速率增大一倍,ⅢⅣ数据分析,H2浓度不变,NO浓度增大一倍,反应速率增大到4倍,据此得到速率方程,v=Kc2(NO)•c(H2),依据Ⅰ中数据计算K=5000,则速率方程v=5000c2(NO)•c(H2),故C正确;D.反应2NO(g)+2H2(g)═N2(g)+2H2O(g)中,每生成7gN2放出166kJ的热量,生成28gN2放热664KJ,热化学方程式为:2NO(g)+2H2(g)═N2(g)+2H2O(g)△H=﹣664kJ•mol﹣1,故D正确;故选B.【点评】本题考查了化学反应能量变化分析,热化学方程式书写,主要是催化剂作用,速率方程的推导和计算应用,题目难度中等.二、解答题(共3小题,满分43分)8.联苄()是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:(一)催化剂的制备:图1是实验室制取少量无水AlCl3的相关实验装置的仪器和药品:(1)将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e, f 接g ,h 接 a , b 接 c .(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3.你认为这样做是否可行不可行(填“可行”或“不可行”),你的理由是制得的Cl2中混有的HCl与Al 反应生成H2,H2与Cl2混合加热时会发生爆炸.(3)装置A中隐藏着一种安全隐患,请提出一种改进方案:在硬质玻璃管与广口瓶之间用粗导管连接,防止AlCl3冷凝成固体造成堵塞.(二)联苄的制备联苄的制取原理为:反应最佳条件为n(苯):n(1,2﹣二氯乙烷)=10:1,反应温度在60﹣65℃之间.实验室制取联苄的装置如图2所示(加热和加持仪器略去):实验步骤:在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7mL1,2﹣二氯乙烷,控制反应温度在60﹣65℃,反应约60min.将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g.相关物理常数和物理性质如下表熔点/℃沸点/℃溶解性名称相对分子质量密度/(g•cm﹣3)苯780.88 5.580.1难溶水,易溶乙醇1,2一二氯乙烷99 1.27﹣35.383.5难溶水,可溶苯无水氯化铝133.5 2.44190178(升华)遇水水解,微溶苯联苄1820.9852284难溶水,易溶苯(4)仪器a的名称为球形冷凝管,和普通分液漏斗相比,使用滴液漏斗的优点是可以使液体顺利滴下.(5)洗涤操作中,水洗的目的是洗掉氯化铝、盐酸和碳酸钠等可溶性无机物;无水硫酸镁的作用是干燥.(6)常压蒸馏时,最低控制温度是83.5℃.(7)该实验的产率约为73.00% .(小数点后保留两位有效数字)【考点】制备实验方案的设计.【专题】实验分析题;实验评价题;演绎推理法;制备实验综合.【分析】(一)实验室用浓盐酸和二氧化锰在加热条件下制备氯气,可用食盐晶体和浓硫酸替代盐酸,为得到干燥的氯化铁,生成的氯气需除去氯化氢、水,可分别通过饱和食盐水、浓硫酸,然后在装置A中反应生成氯化铝,为防止污染空气和氯化铝的水解,A还要连接E装置,以吸收氯气和水,以此解答该题;(二)(4)由仪器结构特征,可知仪器a为球形冷凝管;滴液漏斗可以平衡漏斗内液体和下面的三颈烧瓶中的压强,便于漏斗内液体流下;(5)第二次用水洗涤是为了除去可溶性杂质,无水硫酸镁是为是吸收少量水;(6)常压蒸馏时,主要是除去混合物中的未反应的1,2一二氯乙烷,因为1,2一二氯乙烷的沸点为83.5℃,据此控制温度;(7)由方程式可知:n(1,2一二氯乙烷)=2n(苯)=n(1,l﹣二苯乙烷),过量计算,根据不足量物质计算理论生成1,l﹣二苯乙烷的质量,产率=×100%;【解答】解:(一)实验室用浓盐酸和二氧化锰在加热条件下制备氯气,可用食盐晶体和浓硫酸替代盐酸,为得到干燥的氯化铁,生成的氯气需除去氯化氢、水,可分别通过饱和食盐水、浓硫酸,然后在装置A中反应生成氯化铝,为防止污染空气和氯化铝的水解,A还要连接E装置,以吸收氯气和水,(1)根据上面的分析可知,将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d→e→f→g→h→a→b→c,故答案为:f;g;h;a;b;c;(2)如果将上述装置中D去掉,其余装置和试剂不变,则制得的Cl2中混有的HCl与Al反应生成H2,H2与Cl2混合加热时会发生爆炸,所以D装置不能去掉,故答案为:不可行;制得的Cl2中混有的HCl与Al反应生成H2,H2与Cl2混合加热时会发生爆炸;(3)装置A中制得的氯化铝容易将导管堵塞,所以可以在硬质玻璃管与广口瓶之间用粗导管连接,防止AlCl3冷凝成固体造成堵塞,故答案为:在硬质玻璃管与广口瓶之间用粗导管连接,防止AlCl3冷凝成固体造成堵塞;(二)(4)由仪器结构特征,可知仪器a为球形冷凝管;滴液漏斗可以平衡漏斗内液体和下面的三颈烧瓶中的压强,便于漏斗内液体流下,故答案为:球形冷凝管;可以使液体顺利滴下;(5)第二次用水洗涤是为了洗掉氯化铝、盐酸和碳酸钠等可溶性无机物,无水硫酸镁是为是吸收少量水,即干燥作用,故答案为:洗掉氯化铝、盐酸和碳酸钠等可溶性无机物;干燥;(6)常压蒸馏时,主要是除去混合物中的未反应的1,2一二氯乙烷,因为1,2一二氯乙烷的沸点为83.5℃,所以常压蒸馏时,最低控制温度是83.5℃,故答案为:83.5℃;(7)苯物质的量为=1.35mol,1,2一二氯乙烷的物质的量为mol=0.137mol,由方程式可知苯过量,则n(1,2一二氯乙烷)=n(1,l﹣二苯。
2020届中考化学第一轮科学探究能力《测定空气里氧气含量的探究》测试题(word版有答案)
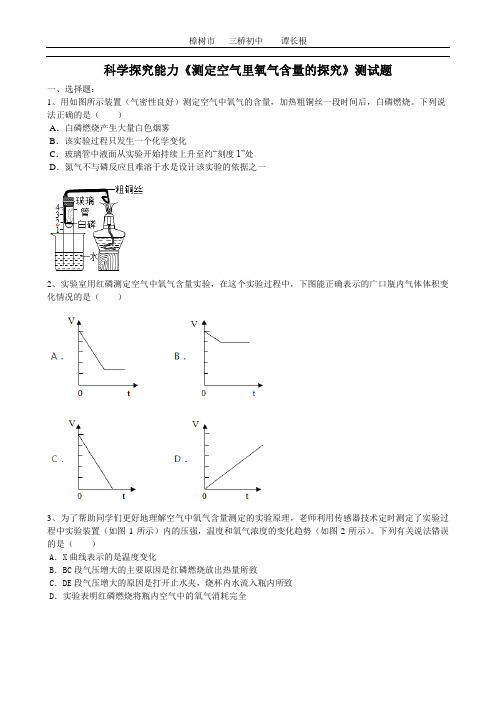
科学探究能力《测定空气里氧气含量的探究》测试题一、选择题:1、用如图所示装置(气密性良好)测定空气中氧气的含量,加热粗铜丝一段时间后,白磷燃烧。
下列说法正确的是()A.白磷燃烧产生大量白色烟雾B.该实验过程只发生一个化学变化C.玻璃管中液面从实验开始持续上升至约“刻度1”处D.氮气不与磷反应且难溶于水是设计该实验的依据之一2、实验室用红磷测定空气中氧气含量实验,在这个实验过程中,下图能正确表示的广口瓶内气体体积变化情况的是()3、为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验过程中实验装置(如图1所示)内的压强,温度和氧气浓度的变化趋势(如图2所示)。
下列有关说法错误的是()A.X曲线表示的是温度变化B.BC段气压增大的主要原因是红磷燃烧放出热量所致C.DE段气压增大的原因是打开止水夹,烧杯内水流入瓶内所致D.实验表明红磷燃烧将瓶内空气中的氧气消耗完全4、某同学用如图所示装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后再进行后续操作,下列说法正确的是()A.所用红磷要过量,以保证集气瓶内空气里的氧气能充分反应B.在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡皮塞C.仍用本装置,只把红磷换成燃烧的木炭,能够更精确测定空气里氧气的含量D.红磷燃烧时,要打开止水夹,以免瓶因温度升高,气压较大,造成橡皮塞从瓶口脱落5、暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见如图)。
以下对此改进实验的叙述,错误的是()A.此实验中食盐能加快铁粉生锈B.此实验中发热剂的多少不影响测量结果C.此实验测出氧气的体积分数约是18.3%D.实验前一定要检查装置的气密性6、在图1所示装置中燃烧红磷来测定空气中的氧气含量,并用传感器记录集气瓶中压强随时间变化的情况,得图2所示数据。
下列说法正确的是()A.a点处压强增大是因为少量空气进入B.ab段压强减小的原因只有氧气被消耗C.c点时打开了弹簧夹D.d点集气瓶中的温度一定等于室温7、下列装置都可用于测定空气里氧气的含量,a、b两物质的选择正确的是()A.a是汞,b是红磷B.a是铜,b是木炭C.a是汞,b是硫磺D.a是汞,b是木炭8、某同学用如图所示装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后再进行后续操作,下列说法正确的是()A.在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡皮塞B.所用红磷必须过量,以保证集气瓶内空气里的氧气能充分反应C.红磷燃烧时,要打开止水夹,以免瓶因温度升高,气压较大,造成橡皮塞从瓶口脱落D.仍用本装置,只把红磷换成燃烧的本炭,能够更精确测定空气里氧气的含量9、如图所示的装置是测定空气中氧气的含量,对该实验认识正确的是()A.使用红磷的量多或少,都不会影响实验结果B.燃烧足够的红磷可使进入容器里的水占容器的总体积四分之一C.红磷燃烧消耗空气中的氧气,使容器内的压强减小,水从烧杯进入容器D.红磷一燃烧完,就立即观察并记录水进入容器的刻度10、暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化。
2020届山东省新高考高三好教育云平台3月内部特供卷化学试题全国1卷模拟试题(二)(word版附图片版答案)

QRYZ3 =====4 3 4 3――→ 2 3 2 A 2019-2020 学年下学期好教育云平台 3 月内部特供卷B .2.8g N 2 中含有共用电子对的数目为 0.3N AC .56g Fe 与足量热浓硝酸反应生成 NO 2 分子的数目为 3N A 高三化学(二)D .0.1mol·L −1 NH NO 溶液中,NH +的数目小于 0.1N434A注意事项:1.答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,并将准考证号条形 码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂 黑,写在试题卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用签字笔直接答在答题卡上对应的答题区域内。
写在试题卷、草 稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Al 27 S 32 Cl 35.5 Fe 56 Ba 137一、选择题(每小题 6 分,共 42 分)7.《天工开物》中对“海水盐”有如下描述:“凡煎盐锅古谓之牢盆……其下列灶燃薪,多者十 二三眼,少者七八眼,共煎此盘……火燃釜底,滚沸延及成盐。
”文中涉及的操作是A .萃取B .结晶C .蒸馏D .过滤8.下列离子方程式书写正确的是A .氢氧化钡溶液中加入硫酸铵:Ba 2++OH −+NH ++SO 2−=BaSO ↓+NH ·H O11.X 、Y 、Z 、Q 、R 均为短周期元素,且 Y 、Z 、Q 、R 在周期表中的位置关系如下图所示。
已知 X 与 Y 同主族,X 与 Q 能形成最简单的有机物。
则下列有关说法正确的是A .原子半径:r(Z)>r(Y)>(R)>r(Q)B .气态化合物的稳定性:QX 4>RX 3C .X 与 Y 形成的化合物中含有离子键D .最高价含氧酸的酸性:X 2QO 3>XRO 312.氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。
2024届山东省实验中学高三下学期一模英语试题

绝密★启用并使用完毕前山东省实验中学2024届高三第一次模拟考试英语试题2024.04(本试卷共10页, 共三部分: 全卷满分120分, 考试用时100分钟)注意事项:1. 答卷前, 先将自己的姓名、准考证号填写在试卷和答题纸上。
2. 选择题的作答: 每小题选出答案后, 用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动, 用橡皮擦干净后, 再选涂其他答案标号。
3. 非选择题的作答: 用0.5mm黑色签字笔直接答在答题卡上对应的答题区域内, 写在试卷、草稿纸和答题卡上的非答题区域均无效。
第一部分阅读理解(共两节, 满分50分)第一节(共15小题; 每小题2.5分, 满分37.5分)阅读下列短文, 从每题所给的A、B、C、D四个选项中选出最佳选项。
AIntroduction to Drama ExamsOur exams inspire and enable learners across the globe to be confident communicators. Exams are open to anyone looking to gain confidence and experience in speech, communication and performance. There are no age restrictions. As one of the UK's oldest and most respected drama schools and awarding organizations, we examine over 100,000candidates and deliver exams both online and in person in many countries across the globe.Now we are pleased to offer free, online "Introduction to Examinations" information session. Booking is now opening for events until Summer 2024.The 1.5-hour session will begin with an Introduction to Examinations, their history and the format of assessment. Work will then focus on the subjects available to take, and will end with a Q&A phase where participants will be invited to write in their questions to the host organizer.Ifyouhaveanyquestionsregardingthis,********************************.ukandwewillbehappytohelp. Looking forward to seeing you online at this event.1. What is an advantage of the drama exam?A. It is free of charge.B. It offers flexible schedules.C. It suits a wide range of people.D. It puts restrictions on nationality.2. What is required to register for the sessions?A. Payment in advance.B. Contact information.C. Education background.D. Performance experience.3. What should you do if you have a question during the online session?A. Email it to the drama school.B. Write it down before the session.C. Propose it at the beginning of the session.D. Send it to the host organizer in Q&A phase.BCafeterias have been filled with challenges—right from planning, purchasing, and preparing, to reducing waste, staying on budget, managing goods, and training staff. Through the tedious process, restaurateurs lacked a unified platform for efficient management. To bring consistency to the unorganised catering(餐饮)industry, childhood friends Arjun Subramanian and Raj Jain, who shared a passion for innovation, decided to partner in 2019 to explore opportunities in the cafeteria industry.In May 2020, they co-founded Platos, a one-stop solution for restaurants with a custom technology kit to streamline all aspects of cafeteria management. The company offers end-to-end cafeteria management, staff selection and food trials to ensure smooth operations and consistent service. "We believe startups solve real problems and Platos is our shot at making daily workplace food enjoyable again. We aim to simplify the dining experience, providing a convenient and efficient solution that benefits both restaurateurs and customers and creating a connected ecosystem, "says Subramanian, CEO and co-founder.Platos guarantees that a technology-driven cafeteria allows customers to order, pay, pick up, and provide ratings and feedback. It also offers goods and menu management to effectively perform daily operations. Additionally, its applications connect all shareholders for a smart cafeteria experience. "We help businesses that are into catering on condition that they have access to an industrial kitchen setup where they' re making food according to certain standards," Jain states.Since the beginning, Platos claims to have transformed 45 cafeterias across eight cities in the country. Currently, it has over 45,000 monthly users placing more than 200,000 orders. Despite facing challenges in launching cafeterias across major cities in the initial stages, Platos has experienced a 15% increase in its month-over-month profits.As for future plans, the startup is looking to raise $1 million from investors as strategic partners, bringing in capital, expertise, and networks. "Finding the right lead investor is the compass that points your startup toward success," Subramanian says.4. What does the underlined word "tedious" in Paragraph 1 mean?A. Time-consuming.B. Breath-taking.C. Heart-breaking.D. Energy-saving.5. What is the purpose of founding Platos?A. To connect customers with a greener ecosystem.B. To ensure food security and variety in cafeterias.C. To improve cafeteria management with technology.D. To make staff selection more efficient and enjoyable.6. What can we learn from the statistics in Paragraph 4?A. Platos has achieved its ultimate financial goal.B. Platos has gained impressive marketing progress.C. Challenges in food industry can be easily overcome.D. Tech-driven cafeterias have covered most urban areas.7. What is Subramanian's future plan for Platos?A. To reduce costs.B. To increase profits.C. To seek investment.D. To innovate technology.CWith a brain the size of a pinhead, insects possess a great sense of direction. They manage to locate themselves and move through small openings. How do they do this with their limited brain power? Understanding the inner workings of an insect's brain can help us in our search towards energy-efficient computing, physicist Elisabetta Chicca of the University of Groningen shows with her most recent result: a robot that acts like an insect.It's not easy to make use of the images that come in through your eyes when deciding what your feet or wings should do. A key aspect here is the apparent motion of things as you move. "Like when you're on a train,” Chicca explains. "The trees nearby appear to move faster than the houses far away." Insects use this information to infer how far away things are. This works well when moving in a straight line, but reality is not that simple. To keep things manageable for their limited brain power, they adjust their behaviour: they fly in a straight line, make a turn, then make another straight line.In search of the neural mechanism(神经机制)that drives insect behaviour, PhD student Thorben Schoepe developed a model of its neuronal activity and a small robot that uses this model to find the position. His model is based on one main principle: always head towards the area with the least apparent motion. He had his robot drive through a long passage consisting of two walls and the robot centred in the middle of the passage, as insects tend to do. In other virtual environments, such as a space with small openings, his model also showed similar behaviour to insects.The fact that a robot can find its position in a realistic environment is not new. Rather, the model gives insight into how insects do the job, and how they manage to do things so efficiently. In a similar way, you could make computers more efficient.In the future, Chicca hopes to apply this specific insect behaviour to a chip as well. "Instead of using a general-purpose computer with all its possibilities, you can build specific hardware; a tiny chip that does the job, keeping things much smaller and energy-efficient." She comments.8. Why is "a train" mentioned in Paragraph 2?A. To illustrate the principle of train motion.B. To highlight why human vision is limited.C. To explain how insects perceive distances.D. To compare the movement of trees and houses.9. What does Paragraph 3 mainly talk about concerning Schoepe's model?A. Its novel design.B. Its theoretical basis.C. Its possible application.D. Its working mechanism.10. What do the researchers think of the finding?A. Amusing.B. Discouraging.C. Promising.D. Contradictory.11. What will Chicca's follow-up study focus on?A. Inventing insect-like chips.B. Studying general-purpose robots.C. Creating insect-inspired computers.D. Developing energy-efficient hardware.DWith the help from an artificial language(AL)model, MIT neuroscientists have discovered what kind of sentences are most likely to fire up the brain's key language processing centers. The new study reveals that sentences that are more complex, because of either unusual grammar or unexpected meaning, generate stronger responses in these language processing centers. Sentences that are very straightforward barely engage these regions, and meaningless orders of words don't do much for them either.In this study, the researchers focused on language-processing regions found in the left hemisphere(半球)of the brain. By collecting a set of 1,000 sentences from various sources, the researchers measured the brain activity of participants using functional magnetic resonance imaging(fMRI)while they read the sentences. The same sentences were also fed into a large language model, similar to ChatGPT, to measure the model's activation patterns. Once the researchers had all of those data, they trained the model to predict how the human language network would respond to any new sentence based on how the artificial language network responded to these 1,000 sentences.The researchers then used the model to determine 500 new sentences that would drive highest brain activity and sentences that would make the brain less active, and their findings were confirmed in subsequent human participants. To understand why certain sentences generate stronger brain responses, the model examined the sentences based on 11 different language characteristics. The analysis revealed that sentences that were more surprising resulted in greater brain activity. Another linguistic(语言的)aspect that correlated with the brain's language network responses was the complexity of the sentences, which was determined by how well they followed English grammar rules and bow logically they linked with each other.The researchers now plan to see if they can extend these findings in speakers of languages other than English. They also hope to explore what type of stimuli may activate language processing regions in the brain's right hemisphere.12. What sentences make our brain work harder?A. Lengthy.B. Logical.C. Straightforward.D. Complicated.13. What is the function of the AL model in the research?A. To examine language network.B. To reduce language complexity.C. To locate language processing area.D. To identify language characteristics.14. How did the researchers carry out their study?A. By conducting interviews.B. By collecting questionnaires.C. By analyzing experiment data.D. By reviewing previous studies.15. Which of the following is a suitable title for the text?A. AL Model Stimulates Brain ActivitiesB. AL Model Speeds Up Language LearningC. AL Model Reveals the Secrets of Brain ActivationD. AL Model Enhances Brain Processing Capacity第二节(共5小题; 每小题2.5分, 满分12.5分)根据短文内容, 从短文后的选项中选出能填入空白处的最佳选项。
河南省实验中学2020届高三上学期期中考试+生物+Word版含答案

河南省实验中学2019——2020学年上期期中试卷高三生物命题人:王慧杰审题人:佟曼秋(时间:90分钟,满分:100分)一、单选题(本大题共30小题,每小题2分,共60分)1、核酸是细胞中一类重要的生物大分子,下列相关说法正确的是()A.原核细胞中的DNA是环状的,真核细胞中的核DNA都是链状的B.人体细胞中的RNA是由DNA转录而得到的单链核酸,无碱基对存在C.DNA和RNA所含的碱基不同,五碳糖和磷酸也不同D.细胞生物同时含有DNA和RNA,主要遗传物质是DNA2、下列关于细胞结构与功能的叙述中,不正确的是()A.性腺细胞的内质网较肌肉细胞的发达B.核糖体的形成一定与核仁有关C.吞噬细胞中的溶酶体较肾小管细胞中的多D.唾液腺细胞释放唾液淀粉酶能体现细胞膜具有流动性3、如图1为物质A通过细胞膜的示意图,图2为细胞膜的局部放大图,据图分析,下列说法正确的是()A.图1中物质A的跨膜运输与细胞呼吸强度无关B.如果图1中物质A正在进入细胞,则运输方向为图2中的I→IIC.流动镶嵌模型能解释生物膜的结构和特点,观察图2结构需要借助高倍显微镜D.图1中物质B的化学本质是蛋白质,生物膜系统中只有细胞膜上有蛋白质4、下列化学反应属于水解反应的是 ( )①ATP→ADP ②葡萄糖→丙酮酸③核酸→核苷酸A.①②B.①③C.②③D.①②③5、某实验小组在室温条件下,将紫色洋葱鳞片叶外表皮细胞置于一定浓度的某溶液中,测得细胞液浓度与该溶液浓度的比值(P值)随时间的变化曲线如图所示。
下列相关叙述正确的是()A.该溶液是一定浓度的蔗糖溶液B.细胞在t1时刻开始从外界溶液中吸收溶质C.若降低温度,则t1〜t2时间段会变长D. t2时刻后P值不再增大主要是由于细胞壁的限制6、下列关于酶和ATP的叙述中,正确的是()A.酶和ATP的组成元素不可能相同B.无氧呼吸的每一阶段均需要酶,且均能产生ATPC.酶可以重复使用,但ATP不能重复使用D.叶绿体中CO2的固定过程与酶的催化和ATP的水解均有关7、下列关于植物细胞中“0”转移途径叙述正确的是()A.在根尖细胞中,H2O中的0可转移到02中B.在叶肉细胞中,吸收的C02中的0可以转移到丙酮酸中C.在马铃薯块茎细胞中,C6H1206中的0可以转移到C2H5OH中D.为叶肉细胞提供02,其中的0只能转移到H2O中8、下列关于下图的叙述,错误的是()A.若过程①表示光反应,a代表水B.肝细胞中,过程②发生在线粒体内膜C.过程③受b的制约,还受过程①的影响D.过程①产生的[H]和过程④产生的[H]是同一种物质9、呼吸商(RQ=放出的CO2量/吸收的O2量)可作为描述细胞呼吸过程中氧气供应状态的一种指标。
2020届中考化学第一轮科学探究能力《测定空气里氧气含量的探究》测试试题(word版有答案)

科学探究能力《测定空气里氧气含量的探究》测试题一、选择题:1、用如图所示装置(气密性良好)测定空气中氧气的含量,加热粗铜丝一段时间后,白磷燃烧。
下列说法正确的是()A.白磷燃烧产生大量白色烟雾B.该实验过程只发生一个化学变化C.玻璃管中液面从实验开始持续上升至约“刻度1”处D.氮气不与磷反应且难溶于水是设计该实验的依据之一2、实验室用红磷测定空气中氧气含量实验,在这个实验过程中,下图能正确表示的广口瓶内气体体积变化情况的是()3、为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验过程中实验装置(如图1所示)内的压强,温度和氧气浓度的变化趋势(如图2所示)。
下列有关说法错误的是()A.X曲线表示的是温度变化B.BC段气压增大的主要原因是红磷燃烧放出热量所致C.DE段气压增大的原因是打开止水夹,烧杯内水流入瓶内所致D.实验表明红磷燃烧将瓶内空气中的氧气消耗完全4、某同学用如图所示装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后再进行后续操作,下列说法正确的是()A.所用红磷要过量,以保证集气瓶内空气里的氧气能充分反应B.在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡皮塞C.仍用本装置,只把红磷换成燃烧的木炭,能够更精确测定空气里氧气的含量D.红磷燃烧时,要打开止水夹,以免瓶因温度升高,气压较大,造成橡皮塞从瓶口脱落5、暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见如图)。
以下对此改进实验的叙述,错误的是()A.此实验中食盐能加快铁粉生锈B.此实验中发热剂的多少不影响测量结果C.此实验测出氧气的体积分数约是18.3%D.实验前一定要检查装置的气密性6、在图1所示装置中燃烧红磷来测定空气中的氧气含量,并用传感器记录集气瓶中压强随时间变化的情况,得图2所示数据。
下列说法正确的是()A.a点处压强增大是因为少量空气进入B.ab段压强减小的原因只有氧气被消耗C.c点时打开了弹簧夹D.d点集气瓶中的温度一定等于室温7、下列装置都可用于测定空气里氧气的含量,a、b两物质的选择正确的是()A.a是汞,b是红磷B.a是铜,b是木炭C.a是汞,b是硫磺D.a是汞,b是木炭8、某同学用如图所示装置测定空气里氧气的含量,实验时,连接好装置并检查不漏气后再进行后续操作,下列说法正确的是()A.在空气里点燃红磷后,应缓慢把燃烧匙伸入瓶内并塞紧橡皮塞B.所用红磷必须过量,以保证集气瓶内空气里的氧气能充分反应C.红磷燃烧时,要打开止水夹,以免瓶因温度升高,气压较大,造成橡皮塞从瓶口脱落D.仍用本装置,只把红磷换成燃烧的本炭,能够更精确测定空气里氧气的含量9、如图所示的装置是测定空气中氧气的含量,对该实验认识正确的是()A.使用红磷的量多或少,都不会影响实验结果B.燃烧足够的红磷可使进入容器里的水占容器的总体积四分之一C.红磷燃烧消耗空气中的氧气,使容器内的压强减小,水从烧杯进入容器D.红磷一燃烧完,就立即观察并记录水进入容器的刻度10、暖宝宝贴(主要成分为铁粉、木炭、食盐)的热量来源于铁粉的氧化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
济宁北大培文实验学校2016级高三上期中考试化学试题2018.11 注意事项:1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
时间90分钟,满分100分。
2.考生须将第Ⅰ卷所有题目的答案涂在答题卡上,第Ⅱ卷所有题目的答案须用黑色签字笔、黑色钢笔或黑色圆珠笔按要求填写在答题纸指定位置,考试结束后将答题卡和答题纸一同上交。
3.可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 27 C1 35.5 Mg 24 Fe56 Cu---64第Ⅰ卷(选择题,共48分)一、选择题(本题包括16小题,每小题3分,共48分。
每小题只有一个....选项符合题意。
)1. 化学是一门与社会、生活、科研密切相关的自然科学。
下列有关叙述中,不正确的是( )A.大量使用燃煤发电是形成雾霾的主要原因B.天然气、煤气大量泄漏遇到明火会爆炸C.“绿水青山就是金山银山”,矿物燃料的脱硫脱硝,可以减少SO2、NO2的排放D.利用化学反应可实现12C到14C的转化2.等质量的下列物质与足量的稀硝酸反应,放出NO物质的量最多的是()A、氧化亚铁B、三氧化二铁C、四氧化三铁D、硫酸亚铁3.下列各组物质的分类正确的是()①混合物:氯水、氨水、水玻璃、水银②电解质:明矾、冰醋酸、石膏、纯碱③同位素:1H+、2H+、3H+④同素异形体:C60、C80、金刚石、石墨⑤弱电解质:HF、SO2、NH3、H2OA.②④B.②③④C.②④⑤D.全部正确4、下列说法正确的是()A.生活中可以使用明矾对饮用水进行消毒、杀菌、除杂B.雾、有色玻璃、葡萄糖溶液中分散质的粒子直径大小均在1~100 nm之间C.过氧化钠能与二氧化碳反应产生氧气,可用于高空飞行或潜水的供氧剂D.煤的干馏是化学变化,煤的气化和液化是物理变化5、下列叙述不正确的是( )A.10mL质量分数为98%的H2SO4用10mL水稀释后;H2SO4的质量分数大于49%B.配制0.1 mol·L-1的Na2CO3溶液480mL,需用500ml容量瓶C.在标准状况下,将22.4L氨气溶于1L水中,得到1mol·L-1的氨水D.向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变) 6.设N A为阿伏伽德罗常数的值。
下列说法不正确的是()A.标准状况下,5.6LCl2与足量NaOH反应转移的电子数为0.25 N AB.将2.24 L(标准状况下)CO2通入1 L 0.15 mol·L-1的NaOH溶液中,所得CO2-3和HCO-3物质的量均为0.05 mol(不考虑水解、电离)C.0.01 mol Mg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数目为0.02N A D.常温常压下,Na2O2与足量CO2反应生成2.24 L O2,转移电子数为0.2N A 7、能正确表示下列反应的离子方程式是()A.在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+===4Fe3++2H2O B.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO-3+Ba2++2OH-===BaCO3↓+2H2O+CO2-3C.氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+===Fe2++2H2OD.澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO-3===CaCO3↓+H2O 8.常温下,下列各组离子在指定溶液中一定能大量共存的是()A.水电离产生的c(H+)=10-12 mol·L-1的溶液:K+、Na+、ClO-、I-B.c(H+)/c(OH-)=1×10-12的溶液:K+、AlO-2、CO2-3、Na+C.硫化钠溶液:Cu2+、SO2-3、Br-、H+D.pH=13的溶液:AlO2-、Cl-、HCO-3、SO2-39、如图表示1g O2与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )A.C2H4B.CH4C.CO2D.NO10、下列有关物质的性质与应用相对应的是()A.碳酸钠水解溶液呈碱性,可用于洗去铁屑表面的油污B.铝易发生钝化,可用于作飞机、火箭的结构材料C.炭具有还原性,可用于冶炼钠、镁、铝等金属D.浓硫酸具有强氧化性,可用于干燥二氧化硫气体11.类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是( )12.2016年10月17日,“神舟十一号”在酒泉发射升空,其所用燃料是偏二甲肼(C2H8N2)(其中N的化合价为-3)和四氧化二氮(N2O4),发生反应:C2H8N2+ 2N2O4=2CO2+3N2+4H2O。
下列有关叙述正确的是A.该燃料绿色环保,在燃烧过程中不会造成任何环境污染B.每有0.6 mol N2生成,转移电子数目为2.4N AC.N2既是氧化产物又是还原产物,CO2既不是氧化产物也不是还原产物D.该反应中N2O4是氧化剂,偏二甲肼是还原剂13.在200 mL 含Mg2+、Al3+、NH4+、H+、Cl-的溶液中,逐滴加入5 mol·L-1 NaOH 溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。
下列叙述不正确...的是A.原溶液中c(Cl-)=0.75 mol·L-1B.x—y=0. 01 molC.原溶液的pH=1 D.原溶液中n(Mg2+)∶n(Al3+)=5∶114、将氧气、甲烷、过氧化钠放入封闭容器中,在150℃条件下用电火花引发反应后,恰好完全,容器内压强为零,由此得出混合物中甲烷、氧气、过氧化钠的物质的量之比为()A、1:1:5B、1:2:6C、2:1:6D、2:3:6中物质含有同种元素,它们之间存在如下转化关系:,下列推断错误的是()A.若甲为氯气,则丁可以是铁B.若甲为铁,则丁可以是氯气C.若甲为氢氧化钠,则丁可以是二氧化碳D.若甲为二氧化碳,则丁可以是氢氧化钠16.向仅含Fe2+、I-、Br-的溶液中(忽略由水电离出的H+和OH-)通入一定量的氯气,溶液中这三种离子物质的量的变化如图所示。
下列说法中不正确的是()A.③代表Br-的变化情况B.①代表I-的变化情况C.m的数值等于9D.原混合溶液中n(FeBr2)=3 mol第Ⅱ卷(共52分)二、非选择题(共52分)(请把标准答案写在答题纸的相应位置,注意写清题号。
)17、(19分)已知:A为含金属离子的淡黄色固体化合物,E、X为空气中常见气体,A、B、C、D含有相同的金属离子,其转化关系如下图(部分产物已略去)。
(1)这种金属离子的离子结构示意图为____________。
(2) 请写出A的电子式______________________________________。
常温常压下,15.6 g A与足量的水充分反应放出热量a kJ,写出该反应的热化学方程式为_________________________________________________________。
(3)①D常用于一种泡沫灭火器,构造如图。
内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火。
从液态试剂在灭火器中长久放置和快速灭火两个角度分析,则a中盛________,b中盛________,反应的化学方程式为________________________②写出D溶液与偏铝酸钠溶液反应的离子方程式为__________________________。
(4)将一定量的气体X通入2 L B的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。
请回答:b点溶液中所含溶质的化学式为___________,物质的量之比为__ ____,请写出b点溶液中离子浓度由大到小的顺序_____________________________________。
(5)将C溶液与氢氧化钡溶液混合可得不溶物F. F的Ksp=2.5×10−9. 现将该不溶物放入0.5mol⋅L-1的BaCl2溶液中,其Ksp___(填“增大”、“减小”或“不变”),组成不溶物F的阴离子在溶液中的浓度为___mol⋅L-1.18、(10分)2015年8月12日天津港特大爆炸事故,再一次引发了人们对环境问题的关注。
据查危化仓库中存有大量的钠、钾、白磷(P4)、硝酸铵和氰化钠(NaCN)。
(1)白磷有毒能和氯酸溶液发生氧化还原反应:3P4 + 10HClO3 + 18H2O = 10HCl + 12H3PO4,该反应的氧化产物是,若有1 mol P4参加反应转移电子为mol。
(2)氰化钠(NaCN)是一种化工原料,用于基本化学合成、电镀、冶金和有机合成医药、农药及金属处理等方面。
①已知:25℃时,HCN的电离平衡常数K a=6.2×10-10,H2CO3在25℃时的电离平衡常数是K a1= 4.5×10-7、K a2 = 4.7×10-11,则向NaCN溶液通入少量CO2反应的离子方程式是:。
②常温下,氰化钠能与过氧化氢溶液反应,生成碳酸氢钠和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。
该反应的化学方程式是:。
③工业上用氨气制备硝酸,将一定质量的铁粉加入到100mL某浓度的稀硝酸中充分反应后,容器中剩余m1 g铁粉,此时共收集到NO气体896mL(标准状况)。
然后向上述混合物中加入稀硫酸至不再产生NO为止,容器剩余铁粉m2 g,。
