钯催化交叉偶联反应
第9章 钯催化C-C键交叉偶联反应的机理
C-H活化芳基化反应
1 转移金属化过程是反应的决速步 2 钯不与氢原子直接作用,碱与质子结合后形成卡宾可以 与钯结合形成稳定的环状过渡态 3 Concerted metalation deprotonation (CMD)机 理
实用文档
2.3 还原消除
trans
cis
cis
1 只有顺式产物会进行还原消除 2 还原消除过程不可逆 3 过渡态能垒大小:vinyl < Ph < ethynyl < Me, 马来酰胺 < “empty” < ethylene < PMe3 ≈ MeCN 4 能垒大小与π电子接受能力成反比,因此π电子接受能力差的配体(PMe3)会在还原消除过程前 解离。
实用文档
3. 结论
计算化学 Computational
Chemistry
实验化学 Experimenta l Chemistry
有机反应机理
实用文档
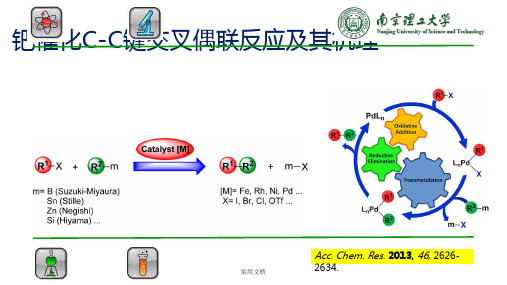
钯催化C-C键交叉偶联反应及其机理
实用文档
Acc. Chem. Res. 2013, 46, 26262634.
1. 钯催化C-C键交叉偶联反应
实用文档
Angew. Chem. Int. Ed. 2012, 51, 50625085.
实用文档
2. 反应机理
1 氧化加成
2 转移金属化
3 还原消除
存在问题:
1 缺乏更为具体深入的理论和验证研究。 2 对于具体的因素和条件对于反应的影响缺乏明确 和系统解释和依据,如配体、金属和底物的类型 对于反应的影响。
实用文档
2.1 氧化加成
协同机理: 1 构型保持 2 气相反应 3 某些极性溶剂
SN2机理: 1 构型反转 2 液相反应
钯催化的交叉偶联反应——2010诺贝尔化学奖简介

产治疗高血压 、 肾脏病等方 面的药 物 。 1本 医药 公司用 3
铃木 反应生产 的 降压 药 .0 9年在 1本 国 内就有 10 20 3 40
亿 1 ( 10 3 约 2 亿人 民币 ) 元 的销售额。电子领域也开始瞩
目“ 钯催 化的交叉偶 联反应 ” 相关成 果不 断被推 出 , , 手
21年 1 00 0月 61瑞典 皇家科学 院诺 贝尔颁奖委员 3 会把今 年 的诺贝尔化学 奖授予 美 国科学家 7 9岁的理 查 德一 赫克 ( i a ek 、 Rc r H c ) 1 hd 3本科学 家 7 5岁 的根岸英 一 ( iih E—ci ei i N g h)和 1本科学家 8 的铃木 章( kr s 3 0岁 A i a
铃木章 。 本公 民。9 0 出生于 1本北海道 。9 9 3 1 13 年 3 15 年在北 海道大学获得博士学位 。16 9 3年一 9 5 , 16 年 铃木 章在美 国普渡大学赫伯特 ・ 布朗教授指导下完成 博士后
研究 。 9 3 17 年起在北海道大学任教授。17 年 , 明“ 99 发 铃 木反应” 。铃木教授 的论文数量不多 。 且大都 以 1文的形 3 式发表在 了 1本 的学术 刊物 上。但 是 . 3 他的研究非 常严 密 , 出来的结果经得起反 复推 敲。为 了证实 自己的研 做 究结果具有可重复性 . 铃木教授不 惜购买全套 的新实验
尔化学奖的赫伯特 ・ 布朗( re rw ) 9 7 , He rB o n 。17 年 发明 bt “ 根岸反应” 。根岸现为美 国普 渡大学化学教授。当根岸 教授在大教 室照常讲授他 的课程 “ 有机化合物 的性质 ”
一
者, 真可谓名师出高徒。
二、 有机合成 中的钯催化交叉偶联反应
钯催化交叉偶联反应

钯催化的交叉偶联反应一、偶联反应综述1.交叉偶联反应偶联反应,从广义上讲,就是由两个有机分子进行某种化学反应而生成一个新有机分子的过程。
狭义的偶联反应是涉及有机金属催化剂的碳-碳键生成的反应,根据类型的不同,又可分为自身偶联反应和交叉偶联。
交叉偶联反应是一个有机分子与另一有机分子发生的不对称偶联反应。
2.碳碳键形成的重要性新碳-碳键的形成在有机化学中是极其重要的。
人们了解了天然有机物质的结构和性能,并根据有机物质的结构,通过碳原子组装成链,建立有机分子,最终实现天然有机物质的人工合成。
目前为止,人类已经利用有机合成化学手段创造出几千万种物质,且越来越多的有机物质已经广泛应用到制药、建材、食品、纺织等人类生活领域,我们的生活也几乎离不开有机物了。
合成药物、塑料等有机物质时,需要用小的有机分子将碳原子连接在一起构建新的复杂大分子,因而有机合成中高效的连接碳-碳键的方法是有机合成化学中的重要工具。
从以往该领域诺贝尔化学奖的授予情况也可以看出合成新碳-碳键的重要性:1912年维克多·格林尼亚因发明格林尼亚试剂——有机镁试剂获奖,1950年迪尔斯和阿尔德因发明双烯反应迪尔斯-阿尔德反应获奖,1979年维蒂希与布朗因发明维蒂希反应共同获奖,2005年伊夫·肖万、罗伯特·格拉布、理查德·施罗克因在有机化学的烯烃复分解反应研究方面作了突出贡献获奖。
3.有机合成中的钯催化交叉偶联反应随着时代发展,合成有机化学的研究愈加深入,20世纪后半期,科学家们发现了大量通过过渡金属催化来创造新有机分子的反应,促使有机合成化学快速发展。
特别是赫克、根岸英一和铃木章发现的钯催化交叉偶联反应,为化学家们提供了一个更为精确有效的工具。
三位科学家发现的钯催化交叉偶联反应中都使用了金属钯作为反应的催化剂,当碳原子与钯原子连在一起时,钯原子唤醒了“懒惰”的碳原子但又不至于使它太活泼,于是形成温和的碳-钯键,在反应过程中,钯原子又可以把别的碳原子吸引过来,形成另一个金属-碳键,此时两个碳原子都连接在钯原子上,它们的距离足够接近而发生反应,生成新的碳-碳单键。
钯催化的偶联反应

AgNO3/KF作用下的Pd催化2-溴噻吩S原子邻位上的C-H键选择性偶联反应摘要:溴噻吩的衍生物与芳基碘在加入了钯的硝酸银/氟化钾催化剂的催化下发生C—H键的偶联反应,而C—Br键未发生变化。
这些含有C —Br键的偶联产物在钯的进一步催化下使溴噻吩和芳基碘的C—C键相连接从而得到理想的产量。
引言:狭义上的偶联反应是涉及由基金属催化剂的C-C键生成的反应,根据类型不同,可分为交叉偶联反应和自身偶联反应。
交叉偶联反应是一个有机分子与另一有机分子发生的不对称偶联反应。
例如:烯丙基锂与2-氯辛烷可以发生交叉偶联反应生成4-甲基-1-癸烯。
格利雅试剂、有机铝、有机锌、有机锡、有机铜、有机铅、有机汞等多种有机金属化合物也都可以与卤化烷等烃基化试剂发生交叉偶联反应,生成相应的不对称烃,是合成不对称烃,特别是单烷基芳烃和含有三级碳原子的链烃的有效方法。
交叉偶联反应的范围很广,像芳烃重氮盐与苯酚或N,N-二甲基苯胺的偶联反应,也属于交叉偶联反应。
正文:芳香族化合物与有机卤化物的C-H键取代反应和那些含金属试剂与相同的有机卤化物的偶联反应相比,在有机合成中更有前景。
【1】相比之下,C-H键上的直接反应将有利于含有不同种类的官能团的衍生物的合成,并且,反应也会加强合成中原子的效应。
我们注意到噻吩衍生物的偶联反应是发生在C-H键上,从而形成了联噻吩。
在添加了AgF后,反应效率得到了提高。
【2】当噻吩与2-溴噻吩反应生成正联溴噻吩时,仍然是C-H键发生偶联,而C-Br键未发生变化。
我们的注意力集中到溴噻吩衍生物C-H键的交叉耦合上,来介绍噻吩环上的取代基。
【3】溴噻吩上的C-H键偶联,如果可以通过C-Br键的反应而进一步改变偶联产物,那么C-H键和C-Br键的偶联反应的相互结合将得到一种新的合成取代噻吩的方法。
这将把人们的注意力都吸引到设计更先进的有机金属材料来揭示液晶、光发射和有机半导体的特点。
【4】在此,我们报告一个新的催化剂系统—AgNO3/KF,它有助于提高钯催化下溴噻吩衍生物C-H键的取代反应发的效率。
有机合成中钯催化下的交叉偶联反应

有机合成中钯催化下的交叉偶联反应-2010年诺贝尔化学奖简介陈明华( 兴义师范学院化学生物系,贵州兴义 562400)摘要:介绍了2010年诺贝尔化学奖的科学背景,即“有机合成中钯催化下的交叉偶联反应”的产生、发展和应用,体现了有机化学已经发展成为一门艺术形式,在这个形式下,科学家们在试管里创造性的产生出不可思议的化学物质的过程。
关键词:钯催化剂;交叉偶联反应;赫克反应;铃木反应;根岸反应Palladium-Catalyzed Cross Couplings in Organic SynthesisCHEN Ming-Hua(Department of Chemistry and Biological, Xingyi Normal College, Xingyi, Guizhou 562400)Abstract: This paper introduces scientific background of the Nobel Prize in Chemistry for 2010, it’s palladium-catalyzed cross couplings in organic synthesis.And this fack had been presents that “Organic chemistry has developed into an art form where scientists produce marvelous chemical creations in their test tubes”.Key words: palladium catalyst; cross-coupling reaction; heck reaction; suzuki reaction; negishi reaction2010年10月6日,瑞典皇家科学院决定授予美国特拉华大学(University of Delaware) 理查德-赫克(Richard F. Heck), 普渡大学(Purdue University)根岸荣一(Ei-ichi Negishi)和日本北海道大学(Hokkaido University)的铃木彰(Akira Suzuki)三位教授2010年的诺贝尔化学奖,以表彰他们在“有机合成中钯催化下的交叉偶联反应”作出的贡献[1]。
钯催化的交叉偶联反应——2010年诺贝尔化学奖获奖工作介绍

2011年第31卷 有 机 化 学V ol. 31, 2011 * E-ma i l: nxwang@ma i l.iReceived December 9, 2010; revised and accepted March 10, 2011.·学术动态·钯催化的交叉偶联反应——2010年诺贝尔化学奖获奖工作介绍王乃兴(中国科学院理化技术研究所 北京 100190)摘要 钯催化的交叉偶联反应是非常实用的合成新方法. 文章给出了Heck 反应、Negishi 反应和Suzuki 反应的概念, 对其反应机理作了详细的说明, 并对其在复杂化合物和天然产物全合成中的应用作了评价. 关键词 钯催化; Heck 反应; Negishi 反应; Suzuki 反应Palladium-Catalyzed Cross-Coupling Reactions —Introduction of Nobel Prize in Chemistry in 2010Wang, Naixing(Technical Institute of Physics and Chemistry , Chinese Academy of Sciences , Beijing 100190)Abstract Palladium-catalyzed cross-coupling reactions provide chemists with a more precise and efficient new methodologies. The concepts of the Heck reaction and Negishi reaction as well as Suzuki reaction are given, the reaction mechanisms are proposed, and applications of these reactions in the total synthesis of natural products are commented.Keywords palladium-catalyzed; Heck reaction; Negishi reaction; Suzuki reaction2009年10月6日, 瑞典皇家科学院宣布, 美国科学家Richard F. Heck(理查德 赫克)、日本科学家Ei-ichi Negishi(根岸英一)和Akira Suzuki(铃木章)共同获得今年的诺贝尔化学奖. 美国教授Richard F. Heck, 1931年出生于美国的斯普林菲尔德, 1954年在美国加利福尼亚大学洛杉矶分校获得博士学位. 随后他进入瑞士苏黎世联邦工学院从事博士后研究, 后在美国特拉华大学任教, 于1989年退休. Richard F. Heck 现为特拉华大学名誉教授. Ei-ichi Negishi 教授是日本人, 1935年出生于中国长春, 1958年从东京大学毕业后进入帝人公司, 1963年在美国宾夕法尼亚大学获得博士学位, 现任美国普渡大学教授. Akira Suzuki 也是日本人, 1930年出生于日本北海道鹉川町, 1959年在北海道大学获得博士学位, 随后留校工作了一段时间. 1963年到1965年, Akira Suzuki 在美国普渡大学从事了两年的博士后研究工作. Akira Suzuki 于1973年任北海道大学工学系教授, 现在是北海道大学名誉教授.钯催化的交叉偶联反应是一种可靠而又实用的工具, 对有机合成具有长久和深远的影响力, 该反应得到了合成化学工作者的普遍应用.笔者于2004年在《有机反应——多氮化物的反应及有关理论问题(第二版)》的第4.13节中列举了5个较新的人名反应[1], 其中有Heck 反应、Negishi 反应和Suzuki 反应. 对其定义分别为: Heck 反应是钯催化下, 不饱和有机卤化物或三氟磺酸酯与烯烃进行的偶联反应. Negishi 反应是钯催化下的不饱和有机锌试剂和芳基或乙烯基卤化物等进行偶联的反应. Suzuki 反应是钯催化下不饱和有机硼试剂和芳基或乙烯基卤化物等进行偶联的反应. 这是钯催化的交叉偶联反应的基本概念. 最初的Suzuki 反应还需要在无氧无水的条件下来进行, 后来发展的一些反应条件已经无需无氧无水操作了.这几种钯催化的交叉偶联反应机理不尽相同, 对机1320有 机 化 学 V ol. 31, 2011理的说明也不止一种, 一些可能的机理对研究生也较难接受. 如Heck 反应, 即使一些已经出版的专门论述人名反应的专著也较为简略[2,3] Heck 本人最先提出的Heck 反应机理是应该接受的.1 反应机理1.1 Heck 反应机理目前关于Heck 反应机理描述较多, 但一些机理过于简单, 一些机理的描述很难让有机化学家接受. 笔者认为Jutand 等[4]最近在Heck 反应的专门著作中总结的Heck 反应机理最为贴切和容易接受(Scheme 1). 这个详细的反应过程实际上是Heck 首先建议的.Scheme 1理解各步过程并不困难. 关键是整个机理中左下角画箭头处, 表示出一个负氢迁移过程, 双键上的电子是由钯直接提供的.Heck 反应的机理主要分为四个步骤:(1)氧化加成. 上式催化循环的第一步是芳基卤和Pd(0)的氧化加成, Titton 报道的芳基卤和Pd 0(PPh 3)4的作用支持了氧化加成步骤的机理, Titton 还报道了芳基卤活性次序: ArI >ArBr >>ArCl.(2)烯烃插入. 氧化加成给出反式的σ芳基Pd(II)卤化物ArPdXL 2, 脱去一个PPh 3配体后与烯烃配位, 再经过烯的顺式插入, 得到σ烷基Pa(II)卤化物[5,6], 读者可以参照上述催化循环机理图.(3) β负氢消除. 上述催化循环机理图中的σ烷基Pa(II)卤化物有一个C —C 键内旋转, 结果使得β氢原子(与sp 3碳原子相连)和Pd 原子处于顺式位置, 接着产生了顺式的β负氢消除. 这个顺式的β负氢消除反应会是一个可逆的过程.(4)还原消除. 钯催化的偶联反应产物(与芳基直接相连的烯烃衍生物)游离产生以后, H —Pd(II)的卤化物再经过一个可逆还原消除过程, 再生出具有催化活性的Pd(0)的络合物. 碱性的辅助催化剂通过粗灭产生的卤化氢, 促使还原消除过程向Pd(0)络合物催化剂方向移动.Heck 不仅发现了这个钯催化的偶联反应, 而且对其机理做出了透彻的阐述. Heck 提出的氧化加成、烯烃插入、β负氢消除、还原消除这四个主要步骤在实验中都得到了证实. β负氢消除是一个重要过程, 钯提供了一对电子形成了双键. 最近认为β负氢消除通过一个顺式消除过程. 实际上Heck 反应不能仅看作交叉偶联反应, 它只是偶联反应一种.机理中涉及一些不同的Pd(0)和Pd(II)的中间体, 这些中间体的结构和活性依靠实验条件, 钯催化剂可以是Pd(0)的络合物, 如Pd(PPh 3)4, 可以是Pd(OAc)2等. 当Pd(OAc)2作为催化剂时, 需要加入1,3-二(二苯基膦基)丙基(dppp), 首先形成Pd(OAc)2(dppp), 再得到离子型络合物Pd 0(dppp)(OAc)- [7], Pd 0(dppp)(OAc)-分解得到Pd(0)络合物Pd(dppp). 1.2 Suzuki 反应机理笔者[8]曾研究过Suzuki 反应, 利用苯硼酸和2,2'-二溴-5,5'-二噻吩通过催化量的金属钯络合物Pd(PPh 3)4进行交叉偶联反应(Eq. 1).当时采用的反应条件还是无氧无水操作[8], 产物熔点是145 ℃, 产率为51%.笔者在文献的基础上[9~11], 提出了一个离子型的反应机理, 该论文发表在一个国外化学期刊上[8]. 该反应可能的机理由三个主要步骤完成的: (a)氧化加成; (b)硼试剂参与; (c)还原消除.(1)氧化加成. 反应过程中, Pd(0)被加到有机卤化物中间, 有机卤化物中的碳原子通过极性转换由原来荷正电变为荷负电, 钯原子被氧化为Pd(II) (Scheme 2). 氧化加成的过程是速率决定步骤, 反应中, 有机卤化物的活性按卤原子如下次序递减: I >Br >>C.N o. 8王乃兴:钯催化的交叉偶联反应——2010年诺贝尔化学奖获奖工作介绍1321Scheme 2(2)硼试剂参与. 接着, 硼试剂中的C —B 键异裂, 碳原子荷负电, 形成的芳基负离子与钯正离子结合为ArPdAr', 而游离出来的卤离子(X -)与硼正离子配位得到XB(OH)2 (Eq. 2).(3)消除反应. 最后是还原消除过程, 钯有机物分解, 形成新的C —C 键, 金属钯游离出来, 再与PPh 3络合, 再生出活性钯催化剂Pd(PPh 3)4, 完成了催化过程.Scheme 3笔者在当时研究苯硼酸和2,2'-二溴-5,5'-二噻吩通过Pd(PPh 3)4催化进行的交叉偶联反应, 发现该反应采用弱碱Ba(OH)2作为辅助催化剂比其它强碱反应快, 收率高, 甚至用碳酸钾代替Ba(OH)2也往往引起副产物增加. 笔者采用了甲醇和甲苯(V ∶V =1∶1)的混合溶剂. 就溶剂效应而言, 甲醇溶剂对反应有利. 在反应过程中的氧化加成阶段, 甲醇产生的烷氧基负离子MeO -能够置换配位在钯上的卤负离子, 容易生成ArPdOR 中间体(Scheme 4).Scheme 4RPdOMe 的形成被认为是一个重要的中间体, 曾被分离得到过[12,13]. 1.3 Negishi 反应机理笔者曾制备了有机锌试剂[8], 采用一锅反应方法, 利用溴锌苯和2,5-二溴噻吩通过催化量的金属钯络合物Pd(PPh 3)4进行交叉偶联反应(Scheme 5).Scheme 5与Suzuki 反应相比, 利用Negishi 反应合成目标化合物, 产率没有Suzuki 反应高[8,14].Negishi 反应的机理与Suzuki 反应非常类似, 也是通过氧化加成、有机锌试剂(亲核试剂)参与和还原消除的三个主要步骤进行的, 下面用离子反应历程作以描述(Eq. 3, Schemes 6, 7):(1)氧化加成Scheme 6(2)有机锌试剂参与(3)消除反应Scheme 7Pd(0)游离出来, 再与PPh 3络合再生出催化剂Pd(PPh 3)4, 完成了催化循环.另外需要说明的是, 交叉偶联反应有许多种, 一些虽然没有得到诺贝尔化学奖, 但应用价值还是比较高, 例如Songashira 反应. Sonogashira 反应是钯配合物催化的卤代芳烃或者卤代烯烃与末端炔烃的交叉偶联反应, 它是一种合成芳炔、烯炔和炔酮等化合物的有效方法. 其反应如Eq. 4.Sonogashira 反应的本质是PdCl 2与CuI 复合催化剂催化末端炔烃与碘、溴代芳或者烯烃的交叉偶联反应. 2007年发表在Chem. Rev.上的Sonogashira 反应机理, 说明了铜盐作为助催化剂的过程, 是一个容易接受的机理(Scheme 8)[15].铜盐作为助催化剂的作用一些文献也作了报道[16]. 近年来Sonogashira 反应的应用报道较多, 读者可以参考相关文献[17~19].2 结束语Heck 反应、Negishi 反应和Suzuki 反应, 代表了钯催化的交叉偶联反应的最高成就, 反应非常新颖独特,1322有机化学V ol. 31, 2011Scheme 8确实在有机合成方法学的最前沿取得了重大突破, 这些原创性的成就卓有建树, 这些新方法首先在有机合成领域得到了普遍应用, 对发展有机合成的策略和技巧产生了长久和深远的影响.人类健康对特效新药的发展不断提出更高的要求, 天然产物作为先导药, 在这方面寄托了人们的无限期望[20]. 近年来, 海洋天然产物的生物医学活性引起了人们的高度重视. 海绵、珊瑚以及海洋微生物的次生代谢的天然产物, 结构新颖而活性显著, 已经成为人们挖掘具有自主知识产权的创新先导抗肿瘤等新药的战略新领域. 人工全合成这类复杂的化合物和天然产物对人类来说是一种艰难的挑战, Heck反应、Negishi反应和Suzuki反应的新方法无疑在这方面会发挥出巨大的作用.近年来, 围绕Heck反应、Negishi反应和Suzuki反应, 化学家发展了一些新的反应方法和条件, 如Ni代替Pd进行催化的交叉偶联反应. Iyer等[21]报道了Cu催化(CuI催化剂)的Heck反应, 相对Pd和Ni催化剂更为经济. 最近, Darcel等[22]报道了Fe催化的Suzuki反应, 产率较高. Nakamura等[23]不久前报道了Fe催化的Negishi 反应, 产物收率高且有立体专一性. 反应条件已经从开始需要无氧无水操作到现在可以在水相反应体系中进行. Chao等[24]报道了在水合溶剂中进行Suzuki反应的研究结果, 产物能够获得中等以上的收率. Bach等[25]在Tetrahedron的一篇文章中(其参考文41), 对笔者关于Suzuki反应和Negishi反应的报道作了一些介绍. 相信以后还会有一些新的关于催化的交叉偶联反应的研究论文不断发表出来.Heck不仅开创了著名的Heck反应, 而且他提出的有机化学反应机理也非常之透彻和精到, 可见他的有机化学之功底和对该方法的深刻的理解. 可是, Heck在完成Heck反应研究之后, 一度连科研经费都没有, 甚至不得不离开科学界. 笔者刚在德国应用化学刊物(Angew. Chem. Int. Ed. 2010,49, 2092)看到一篇关于德国合成化学教授H. Kunz的作者介绍, H. Kunz教授列出了他的五篇文章, 其中第二篇文章发表在Tetrahedron 上, 第三篇发表在Synthesis上. 笔者在中国科学院研究生院为硕博连读生讲授“有机反应”专业课, 学生对Heck反应、Negishi反应和Suzuki反应的兴趣非常浓厚. 希望年青一代的学者, 通过研究和借鉴Heck反应、Negishi反应和Suzuki反应, 提升我国在有机合成方法学方面的整体水平.在这篇简介文章结束时, 笔者再介绍几篇关于钯催化的交叉偶联反应的代表性综述文章. 一篇是Suzuki本人1995年在Chem. Rev.上的综述[26], 希望有兴趣的读者参阅. 另外3篇对相关钯催化的交叉偶联反应最新进展作了详细综述[27~29], 希望读者特别是青年学者能够继续深入学习和掌握这一研究领域. 最近, Suzuki和Negishi[30~31]还分别发表了他们的诺贝尔化学奖获奖演说. 就在这篇文章付印之际,作者又读到了一篇最新的关于非对映选择性的Negishi反应的论文, 该方法为此类反应的立体控制开拓了又一个新生面[32]. References1 Wang,N.-X. Organic Reac tions—The Reac tion of Polyni-trogen Compounds and Some Theoretic Questions, 2nd ed., Chemical Industry Press, Beijing, 2004, pp. 165~171 (in Chinese).(王乃兴, 有机反应—多氮化物的反应及有关理论问题(第二版), 化学工业出版社, 北京, 2004, pp. 165~171.)2 Li, J. J. Name Reactions, Springer, New York, 2006, p. 285.3 Kürti, L.; Czakó, B. Strategic Applications of Named Reac-tions in Organic Synthesis, Elsevier Academic Press, 2005, p. 196.4 Jutand, A. In The Mizoroki-Hec k Reac tion, Ed.: Oestreich,M., Wiley, United Kingdom, 1999, pp. 1~5.5 Dieck, H. A.; Heck, R. F. J. Am. Chem. Soc.1974, 96, 1133.6 Ziegler, C. B.; Heck, R. F. J. Org. Chem. 1978, 43, 2941.7 Kozuch, S.; Shaik, S.; Jutand, A.; Amatore, C. Chem. Eur. J.2004, 10, 3072.8 Wang,N.-X. Synth. Commun. 2003, 33, 2119.9 Anderson, C. B.; Burreson, B. J.; Michalowski, J. T. J. Org.Chem. 1976, 41, 1990.10 Zask, A.; Helquist, P. J. Org. Chem. 1978, 43, 1619.11 Aliprantis, A. O.; Canary, J. W. J. Am. Chem. Soc. 1994,116, 6985.12 Yoshida, T.; Okano, T.; Otsuka, S. J. Chem. Soc., DaltonTrans. 1976, 993.13 Grushin, V. V.; Alper, H. Orgnometallics1993, 12, 1890.14 Wang,N.-X. Chin. . Chem. 2004, 24, 350 (in Chi-N o. 8 王乃兴:钯催化的交叉偶联反应——2010年诺贝尔化学奖获奖工作介绍1323nese).(王乃兴, 有机化学, 2004, 24, 350.)15 Chinchilla, R.; Nájera, C. Chem. Rev. 2007, 107, 874.16 Doucet, H.; Hierso, J. C. Angew. Chem., Int. Ed. 2007, 46,834.17 Gelman, D.; Buchwald, S. L. Angew. Chem., Int. Ed. 2003,42, 5993.18 Saha, D.; Dey, R.; Ranu, B. C. Eur. J. Org. Chem. 2010,6067.19 Karpov, A. S.; Merkul, E.; Rominger, F.; Müller, T. J. J.Angew. Chem., Int. Ed. 2005, 44, 6951.20 Harmata, M. Strategies and Tac tic s in Organic Synthesis,Elsevier, Oxford, 2010.21 Iyer, S.; Ramesh, C.; Sarkar, A.; Wadgaonkar, P. P. Tetrahe-dron Lett. 1997, 38, 8113.22 Bźziera, D.; Darcela, C. Adv. Synth. Catal. 2009, 351, 1732.23 Hatakeyama, T.; N akagawa, N.; N akamura, M. Org. Lett.2009, 11, 4496.24 Cho, S. Y.; Kang, S. K.; Ahn, J. H.; Ha, J. D.; Choi, J. K.Tetrahedron Lett. 2006, 47, 5237.25 Schröter, S.; Stock, C.; Bach, T. Tetrahedron2005, 61,2245.26 Norio Miyaura, N.; Suzuki, A. Chem. Rev. 1995, 95, 2457.27 Roglans, A.; Pla-Quintana, A.; Moreno-Mañas, M. Chem.Rev. 2006, 106, 4622.28 Martin, R.; Buchwald, S. L. Acc. Chem. Res. 2008, 41,1461.29 Denmark, S. E.; Regens, C. S. Acc. Chem. Res. 2008, 41,1486.30 Suzuki, A. Angew. Chem., Int. Ed.2011, 50, 6723.31Negishi, E. Angew. Chem., Int. Ed.2011, 50, 6738.32 Seel, S.; Thaler, T.; Takatsu, K.; Zhang, C.; Zipse, H.;Bernd, F.; Straub, B. F.; Mayer, P.; Knochel, P. J. Am. Chem.Soc. 2011, 133, 4774.(Y1012093 Li, L.)。
有机合成钯催化交叉偶联反应(精选文档)

1.格氏试剂——拉开钯催化交叉偶联反应的序幕
有机合成化学所构造出来的物质大部分都是以碳胳为骨架所构建起来的,然而碳原子本身十分稳定,在化学反应中并不活泼。因此化学家们希望通过各种化学反应,来激活碳原子,使其更容易参与到反应中并与其它碳原子相连,构造更
复杂的有机物。通过多年的尝试与努力, Grignard (格林尼亚发明了有机镁试剂(即格氏试剂,并利用其活化了碳原子,成功将碳原子连接在一起。以下为利用格氏试剂所进行的烷基化反应:
赫克反应与格氏反应相比,具有更好的化学选择性,减少反应的副产物,而且赫克反应在常温下进行,反应条件温和,对于工业生产具有重要的应用价值。不过赫克反应的局限之处在于,它往往只能用于有机合成中碳碳单键的合成,在合成一些更大的分子时会显示出其缺陷及产生较多的副产物。化学家们并不满足于停留在当前的成果中,而是孜孜不倦地进一步改进钯催化交叉偶联反应。
为铃木反应。
铃木反应与根岸反应相
似,均经历了三个过程:氧
构建单键最重要的反应之
一,并以他自己的名字赫克对
反应命名。
赫克反应的反应机理如
下(见右图:反应开始,活泼
的钯Pd(0催化剂与卤代烃发
生被称为氧化-加成的反应,
在这步反应中,生成了R-Pd-X ,钯的氧化态形式上从(0转化为(Ⅱ ,也就意味着生成了Pd-C键;第二步,烯烃与钯配位,此时烯烃和R基团同时与钯连接,这样就使它们能够相互发生反应;第三步, R基团迁移到烯烃的碳原子上,而钯同时与烯烃的另一个碳原子相连,这一步称为迁移-插入,结果生成了C-C键;第四步, R替换了底物烯烃上的一个氢原子,即通过消除烯烃的β-H得到了一个新的取代烯烃,同时还生成了HPdX ,它随即失去HX得到Pd(0,进入另一次催化循环。
贵金属钯Pd催化的偶联反应

通过调整钯催化剂的反应条件(温度、溶剂、配体、碱和其他添加剂),可使钯催化成为有机化学合成中用途广泛的工具。
其中,钯催化的交叉偶联反应彻底改变了分子的构造方式。
从有机合成和药物化学领域,到材料科学和聚合物化学,交叉耦合已经影响到多个科学领域。
在偶联反应中,钯催化剂不但可以形成C-C、C-O、C-N和C-F等碳键,而且对各种官能团具有很高的耐受性,通常能够提供良好的空间和区域特异性,可以不用引入保护基团。
常用的偶联反应包括Heck偶联、Suzuki偶联、Stille偶联、Hiyama偶联、Sonogashira偶联、Negishi偶联、Buchwald-Hartwig胺化等等。
具体反应如下所示:1、Negeshi偶联反应(C-C) [1](其中,R/R’可以是烷基、烯基、芳基、烯丙基、炔基或炔丙基,X/X’可以是氯、溴、碘或其他基团,催化剂是钯)2、Suzuki偶联反应(C-C) [2](其中,R可以是烯基,芳基或烷基,R’可以是烯基,芳基、炔基或烷基,Y可以是烷基,羟基或者氧烷基,X可以是氯、溴、碘或三氟甲磺酸)3、Stille偶联反应(C-C) [3](其中,R可以是烯基、芳基、酰基,R’可以是烯基、芳基或者烷基,R’’可以是烷基,X可以是氯、溴、碘或者三氟甲磺酸)4、Buchwald–Hartwig偶联反应(C-N/C-O)[4](其中,R是芳基,R’可以是邻、间芳基或烷基,R”可以是烷基或芳基,X可以是氯、溴、碘或者三氟甲磺酸)5、Heck偶联反应(C-C) [5](其中,R可以是烯基、芳基和不含有β氢的烷基,R’可以是烯基,芳基和烷基,X可以是氯、溴、碘、三氟甲磺酸、对甲基苯磺酰氯或者N2+)6、Sonogashira偶联反应(C-C) [6](其中,R可以是烯基或者芳基,R’可以是H、炔基、芳基、烷基或者硅烷基,X可以是氯、溴、碘或者三氟甲磺酸)。
suzuki交叉偶联反应

suzuki交叉偶联反应交叉偶联反应是有机化学中一种重要的反应类型,通常用于合成有机分子中的碳—碳键。
suzuki交叉偶联反应是其中最常见和广泛应用的一种,它以四氢呋喃为溶剂,在存在钯催化剂和有机硼试剂的条件下进行。
本文将系统介绍suzuki交叉偶联反应的反应机理、应用领域以及相关的实验条件。
suzuki交叉偶联反应的反应机理可以分为两个主要步骤:(1)钯与有机硼试剂发生配位,形成一个活性的钯配合物;(2)该钯配合物与称为亲电试剂的底物发生交叉偶联反应,生成所需的产物。
在这个反应中,钯是关键的催化剂。
它可以与有机硼试剂形成一个烯烃配合物,其中钯与硼之间形成了一个稳定的钯—硼键。
这个钯—硼配合物可以在反应溶剂中与亲电试剂反应,发生碳—碳键的形成。
最终,用于交叉偶联反应的有机硼试剂和亲电试剂都会耗尽,而生成的产物则是两者的结合物。
suzuki交叉偶联反应被广泛应用于有机合成中。
因为它能够有效地构建复杂的有机分子骨架,并且具有较高的化学选择性和几乎没有废气产生。
这使得suzuki交叉偶联反应成为药物合成、天然产物合成以及有机电子材料合成等领域中的重要工具。
在实际应用中,suzuki交叉偶联反应通常在四氢呋喃或二甲基亚砜等溶剂中进行。
所需的钯催化剂可以通过还原钯盐与配体进行现场生成,也可以直接购买商用的钯配合物。
有机硼试剂可以使用各种不同的试剂,如芳香硼酸、芳香硼酸酯和芳香硼酸酰胺等。
亲电试剂的选择则取决于所需的化学转化。
此外,suzuki交叉偶联反应还可以在不同的温度下进行,通常在室温或略高温的条件下进行。
反应时间也可以根据底物的性质和反应的需要进行调节。
反应之后,产物可以通过简单的工艺步骤进行分离和纯化。
虽然suzuki交叉偶联反应在有机合成中具有广泛的应用,但也存在一些限制。
特别是,底物中的制约基团可能会对反应产率和选择性产生影响。
此外,一些复杂的底物可能需要更高的反应条件。
总之,suzuki交叉偶联反应是有机合成领域中一种重要的反应类型。
钯催化偶联反应

钯催化偶联反应钯催化偶联反应是一种重要的有机合成方法,它可以将两个有机物分子通过钯催化剂的作用连接起来,形成新的化合物。
这种反应在有机合成领域中应用广泛,可以用于制备药物、天然产物、高分子材料等。
1. 钯催化偶联反应的基本原理钯催化偶联反应是一种通过钯催化剂促进两个有机物分子之间发生键合的反应。
在这种反应中,钯催化剂作为一个中间体起到了关键作用。
它能够与底物形成络合物,并降低底物之间键结合的能量,从而促进它们之间的反应。
2. 钯催化偶联反应的类型目前已经发现了多种类型的钯催化偶联反应,其中最常见的包括:(1) Suzuki 偶联反应:该反应是将芳香族卤代烃和芳香族硼酸酯或硼酸进行偶联。
该反应具有高效率、选择性好等特点,在制备药物、农药等方面得到广泛应用。
(2) Heck 偶联反应:该反应是将烯烃和芳香族卤代烃进行偶联。
该反应具有高效率、反应条件温和等特点,在制备香料、染料等方面得到广泛应用。
(3) Stille 偶联反应:该反应是将有机锡化合物和芳香族卤代烃进行偶联。
该反应具有高效率、选择性好等特点,在制备药物、天然产物等方面得到广泛应用。
(4) Negishi 偶联反应:该反应是将有机锌化合物和芳香族卤代烃进行偶联。
该反应具有高效率、选择性好等特点,在制备药物、农药等方面得到广泛应用。
3. 钯催化剂的种类钯催化偶联反应中使用的钯催化剂种类多样,常见的包括:(1) 三苯基膦钯催化剂:该催化剂在 Suzuki 偶联反应中常用,具有高效率、选择性好等特点。
(2) 二茂铁基钯催化剂:该催化剂在 Heck 偶联反应中常用,具有高效率、稳定性好等特点。
(3) 二苯基甲酰胺钯催化剂:该催化剂在 Stille 偶联反应中常用,具有高效率、选择性好等特点。
(4) 氯化钯催化剂:该催化剂在 Negishi 偶联反应中常用,具有高效率、稳定性好等特点。
4. 钯催化偶联反应的优缺点钯催化偶联反应具有如下优点:(1) 反应条件温和,适用于多种底物。
钯催化交叉偶联反应

钯催化交叉偶联反应什么是钯催化交叉偶联反应?钯催化交叉偶联反应(Palladium-Catalyzed Cross-Coupling Reaction)是一种重要的有机合成反应。
它是一类碳-碳键构造的反应,是通过将两种不同的碳基官能团或碳碳键连接在一起,以形成新的C-C化合物。
反应机理在钯催化交叉偶联反应中,两个分子的有机基团进行偶联,然后由钯离子起催化作用,生成新的碳碳键。
催化剂形式上是Pd(0)配合物,反应机理如下:1.钯催化剂先通过脱对氢化学计量通常分配Pdcatalyst (I)。
2.钯催化剂进一步和配体形成配合物(PdL2)。
3.配合物和卤代烃发生交换生成过渡态PdL2(RX)。
过渡态中,钯离子与亲电吸引剂的卤素原子形成键;此过程中C-X钩体断裂,形成第一级碳中间体。
4.结合第二个有机基团生成PdL2(RY)介于新的物种。
5.最后的反应产物通常通过还原反应,将钯催化剂还原为Pd(0)。
应用钯催化交叉偶联反应已经成为有机合成中的重要反应之一,广泛应用于制药、化工、材料科学等领域。
其重要应用包括:•制备非对映选择性或对映选择性的C-C连接化合物。
•制备有机材料。
•合成复杂天然产物的合成方法研究。
反应类型钯催化交叉偶联反应可以根据反应物和类型进行分类。
最常用的交叉偶联反应类型是官能团反应 (Functional Group Coupling) 和碳-碳双键偶联反应 (Carbon-Carbon Double Bond Coupling),这些反应分类包括下列:1.骨架化反应 (Fragmentation Reaction)2.偶联反应 (Cross-Coupling Reaction)3.代换反应 (Substitution Reaction)4.重排反应 (Rearrangement Reaction)反应优点由于钯催化交叉偶联反应具有高效性、选择性、重复性和收率高的特点,它已经成为有机化学领域极为重要的反应之一。
钯催化交叉偶联反应

钯催化交叉偶联反应钯催化交叉偶联反应钯催化交叉偶联反应是一类用于碳碳键形成的重要化学反应,在有机合成中应用十分广泛。
简介:为制造复杂的有机材料,需要通过化学反应将碳原子集合在一起。
但是碳原子在有机分子中与相邻原子之间的化学键往往非常稳定,不易与其他分子发生化学反应。
以往的方法虽然能令碳原子更加活跃,但是,过于活跃的碳原子却又会产生大量副产物,而用钯作为催化剂则可以解决这个问题。
钯原子就像“媒人”一样,把不同的碳原子吸引到自己身边,使碳原子之间的距离变得很近,容易结合——也就是“偶联”。
这样的反应不需要把碳原子激活到很活跃的程度,副产物比较少,因此更加精确而高效。
赫克、根岸英一和铃木章通过实验发现,碳原子会和钯原子连接在一起,进行一系列化学反应。
这一技术让化学家们能够精确有效地制出他们需要的复杂化合物。
发展阶段:一、大约100年前,法国化学家维克多·格林尼亚发现,将一个镁原子同一个碳原子偶联在一起,会将额外的电子推向这个碳原子,使得它能够更容易同另外一个碳原子连接在一起。
不过,科学家们发现,这样的方法在创造简单的分子时起到了效果,但是在对更为复杂的分子进行合成时,却在试管里发现了很多并不需要的副产品。
二、早在上世纪60年代,赫克就为钯催化交叉偶联反应奠定了基础,1968年,他报告了新的化学反应——赫克反应,该反应使用钯作为主要的催化剂来让碳原子连接在一起。
三、1977年,根岸英一对其成果进行了精练,他使用一种有机氯化物作为催化剂;两年后,铃木章发现使用有机硼化合物的效果会更好。
应用:如今,“钯催化交叉偶联反应”被应用于许多物质的合成研究和工业化生产。
例如合成抗癌药物紫杉醇和抗炎症药物萘普生,以及有机分子中一个体格特别巨大的成员——水螅毒素。
科学家还尝试用这些方法改造一种抗生素——万古霉素的分子,用来灭有超强抗药性的细菌。
此外,利用这些方法合成的一些有机材料能够发光,可用于制造只有几毫米厚、像塑料薄膜一样的显示器。
钯催化偶联反应的最新进展

3.1 亲电试剂
碘代物成为C-N偶联反应中较难反应的底物之一
OMe MeO i-Pr PCy2 i-Pr PCy2 Oi-Pr
i-PrO
L
Pd
NH2 Cl
i-Pr L1
1: L=L1 4: L=L2 L2
甲苯是碘代物C-N反应较 好的溶剂,因为它对I负 离子的溶解性最小
J. Am. Chem. Soc.,2009, 131, 5766–5768 Buchwald coupling Reaction
39
3.2 亲核试剂:芳香胺类
BrettPhos对于这类碱性较弱 的芳香杂环胺类也具有较高 的催化活性
X. H. Huang, K. W. Anderson, D. Zim, L. Jiang, A. Klapars and S. L. Buchwald, J. Am. Chem. Soc., 2003, 125, 6653–6655.
Buchwald coupling Reaction
12
酰胺和磺酰芳烃反应的首次报道
1160861-60-8
9
0.25g/Aldrich/¥2800 1g/Alfa/¥548
1g/Aldrich/¥533 1g/Aldrich/¥479
Buchwald coupling Reaction
2.1 配体
此配体同时适用Suzuki和Ketone Arylation反应
D. W. Old, J. P. Wolfe and S. L. Buchwald, J. Am. Chem. Soc., 1998,120, 9722–9723. Buchwald coupling Reaction
Org. Lett., 2010, 12,2350–2353
hiyama交叉偶联反应

hiyama交叉偶联反应Hiyama交叉偶联反应是一种重要的有机合成方法,可以用于构建碳-碳键和碳-硅键。
该反应以有机卤化物和有机硅试剂为底物,在催化剂的作用下进行反应,生成交叉偶联产物。
本文将介绍Hiyama交叉偶联反应的原理、应用和研究进展。
一、Hiyama交叉偶联反应的原理Hiyama交叉偶联反应是由日本化学家Hiyama于1988年首次报道的。
该反应属于钯催化的交叉偶联反应,以有机卤化物和有机硅试剂为反应底物,在钯催化剂的作用下,发生碳-硅键的形成。
催化剂通常采用钯配合物,如[Pd(PPh3)4]、Pd2(dba)3和[PdCl2(dppf)]等。
有机硅试剂可以是硅醚、硅酮、硅酸酯等。
在反应中,有机卤化物首先与钯催化剂形成配合物,然后发生氧化加成,生成中间产物。
接着,有机硅试剂与中间产物发生还原消除,生成交叉偶联产物。
整个反应过程中,钯催化剂起到了关键的催化作用,促进了反应的进行。
二、Hiyama交叉偶联反应的应用Hiyama交叉偶联反应在有机合成中具有广泛的应用价值。
首先,该反应可以用于构建碳-碳键。
有机卤化物可以是烷基卤化物、芳基卤化物等,有机硅试剂可以是芳基硅试剂、烷基硅试剂等。
通过Hiyama交叉偶联反应,可以将不同的有机基团连接在一起,构建复杂的有机分子骨架。
Hiyama交叉偶联反应还可以用于构建碳-硅键。
有机硅试剂可以是含有硅醚、硅酮等官能团的化合物,通过与有机卤化物的反应,可以在分子中引入硅基团。
硅基团在有机合成中具有重要的应用,可以参与到后续的反应中,进一步改变分子的性质。
Hiyama交叉偶联反应还可以用于天然产物的合成。
很多天然产物中含有复杂的碳-硅键结构,通过Hiyama交叉偶联反应,可以高效地合成这些天然产物的类似物。
这对于药物研究和化学生物学研究具有重要意义。
三、Hiyama交叉偶联反应的研究进展近年来,研究人员对Hiyama交叉偶联反应进行了深入的研究,不断改进反应条件和催化剂体系,提高反应的效率和选择性。
钯催化烯烃偶联

钯催化烯烃偶联是一种在强碱和钯催化剂的存在下,将烯烃与有机卤化物交叉偶联生成取代烯烃的化学反应。
这种反应类型在合成生物学和有机化学领域有广泛的应用。
该反应的主要步骤包括:
钯配合物与含有离去基的试剂进行氧化加成反应,钯的氧化态上升,也即是被氧化。
含有π键的钯与烯烃的π键进行配合,将烯烃拉近活性强的金属中心。
烯烃插入到钯与R4中间。
该分子进行β-H消除,并获得目标偶联烯烃。
钯部分经过还原消除,获得HX和原本的钯化合物,开启新一轮的催化循环。
请注意,此反应对烯烃的耐受性较好,可以适用于多种类型的烯烃,包括烷基、芳基、烯基和卤素等。
然而,对于烯丙醇,由于其容易发生重排,因此需要注意。
同时,芳基氯化物反应缓慢,导致产率较低。
以上信息仅供参考,如需了解更多信息,建议查阅化学专业书籍或咨询专业化学专家。
每天一个人名反应--Buchwald-Hartwig交叉偶联反应
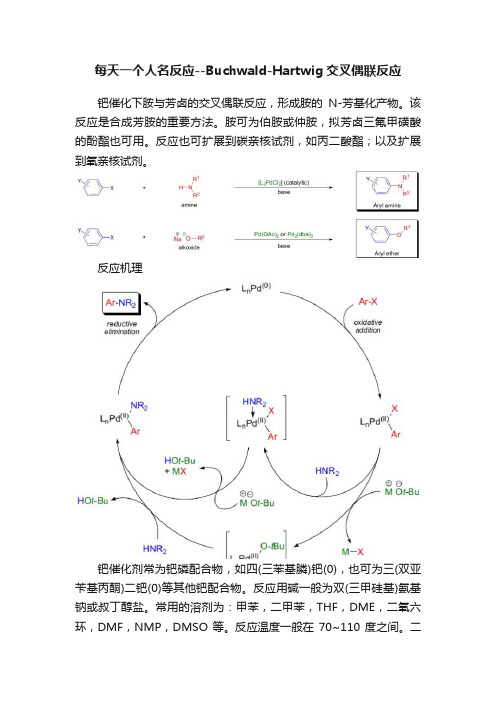
每天一个人名反应--Buchwald-Hartwig交叉偶联反应钯催化下胺与芳卤的交叉偶联反应,形成胺的N-芳基化产物。
该反应是合成芳胺的重要方法。
胺可为伯胺或仲胺,拟芳卤三氟甲磺酸的酚酯也可用。
反应也可扩展到碳亲核试剂,如丙二酸酯;以及扩展到氧亲核试剂。
反应机理钯催化剂常为钯磷配合物,如四(三苯基膦)钯(0),也可为三(双亚苄基丙酮)二钯(0)等其他钯配合物。
反应用碱一般为双(三甲硅基)氨基钠或叔丁醇盐。
常用的溶剂为:甲苯,二甲苯,THF,DME,二氧六环,DMF,NMP,DMSO等。
反应温度一般在70~110度之间。
二氧六环/间二甲苯,甲苯/叔丁醇等混合溶剂因为能增加碱的溶解度,有时也会使用。
反应实例从邻二卤苯出发可进行连续Buchwald-Hartwig交叉偶联反应。
Buchwald-Hartwig交叉偶联反应可扩展到芳醚,特别是二芳醚的合成。
参考文献1. Kosugi, M., Kameyama, M., Migita, T. Chem. Lett. 1983,927-928.2. Guram, A. S., Buchwald, S. L. J. Am. Chem. Soc. 1994, 116, 7901-7902.3. Paul, F., Patt, J., Hartwig, J. F. J. Am. Chem. Soc. 1994, 116, 5969-5970.4. Hartwig, J. F. Synlett 1997, 329-340.5. Hartwig, J. F. Acc. Chem. Res. 1998, 31, 852-860.6. Hartwig, J. F. Angew. Chem., Int. Ed. Engl. 1998, 37, 2046-2067.7. Wentland, M. P., Xu, G., Cioffi, C. L., Ye, Y., Duan, W., Cohen,D. J., Colasurdo, A. M., Bidlack, J. M. Med. Chem.Lett. 2000, 10, 183-187.8. Emoto, T., Kubosaki, N., Yamagiwa, Y., Kamikawa, T. Tetrahedron Lett. 2000, 41, 355-358.本文来自 Name Reactions:A Collection of Detailed Mechanismsand Synthetic Applications--Fifth Edition,,有机人名反应——机理及应用第四版。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钯催化的交叉偶联反应
一、偶联反应综述
1.交叉偶联反应
偶联反应,从广义上讲,就是由两个有机分子进行某种化学反应而生成一个新有机分子的过程。
狭义的偶联反应是涉及有机金属催化剂的碳-碳键生成的反应,根据类型的不同,又可分为自身偶联反应和交叉偶联。
交叉偶联反应是一个有机分子与另一有机分子发生的不对称偶联反应。
2.碳碳键形成的重要性
新碳-碳键的形成在有机化学中是极其重要的。
人们了解了天然有机物质的结构和性能,并根据有机物质的结构,通过碳原子组装成链,建立有机分子,最终实现天然有机物质的人工合成。
目前为止,人类已经利用有机合成化学手段创造出几千万种物质,且越来越多的有机物质已经广泛应用到制药、建材、食品、纺织等人类生活领域,我们的生活也几乎离不开有机物了。
合成药物、塑料等有机物质时,需要用小的有机分子将碳原子连接在一起构建新的复杂大分子,因而有机合成中高效的连接碳-碳键的方法是有机合成化学中的重要工具。
从以往该领域诺贝尔化学奖的授予情况也可以看出合成新碳-碳键的重要性:1912年维克多·格林尼亚因发明格林尼亚试剂——有机镁试剂获奖,1950年迪尔斯和阿尔德因发明双烯反应迪尔斯-阿尔德反应获奖,1979年维蒂希与布朗因发明维蒂希反应共同获奖,2005年伊夫·肖万、罗伯特·格拉布、理查德·施罗克因在有机化学的烯烃复分解反应研究方面作了突出贡献获奖。
3.有机合成中的钯催化交叉偶联反应
随着时代发展,合成有机化学的研究愈加深入,20世纪后半期,科学家们发现了大量通过过渡金属催化来创造新有机分子的反应,促使有机合成化学快速发展。
特别是赫克、根岸英一和铃木章发现的钯催化交叉偶联反应,为化学家们提供了一个更为精确有效的工具。
三位科学家发现的钯催化交叉偶联反应中都使用了金属钯
作为反应的催化剂,当碳原子与钯原子连在一起时,钯原子唤醒了“懒惰”的碳原子但又不至于使它太活泼,于是形成温和的碳-钯键,在反应过程中,钯原子又可以把别的碳原子吸引过来,形成另一个金属-碳键,此时两个碳原子都连接在钯原子上,它们的距离足够接近而发生反应,生成新的碳-碳单键。
以下两个反应式代表了典型的两类钯催化交叉偶联反应。
上述两个反应的催化剂都是零价的金属钯,都使用卤代烃RX(或卤代烃的类似物)作为亲电偶联试剂。
区别在于两个反应所选用的亲核偶联试剂,在反应(1)中,选用的是烯烃,反应(2)中则是一种有机金属化合物R〃M(M为Zn,B,Al或Sn)。
我们所熟知的赫克反应属于反应(1)这一类的交叉偶联反应,根岸反应和铃木反应属于反应(2)这一类。
由于反应底物不同,三个反应的应用范围和适用途径也各不相同。
4.“钯催化的交叉偶联反应”内容及反应原理
(1)Heck反应
Heck反应以有机钯配合物为催化剂得到具有立体专一性的芳香代烯烃(图1)。
反应物主要是卤代芳烃(碘、溴)与含有吸电子基团的烯烃。
该反应的催化剂通常用Pd(0),Pd(II)或含Pd的配合物(常用醋酸钯和三苯基膦)。
卤代烃首先与A 发生氧化加成反应,C-X键的断裂与Pd-C和Pd-X键的形成是同步进行的。
氧化加成反应是偶联反应中最常见的决速步骤,经过氧化加成化合物A生成中间体B,B 再经过配体解离,得到化合物RPdLX。
RPdLX先与烯烃配位,然后再经烯烃插入,配体配位得到中间体C。
中间体C的C-C键旋转,得到其构象异构体,从而可以进行β-消除反应,生成化合物D和目标产物——烃基化的烯烃。
在碱性(如三乙胺)条件下,碱与化合物D生成具有催化活性的零价钯,完成整个催化循环反应。
图1 Heck反应机理
(2)Negishi反应
Negishi反应的催化剂也是用具有催化活性的零价金属,如钯、镍等。
反应整体上经历氧化加成、金属转移、还原消除等步骤(图2)。
芳基卤代烃首先与零价钯发生氧化加成反应,得到中间体RPdX,卤化烃基锌R’ZnX向中间体RPdX迁移,并进行金属转移得到ZnX2和中间体RPdR’,中间体RPdR’经异构化得到顺式的络合物从而能很快地发生还原消除反应,得到化合物RR’,钯催化剂进入下一轮的催化。
图2 Negishi反应机理
(3)Suzuki反应
溴代芳烃和碘代芳烃是Suzuki反应(图3)中常见的亲电试剂,当然也可以是三氟甲基磺酸酯、重氮盐等。
芳基硼酸通常是由芳基锂或格氏试剂与烷基硼酸酯反应制得,芳基硼酸在空气中稳定,可以长期保存。
Suzuki反应机理与Negishi反应类似,经历了三个过程:氧化加成、芳基阴离子向金属中心迁移和还原消除。
卤代芳烃首先与Pd(0)进行氧化加成,得到ArPdX中间体,该中间体再与一分子碱作用得到中间体ArPdOH;另一分子的碱与硼酸作用得到硼酸盐,从而使得芳基具有更强的富电性,有利于芳基向ArPdOH中间体的金属原子迁移,一般来说,只有Pd(II)才能发生金属中心迁移。
金属中心迁移作用是通过一个四员环过渡态(four-centerintermediate)进行的。
但是值得注意的是,一些反应的添加剂可以通过改变过渡态的结构加速金属中心迁移作用,例如碱可以加速Suzuki反应。
在Ar’PdOH和ArB’OH的协同作用下,得到配合物中间体ArPdAr’,该中间体经过还原消除得到芳基偶联产物和零价钯,完成整个循环过程。
图3 Suzuki反应机理
二、合成目标产物
N
N
Benzenamine, 4-(2-phenylethynyl)-N-(2-pyridinylmethylene)-
图4 目标产物
1.反应方程式:
①
A B C
②
D E
2.具体实验步骤与分离纯化方法:
(1)进行反应①:
在放有磁子的50 mL圆底烧瓶中加入A(0.01 mol)和B(0.02 mol)。
将烧瓶0置于微波合成仪中,确认磁子旋转后关闭炉门,开始实验。
实验结束后,将反应液加入乙醇溶液中,降温至30 ℃以下,析出的结晶使混合物呈稀粥状,冷却后过
滤,干燥,即得产品C。
(2)进行反应②:
在schlenk管中加入醋酸钯(0.03mmol)、2-氨基-4,6-二羟基嘧啶(0.06mmol),碳酸铯(1.2mmol),再加入C(1.0mmol),苯乙炔(l.2mmol),乙腈(4ml),用氮气保护,在室温下反应直到完全。
(3)分离纯化:
反应完全后用层板柱加入2cm硅胶进行前处理,乙醚淋洗,旋转蒸发仪蒸出溶剂,然后用正己烷为展开剂,经柱层析提纯得纯产物。
参考文献:
[1] 张旭东.胺为配体促进钯催化交叉偶联反应的研究[J].湖南师范大学,2006.
[2] 肖唐鑫,刘立,强琚莉,王乐勇.钯催化的交叉偶联反应——2010年诺贝尔化学奖简介[J].自然杂志,2010,32(6):332-337.
[3] 李媛,马宏佳,葛春洋,杨民富.钯催化的交叉偶联反应——2010诺贝尔化学奖简介[J].化学教与学,2010(11):2-4.
[4] 杨发丽,刘克文,杨光.钯催化交叉偶联反应———2010年诺贝尔化学奖成果介绍[J].中国校外教育,2011(7):66-67.
[5] 匡华.钯催化交叉偶联反应及其在有机合成中的应用[J].江苏技术师范学院学报,2010,16(12):8-13.。
