碱水制氢生产工艺
电解水制氢的原理

电解水制氢的原理一、氢气的工业制法在工业上通常采用如下几种方法制取氢气:一是将水蒸气通过灼热的焦炭(称为碳还原法),得到纯度为75%左右的氢气;二是将水蒸气通过灼热的铁,得到纯度在97%以下的氢气;三是由水煤气中提取氢气,得到的氢气纯度也较低;第四种方法就是电解水法,制得的氢气纯度可高达99%以上,这是工业上制备氢气的一种重要方法。
在电解氢氧化钠(钾)溶液时,阳极上放出氧气,阴极上放出氢气。
电解氯化钠水溶液制造氢氧化钠时,也可得到氢气。
对用于冷却发电机的氢气的纯度要求较高,因此,都是采用电解水的方法制得。
二、电解水制氢原理所谓电解就是借助直流电的作用,将溶解在水中的电解质分解成新物质的过程。
1、电解水原理在一些电解质水溶液中通入直流电时,分解出的物质与原来的电解质完全没有关系,被分解的是作为溶剂的水,原来的电解质仍然留在水中。
例如硫酸、氢氧化钠、氢氧化钾等均属于这类电解质。
在电解水时,由于纯水的电离度很小,导电能力低,属于典型的弱电解质,所以需要加入前述电解质,以增加溶液的导电能力,使水能够顺利地电解成为氢气和氧气。
氢氧化钾等电解质不会被电解,现以氢氧化钾为例说明:(1)氢氧化钾是强电解质,溶于水后即发生如下电离过程:于是,水溶液中就产生了大量的K+和OH-。
(2)金属离子在水溶液中的活泼性不同,可按活泼性大小顺序排列如下:K>Na>Mg>Al>Mn>Zn>Fe>Ni>Sn>Pb>H>Cu>Hg>Ag>Au在上面的排列中,前面的金属比后面的活泼。
(3)在金属活泼性顺序中,越活泼的金属越容易失去电子,否则反之。
从电化学理论上看,容易得到电子的金属离子的电极电位高,而排在活泼性大小顺序前的金属离子,由于其电极电位低而难以得到电子变成原子。
H+的电极电位=-1.71V,而K+的电极电位=-2.66V,所以,在水溶液中同时存在H+和K+时,H+将在阴极上首先得到电子而变成氢气,而K+则仍将留在溶液中。
(4)水是一种弱电解质,难以电离。
电解水制氢

电解水制氢在工业上通常采用如下几种方法制取氢气:一是将水蒸气通过灼热的焦炭(称为碳还原法),得到纯度为75%左右的氢气;二是将水蒸气通过灼热的铁,得到纯度在97%以下的氢气;三是由水煤气中提取氢气,得到的氢气纯度也较低;第四种方法就是电解水法,制得的氢气纯度可高达99%以上,这是工业上制备氢气的一种重要方法。
在电解氢氧化钠(钾)溶液时,阳极上放出氧气,阴极上放出氢气。
电解氯化钠水溶液制造氢氧化钠时,也可得到氢气。
对用于冷却发电机的氢气的纯度要求较高,因此,都是采用电解水的方法制得。
一、电解水制氢原理所谓电解就是借助直流电的作用,将溶解在水中的电解质分解成新物质的过程。
1、电解水原理在一些电解质水溶液中通入直流电时,分解出的物质与原来的电解质完全没有关系,被分解的是作为溶剂的水,原来的电解质仍然留在水中。
例如硫酸、氢氧化钠、氢氧化钾等均属于这类电解质。
在电解水时,由于纯水的电离度很小,导电能力低,属于典型的弱电解质,所以需要加入前述电解质,以增加溶液的导电能力,使水能够顺利地电解成为氢气和氧气。
氢氧化钾等电解质不会被电解,现以氢氧化钾为例说明:(1)氢氧化钾是强电解质,溶于水后即发生如下电离过程:于是,水溶液中就产生了大量的K+和OH-。
(2)金属离子在水溶液中的活泼性不同,可按活泼性大小顺序排列如下:K>Na>Mg>Al>Mn>Zn>Fe>Ni>Sn>Pb>H>Cu>Hg>Ag>Au在上面的排列中,前面的金属比后面的活泼。
(3)在金属活泼性顺序中,越活泼的金属越容易失去电子,否则反之。
从电化学理论上看,容易得到电子的金属离子的电极电位高,而排在活泼性大小顺序前的金属离子,由于其电极电位低而难以得到电子变成原子。
H+的电极电位=-1.71V,而K+的电极电位=-2.66V,所以,在水溶液中同时存在H+和K+时,H+将在阴极上首先得到电子而变成氢气,而K+则仍将留在溶液中。
(4)水是一种弱电解质,难以电离。
烧碱生产工艺详解

烧碱生产工艺详解我国烧碱(氢氧化钠)行业起源于1929年上海天元电化厂的成立,烧碱生产工艺包括苛化法和电解法两种。
其中,苛化法即纯碱苛化法,电解法又可分为水银法、隔膜法、离子交换膜法。
目前,离子交换膜电解法是烧碱行业主流的生产工艺。
起初苛化法在国内的应用较为广泛,但是2000年以后,电解法逐步取代苛化法成为主要的生产方法。
目前,国内在产的烧碱企业都使用离子交换膜电解法。
一、烧碱苛化法生产工艺苛化法制烧碱以纯碱为原料,主要依靠天然碱矿资源,生产成本较低,经济效益高。
不过,由于我国碱矿资源有限、苛化法产量较小,国家政策予以限制,2000年前后,我国企业全面淘汰该生产工艺。
苛化法生产工艺并不复杂,其反应式为Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。
苛化法主要有三个生产步骤:第一步是苛化,第二步是蒸发,第三步是盐析。
在苛化阶段,苛化槽中需配置纯碱溶液,加入生石灰,不断搅拌发生苛化反应,而后过滤得到清卤液。
在蒸发阶段,制作合格的清卤液依次进行中浓蒸发和高浓蒸发,去除硫酸钠、碳酸钠和氯化钠杂质,获得高浓度氢氧化钠。
在盐析阶段,高浓液进一步析出晶体、过滤,送入冷析桶,达标后的产品用间歇沉淀槽进行沉淀,即可得到片碱。
二、烧碱电解法生产工艺根据电解槽结构、电极材料和隔膜材料的不同,电解法可以分为水银法、隔膜法和离子交换膜法。
目前,离子交换膜电解法是我国烧碱生产的主流工艺,其化学反应式是2NaCl+2H2O = 2NaOH+Cl2↑+H2↑。
1、水银电解法水银电解法是通过生产钠汞齐来使氯气分开,得到烧碱的方法。
其电解槽由电解室和解汞室组成,该工艺的优点是电解槽流出溶液产物中氢氧化钠浓度较高,其质量分数可高达50%,无需蒸发增浓;产品质量高,含盐低,但是由于该工艺能耗高,且水银是有害物质,该工艺目前已基本被淘汰。
2、隔膜电解法隔膜电解法是利用多孔渗透性的石棉隔膜作为隔层,以石墨为阳极、铁为阴极,把阳极产生的氯气与阴极产生的氢氧化钠和氢气分开,获得烧碱的一种方法。
电解水制氢工艺描述
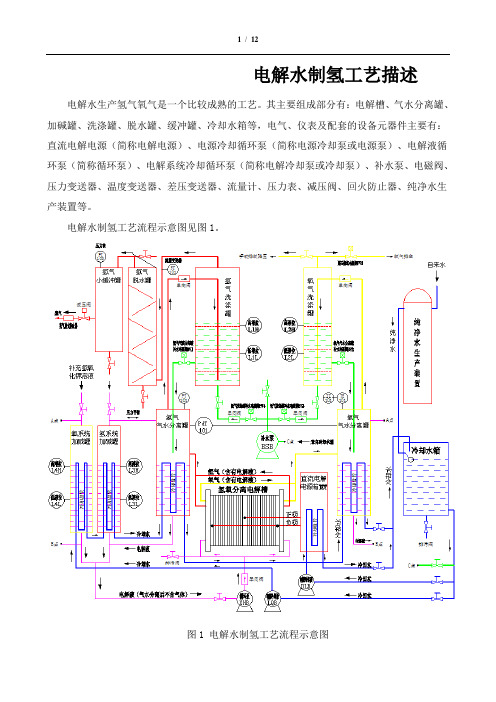
电解水制氢工艺描述电解水生产氢气氧气是一个比较成熟的工艺。
其主要组成部分有:电解槽、气水分离罐、加碱罐、洗涤罐、脱水罐、缓冲罐、冷却水箱等,电气、仪表及配套的设备元器件主要有:直流电解电源(简称电解电源)、电源冷却循环泵(简称电源冷却泵或电源泵)、电解液循环泵(简称循环泵)、电解系统冷却循环泵(简称电解冷却泵或冷却泵)、补水泵、电磁阀、压力变送器、温度变送器、差压变送器、流量计、压力表、减压阀、回火防止器、纯净水生产装置等。
电解水制氢工艺流程示意图见图1。
图1 电解水制氢工艺流程示意图压力的单位为Mpa,小数点后面保留3位。
差压的单位为kPa,小数点后面保留2位,流量单位为m3/h,小数点后面保留2位。
温度的单位为°C,小数点后面保留1位,累计流量的单位为m3,小数点后面保留1位,累计工作时间的单位为h,小数点后面保留1位。
所有的电磁阀均为电开阀,通电开启,断电关闭。
一、电解电源DDY、电源冷却泵DLB、循环泵XHB及冷却泵LQB控制表1 电解系统与冷却系统对应输入输出关系表1、氢气压力PH 由压力变送器PT101变送为4~20mA直流信号,根据氢气压力PH控制电解电源DDY(电解电源DDY由一个开关量信号控制运行与停止)、电源冷却泵DLB和循环泵XHB(电源冷却泵DLB和循环泵XHB与电解电源DDY同步受氢气压力PH控制)的通断,氢气压力可以在触摸屏上设置:○1氢气压力上限设定值(简称压力设定上限)PHH的设置范围0~3.00Mpa(参考值0.40Mpa);○2氢气压力下限设定值(简称压力设定下限)PHL的设置范围0~3.00MPa(参考值0.35Mpa)。
参考值就是第一次开机设置时(或者长时间断电数据丢失时)推荐使用的数值。
○3当氢气压力PH 高于压力设定上限PHH,PH>PHH,DO1输出为OFF,电解电源DDY、电源泵DLB和循环泵XHB停止运行;○4氢气压力PH 低于压力设定下限PHL,PH<PHL, DO1输出为ON,电解电源DDY、电源泵DLB和循环泵XHB通电运行。
水电解制氢工序操作规程

水电解制氢工序操作规程编制:审核:批准:生效日期:2013年10 月目录第一节生产的目的及工作原理一、生产的目的二、工作原理(一)电解工作原理..........................................(二)纯化工作原理..........................................第二节质量标准及技术参数一、原料质量标准(一)脱盐水质要求:........................................(二)氢氧化钾..............................................(三)冷却水................................................(四)电源..................................................(五)氮气..................................................(六)仪表气源..............................................二、工艺及设备技术参数(一)电解槽工艺技术参数....................................(二)纯化装置工艺技术参数..................................三、产品质量标准错误!未定义书签。
第三节工艺流程简介一、制氢装置工艺流程简介(一)碱液循环系统..........................................(二)氢气系统..............................................(三)氧气系统..............................................(四)原料水补充系统........................................(五)冷却水系统............................................(六)充氮和氮气吹扫系统....................................(七)排污系统(八)整流系统(九)控制系统二、纯化系统工艺流程简介(一)工艺流程简图..........................................(二)工艺流程解释..........................................第四节电解液配置岗位操作法一、制氢系统的操作(一)开车前的准备(二)、电解液的配制(三)稀碱运行(1#电解槽为例,其它电解槽运行同1#电解槽)(四)浓碱运行(以1#电解槽为例,其他电解槽运行同1#)(五)自控部分的调试(六)装置正常运行工作(七)停车操作(八)应急停车操作(九)常见故障及排除方法三、纯化系统的操作(一)开车前的检查与准备(二)气密性试验(包括氢气储罐及缓冲罐)(三)、开车操作步骤(四)装置正常运行工作(五)、停车操作(六)生产中常见事故及处理第五节事故应急处置程序与处置措施一、触电急救(一)发现触电后,应迅速使触电者脱离电源。
(完整word版)电解水制氢

电解水制氢在工业上通常采用如下几种方法制取氢气:一是将水蒸气通过灼热的焦炭(称为碳还原法),得到纯度为75%左右的氢气;二是将水蒸气通过灼热的铁,得到纯度在97%以下的氢气;三是由水煤气中提取氢气,得到的氢气纯度也较低;第四种方法就是电解水法,制得的氢气纯度可高达99%以上,这是工业上制备氢气的一种重要方法。
在电解氢氧化钠(钾)溶液时,阳极上放出氧气,阴极上放出氢气。
电解氯化钠水溶液制造氢氧化钠时,也可得到氢气。
对用于冷却发电机的氢气的纯度要求较高,因此,都是采用电解水的方法制得。
一、电解水制氢原理所谓电解就是借助直流电的作用,将溶解在水中的电解质分解成新物质的过程。
1、电解水原理在一些电解质水溶液中通入直流电时,分解出的物质与原来的电解质完全没有关系,被分解的是作为溶剂的水,原来的电解质仍然留在水中。
例如硫酸、氢氧化钠、氢氧化钾等均属于这类电解质。
在电解水时,由于纯水的电离度很小,导电能力低,属于典型的弱电解质,所以需要加入前述电解质,以增加溶液的导电能力,使水能够顺利地电解成为氢气和氧气。
氢氧化钾等电解质不会被电解,现以氢氧化钾为例说明:(1)氢氧化钾是强电解质,溶于水后即发生如下电离过程:于是,水溶液中就产生了大量的K+和OH-。
(2)金属离子在水溶液中的活泼性不同,可按活泼性大小顺序排列如下:K>Na>Mg>Al>Mn>Zn>Fe>Ni>Sn>Pb>H>Cu>Hg>Ag>Au在上面的排列中,前面的金属比后面的活泼。
(3)在金属活泼性顺序中,越活泼的金属越容易失去电子,否则反之。
从电化学理论上看,容易得到电子的金属离子的电极电位高,而排在活泼性大小顺序前的金属离子,由于其电极电位低而难以得到电子变成原子。
H+的电极电位=-1.71V,而K+的电极电位=-2.66V,所以,在水溶液中同时存在H+和K+时,H+将在阴极上首先得到电子而变成氢气,而K+则仍将留在溶液中。
(4)水是一种弱电解质,难以电离。
(完整word版)电解水制氢的原理

电解水制氢的原理一、氢气的工业制法在工业上通常采用如下几种方法制取氢气:一是将水蒸气通过灼热的焦炭(称为碳还原法),得到纯度为75%左右的氢气;二是将水蒸气通过灼热的铁,得到纯度在97%以下的氢气;三是由水煤气中提取氢气,得到的氢气纯度也较低;第四种方法就是电解水法,制得的氢气纯度可高达99%以上,这是工业上制备氢气的一种重要方法。
在电解氢氧化钠(钾)溶液时,阳极上放出氧气,阴极上放出氢气。
电解氯化钠水溶液制造氢氧化钠时,也可得到氢气。
对用于冷却发电机的氢气的纯度要求较高,因此,都是采用电解水的方法制得。
二、电解水制氢原理所谓电解就是借助直流电的作用,将溶解在水中的电解质分解成新物质的过程。
1、电解水原理在一些电解质水溶液中通入直流电时,分解出的物质与原来的电解质完全没有关系,被分解的是作为溶剂的水,原来的电解质仍然留在水中。
例如硫酸、氢氧化钠、氢氧化钾等均属于这类电解质。
在电解水时,由于纯水的电离度很小,导电能力低,属于典型的弱电解质,所以需要加入前述电解质,以增加溶液的导电能力,使水能够顺利地电解成为氢气和氧气。
氢氧化钾等电解质不会被电解,现以氢氧化钾为例说明:(1)氢氧化钾是强电解质,溶于水后即发生如下电离过程:于是,水溶液中就产生了大量的K+和OH-。
(2)金属离子在水溶液中的活泼性不同,可按活泼性大小顺序排列如下:K>Na>Mg>Al>Mn>Zn>Fe>Ni>Sn>Pb>H>Cu>Hg>Ag>Au在上面的排列中,前面的金属比后面的活泼。
(3)在金属活泼性顺序中,越活泼的金属越容易失去电子,否则反之。
从电化学理论上看,容易得到电子的金属离子的电极电位高,而排在活泼性大小顺序前的金属离子,由于其电极电位低而难以得到电子变成原子。
H+的电极电位=-1.71V,而K+的电极电位=-2.66V,所以,在水溶液中同时存在H+和K+时,H+将在阴极上首先得到电子而变成氢气,而K+则仍将留在溶液中。
(4)水是一种弱电解质,难以电离。
碱水制氢控制系统方法与流程

碱水制氢控制系统方法与流程
碱水制氢控制系统方法主要包括以下步骤:
1. 电解槽:电解槽是碱水制氢系统的核心部分,包括数十个甚至上百个电解小室,每个电解小室由螺杆和端板压在一起形成圆柱状或正方形,电解小室以相邻的2个极板为分界,包括正负双极板、阳极电极、隔膜、密封垫圈、阴极电极6个部分。
2. 控制系统:控制系统是用来实时监测装置内温度、压力、流量、气体纯度等参数的,包括制氢控制系统和PLC控制柜。
3. 辅助系统:辅助系统包括电源供应系统、气液分离系统、纯化系统、碱液系统、补水系统、冷却干燥系统及附属系统等8大系统。
其中,电源供应系统将交流电转化为稳定的直流电源;气液分离系统将氢气和氧气分别与碱液进行分离;纯化系统对气体进行提纯;碱液系统保证碱液的稳定、连续供给;补水系统保证水源的稳定、连续供给。
4. 温度控制系统:该系统包含纯水箱、电解水制氢系统、氢气储罐,纯水箱设置在电解水制氢系统上游管路上,电解水制氢系统下游管路上设置氢气储罐。
温度控制系统还包括热源控制系统和冷源控制系统,这两个系统与出口管路和入口管路相连,用于控制电解过程中所需的温度。
具体的碱水制氢控制系统方法需要综合考虑设备选型、工艺流程以及操作条件等多个因素,建议咨询化学工程专家或查阅相关文献资料。
alk电解水制氢 工艺

alk电解水制氢工艺
电解水制氢是一种常见的氢气生产方法,其中碱性电解水(ALK 电解水)是一种常用的电解水方法之一。
碱性电解水通常使用氢氧化钠((NaOH)等碱性电解质来增加电解液的导电性。
以下是碱性电解水制氢的基本工艺:
主要步骤:
1.准备电解槽:设置电解槽,通常为两个电极槽,通过一块隔膜隔开。
电解槽内装有阳极和阴极,它们通常是由导电材料((如铂或其他合适的材料)制成。
2.准备电解液:在电解槽中加入碱性电解液,通常使用氢氧化钠(NaOH)溶液。
这样的碱性环境有助于提高水的电导率。
3.施加电压:将直流电源连接到电解槽的阳极和阴极。
通常,水会在电解过程中分解成氢气和氧气。
4.电解反应:
•在阳极:(4OH−→2H2O+O2+4e−(水在阳极释放氧气)。
•在阴极:(2H2O+2e−→H2+2OH−(水在阴极释放氢气)。
5.收集氢气:通过适当的设备,收集在阴极生成的氢气。
6.收集氧气:在阳极生成的氧气也可以通过相应的设备进行收集或释放到大气中。
工艺控制:
1.电压和电流控制:控制施加到电解槽的电压和电流,以确保反应的进行和安全性。
2.温度控制:电解过程中的温度控制是重要的,以维持反应的稳定性和效率。
3.电解液浓度控制:确保电解液中碱性物质的适当浓度,以保持足够的电导率。
4.防气漏控制:由于氢气是易燃气体,需要采取措施防止氢气漏出并引发安全问题。
碱性电解水制氢是一种相对简单且广泛应用的氢气生产方法之一。
然而,考虑到能源效率和环境友好性,氢气的生产方法正在不断研究和改进。
氢气生产工艺

氢气生产工艺
氢气生产工艺是指将水分解成氢气和氧气的过程。
氢气是一种清洁、高效的能源,被广泛应用于燃料电池、化工、金属加工等领域。
本文将介绍氢气生产的工艺流程和技术特点。
氢气生产的工艺流程主要包括水电解、天然气重整和煤炭气化等几种方式。
其中,水电解是最常用的方法。
水电解是指将水分解成氢气和氧气的过程,需要通过电解池将水分解成氢气和氧气。
电解池通常由两个电极和一个电解质组成。
电解质可以是酸、碱或盐,其中最常用的是碱性电解质。
在电解质的作用下,水分子被分解成氢离子和氧离子,氢离子在阴极处接受电子,生成氢气,氧离子在阳极处失去电子,生成氧气。
水电解的优点是原料来源广泛,可以使用普通自来水,同时产生的氧气也可以用于工业生产。
天然气重整是指将天然气转化为氢气的过程。
天然气中含有丰富的甲烷,通过重整反应可以将甲烷转化为氢气和二氧化碳。
重整反应需要高温和高压的条件,通常需要使用催化剂来促进反应。
天然气重整的优点是氢气产量高,同时可以利用天然气中的甲烷资源。
煤炭气化是指将煤炭转化为氢气和一些其他气体的过程。
煤炭气化需要高温和高压的条件,通常需要使用催化剂来促进反应。
煤炭气化的优点是可以利用煤炭这种广泛存在的资源,同时可以产生其他有用的气体。
总的来说,氢气生产工艺具有原料来源广泛、产量高、清洁环保等优点。
随着氢能技术的不断发展,氢气生产工艺也在不断创新和改进,未来将会有更多的新技术应用于氢气生产中。
电解水制氢的原理[内容详细]
![电解水制氢的原理[内容详细]](https://img.taocdn.com/s3/m/1ee57de45022aaea998f0f88.png)
电解水制氢的原理字体大小:大- 中- 小SBEPL发表于09-06-03 06:37 阅读(1274) 评论(0)日志复制网址隐藏签名档大字体第二节电解水制氢的原理一、氢气的工业制法在工业上通常采用如下几种方法制取氢气:一是将水蒸气通过灼热的焦炭(称为碳还原法),得到纯度为75%左右的氢气;二是将水蒸气通过灼热的铁,得到纯度在97%以下的氢气;三是由水煤气中提取氢气,得到的氢气纯度也较低;第四种方法就是电解水法,制得的氢气纯度可高达99%以上,这是工业上制备氢气的一种重要方法。
在电解氢氧化钠(钾)溶液时,阳极上放出氧气,阴极上放出氢气。
电解氯化钠水溶液制造氢氧化钠时,也可得到氢气。
对用于冷却发电机的氢气的纯度要求较高,因此,都是采用电解水的方法制得。
二、电解水制氢原理所谓电解就是借助直流电的作用,将溶解在水中的电解质分解成新物质的过程。
1、电解水原理在一些电解质水溶液中通入直流电时,分解出的物质与原来的电解质完全没有关系,被分解的是作为溶剂的水,原来的电解质仍然留在水中。
例如硫酸、氢氧化钠、氢氧化钾等均属于这类电解质。
在电解水时,由于纯水的电离度很小,导电能力低,属于典型的弱电解质,所以需要加入前述电解质,以增加溶液的导电能力,使水能够顺利地电解成为氢气和氧气。
氢氧化钾等电解质不会被电解,现以氢氧化钾为例说明:(1)氢氧化钾是强电解质,溶于水后即发生如下电离过程:于是,水溶液中就产生了大量的K+和OH-。
(2)金属离子在水溶液中的活泼性不同,可按活泼性大小顺序排列如下:K>Na>Mg>Al>Mn>Zn>Fe>Ni>Sn>Pb>H>Cu>Hg>Ag>Au在上面的排列中,前面的金属比后面的活泼。
(3)在金属活泼性顺序中,越活泼的金属越容易失去电子,否则反之。
从电化学理论上看,容易得到电子的金属离子的电极电位高,而排在活泼性大小顺序前的金属离子,由于其电极电位低而难以得到电子变成原子。
H+的电极电位=-1.71V,而K+的电极电位=-2.66V,所以,在水溶液中同时存在H+和K+时,H+将在阴极上首先得到电子而变成氢气,而K+则仍将留在溶液中。
电解水制氢工艺描述
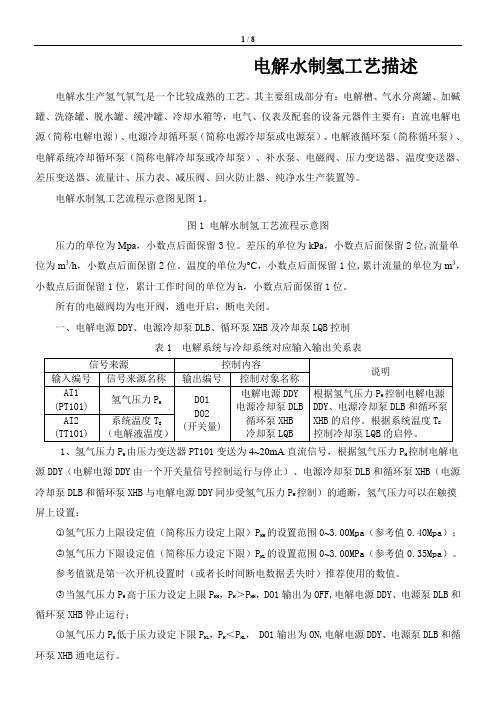
电解水制氢工艺描述电解水生产氢气氧气是一个比较成熟的工艺。
其主要组成部分有:电解槽、气水分离罐、加碱罐、洗涤罐、脱水罐、缓冲罐、冷却水箱等,电气、仪表及配套的设备元器件主要有:直流电解电源(简称电解电源)、电源冷却循环泵(简称电源冷却泵或电源泵)、电解液循环泵(简称循环泵)、电解系统冷却循环泵(简称电解冷却泵或冷却泵)、补水泵、电磁阀、压力变送器、温度变送器、差压变送器、流量计、压力表、减压阀、回火防止器、纯净水生产装置等。
电解水制氢工艺流程示意图见图1。
图1 电解水制氢工艺流程示意图压力的单位为Mpa,小数点后面保留3位。
差压的单位为kPa,小数点后面保留2位,流量单位为m3/h,小数点后面保留2位。
温度的单位为°C,小数点后面保留1位,累计流量的单位为m3,小数点后面保留1位,累计工作时间的单位为h,小数点后面保留1位。
所有的电磁阀均为电开阀,通电开启,断电关闭。
一、电解电源DDY、电源冷却泵DLB、循环泵XHB及冷却泵LQB控制表1 电解系统与冷却系统对应输入输出关系表1、氢气压力PH 由压力变送器PT101变送为4~20mA直流信号,根据氢气压力PH控制电解电源DDY(电解电源DDY由一个开关量信号控制运行与停止)、电源冷却泵DLB和循环泵XHB(电源冷却泵DLB和循环泵XHB与电解电源DDY同步受氢气压力PH控制)的通断,氢气压力可以在触摸屏上设置:○1氢气压力上限设定值(简称压力设定上限)PHH的设置范围0~3.00Mpa(参考值0.40Mpa);○2氢气压力下限设定值(简称压力设定下限)PHL的设置范围0~3.00MPa(参考值0.35Mpa)。
参考值就是第一次开机设置时(或者长时间断电数据丢失时)推荐使用的数值。
○3当氢气压力PH 高于压力设定上限PHH,PH>PHH,DO1输出为OFF,电解电源DDY、电源泵DLB和循环泵XHB停止运行;○4氢气压力PH 低于压力设定下限PHL,PH<PHL, DO1输出为ON,电解电源DDY、电源泵DLB和循环泵XHB通电运行。
碱水制氢控制系统方法与流程

碱水制氢控制系统方法与流程
制备氢气的一种方法是通过碱水(氢氧化钠或氢氧化钾溶液)与铝反应产生氢气。
以下是碱水制氢气的控制系统方法和流程的简要描述:
1.准备碱水槽:准备一个容器,用来放置碱水溶液。
该容器
应具有足够的容量以容纳所需的溶液。
2.加入碱水:将适量的氢氧化钠(NaOH)或氢氧化钾(KOH)
溶解在水中,制备碱水溶液。
注意在制备碱水溶液时要安
全操作,避免溅溶液或进入眼睛和皮肤。
3.加热碱水:将碱水溶液加热至适当的温度。
高温有助于加
快反应速率。
4.准备铝片:准备铝片或铝箔。
铝片将作为反应的还原剂。
5.控制进气:在碱水槽中设置进气管道,以便通过控制阀调
节氢气的进气量。
确保进气系统安全可靠,并控制进气速
度。
6.开始反应:将铝片放入碱水槽中,并确保与碱水溶液充分
接触。
铝与碱水反应时产生氢气。
7.控制反应速率:通过控制进气量和铝片的数量和面积,控
制反应速率和产生的氢气量。
确保反应的平稳进行,并避
免过度反应或溢出。
8.收集氢气:将产生的氢气通过管道或管道系统导入收集容
器中,以便进行后续的储存或使用。
9.监测和控制:在制氢的过程中,监测氢气的流量、压力和
温度等参数。
确保系统的稳定性和安全性,及时做出调整和控制。
需要注意的是,制备氢气涉及气体的操作和安全问题。
在进行碱水制氢的过程中,应严格遵守安全操作规程,并佩戴合适的防护设备。
确保操作环境通风良好,远离可燃物和火源。
定期检查和维护制氢设备。
碱水制氢 流程

碱水制氢流程碱水制氢是一种超有趣的制氢方法呢,那我来给你好好讲讲它的流程吧。
一、准备工作。
咱得先把材料准备好。
碱水制氢需要有碱,常见的就是氢氧化钠或者氢氧化钾啦。
这就好比做饭得先把食材准备好一样重要呢。
然后还得有个合适的容器,这个容器得能耐受住碱水的腐蚀性哦,可不能随便找个容易被腐蚀坏的容器,不然就像穿着纸糊的盔甲上战场,肯定不行啦。
另外,电极也是必不可少的,一般会用到金属电极,像铂电极就很不错,不过它有点小贵,就像奢侈品一样,但为了制氢效果好,有时候也是值得的。
二、配置碱水。
把准备好的碱,按照一定的比例加入到水中。
这个比例可不能瞎搞哦。
如果碱放得太多,就像做菜盐放多了一样,会影响整个制氢的过程,可能还会有一些危险情况出现呢。
要是碱放得太少,那就像炒菜没放盐,制氢的效率会特别低,等半天都制不出多少氢气来。
这个过程就像是在调配魔法药水,要小心翼翼地控制好比例,让碱和水完美地融合在一起。
三、电极安装。
把电极安装到容器里,这一步可不能马虎。
电极要安装得稳稳当当的,就像盖房子打地基一样,地基不稳房子就会塌,电极安装不好,制氢的过程就会出乱子。
电极要确保能和碱水充分接触,这样电流才能顺利地通过电极,让制氢反应能够顺利地进行。
四、通电反应。
一切准备就绪,就可以通电啦。
这时候就像打开了一个神奇的开关,电流在电极和碱水之间穿梭,化学反应就开始啦。
水在碱的帮助下,开始分解成氢气和氧气。
氢气就像一个个调皮的小泡泡,开始在容器里冒出来。
看着那些小泡泡不断地产生,就感觉特别有成就感,就像是自己亲手创造了一个小小的奇迹一样。
五、氢气收集。
等氢气产生得差不多了,咱们就得把氢气收集起来。
可以用专门的收集装置,比如排水法收集氢气。
把一个装满水的容器倒扣在产生氢气的容器上,氢气就会慢慢地跑到倒扣的容器里,把水挤出去。
这个过程就像把调皮的小氢气们都赶到一个小房子里一样,特别好玩。
碱水制氢的流程就是这样啦,是不是感觉很有趣呢?每一个步骤都像是在完成一个小小的挑战,而且当看到氢气真的被制出来的时候,那种开心和满足感是无法用言语来形容的。
碱水电解制氢 气体纯度

碱水电解制氢气体纯度碱水电解制氢是一种常见且有效的方法,用于产生高纯度的氢气。
该方法利用电解的原理,在碱性溶液中进行反应,从而将水分解成氢气和氧气。
本文将深入探讨碱水电解制氢的原理、实验过程以及气体纯度的相关问题。
一、碱水电解制氢的原理碱水电解制氢的原理基于电化学反应。
当电流通过碱性溶液中的水时,水分子会发生电解,产生氢气和氧气。
这是因为水分子中的氧原子具有更高的电负性,所以在电场的作用下,氧原子会向阳极移动,而氢原子则向阴极移动。
在阴极上,氢原子接受电子并与水分子结合,形成氢气;而在阳极上,氧原子失去电子,与水分子结合形成氧气。
二、碱水电解制氢的实验过程碱水电解制氢的实验过程通常包括以下几个步骤:1. 准备电解槽:选择一个适当的电解槽,通常由不导电的材料制成。
在电解槽中加入适量的碱性溶液,如氢氧化钠或氢氧化钾溶液。
2. 连接电源:将电解槽的阳极和阴极分别连接到直流电源的正负极,确保电流可以通过溶液。
3. 开始电解:打开电源,使电流通过碱性溶液。
随着电流的通过,水分子会发生电解,产生氢气和氧气。
4. 收集氢气:将收集装置连接到电解槽的阴极,以收集产生的氢气。
收集装置可以是玻璃管或气球等。
5. 检测气体纯度:使用气体分析仪或其他检测方法,对收集到的氢气进行纯度检测。
三、气体纯度的相关问题1. 纯度的定义:气体纯度是指气体中所含目标组分的含量。
在碱水电解制氢中,氢气的纯度是衡量制氢效果的重要指标。
2. 纯度的检测方法:常用的气体纯度检测方法有气相色谱法、质谱法和红外光谱法等。
这些方法可以准确地测量气体中各组分的含量。
3. 纯度的影响因素:制氢过程中影响气体纯度的因素有很多,如电流密度、电解时间、电解槽的设计等。
合理控制这些因素可以提高氢气的纯度。
4. 纯度的应用:高纯度的氢气在许多领域有着广泛的应用,如化学分析、实验室研究、燃料电池等。
只有纯度足够高的氢气才能满足这些应用的要求。
总结:碱水电解制氢是一种简便有效的方法,可以产生高纯度的氢气。
电解水制氢技术描述

电解水制氢技术描述概述电解水制氢技术是一种将水分解为氢气和氧气的过程。
该过程利用电能将水分子分解成氢离子和氢氧离子,然后通过反应器收集氢气并排出氧气。
这种技术广泛应用于氢能源领域,并被认为是一种可持续发展的能源生产方法。
原理电解水制氢技术主要基于电解反应原理。
在一个电解池中,通常使用两个电极(阳极和阴极),以及一个电解质溶液。
当电流通过电解质溶液时,阳极上的阴极反应会产生氧气,而阴极上的阴极反应会产生氢气。
这些气体可以通过合适的收集装置进行收集和分离。
设备和工艺电解水制氢技术所需的主要设备包括电解池、电源、电解质溶液和气体收集装置。
电解池通常由两个电极和一个分隔阻挡物组成,以防止阳极上产生的氧气与阴极上产生的氢气混合。
电源则用于提供所需的电流,以促使电解反应发生。
而电解质溶液则是用于使电流能够传导的介质。
在工艺方面,电解水制氢技术可以采用不同的电解质溶液和工作条件。
常用的电解质溶液包括硫酸、盐酸和碱性水溶液。
同时,工作条件的选择也会影响电解效果和氢气产率。
应用和前景电解水制氢技术在氢能源的生产和储存中起着重要作用。
由于氢气是一种清洁能源,可以通过燃烧产生水和热,因此广泛应用于燃料电池、氢气动力车辆以及工业生产中的能源供应。
随着对可再生能源的需求不断增加,电解水制氢技术的前景也变得更加重要。
它可以通过利用太阳能或其他可再生能源产生的电力来制备氢气,使得氢能源的生产更加环保和可持续。
因此,电解水制氢技术被认为是未来能源发展中的重要方向之一。
结论电解水制氢技术通过电解水分子将水分解为氢气和氧气。
它是一种广泛应用于氢能源领域的可持续发展的能源生产方法。
电解水制氢技术的设备和工艺包括电解池、电源、电解质溶液和气体收集装置。
它在燃料电池、氢气动力车辆等领域的应用前景广阔,将对未来能源发展产生重要影响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碱水制氢生产工艺
碱水制氢是一种常见的制氢生产工艺,它通过碱性溶液电解水分解产生氢气和氧气。
这种工艺具有简单、易操作、安全可靠的优点,在工业中得到了广泛应用。
碱水制氢的主要设备包括电解槽、阳极、阴极、电源等。
电解槽是制氢过程中最重要的设备,它通常由一对金属板组成,其中一块为阳极,另一块为阴极。
阳极和阴极之间通过电源接通电流,将碱性溶液进行电解。
在碱水制氢的过程中,碱性溶液起到电导作用,通过溶液中的电离反应来传递电子。
在阴极处,水分子接受电子,并与碱性溶液中的氢离子结合,生成氢气。
而在阳极处,水分子失去电子,并与碱性溶液中的氧离子结合,生成氧气。
整个过程可表述为:
2H2O + 2e- -> H2 + 2OH- (阴极反应)
2H2O -> O2 + 4H+ + 4e- (阳极反应)
这样,通过电解水的方式,我们可以得到高纯度的氢气和氧气。
制氢设备中的电源一般采用直流电源,控制电解槽中的电流和电压,保证反应的进行和稳定性。
而碱性溶液主要采用氢氧化钾或氢氧化钠溶液,通过调节溶液的浓度和温度,可以控制反应速率和产气效率。
碱水制氢工艺具有许多优点。
首先,该工艺所需设备简单、容易制造和维修,成本相对较低。
其次,碱性溶液作为电解液具
有良好的电导性能,可高效地传递电子。
此外,碱性溶液可重复使用,减少对环境的污染。
最后,碱水制氢的反应较为稳定,操作相对安全可靠。
然而,碱水制氢也存在一些问题。
首先,由于反应中生成的氢气和氧气都是混合在一起的,需要进一步进行分离和纯化,才能得到所需的高纯度氢气。
其次,制氢过程需要较高的能量消耗,电解水的能量效率较低。
此外,由于碱性溶液具有腐蚀性,对设备的材料和密封性要求较高。
综上所述,碱水制氢是一种简单、易操作、安全可靠的制氢生产工艺。
通过电解碱性溶液,我们可以得到高纯度的氢气和氧气。
尽管碱水制氢存在一些问题,但在工业中得到了广泛应用,为各行业提供了重要的氢气资源。
随着科技的发展和工艺的改进,碱水制氢工艺将继续得到优化和改进,为氢能产业的发展做出更大的贡献。
