土壤有机质测定(1)
土壤有机质含量的测定实验报告

土壤有机质含量的测定实验报告
一、实验目的
本实验旨在测定土壤有机质含量,为研究土壤改良、肥料加施、植物生长及土壤质量评价等提供依据。
二、实验原理
本实验使用碱氧化法测定土壤有机质含量,即采用碱液(高氯酸或稀硫酸)氧化有机质,然后通过BaCl2溶液进行检测,最终得出该种有机质的重量分数。
三、实验方法
1.采集土壤样品:采集土壤样品后,按照相应重量(抽样量为300~500g),将土壤样品置于一容器中,接着,加入相应量的分解剂(用1:1酒精醋酸混合物浸泡30min),同时,将土壤样品加入50ml 稀硫酸,摇匀后,用50ml高氯酸进行二次混匀,置于水浴中回收有机质,滤过纸后,收集上清液(碱液)。
2.实验测定:将碱液容器加入适量的BaCl2溶液(比重为1.25),至出现明显的黄色反应,然后,采用稀释法加入分析纯水,调节比重为1.2,通过试管热能计热量法计算土壤有机质含量。
四、实验结果
实验后得出的土壤有机质含量为:31.5%。
五、结论
本实验通过碱氧化法成功地测定了该土壤样品的有机质含量,结果表明,该样品的有机质含量为31.5%。
土壤理化性质测定的方法

1、土壤有机质的测定(重铬酸钾容量法)土壤有机质既是植物矿质营养和有机营养的源泉,又是土壤中异养型微生物的能源物质,同时也是形成土壤结构的重要因素。
测定土壤有机质含量的多少,在一定程度上可说明土壤的肥沃程度。
因为土壤有机质直接影响着土壤的理化性状。
测定原理在加热的条件下,用过量的重铬酸钾—硫酸(K 2Cr 2O 7-H 2SO 4)溶液,来氧化土壤有机质中的碳,Cr 2O -27等被还原成Cr +3,剩余的重铬酸钾(K 2Cr 2O 7)用硫酸亚铁(FeSO 4)标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳量,再乘以常数1.724,即为土壤有机质量。
其反应式为:重铬酸钾—硫酸溶液与有机质作用:2K 2Cr 2O 7+3C+8H 2SO 4=2K 2SO 4+2Cr 2(SO 4)3+3CO 2↑+8H 2O硫酸亚铁滴定剩余重铬酸钾的反应:K 2Cr 2O 7+6FeSO 4+7H 2SO 4=K 2SO 4+Cr 2(SO 4)3+3Fe 2(SO 4)3+7H 2O测定步骤:1.在分析天平上准确称取通过60目筛子(<0.25mm)的土壤样品0.1—0.5g(精确到0.0001g)(0.3000),用长条腊光纸把称取的样品全部倒入干的硬质试管中,用移液管缓缓准确加入0.136mol/L 重铬酸钾—硫酸(K 2Cr 2O 7-H 2SO 4)溶液10ml ,(在加入约3ml 时,摇动试管,以使土壤分散),然后在试管口加一小漏斗。
2.预先将液体石蜡油或植物油浴锅加热至185—190℃,将试管放入铁丝笼中,然后将铁丝笼放入油浴锅中加热,放入后温度应控制在170—180℃,待试管中液体沸腾发生气泡时开始计时,煮沸5分钟,取出试管,稍冷,擦净试管外部油液。
3.冷却后,将试管内容物小心仔细地全部洗入250ml 的三角瓶中,使瓶内总体积在60—70ml,保持其中硫酸浓度为1—1.5mol/l,此时溶液的颜色应为橙黄色或淡黄色。
土壤有机质含量的测定-重铬酸钾发

测定所需试剂1 土壤有机质的测定一重铬酸钾容量法——外热法1 原理:用定量的重铬酸钾-硫酸溶液,在电加热条件下,使土壤中的有机质氧化,剩余的重铬酸钾用硫酸亚铁标准溶液滴定,并以二氧化硅为添加剂作实际空白标定,根据氧化前后氧化剂质量差值,计算出有机碳量,再乘以系数1.724,即为土壤有机质含量。
2 仪器设备:1/10000的分析天平;电沙浴(石蜡浴);大试管;弯颈漏斗;容量瓶定时钟;滴定管: 5.00ml;温度计:200~300℃;铜丝筛:孔径0.25mm;3 试剂除特别注明外,所用试剂皆为分析纯。
3.1 硫酸银:研成粉末;3.2 二氧化硅:粉末状;3.3 邻菲啰啉指示剂:称取邻菲哆啉1.490g溶于含有0.700g硫酸亚铁的100ml水溶液中,此指示剂易变质,应密封保存于棕色瓶中备用;3.4 0.4mol·L-1(1/6 K2Cr2O7重铬酸钾)重铬酸钾-硫酸溶液:称取重铬酸钾40.0g,溶于600~800ml蒸馏水中,待完全溶解后,加水稀释至1L,将溶液移入3L大烧杯中;另取1L比重为1.84的浓硫酸,慢慢的倒入重铬酸钾水溶液中,不断搅动,为避免急剧升温,每加约100ml硫酸后稍停片刻,并把大烧杯放在盛有冷水的盆内冷却,待溶液的温度降到不烫手时再加另一份硫酸,直到全部加完为止;3.50.1m o l·L-1重铬酸钾标准溶液:称取经130℃烘2~3h的优级纯重铬酸钾4.904g。
先用少量水溶解,然后移入1L容量瓶内,加水定容。
3.6 0.1 mol·L-1硫酸亚铁标准溶液:称取FeSO4·7H2O硫酸亚铁28g,溶于600~800ml水中,加浓硫酸20ml,搅拌均匀,加水定容至1L(必要时过滤),贮于棕色瓶中保存。
此溶液易受空气氧化,使用时必须每天标定一次标准浓度。
4 操作步骤:4.1 选取有代表性风干土壤样品,用镊子挑除植物根叶等有机残体,然后用木棍压细,使之通过1mm筛。
土壤有机质含量的测定(精)

实训六土壤有机质含量的测定一、目的要求土壤有机质含量是衡量土壤肥力的重要指标,对了解土壤肥力状况,进行培肥、改土有一定的指导意义。
通过实验了解土壤有机质测定原理,初步掌握测定有机质含量的方法既注意事项。
能比较准确地测出土壤有机质含量。
二、方法原理在加热条件下,用稍过量得标准重铬酸钾—硫酸溶液,氧化土壤有机碳,剩余的重铬酸钾用标准硫酸亚铁(或硫酸亚铁铵)滴定,由所消耗标准硫酸亚铁的量计算出有机碳量,从而推算出有机质的含量,其反应式如下:2K2Cr2O7+3C+8H2SO4→K2SO4+2Cr2(SO4)3+3CO2+8H2OK2Cr2O7+6FeSO4+7H2SO4→K2SO4+ Cr2(SO4)3+3Fe2(SO4)3+8H2O 用Fe2+滴定剩余的K2Cr2O72-时,以邻啡罗啉(C2H8N2)为氧化还原指示剂,在滴定过程中指示剂的变色过程如下:开始时溶液以重铬酸钾的橙色为主,此时指示剂在氧化条件下,呈淡蓝色,被重铬酸钾的橙色掩盖,滴定时溶液逐渐呈绿色(Cr3+),至接近终点时变为灰绿色。
当Fe2+溶液过量半滴时,溶液则变成棕红色,表示颜色已到终点。
三、仪器试剂1. 仪器用具硬质试管(18mm×180mm)、油浴锅、铁丝笼、电炉、温度计(0~200℃)、分析天平(感量0.0001g)、滴定管(25ml)、移液管(5ml)、漏斗(3~4cm),三角瓶(250ml)、量筒(10ml,100ml)、草纸或卫生纸。
2. 试剂配制1.0.1333mol/L重铬酸钾标准溶液称取经过130℃烘烧3~4h的分析纯重铬酸钾39.216g,溶解于400ml蒸馏水中,必要时可加热溶解,冷却后架蒸馏水定容到1000ml,摇匀备用。
2.0.2mol/L硫酸亚铁(FeSO4.7H2O)或硫酸亚铁铵溶液称取化学纯硫酸亚铁55.60g或硫酸亚铁铵78.43g,溶于蒸馏水中,加6mol/L H2SO41.5ml,再加蒸馏水定容到1000ml备用。
土壤有机质的测定

土壤有机质的测定油浴加热重铬酸钾氧化——容量法1 方法提要在加热条件下,用过量的重铬酸钾-硫酸溶液氧化土壤有机碳,多余的重铬酸钾用硫酸亚铁铵标准溶液滴定,以样品和空白消耗重铬酸钾的差值计算出有机碳量。
因本方法与干烧法对比只能氧化90%的有机碳,因此,将测得的有机碳乘以校正系数1.1,再乘以常数1.724(按土壤有机质平均含碳58%计算),即为土壤有机质含量。
2 适用范围本方法适用于有机质含量低于150g·kg-1的土壤有机质的测定。
3 主要仪器设备3.1 油浴锅:用紫铜皮做成或用高度约20cm~26cm的不锈钢锅代替,内装固体石蜡(工业用)。
3.2 硬质试管:18~25mm×200mm;3.3 铁丝笼:大小和形状与油浴锅配套,内有若干小格,每格内可插入一支试管;3.4 滴定管:10.00、25.00mL;3.5 温度计:300o C3.6 电炉:1000W;4 试剂4.1重铬酸钾-硫酸溶液[C(1/6K2Cr2O7)= 0.4mol·L-1]:称取40.0g重铬酸钾溶于600mL~800mL水中,用滤纸过滤到1L量筒内,用水洗涤滤纸,并加水至1L。
将此溶液转移至3L 大烧杯中;另取1L密度为1.84的浓硫酸,慢慢地倒入重铬酸钾水溶液中,不断搅动。
为避免溶液急剧升温,每加约100mL浓硫酸后可稍停片刻,并把大烧杯放在盛有冷水的大塑料盆内冷却,当溶液温度降到不烫手时再加另一份浓硫酸,直到全部加完为止。
4.2 重铬酸钾标准溶液[c(1/6K2Cr2O7)= 0.2000mol·L-1]:准确称取130o C烘2~3小时的重铬酸钾(优级纯)9.807g,先用少量水溶解,然后无损地移入1000mL容量瓶中,加水定容。
4.3硫酸亚铁铵溶液[c(Fe(NH4)2(SO4)2·6H2O)= 0.2mol·L-1]:称取硫酸亚铁铵78.4g,溶解于600mL~800 mL水中,加浓硫酸20mL,搅拌均匀,加水定容至1000mL(必要时过滤),贮于棕色瓶中保存。
土壤有机质含量如何测定?土壤有机质测定方法

土壤有机质含量如何测定?土壤有机质测
定方法
【常见问题】土壤有机质测定方法有哪些?
【专家解答】土壤有机质是土壤的重要组成部分,对土壤形成、土壤肥力、环境保护及农林业可持续发展等方面都有着极其重要作用的意义,下面本人为您介绍几个土壤有机质测定方法:
1、容量法(外加热法)重铬酸钾氧化一油浴加热法来测定土壤有机质含量。
2、重铬酸钾容量法测定土壤中的有机质是用氧化性强的重铬酸钾硫酸溶液与土壤中的有机碳发生氧化还原反应,它们之间存在定量关系。
再用标准还原剂(硫酸亚铁)滴定剩余的重铬酸钾。
3、目视比色法。
测定原理。
用不同浓度的葡萄糖标准溶液作出一系列浓度的标准对照品,并用重铬酸钾氧化土壤有机质,氧化后的溶液颜色与有机质含量成直线相关关系,通过与标准对照品比色对照直接得出结果。
4、灼烧法(重量法)测定原理。
通过测定土壤灼烧前后重量的变化情况,计算出土壤有机质的含量。
5、光度比色法。
测定原理。
该方法是以硫酸亚铁为标准溶液进行土壤有机质的分光光度测定。
【本人结语】土壤有机质与土壤肥力密切相关,呈正对比,土壤有机质含量也可以提高土壤肥力,想知道怎么提高土壤有机质含量的方法可以关注我们网站《提高土壤有机质含量的方法》等文,感谢您的支持。
土壤有机质的测量方法

土壤有机质的测量方法
土壤有机质是土壤中的一种重要组成部分,对于土壤生物活性、水分保持能力和养分供应具有重要的影响。
因此,准确测量土壤有机质含量对于土壤质量评价和农田管理至关重要。
下面将介绍几种常用的土壤有机质测量方法。
1. 燃烧法
燃烧法是最常用的土壤有机质测量方法之一。
该方法通过将土壤样品在高温(约550°C)条件
下加热,将有机物氧化为CO2和H2O,然后使用气体分析仪测量气体体积,从而计算出土壤
中有机物的含量。
2. 红外光谱法
红外光谱法是一种非破坏性的土壤有机质测量方法。
该方法通过将土壤样品置于红外光谱仪中,利用土壤中有机物特定的红外光谱吸收特征,通过对比样品的光谱图和标准光谱图,测量出土壤样品中的有机物含量。
3. 溶解有机碳测量法
溶解有机碳测量法是一种直接测定土壤中溶解态有机碳含量的方法。
该方法将土壤样品置于水中浸泡,通过过滤和酸化等处理,将有机碳转化为溶解态有机碳,再使用专业仪器测定溶解态有机碳的含量。
4. 棕色化测定法
棕色化测定法是一种间接测定土壤有机质含量的方法。
该方法利用土壤中有机质分解的过程中,产生的棕色化物质的形成与土壤样品中有机质含量相关。
通过测定土壤样品中棕色化物质的浓度,可以估计土壤有机质的含量。
需要注意的是,不同的土壤有机质测量方法适用于不同的土壤类型和研究目的。
因此,在选择测量方法时,需要考虑到实际情况和研究需求,并根据标准操作程序进行测试和分析。
此外,为了确保测量结果的准确性,还应注意样品处理和实验条件的控制。
土壤有机质的测定

一、目的要求 土壤有机质是土壤的重要组成部分,是 养料的源泉,它影响着土壤的理化性质。 因此,土壤有机质含量的高低,是衡量土 壤肥力水平的重要标志之一。通过本次实 习要求进一步熟悉实验室基本操作,掌握 测定土壤有机质的基本原理和操作方法。
ห้องสมุดไป่ตู้
二、基本原理
三、方法步骤
称取过0.25mm筛孔的风干土0.1~0.5g,放入一干 称取过0.25mm筛孔的风干土0.1~0.5g,放入一干 燥、洁净的试管中,准确加入0.8molL 燥、洁净的试管中,准确加入0.8molL-1 1/6K2Cr2O7溶液5ml后,再慢慢准确地加浓 溶液5ml后,再慢慢准确地加浓 5ml。将试管放入石蜡锅中,在 大约180度 H2SO45ml。将试管放入石蜡锅中,在 大约180度 的温度下微沸五分钟。 消煮完毕后,将试管从石蜡锅中取出,稍冷后将 试管内液体洗涤收集于三角瓶中,瓶内溶液的总 体积控制在30-35ml左右。向三角瓶内加邻啡啰啉 体积控制在30-35ml左右。向三角瓶内加邻啡啰啉 指示剂2 滴,用0.2molL 指示剂2-3滴,用0.2molL-1FeSO4溶液滴定剩余下 。溶液的变色过程由橙→ 淡绿→ 来的K 来的K2Cr2O7。溶液的变色过程由橙→绿→淡绿→ 橙红→ 橙红→红棕为终点。 同时做行空白实验
四、计算
土壤有机碳
土壤有机质=土壤有机碳化物× 土壤有机质=土壤有机碳化物×1.724
注:空白样由于没有消煮完全,使得滴定 不能产生红棕色。用一个上个班做的空白 样的数据。 V0=21.7ml
土壤有机质及腐殖质组成测定

土壤有机质及腐殖质组成测定Prepared on 22 November 2020土壤有机质及腐殖质组成测定一、土壤有机质测定土壤的有机质含量通常作为土壤肥力水平高低的一个重要指标。
它不仅是土壤各种养分特别是氮、磷的重要来源,并对土壤理化性质如结构性、保肥性和缓冲性等有着积极的影响。
测定土壤有机质的方法很多。
本实验用重铬酸钾容量法。
(一)重铬酸钾容量法1、方法原理:在170—180℃条件下,用过量的标准重铬酸钾的硫酸溶液氧化土壤有机质(碳),剩余的重铬酸钾以硫酸亚铁溶液滴定,从所消耗的重铬酸钾量计算有机质含量。
测定过程的化学反应式如下:2K2Cr207+3C+8H2S04——→2K2S04十2Cr2(SO4)3+3CO2+8H20K2Cr207+6FeSO4+7H2S04——→K2S04十Cr2(SO4)3+3Fe2(SO4)3+7H202、操作步骤方法一:(1)准确称取通过筛孔的风干土样克,倒入干燥硬质玻璃试管中,加入(1/6 K2Cr207)毫升,再用注射器注入5毫升浓硫酸,小心摇匀,管口放一小漏斗,以冷凝蒸出的水汽。
试管插入铁丝笼中。
(2)预先将热浴锅(石蜡或磷酸)加热到180—185℃,将插有试管的铁丝笼放入热浴锅中加热,待试管内溶液沸腾时计时,煮沸5分钟,取出试管,稍冷,擦去试管外部油液。
消煮过程中,热浴锅内温度应保持在170—180℃。
(3)冷却后,将试管内溶液小心倾入250毫升三角瓶中,并用蒸馏水冲洗试管内壁和小漏斗,洗入液的总体积应控制在50毫升左右,然后加入邻啡罗林指示剂3滴,用滴定溶液,先由黄变绿,再突变到棕红色时即为滴定终点(要求滴定终点时溶液中H2SO4的浓度为1—)。
(4)测定每批(即上述铁丝笼中)样品时,以灼烧过的土壤代替土样作二个空白试验。
方法二:(1)准确称取通过筛孔的风干土样克,倒入150ml三角瓶中,加入(1/6 K2Cr207)毫升,再用注射器注入5毫升浓硫酸,小心摇匀,管口放一小漏斗,以冷凝蒸出的水汽。
土壤有机质的测定(精)

CO--CO2
MnO2
纯 化 阱 ) 球形 CO2 吸收阱 和 ( 碱 石 灰
H2SO4
CuO
HClO4
H2SO4
HClO4
)
3.2.2 湿烧法将C→CO2测定OM的原理
土壤与含有氧化剂(重铬酸钾、铬酸高锰酸 钾等)、硫酸和磷酸的混合物消化,在煮沸的温 度下(180~210 ℃)可将有机物完全氧化为CO2,用适
含量:%数量级。
分布: – 受生物气候带、质地和农耕措施的影响由北→南, 东→西逐步降低。
问题: 若个别样品有机质含量特别高,原因是什么?
中国土壤有机质含量图
全国水田土壤有机质和全氮含量分级 * 面积统计 (万公顷)
级别 一级 273.46 有机质 (8.95)** 394.56 全氮 (12.92) 二级 541.87 (17.74) 706.35 (23.12) 三级 1038.62 (34) 1025.03 (33.55) 四级 795.02 (26.02) 421.53 (13.8) 五级 71.71 (2.35) 146.63 (4.8) 六级 21.39 (0.7) 47.95 (1.57)
问题: 1、从反应原理看,还可以用哪些方法进行测定?
2、方法的优缺点和适用范围如何?
有机碳的氧化校正系数
有机质含量的计算:
Van Bemmelen Factor=1.724 (也有人用1.9~2.5)
仪器、试剂、操作和计算
1、仪器:控温电炉、油浴锅等。 2、试剂:0.8000mol/L (1/6K2Cr2O7)等。
K2Cr2O7标准液和浓H2SO4各5ml →180 ℃沸5min →冷 却后洗入250mL三角瓶至体积60~70mL →邻啡罗啉 指示剂3滴→FeSO4滴定由橙黄-亮绿-砖红色。(每批 消化同时做空白)
土壤有机质测定

有机质测定方法—— 外加热重铬酸钾容量法
2K2CrO7 + 8H2SO4 + 3C → 2K2SO4 + 2Cr(SO4)3 + 3CO2 + 8H2O 2K2CrO7 + 6FeSO4 + 7H2SO4 → K2SO4 + 3Cr(SO4)3 + 3Fe2(SO4)3 + 7H2O 与干烧法相比,该法只能氧化90%有机碳。 滴定酸度:1mol/L H2SO4 ; 突跃电位:0.85~1.22V。
土壤有机质的测定
有机质(OM)的形态 包括三类形态:
2、动植物残体的半分解产物及微生物代谢产物;
3、有机质分解和合成的较稳定的高分子化合物—— 腐殖酸类物质。 土壤有机质——(除专门研究外)指操作者借 助放大镜用摄子剔除动物残体和植物细根后的 土壤有机物质总量。
1、分解很少,仍保持原来形态学特征的动植物残体;
方法原理
在加热条件下,用稍过量的标准重铬酸钾—硫酸溶液,氧化土 壤有机碳,剩余的重铬酸钾用标准硫酸亚铁(或硫酸亚铁铵) 滴定,由所消耗标准硫酸亚铁的量计算出有机碳量,从而推算 出有机质的含量,其反应式如下:
2K2CrO7 + 8H2SO4 + 3C → 2K2SO4 + 2Cr(SO4)3 + 3CO2 + 8H2O 2K2CrO7 + 6FeSO4 + 7H2SO4 → K2SO4 + 3Cr(SO4)3 + 3Fe2(SO4)3 + 7H2O
问题: 如何降低动植物残体对测定结果的影响,提高测定结果的精密度?
OM的含量与分布
含量:%数量级。 分布:
受生物气候带、质地和农耕措施的影响由北→南,东 →西逐步降低。
土壤有机质含量的测定 重铬酸钾

土壤有机质含量的测定重铬酸钾土壤有机质是土壤中的一种重要成分,对土壤肥力和农作物的生长发育具有重要影响。
因此,准确测定土壤有机质含量对于土壤肥力评价和合理施肥具有重要意义。
本文将介绍一种测定土壤有机质含量的方法——重铬酸钾法,并详细介绍其操作步骤和注意事项。
重铬酸钾法是测定土壤有机质含量的经典方法之一。
该方法利用重铬酸钾作为氧化剂,将土壤中的有机物氧化为二氧化碳和水,并通过测定反应过程中的铬酸盐的消耗量来计算土壤中的有机质含量。
具体操作步骤如下:步骤一:样品的处理1. 从不同位置采集土壤样品,并将其混合均匀。
2. 将样品中的杂质和根系等物质去除,留下土壤颗粒。
3. 将土壤颗粒晾干,并过一筛,以获得均匀的颗粒。
步骤二:制备试剂1. 准备重铬酸钾溶液,将适量重铬酸钾溶解在蒸馏水中,得到浓度为0.5 mol/L的重铬酸钾溶液。
2. 准备硫酸铁铵试剂,将适量硫酸铁铵溶解在蒸馏水中,得到浓度为0.5 mol/L的硫酸铁铵溶液。
步骤三:进行实验1. 取精确的样品重量(通常为10克),放入锥形瓶中。
2. 加入适量的重铬酸钾溶液,并用搅拌棒充分搅拌均匀。
3. 加入少量硫酸铁铵试剂,并再次充分搅拌均匀。
4. 盖上锥形瓶,在摇床上以较慢的速度摇荡,使反应充分进行。
5. 取一空白锥形瓶,用相同的方法进行反应。
6. 当反应液由鲜橙色变为绿色时,表示土壤中的有机物已被完全氧化。
7. 记录反应液的颜色,可以根据颜色的深浅估计有机质含量的多少。
步骤四:计算有机质含量1. 根据反应液的颜色深浅,将其与标准曲线进行比较,得到有机质的质量浓度。
2. 根据所取样品的质量和溶液的体积,计算出土壤中的有机质含量。
重铬酸钾法测定土壤有机质含量的结果可信度较高,但在操作过程中也需要注意以下几点:1. 正确选择土壤样品。
样品应尽可能代表待测区域的整体情况,避免单一土壤类型或区域的干扰。
2. 操作过程中避免皮肤接触试剂,以免引起刺激或损伤。
3. 严格按照实验步骤进行操作,尽量减少操作误差,保证实验结果的准确性。
土壤有机质的测定实验报告

土壤有机质的测定实验报告实验目的:掌握土壤有机质含量的测定方法,了解土壤有机质对土壤肥力的影响。
实验原理:土壤有机质是土壤中的一种重要组成部分,对土壤的肥力和水分保持能力起着重要作用。
测定土壤有机质含量的目的是为了评估土壤的质量和肥力。
常用的测定土壤有机质的方法有色度法和高温燃烧法。
本实验使用高温燃烧法测定土壤有机质含量。
实验步骤:1. 实验前准备:a. 将待测土壤样品晾干并研磨成细粉末状。
b. 称取10克土壤样品放入坩埚。
c. 将坩埚放入已预热至550℃的炉中燃烧2小时。
d. 取出坩埚并冷却至室温。
e. 将坩埚和残余物重量分别称量。
2. 实验操作:a. 将之前称量好的坩埚和残余物放入干燥器中,干燥30分钟。
b. 取出坩埚和残余物并冷却至室温。
c. 称量坩埚和残余物的质量。
d. 计算土壤有机质含量。
实验数据:1. 土壤样品重量(g):10.002. 坩埚和残余物的质量(g):- 坩埚和残余物重量(燃烧后):7.20- 坩埚重量(燃烧后):3.40实验结果和分析:根据实验数据,可以计算土壤有机质含量的百分比。
计算方法如下:土壤有机质含量(%)= (坩埚和残余物重量 - 坩埚重量) / 土壤样品重量 * 100代入实验数据得到:土壤有机质含量(%)= (7.20 - 3.40) / 10.00 * 100 = 38.0%实验结论:通过高温燃烧法测定,本实验得到的土壤样品的有机质含量为38.0%。
有机质含量是衡量土壤肥力的重要指标,本实验结果表明该土壤样品具有较高的有机质含量,说明该土壤具有较好的肥力和水分保持能力。
实验注意事项:1. 实验过程中需注意安全,操作时需佩戴实验手套和眼镜。
2. 实验设备需提前进行清洁和烘干处理,以免影响实验结果。
3. 注意保持实验环境的清洁和整洁,避免外来污染对实验结果产生干扰。
4. 实验前后要准确称量土壤样品和坩埚,并记录质量数据,以确保实验结果的准确性。
以上是土壤有机质的测定实验报告,实验结果表明本实验使用的土壤样品具有较高的有机质含量。
土壤 有机质的测定

土壤有机质的测定土壤是地球上一种非常重要的自然资源,其质地的好坏直接关系着农作物的生长和土壤生态系统的平衡。
而土壤中的有机质作为土壤的重要组成部分,在维持土壤生态系统平衡和提高土壤肥力等方面起着至关重要的作用。
因此,对土壤中有机质的测定成为了土壤学领域的重要研究内容。
一、有机质的定义与重要性有机质是指土壤中的含碳有机物质,包括残体和异化物质或其分解产物。
有机质的主要来源包括植物残体、动物残体、微生物生物体、泥煤、煤等。
有机质在土壤中具有多种功能,首先,有机质是土壤中最活跃的有机物,对土壤肥力的影响最为显著。
其次,有机质是土壤中微生物的营养基础,对土壤微生物生长繁殖发挥着至关重要的作用。
最后,有机质还能改善土壤的物理性状,提高土壤的透水性和保水性,对土壤结构的改良至关重要。
二、有机质的测定方法1. 燃烧法燃烧法是目前应用最为广泛的有机质测定方法之一。
其原理是将土壤样品在高温下氧化燃烧,通过测定燃烧后残渣中的无机物质的含量,计算出有机质的含量。
燃烧法的优点是简单、快速、准确,但也存在着对仪器设备和实验操作技术的要求较高的缺点。
2. 酸碱氧化法酸碱氧化法是另一种常用的有机质测定方法。
其原理是将土壤样品用酸性或碱性氧化剂处理,将土壤中的有机质转化为无机物质,再通过测定无机物质的含量,计算出有机质的含量。
酸碱氧化法的优点是操作简便,适用于多种土壤类型,但也存在着操作过程中易受外界因素影响的缺点。
3. 光谱法光谱法是近年来发展起来的一种新型有机质测定方法。
其原理是通过测定土壤样品在不同波长下的吸收光谱,推算出土壤中的有机质含量。
光谱法具有快速、无损伤、高效的优点,但也存在着操作难度较大、需要专业知识和设备等缺点。
三、影响有机质测定的因素1. 土壤类型不同类型的土壤中有机质的含量差异较大,因此在测定有机质时需要根据土壤类型的不同采用不同的测定方法和标准。
2. 土壤pH值土壤的pH值对有机质的测定有一定的影响,通常情况下,酸性土壤中有机质的释放会比碱性土壤中多一些。
土壤有机质的测定
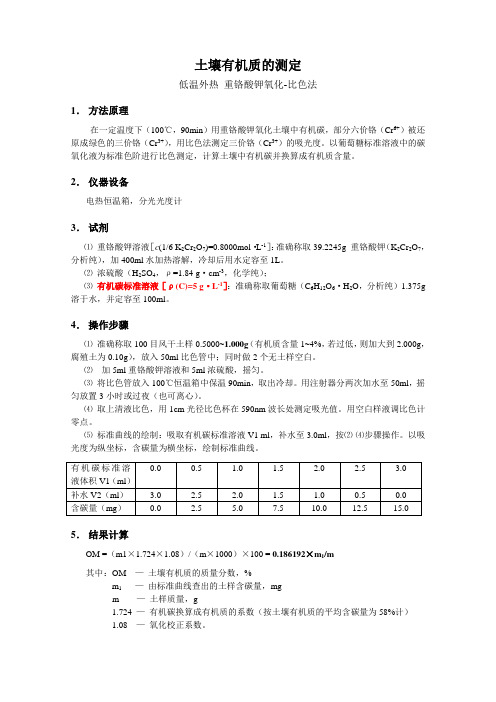
土壤有机质的测定低温外热重铬酸钾氧化-比色法1.方法原理在一定温度下(100℃,90min)用重铬酸钾氧化土壤中有机碳,部分六价铬(Cr6+)被还原成绿色的三价铬(Cr3+),用比色法测定三价铬(Cr3+)的吸光度。
以葡萄糖标准溶液中的碳氧化液为标准色阶进行比色测定,计算土壤中有机碳并换算成有机质含量。
2.仪器设备电热恒温箱,分光光度计3.试剂⑴重铬酸钾溶液[c(1/6 K2Cr2O7)=0.8000mol·L-1]:准确称取39.2245g 重铬酸钾(K2Cr2O7,分析纯),加400ml水加热溶解,冷却后用水定容至1L。
⑵浓硫酸(H2SO4,ρ=1.84 g·cm-3,化学纯);⑶有机碳标准溶液[ρ(C)=5 g·L-1]:准确称取葡萄糖(C6H12O6·H2O,分析纯)1.375g 溶于水,并定容至100ml。
4.操作步骤⑴准确称取100目风干土样0.5000~1.000g(有机质含量1~4%,若过低,则加大到2.000g,腐殖土为0.10g),放入50ml比色管中;同时做2个无土样空白。
⑵加5ml重铬酸钾溶液和5ml浓硫酸,摇匀。
⑶将比色管放入100℃恒温箱中保温90min,取出冷却。
用注射器分两次加水至50ml,摇匀放置3小时或过夜(也可离心)。
⑷取上清液比色,用1cm光径比色杯在590nm波长处测定吸光值。
用空白样液调比色计零点。
⑸标准曲线的绘制:吸取有机碳标准溶液V1 ml,补水至3.0ml,按⑵-⑷步骤操作。
以吸光度为纵坐标,含碳量为横坐标,绘制标准曲线。
5.结果计算OM =(m1×1.724×1.08)/(m×1000)×100 = 0.186192×m1/m其中:OM —土壤有机质的质量分数,%m1—由标准曲线查出的土样含碳量,mgm—土样质量,g1.724 —有机碳换算成有机质的系数(按土壤有机质的平均含碳量为58%计)1.08 —氧化校正系数。
土壤有机质的测定实验报告

土壤有机质的测定实验报告一、实验目的土壤有机质是土壤的重要组成部分,它对土壤的肥力、结构和生态功能有着重要影响。
本实验的目的是掌握测定土壤有机质含量的方法,了解土壤有机质的特性和在土壤中的作用,为土壤肥力评估和农业生产提供科学依据。
二、实验原理在加热条件下,用一定浓度的重铬酸钾硫酸溶液氧化土壤中的有机碳,剩余的重铬酸钾用硫酸亚铁标准溶液滴定,根据消耗的重铬酸钾量计算出有机碳含量,再乘以常数 1724,即为土壤有机质含量。
反应方程式为:2K₂Cr₂O₇+ 3C + 8H₂SO₄= 2K₂SO₄+ 2Cr₂(SO₄)₃+3CO₂↑ + 8H₂OK₂Cr₂O₇+ 6FeSO₄+ 7H₂SO₄= K₂SO₄+ Cr₂(SO₄)₃+3Fe₂(SO₄)₃+ 7H₂O三、实验仪器和试剂1、仪器分析天平:精确到 00001g。
硬质玻璃试管:25mm×200mm。
油浴锅:内装固体石蜡或植物油。
铁丝笼:能插入试管并固定在油浴锅中。
温度计:0 200℃。
滴定管:25ml 或 50ml。
移液管:5ml、10ml、20ml。
三角瓶:250ml。
小漏斗。
2、试剂08000mol/L 重铬酸钾标准溶液:称取 392245g 重铬酸钾(K₂Cr₂O₇,分析纯)溶于水中,定容至 1000ml。
02mol/L 硫酸亚铁标准溶液:称取560g 硫酸亚铁(FeSO₄·7H₂O,分析纯)溶于水中,加 15ml 浓硫酸,冷却后用水稀释至 1000ml。
使用前用 01mol/L 重铬酸钾标准溶液标定。
浓硫酸(H₂SO₄,ρ=184g/cm³,化学纯)。
邻菲啰啉指示剂:称取 1485g 邻菲啰啉(C₁₂H₈N₂·H₂O)和0695g 硫酸亚铁(FeSO₄·7H₂O)溶于 100ml 水中,贮于棕色瓶中。
四、实验步骤1、称取通过 025mm 筛孔的风干土样 01000 05000g(精确到00001g),放入干燥的硬质玻璃试管中。
土壤有机质的测定(油浴加热重铬酸钾容量法)

土壤有机质的测定(油浴加热重铬酸钾容量法)土壤有机质是土壤的重要组成部分,土壤的许多属性都直接或间接地与有机质的存在相关。
在现代农业生产中,增施有机肥料仍是作物高产高效必不可少的重要措施。
土壤有机质主要来源于各种植物茎、秆、根茬和落叶,土壤中的动物和微生物以及施入的各种有机肥料。
土壤有机质的组成是很复杂的,包括以下三类物质:第一,分解很少,仍保持原来形态的动植物残体。
第二,动植物残体的半分解产物及微生物的代谢产物。
第三,有机质的分解和合成而形成的特殊有机物质—腐殖质。
有机质中含有N、P、C、H、O、S等植物所必需的营养元素,所以是土壤养分的重要来源。
另外还含有少量的灰分元素如Mg、K、Fe、Si及B、Mn、Cn等一些微量元素,因此,一般来说土壤有机质含量的多少,是土壤肥力高低的一个重要组成指标。
1方法原理在加热的条件下,用过量的重铬酸钾—硫酸溶液氧化土壤有机碳,多余的重铬酸钾用硫酸亚铁溶液滴定,由消耗的重铬酸钾量按氧化校正系数计算出有机碳的量,再乘以1.724,即为土壤有机质的含量。
化学反应如下:2K2Cr2O7+8H2SO4+3C→2K2SO4+2Cr Y2(SO4)3+3CO2↑+8H2O,多余的K2Cr2O7的还原:K2Cr2O7+6FeSO4+7H2SO4→K2SO4+Cr2(SO4)3+3Fe2(SO4)3 +7H2O 2主要仪器设备电炉:1000W;硬质试管:25mm×200mm;油浴锅:用紫铜皮做成或用高度约为15~20cm的铝锅代替,内装甘油(工业用)或固体石腊(工业用);铁丝笼:大小、形状与油浴锅相配套,内装有若干个小格,每格内可插入1支小试管;自动调零滴定管;温度计:300℃;三角瓶:250mL三角瓶;小玻璃漏斗。
3试剂3.10.40mol/L重铬酸钾-硫酸溶液称取40g(化学纯)重铬酸钾,溶于600~800mL蒸溜水使其溶解,加水至1 000mL,将此溶液转移到3 000ml大烧杯中;另取浓硫酸(密度为1.84,化学纯) 1 000mL慢慢倒入重铬酸钾水熔液中不断搅动,为避免溶液急剧升温,每加100mL浓硫酸后可稍停片刻,并把大烧杯放在盛有冷水的大塑料盆内冷却,当溶液的温度下降到不烫手时再加浓硫酸,直到全部加完为止。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
土壤有机质测定5.2.1重铬酸钾容量法——外加热法5.2.1.1方法原理在外加热的条件下(油浴的温度为180,沸腾5分钟),用一定浓度的重铬酸钾——硫酸溶液氧化土壤有机质(碳),剩余的重铬酸钾用硫酸亚铁来滴定,从所消耗的重铬酸钾量,计算有机碳的含量。
本方法测得的结果,与干烧法对比,只能氧化90%的有机碳,因此将得的有机碳乘以校正系数,以计算有机碳量。
在氧化滴定过程中化学反应如下:2K2Cr2O7+8H2SO4+3C→2K2SO4+2Cr2(SO4)3+3CO2+8H2OK2Cr2O7+6FeSO4→K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H20在1mol·L-1H2SO4溶液中用Fe2+滴定Cr2O72-时,其滴定曲线的突跃范围为1.22~0.85V。
从表5—4中,可以看出每种氧化还原指示剂都有自己的标准电位(E0),邻啡罗啉(E0=1.11V),2-羧基代二苯胺(E0=1.08V),以上两种氧化还原指示剂的标准电位(E0),正落在滴定曲线突跃范围之内,因此,不需加磷酸而终点容易掌握,可得到准确的结果。
例如:以邻啡罗啉亚铁溶液(邻二氮啡亚铁)为指示剂,三个邻啡罗啉(C2H8N2)分子与一个亚铁离子络合,形成红色的邻啡罗啉亚铁络合物,遇强氧化剂,则变为淡蓝色的正铁络合物,其反应如下:[(C12H8N2)3Fe]3++e [(C12H8N2)3Fe]2+淡蓝色红色滴定开始时以重铬酸钾的橙色为主,滴定过程中渐现Cr3+的绿色,快到终点变为灰绿色,如标准亚铁溶液过量半滴,即变成红色,表示终点已到。
但用邻啡罗啉的一个问题是指示剂往往被某些悬浮土粒吸附,到终点时颜色变化不清楚,所以常常在滴定前将悬浊液在玻璃滤器上过滤。
从表5-4中也可以看出,二苯胺、二苯胺磺酸钠指示剂变色的氧化还原标准电位(E0)分别为0.76V、0.85V。
指示剂变色在重铬酸钾与亚铁滴定曲线突跃范围之外。
因此使终点后移,为此,在实际测定过程中加入NaF或H3PO4络合Fe3+,其反应如下:Fe3++2PO-34Fe(PO4)-32Fe3++6F-[FeF6]3-加入磷酸等不仅可消除Fe3+的颜色,而且能使Fe3+/Fe2+体系的电位大大降低,从而使滴定曲线的突跃电位加宽,使二苯胺等指示剂的变色电位进入突跃范围之内。
根据以上各种氧化还原指示剂的性质及滴定终点掌握的难易,推荐应用2-羧基二苯胺。
价格便宜,性能稳定,值得推荐采用。
5.2.1.2主要仪器油浴消化装置(包括油浴锅和铁丝笼)、可调温电炉、秒表、自动控温调节器。
5.2.1.3试剂(1)0.008mol·L-1(1/6K2Cr2O7)标准溶液。
重铬酸钾放入干燥箱中120℃烘干2h后,放入干燥器中冷却至室温后称取39.2245g(K2Cr2O7,分析纯)加入400mL 水,加热溶解,冷却后用水定容至1L。
重铬酸钾放入干燥箱前简单称量下其质量,使质量大于39.2245g,经验,称取42g以上即可。
用完后多余的药品可以放回去。
(2)H2SO4。
浓硫酸(H2SO4,GB625-77,分析纯)。
(3)0.2mol·L-1FeSO4溶液。
称取硫酸亚铁(FeSO4·7H2O,GB664-77,分析纯)56.0g溶于水中,加浓硫酸5mL,稀释至1mL。
(4)指示剂①邻啡罗啉指示剂:称取邻啡罗啉(GB1293-77,分析纯)1.485g)与FeSO4·7H2O0.695g,溶于100mL水中。
②2-羧基代二苯胺(O-phenylanthranilicacid,又名邻苯氨基苯甲酸,C13H11O2N))指示剂:称取0.25g试剂于小研钵中研细,然后倒入100mL小烧杯中,加入0.18mol·L-1NaOH溶液12mL,并用少量水将研钵中残留的试剂冲洗入100mL小烧杯中,将烧杯放在水浴上加热使其溶解,冷却后稀释定容到250mL,放置澄清或过滤,用其清液。
(5)Ag2SO4。
硫酸银(Ag2SO4,HG3-945-76,分析纯),研成粉末。
(6)SiO2。
二氧化硅(SiO2,Q/HG22-562-76,分析纯),粉末状。
5.2.1.4操作步骤称取通过0.149mm(100目)筛孔的风干土样0.1~1g(精确到0.0001g),放入一干燥的硬质试管中,用移液管准确加入0.8000mol·L-1(1/6K2Cr2O7)标准溶液5mL(如果土壤中含有氯化物需先加入Ag2SO40.1g),用注射器加入浓H2SO45mL充分摇匀,管口盖上弯颈小漏斗,以冷凝蒸出之水汽。
将8~10个试管放入自动控温的铝块管座中(试管内的液温控制在约170℃),[或将8~10个试管盛于铁丝笼中(每笼中均有1~2个空白试管),放入温度为185~190℃的石蜡油锅中,要求放入后油浴锅温度下降至170~180℃左右,以后必须控制电炉,使油浴锅内始终内维持在170~180℃],待试管内液体沸腾发生气泡时开始计时,煮沸5min,取出试管(用油浴法,稍冷,擦净试管外部油液)。
冷却后,将试管内容物倾入250mL 三角瓶中,用水洗净试管内部及小漏斗,这三角瓶内溶液总体积为60~70mL ,保持混合液中(1/2H 2SO 4)浓度为2~3mol·L -1,然后加入2-羧基代二苯胺指示剂12~15滴,此时溶液呈棕红色。
用标准的0.2mol·L -1硫酸亚铁滴定,滴定过程中不断摇动内容物,直至溶液的颜色由棕红色经紫色变为暗绿(灰蓝绿色),即为滴定终点。
如用邻啡罗啉指示剂,加指示剂2~3滴,溶液的变色过程中由橙黄→蓝绿→砖红色即为终点。
记取FeSO 4滴定毫升数(V )。
每一批(即上述每铁丝笼或铝块中)样品测定的同时,进行2~3个空白试验,即取0.500g 粉状二氧化硅代替土样,其他手续与试样测定相同。
记取FeSO 4滴定毫升数(V 0),取其平均值。
5.2.1.5结果计算土壤有机碳(g·kg -1)=10001.10.310)(5300⨯⨯⨯⨯⨯-⨯⨯-km V V V c 式中:c ——0.8000 mol·L -1 (1/6K 2Cr 2O 7)标准溶液的浓度;5——重铬酸钾标准溶液加入的体积(mL );V 0——空白滴定用去FeSO 4体积(mL );V ——样品滴定用去FeSO 4体积(mL );3.0——1/4碳原子的摩尔质量(g·mol -1);10-3——将mL 换算为L ;1.1——氧化校正系数;m ——风干土样质量(g);k ——将风干土样换算成烘干土的系数。
5.2.1.6注释:注1.含有机质高于50g·kg -1者,称土样0.1g ,含有机质高于20~30g·kg -1者,称土样0.3g ,少于20g·kg -1者,称土样0.5g 以上。
由于称样量少,称样时应用减重法以减少称样误差。
注2.土壤中氯化物的存在可使结果偏高。
因为氯化物也能被重铬酸钾所氧化,因此,盐土中有机质的测定必须防止氯化物的干扰,少量氯可加少量Ag 2SO 4,使氯根沉淀下来(生成AgCl )。
Ag 2SO 4的加入,不仅能沉淀氯化物,而且有促进有机质分解的作用。
据研究,当使用Ag 2SO 4时,校正系数为1.04,不使用Ag 2SO 4时校正系数为1.1Ag 2SO 4的用量不能太多,约加0.1g ,否则生成Ag 2Cr 2O 7沉淀,影响滴定。
在氯离子含量较高时,可用一个氯化物近似校正系数1/12来校正之,由于Cr 2O 7-1与Cl -1及C 的反应是定量的:Cr 2O 72-+6Cl -1+14H +→2Cr 3++3Cl 2+7H 2O2Cr 2O 72-+3C+16H +→4Cr 3+3CO 2+8 H 2O由上二个反应式可知C/4Cl-1=12/4×35.5≈1/12土壤含碳量(g·kg-1)=未经校正土壤含碳量(g·kg-1)-12) (1-⋅kggCl含量土壤此校正系数在Cl:C比为5:1以下时适用。
注3.对于水稻土、沼泽土和长期渍水的土壤,由于土壤中含有较多的Fe2+、Mn2+及其它还原性物质,它们也消耗K2Cr2O7,可使结果偏高,对这些样品必须在测定前充分风干。
一般可把样品磨细后,铺成薄薄一层,在室内通风处风干10天左右即可使Fe2+全部氧化。
长期沤水的水稻土,虽经几个月风干处理,样品中仍有亚铁反应,对这种土壤,最好采用铬酸磷酸湿烧——测定二氧化碳法(见5.2.2)。
注4.这里为了减少0.4mol·L-1(1/6K2Cr2O7)—H2SO4溶液的黏滞性带来的操作误差,准确加入0.800mol·L-1(1/6K2Cr2O7)水溶液5mL及浓H2SO45mL,以代替0.4mol·L-1(1/6K2Cr2O7) 溶液10mL。
在测定石灰性土壤样品时,也必须慢慢加入K2Cr2O7—H2SO4溶液,以防止由于碳酸钙的分解而引起激烈发泡。
注5.最好不采用植物油,因为它可被重铬酸钾氧化,而可能带来误差。
而矿物油或石蜡对测定无影响。
油浴锅预热温度当气温很低时应高一些(约200℃)。
铁丝笼应该有脚,使试管不与油浴锅底部接触。
注6.用矿物油虽对测定无影响,但空气污染较为严重,最好采用铝块(有试管孔座的)加热自动控温的方法来代替油浴法。
注7.必须在试管内溶液表面开始沸腾才开始计算时间。
掌握沸腾的标准尽量一致,然后继续消煮5min,消煮时间对分析结果有较大的影响,故应尽量记时准确。
注8.消煮好的溶液颜色,一般应是黄色或黄中稍带绿色,如果经绿色为主,则说明重铬酸钾用量不足。
在滴定时消耗硫酸亚铁量小于空白用量的1/3时,有氧化不完全的可能,应弃去重做。
N的测定1试剂配制1.1混合催化剂:硫酸钾(K2SO4)100g,硫酸铜(CuSO4)10g,硒(Se)1g,分别研磨成粉,再混合均匀。
1.2硫酸(H2SO4,ρ=1.84g•cm-3)。
1.3NaOH溶液:200g氢氧化钠放入500ml的烧杯中,加入500ml的蒸馏水。
溶解冷却后,存入塑料瓶中。
1.4混合指示剂:容积0.099g的溴甲酚绿和0.066g的甲基红于100ml的乙醇(95%)。
1.5硼酸指示剂溶液:溶解20g硼酸于950ml的热蒸馏水中,冷却后,加入20ml的混指示剂,充分混合后,小心滴加氢氧化钠溶液,直到溶液呈红紫色,pH约为4.5,定容1L。
1.6硫酸标准液:先配制C(H2SO4)=0.08367mol•L-1溶液,2.23ml的浓H2SO4(ρ=1.84g•cm-3))溶入400ml的蒸馏水中,然后定容至500ml。
2操作步骤总氮采用凯氏消煮法。
