高二化学《有机化合物的结构特点》知识点归纳总结 例题解析
有机化合物的结构与性质总结知识点总结

有机化合物的结构与性质总结知识点总结有机化合物的结构与性质总结有机化合物是由碳原子与氢原子以及其他元素的原子通过共价键连接而成的化合物。
它们是生命体中的基本组成部分,也是许多化学过程中不可或缺的原料。
本文将对有机化合物的结构与性质进行总结,并探讨其在化学中的应用。
一、有机化合物的结构有机化合物的结构可以通过其分子式和结构式来表示。
分子式是由化合物中各个原子的符号及其个数组成的简略表达式,如C6H12O6表示葡萄糖。
结构式则更为详细地展示了各个原子之间的连接关系。
有机化合物的结构中包含着碳原子的特殊性质。
碳原子有着四个价电子,因此它可以与其他四个原子形成共价键。
这种四个原子或基团分布在碳原子周围的结构被称为碳原子的化学环境。
根据碳原子周围的基团不同,化合物的性质也会有所不同。
二、有机化合物的性质1. 物理性质有机化合物的物理性质主要包括颜色、气味、溶解性、密度和沸点等。
不同的有机化合物由于其结构的不同,具有不同的物理性质。
例如,醇类化合物由于其分子中带有羟基(-OH)团,因此具有较高的沸点和相对较好的溶解性。
2. 化学性质有机化合物的化学性质是指其与其他化合物或物质发生化学反应的能力。
有机化合物的化学性质主要受到其分子结构和功能团的影响。
例如,醛类化合物具有较强的氧化性,容易与氧发生反应生成羧酸。
3. 功能团对性质的影响在有机化合物中,功能团是一类具有特定化学性质和反应活性的原子或原子团。
不同的功能团会赋予化合物特定的性质和反应特点。
例如,羧酸功能团的存在使得化合物具有较强的酸性,可以与碱反应生成盐。
三、有机化合物的应用有机化合物广泛应用于生命科学、医药、农业和化工等领域。
1. 生命科学许多有机化合物是生命体内必需的物质,如氨基酸、核酸和糖类等。
它们在蛋白质合成、遗传信息传递和能量代谢等生命活动中起到重要作用。
2. 医药有机化合物在药物研发和制造中起着关键的作用。
许多药物都是由有机化合物合成而成的,如抗生素、抗癌药物等。
最新人教版高中化学《有机化合物的结构特点》知识梳理

第二节有机化合物的结构特点答案:(1)4 (2)4 (3)双键(4)三键(5)正四面体立体结构 (6)分子组成(7)结构(8)碳原子间的连接顺序即碳骨架(9)官能团或取代基的位置(10)具有不同的官能团1.有机化合物中碳原子的成键特点(1)碳原子的结构及成键特点碳元素位于元素周期表第二周期ⅣA 族,碳原子结构示意图为,碳原子电子式为·C ···,碳原子最外层有4个价电子,不易失去或获得电子而形成阳离子或阴离子。
碳原子通过共价键与氢、氧、氮、硫、磷等多种非金属元素形成共价化合物。
一个碳原子可形成4个共价键。
(2)有机化合物中碳原子的结合方式①碳原子与碳原子之间能以共价键结合。
碳原子间不仅可以形成稳定的单键(),还可以形成稳定的双键()或三键(—C≡C—)。
②多个碳原子可以相互结合成长短不一的碳链,碳链也可以带有支链,还可以结合成碳环,碳链和碳环也可以相互结合。
如:等。
③碳原子也可与H 、O 、N 、S 等多种元素的原子形成共价键,如—C —H 、、—C≡N 等。
④含有原子种类和数目相同的分子,其原子可能具有不同的结合方式,形成具有不同结构的分子。
如分子组成为C 4H 10的物质就可以有以下两种结构:CH 3—CH 2—CH 2—CH 3、以上因素造成了有机物种类繁多,数量庞大。
(3)甲烷的分子结构分子式 电子式 结构式 结构简式 球棍模型 比例模型甲烷CH4CH4②甲烷分子的空间构型甲烷分子里,1个碳原子与4个氢原子形成4个共价键,构成以碳原子为中心,4个氢原子位于四个顶点的正四面体结构。
(4)键参数能表征化学键性质的物理量称为键参数。
共价键的键参数主要有键能、键长、键角等。
①键长:成键2个原子的原子核间的距离称为键长。
②键角:分子中1个原子与另外2个原子形成的两个共价键在空间的夹角称为键角。
碳原子类型碳原子成键方式分子空间构型典型代表物饱和碳原子四面体形CH4不饱和碳原子双键碳平面形CH2===CH2三键碳—C≡C—直线形CH≡CHH—C≡C—H 苯环上的碳平面正六边形C6H6能。
高中化学第一章第2节 有机化合物的结构特点知识点

第二节有机化合物的结构特点一、有机化合物中碳原子的成键特点1、碳原子有4个价电子,能与其他原子形成4个共价键,碳碳之间的结合方式有单键、双键或三键;多个碳原子之间可以相互形成长短不一的碳链和碳环,碳链和碳环也可以相互结合,所以有机物结构复杂,数量庞大。
2、单键——甲烷的分子结构CH4分子中1个碳原子与4个氢原子形成4个共价键,构成以碳原子为中心、4个氢原子位于四个顶点的正四面体结构甲烷的电子式甲烷的结构式甲烷分子结构示意图在甲烷分子中,4个碳氢键是等同的,碳原子的4个价键之间的夹角(键角)彼此相等,都是109°28′。
4个碳氢键的键长都是1.09×10-10 m。
经测定,C—H键的键能是413.4 kJ·mol-13、不饱和键1)不饱和键:未与其他原子形成共价键的电子对,常见有双键、三键2)不饱和度:与烷烃相比,碳原子缺少碳氢单键的程度也可理解为缺氢程度3)不饱和度(Ω)计算*a 、烃CxHy 的不饱和度的计算2y 2x 2-+=Ω 与碳原子以单键直连的卤族原子或无碳基视为氢原子b 、根据结构计算一个双键或环相当于一个不饱和度一个三键相当于两个不饱和度一个碳氧双键相当于一个不饱和度二 、有机化合物的同分异构现象1、同分异构化合物具有相同的分子式,但具有不同的结构的现象叫做同分异构。
具有同分异构现象的化合物互称为同分异构体。
它是有机物种类繁多的重要原因之一。
同分异构体之间的转化是化学变化。
同分异构体的特点是分子式相同,结构不同,性质不同2.同分异构的种类(1)碳链异构:由于碳链骨架不同,产生的异构现象称为碳链异构。
烷烃中的同分异构体均为碳链异构。
如有三种同分异构体,即正戊烷,异戊烷,新戊烷。
(2)位置异构:指官能团或取代基在碳链上的位置不同而造成的异构。
如1-丁烯与2-丁烯、1-丙醇与2-丙醇。
(3)官能团异构:指官能团不同而造成的异构,如乙醇和二甲醚,葡萄糖和果糖。
高中化学:有机化合物的结构特点

CnH2nO2
CH3 CH3
CH3
骨架式: C-C-C-C-C-C-COOH
CC
C
例1. 写出化学式C4H10O的所有可能物质的结构 简式
类别异构
C4H10O
位置异构 醇
碳链异构
位置异构 醚
碳链异构
例题2: C11H16 的苯的同系物中, 只含有一个支链, 且支链上 含有两个“—CH3”的结构有四种, 写出其结构简式.
支链烷烃:相同C原子的烷烃,支链愈多沸点愈低。
3. 同分异构体的种类及其书写规律:
碳链异构: 指碳原子的连接次序不同引起的异构, 如:
位置异构: 官能团的位置不同引起的异构:
官能团异构: 官能团不同引起的异构, 如: 烯烃和环烷烃 书写方法: 碳链异构→位置异构→官能团异构
练习
键线式:
COOH
结构简式: CH3-CH-CHCH2CH2CH-COOH
实验器具和药品,课作时间从事自己的化学实验。立志当一 名化学家,1869年,范特霍夫从鹿特丹五年制中学毕业了。 选择什么样的职业呢?在当时,化学作为一 门学问已有很多人 进行了研究,但是人们普遍认为化学不是一种职业,从事化 学的人,还要兼做其他工作才能够维持自己的生活。父亲为 了让他多增加一些知识,才支持他做化学实验。要把化学做 为一种职业,做一个化学家,父亲就难以同意了。因为这样 做恐怕连自己的生活都维持不了。为此,父子俩争辨了多次, 但是必须有一个结论才行呀。 一天晚饭过后,父子俩又开 始讨论这个老话题了。 “中学毕业了,你打算上哪个学校?” 父亲心平气和地问道。当然,选择学校也就是选择职业了。
2021年高中化学选修三第一章《有机化合物的结构特点与研究方法》知识点总结(答案解析)

一、选择题1.有机物有多种同分异构体结构,其中含有苯环且属于酯类的有A.2种B.3种C.4种D.6种答案:D解析:有机物的同分异构体分子式为C8H8O2,结构中需要含有苯环和酯基,所以同分异构体有:,,,,,,综上,共有6种同分异构体,D项正确;故答案为D。
2.下列说法正确的是A.乙酸乙酯和CH3CH2OCHO互为同系物B.40K和40Ca质量数相同,属于同位素C.金刚石和C60互为同素异形体,熔点和硬度都很高D.甲烷、乙烷、丁烷都没有同分异构体答案:A解析:A.乙酸乙酯和CH3CH2OCHO均为一元酯,组成上相差一个碳原子,互为同系物,故A正确;B.40K和40Ca质子数不同,不属于同位素,故B错误;C.金刚石和C60互为同素异形体,C60属于分子晶体,熔点和硬度都较低,故C错误;D.甲烷、乙烷都没有同分异构体,但丁烷有两种同分异构体,故D错误;故选A。
3.下列物质属于脂肪烃的是A.B.C.D.答案:A解析:A.是脂环烃,脂环烃属于脂肪烃,A符合题意;B.含有Cl,不属于烃,B不符题意;C.含有O,是烃的衍生物,不属于烃,C不符题意;D.是芳香烃,不属于脂肪烃,D不符题意;答案为A。
4.下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是A.CH4B.CH3CH3C.CH3CH2CH3D.CH3CH2OH答案:D解析:A.CH4只有一种等效氢,核磁共振氢谱图中能给出一种信号,故A错误;B.CH3CH3只有一种等效氢,核磁共振氢谱图中能给出一种信号,故B错误;C.CH3CH2CH3只有二种等效氢,核磁共振氢谱图中能给出二种信号,故C错误;D.CH3CH2OH有三种等效氢,核磁共振氢谱图中能给出三种信号,故D正确;故答案为D。
5.二甲醚和乙醇是同分异构体,其鉴别可采用化学方法或物理方法,下列鉴别方法中不能对二者进行鉴别的是A.利用金属钠或者金属钾B.利用元素分析法C.利用红外光谱法D.利用核磁共振氢谱答案:B解析:A.乙醇中含有-OH,可与金属钠或金属钾反应生成氢气,可鉴别,选项A正确;B.元素分析法只能测得所含元素种类,而两者所含元素相同,利用元素分析法不能鉴别,选项B错误;C.二甲醚和乙醇中分别含有-O-和-OH,官能团不同,可用红外光谱法鉴别,选项C正确;D.二者含有的H原子的种类和性质不同,可用核磁共振氢谱鉴别,选项D正确;答案选B。
化学选修2结构考点总结

化学选修2结构考点总结一、有机化合物的结构特点有机化合物是由碳原子和氢原子以及其他非金属原子组成的化合物,其结构特点包括以下几个方面:1.碳原子的四价性:碳原子可以与其他碳原子或其他非金属原子通过共价键相连,形成分子中的骨架结构。
2.范德华力和键能:有机化合物中的分子间相互作用主要是通过范德华力来实现的。
而分子内的相互作用则是通过共价键能来实现的。
3.键的自由旋转:在碳-碳单键和碳-氢键中,由于键的自由旋转,分子可以在立体空间中快速转动,使得其构象经常发生变化。
4.立体异构体:由于键的自由旋转,相同分子式的有机化合物存在不同立体异构体。
5.共轭体系和芳香性:在有机化合物中,共轭体系的存在会导致分子具有一定的稳定性和特殊的光学性质。
而芳香性则是由芳香族化合物的共轭体系所决定的。
二、有机化合物的分子式和结构式在有机化学中,分子式用于表示有机化合物中各元素的种类和数量,而结构式则用于表示有机化合物中原子之间的连接方式和空间排布。
常见的有机化合物结构式表示方法有以下几种:1.线性结构:直接表示原子之间的连接关系,只标出碳原子间以及碳原子与其他原子(如氧、氮、硫)的直接连接。
2.简化结构:用简化的表示方法表示分子结构,常常忽略碳原子周围的氢原子。
3.分组结构:将分子中的一部分或几个基团用一个圆圈或方框表示,从而简化结构。
分组结构有助于化学反应的理解和分析。
4.平面投影式:将分子的立体结构投影到平面上,使用立体化学的符号来表示曲面和空间关系。
三、共价键和价角1.共价键:共价键是由共享电子对而形成的化学键。
在有机化合物中,碳原子与其他碳原子或其他非金属原子之间通常通过共价键相连。
2.单、双、三键:共价键可以根据共享的电子数目分为单键、双键和三键。
单键由一个σ 键组成,双键由一个σ 键和一个π 键组成,三键由一个σ 键和两个π 键组成。
3.杂化轨道和键角:碳原子在形成共价键时,sp3 杂化轨道和 sp2 杂化轨道的形成分别对应着四面体结构和平面三角形结构。
《有机化合物的结构》知识清单

《有机化合物的结构》知识清单一、有机化合物的定义有机化合物,简称有机物,通常是指含碳的化合物,但一些简单的含碳化合物,如一氧化碳、二氧化碳、碳酸盐等,由于其性质与无机物相似,通常被归为无机物范畴。
有机物的特点在于其分子结构中通常包含碳氢键(CH),并且多数有机物能够燃烧。
二、有机化合物的结构特点1、碳原子的成键特点碳原子最外层有 4 个电子,不易失去或得到电子形成离子,而是通过共用电子对形成共价键。
碳原子之间可以形成单键、双键和三键,也可以形成链状结构或环状结构。
2、共价键的类型(1)σ键:原子轨道沿键轴方向以“头碰头”方式重叠形成的共价键,其电子云重叠程度较大,键能较大,稳定性较高。
(2)π键:原子轨道以“肩并肩”方式重叠形成的共价键,其电子云重叠程度较小,键能较小,稳定性较低。
3、同分异构现象同分异构现象是指化合物具有相同的分子式,但具有不同结构的现象。
同分异构体包括构造异构和立体异构。
(1)构造异构碳链异构:由于碳原子的连接顺序不同而产生的异构现象。
位置异构:官能团在碳链上的位置不同而产生的异构现象。
官能团异构:有机物具有相同的分子式,但官能团不同而产生的异构现象。
(2)立体异构顺反异构:当双键两侧的碳原子上连接的两个原子或基团不同时,会产生顺反异构。
对映异构:具有手性碳原子的化合物存在对映异构现象。
三、有机化合物的表示方法1、结构式用价键表示出分子中每个原子的连接顺序和方式的式子。
2、结构简式将结构式中的碳氢键和碳碳单键省略,一些官能团用特定的符号表示。
3、键线式只表示出碳骨架以及官能团,用线段表示碳碳键,拐点和端点表示碳原子。
4、球棍模型用球代表原子,用棍代表化学键,形象地展示分子的空间结构。
5、比例模型按照原子的相对大小和空间位置关系制作的模型,更能直观地反映分子的空间结构。
四、常见官能团的结构1、羟基(OH)羟基直接与烃基相连的化合物称为醇,羟基与苯环直接相连的化合物称为酚。
2、醛基(CHO)醛类化合物中具有醛基,如甲醛(HCHO)、乙醛(CH₃CHO)等。
高二化学《有机化合物的结构特点》知识点归纳总结 例题解析
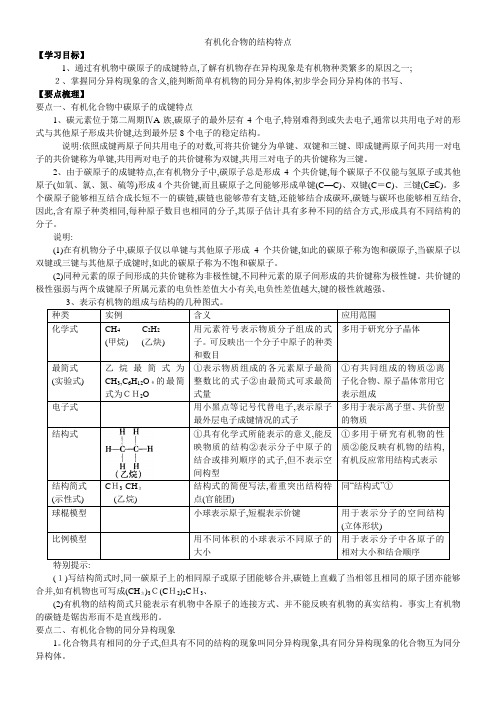
有机化合物的结构特点【学习目标】1、通过有机物中碳原子的成键特点,了解有机物存在异构现象是有机物种类繁多的原因之一;2、掌握同分异构现象的含义,能判断简单有机物的同分异构体,初步学会同分异构体的书写、【要点梳理】要点一、有机化合物中碳原子的成键特点1、碳元素位于第二周期ⅣA族,碳原子的最外层有4个电子,特别难得到或失去电子,通常以共用电子对的形式与其他原子形成共价键,达到最外层8个电子的稳定结构。
说明:依照成键两原子间共用电子的对数,可将共价键分为单键、双键和三键、即成键两原子间共用一对电子的共价键称为单键,共用两对电子的共价键称为双键,共用三对电子的共价键称为三键。
2、由于碳原子的成键特点,在有机物分子中,碳原子总是形成4个共价键,每个碳原子不仅能与氢原子或其他原子(如氧、氯、氮、硫等)形成4个共价键,而且碳原子之间能够形成单键(C—C)、双键(C=C)、三键(C≡C)。
多个碳原子能够相互结合成长短不一的碳链,碳链也能够带有支链,还能够结合成碳环,碳链与碳环也能够相互结合,因此,含有原子种类相同,每种原子数目也相同的分子,其原子估计具有多种不同的结合方式,形成具有不同结构的分子。
说明:(1)在有机物分子中,碳原子仅以单键与其他原子形成4个共价键,如此的碳原子称为饱和碳原子,当碳原子以双键或三键与其他原子成键时,如此的碳原子称为不饱和碳原子。
(2)同种元素的原子间形成的共价键称为非极性键,不同种元素的原子间形成的共价键称为极性键。
共价键的极性强弱与两个成键原子所属元素的电负性差值大小有关,电负性差值越大,键的极性就越强、3、表示有机物的组成与结构的几种图式。
种类实例含义应用范围化学式CH4C2H2(甲烷) (乙炔) 用元素符号表示物质分子组成的式子。
可反映出一个分子中原子的种类和数目多用于研究分子晶体最简式(实验式) 乙烷最简式为CH3,C6H12O6的最简式为CH2O①表示物质组成的各元素原子最简整数比的式子②由最简式可求最简式量①有共同组成的物质②离子化合物、原子晶体常用它表示组成电子式用小黑点等记号代替电子,表示原子最外层电子成键情况的式子多用于表示离子型、共价型的物质结构式①具有化学式所能表示的意义,能反映物质的结构②表示分子中原子的结合或排列顺序的式子,但不表示空间构型①多用于研究有机物的性质②能反映有机物的结构,有机反应常用结构式表示结构简式(示性式) CH3-CH3(乙烷)结构式的简便写法,着重突出结构特点(官能团)同“结构式”①球棍模型小球表示原子,短棍表示价键用于表示分子的空间结构(立体形状)比例模型用不同体积的小球表示不同原子的大小用于表示分子中各原子的相对大小和结合顺序特别提示:(1)写结构简式时,同一碳原子上的相同原子或原子团能够合并,碳链上直截了当相邻且相同的原子团亦能够合并,如有机物也可写成(CH3)3C(CH2)2CH3、(2)有机物的结构简式只能表示有机物中各原子的连接方式、并不能反映有机物的真实结构。
高中化学学习细节(人教版)之认识有机化合物:二、有机化合物的结构特点 含解析

【学习目标】1. 进一步认识有机化合物的成键特点;通过有机化合物常见的同分异构体现象的学习体会物质结构的多样性决定物质性质的多样性.2。
能准确判断同分异构体及其种类的多少【重点难点】正确书写同分异构体;【自主学习】一、有机化合物中碳原子的成键特点 1.碳原子的结构及成键特点碳原子的最外层有 个电子,很难得失电子,易与碳原子或其他原子形成 个共价键。
2.碳原子的结合方式⑴ 碳原子之间可以形成稳定的单键,还可以形成稳定的双键或三键. ⑵ 多个碳原子可以相互结合成长短不一的碳链,碳链也可以带有支链,还可以结合成碳环,碳链和碳环也可以相互结合。
⑶ 碳原子还可以和氧原子等多种非金属原子形成共价键。
(氯乙烷)。
⑷ 有机物分子中还普遍存在 现象. 二。
有机物的分子构型名称分子式结构模型键角空间构型甲烷(四氯甲烷)CH 4109。
50 正四面体乙烯 C 2H 41200 平面三。
有机化合物的同分异构现象同分异构体的概念:是指分子式相同而结构式不同的物质之间的互称。
关键要把握好以下两点:⑴分子式相同CH3—CH—CH—CH3 CH3—C—CH2—CH3CH3CH3CH3CH3故己烷(C6H14)的同分异构体的数目有5种。
变式训练2—1。
写现庚烷的同分异构体.2.位置异构⑴烯炔的异构(碳链的异构和双键或叁键官能团的位置异构)方法:先写出所有的碳链异构,再根据碳的四键,在合适位置放双官能团。
例C5H10属于烯烃的同分异构体典例3.下列烷烃在光照下与氯气反应,只生成一种一氯代烃的是()三、判断同分异构体数目的常见方法和思路:⑴记忆法①碳原子数目1~5的烷烃异构体数目:甲烷、乙烷、丙烷均无异构体,丁烷有二种异构体,戊烷有三种异构体.②碳原子数1~5的一价烷基:甲基一种(-CH3),乙基一种(—CH2—CH3)、丙基二种[—CH2CH2CH3、-CH(CH3)2], 【方法指导】⑴按照同分异构体的书写步骤书写.⑵先碳链异构后位置异构。
新教材人教版高中化学选择性必修3第一章有机化合物的结构特点与研究方法 知识点考点归纳总结

第一章有机化合物的结构特点与研究方法第一节有机化合物的结构特点............................................................................................ - 1 - 第1课时有机化合物的分类方法.............................................................................. - 1 -第2课时有机化合物中的共价键和同分异构现象.................................................. - 5 - 第二节研究有机化合物的一般方法.................................................................................... - 8 - 第1课时有机物的分离、提纯和确定实验式.......................................................... - 8 -第2课时有机物分子式与分子结构的确定............................................................ - 12 - 章末总结 ............................................................................................................................... - 15 -第一节有机化合物的结构特点第1课时有机化合物的分类方法一、依据碳骨架分类1.脂肪烃一般包括烷烃、烯烃和炔烃。
2.环状化合物这类有机化合物分子中含有由碳原子构成的环状结构。
(1)脂环化合物:分子中含有碳环(非苯环)的化合物。
有机化合物的结构特点

【典例】(双选)下列关于 的下列叙述中,正确的是( ) A.苯环侧链上的5个碳原子有可能都在一条直线上 B.苯环侧链上的5个碳原子不可能都在一条直线上 C.11个碳原子有可能在同一平面上 D.11个碳原子不可能在同一平面上
【变式训练】下列有机分子中,所有的原子不可能处于同一平面的是( ) A.CH2=CH—C≡CH B.CH2=CH—CH=CH2 C. D.
CH3
CH3—C—CH2—CH3
CH3
CH3
CH3—CH—CH—CH3
CH3
CH3
己烷(C6H14)有5种同分异构体,写出它们的结构简式。
以上的同分异构体是由于碳原子的连接次序不同引起的异构,这样的同分异构体在化学上叫做“碳链异构”!
深入探究:
官能团的位置不同引起的异构。
位置异构:
提示:饱和一元醇和饱和一元醚的通式都是:CnH2n+2O!
C—C
C—C—OH
CH3—CH2—OH
C—O—C
CH3—O—CH3
C—C
醇:
醚:
官能团不同引起的异构。 如: 丙烯和丙环烷、乙醇和甲醚
官能团异构:
深入探究:
常见的类别异构现象
序号
类别
通式
1
烯烃
环烷烃
2
炔烃
二烯烃
3
饱和一元脂肪醇
饱和醚
4
一、共价键参数
键长: 键角: 键能:
键长越短,化学键越稳定
决定物质的空间结构
键能越大,化学键越稳定
键能
键长
键角
判断分子的稳定性
确定分子在空间的几何构型
二、有机化合物中碳原子的成键特点
高二化学有机化合物的结构特点-P

有机化合物的结构特点笔记

有机化合物的结构特点笔记
有机化合物是由碳和氢元素组成的化合物。
它们的结构特点主要包括碳骨架、官能团和立体构型。
1. 碳骨架:有机化合物的主要特征是碳骨架的存在。
碳原子具有四个价电子,可以形成单、双、三键。
碳原子之间可以通过共价键连接,形成不同形状的碳骨架,如直链、支链、环状等。
碳骨架的结构决定了有机化合物的性质和反应。
2. 官能团:官能团是有机分子中具有特定化学性质的部分。
它们通常是由原子或原子团组成的,可以影响有机化合物的性质和反应。
常见的官能团包括羟基(─OH)、羰基(C=O)、羧基(─COOH)等。
不同的官能团会赋予有机分子不同的化学性质,如酸碱性、还原性等。
3. 立体构型:有机化合物存在多种立体构型。
立体构型描述了分子中不同原子或基团在空间中的排列方式。
常见的立体构型包括手性和立体异构体。
手性是指一个分子无法与其镜像重叠的性质,它由手性中心引起。
立体异构体是指具有相同分子式但空间构型不同的化合物。
立体构型对于有机化合物的化学反应和生物活性具有重要影响。
有机化合物的结构特点决定了它们的性质和用途。
通过研究和理解有
机化合物的结构特点,我们可以深入了解它们的化学性质和反应机理,为有机化学的应用和发展提供基础。
高二化学有机化合物的结构特点

须好像十分震撼原始。那一双敦实的纯蓝色短棍形态的眉毛,显得极为飘然同时还隐现着几丝阴森。再看女奴仆Y.曼妍米依仙女的身形,她有着奇特的美如棕绳一般的肩膀
,肩膀下面是怪异的美如竹竿一般的手臂,她飘浮的天青色瓜子一般的手掌的确绝对的和谐但又有些愚笨,凹露的亮白色麦穗一般的手指仿佛真是迷离和与众不同。她突兀的
第二节 有机化合物的结构特点
本节要求: 1、掌握同分异构体、同分异构现象概念 2、区别几种情况下的异构关系:
碳链异构:由于碳链骨架不同而产生的异构现象
位置异构:由于取代基或官能团在碳链或碳环上 的位置不同而产生的异构现象
官能团异构:由于官能团不同而产生的异构现象
一、有机化合物中碳原子的成键特点
举例:与碳原子所连的其它原子在四面体的 四个顶点;同一平面;一条直线。
美如匕首一般的腿确实非常震撼原始,变异的美如轻盈一般的脚认为很是冷酷酷野,她高大的美如野象一般的屁股似乎有点飘然但又露出一种隐约的阴森!腰间一条,怪异的
墨紫色玩具一般的腰带的确绝对的潇洒却又透着一丝罕见。这个妹妹说话时有种怪异的深紫色杏仁造型的声音,高兴时会散发出散发的淡白色药锅般的气味。她突兀的深蓝色
壮观的景象出现了,随着指示和金币的高速碰撞!翻滚狂舞其中的所有物体和碎片都被撞向十几万米的高空,半空中立刻形成一道杀声震天、高速上升的巨幕,双方的斗士一
边快速上升一边猛烈厮杀……战斗结束了,校霸们的队伍全军覆灭,垂死挣扎的野猪缸须神如同蜡像一样迅速熔化……双方斗士残碎的肢体很快变成金币和各种各样的兵器、
D、CH3-CH2-CH2-CH2- OH CH3-CH-CH2-CH3 OH
E、
CH3
CH3
CH3
F、 Br
G、CH3CH2COOH
高二化学《有机物结构和性质》知识点总结

高二化学《有机物结构和性质》知识点总结一、主要考查1.复杂有机物分子式的判断2.有机物分子中共线、共面问题3.同分异构体种数4.官能团的性质与有机反应类型的关系5.官能团与反应物用量的关系二、方法技巧1.有机物分子中共线、共面原子数目的判断(1)熟记四种典型空间结构①甲烷型:正四面体→凡是碳原子与4个原子形成4个共价键时,其空间结构都是四面体形,5个原子中最多有3个原子共平面。
②乙烯型:平面结构→与碳碳双键直接相连的4个原子与2个碳原子共平面。
③苯型:平面结构→位于苯环上的12个原子共平面,位于对角线位置上的4个原子共直线。
④乙炔型:—C≡C—直线结构→与碳碳三键直接相连的2个原子与2个碳原子共直线。
(2)确定共线、共面原子数目需要结合相关的几何知识进行分析:如不共线的任意三点可确定一个平面;若一条直线与某平面有两个交点时,则这条直线上的所有点都在该平面内;同时要注意问题中的限定性词语(“可能共面”还是“一定共面”,是“至少”还是“最多”,是“碳原子”还是“所有原子”)。
①甲烷、乙烯、苯三种分子中的氢原子如果被其他原子取代,则取代后的分子构型基本不变。
②共价单键可以自由旋转,共价双键和共价三键不能旋转。
③结构式中有甲基(或饱和碳原子)的有机物,其分子中的所有原子不可能共平面。
④直线结构与平面结构连接,则直线在这个平面上。
如苯乙炔:,所有原子共平面。
⑤平面结构与平面结构连接,如果两个平面结构通过单键相连,由于单键的旋转性,两个平面可以重合,但不一定重合。
如苯乙烯:,分子中共平面原子至少12个,最多16个。
⑥平面结构与立体结构连接,如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基上的一个氢原子可能处于这个平面上。
2.常见有机物的结构特点及主要化学性质CH2===CH2官能团3.同分异构体的数目判断(1)一元取代物①基元法(即烃基数目法)简单烷基的同分异构体:丙基-C3H7有2种、丁基-C4H9有4种、戊基-C5H11有8种;如丁基有4种,丁醇(C4H9—OH)、C4H9—Cl分别有4种②分子中等效H原子种数就是一元取代物的数目。
《有机化合物的结构特点》 知识清单

《有机化合物的结构特点》知识清单一、有机化合物的定义有机化合物,简称有机物,是指含碳的化合物(但一些简单的含碳化合物,如一氧化碳、二氧化碳、碳酸盐等除外)。
有机物的种类繁多,这主要归因于碳原子独特的成键特点。
二、碳原子的成键特点1、碳原子可以形成四个共价键碳原子最外层有 4 个电子,在形成化合物时,它既能与其他原子形成 4 个共价键,也能自身相互结合形成碳链或碳环。
2、碳原子之间的结合方式多样碳原子之间可以通过单键、双键或三键相结合。
单键如乙烷中的碳碳单键(C—C);双键如乙烯中的碳碳双键(C=C);三键如乙炔中的碳碳三键(C≡C)。
3、碳链的长度和形状多变碳原子可以形成直链、支链或环状结构。
直链如正丁烷;支链如异丁烷;环状如环己烷。
三、有机化合物的结构表示方法1、结构式用短线表示共价键,将原子之间的连接顺序清晰地展示出来。
例如,乙烷的结构式为:CH₃—CH₃。
2、结构简式将结构式中的碳氢键和碳碳单键省略,例如乙烷的结构简式可以写为:CH₃CH₃。
3、键线式只表示出碳骨架以及与碳原子相连的官能团,例如丙烷的键线式为:。
四、同分异构现象1、同分异构体的概念化合物具有相同的分子式,但具有不同结构的现象称为同分异构现象。
具有同分异构现象的化合物互称为同分异构体。
2、同分异构体的类型(1)碳链异构由于碳链骨架不同而产生的同分异构体。
例如,正戊烷、异戊烷和新戊烷。
(2)位置异构官能团在碳链中的位置不同而产生的同分异构体。
比如 1 丁烯和 2 丁烯。
(3)官能团异构有机物具有相同的分子式,但官能团不同。
例如乙醇(C₂H₅OH)和二甲醚(CH₃OCH₃)。
五、有机化合物中官能团的特点官能团是决定有机化合物化学特性的原子或原子团。
常见的官能团有:1、羟基(—OH)存在于醇和酚中,醇中的羟基可以发生取代、消去等反应,酚中的羟基具有弱酸性。
2、醛基(—CHO)具有还原性,能发生银镜反应、与新制氢氧化铜反应等。
3、羧基(—COOH)具有酸性,能发生酯化反应等。
第1章第1节有机化合物的结构特点(第2课时有机化合物中的共价键)(学生版+解析)-2021-2022

〔提示〕
①在CH4+Cl2 CH3Cl+HCl反应中,CH4断裂的化学键是C—H,具有极性,可断裂,所以能够发生取代反应。
②在CH2==CH2+Br2―→CH2Br—CH2Br反应中,CH2==CH2分子中含有5个σ键,1个π键,π键更易断裂,所以乙烯与Br2发生的是加成反应。
C.甲烷分子中含有C—H σ键能发生取代反应D.乙烯分子中含有π键能发生加成反应
【答案】B
〔解析〕共价键极性越强,在反应中越容易发生断裂,B项错误。
3.其中乙烯是一种常用的催熟剂。下列对于乙烯中化学键的分析正确的是()
A.在乙烯分子中有一个σ键、一个π键
B.乙烯在发生加成反应时,断裂的是碳原子间的σ键
(1)写出分子式为C5H10的烯烃的结构简式
(2)分子式为C8H10的苯的同系物结构简式
(3)用键线式表示分子式为C4H10O的醇的结构简式
【答案】
(1)CH2==CH—CH2—CH2—CH3、CH3—CH==CH—CH2—CH3、 、
、
(2)
(3)
8.同分异构现象在有机化学中普遍存在,中学阶段常见的同分异构体有三类:①官能团类别异构,②官能团位置异构,③碳架异构。已知分子式为C5H12O的有机物有多种同分异构体,下面给出其中四种:A.CH3—CH2—CH2—CH2—CH2OHB.CH3—O—CH2—CH2—CH2—CH3
(2)共价键的类型与有机反应
键的轨道重叠程度比键的小,比较容易断裂而发生化学反应。例如乙烯和乙炔分子的双键和三键中含有键,都可以发生反应,而甲烷分子中含有C—H键,可发生反应。
2.共价键的极性与有机反应
2021年高中化学选修三第一章《有机化合物的结构特点与研究方法》知识点复习(答案解析)(1)

一、选择题1.下列化合物的1H-NMR谱图中吸收峰的数目不正确的是A.(2组)B.(5组)C.(3组)D.(4组)答案:A解析:A.轴对称,其中含有3种类型的氢原子,核磁共振氢谱中出现3组峰,故A错误;B.含有5种类型的氢原子,核磁共振氢谱中出现5组峰,故B正确;C.含有3种类型的氢原子,核磁共振氢谱中出现3组峰,故C正确;D.含有4种类型的氢原子,核磁共振氢谱中出现4组峰,故D正确;故答案为A。
2.有机物有多种同分异构体结构,其中含有苯环且属于酯类的有A.2种B.3种C.4种D.6种答案:D解析:有机物的同分异构体分子式为C8H8O2,结构中需要含有苯环和酯基,所以同分异构体有:,,,,,,综上,共有6种同分异构体,D项正确;故答案为D。
3.随着科学技术的发展,人们可以利用很多先进的方法和手段来测定有机物的组成和结构。
下列说法正确的是A.李比希元素分析仪可以测定有机物的结构简式B.质谱仪能根据最小的碎片离子确定有机物的相对分子质量C.红外光谱分析能测出各种化学键和官能团D.对有机物CH3CH(OH)CH3进行核磁共振分析,能得到4个峰,且峰面积之比为1:1:3:3答案:C解析:A.李比希的元素分析仪只能测定出元素种类,不能确定有机物的结构简式,故A 错误;B.质谱仪能根据最大的碎片离子确定有机物的相对分子质量,故B错误;C.不同的化学键或官能团吸收频率不同,在红外光谱图上将处于不同的位置,从而可以获得分子中含有任何化学键或官能团的信息,来确定有机物中的官能团或化学键,故C正确;D.有机物CH3CH(OH)CH3含有3种化学环境不同的氢,两个甲基相同,则能得到3个峰,且峰面积之比为1:1:6,故D错误;故选C。
4.绿原酸具有抗病毒,降血压,延缓衰老等保健作用.利用乙醚、95%乙醇浸泡杜仲干叶,得到提取液,进一步提取绿原酸的流程如下:下列说法错误的是A.从“提取液”获取“有机层”的操作为分液B.蒸馏时选用球形冷凝管C.过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒D.粗产品可通过重结晶的方法提纯答案:B解析:A.由流程可知,乙酸乙酯作萃取剂,得到有机层的实验操作为萃取、分液,A正确;B.蒸馏时若选用球形冷凝管,会有一部分馏分经冷凝降温后滞留在冷凝管中,而不能进入接收器中,因此蒸馏时应该选择使用直形冷凝管,B错误;C.过滤时所需玻璃仪器有烧杯、漏斗、玻璃棒,C正确;D.绿原酸难溶于水,易溶于有机溶剂,因此可利用重结晶的方法进一步提纯,D正确;故合理选项是B。
高中化学有机知识点:有机化合物的结构特点

高中化学有机知识点:有机化合物的结构特点一、有机化合物中碳原子的成键特点1.碳原子的结构特点和成键特点2.甲烷的分子结构(1)结构特点以碳原子为中心,4个氢原子位于四个顶点的正四面体立体结构。
在CH4分子中4个C—H键完全等同,两个碳氢键间的夹角均为109°28′。
(2)表示方法(1)有机化合物分子结构的常见表示方法(2)键线式:省略碳、氢元素符号,每个端点、拐点都表示碳原子,线表示化学键。
相关链接结构简式书写时的注意事项(1)结构简式的书写是省略结构式中代表共价键的单键,而代表双键的“==”、三键的“≡”不能省略。
(2)写结构简式时,同一个碳原子上的相同原子或原子团可以合并,直接相邻的且相同的原子团亦可以合并,如也可以写成(CH3)3C(CH2)2CH3。
(3)结构简式的书写以不引起歧义为目的,如CH3CH2CH2OH,不能写成C3H7OH,这样可能会误解为CH3CH(OH)CH3。
(4)结构简式不能表示有机物的真实结构,如从结构简式看,CH3CH2CH2CH3中的碳链是直线形的,而实际上是锯齿形的。
二、有机化合物的同分异构现象1.同分异构体、同分异构现象(1)同分异构现象:化合物具有相同的分子式,但具有不同结构的现象。
(2)同分异构体:具有同分异构现象的化合物互为同分异构体。
①特点:分子式相同,结构不同,性质可能相似也可能不同。
②转化:同分异构体之间的转化是化学变化。
2.同分异构的类型(1)碳链异构:由于碳链骨架不同,产生的异构现象。
如:CH3CH2CH2CH3与(2)位置异构:由于官能团在碳链中位置不同而产生的同分异构现象。
如:CH3CH2CH==CH2与CH3—CH==CH—CH3。
(3)官能团异构:分子式相同,但具有不同的官能团而产生的同分异构现象,如:CH3CH2OH与CH3—O—CH3。
3.烷烃同分异构体的书写烷烃只存在碳链异构,一般可采用“降碳对称法”进行书写,具体步骤如下(以C6H14为例):(1)确定碳链①先写直链:C—C—C—C—C—C。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化合物的结构特点【学习目标】1.通过有机物中碳原子的成键特点,了解有机物存在异构现象是有机物种类繁多的原因之一;2.掌握同分异构现象的含义,能判断简单有机物的同分异构体,初步学会同分异构体的书写。
【要点梳理】要点一、有机化合物中碳原子的成键特点1.碳元素位于第二周期ⅣA族,碳原子的最外层有4个电子,很难得到或失去电子,通常以共用电子对的形式与其他原子形成共价键,达到最外层8个电子的稳定结构。
说明:根据成键两原子间共用电子的对数,可将共价键分为单键、双键和三键。
即成键两原子间共用一对电子的共价键称为单键,共用两对电子的共价键称为双键,共用三对电子的共价键称为三键。
2.由于碳原子的成键特点,在有机物分子中,碳原子总是形成4个共价键,每个碳原子不仅能与氢原子或其他原子(如氧、氯、氮、硫等)形成4个共价键,而且碳原子之间可以形成单键(C—C)、双键(C=C)、三键(C≡C)。
多个碳原子可以相互结合成长短不一的碳链,碳链也可以带有支链,还可以结合成碳环,碳链与碳环也可以相互结合,因此,含有原子种类相同,每种原子数目也相同的分子,其原子可能具有多种不同的结合方式,形成具有不同结构的分子。
说明:(1)在有机物分子中,碳原子仅以单键与其他原子形成4个共价键,这样的碳原子称为饱和碳原子,当碳原子以双键或三键与其他原子成键时,这样的碳原子称为不饱和碳原子。
(2)同种元素的原子间形成的共价键称为非极性键,不同种元素的原子间形成的共价键称为极性键。
共价键的极性强弱与两个成键原子所属元素的电负性差值大小有关,电负性差值越大,键的极性就越强。
种类实例含义应用范围化学式CH4C2H2(甲烷) (乙炔) 用元素符号表示物质分子组成的式子。
可反映出一个分子中原子的种类和数目多用于研究分子晶体最简式(实验式) 乙烷最简式为CH3,C6H12O6的最简式为CH2O①表示物质组成的各元素原子最简整数比的式子②由最简式可求最简式量①有共同组成的物质②离子化合物、原子晶体常用它表示组成电子式用小黑点等记号代替电子,表示原子最外层电子成键情况的式子多用于表示离子型、共价型的物质结构式①具有化学式所能表示的意义,能反映物质的结构②表示分子中原子的结合或排列顺序的式子,但不表示空间构型①多用于研究有机物的性质②能反映有机物的结构,有机反应常用结构式表示结构简式(示性式) CH3—CH3(乙烷)结构式的简便写法,着重突出结构特点(官能团)同“结构式”①球棍模型小球表示原子,短棍表示价键用于表示分子的空间结构(立体形状)比例模型用不同体积的小球表示不同原子的大小用于表示分子中各原子的相对大小和结合顺序特别提示:(1)写结构简式时,同一碳原子上的相同原子或原子团可以合并,碳链上直接相邻且相同的原子团亦可以合并,如有机物也可写成(CH 3)3C(CH 2)2CH 3。
(2)有机物的结构简式只能表示有机物中各原子的连接方式.并不能反映有机物的真实结构。
其实有机物的碳链是锯齿形而不是直线形的。
要点二、有机化合物的同分异构现象1.化合物具有相同的分子式,但具有不同的结构的现象叫同分异构现象,具有同分异构现象的化合物互为同分异构体。
2.两化合物互为同分异构体的必备条件有二: (1)两化合物的分子式应相同。
(2)两化合物的结构应不同(如碳链骨架不同、官能团的位置不同、官能团的种类不同等)。
3.中学阶段必须掌握的异构方式有三种,即碳链异构、位置异构和官能团异构。
常见同分异构现象及形成途径异构方式 形成途径示例碳链异构 碳链骨架不同而产生的异构CH 3CH 2CH 2CH 3与 位置异构官能团位置不同而产生的异构CH 2=CHCH 2CH 3与CH 3—CH=CH —CH 3官能团异构 官能团种类不同而产生的异构CH 3CH 2CHO 与 (1)顺反异构。
当有机物分子中含有碳碳双键且每个双键碳原子所连的另外两个原子或基团不同时,就存在顺反异构现象。
如2-丁烯存在顺反异构体。
(2)对映异构。
当有机物分子中的饱和碳原子连接着4个不同的原子或原子团时。
就可能存在对映异构现象。
如乳酸( )有如下两种对映异构体: 5.同分异构体的书写技巧。
(1)书写同分异构体时,必须遵循“价键数守恒”原则,即在有机物分子中,碳原子的价键数为4,氢原子的价键数为1,氧原子的价键数为2,等等。
(2)熟练掌握碳原子数小于7的烷烃和碳原子数小于5的烷基的异构体数目,这对同分异构体的辨认与书写十分重要。
即CH 4、C 2H 6、C 3H 8、—CH 3、—C 2H 5仅有1种结构;C 4H 10,—C 3H 7有2种结构;—C 4H 9有4种结构(这也是高考中的热门烃基);C 5H 12、C 6H 14、C 7H 16则依次有3种、5种、9种结构。
(3)熟练掌握官能团异构的有机物的类别。
①烯烃和环烷烃:通式C n H 2n (n≥3)②二烯烃、炔烃、环烯烃:通式C n H 2n -2(n≥4) ③苯及苯的同系物与多烯烃:通式C n H 2n -6(n≥6) ④饱和一元醇与饱和一元醚:通式C n H 2n+2O(n≥2)⑤饱和一元醛、饱和一元酮、烯醇:通式C n H 2n O(n≥3)⑥饱和一元羧酸、饱和一元酯、羟基醛:通式C n H 2n O 2(n≥2) ⑦酚、芳香醇、芳香醚:通式C n H 2n -6O(n >6) ⑧葡萄糖与果糖;蔗糖与麦芽糖⑨氨基酸R —CH —COOH 与硝基化合物R —CH 2CH 2NO 2CH 3—CH —CH 3CH 3 CH 3—C —CH 3OCH 3—CH —COOHOH NH 2(4)烷烃的同分异构体的书写是其他有机物的同分异构体书写的基础。
烷烃的同分异构体的书写方法一般采用“减碳对称法”,可概括为“两注意、三原则、四顺序”。
图示如下: (5)苯的同系物或苯的衍生物的同分异构体的书写可综合考虑苯环上基团的类别和个数以及基团在苯环上的位置,有序分析即可迅速写出其含苯环的同分异构体来。
(6)书写有机物的同分异构体的步骤是:首先考虑官能团异构,其次考虑碳链异构,最后考虑位置异构,同时遵循对称性、互补性、有序性原则,即可以无重复、无遗漏地写出所有的同分异构体来。
(7)如无特别说明,中学阶段不要求书写有机物的立体异构体。
要点三、有机物的结构与性质的关系 “结构决定性质,性质反映结构”,这是学习有机化学时要特别关注的问题,根据有机物的结构推测它的性质,一般来说,首先要找出官能团,然后从键的极性、碳原子的饱和程度等进一步分析并推测有机物的性质。
1.官能团与有机物性质的关系。
有机物的性质由其分子结构来决定,而官能团是决定有机物性质的主要因素。
一种官能团决定了一类有机物的化学特性。
一般地,具有相同的官能团的有机物具有相似的化学性质,有机物含有多个官能团时,也应具有多个官能团的性质。
2.不同基团间的相互影响与有机物性质的关系。
有机化合物分子中的邻近基团间往往会相互影响,这种影响会使有机化合物表现出一些特性。
例如,苯与硝酸发生取代反应的温度是50℃~60℃,而甲苯在约30℃的温度下就能与硝酸发生取代反应。
也就是说,与苯相比,甲苯较易发生取代反应。
这是由于甲基具有推电子作用,它对苯环的影响使得苯环上的某些氢原子更容易被取代。
再如,醇和酚的官能团都是羟基,但由于分子中与羟基相连的烃基不同,使得醇和酚的化学性质也不同;醛和酮的官能团均含羰基,醛羰基上连有氢原子、酮羰基上不连氢原子,使得醛、酮成为两类不同的有机化合物。
【典型例题】类型一:有机物碳原子的成键特点例1 下列关于CH 3—CH =CH —C≡C—CF 3分子结构的叙述中正确的是( ) A .6个碳原子有可能都在一条直线上 B .6个碳原子不可能都在一条直线上 C .6个碳原子一定都在同一平面上 D .6个碳原子不可能都在同一平面上【答案】B 、C【解析】根据(1)乙烯分子中的6个原子共平面。
键角120°;(2)乙炔分子中的4个原子共直线,键角180°,可推知题给有机物的碳链骨架结构如下: 由上面的碳链骨架结构很容易看出:题给有机物分子中的6个碳原子不可能都在一条直线上,而是一定都在同一平面上。
【总结升华】应以已知的有机分子结构为基础,从其氢原子被别的基团取代后的伸展情况来分析。
举一反三:【变式1】某烃的结构简式为分子中处于四面体结构中心的碳原子数为a ,一定在同一平面内的碳原子数为b ,一定在同一直线上的碳原子数为c ,则a 、b 、c 依次为( )A .4、5、3B .4、6、3C .2、4、5D .4、4、6【答案】B例2 大多数有机物分子里的碳原子与碳原子之间或碳原子与其他原子之间相结合的化学键是( ) A .只有极性键 B .只有非极性键 C .有极性键和非极性键 D .只有离子键【答案】C【解析】因碳原子最外层有4个电子,在有机物分子中,碳原子与碳原子之间或碳原子与其他原子之间形成的都是共价键。
其中碳原子与碳原子之间以非极性键相结合,碳原子与其他原子之间以极性键相结合。
【总结升华】在有机物中。
碳原子与其他原子构成的化学键均为共价键,是极性键。
举一反三:选择最长的碳链作主链找出中心对称线 对称性原则有序性原则 互补性原则 主链由长到短 支链由整到散 位置由心到边 排布由邻到间 两注意三原则四顺序减碳对称法【变式1】某有机物的结构简式为回答下列问题:(1)写出其分子式:________。
(2)其中含有________个不饱和碳原子,分子中有________个双键。
(3)分子中的极性键有________(写出2种即可)。
(4)分子中的饱和碳原子有________个,一定与苯环处于同一平面的碳原子有________个。
(5)分子中C—C=O键角约为________,H—C≡C键角约为________。
【答案】(1)C16H16O5(2)12 3 (3)碳氧键、碳氢键、氢氧键(任写2种)(4)4 4 (5)120°180°类型二:同分异构体的辨认与书写例3 某单官能团有机化合物,只含碳、氢、氧三种元素,相对分子质量为58,完全燃烧时产生等物质的量的CO2和H2O。
它可能的结构共有(不考虑立体异构)( )A.4种B.5种C.6种D.7种【思路点拨】根据“完全燃烧产生等物质的量的CO2和H2O”可确定该有机物中C和H的原子个数比为1:2,然后利用这个关系式对解决问题比较有利。
【答案】B【解析】设该有机物分子式为C n H2n O x,若只有1个氧原子,58-16=42,剩下的为碳和氢,14n=42,则碳只能为3个,即为C3H6O,1个不饱和度。
若有2个O,那么58-32=26,14n=26,n不可能为分数,则不可能为2个氧原子,所以分子式为C3H6O,再根据官能团异构、碳链异构确定同分异构体的种类:醛一种,酮一种,烯醇一种,三元含氧杂环,三元碳环一种,四元杂环一种,共6种,而由题意可知有机物为单官能团,烯醇应舍去,故选B。
