进货评审报告
药品购进质量评审报告

药品购进质量评审报告广东启元药业有限公司2014年GSP进货质量评审记录2015年1月05日保存年限3年(自2015年1月至2018年12月)装订人: 孙晓珊装订日期:2015年1月05日存放地点:质管部广东启元药业有限公司2014年度年药品购进质量评审报告一、评审目的:为了掌握药品进货质量情况,提高质量意识,树立质量第一的思想,严格按照药监部门批准的《药品经营许可证》核准的经营范围和经营方式从事药品经营,规范公司经营行为,良好地实施公司质量体系,确保了药品经营质量。
二、评审依据:《药品经营质量管理规范》、本公司的有关制度程序和国家的相关法律法规。
三、评审机构及人员:评审机构:质量领导小组;评审人员:洪淑琴、吴洁琼、孙晓珊、洪世从、蔡伟华、陈锐沛四、综合评价: ,、进货质量:业务部购进的药品品种质量情况良好,能针对市场需求,产品适销,销售情况良好。
购进药品的原则以销定购为前提。
依据公司制定的药品采购管理制度,由采供部编制年度购货计划,质量管理部参与审核,公司领导审批签字。
对首营品种、首营企业实行了购销合同管理,并制订相应的质量保证协议。
做到采购药品量足、质高、规格齐、品种对路、价格适宜,满足了市场需求扩大了销售提高了效益。
,、供应商情况:公司严格按照《药品经营质量管理规范》及《实施细则》的要求把质量放在选择药品和供货单位的首位。
公司所购近药品都来自正规的药品生产、经营企业,进货前严格审查了供货方的法定资格、经营范围和质量信誉。
对首营企业进行了包括企业资质和质量保证能力的审核,审核由质量管理部会同业务部共同进行,并经质量质量人批准。
分别建立了供货企业质量档案和首营品种质量档案。
供货方合法证照齐全(包括首营企业、首营品种之所需资料)。
经营行为与范围与证照内容一致,履行合同能力包括药品、数量、价格、交货期、票、账、货、款均相符及服务等方面均符合规定要求。
全年审核首营企业**家,首营品种**个。
对与本公司进行业务联系的供货单位销售人员也进行合法资格的验证,严格杜绝伪劣药品进入流通领域,从企业业务经营的源头确保消费者的合法权益。
采购部评审报告

采购部评审报告
采购部建立供应商过程跟踪机制,对货物进行过程跟踪,把主材的合格率控制在98%以上。
对其辅材供应商、外协件加工,实行100%合格验收,及时退换机制,其合格率,基本达到100%。
本年一季度进货批次为160次,不合格次数为2次,合格率为98.7%,其主要原因为来料途中,货物相互挤压,造成整体或部分变形。
对于不合格品,实行立即退换货制度,及时进行了处理辅材及外协加工件,进货批次为96次,不合格次数为0。
由于对供货商,开展过程控制,时时跟踪,入库前,以基本完毕。
为提高供应商质量、合格率、交货准时性。
采购部及时与各供应商沟通,明确各项质量目标及周期。
定期对供应商进行评估与考核。
对不合格工厂,实行立即停用整改措施,如无明显提高,立即更换。
采购部对所有的供应商,实行招标选定机制,由使用方,质量控制方,成本控制方,共同选定。
并对中标方,实行严格的质量理念控制机制。
采购部在与供应商的合作过程中,也发现了很多问题。
主要原因是供应商还没有养成,过程汇报的习惯,需要采购部时时跟踪,造成信息滞后。
采购部今后,除不断提高产品质量外,着重需要培养,供应商的反馈机制。
做到信息及时,准确。
供应商审核报告

日期:____年____月____日
供应商审核报告
供应商名称:_______________________________________
主要业务:______________________________________
地点:______________________________________
是否根据试验的结果(合格或不合格)检验、过程试验和判定产品
产品是否保存直至所有进货检验和过程检验都已完成并且相关的数据文件显示都可用(返工和复测后的最终报告)
是否有文件化的最终检验程序确保产品符合标准(最终检验和试验)
是否保存记录作为产品是否通过检验和试验的依据
产品最终检验(出厂检验)人员是否通过培训并有相应资格
来自所有产品的认证和执行的可靠性试验的可靠性记录是否保存
可靠性测试记录是否包括有以下的内容:产品标识、试验类型和目的、试验条件、试验周期、样本大小和失效数
为产品系列记录是否有可靠性预报
内
部
质
量
审
核
是否建立并维持了用于策划并实施内部质量审核和跟踪活动的文件化的程序
是否有效地安排了内部审核,内部审核是否是根据状态的重要性来安排日程的
设备的适当维护是否已列入计划并执行,确保连续的过程能力
是否有良好的内务环境及防静电措施,是否有明确定义的工艺纪律(规范)及相应的书面化的职责
操作者是否参与持续质量改进活动
是否将产量/缺陷向内外部客户进行通报
检
验
和
试
验
是否检验进厂产品与规定的要求的适应性
正在加工过程中的产品是否根据文件化的程序或质量计划经过检验和试验
联系人:______________________________________
供应商初评报告范文

供应商初评报告范文Supplier Initial Evaluation Report Sample供应商初评报告范文This report aims to provide a comprehensive overview of the initial evaluation of the selected supplier.本报告旨在全面概述所选供应商的初步评估情况。
The supplier, XYZ Company, has been chosen based on its reputation in the industry and its ability to meet our specific requirements.供应商XYZ公司因其在行业声誉和满足我们特定需求的能力而被选中。
During the initial evaluation, XYZ Company demonstrated a strong commitment to quality and timely delivery.在初步评估中,XYZ公司表现出对质量和及时交货的强烈承诺。
Their production facilities were inspected, and it was found that they comply with industry standards and safety regulations.我们对他们的生产设施进行了检查,发现其符合行业标准和安全规定。
Moreover, the supplier's team displayed a high level of professionalism and cooperation during the evaluation process.此外,在评估过程中,供应商的团队表现出高度的专业精神和合作精神。
Overall, XYZ Company appears to be a reliable and capable supplier, and we look forward to further discussing potential business opportunities with them.总的来说,XYZ公司似乎是一个可靠且有能力的供应商,我们期待与他们进一步探讨潜在的业务机会。
浅谈药品进货质量的评审

本文 中我们就循环改进 管理模式在改善 护理人员工 作懈怠感 中的效果进 行观察研究 ,并将研究 效果与采用 常规管理模式 的护理 人员进行 比较 ,结果显示 ,循环改 进管理模式在改善护理人员 的工作倦怠感 方面发挥 出积 极的作用 ,工作懈怠感 量表及 自我感觉懈 怠感评估结果 均显著改善 ,说 明了循 环改进护理模式在 护理人员工作 状态改善 中的效 果 ,而其 具有 的这些优 势均能与循 环改 进管理模式 自身 的 “ 循环 与持续”改进 的特点有关 ,其 在实施 的过程 中不 断改进不足 ,提升管理质 量 ,且 融合 护理人员的需求 ,因此效果较佳 。综上所述 ,我们认 为循环改进管理模式 在改善护理人 员工作懈怠感 中的效 果明显 ,有助于提升护理人员的工作积极性 。
果,并存 档备 查。质 量管理部 门每年应对购进药品情况进行综合质量评审,才能确保质量 管理过程的持续改进 ,促进购进 药品的结构
优 化 , 不 断提 高 药 品 经 营 质 量 。
关 键词 :药 品 ;进 货 质 量 ;评 审
d o i : 1 0 . 3 9 6 9 / ] . i s s r L 1 6 7 2 - 2 7 7 9 . 2 0 1 3 . 2 2 . 1 1 7 文章编号 : 1 6 7 2 - 2 7 7 9 ( 2 0 1 3 ) 一 2 2 - 0 1 5 2 - 0 2
相关分析[ J ] . 现代生物医学进展 , 2 0 1 3 , 1 3 ( 1 2 ) : 2 3 6 2  ̄ 2 3 6 4 , 2 3 5 5 .
( 本文校对 : 吴义红 收稿 日期: 2 0 1 3 - 0 9 - 0 9 )
供货方审核总结报告范文

第三方审核报告是什么第三方审核:又叫做外部审核,所颁发的报告又叫做第三方审核报告。
也有产品上的第三方审核,有管理体系的第三方审核,审核机构必须具有相关的资质证书才能得到认可,一般来说规模较大知名机构所所颁发的公信力和认可度要相对高些。
简单的比如质检报告:根据目前所有产品在你出售之前都需要通过质量检查的,并需要对公司产品合格数的统计,主要是鉴定产品质量达标书面证明(必须具有CNAS和CM两份资质证书的机构来鉴定)。
他是经过对产品和设备的质量检测得出结果。
是保证产品质量体系标准。
审核报告也与此相同,年审的审核报告能全面、客观地反映公司的信息,一般是由独立于供需双方的第三方专业检验机构完成的(必须具有相关资质)。
第三方专业检验机构具有相对的独立性和公正性,有资格向社会出具公正数据(年审报告)。
生产企业对自己内部所做的检验报告,称为第一方(供方)检验报告,由于利益相关,没有向社会出具公正数据的资格。
为了保证第三方检验机构的检验能力和检验工作的科学性和公正性,国家有关部门在确认了检验机构的计量能力后,授予计量认证合格证书,并允许其在检验报告上加盖相关公章,审核报告是根据标准化的要求,对公司等相关情况进行检查与质量监督,并加以分析研究后写出的反映产品和工程质量情况的书面报告。
它是审核的结果和信息反馈的载体。
在经济活动中,它已成为把住质量关的管理手段,成为维护社会正常经济秩序,维护用户合法权益和实施仲裁的依据。
当然,部分也可以进行自我监督审核,这又是另一类型了。
GSP中在购进程序中对供货方的审核问题简单说,首营企业是本企业与生产企业或批发企业首次进行的供需关系的体现;而首营品种只是本企业与生产企业首次进行的供需关系的体现。
首营企业的审核原则是这样的:供货企业(包括生产企业、批发企业)在企业法人、企业负责人、质量负责人、经营范围(或生产范围)、经营地址、仓库地址放生变更时必须进行重新审核。
首营品种的审核:除以上还包括新包装、新剂型、新批准文号发生变更时必须重新审核。
家具合同评审报告模板

家具合同评审报告模板一、合同背景甲方为家具制造商,乙方为家具经销商,双方本着互利共赢的原则,就家具销售相关事宜达成以下合作协议。
二、合同内容1. 商品描述:甲方将提供家具产品,包括沙发、床、桌子、椅子等各类家具。
乙方将负责销售及推广甲方的家具产品。
2. 价格条款:双方协商确定家具产品的售价,并约定分期付款的方式。
同时规定好订金及尾款支付的时间和方式。
3. 交付条款:甲方负责家具产品的生产和交付,双方约定交付时间及交付方式。
4. 质量保证:甲方承诺家具产品的质量均符合国家标准,并提供一定的质量保修期。
5. 维修服务:家具产品出现质量问题或损坏,乙方可提供维修服务。
6. 知识产权:甲方保留家具产品的知识产权,乙方需承诺不得侵犯甲方的知识产权。
7. 合同终止:双方约定合同终止条件及解除方式。
三、评审内容1. 商品描述评审:甲方提供的家具产品是否符合市场需求,乙方是否具备销售这些产品的能力。
2. 价格条款评审:双方协商的价格是否合理,是否能够保障双方的利益。
3. 交付条款评审:甲方是否有能力按时交付产品,交付方式是否便捷。
4. 质量保证评审:甲方质量保证是否具体明确,维修服务是否及时有效。
5. 知识产权评审:甲方的知识产权保护措施是否完善,乙方是否有侵犯知识产权的风险。
6. 合同终止评审:合同终止条件是否合理,双方解除合同的方式是否公平。
四、结论与建议在对家具合同进行全面评审后,我们认为双方协议内容基本合理,但仍存在一些可改进之处。
建议双方在价格条款中进一步细化分期付款方式,确保双方利益达到最大化。
在质量保证方面,建议甲方提供更长的质量保修期,并加强售后服务。
同时,双方应在合同中明确规定知识产权的保护措施,防范知识产权风险。
最后,建议双方进一步完善合同终止条件,确保合同解除的合理性和公平性。
综上所述,我们认为此家具合同具有一定的合理性和可执行性,但仍需双方进一步沟通完善,以确保合作顺利进行。
感谢各位的配合和支持。
进货检验报告范文

进货检验报告范文一、引言本次进货检验是针对20日用品公司最新批量进货产品的质量进行检验和评估。
通过对产品的外观、功能、安全性、加工工艺等方面的检验,对产品的合格率和不合格项目进行分析和总结,为公司的进货决策提供参考。
二、检验方法和过程1.检验方法本次检验主要采用抽样检验的方法,通过对样本产品的检验来评估整批产品的质量情况。
同时,还结合了实地观察和测试等方法,对产品的外观、功能和安全性进行评估。
2.检验过程(1)选取样本:从本次批量进货的产品中,随机选取了50个样本进行检验。
(2)外观检验:对产品的外观质量进行检验,包括产品的颜色、形状、表面光洁度等方面的评估。
(3)功能检验:对产品的功能进行检验,包括产品的使用寿命、使用效果等方面的评估。
(4)安全性检验:对产品的安全性进行检验,包括产品的材质、有毒有害物质等方面的评估。
(5)加工工艺检验:对产品的加工工艺进行检验,包括产品的制作工艺、精度等方面的评估。
(6)检验数据录入和分析:将各个检验项目的结果进行记录和归纳,分析产品的合格率和不合格项目。
三、检验结果1.外观检验结果在对样本产品进行外观检验时,发现有10%的产品存在色差、瑕疵、刮痕等问题,其中以色差问题最为严重,占总不良品数的40%。
2.功能检验结果通过对样本产品的使用测试,发现有5%的产品存在使用寿命不达标、功能不完善等问题,其中以使用寿命不达标问题最为突出,占总不良品数的60%。
3.安全性检验结果经过对产品的材质和有毒有害物质的检验,发现所有样本产品均符合相关标准,不存在安全性问题。
4.加工工艺检验结果对样本产品的加工工艺进行检验后,发现有20%的产品存在制作工艺不精细、尺寸不准确等问题,其中以尺寸不准确问题占总不良品数的30%。
四、问题分析与建议1.外观问题分析外观问题可能是由于制作工艺不精细、储存条件不佳等原因所致。
建议加强产品制作工艺和储存管理,以提高产品的外观质量。
2.功能问题分析功能问题可能是由于产品设计不合理、材料质量不过关等原因所致。
生产部管理评审报告

生产部管理评审报告版本:A/0从我公司2012年11月10日实施ISO9001:2008质量管理体系以来,结合我部门的实际情况,作如下汇报:1、设施管理我部门对我公司的实施、设备进行统一编号登记入册管理,其中对设备制定了日常保养、年度保养的要求,并根据生产的实际情况制定了年度保养计划表,生产作业人员也确实按规定做好了日常保养工作,设备保养人员也按照保养计划的时间安排按时做到了年度保养工作,取得了良好的效果,对于实施故障及时进行了维修.保证了产品的正常生产,现场保持了清洁,有效地保证产品质量。
2、工作环境管理我部门对生产车间布置进行了适当调整,并在生产过程中对生产车间的灰尘等采取了相应措施,实施控制,保持车间无油污、清洁、整齐,机台上无脏布及杂物,并在机器四周留出安全通道,对车间根据生产需要进行了适当的维护,确保产品符合要求.3、产品实现的策划为使产品质量符合规定要求,我部门对产品制造的实现进行策划。
根据本公司质量管理体系的要求确定了产品的质量目标和要求为产品最终检验合格率大于等于98%;通过产品质量技术要求等编制原材料和半成品检验文件、工艺图纸、工序作业指导书等文件,明确产品所要求的验证、确认、监视、检验和试验活动,以及产品接收准则.通上述规定要求编制确定了为实现过程及其产品满足要求提供证据所需的记录如进货验证记录、出厂检验记录等。
4、生产过程的管理我部门对销售部所接的订单配合做好了合同评审,并按照生产任务单及时排好生产任务,下达生产指令,按时完成生产任务。
对作业员都做到了一定的培训,保证了各岗位人员能胜任本岗位工作能力。
在生产过程中作业员按照产品配料单、技术要求、工序作业指导书要求进行操作,并将生产情况填写在生产记录并配合检验员做好了中间检验工作和产品标识,对在现场用料做好了标识工作,并按此放置.同时操作员也做到了积极配合检验人员的检验工作和检验员的对产品判定处理,对生产中的不合格品及时做了相应的处理。
药品进货质量评审报告

药品进货质量评审报告药品进货质量评审报告时间:2022年01月07日地点:公司会议室主持:XXXX参加部门:采购部、销售部、质量管理部部、仓储部、运输部、财务部参加人员:评审目的:对供货企业及购进药品进行综合评价、比照、分析,确定2022年药品合格供货方及合格经营品种,为2022年度制定药品购进方案提供质量依据。
评审范围:对2022年度药品生产企业和经营企业的药品进货情况进行质量评审。
评审依据:1、药品经营质量管理标准及实施细那么;2、公司相关质量体系文件;3、公司内外部质量信息。
评审内容:供货企业的合法性、质量信誉度和售后质量效劳;销售退回药品质量情况;药品售出后的质量投诉、质量查询、药品不良反响信息等情况;药品质量信息反响情况等。
药品供货企业的合法资质和质量保证能力以及供货企业药品售后效劳工作;首营企业审核、药品首营品种审核,到货药品验收合格率;药品在库储存、保管、养护的质量稳定性信息、药品销售及客户资质的审核、药品不良反响信息反响等情况。
张总经理在针对2022年度公司药品经营工作的根底上,强调要提高质量管理意识并提出新一年的工作目标:1、顺应市场,提高个性化效劳,稳步提升。
2、提高员工素质,进一步加强GSP在实际工作中的贯彻执行。
销售部经理XX对药品销售工作以及合法客户资质审核、用户访问、售后效劳工作、公司销售的药品质量、效劳质量意见征询、客户意见反响以及对客户的售后效劳工作到达满意程度等工作进行了认真总结。
质量管理部经理XX对公司质量管理、药品验收、药品在库养护工作做了全面的总结,指出要加强药品的质量管理目标以及在日常的药品质量管理和验收、养护工作中需要注意的方面。
仓储部经理XXX对药品的保管储存、出库复核的重要性以及对温度有特殊要求的药品的储存、出库等考前须知做了总结。
运输部经理XX针对在配送的过程中应注意的环节,对购货单位回执单、运输记录等方面的标准管理做出了总结。
财务部经理XXX对于票据的管做了总结。
药品批发企业年度购货单位质量体系评审评审报告

评审时间:20xx年xx月xx日评审对象:药品批发企业一、项目背景为了确保药品批发企业的质量管理体系能够持续改进和有效运行,提高药品质量管理水平,该企业对购货单位进行了年度质量体系评审。
以评估购货单位在质量体系建设上的成效,为企业制定下一阶段的质量管理目标提供参考。
二、评审内容本次评审主要针对以下内容进行评估:1.购货单位质量体系的建立和有效运行情况;2.购货单位对药品质量的控制和管理措施的落实情况;3.购货单位对药品质量的监测和监控体系的运行情况;4.购货单位的培训和知识管理情况。
三、评审结果1.购货单位质量体系的建立和有效运行情况:购货单位建立了完善的质量管理体系,包括质量控制流程、质量手册、程序文件等。
各项质量管理文件得到了有效执行,并进行了相应的修订和更新。
但在实际运行中,存在一些流程的改进空间,建议加强对流程的优化和标准化。
2.购货单位对药品质量的控制和管理措施的落实情况:购货单位对药品质量的控制和管理措施的落实情况较为良好。
在采购过程中,能够按照相关法规和标准要求进行货品的验收和放行,并且建立了与供应商的合作关系,对供应商的质量管理进行有效监控和评估。
但仍有个别供应商的质量管理存在一定的问题,需要进一步加强管理。
3.购货单位对药品质量的监测和监控体系的运行情况:购货单位建立了完善的药品质量监测和监控体系,包括对进货药品、存货药品的质量检验、复查以及不良品处理等环节的管理。
并且定期进行质量监测和分析,对药品质量进行评估和改进。
但存在一定程度的人力资源短缺和检测设备的更新需要,需要加大对检测能力的投入和提升。
4.购货单位的培训和知识管理情况:购货单位建立了培训档案和知识管理档案,对新员工进行入职培训和在职培训。
并且定期组织和参与相关培训和学习交流活动,提升员工的专业素质和质量意识。
但仍存在一些培训和知识管理的薄弱环节,建议进一步加强对培训和知识管理的监督和指导。
四、评审结论综上所述,购货单位在质量体系建设方面取得了一定的成效,但仍存在一些问题和改进空间,特此提出以下改进建议:1.进一步加强对质量体系流程的优化和标准化,提升流程的高效性和一致性;2.加强对供应商的质量管理,建立更加严格的供应商评估和监控机制;3.加大对质检设备和人力资源的投入和提升,提高质量监测和检验能力;4.加强对培训和知识管理的监督和指导,提升员工的专业素质和质量意识。
产品审核报告
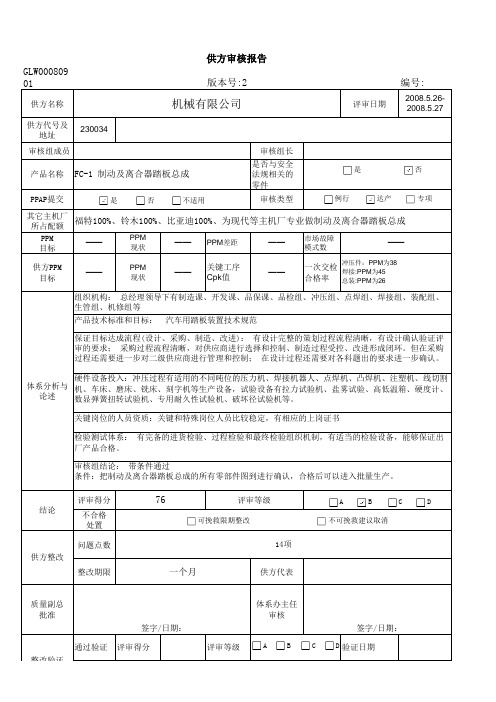
PPM 目标
——
PPM 现状
—— PPM差距
——
市场故障 模式数
——
供方PPM 目标
——
PPM 现状
——
关键工序 Cpk值
——
一次交检 合格率
冲压件:PPM为38 焊接:PPM为45 总装:PPM为26
ቤተ መጻሕፍቲ ባይዱ
组织机构: 总经理领导下有制造课、开发课、品保课、品检组、冲压组、点焊组、焊接组、装配组、 生管组、机修组等
检验测试体系: 有完备的进货检验、过程检验和最终检验组织机制,有适当的检验设备,能够保证出 厂产品合格。
审核组结论: 带条件通过 条件:把制动及离合器踏板总成的所有零部件图到进行确认,合格后可以进入批量生产。
结论 供方整改
评审得分 不合格 处置
问题点数
整改期限
76
评审等级
可挽救限期整改
14项
一个月
供方代表
产品技术标准和目标: 汽车用踏板装置技术规范
保证目标达成流程(设计、采购、制造、改进): 有设计完整的策划过程流程清晰,有设计确认验证评 审的要求; 采购过程流程清晰,对供应商进行选择和控制、制造过程受控、改进形成闭环。但在采购 过程还需要进一步对二级供应商进行管理和控制; 在设计过程还需要对各科题出的要求进一步确认。
GLW00080901
供方审核报告 版本号:2
编号:
供方名称
机械有限公司
评审日期
2008.5.262008.5.27
供方代号及 地址
230034
审核组成员
产品名称 FC-1 制动及离合器踏板总成
审核组长
是否与安全 法规相关的 零件
是
否
供应商现场评审报告

3、生产图纸、工艺文是否经过培训□□□
5、*生产过程中的检验方式:
6、过程检验是否有记录□□□
7、对关键工序过程参数是否有控制□□□
8、对设备、工装、模具有进行维护、保养吗□□□
9、是否有维修、保养记录□□□
10、是否有设备、模具台帐□□□
1、成品出厂是否有检验□□□
2、*检验方式:
3、是否有检验标准□□□
4、成品检验是否有记录□□□
5、成品检验是否得到有效控制□□□
说明:
生产现场、仓库:好(2分)一般(1分)差(0分)
1、现场物料标识是否清楚□□□
2、检验状态标识是否清楚□□□
3、生产现场是否开展定置管理□□□
4、仓库材料标识是否清楚□□□
说明:
不合格品的控制:好(2分)一般(1分)差(0分)
1、不合格品是否有评审□□□
2、生产过程中的不合格品是否有标识、并隔离存放□□□
3、*生产过程中不合格品的处理方式:
4、*进货不合格品的处理方式?
5、不合格品是否有处理记录□□□
6、不合格品是否能够有效控制□□□
说明:
成品控制:好(3分)一般(1分)差(0分)
说明:
计量:好(2分)一般(1分)差(0分)
1、现场使用的计量器具是否□□□
经过计量检定部门检定?
2、是否建立计量管理台帐□□□
(总台帐、送检台帐)
说明:
纠正及预防措施:好(2分)一般(1分)差(0分)
1、公司内发现的质量问题是否有部门负责跟进□□□
2、对客户反馈的质量问题是否采取了有效的整改措施□□□
供应商现场评审报告
现场评审报告
供方名称
药品进货情况质量评审操作规程

药品进货情况质量评审操作规程一、目的对供货单位进行筛选,选择产品质量佳、信誉好的供应商。
二、依据《药品管理法》、2012新版《药品经营质量管理规范》。
三、适用范围本公司药品的供应商。
四、责任人采购部、质量管理部、仓储部。
五、内容1、采购部每年对供应商供货情况进行一次质量评审,质量管理员参加评审。
评审内容应包括到货拒收、验收不合格、销后退回、售后投诉等药品质量管理情况,以及监督抽验情况、供货单位质量信誉等。
评审后形成“药品购进质量评审报告表”,报质量管理部经理审核,总经理批准。
评审报告表应及时归档备查。
2、各部门对每个供应商的药品提供以下数据:①全年供货次数、一次验收合格次数;②内在质量原因不合格品的品种数、全年送货总品种数;③销后退回品种数、全年送货总品种数;④药品全年质量投诉的总次数;⑤药品全年药检部门抽样结果。
⑥药品库存周转情况是正常还是不正常。
3、评审公式:①验收合格率=一次验收合格率×100%②品种在库储存的稳定性;药品在符合储存要求的条件下由于内在质量原因导致不合格品率来反映稳定性。
内在质量原因不合格品率=内在质量原因不合格的品种数/全年送货总品种数×100%③销后退回率;销后退回率=销后退回品种数/全年送货总品种数×100%4、评审标准及结论:只有全部符合以下各项指标的供应商,质量评审为合格。
合格供应商标准:①一次验收合格率≥95%;②药品内在质量原因不合格品率≤10%;③药品销后退回率≤10%;④药品全年质量投诉的总次数为0;⑤药品全年药检部门抽样结果为合格。
⑥药品库存周转情况正常5、评审结果处理经评审不合格的供应商从《合格供应商名录》中除掉,在以后的经营过程中不得从不合格的供货商处购进药品。
6、对发生药品质量问题的、质量公告上被公告的、有信誉不良记录及其他不良行为的供货单位,应对供货单位进行实地考察,重点考察其质量管理体系是否健全、发生质量问题的原因及纠正措施是否有效。
产销型供应商评审报告

2 2 3 2
无作业指导书 无员工培训 无生产该产品核 心生产设备、工导 书、且作业指导书内容体现重 点检验方法 有员工培训计划,且有 有员工培训计划,且有关键工 有首件生产要点培训 关键工序员工培训 序员工培训,关键工序员工完 相关生产设备/工装模具 生产设备/工装模具齐全 生产设备/工装模具在行业具 齐全 且符合质量精度要求 有领先 有作业指导书 有关键工序标识、有作 业指导书 有质量记录且基本完整 有质量记录,且相关记 录能够反映控制要点 可追溯性标识齐全规范 有质量记录,且相关记录齐全 反映质量控制要点 可追溯性标识齐全规范,且有 产品标识管理办法 不合格品标识记录都明确,相 关处理流程经过评审并记录齐 全 生产过程有分区各区,且各分 区标识清楚满足我司要求 包装、运输符超出我司要求 有生产区域划分,生产现场各 种工具、设备明确标识,且各 部分有责任人,现场管理清爽 0 成品检验作业指导书体 现了我司对该类产品的 要求 有基本满足我司要求的 标准、指导书,且相关 检验要有记录 有流程且记录清楚 成品标准和检验作业指导书在 该行业领先 有基本满足我司要求的标准、 指导书,且相关检验要有记 录,检验记录有专人审核 有非常清楚的审批流程,且有 审批记录
2
无检测能力
2
来料无标示
1
无储存时效管理 无不合格品让步 接收、待用无审 批流程 无不合格物料分 析 无仓库、或者仓 库混料 无关键工序控制 方法 生产设备、仪器 没有作业指导 生产过程无检验 文件 无设备 无检验记录
1
对供应商建立了停货、 质量整改、没有淘汰机 制, 进货检的制度完成,且 能检出不良品 检验报告不全面,但关 键的物料有检验报告, 能体现物料的关键特性 具备该类物料的日常检 测/型式试验能力80%以 上测试能力,其他测试 来料有清楚的标识,不 合格品有处理流程,且 有整改措施。 仓库基本能够实现先进 先出,从物料标识颜色 上可以看出库龄 无不合格品让步接收、 待用有审批流程,且有 相关记录 有不合格记录,且有按 月度进行分析 有仓库,有分区、原材 料能整齐存放。 关键工序标识清楚,人 员有认证 有作业指导书、且内容 符合我司要求 检验文件符合重要技术 要求 有设备且有校准标识 有检验记录,且检验记 录频率在2次/小时
进货情况质量评审记录

进货情况质量评审记录******医药有限公司进货情况质量评审记录(2016年6月)目录1.进货质量评审计划2.进货质量评审记录3.进货质量评审报告4.合格供货方目录******医药有限公司2016年6月进货情况质量评审计划一、评审时间2014年6月5日-6日二、评审目的根据新版《药品经营质量管理规范》的要求,公司更换了计算机软件系统,对相关岗位人员进行了岗位调整,对仓库进行了改造,按照公司《药品购进情况质量评审程序》的要求,为有效控制药品进货质量,选择合格的供应商,对公司2014年6月之前的供应商和所构进的药品进行综合质量评审和分析,为药品购进提供决策依据。
三、评审依据1.药品经营质量管理规范及实施细则;2.公司相关质量体系文件;3.公司内外部质量信息(质量档案等)。
四、评审范围及内容1.供货企业的法定资格和质量保证能力包括供货企业生产(经营)许可证、营业执照、质量体系认证和运行情况;供货单位与我公司业务联系的销售人员的合法资格的验证2.供货企业提供品种的合法性和质量可靠性主要评价指标:验收合格率≥95%供货合格率≥95%准时到货率≥90%准确到货率≥95%库存药品检查合格率≥99%药品质量报废率≤1%客户投诉次数少于3次(含3次)重大不良反应少于3次(含3次)3.供货企业质量信誉包括供货企业与我公司签定的合同、质量保证协议的执行情况五、参加评审人员1质量评审工作由质管部负责组织进行;2评审参加人员应包括:质量负责人、质管部经理、采购部经理、销售部经理、质管员、验收员、养护员、储运部经理;六、评审过程各业务环节及质量管理人员根据各自工作中掌握的情况,对公司所经营的药品和供货企业情况做出总结和评价;质量管理部做好《药品购进情况质量评审表》,并根据记录做出评审报告;评审报告经相关部门和负责人审阅,质量管理部进行存档。
****医药有限公司质量管理部2016年6月31日****医药有限公司2016年6月进货情况质量评审报告2014年6月5日-6日,公司质量管理部根据制定的评审计划,会同采购部、储运部相关人员对公司2013年全年所购入药品及供货企业等进货情况进行了质量评审,现将评审情况总结及报告如下。
控制计划评审报告

是否每一工序都有具体的规范/公差
是否都有抽样容量/频率
是否都有控制方法
每一项是否都有具体的反应计划
最终认定:
可按规定不作修改需作更改
小组成员/职务/日期小组成员/职务/日期
小组成员/职务/日期小组成员/职务/日期
控制计划评审报告
顾客:XXXXXXX有限公司日期:20XX/XX/XXX
零件号:XX-XXXXX零件名称:XXXX-XXXXX
是
否
问题
在制定控制计划时是否使用了第6章所述的控制计划方法
是否按规定使用固定表单
是否已考虑过程FMEA
是否已考虑过程流程图
是否包括所有特殊特性
是否参考了类似零件的控制计划
小组是否了解整个过程
小组成员/职务/日期小组成员/职务/日期
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
睢县药业有限责任公司
2015年度进货质量评审报告
一、评审时间:2015年元月5日至2015年元月10日
二、评审目的:通过对供货方质量管理体系、药品质量、药品流转中质量状况进行回顾性评价,选择合适的供货商,有效控制药品经营质量。
三、评审依据:GSP条款及公司质量管理制度。
四、评审方法;对供货单位逐一进行评审,包括:
1、质管部对供货方资料存档情况、考察情况;
2、业务部门对供货单位的供货能力及药品流转情况;
3、质管部与业务部共同对供货单位质保能力及商业信誉进行综合评审。
五、参加人员:
陈勇曹新忠徐照军吴继章杨磊钮磊肖传丽曹益玮崔建华申奥林李广朝黄伟
六、评审内容:
1、购进企业情况:本年度共从46家单位进货,其中,生产企业3家,经营企业43家。
供货单位有:安徽阜阳新特药有限责任公司、哈药集团世一堂百川医药商贸有限公司、河南九州通医药有限公司、商丘市华杰医药有限公司、河南省一顺药业有限公司、河南省中科医药有限公司、河南省国药医药有限公司等(详见附表)。
这些单位资料齐全,销售人员资质合法,质管部门审核程序严格,对其供货能力、
药品流转情况、质量保证能力、商业信誉进行了逐一评审。
2、入库验收情况:本年度共验收入库7345个批次。
3、进货退出情况:本年度共采购退出18个批次,退出原因为滞销、包装破损等因素。
4、销后退回情况:本年度共销后退回2384个批次,退回原因为价格较高、回款不及时、剂型开错等因素。
5、在库储存情况:本年度共养护8712个批次。
根据药品流转情况,对这些批次药品进行外观和包装质量抽查,未发现异常情况。
6、监督抽查情况:本年度共监督抽查药品72批次;医疗器械2批次。
均合格。
7、顾客投诉情况:无顾客投诉。
七、综合报告:本年度共从46家单位进货,供货总数为7363个批次,质量合格率98.24%;
通过进货质量评审有37家企业信誉良好,9家企业质量信誉较好。
46家企业资料齐全,销售人员资质合法,药品供应及时,质量保证能力及流转情况良好。
质量管理部业务部
睢县药业有限责任公司
2015年元月11日。
