高考化学专题有机化学复习
高中化学高考复习有机化学必记知识点(共48条)

高中化学有机化学必记知识点1、常温常压下为气态的有机物:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。
2、在水中的溶解度:碳原子较少的醛、醇、羧酸(如甘油、乙醇、乙醛、乙酸)易溶于水;液态烃(如苯、汽油)、卤代烃(溴苯)、硝基化合物(硝基苯)、醚、酯(乙酸乙酯)都难溶于水;苯酚在常温微溶与水,但高于65℃任意比互溶。
3、有机物的密度:所有烃、酯、一氯烷烃的密度都小于水;一溴烷烃、多卤代烃、硝基化合物的密度都大于水。
4、能使溴水反应褪色的有机物有:烯烃、炔烃、苯酚、醛、含不饱和碳碳键(碳碳双键、碳碳叁键)的有机物。
能使溴水萃取褪色的有:苯、苯的同系物(甲苯)、CCl4、氯仿、液态烷烃等。
5、能使酸性高锰酸钾溶液褪色的有机物:烯烃、炔烃、苯的同系物、醇类、醛类、含不饱和碳碳键的有机物、酚类(苯酚)。
6、碳原子个数相同时互为同分异构体的不同类物质:烯烃和环烷烃、炔烃和二烯烃、饱和一元醇和醚、饱和一元醛和酮、饱和一元羧酸和酯、芳香醇和酚、硝基化合物和氨基酸。
7、无同分异构体的有机物是:烷烃:CH4、C2H6、C3H8;烯烃:C2H4;炔烃:C2H2;氯代烃:CH3Cl、CH2Cl2、CHCl3、CCl4、C2H5Cl;醇:CH4O;醛:CH2O、C2H4O;酸:CH2O2。
8、属于取代反应范畴的有:卤代、硝化、磺化、酯化、水解、分子间脱水(如:乙醇分子间脱水)等。
9、能与氢气发生加成反应的物质:烯烃、炔烃、苯及其同系物、醛、酮、不饱和羧酸(CH2=CHCOOH)及其酯(CH3CH=CHCOOCH3)、油酸甘油酯等。
10、能发生水解的物质:金属碳化物(CaC2)、卤代烃(CH3CH2Br)、醇钠(CH3CH2ONa)、酚钠(C6H5ONa)、羧酸盐(CH3COONa)、酯类(CH3COOCH2CH3)、二糖(C12H22O11)(蔗糖、麦芽糖、纤维二糖、乳糖)、多糖(淀粉、纤维素)((C6H10O5)n)、蛋白质(酶)、油脂(硬脂酸甘油酯、油酸甘油酯)等。
高考化学一轮复习有机化学基础

转化关系和一些基本概念、基本理论的掌握和应 用能力;进行结构简式的判断时,注意结合题目 中已知物质的结构简式进行分析,找出不同之 处,这些地方是断键或生成键,一般整个过程中 碳原子数和碳原子的连接方式不变,从而确定结 构简式,特别注意书写的正确性,如键的连接方 向。
探究三 有机合成与有机推断
一、知识归纳 1.有机合成题的解题思路与解题步骤 (1)有机合成题的解题思路
A.Y 的结构有 4 种 B.X、Z 能形成戊酸丁酯,戊酸丁酯有 4 种 C.与 X 互为同分异构体,且不能与金属钠 反应的有机物有 4 种 D.与 Z 互为同分异构体,且能发生水解反 应的有机物有 9 种
【解析】A.丁基有
四种结构,Y 是丁基和溴原
子结合而成,所以有四种结构,故 A 正确;B.戊酸丁酯中 的戊酸,相当于丁基连接一个—COOH,所以有四种结构, 而丁醇是丁基连接一个—OH,所以也有四种结构,但戊 酸由丁醇转化得到,一一对应,因此戊酸丁酯有四种,故 B 正确;C.X 为丁醇,其同分异构体中不能与金属钠反应 的是醚,分别是 C—O—C—C—C、C—C—O—C—C 和
2.重要的有机反应类型与主要有机物类型之间
的关系
基本类型
有机物类别
取 代 反 应
卤代反应 酯化反应 某些水解反应 硝化反应 磺化反应
饱和烃、苯和苯的同系物、酚等 醇、羧酸、糖类等
卤代烃、酯、蛋白质等 苯和__苯_的__同__系__物___等 苯和苯的同系物等
加成反应
烯烃、炔烃、苯和苯的同系物、 醛等
【解析】(1)根据上述分析,A 的结构简式为
。 (2)根据上述分析,可知 B 的结构简式为 CH3CH(OH)CH3,依据醇的命名,其化学名称为 2-丙醇或异丙醇。
高中有机化学复习资料汇总

高考有机化学总复习专题一:有机物的结构和同分异构体:(一)有机物分子式、电子式、结构式、结构简式的正确书写:1、分子式的写法:碳-氢-氧-氮(其它元素符号)依次。
2、电子式的写法:驾驭7种常见有机物和4种基团:7种常见有机物:CH4、C2H6、C2H4、C2H2、CH3CH2OH、CH3CHO、CH3COOH。
4种常见基团:-CH3、-OH、-CHO、-COOH。
3、结构式的写法:驾驭8种常见有机物的结构式:甲烷、乙烷、乙烯、乙炔、乙醇、乙醛、乙酸、乙酸乙酯。
(留意键的连接要精确,不要错位。
)4、结构简式的写法:结构简式是结构式的简写,书写时要特殊留意官能团的简写,烃基的合并。
要通过练习要能识别结构简式中各原子的连接依次、方式、基团和官能团。
驾驭8种常见有机物的结构简式:甲烷CH4、、乙烷C2H6、乙烯C2H4、、乙炔C2H2、乙醇CH3CH2OH、乙醛CH3CHO、乙酸CH3COOH、乙酸乙酯CH3COOCH2CH3。
(二)同分异构体:要与同位素、同素异形体、同系物等概念区分,留意这四个“同”字概念的内涵和外延。
并能娴熟地作出推断。
1、同分异构体的分类:碳链异构、位置异构、官能团异构。
2、同分异构体的写法:先同类后异类,主链由长到短、支链由整到散、位置由心到边。
3、烃卤代物的同分异构体的推断:找对称轴算氢原子种类,留意从对称轴看,物与像上的碳原子等同,同一碳原子上的氢原子等同。
专题二:官能团的种类及其特征性质:(一)、烷烃:(1)通式:C n H2n+2,代表物CH4。
(2)主要性质:①、光照条件下跟卤素单质发生取代反应。
②、在空气中燃烧。
③、隔绝空气时高温分解。
(二)、烯烃:(1)通式:C n H2n(n≥2),代表物CH2=CH2,官能团:-C=C-(2)主要化学性质:①、跟卤素、氢气、卤化氢、水发生加成反应。
②、在空气中燃烧且能被酸性高锰酸钾溶液氧化。
③、加聚反应。
(三)、炔烃:(1)通式:C n H2n-2(n≥2),代表物CH≡CH,官能团-C≡C-(2)主要化学性质:①、跟卤素、氢气、卤化氢、水发生加成反应。
高考化学专题突破:有机化学选择题及知识点总结

高考化学专题突破:有机化学选择题 一、计算1、与Na 、NaOH 、Na 2CO 3、NaHCO 3反应醇酚羧酸酯、卤代烃Na √ √ √ × NaOH × √ √ √ Na 2CO 3 ×√ √ × NaHCO 3 ××√×备注酸性:醋酸>碳酸>苯酚>HCO 3->H 2O 重要反应:ONa OH NaHCO 3+CO 2++H 2O(现象:溶液变浑浊)例:1mol 该物质与足量的下列物质反应各消耗多少mol Na:3mol,产生H 21.5molNaOH:8mol Na 2CO 3:2mol NaHCO 3:1mol2、与H 2,HX(HCl,HBr),X 2(Cl 2,Br 2)加成 烯烃,炔烃 苯 醛,酮 羧酸,酯H 2√ √ √ × HX(HCl,HBr) √ × √ × X 2(Cl 2,Br 2)√×××例:1mol 该物质与足量的下列物质反应各消耗多少mol H 2HX(HCl,HBr)X 2(Cl 2,Br 2)3、不加条件与HX(HCl,HBr),X (Cl ,Br )取代 酚(邻位、对位可取代) 醇HX(HCl,HBr) × √ X 2(Cl 2,Br 2)√×+3 Br2→↓+3HBr+4 Br2→+4HBr +3 Br2→+3HBr CH3OH+HX→CH3X+H2O例:1mol该物质与足量的下列物质反应各消耗多少molHX(HCl,HBr):加成(5mol)取代(2mol)X2(Cl2,Br2):加成(3mol)取代(2mol)二、物理性质标况下状态熔沸点水溶性密度烃类C≦4为气态(新戊烷例外) 因为有机物均为分子晶体,所以熔沸点均随相对分子质量增大而增大。
②支链增加,熔沸点降低③醇和羧酸中含有氢键,熔沸点会增大难溶于水小于水(1)卤代烃C≦3的一氟烷烃一氯甲烷(CH3Cl,沸点 -24.2℃)氟里昂(CCl2F2沸点 -29.8℃)氯乙烯(CH2==CHCl,沸点 -13.9℃)四氟乙烯(CF2==CF2,沸点 -76.3℃)难溶于水一氟代烷、一氯代烷<1;一溴代烷,一碘代烷>1;C↑密度↓;醇非气态C≦4:互溶5≦C≦11:能溶C≧12:不溶烷烃<烷醇<1; 芳香醇>1酚非气态T<650C,不溶T>650C,互溶大于1醚甲醚(CH3OCH3,沸点为-23℃)甲醚溶于水,乙醚溶解度为10g小于1醛酮甲醛(...HCHO....,沸点... -.21..℃)..C≦4:互溶小于1羧酸非气态C≦4:互溶C≧5:不溶大于1 酯非气态难溶于水小于1 硝基化合物非气态难溶于水大于1 常见标况下22.4LCHCl3中含有的原子数鉴别:溴苯,苯,乙醇三、性质1、能使高锰酸钾溶液褪色的物质及有关化学反应原理分别为:(均为发生氧化还原反应褪色)①与烯烃、炔烃、二烯烃等不饱和烃类反应,使高锰酸钾溶液褪色;与苯的同系物(甲苯、乙苯、二甲苯等)反应,使酸性高锰酸钾溶液褪色。
高考常考有机化学知识点总结

(摘编整理)
1.需水浴加热的反应有:(1)银镜反应(2)乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)酚醛树脂的制取(6)固体溶解度的测定
2.需用温度计的实验有:(1)实验室制乙烯(170℃)(2)蒸馏 (3)固体溶解度的测定(4)乙酸乙酯的水解(70-80℃) (5)中和热的测定 (6)制硝基苯(50-60℃)
16.能使溴水褪色的物质有:
(1)含有碳碳双键和碳碳叁键的烃和烃的衍生物(加成)
(2)苯酚等酚类物质(取代)
(3)含醛基物质(氧化)
(4)碱性物质(如NaOH、Na2CO3)(氧化还原――歧化反应)
(5)较强的无机还原剂(如SO2、KI、FeSO4等)(氧化)
(6)有机溶剂(如苯和苯的同系物、四氯甲烷、汽油、已烷等,属于萃取,使水层褪色而有机层呈橙红色。)
⑷淀粉遇碘单质变蓝色
⑸蛋白质遇浓硝酸呈黄色(颜色反应)
15.能使高锰酸钾酸性溶液褪色的物质有:
(1)含有碳碳双键、碳碳叁键的烃和烃的衍生物、苯的同系物
(2)含有羟基的化合物如醇和酚类物质
(3)含有醛基的化合物
(4)具有还原性的无机物(如SO2、FeSO4、KI、HCl、H2O2等)
19.能使蛋白质变性的物质有:强酸、强碱、重金属盐、甲醛、苯酚、强氧化剂、浓的酒精、双氧水、碘酒、三氯乙酸等。
8.能与NaOH溶液发生反应的有机物:
(1)酚
(2)羧酸
(3)卤代烃(水溶液:水解;醇溶液:消去)
(4)酯(水解,不加热反应慢,加热反应快)
(5)蛋白质(水解)
9.能与Na2CO3溶液发生反应的有机物:酚、羧酸
10.显酸性的有机物有:含有酚羟基和羧基的化合物。
高考化学推断题综合题专题复习【认识有机化合物】专题解析及答案

高考化学推断题综合题专题复习【认识有机化合物】专题解析及答案一、认识有机化合物练习题(含详细答案解析)1.(1)的系统名称是_________;的系统名称为__________。
(2)2,4-二甲基-3-乙基戊烷的结构简式是_____,1mol该烃完全燃烧生成二氧化碳和水,需消耗氧气_______mol。
(3)键线式表示的物质的结构简式是__________________。
【答案】3,4-二甲基辛烷 1,2,3-三甲苯 14mol CH3CH2CH=CH2【解析】【分析】(1)命名烷烃时,先确定主链碳原子为8个,然后从靠近第一个取代基的左端开始编号,最后按取代基位次—取代基名称—烷烃名称的次序命名。
命名苯的同系物时,可以按顺时针编号,也可以按逆时针编号,但需体现位次和最小。
(2)书写2,4-二甲基-3-乙基戊烷的结构简式时,先写主链碳原子,再编号,再写取代基,最后按碳呈四价的原则补齐氢原子,1mol该烃耗氧量,可利用公式312n进行计算。
(3)键线式中,拐点、两个端点都是碳原子,再确定碳原子间的单、双键,最后依据碳呈四价的原则补齐氢原子,即得结构简式。
【详解】(1) 主链碳原子有8个,为辛烷,从左端开始编号,最后按取代基位次—取代基名称—烷烃名称的次序命名,其名称为3,4-二甲基辛烷。
命名时,三个-CH3在1、2、3位次上,其名称为1,2,3-三甲苯。
答案为:3,4-二甲基辛烷;1,2,3-三甲苯;(2)书写2,4-二甲基-3-乙基戊烷的结构简式时,主链有5个碳原子,再从左往右编号,据位次再写取代基,补齐氢原子,得出结构简式为;1mol该烃耗氧量为3912⨯+mol=14mol 。
答案为:;14mol ;(3)键线式中,共有4个碳原子,其中1,2-碳原子间含有1个双键,结构简式为CH 3CH 2CH=CH 2。
答案为:CH 3CH 2CH=CH 2。
【点睛】给有机物命名,确定主链时,在一条横线上的碳原子数不一定最多,应将横线上碳、取代基上碳综合考虑,若不注意这一点,就会认为的主链碳原子为7个,从而出现选主链错误。
高考化学 有机化学知识点归纳(全)

催化剂 催化剂 加热、加压 有机化学知识点归纳一、有机物的结构与性质1、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无 ;通式:CnH2n+2;代表物:CH4B) 结构特点:键角为109°28′,空间正四面体分子。
烷烃分子中的每个C 原子的四个价键也都如此。
C) 物理性质:1.常温下,它们的状态由气态、液态到固态,且无论是气体还是液体,均为无色。
一般地,C1~C4气态,C5~C16液态,C17以上固态。
2.它们的熔沸点由低到高。
3.烷烃的密度由小到大,但都小于1g/cm^3,即都小于水的密度。
4.烷烃都不溶于水,易溶于有机溶剂D) 化学性质: ①取代反应(与卤素单质、在光照条件下), ,……。
②燃烧 ③热裂解C16H34 C8H18 + C8H16 ④烃类燃烧通式: O H 2CO O )4(H C 222y x y x t x +++−−−−→−点燃⑤烃的含氧衍生物燃烧通式:O H 2CO O )24(O H C 222y x z y x z y x +-++−−−−→−点燃 E) 实验室制法:甲烷:3423CH COONa NaOH CH Na CO +→↑+注:1.醋酸钠:碱石灰=1:3 2.固固加热 3.无水(不能用NaAc 晶体) 4.CaO :吸水、稀释NaOH 、不是催化剂(2)烯烃:A) 官能团: ;通式:CnH2n(n ≥2);代表物:H2C=CH2B) 结构特点:键角为120°。
双键碳原子与其所连接的四个原子共平面。
C) 化学性质:①加成反应(与X2、H2、HX 、H2O 等)②加聚反应(与自身、其他烯烃) ③燃烧 ④氧化反应 2CH2 = CH2 + O2 2CH3CHOCH 4 + Cl 2CH 3Cl + HCl 光 CH 3Cl + Cl 2CH 2Cl 2 + HCl 光 CH 4 + 2O 2CO 2 + 2H 2O 点燃 CH 4 C + 2H 2 高温 隔绝空气C=C CH 2=CH 2 + HX CH 3CH 2X催化剂 CH 2=CH 2 + 3O 22CO 2 + 2H 2O 点燃 n CH 2=CH 2 CH 2—CH 2 n 催化剂 CH 2=CH 2 + H 2O CH 3CH 2OH 催化剂 加热、加压 CH 2=CH 2 + Br 2BrCH 2CH 2Br CCl 4 原子:—X 原子团(基):—OH 、—CHO (醛基)、—COOH (羧基)、C 6H 5— 等化学键: 、 —C ≡C — C=C 官能团 CaO △⑤烃类燃烧通式:O H 2CO O )4(H C 222y x y x y x +++−−−−→−点燃D) 实验室制法:乙烯:CH 3CH 2OH C H 2CH 22SO4+↑H 2O 注:1.V 酒精:V 浓硫酸=1:3(被脱水,混合液呈棕色)2. 排水收集(同Cl2、HCl )控温170℃(140℃:乙醚)3.碱石灰除杂SO2、CO24.碎瓷片:防止暴沸E) 反应条件对有机反应的影响:CH2=CH -CH3+HBr CH 3CH 3Br(氢加在含氢较多碳原子上,符合马氏规则)CH2=CH -CH3+HBr CH3-CH2-CH2-Br (反马氏加成) F )温度不同对有机反应的影响: CH 2CHCH CH 22CH CH 2Br Br + Br 2 CH 2CH CH CH 260℃2CH CH CH 2Br Br + Br 2(3)炔烃:A) 官能团:—C≡C— ;通式:CnH2n —2(n ≥2);代表物:HC≡CHB) 结构特点:碳碳叁键与单键间的键角为180°。
高考化学专题复习有机化合物的推断题综合题含答案
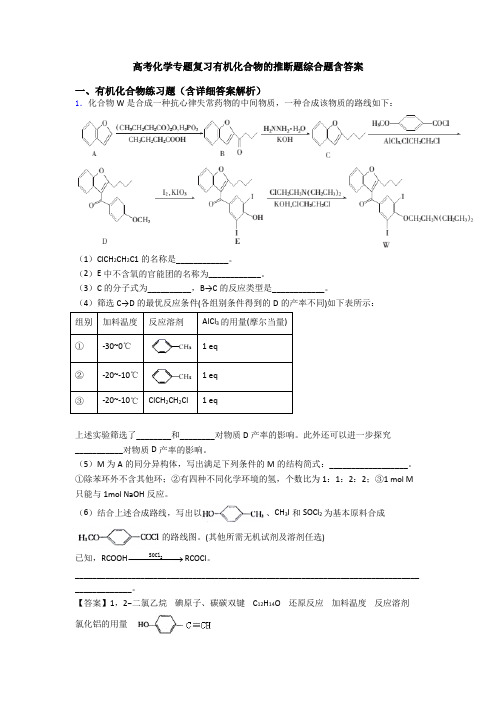
高考化学专题复习有机化合物的推断题综合题含答案一、有机化合物练习题(含详细答案解析)1.化合物W 是合成一种抗心律失常药物的中间物质,一种合成该物质的路线如下:(1)ClCH 2CH 2C1的名称是____________。
(2)E 中不含氧的官能团的名称为____________。
(3)C 的分子式为__________,B→C 的反应类型是____________。
(4)筛选C→D 的最优反应条件(各组别条件得到的D 的产率不同)如下表所示: 组别 加料温度 反应溶剂AlCl 3的用量(摩尔当量) ①-30~0℃ 1 eq ②-20~-10℃ 1 eq ③ -20~-10℃ ClCH 2CH 2Cl 1 eq上述实验筛选了________和________对物质D 产率的影响。
此外还可以进一步探究___________对物质D 产率的影响。
(5)M 为A 的同分异构体,写出满足下列条件的M 的结构简式:__________________。
①除苯环外不含其他环;②有四种不同化学环境的氢,个数比为1:1:2:2;③1 mol M 只能与1mol NaOH 反应。
(6)结合上述合成路线,写出以、CH 3I 和SOCl 2为基本原料合成的路线图。
(其他所需无机试剂及溶剂任选)已知,RCOOH 2SOCl −−−−−→RCOCl 。
____________________________________________________________________________________________。
【答案】1,2−二氯乙烷 碘原子、碳碳双键 C 12H 14O 还原反应 加料温度 反应溶剂 氯化铝的用量322CH I ClCH C 1OH H K C −−−−−−→、+4KMnO (H )−−−−−−→2SOCl−−−−−→【解析】【分析】A 发生取代反应生成B ,B 发生还原反应生成C ,C 发生取代反应生成D ,D 发生取代反应生成E ,E 发生取代反应生成W ;(1)该分子中含有2个碳原子,氯原子位于1、2号碳原子上;(2)E 中含有的官能团是醚键、碳碳双键、羰基、碘原子、酚羟基;(3)根据结构简式确定分子式;B 分子去掉氧原子生成C ;(4)对比表中数据不同点确定实验筛选条件;还可以利用氯化铝量的不同探究氯化铝对D 产率的影响;(5)M 为A 的同分异构体,M 符合下列条件:①除苯环外不含其他环;②有四种不同化学环境的氢,个数比为1:1:2:2;③l mol M 只能与1 molNaOH 反应,说明含有1个酚羟基;根据其不饱和度知还存在1个碳碳三键;(6)以、CH 3I 和SOCl 2为基本原料合成,可由和SOCl 2发生取代反应得到,可由发生氧化反应得到,可由和CH 3I 发生取代反应得到。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实用标准
文档大全高考化学专题复习——有机化学
七、有机反应类型与对应物质类别
1.取代反应
(1)定义:
有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
(2)能发生取代反应的物质:
①烷烃:光照条件下与X2取代;
②芳香烃:Fe(FeX3)条件下与X2发生苯环上的取代;与浓硝酸浓硫酸在50~60℃水浴下的硝化反应;与浓硫酸在70~80℃水浴条件下的磺化反应;在光照下与X2发生烷基上的取代;
③醇:与HX取代;与含氧酸酯化;分子间脱水;
注:醇与钠的反应归入置换反应。
④酚:与浓溴水生成2,4,6-三溴苯酚;与浓硝酸生成2,4,6-三硝基苯酚;
注:液态酚与钠的反应仍属于置换反应。
⑤酯:酯的水解;
⑥羧酸:羧酸的酯化反应;
⑦卤代烃:与NaOH溶液共热水解。
(3)典型反应
CH4+Cl2 CH3Cl+HCl
实用标准
文档大全
CH3CH2OH+HBr
CH3CH2Br+H2O
CH3CH2OH+HOCH2CH 3 CH3CH2OCH2CH3
2.加成反应
(1)定义:
有机物分子里不饱和的碳原子跟其他原子或原子团直接结合生成别的物质。
(2)能发生加成反应的物质,包括含C=C、 C C、-CHO、羰基、苯环的物质,具体如下:
①烯烃:与H2、X2、HX、H2O、HCN等加成;
②炔烃:与H2、X2、HX、H2O、HCN等加成;
③苯及同系物:与H2在Ni催化下加成、与Cl2在紫外光下加成;
④醛:与HCN、H2等;
⑤酮:H2;
实用标准
文档大全⑥还原性糖:H2;
⑦油酸、油酸盐、油酸某酯、油(不饱和高级脂肪酸甘油酯)的加成:H2、H2O、X2等;
⑧不饱和烃的衍生物,如卤代烯烃、卤代炔烃、烯醇、烯醛、烯酸、烯酸酯、烯酸盐等等。
说明:
一般饱和羧酸、饱和酯不发生加成反应。
(3)典型反应
CH2=CH2+Br2→CH2Br—CH2Br
3.加聚反应
(1)定义:
通过加成聚合反应形成高分子化合物。
(2)特征:①是含C=C双键物质的性质。
②生成物只有高分子化合物。
(3)能发生加聚反应的物质:烯、二烯、含C=C的其他类物质。
(4)典型反应
实用标准
文档大全
4.缩聚反应
(1)定义:通过缩合(缩去HX、H2O、NH3等)反应生成高分子化合物的反应。
(2)特征:生成高分子化合物和小分子物质。
(3)能发生缩聚反应的物质
①苯酚与甲醛②二元醇与二元酸③羟基羧酸④氨基酸⑤葡萄糖
(4)典型反应
说明:
(1)加聚反应与缩聚反应,是合成高分子化合物的两大反应,但区别很大。
(2)加聚反应是由不饱和的单体聚合成高分子的反应,其产物只有一种高分子化合物。
(3)参加缩聚反应的单体一般含有两种或两种以上能相互作用的官能团(或两个或两
个以上易断裂的共价键)的化合物,产物中除一种高分子化合物外,还生成有小分子.如H2O、HCl、NH3等。
链节的组成与参加反应的任何一种单体均不相同。
(4)从反应机理上看,加聚反应是不饱和分子中的双键发生的,实质还是加成反应。
双键是发生加聚反
实用标准
文档大全应的内因。
缩聚反应是通过单体中的官能团相互作用经缩合生成小分子,同时又聚合成大分子的双线反应。
发生缩聚反应的内因是相互能作用的官能团(或较活动的
原子)。
(5)发生加聚反应的单体不一定是一种物质。
也可以是两种或两种以上。
如丁苯橡胶就是由单体1,3—丁二烯和苯乙烯加聚而成,缩聚反应的单体不一定就是两种,也有
一种的,如单糖缩聚成多糖、氨基酸缩聚成多肽,也可以是两种以上的。
5.消去反应
(1)定义:
从一个有机分子中脱去小分子(如H2O,HX等),而生成不饱和化合物(含双键或叁键)的反应。
(2)能发生消去反应的物质:醇、卤代烃。
(3)典型反应
6.氧化反应
(1)含义:有机物去H或加O的反应.
(2)类型:
①在空气或氧气中燃烧。
②在催化剂存在时被氧气氧化。
如:
③有机物被某些非O2的氧化剂氧化。
包括:
a.能被酸性KMnO4氧化的是含C=C、 C
C、-CHO及部分含-OH的物质,具体包括:
烯、炔、二烯、油脂(含C=C)、苯的同系物、酚、醛、葡萄糖、部分醇等。
说明:
实用标准
文档大全饱和的羧酸、饱和的酯一般不能被酸性高锰酸钾氧化。
b.能被银氨溶液或新制备的Cu(OH)2悬浊液氧化的是含-CHO的物质,包括:
醛类、甲酸及甲酸酯、甲酸盐、葡萄糖、麦芽糖。
RCHO+2Cu(OH) 2 RCOOH+Cu2O↓+2H2O
7.还原反应
(1)含义:有机物加H去O的反应。
(2)类型:含C=C、 C
C、-CHO、羰基、苯环的物质,包括:
烯、二烯、炔、芳香族化合物、油脂、醛、甲酸及其盐和酯、酮、葡萄糖、麦芽糖等。
如:
8.酯化反应(属于取代反应)
(1)定义:酸跟醇起作用,生成酯和水的反应。
(2)能发生酯化反应的物质:羧酸与醇、无机含氧酸与醇、无机含氧酸与纤维素。
(3)典型反应
9.水解反应(属于取代反应)
(1)反应特征:有水参加反应,有机物分解成较小的分子。
(2)能够水解的物质:碳化钙等、
CH3COOC2H5+NaOH
CH3COONa+CH3CH2OH
实用标准
文档大全
注:
其他水解的物质有CaC2、Al2S3、弱酸根、弱碱的阳离子等。
举例如下:
CaC2+2H2O
Ca(OH)2↓+H2O
Al2S3+6H2O=2Al(OH)3↓+3H2S↑
Fe3++3H2O Fe(OH)3+3H+
CO32-+H2O HCO3-+OH-
10. 其它反应
①有机物跟钠反应
②碳化
③氨基酸的两性
④低聚合:
八、常见有机物的鉴别
常见有机物的鉴别试剂、反应现象(或能否反应)如下表:(注:能反应的打“√”,不能反应的略)
实用标准
文档大全碳双碳叁甲苯卤代烃醇苯酚醛甲酸乙酸甲酸
酯葡萄糖淀粉蛋白质
Na
NaOH
水解加硝水
NC
NaHC
B萃白沉
KMn伯醇
石芯试
银氨溶
新Cu(OH常溶溶
加
FeC
说明:
能使溴水、H+、KMnO4溶液褪色,且能发生银镜反应的还有葡萄糖溶液。
