全国高中学生化学竞赛有机化学专项练习答案
全国竞赛高中学生化学(省级赛区)试题及答案

中国化学会全国高中学生化学竞赛(省级赛区)试卷、答案及评分标准题号1234567891011总分满分155781181361179100评分通则1.凡要求计算或推导的,必须示出计算或推导过程。
没有计算或推导过程,即使结果正确也不得分。
2.有效数字错误,扣0.5 分,但每一大题只扣 1 次。
3.单位不写或表达错误,扣0.5 分,但每一大题只扣 1 次。
4.只要求 1 个答案、而给出多个答案,其中有错误的,不得分。
5.方程式(不是反应式!)不配平不得分。
6.用铅笔解答(包括作图)无效。
7.使用涂改液涂改的解答无效。
8.不包括在标准答案的 0.5 分的题,可由省、市、自治区评分组讨论决定是否给分。
9.答案中红色字为标准答案,而蓝字体(加下划线)为注释语不属于答案。
H元素周期表He 1.008 4.003Li Be B C N O F Ne6.941 9.01210.81 12.01 14.01 16.00 19.00 20.18Na Mg Al Si P S Cl Ar22.99 24.3126.98 28.09 30.97 32.07 35.45 39.95K Ca Sc Ti VCr Mn Fe Co NiCu Zn Ga Ge As Se Br Kr39.1040.08 44.96 47.88 50.94 52.00 54.9455.8558.93 58.69 63.5565.3969.72 72.61 74.92 78.96 79.90 83.80Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe85.4787.62 88.91 91.2292.9195.94 98.91101.1102.9 106.4 107.9112.4114.8 118.7 121.8 127.6 126.9 131.3Cs Ba Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn 132.9137.3 La-Lu 178.5180.9183.9 186.2 190.2192.2 195.1 197.0200.6204.4 207.2 209.0[210] [210]] [222]Fr RaAc-Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo[223][226]La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb LuAc Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr气体常数R= 8.31447 J K 1 mol 1法拉第常数 F = 96485 C mol 1阿佛加德罗常数N A=6.022142 ×1023 mol 1第1题 (15分)1-1 2009年10月合成了第117号元素,从此填满了周期表第七周期所有空格,是元素周期系发展的一个里程碑。
高中化学竞赛样题及答案

高中化学竞赛样题及答案一、选择题1. 下列关于元素周期表的描述,错误的是:A. 元素周期表是按照原子序数递增的顺序排列的B. 同一周期内,原子核外电子层数相同C. 同一族元素,最外层电子数相同D. 过渡元素包括副族和第Ⅷ族元素答案:B二、填空题2. 酸碱中和反应的实质是______与______的反应。
答案:H⁺;OH⁻三、判断题3. 燃烧是一种氧化还原反应。
答案:对四、简答题4. 请简述酸碱中和反应的原理。
答案:酸碱中和反应是指酸和碱在一定条件下反应生成盐和水的化学反应。
酸碱中和反应的实质是氢离子(H⁺)和氢氧根离子(OH⁻)的反应。
在反应过程中,酸释放出H⁺离子,碱释放出OH⁻离子,二者结合生成水,同时形成盐。
五、计算题5. 某溶液中含有KOH和NaOH,其浓度分别为0.2 mol/L和0.3 mol/L。
求该溶液的pH值。
答案:首先,我们需要计算出溶液中氢氧根离子(OH⁻)的浓度:c(OH⁻) = c(KOH) + c(NaOH) = 0.2 mol/L + 0.3 mol/L = 0.5mol/L然后,根据水的离子积(Kw = 10⁻¹⁴)计算出氢离子(H⁺)的浓度:c(H⁺) = Kw / c(OH⁻) = 10⁻¹⁴ / 0.5 mol/L = 2 × 10⁻¹⁴ mol/L最后,根据pH的定义计算出溶液的pH值:pH = -lg(c(H⁺)) = -lg(2 × 10⁻¹⁴) ≈ 13.7六、实验题6. 设计一个实验方案,用于检验某溶液中是否含有Cl⁻离子。
答案:实验步骤:1. 取一定量的待测溶液放入试管中。
2. 向溶液中加入过量的硝酸钡溶液,过滤掉沉淀。
3. 向滤液中加入硝酸银溶液。
4. 观察是否生成白色沉淀。
实验现象及结论:若生成白色沉淀,说明原溶液中含有Cl⁻离子;若没有生成白色沉淀,说明原溶液中不含Cl⁻离子。
实验原理:氯离子(Cl⁻)与银离子(Ag⁺)反应生成不溶于稀硝酸的白色沉淀——氯化银(AgCl)。
中国化学会第届全国高中学生化学竞赛试题及答案

中国化学会第25届全国高中学生化学竞赛1.008Zr Nb Mo Tc Ru Rh Pd Ag CdIn Sn Sb Te I Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Ac-Lr HLi BeB C N O F Na MgAl Si P Cl S K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Rb Cs Fr Sr BaRaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar KrXe Rn 相对原子质量Rf Db Sg Bh Hs Mt评分通则:1.凡要求计算的,没有计算过程,即使结果正确也不得分。
2.有效数字错误,扣0.5分,但每大题只扣1次。
3.单位不写或表达错误,扣0.5分,但每大题只扣1次。
4.只要求1个答案、而给出多个答案,其中有错误的,不得分。
5.方程式不配平不得分。
6.不包括在此标准答案的0.5分的题,可由评分组讨论决定是否给分。
第1题(15分)1-1 2011年是国际化学年,是居里夫人获得诺贝尔化学奖100周年。
高中化学竞赛试题(有机化学)

高中化学竞赛试题(有机化学)高中化学竞赛试卷(有机化学)高二化学(实验班)第ⅰ卷(60分)一、多项选择题(每个问题只有一个选项,每个问题得2分)1。
以下化合物具有顺式和反式异构体a.1-丁烯b、 2-丁烯c.1,1-二氯-1-丙烯d、 2-甲基-1-丙烯2.(ch3)2chch2cl与(ch3)3ccl是什么异构体(a)碳架异构(b)位置异构(c)官能团异构(d)互变异构3.异戊二烯经臭氧化,在锌存在下水解,可得到哪一种产物?(a)hcho+ohcch2cho(c)hcho+ch3cocho(b) hcho+HOOCH2COOH(d)ch3cocho+co2+h2o4.在naoh水溶液中,(ch3)3cx(i),(ch3)2chx(ii),ch3ch2ch2x(iii),ch2=chx(iv)各卤代烃的反应活性次序为:(a)i>ii>iii>iv(b)i>ii>iv>iii(c)iv>i>ii>iii(d)iii>ii>i>iv5.下列四种离子,碱性最强的是:(a)ho-(b)ch3o-(c)c6h5o-(d)ch3coo-6.下列化合物哪个没有芳香性+a、不列颠哥伦比亚省。
7.沸点升高的顺序是:(a)一,二,三,四(a)c6h5coch3(c) c6h5cch2ch3o++(b)四、三、二、一ch3c6h5cch2ch3(c)i,ii,iv,iii(d)iii,iv,ii,i8.哪些方法不能用于格氏试剂的合成?ohch3ch2mgbr(b)ch3ch2cch3o+c6h5mgbrch3mgi(d)c6h5mgbrch+3cho9.ch3ch2ohch2nh2(1)h(2)br(3)clnh2brhphch2nhch3ch3上述配置的正确名称是:(a)(1)r(2)r(3)s(b)(1)r(2)s(3)s(c)(1)s(2)s(3)s(d)(1)r(2)r(3)R10。
全国高中学生化学竞赛(初赛)试题与答案

全国高中学生化学竞赛(初赛)试题与答案全国高中学生化学竞赛(初赛)试题与答案1.1999年是人造元素丰收年,一年间得到第114、116和118号三个新元素。
按已知的原子结构规律,118号元素应是第周期第族元素,它的单质在常温常压下最可能呈现的状态是(气、液、固选一填入)态。
近日传闻俄国合成了第166号元素,若已知原子结构规律不变,该元素应是第周期第族元素。
(5分)答案】七;零;气;八;VIA(5分,每个填空得1分)2.今年是XXX(Le Chatelier1850-1936)诞生150周年。
请用勒沙特列原理解释如下生活中的常见现象:打开冰镇啤酒瓶把啤酒倒入玻璃杯,杯中立即泛起大量泡沫。
(6分)答案】1)啤酒瓶中二氧化碳气体与啤酒中溶解的二氧化碳达到平衡:CO2(气)CO2(溶液),打开啤酒瓶,二氧化碳气体的压力下降。
根据勒沙特列原理,平衡向放出二氧化碳气体的方向移动,以减弱气体压力下降对平衡的影响。
2)温度是保持平衡的条件,玻璃杯的温度比冰镇啤酒的温度高,根据勒沙特列原理,平衡应向减弱温度升高的方向移动,即应向吸热方向移动,从溶液中放出二氧化碳气体是吸热的,因而,应从溶液中放出二氧化碳气体。
注:压力和温度各3分,不与勒沙特列原理挂钩不给分。
3.1999年合成了一种新化合物,本题用X为代号。
用现代物理方法测得X的相对分子质量为64;X含碳93.8%,含氢6.2%;X分子中有3种化学情况分歧的氢原子和4种化学情况分歧的碳原子;X份子中同时存在C—C、C=C和C≡C三种键,并发觉其C=C键比寻常的C=C短。
1.X的分子式是____(2分)2.请画出X的可能布局。
(4分)答案】1.C5H42.如右右上图注:只有一种可能布局;重键位置必须正确,而键角和平面结构则不必要求。
右上图是用Chemsketch程序制作的立体结构图,图形未画出重键,仅供参考,不是答案。
4.空想的宏观单一晶体呈规则的多面体外形。
多面体的面叫晶面。
高中化学奥林匹克竞赛(有机化学)高二检测题(附答案)
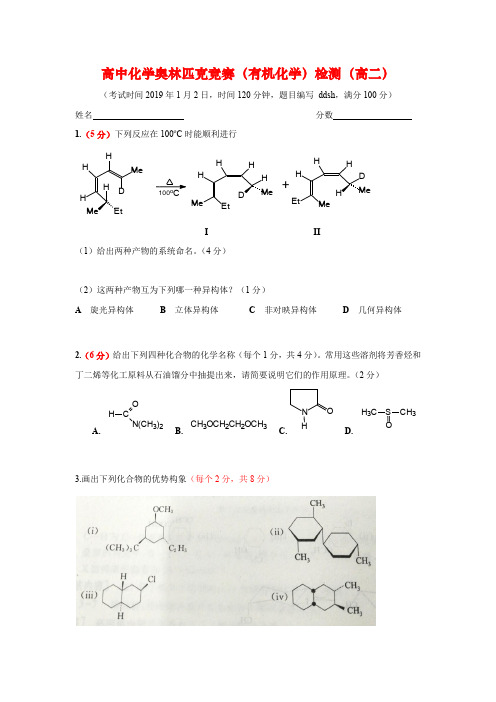
高中化学奥林匹克竞赛(有机化学)检测(高二)(考试时间2019年1月2日,时间120分钟,题目编写 ddsh ,满分100分) 姓名 分数 1.(5分)下列反应在100o C 时能顺利进行I II(1)给出两种产物的系统命名。
(4分)(2)这两种产物互为下列哪一种异构体?(1分)A 旋光异构体B 立体异构体C 非对映异构体D 几何异构体2.(6分)给出下列四种化合物的化学名称(每个1分,共4分)。
常用这些溶剂将芳香烃和丁二烯等化工原料从石油馏分中抽提出来,请简要说明它们的作用原理。
(2分)A. B.C.D.3.画出下列化合物的优势构象(每个2分,共8分)+H CO N(CH 3)2CH 3OCH 2CH 2OCH 3N OHH 3C S OCH 34.判断下列分子是否具有光学活性(共10分)5.下列各组化合物都能够发生分子内的SN2反应。
对各组反应的难易程度进行排序(6分)6.(每式1分,每个命名1分,共9分)2004年是俄国化学家马科尼可夫(V . V . Markovnikov ,1838-1904)逝世100周年。
马科尼可夫因提出C =C 双键的加成规则(Markovnikov Rule )而著称于世。
本题就涉及该规则。
给出下列有机反应序列中的A 、B 、C 、D 、E 、F 和G 的结构式,并给出D 和G 的系统命名。
7.(13分)写出下列反应的每步反应的主产物(A 、B 、C )的结构式;若涉及立体化学,请用Z 、E 、R 、S 等符号具体标明。
(B 是两种几何异构体的混合物)8.(13分)以氯苯为起始原料,用最佳方法合成1-溴-3-氯苯(限用具有高产率的各反应,标明合成的各个步骤)。
CH 2COOH CH 2COOHACH CHO(等摩尔)BHBrC9.(10分)用苯、不超过四个碳的有机化合物和合适的无机试剂为原料合成以下产物:10.(20分)写出下列转化的反应流程高中化学奥林匹克竞赛(有机化学)检测(高二)(答案和评分)(满分100分,时间120分钟)考试时间2019年1月2日 试题编制 dds姓名 分数 1. (5分) 下列反应在100o C 时能顺利进行:I II(1)给出两种产物的系统命名。
2023年化学竞赛有机化学专项训练
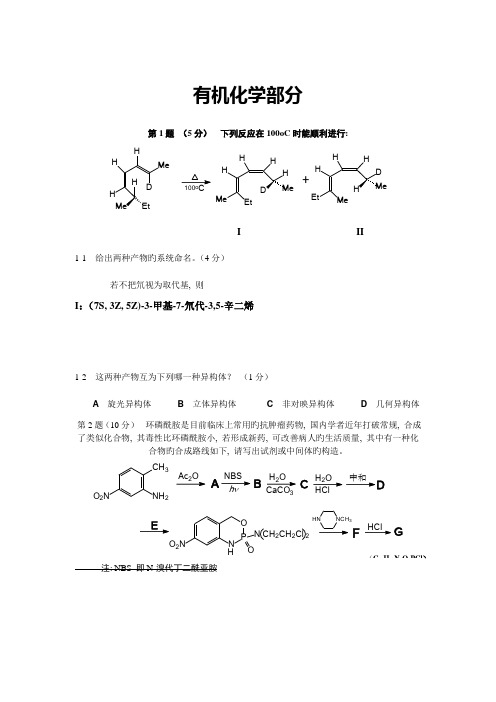
有机化学部分第1题(5分)下列反应在100oC时能顺利进行:+I II1-1 给出两种产物旳系统命名。
(4分)若不把氘视为取代基, 则I:(7S, 3Z, 5Z)-3-甲基-7-氘代-3,5-辛二烯1-2 这两种产物互为下列哪一种异构体?(1分)A旋光异构体B立体异构体C非对映异构体D几何异构体第2题(10分)环磷酰胺是目前临床上常用旳抗肿瘤药物, 国内学者近年打破常规, 合成了类似化合物, 其毒性比环磷酰胺小, 若形成新药, 可改善病人旳生活质量, 其中有一种化合物旳合成路线如下, 请写出试剂或中间体旳构造。
CH3O2N NH22AhB H2O3C H2OHClEO2N NPOON CH2CH2ClHNCH3HNHCl G 注: NBS 即N-溴代丁二酰亚胺第3题 (10分) 以氯苯为起始原料, 用最佳措施合成1-溴-3-氯苯(限用品有高产率旳各反应, 标明合成旳各个环节)。
第4题 (11 分)4-1画出下列转换中A.B.C 和D 旳构造简式(不规定标出手性)。
A (C 14H 26O 4) B (C 12H 22O 2)12H 24O )D (C 12H 22Br 1. Mg/苯1. LiAlH 4 无水醚22. H 2O4-2 画出下列两个转换中产物1.2和3旳构造简式, 并简述在相似条件下反应, 对羟基苯甲醛只好到一种产物, 而间羟基苯甲醛却得到两种产物旳原因。
CHOOHCH 3(CH 2)11Br, K 2CO 3丙酮,回流1CH 3(CH 2)11Br, K 2CO 3丙酮,回流2CHOOH3+原因:第5题 ( 7 分) 灰黄霉素是一种抗真菌药, 可由A 和B 在三级丁醇钾/三级丁醇体系中合成, 反应式如下:(CH 3)3COK/ (CH 3)3COHOOOCH 3H 3COClOO OCH 3H 3COClO HCH 3OH 3COCCCCH +AB灰黄霉素OCHCH 3CH35-1在下面灰黄霉素构造式中标出不对称碳原子旳构型。
全国化学竞赛有机化学部分试题
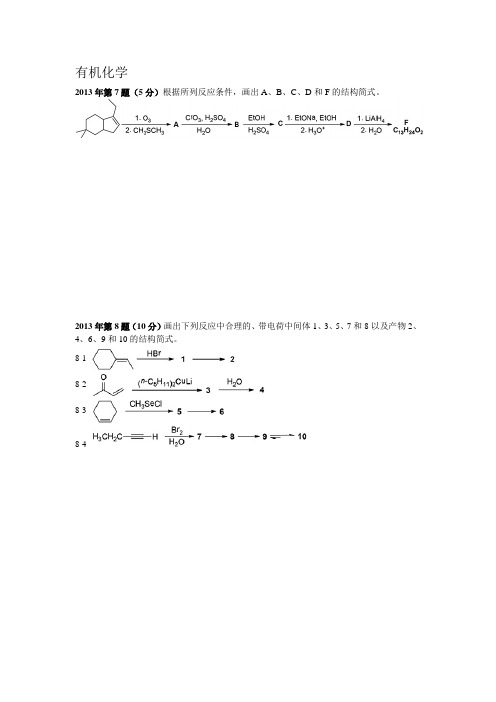
有机化学2013年第7题(5分)根据所列反应条件,画出A、B、C、D和F的结构简式。
2013年第8题(10分)画出下列反应中合理的、带电荷中间体1、3、5、7和8以及产物2、4、6、9和10的结构简式。
8-18-28-38-42013年第9题(12分)9-1 常用同位素标记法研究有机反应历程。
如用18O标记的甲醇钠研究如下反应,发现最终产物不含18O。
根据实验事实画出中间体的结构简式。
9-2 某同学进行如下实验时在碱性条件下得到两个产物D和E,产率分别为74.3%和25.7%。
⑴画出产物D和E的结构简式。
⑵指明此反应所属的具体反应类型。
⑶简述D产率较高的原因。
⑷简述反应体系加入二氧六环的原因。
2012年第9题(12分)Knoevenagel反应是一类有用的缩合反应。
如下图所示,丙二酸二乙酯与苯甲醛在六氢吡啶催化下生成2-苯亚甲基丙二酸二乙酯。
9-1 指出该反应中的亲核试剂。
9-2 简述催化剂六氢吡啶在反应中的具体作用。
9-3 化合物A是合成抗痉挛药物D(gabapentin)的前体。
根据上述反应式,写出合成A的2个起始原料的结构简式。
COOCH2CH3COOCH2CH3A9-4 画出由A制备D过程中中间体B、C和产物D的结构简式。
2012年第10题(6分)辣椒的味道主要来自辣椒素类化合物。
辣椒素F的合成路线如下:画出化合物A、B、C、D、E和F的结构简式。
2012年第11题(12分)11-1 烯烃羟汞化反应的过程与烯烃的溴化相似。
现有如下两个反应:4-戊烯-1-醇在相同条件下反应的主要产物为B。
画出化合物A和B的结构简式。
A OHB O1分3分11-2 下列有机化合物中具有芳香性的是。
化合物A经过如下两步反应后生成化合物D,回答如下问题:11-3 写出化合物B的名称。
11-4 圈出C中来自原料A中的氧原子。
11-5 画出化合物D的结构简式。
2011年第8题(10分)化合物B 是以β-紫罗兰酮为起始原料制备维生素A 的中间体。
全国高中学生化学竞赛(省级赛区)试题与答案(Word版)1

全国奥林匹克化学竞赛(浙江赛区)试题第1题(6分)配平方程式(1)CrCl3+KMnO4+H2O=K2Cr2O7+MnCl2+HCl+MnCr2O7(2)As2S2+HNO3+H2O=H3AsO4+NO↑+H2SO4第2题(12分)(1)实验证明,硫化铜与硫酸铁在细菌作用下,在潮湿多雨的夏季,成为硫酸和硫酸盐而溶解于水,这就是废石堆渗沥水,矿坑水成为重金属酸性废水的主要原因,试写出配平的化学方程式。
(2)从金矿中提取金,传统的也是效率极高的方法是氰化法。
氰化法提金是在氧存在下氰化物盐类可以溶解金。
试写出配平的化学方程式。
(3)对二乙苯在酸性高锰酸钾溶液中被氧化并有气体产生,试写出配平的反应式。
第3题(12分)(1)用石灰乳跟硫熬煮而成的石硫合剂含多硫化钙(CaS n)。
多硫化钙在空气中与二氧化碳等酸性物质接触易析出多硫化氢,多硫化氢是一种极不稳定的黄色液体,试用化学方程式说明多硫化钙具有杀虫作用的原因。
(2)在强碱B-:(如NH4+NH2-),的存在下CH3CH2CH2CH2Cl可按下列两种历程发生消除反应,分别称之为Eα消除和E2消除:Eα:E2:试构思一个实验证实上述历程。
第4题(12分)(1)实验室中所用的氧化钢(CuO)是黑色粉末。
在使用电烙铁时,其头部是一铜制的烙铁头,长期使用,表面被氧化,但脱落下来的氧化膜却是红色的,试说明原因。
(2)法医鉴定砷中毒(通常为砒霜)的方法是用锌、盐酸和试样混在一起,将生成的气体导入热玻璃管,如果试样中有砷化物存在,则在玻璃管的壁上出现亮黑色的“砷镜”。
试写出有关的反应式。
(3)把CO2气体通入澄清的石灰水,立即会产生浑浊,但把SO2气体通入澄清的石灰水,却不容易看那浑浊,而CaCO3和CaSO3都是难溶的电解质,试说明原因。
第5题(6分)分子式为C7H10的开经烃A,可发生下列反应:(1)A经催化加氢可生成3一乙基戊烷。
(2)A与硝酸银氨溶液反应可产生白色沉淀。
化学竞赛有机化学试题(含答案)
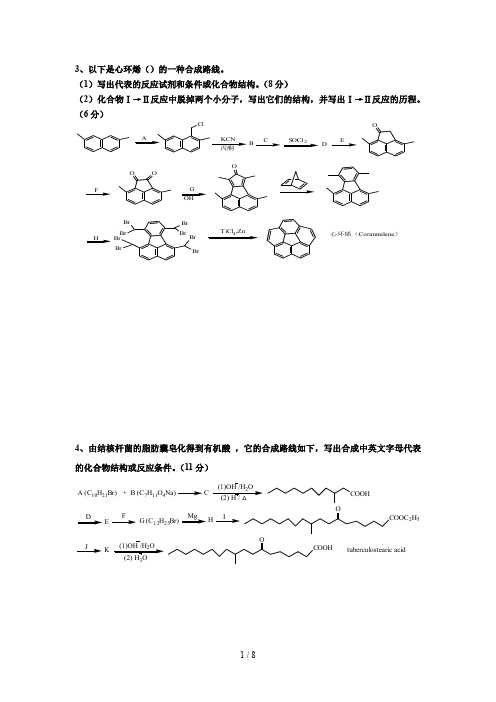
3、以下是心环烯()的一种合成路线。
(1)写出代表的反应试剂和条件或化合物结构。
(8分)(2)化合物Ⅰ→Ⅱ反应中脱掉两个小分子,写出它们的结构,并写出Ⅰ→Ⅱ反应的历程。
(6分)ClKCN 丙酮S OCl 2EOOOG OHOBr BrBrBrBrBr Br BrTiCl 4,Zn心环烯(Corannulene )ABCDFH4、由结核杆菌的脂肪囊皂化得到有机酸 ,它的合成路线如下,写出合成中英文字母代表的化合物结构或反应条件。
(11分)A (C 10H 21Br)+B (C 7H 11O 4Na)C(1)OH /H 2O (2) H / △COOHDE FG (C 12H 25Br)MgHICOOC 2H 5OJK(1)OH /H 2O (2) H 3OCOOHOtuberculostearic acid5、(K)是一种女性荷尔蒙,控制性别差异及影响生理行为。
已报道了多种合成方法,其中之一以(A)、(B)为原料合成,步骤如下(19分):OCH3C CHOOKOH H2 / Pd H+C6H5CHOH+CH3It-C4H9OKO3(CH3CO)2O HBr KBH4(A)(B)(C)(D)AlCl3(G)(H)(J) +(E)HOH3COHC19H24O2C20H26O5C19H24O2(F)(I)(K)5-1. 推断C、D、E、F、G、H、I、J的结构(8分):5-2. 写出在存在下(A)与(B)反应生成(C)的机理;如果将(A)中的间位取代基3调换到对位,(A)与(B)反应速率是增大还是减小?为什么?(5分)5-3. (E)转化为(F)的反应中,理论上3起什么作用?实际上,至少需要3多少量?请给出合理的解释。
(4分)5-4.(J)有多少种立体异构体?(2分)6、由甲苯、苯及必要的原料和试剂制备间苯甲酰基甲苯,再由间苯甲酰基甲苯合成消炎镇痛药酮基布洛芬()。
(10分)OCOOH CH 37、以下是维生素A 合成的一种重要方法:O +HC CHNH 2/NH 3(l)(1)(2)HAZn-CuOHBBrC O(1)EtO C C MgBr (2)HDH 2/Pd-BaS O 4OHOEtECHOCH 3COCH 3FH 2S O 4G(1)CH 3CH 2COOEt/EtONa (2)HH(2)H(1)BrMgCC C CH H 3CCH 2OMgBrIH 2/Pd-BaS O 4J(1) Ac 2O (2)I 2/PhH (3)H 3OKBa(OH)2(1)写出上述反应中英文字母所代表的中间产物及反应试剂的结构式。
全国高中化学竞赛(初赛)试题与答案

全国高中化学竞赛(初赛)试题与答案
1.写出制备金属硫化物的方法,包括铜、铁等金属和硫反
应的方法。
2.写出制备二氧化硫的方法,包括铜、锌等金属和浓硫酸
反应的方法。
3.介绍磁性材料FeO3的制备方法和反应方程式,以及在
醋酸溶液中K4Fe(CN)6和NaNO2反应得到纯NO的反应式,
以及在酸性溶液中NaNO2和KI反应得到纯NO的应式。
实验结果表明先加NaNO2再加KI制得的NO更纯。
4.硫和石灰乳反应得到五硫化钙(CaS5)和硫代硫酸钙(CaS2O3)。
5.描述了一个实验装置,通过加热硫和O2的反应来得出
结论。
如果内盛空气或N2O,则U形管两侧液汞面不持平。
6.介绍了Fe(Ⅲ)和I在溶液中的反应现象和反应方程式,以及有足量F时Fe(Ⅲ)不和I反应的原因,以及往该溶液
中加足量F的现象和原因。
在足量2mol/dm3HCl溶液中加Fe (Ⅲ)、I、F会产生不同于实验2的反应现象。
7.写出了硫铁矿被氧化的反应方程式,讨论了水淋洗硫铁矿的趋势和反应中被氧化的物质,以及硫铁矿水的酸碱性。
如果反应③中途停止,则FeS仍会继续被氧化。
全国高中化学竞赛教练员习题答案有机化学

第二部分有机化学一、系统命名1.(1) 2,2,4,4 四甲基戊烷(3) 2,3,5,5 四甲基庚烷⑸2,6,8 三甲基 5 异丁基癸烷2.(1) 1,1 二甲基3 异丙基环戊烷⑶1 甲基 3 环丁基环戊烷(5) 二环[2,2,1]庚烷(7) 二环[3,3,1]庚烷(9) 3,6 二甲基二环[3,2,0]庚烷3.(1) (1R,3R) 1 甲基3 异丙基环己烷⑶(1R,2R,4R) 1,2 二甲基 4 氯环己烷⑸(1S,2R,4S) 1,2,4-三甲基环己烷4.(1) 2 甲基2 氯丁烷⑶(2R) 1,1 二甲基 2 氯甲基环戊烷⑸3 氯甲基 2 溴己烷⑺(1R,2S,3S) 1 甲基 3 氟 2 氯环己烷5.(1) 7 甲基 3 仲丁基4 氯1,5辛二烯⑶3 乙烯基1,5 庚二烯(5) 3,5 二甲基4 异丙基1,3 己二烯(7) (E) 2,3 二甲基 1 溴 2 戊烯(9) (E,S) 4 甲基 2 己烯(11) (E,R) 2,7 二甲基5 溴4 壬烯6.(1) (E) 3 戊烯1 炔⑶5 氯 2 戊炔(5) (1R,2S) 1 甲基 2 乙炔基环丙烷⑺5 炔丙基1,3 环己二烯7. (1) 1 甲基1,4 环己二烯(3) (E) 3 亚乙基环己烯⑸(Z) 4 亚乙基环己烯⑵2,5,6 三甲基辛烷⑷3 甲基 4 乙基己烷⑵2 甲基 3 环丙基庚烷⑷螺[3,4]辛烷(6) 二环[4,2,0]辛烷(8) 4 -甲基螺[2,4]庚烷(10) 1,3,8 三甲基二环[4,4,0]癸烷⑵(5S) 5 氯螺[2,5]辛烷⑷顺 1 甲基4(R 仲丁基)环己烷⑵2 甲基 3 氯丁烷⑷2 -乙基-4-氯-1 -丁烯⑹反 1 溴 4 碘环己烷(8) (2S,3S,4R) 2,3,4 三氯己烷⑵2,3,4 三甲基 2 戊烯⑷1 甲基 5 乙基1,3 环己二烯⑹3 亚甲基环戊烯(8) 1 烯丙基2 丙烯基1,3 环己烯(10) (3S,4R) 4 甲基3 氯环戊烯⑵(S) 3 甲基 1 戊烯 4 炔⑷(1R,2S) 1 甲基 2 丙炔基环己烷⑹(Z) 5 庚烯1,3 二炔(8)顺1,2 二甲基反3 乙炔基环丙烷⑵2 甲基1,3 环己二烯⑷(2E,4Z) 2,4 庚二烯⑹1,5 乙二烯 3 炔9.(1) 4,4二甲基--溴唱我醇 ⑷1 -环戊烯基甲醇⑺4,4二甲基乞-环己烯-1诵 (9) 反Z-乙基--环己醇 10.(I) 甲基-3 -氯乙基醚 ⑶4 -肖基苯乙醚 (5) 1,3二乙氧基苯 (7) 2,4二氯43'硝基二苯醚(9) 1,2部氧丁烷(II) (5S,2S) -5 -乙基—-氯氧杂环庚烷 (13)苯并-5-冠- 11.(1) (E) - -丁烯醛(反巴豆醛)⑶1,4我二烯唱-酮(二乙烯基酮)⑸3 -甲基--丁酮(甲基异丙基酮) (7) 1,3二苯基丙酮(二苄基酮) 12.(1) 3 -羟基丁酮 (2) 5谟己醛⑷(E) ~4 -甲基-5 -苯基~4 -己烯-3晒酮 ⑹(Z) 43 -己烯二醛13.(2) 丙基环己基醚 (4) 乙烯基苄基醚⑹5 -甲氧基—我醇(8) 乙二醇二甲醚或1,2二甲氧基乙烷(10) 顺23部氧丁烷(12) 2 -甲基-,3 ■环氧戊烷 (14) 18 冠 -6⑵(E) -3译基丙烯醛(反肉桂醛) ⑷5 -己烯-3 -酮(乙基烯丙基酮) ⑹1,1匸氯丙酮(a a-二氯丙酮)(1) 2 -丁烯酸(2) 2,2 -二甲基丙酸 (3) 4 -溴丁酸 ⑷3 -氧代戊酸(5) 4 -羟基--氟丁酸 (6) 4 -2 -萘基)丁酸 ⑺2羌基唱-氧代戊酸(8) 4 -乙酰基苯甲酸(9) 3 -苯基丙酸 (10) (E) -3-庚烯酸 (11) 3 -乙烯基-4 -己炔酸 (12) 3 -甲酰基苯甲酸 (13) 2 -羟基T ,2,3-丙三酸 (14) 1,3译二甲酸 (15) (9Z, 12Z, 15Z) -9,12,15 -十八三烯酸(16) 4 -甲基-5我内酯-、烷、烯、炔1.2 -甲基丁烷为 CH 3CHCH 2CH 3 分子中有9种不同化学环境的氢,所以其中一氯CH s代物共有四种,分别为(9) (2Z, 4R) 4 甲基2 庚烯 (2) 2,45 炔 O. (1) 4 叔丁基乙苯 二氯甲苯 (3) 3 溴苯乙烯 ⑷3环己基甲苯(5) 4溴苄基氯(6) 2氯 2,苯甲烷(9) 1 基)苯氯 2 ⑺4甲氧基苯甲醛(8)二 (10) (E) 3,4 二(4羟基苯基)3 己烯炔环己烯基)乙炔 溴联苯 (2 氯丙(8)二(1⑺1,3 庚二烯 6⑵3 -丁烯-2 醇⑸3 -环己烯--享(8) (2R,3S) E -甲基-3 -氯-诵 ⑶4 -苯基--丁醇 ⑹(1S,2S)--甲基 -部戊醇 ⑶(E)--甲基-4-己烯--炔-3诩酮 ⑸5 -甲基-3 -氧代--己醇 ⑺2 -环己烯-诩酮CICH 2CHCH 2CH 3ICH 3⑻2 -甲基——氯丁烷 CH 3CH fH CH 3H 3C Cl(c) 2 -甲基~3 —氯丁烷CH 3CCH 2CH 3ICH 3(b) 2 -甲基_2 —氯丁烷CH 3CHCH 2CH 2CIICH 3(d) 3 -甲基——氯丁烷相对比为 a:b:c:d = (6 Xl):(1 5):(3.8 2):(3 K ) = 6:5:763 2. 丙烷中具有两种不同化学环境的氢,一溴化后分别得到(a) 1 -溴丙烷 CH 3CH 2CH 2BrCH 3CH CH 3(b) 2 -溴丙烷 丨Br相对百分比 a:b = (6 XI) : (2 8为 =6:164 = 3:82 百分比为 a: 3/(82+3) = 3.5% ; b: 82/85 = 96.5% 选择性溴化比氯化要高。
历年化学竞赛之有机化学试题汇总及答案

历年化学竞赛之有机化学试题汇总及答案简介本文档为历年化学竞赛中有机化学试题的汇总及答案,旨在帮助学生系统地复和准备有机化学方面的竞赛。
试题汇总以下是历年化学竞赛中的有机化学试题的汇总:1. 2015年试题- 选择题:题目1、题目2、题目3- 解答题:题目42. 2016年试题- 选择题:题目1、题目2、题目3- 解答题:题目4、题目53. 2017年试题- 选择题:题目1、题目2、题目3- 解答题:题目4、题目5、题目64. 2018年试题- 选择题:题目1、题目2、题目3- 解答题:题目4、题目5、题目6、题目75. 2019年试题- 选择题:题目1、题目2、题目3- 解答题:题目4、题目5、题目6、题目7、题目8请注意,此处只是试题的汇总,具体题目内容需要参考相应年份的试卷。
答案以下是上述试题的部分答案(仅供参考):2015年试题答案- 题目1:答案A- 题目2:答案B- 题目3:答案C- 题目4:答案D2016年试题答案- 题目1:答案A - 题目2:答案B - 题目3:答案C - 题目4:答案D - 题目5:答案E2017年试题答案- 题目1:答案A - 题目2:答案B - 题目3:答案C - 题目4:答案D - 题目5:答案E - 题目6:答案F2018年试题答案- 题目1:答案A - 题目2:答案B - 题目3:答案C- 题目4:答案D- 题目5:答案E- 题目6:答案F- 题目7:答案G2019年试题答案- 题目1:答案A- 题目2:答案B- 题目3:答案C- 题目4:答案D- 题目5:答案E- 题目6:答案F- 题目7:答案G- 题目8:答案H请注意,答案仅供参考,具体答案还需参考相应年份试卷和标准答案。
结论本文档提供了历年化学竞赛有机化学试题的汇总及部分答案,希望对学生的复习和准备有所帮助。
为了获得具体且准确的试题内容和答案,请参考相应年份的试卷和标准答案。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化学阶梯练习有机化学阶梯练习参考答案参考答案
河北省石家庄市第二中学 刘浩源 葛洪鑫 屈沛
吉林省东北师范大学附属中学 于涵
第一题
1-1-1 (3分)
1-1-2 (3分)
1-1-3 (共5分,计算过程2分,结果1分,结构式2分)其钠盐的分子量为190.13,其中钠的质量百分数为22.99/190.13×100%=12.09%,比题中所给数据大,钠的个数必为整数个,所以该钠盐中必含有结晶水。
设含n 个结晶水,22.99/(190.13+18.02n)×100%=11.05%,解得n=1,化学式为C 8H 7O 4Na ·H 2O 阴离子结构式如下:
1-2-1 (2分) 1-2-2 (4分,用结构式写出答案) 用ZE 简单表示可写为2Z4Z ,2Z4E ,2E4Z ,2E4E 。
1-2-3 (2分) 因为山梨酸的溶解度比其钾盐的溶解度小,用钾盐可达所需量且不影响食品的口味。
1-3-1 (1分) 3个。
1-3-2 (2分)
1-3-3 (2分) 天冬氨酸和苯丙氨酸。
1-4-1 (2分) 3-叔丁基-4甲氧基苯酚
O O O
O
O
O O O O
O O O H
H 3C C H
CH CH CH COOH
H 3N CH C CH 2O C OH
O
H
N CH C CH 2O O
1-4-2 (6分,其它合理路线亦可)
1-4-3 (2分)络合可以催化氧化反应的金属离子,使之催化性能失效,减缓氧化。
第二题 2-1 (10分
)
2-2 (6分
)
茉莉酮:
ONa OH
2
2
OCH 33
OCH 3
NHCOCH 3C(CH 3)3
OCH 32C(CH 3)3OCH 3C(CH 3)3
NaOH ,熔融稀3(CH 3CO
)2O
HCl ,水解22
第四题
下列图示即可回答前两个问题(7+2=9分),构型发生反转是因为S N2反应(2分)。
图中,11即为副产物。
第六题6-1-1(8分)
6-1-3 (3分)
6-2-1(5分)
6-2-3(4
分)
6-2-4 (1分)异裂后形成更长的共轭体系,电子跃迁能量降低,吸收可见光即可,故显色。
6-2-5 (1分)CH 3O — 在氨基的邻对位
第七题
7-1-1(6分)
3H 3CH 3
C
3
3
+
H 33
C
H 3C
3C
H 3N H
+
O
-O
3
-H O ∆
H 33
N H
CH 3
C
CH 3
O
HCCl 3
+
OH
-
CCl
2
+
H 2O
+Cl -
H 2
H N
H OH
-H O
N
H
CHO
2
H
N
Cl
7-1-3(2分)吲哚甲醛;当吲哚进入β-CD (环糊精)后,卡宾只能从一侧进攻,之后的氢
氧根也只能从该侧进攻,不能有效进攻N 上的H ,故只能按生成醛基方式进攻 7-1-4(3分)
H CH
H 3
3
C
-
N
H H 3
3
N
H C
H 33
O
NHCH 3
7-2-1(13分)
B
OHC
3
O C
H 2D
CH 2
OH CHO
3
E
CH 2
OH CH 2OH
3
F
CH 2
OH
CH 2OAc
3
H
CHO OH
CH 2OAc
3
I CH 2O J
COOH OH
CH 2OAc
3
K
COOH OH
CH 2OH
3
N
O
O
OCH 3
OCH 3OH
H 3CO
A
CH 2
Br /NaOH
C
∆G O 3;Zn/H 2O M
OHC
OCH 3OCH 3
7-2-2(3分)
3
3
O H
+
CHO
OCH 3
OCH 3
O -
3
OCH
3
H +
O
CHO
3
OCH 3
O H OCH 3
OCH
3
B
.
7-2-3(6分)
H
3
3 B Br
Br
G H2O2/OH
-
I CH3
C
H3
O
,干HCl
K
33。
