大学化学课件与习题答案、模拟题第五章剖析
最新大学有机化学课后习题答案 第5章教学讲义PPT课件

(4)
AlCl3 + (CH3)2CHCH2Cl
C(CH3)3
(5) O2N
(6)
NO2
H2SO4 HNO3
NO2
OH Cl2 Fe
Cl
OH
Cl
(7) CH3 CH3
CH3 K2CrO4 CH3 210-285 oC
HO2C HO2C
CO2H CO2H
5. 写出下列反应中反应物的构造式
(1) C8H10 KMnO4
第五章 个人独资和合伙企业法律制度
一、个人独资企业法律制度
二、合伙企业法律制度
一、个人独资企业法律制度
个人独资企业的概念和特征 个人独资企业的设立 个人独资企业的权利义务 个人独资企业的事务管理 个人投资企业的解散和清算
个人独资企业的概念
个人独资企业,简称独资企业,是指由一个 自然人投资,全部资产为投资者个人所有的 营利性经济组织。
CH3
CH2CH3
14.完成下列反应,实验结果说明什么
问题?
NO2
NO2
O
HNO3 H2SO4
[O]
O
O [H]
NO2
O
[O] O
O
15.按照休克尔规则,判断下列化合物是否有芳香性
(1)
(2)
(3)
+ Cl-
-
(4)
(5)
(6) CH2 CH CH CH CH CH2
化合物(3)、(5)有芳香性
CH3 (8)
(6)
Cl NHCOCH3
(7)
NO2
+ N(CH3)3
CH3 (8)
Cl
(9)
CH2
NO2
完整版高考化学一轮复习第五章 化工生产中的重要非金属元素 (讲义及答案)及答案

完整版高考化学一轮复习第五章 化工生产中的重要非金属元素 (讲义及答案)及答案一、选择题1.无机物X 、Y 、Z 、M 的相互转化关系如图所示(部分反应条件、部分反应中的H 、O 已略去)。
X 、Y 、Z 均含有同一种元素。
下列说法正确的是A .若X 是氢氧化钠,则M 不一定为CO 2B .若Y 具有两性,则M 的溶液只可能显碱性C .若Z 是导致酸雨的主要气体,则X 一定是H 2SD .若M 是用途最广的金属,加热蒸干Y 的溶液一定能得到Y 【答案】A 【解析】 【详解】A 、若X 是氢氧化钠,则M 不一定为CO 2,M 为能形成多元酸的酸性氧化物,如:SO 2,故A 正确;B . 若Y 具有两性,则M 的溶液可能显碱性,也可能显酸性,故B 错误;C . 若Z 是导致酸雨的主要气体,则X 也可以是Na 2SO 3,Y 为NaHSO 3,Z 为SO 2,M 为HCl ,故C 错误;D . 若M 是用途最广的金属,Y 为亚铁盐,因为亚铁离子水解,所以加热蒸干Y 的溶液不能得到Y ,故D 错误; 故答案选A 。
2.下列离子方程式书写正确的是A .向明矾溶液中逐滴加入足量Ba(OH)2溶液时,反应为:Al 3++ 2SO 2-4+ 2Ba 2++ 4OH -= 2BaSO 4↓+ AlO -2+ 2H 2OB .硫化亚铁与浓硫酸混合:2H ++FeS=H 2S↑+Fe 2+C .向次氯酸钙溶液中通入SO 2:Ca 2++2ClO -+SO 2+H 2O=CaSO 3↓+2HClOD .磁性氧化铁溶于稀硝酸:3Fe 2++4H ++NO -3=3Fe 3++NO↑+3H 2O 【答案】A 【详解】A .Ba(OH)2足量,故明矾KAl(SO 4)2·12H 2O 完全反应,其中Al 3+与OH -反应生成-2AlO ,即①3+--22Al +4OH = AlO +2H O ,2-4SO 与Ba 2+反应,②2-2+44SO +Ba = BaSO ↓,由于Al 3+、2-4SO 都来源于明矾,故应满足原比例1:2,则总反应为①+②×2,即3+2-2+--4422Al +2SO +2Ba +4OH = 2BaSO +AlO +2H O ↓,A 正确; B .浓硫酸具有强氧化性,可以将FeS 中亚铁氧化为Fe 3+,-2价硫氧化为S 单质,自身被还原为SO2,B错误;SO,自身被还原为Cl-,C错误;C.次氯酸根有强氧化性,能将SO2氧化为2-4D.磁性氧化铁为Fe3O4,书写离子方程式时,Fe3O4不能拆,D错误;故答案选A。
化学人教版选修5学案:第五章 微型专题重点突破(七) Word版含解析

微型专题重点突破(七)[核心素养发展目标] 1. 宏观辨识与微观探析:能根据单体的官能团差异理解加聚反应和缩聚反应的原理,理解单体与聚合物之间的关系,并能根据高分子化合物的结构特点及官能团推测它们的性能。
2.科学态度与社会责任:了解高分子材料的性能和用途,了解高分子材料对环境造成的不良影响。
一、高分子合成材料的组成、结构与性能例1聚乳酸(PLA)是以乳酸为原料生产的新型聚酯材料。
某公司以玉米为原料发酵生产聚乳酸,利用聚乳酸制成生物降解性发泡材料。
该材料的强度、压缩应力、缓冲力等与聚苯乙烯塑料相同,经焚烧后不污染环境,还可肥田。
下列说法不正确的是()A.聚乳酸使用后能被自然界中微生物降解B.聚乳酸适用于吹塑、热塑等各种加工方法,应用十分广泛C.聚乳酸是一种友好的天然高分子聚酯材料D.聚乳酸是以淀粉发酵的乳酸为原料制备的聚酯材料答案 C解析聚乳酸使用后能被自然界中微生物降解,最终生成CO2和H2O;该分子为线型结构,适用于吹塑、热塑等各种加工方法;聚乳酸是以乳酸为原料制备的聚酯材料,不是天然高分子。
常见的合成高分子材料都是由单体通过加聚反应或缩聚反应生成,做题时要结合单体或高聚物的结构或性质进行相互推导,从而确定答案。
变式1关于下列三种常见高分子材料的说法正确的是()酚醛树脂涤纶顺丁橡胶A.顺丁橡胶、涤纶和酚醛树脂都属于天然高分子材料B.顺丁橡胶的单体与反-2-丁烯互为同分异构体C.合成涤纶的单体均可发生酯化反应D.酚醛树脂是通过加聚反应合成的答案 C解析顺丁橡胶、涤纶和酚醛树脂都属于合成高分子材料,A项错误;顺丁橡胶的单体是1,3-丁二烯,与反-2-丁烯的分子式不同,B项错误;合成涤纶的单体是对苯二甲酸和乙二醇,这两种单体均能发生酯化反应,C项正确;酚醛树脂是由苯酚和甲醛缩聚而成的,D项错误。
二、由高分子化合物的结构判断其单体例2高分子化合物A和B的部分结构如下:(1)合成高分子化合物A的单体是__________________,生成A的反应是________反应。
19高考化学大一轮复习课件第五单元总结(共73张PPT)[可修改版ppt]
![19高考化学大一轮复习课件第五单元总结(共73张PPT)[可修改版ppt]](https://img.taocdn.com/s3/m/392192939e314332396893b3.png)
2.下列关于原子结构、元素性质的说法正确的是( )。 A.随着原子序数的递增,元素原子的核外电子数逐渐增多,
原子半径逐渐减小 B.若两种不同的核素具有相同的中子数,则二者一定不属于
同种元素 C.若两种元素原子的最外层电子数相同,则元素最高正价一
定相同 D.电子层结构相同的微粒,其化学性质一定相似
X
…… N(1)
Y M …… N(2)
…… N(3)
则 N 可能和 Y、M 不在同一周期,也可能和 Y、M 在同一周期。
案例示范 2 A、B、C、D、E、F 是原子序数依次增大的短
周期主族元素。A、E 在元素周期表中的相对位置如图所示,A 与
氧元素能形成两种无色气体,C 是地壳中含量最多的元素,D 是地
解析 HF 分子之间容易形成氢键,故 HF 的沸点高于 HCl,A 项错误;Si 在元素周期表中的位置处于 Al 与 P 之间,具有半导体 的性质,B 项正确;NH5 的组成特点为 NH4H,该物质为离子化合物,N 为-3 价,C 项错误;Cl-、S2-、Ca2+、K+四种离子的核外电子排布相 同,核电荷数越大,离子半径越小,即离子半径:S2->Cl->K+>Ca2+,D 项错误。
答案 C
巩固训练 1 四种短周期主族元素在周期表中 的位置如图所示,其中只有 M 为金属元素。下列说 法不.正.确.的是( )。
A.原子半径:Z<M B.Y 的最高价氧化物对应水化物的酸性比 X 的弱 C.X 的最简单气态氢化物的热稳定性比 Z 的弱 D.Z 位于元素周期表中第二周期ⅥA 族
解析 根据元素周期表中短周期部分结构和元素位置可 知,M 为 Al,X 为 Si,Y 为 N,Z 为 O。原子半径 Al>S>O,A 项正确;非 金属性 N>Si,故最高价氧化物对应水化物的酸性 HNO3>H2SiO3,B 项 错误;非金属性 O>Si,故气态氢化物的稳定性 H2O>SiH4,C 项正确;O 原子含有 2 个电子层,最外层含有 6 个电子,因此 O 元素位于元素 周期表中第二周期ⅥA 族,D 项正确。
普通化学第五版浙江大学课后习题答案免费

大众化学第五版第一章习题谜底1.谜底〔1-〕〔2-〕〔3+〕〔4-〕2.谜底〔1c 〕〔2d 〕〔3a 〕〔4d 〕〔5abd 〕〔6ad 〕〔7d 〕〔8d 〕3.谜底〔1〕熄灭前后零碎的温度〔2〕水的品质跟比热〔3〕弹式量热计热容4..谜底:依照曾经明白前提列式K C g K g J g molg mol J b )35.29659.298](120918.4[5.0122100032261111-+⨯⋅⋅-=⨯⋅⋅⨯-----C b =849J.mol -15.谜底:取得的肌肉运动的能量=kJ mol kJ mol g g8.17%3028201808.311=⨯⋅⨯⋅--6.谜底:计划一个轮回3×)(2)(32s Fe s O Fe →×3→)(243s O Fe )(3s FeO ×2〔-58.6〕+2(38.1)+6p q =3(-27.6)17.166)1.38(2)6.58()6.27(3-⋅-=----=mol kJ q p7.谜底:由曾经明白可知ΔH=39.2kJ.mol -1ΔH=ΔU+Δ〔PV 〕=ΔU+P ΔVw ‘=-P ΔV=-1×R ×T=-8.314×351J=-2.9kJ ΔU=ΔH-P ΔV=39.2-2.9=36.3kJ8.以下以应〔或进程〕的q p 与q v 有区不吗?复杂阐明。
〔1〕2.00molNH 4HS 的剖析NH 4HS(s)NH 3(g)+H 2S(g)〔2〕天生1.00mol 的HClH 2(g)+Cl 2(g)2HCl(g) 〔3〕5.00molCO 2(s)〔干冰〕的升华CO 2(s)CO 2(g) 〔4〕积淀出2.00molAgCl(s)AgNO 3(aq)+NaCl(aq)AgCl(s)+NaNO 3(aq)9.谜底:ΔU-ΔH=-Δ〔PV 〕=-Δn g RT(Δn g 为反响发作变更时气体物资的量的变更) (1)ΔU-ΔH=-2×(2-0)×8.314×298.15/1000=-9.9kJ(2)ΔU-ΔH=-2×(2-2)×R ×T=0(3)ΔU-ΔH=-5×(1-0)×8.314×(273.15-78)/1000=-8.11kJ (4)ΔU-ΔH=-2×(0-0)×R ×T=010.〔1〕4NH 3(g)+3O 2(g)=2N 2(g)+6H 2O(l)谜底-1530.5kJ.mol -1〔2〕C 2H 2(g)+H 2(g)=C 2H 4(g)谜底-174.47kJ.mol -1〔3〕NH 3(g)+稀盐酸谜底-86.32kJ.mol -1写出离子反响式。
2021年化学人教版选修5课件 第5章(付,169)

(4)烯烃和二烯烃的聚合反应
例如,乙烯与 1,3-丁二烯的加聚反应就属于此反应类型。 一定条件
nCH2===CH2+nCH2===CH—CH===CH2 ――→ CH2—CH2—CH2—CH===CH—CH2
(5)炔烃单体的加聚反应 例如,乙炔的加聚反应就属于此反应类型。
第五章
进入合成有机高分子化合物的时代
第一节 合成高分子化合物的基本方法
01课前自主学习 03随堂基础巩固
02课堂互动探究 课时作业
一、有机高分子化合物 1.与低分子有机物的区别:
2.有关概念:
(1)聚合物:由单体进行聚合反应形成的高分子化合物。 (2) 单 体 : 能 够 进 行 聚 合 反 应 形 成 高 分 子 化 合 物 的 低分子化合物 。
催化剂 nHOOC—COOH+nHOCH2—CH2OH
(3)缩聚物的表示方法:聚乙二酸乙二酯的结构简式为
, 缩聚物结构式要在方括号外侧写出链节余下的 或 端基原子或原子团 。
探究点一 加聚反应和缩聚反应
一、加聚反应和缩聚反应的比较
类别
加聚反应
缩聚反应
单体 特征
单体 种类
含不饱和键
至少含两个官能团(如—OH、
解析:可以发生加聚反应的单体含有碳碳双键等不饱和键, 符合题意的有 b、d,其加聚产物分别为
含碳碳双键或碳碳 三键的有机物
、—NH2) 酚、醛、醇、羧酸、氨基酸
类别
加聚反应
缩聚反应
聚合 通过不饱和键加成 通过缩合脱去小分子而连接
方式
聚合物 高聚物与单体具有 高聚物和单体具有不同的化学
特征 相同的化学组成 组成
大学化学课后习题答案

第1章化学反应基本规律1.2 习题及详解一.判断题1. 状态函数都具有加和性.. ×2. 系统的状态发生改变时;至少有一个状态函数发生了改变 .. √3. 由于CaCO3固体的分解反应是吸热的;故CaCO3的标准摩尔生成焓是负值 .. ×4. 利用盖斯定律计算反应热效应时;其热效应与过程无关;这表明任何情况下;化学反应的热效应只与反应的起;始状态有关;而与反应途径无关.. ×5.因为物质的绝对熵随温度的升高而增大;故温度升高可使各种化学反应的ΔS大大增加 ..×6. ΔH; ΔS受温度影响很小;所以ΔG受温度的影响不大 .. ×7. 凡ΔGθ大于零的过程都不能自发进行.. ×8. 273K;101.325KPa下;水凝结为冰;其过程的ΔS<0; ΔG=0 .. √9.反应Fe3O4s+4H2g → 3Fes+4 H2Og的平衡常数表达式为2244(/)(/)H OTHp pKp pθθθ=..√10.反应2NO+O2→2NO2的速率方程式是:)()(22OcNOkcv⋅=;该反应一定是基元反应..×二.选择题1. 某气体系统经途径1和2膨胀到相同的终态;两个变化过程所作的体积功相等且无非体积功;则两过程 BA.因变化过程的温度未知;依吉布斯公式无法判断ΔG是否相等B.ΔH相等C.系统与环境间的热交换不相等D.以上选项均正确2. 已知CuCl2s+Cus→2CuCls Δr H mΘ1 =170KJ•mol-1Cus+Cl2g → CuCl2s Δr H mΘ2 =-206KJ•mol-1则Δf H mΘCuCl;s应为D KJ.mol-1A.36B. -36C.18D.-183. 下列方程式中;能正确表示AgBrs的Δf H mΘ的是BA.Ags+1/2Br2g→ AgBrsB.Ags+1/2Br2l→A gBrsC.2Ags+Br2l→ 2AgBrsD.Ag+aq+Br-aq→ AgBrs4. 298K下;对参考态元素的下列叙述中;正确的是 CA.Δf H mΘ≠0;Δf G mΘ=0;S mΘ=0B.Δf H mΘ≠0;Δf G mΘ≠0;S mΘ≠0C.Δf H mΘ=0;Δf G mΘ=0;S mΘ≠0D.Δf H mΘ=0;Δf G mΘ=0;S mΘ=05. 某反应在高温时能自发进行;低温时不能自发进行;则其 BA.ΔH>0; ΔS<0 ;B. ΔH>0; ΔS>0C.ΔH<0; ΔS<0 ;D.ΔH<0; ΔS>06.1mol气态化合物AB和1mol气态化合物CD按下式反应:ABg+CDg→ADg+BCg;平衡时;每一种反应物AB 和CD都有3/4mol转化为AD和BC;但是体积没有变化;则反应平衡常数为BA.16B.9C.1/9D.16/97. 400℃时;反应3H2g+N2g→2NH3g的K673Θ=1.66×10-4..同温同压下;3/2H2g+1/2N2g→NH3g 的Δr G mΘ为D KJ.mol-1..A.-10.57 B.10.57 C.-24.35 D.24.358. 已知下列反应的标准Gibbs函数和标准平衡常数:1Cs+O2g → CO2g ΔG1Θ;K1Θ2CO2g → COg+1/2O2g ΔG2Θ;K2Θ3Cs+1/2O2g → COg ΔG3Θ;K3Θ则它的ΔGΘ;KΘ之间的关系分别是AA.ΔG3Θ=ΔG1Θ+ΔG2ΘB.ΔG3Θ=ΔG1Θ×ΔG2ΘC.K3Θ= K1Θ- K2ΘD.K3Θ= K1Θ+ K2Θ9. 若反应A+B → C对A;B来说都是一级反应;下列说法正确的是 CA.该反应是一级反应B.该反应速率常数的单位可以用min-1C.两种反应物中;无论哪一种物质的浓度增加1倍;都将使反应速率增加一倍D.两反应物的浓度同时减半时;其反应速率也相应减半.10. 对一个化学反应来说;下列叙述正确的是 CA.ΔGΘ越小;反应速率越快B.ΔHΘ越小;反应速率越快C.活化能越小;反应速率越快D.活化能越大;反应速率越快11. 化学反应中;加入催化剂的作用是 CA.促使反应正向进行B.增加反应活化能C.改变反应途径D.增加反应平衡常数12. 升高温度;反应速率常数增加的主要原因是 AA.活化分子百分数增加B.活化熵增加C.活化能增加D.压力增加13. 某反应298K时; Δr GΘ=130KJ•mol-1; Δr HΘ=150KJ•mol-1;下列说法错误的是 CA.可以求得298K时反应的Δr SΘB.可以求得298K时反应的平衡常数C.可以求得反应的活化能D.可以近似求得反应达平衡时的温度14. 某基元反应2Ag+Bg→Cg;其速率常数为k.当2molA与1molB在1L容器中混合时;反应速率是AA.4kB.2kC.1/4kD.1/2k15. 某反应在370K时反应速率常数是300K时的4倍;则这个反应的活化能近似值是 A KJ·mol-1A.18.3B.-9.3C.9.3D.数值不够;不能计算三.填空题1. 对于一封闭系统;定温定容且不做非体积功的条件下;系统热力学能的变化;数值上等于恒容反应热;定温定压且不做非体积功的条件下;系统的焓变;数值上等于恒压反应热 ..2. 一种溶质从溶液中结晶析出;其熵值减小 ;纯碳与氧气反应生成CO;其熵值增加 ..3. 定温定压下; ΔG可以作为过程自发性的判据..4. 当ΔH<0;ΔS<0时;低温下反应可能是自发进行 ;高温下反应可能是非自发进行 ..5.U、S、H、G是状态函数;其改变量只取决于系统的始态和终态 ;而与变化的途径无关;它们都是容量性质;其数值大小与参与变化的物质的量有关..6. 在300K;101.3KPa条件下;100cm3煤气中CO的体积百分数为60% ;此时CO的分压为60.78 KPa;CO的物质的量是 2.437×10-3mol..7.在一固定体积的容器中放置一定量的NH4Cl;发生反应NH4Cls → NH3g+HClg;Δr HΘ=177KJ•mol-1;360℃达平衡时测得PNH3=1.50KPa.则该反应在360℃时的KΘ= 2.25×10-4 ;当温度不变时;加压使体积缩小到原来的1/2; KΘ值不变;平衡向左移动;温度不变时;向容器内充入一定量的氮气; KΘ值不变;平衡不移动;升高温度; K Θ值增大 ;平衡向右移动..8. 反应Ag+Bg→ABg;根据下列每一种情况的反应速率数据;写出反应速率方程式:1当A浓度为原来的2倍时;反应速率也为原来的2倍;B浓度为原来的2倍时;反应速率为原来的4倍.则V= kC A C B2..2当A浓度为原来的2倍时;反应速率也为原来的2倍;B浓度为原来的2倍时;反应速率为原来的1/2倍.则V= kC A C B-1 ..3反应速率与A的浓度成正比;而与B浓度无关.则V= kC A ..9. 非基元反应是由若干基元反应组成的.质量作用定律不适合非基元反应复杂反应 ..10.指出下列过程的ΔSΘ大于零还是小于零:1NH4NO3爆炸ΔSΘ>0 ;2KNO3从溶液中结晶ΔSΘ<0 ;3水煤气转化为CO2及H2ΔSΘ>0 ;4臭氧的生成:3O3g→2O3g ΔSΘ<0 ;5向硝酸银溶液中滴加氯化钠溶液ΔSΘ<0 ;6打开啤酒瓶盖的过程ΔSΘ>0 ..四.计算题1. 标准状态下;下列物质燃烧的热化学方程式如下12C2H2g+5O2g →4CO2g+2H2Ol ΔH1=-2602 KJ22C2H6g+7O2g →4CO2g+6H2Ol ΔH2=-3123 KJ3H2g+1/2O2g →H2Ol ΔH3=-286 KJ根据以上反应焓变;计算乙炔C2H2氢化反应:C2H2g+2H2g →C2H6g的焓变..ΔH= -312 KJ2.在100℃;101.3KPa时;2.00molH2g与1.00molO2g反应生成2.00molH2Og;反应中释放出484.5KJ热量..计算生成每mol H2Og时的焓变ΔH和热力学能的变化ΔU..ΔH=-242.3KJ·mol-1ΔU=-240.7KJ·mol-13. 已知下列物质的生成焓:NH3g NOg H2OgΔH f KJ/mol -46.11 90.25 -241.818试计算在25℃标态时;5molNH3g氧化为NOg及H2Og的反应热效应..5molNH3g的热效应为: ΔH=-226.376×5KJ=-1131.85KJ4. 计算说明用以下反应合成乙醇的条件标准状态下:4CO2g+6H2Ol→2C2H5OHl+6O2g如此高的温度;无实际意义..5由锡石SnO2冶炼制金属锡Sn有以下三种方法;请从热力学原理讨论应推荐哪一种方法..实际上应用什么方法更好为什么1 SnO2s→Sns+O2g2 SnO2s+Cs →Sns+CO2g3 SnO2s+2H2g →Sns+2H2Og6. Ag2O遇热分解:2Ag2Os→4Ags+O2g; 已知在298K时;Ag2O的Δf HΘ=-31.1 KJ·mol-1;Δf G mΘ=-11.2 KJ·mol-1;试求在298K时PO2的压力是多少Pa Ag2O的最低分解温度pO 2=11.9Pa T> 465.6 K7. 反应CaCO 3s →CaOs+CO 2g 在973K 时K θ=2.92×10-2;900℃时K θ=1.04;试由此计算该反应的9731173,r r G G θθ∆∆及r m r m H S θθ∆∆,..r mH θ∆=169.5 KJ·mol -Δr S m Θ=144.8 J·mol -1·K -1Δr G 973Θ=28.6 KJ·mol -1Δr G 1173Θ=-0.382 KJ·mol -18. 金属钙极易与空气中的氧反应:Cas+1/2O 2g→CaOs Δf G Θ=-604 KJ ·mol -1欲使钙不被氧化;在298K 空气中氧气的分压不能超过多少Pa p<1.2×10-207Pa9. 气体混合物中的氢气;可以让它在200℃下与氧化铜反应而较好的除去: CuOs+H 2g→Cus+H 2Og在298K 时;查表计算反应的ΔG Θ; ΔH Θ; ΔS Θ;和K Θ..r m G θ∆=-98.87 KJ·mol -1K Θ=2.14×1017r m S θ∆==48.7J·K -1·mol -1r m H G T S θθθ∆=∆+∆=-84.36KJ·mol -110. 在300K 时;反应2NOClg→2NO+Cl 2的NOCl 浓度和反应速率的数据如下:NOCl 的起始浓度/mol·dm -3 起始速率/ mol·dm -3·s -10.30 3.60×10-90.60 1.44×10-80.90 3.24×10-81写出反应速率方程式. 2求出反应速率常数.3如果NOCl 的起始浓度从0.30 mol ·dm -3增大到0.45 mol ·dm -3;反应速率将增大多少倍1该反应的速率方程式为:2()kc NOCl ν= 211829100.4)30.0(1060.3----⋅⋅⨯=⨯=s mol dm k3 速率增大2.25倍.11. 根据实验测定;在一定温度范围内;2NO+Cl 2→2NOCl 为基元反应.. 1写出该反应的速率方程式..2其它条件不变时;如果将反应容器的体积增大到原来的2倍;反应速率将如何变化 3如果体积不变;将NO 的浓度增大到原来的3倍;反应速率将如何变化1基元反应速率方程式为:22()()kc NO c Cl ν=⋅2 反应速率是原来的1/8倍..3 反应速率是原来的9倍..12. 将0.1mol •L 的Na 3AsO 3和0.1mol •L Na 2SO 3溶液与过量稀H 2SO 4混合均匀;反应: 2H 3AsO 3 + 9H 2SO 3 → As 2O 3s + 3SO 2 + 9H 2O + 3H 2S 4O 6 黄色实验测得在17℃时;从溶液混合开始至刚出现黄色沉淀As 2O 3所需时间为25分15秒.若将上述溶液升温至27℃;重复上述实验;测得所需时间为8分20秒.求该反应的活化能.12.805001515lg290-⋅=⨯⨯mol KJ s sKK第2章溶液与离子平衡一.是非题1.高分子溶液与溶胶都是多相不稳定系统.. ×2.在一定温度下;液体蒸气产生的压力称为饱和蒸气压.. ×3.溶质是强电解质或其浓度较大时;溶液的蒸气压下降不符合拉乌尔定律的定量关系..√4.液体的凝固点就是液体蒸发和凝聚速率相等时的温度.. ×5.质量相等的丁二胺H2NCH24NH2和尿素CONH22分别溶于1000 g水中;所得两溶液的凝固点相同.. ×6.常利用稀溶液的渗透压来测定溶质的相对分子质量.. √7.在100g水中溶解5.2g某非电解质;该非电解质的摩尔质量为60;此溶液在标准压力下的沸点为373.60K.. √8.弱酸或弱碱的浓度越小;其解离度也越小;酸性或碱性越弱.. ×9.在一定温度下;某两种酸的浓度相等;其水溶液的pH值也必然相等.. ×10.当弱电解质解离达平衡时;离子浓度越小;解离常数越小;弱电解质的解离越弱..×11.在缓冲溶液中;只是每次加少量强酸或强碱;无论添加多少次;缓冲溶液始终具有缓冲能力.. ×12.已知K sθA g2CrO4 =1.11×10-12;K sθAgCl=1.76×10-10;在0.0100mol·kg-1K2CrO4和0.1000mol·kg-1KCl的混合溶液中;逐滴加入AgNO3溶液;则CrO24先沉淀..×13. 用EDTA做重金属的解毒剂是因为其可以降低金属离子的浓度.. √14.由于K a HAc>K a HCN;故相同浓度的NaAc溶液的pH比NaCN溶液的pH大.. ×二.选择题1.在质量摩尔浓度为1.00mol·kg-1的NaCl水溶液中;溶质的摩尔分数χB和质量分数ωB为CA.1.00; 18.09% B.0.055; 17.0%C.0.0177; 5.53% D.0.180; 5.85%2. 30%的盐酸溶液;密度为 1.15g·cm-3;其物质的量浓度C B和质量摩尔浓度b B分别为AA.9.452mol·dm-3; 11.74mol·kg-1B.94.52mol·dm-3; 27.39mol·kg-1C.31.51mol·dm-3; 1.74mol·kg-1D.0.945mol·dm-3; 2.739mol·kg-13.下面稀溶液的浓度相同;其蒸气压最高的是 CA.NaCl溶液B.H3PO4溶液C.C6H12O6溶液D.NH3-H2O溶液4.下列物质水溶液中;凝固点最低的是 CA.0.2mol·kg-1 C12H22O11 B.0.2mol·kg-1 HAcC.0.2mol·kg-1 NaCl D.0.1mol·kg-1 HAc5.相同浓度的下列溶液中沸点最高的是 CA.葡萄糖B.NaCl C.CaCl2 D.CuNH34SO46.0.1mol·kg-1 的下列溶液中pH最小的是 B A.HAc B.H2C2O4C.NH4Ac D.H2S7. 下列混合溶液;属于缓冲溶液的是 AA . 50g 0.2mol·kg -1 HAc 与 50g 0.1mol·kg -1 NaOHB . 50g 0.1mol·kg -1 HAc 与 50g 0.1mol·kg -1 NaOHC . 50g 0.1mol·kg -1 HAc 与 50g 0.2mol·kg -1 NaOHD . 50g 0.2mol·kg -1 HCl 与 50g 0.1mol·kg -1 NH 3·H 2O8.若用HAc 和NaAc 溶液配制pH = 4.5的缓冲溶液;则二者浓度之比为 CA . 8.11B . 362.3C .18.1D .989. 配制pH ≈ 7的缓冲溶液;应选择 D A . K θHAc=1.8×10-5 B .K θHCOOH=1.77×10-4C . K θH 2CO 3=4.3×10-7D .K θH 2PO 4-=6.23×10-810. AgCl 在下列物质中溶解度最大的是 B A . 纯水 B . 6mol·kg -1 NH 3·H 2OC . 0.1mol·kg -1 NaClD . 0.1mol·kg -1 BaCl 211.在PbI 2沉淀中加入过量的KI 溶液;使沉淀溶解的原因是 B A .同离子效应 B .生成配位化合物 C .氧化还原作用 D .溶液碱性增强12.下列说法中正确的是 A A .在H 2S 的饱和溶液中加入Cu 2+;溶液的pH 值将变小..B .分步沉淀的结果总能使两种溶度积不同的离子通过沉淀反应完全分离开..C .所谓沉淀完全是指沉淀剂将溶液中某一离子除净了..D .若某系统的溶液中离子积等于溶度积;则该系统必然存在固相..13.下列配合物的中心离子的配位数都是6;相同浓度的水溶液导电能力最强的是D A . K 2MnF 6 B . CoNH 36Cl 3 C . CrNH 34Cl 3 D . K 4FeCN 6三.填空题1.稀溶液的依数性是指溶液的_蒸气压下降_、___沸点升高_____、__凝固点下降___和_渗透压_..它们的数值只与溶质的__粒子数目一定量溶剂中溶质的物质的量_成正比.. 2.下列水溶液;按凝固点由高到低的顺序排列用字母表示 __ D > C > A > B .. A.1mol·kg -1 KCl B.1mol·kg -1 Na 2SO 4 C.1mol·kg -1蔗糖 D.0.1mol·kg -1蔗糖3.HAc 溶液中滴入2滴甲基橙指示剂;溶液显 _红__ 色;若再加入少量NaAcs ;溶液由 _红__ 色变为 __黄__ 色;其原因是 ___同离子效应__..4.Ag 2CrO 4的溶度积常数表达式为()()()θθθb CrO b b Ag b K s -+•=242;其溶解度S 与θs K 的关系为:43θsK S =..6.试确定下列反应向 _右____ 方进行:ZnCO3s + 4CN-ZnCN42-+ CO32-7.形成配位键时;中心原子必须具有 _空轨道_______;配位体必须具有 _孤对电子_..8.根据酸碱质子理论;H2PO -4;H2PtCl6;HSO-4;FeH2O63+ 的共轭碱的化学式分别是24HPO-; HPtCl6- ;-24SO-和FeH2O5OH2+ ..9.已知NH3的K θb为1.76×10-5;NH+4离子的Kθa值为 5.68×10-10 ..10.根据酸碱质子理论;下列物质中NH +4、H3PO4、H2S 是酸;PO-34、CO-23、-、CN-、OH-、NO -2是碱;FeH2O5OH2+、HSO-3、HS-、H2PO-4、HPO-24、H2O是两性物质..四.问答题1.溶液的沸点升高和凝固点降低与溶液的组成有何关系2.怎样衡量缓冲溶液缓冲能力的大小3.试讨论怎样才能使难溶沉淀溶解..4.试用平衡移动的观点说明下列事实将产生什么现象..1向含有Ag2CO3沉淀的溶液中加入Na2CO3..2向含有Ag2CO3沉淀的溶液中加入氯水..3向含有Ag2CO3沉淀的溶液中加入HNO35.试说明什么叫螯合物..6.酸碱质子理论与电离理论有哪些区别五.计算1.在100cm3水密度为1.0g·cm-3中溶解17.1g蔗糖C12H22O11;溶液的密度为1.0638g·cm-3; 试计算:1 溶液的质量分数;2 溶液的物质的量浓度;3 溶液的质量摩尔浓度..4 蔗糖和水的摩尔分数..解:1 溶液的质量分数:%6.14%1001.1171.17=⨯=ggwB2 已知蔗糖摩尔质量为:342g·mol-1;则:物质的量浓度:c B = 0.454mol·dm-33 质量摩尔浓度: 13315.010000.1100342/1.17---⋅=⨯⋅⨯⋅=kg mol g cm g cm mol g g b B4 摩尔分数:H 2O 的物质的量 331100 1.0 5.5618cm g cm n mol g mol --⨯⋅==⋅蔗糖的物质的量molmol g gn 05.03421.171=⋅=-31091.8)05.056.5(05.0-⨯=+=mol molx 糖991.0)05.056.5(56.52=+=mol mol x OH2.将0.450g 某电解质溶于30.0g 水中;使溶液凝固点降到-0.150℃..计算该非电解质的相对分子质量.. M = 186g·mol -1 3.某浓度的蔗糖溶液在-0.250℃时结冰..此溶液在20℃时的蒸气压为多大 渗透压为多大蔗糖的蒸气压为:P 蔗糖 = 2327.53Pa∏蔗糖= 326.4kPa4.计算下列溶液中的b H +、b A c -和1、2的解离度α:10.050mol·kg -1 HAc 溶液; 20.10mol·kg -1 HAc 溶液中加入等质量的0.050 mol·kg -1 KAc 溶液; 30.10 mol·kg -1 HAc 溶液中加入等质量的0.05 mol·kg -1 HCl 溶液; 40.10 mol·kg -1 HAc 溶液中加入等质量的0.05 mol·kg -1 NaOH 溶液..1%88.1%10005.0104.94=⨯⨯=-α2 α=0.07%3 b Ac -=3.52×10-5 mol·kg -1 4b H +=1.76×10-5 mol·kg -1 b Ac -=0.025mol·kg -1 5.0.010mol·kg -1 的某一弱酸溶液;在298K 时;测定其pH 值为5.0;求:1该酸的θa K 和α..2加入1倍水稀释后溶液的pH 值、θa K 和α..解:1()2-5810 1.0100.010a K θ-==⨯%10.0%10001.0105=⨯=-α2()8626100.110071.7005.010071.7---⨯=⨯-⨯=θa K%14.0%100005.010071.76=⨯⨯=-α6.计算20℃时;在0.10 mol·kg -1氢硫酸饱和溶液中: 1b H +、b S 2-和pH ;2如用HCl 调节溶液的酸度为pH =2.00时;溶液中的S 2-浓度是多少 计算结果说明什么问题解:1b H + = b HS - = 9.5×10-5 mol·kg -1b S 2- ≈θ2K = 1.1×10-12 mol·kg -1pH = -lg9.5×10-5 = 4.022b S2-= 1.0×10-16 mol·kg-17.在18℃时;PbSO4的溶度积为1.82×10-8;试求在这个温度PbSO4在0.1mol·kg-1 K2SO4溶液中的溶解度..b Pb2+ = 1.82×10-7 mol·kg-18.在18℃时;AgBr的溶度积为5.35×10-13;在纯水中AgBr的溶解度是多少在0.10mol·kg-1 的NaBr溶液中AgBr的溶解度是多少解:1在纯水中AgBr的溶解度是7.31×10-7 mol·kg-1..2即在0.1mol·kg-1 的NaBr中;AgBr的溶解度为5.35×10-12 mol·kg-19.通过计算说明:1在100g 0.15mol·kg-1 的KAgCN2溶液中加入50g 0.10mol·kg-1 的KI 溶液;是否有AgI 沉淀产生2在上述混合溶液中加入50g 0.20mol·kg-1 的KCN溶液;是否有AgI产生解:1 有AgI 沉淀析出..2无AgI 沉淀析出..10.某溶液中含有Pb2+ 和Ba2+;其质量摩尔浓度分别为0.01 mol·kg−1和0.10mol·kg−1..若向此溶液逐滴加入K2CrO4溶液;问哪种金属离子先沉淀此两种离子有无分离的可能已知K θs PbCrO4=1.77×10−14;Kθs BaCrO4=1.2×10−10..解:从计算结果可知:沉淀Pb2+ 比沉淀Ba2+ 所需的CrO-24少得多;所以;将首先析出PbCrO4沉淀..当BaCrO4开始沉淀时;Pb2+已沉淀完全了..此两种离子可以分离..第3章 氧化还原反应 电化学一.判断题1. 在25℃及标准状态下测定氢的电极电势为零.. X2. 已知某电池反应为,21212B A B A +→+++而当反应式改为B A B A +→+++222时;则此反应的E Θ不变;而Δr G m Θ改变.. √ 3. 在电池反应中;电动势越大的反应速率越快.. X 4. 在原电池中;增加氧化态物质的浓度;必使原电池的电动势增加.. X 5. 标准电极电势中θE 值较小的电对中的氧化态物质;都不可能氧化θE 值较大的电对中 的还原态物质.. X 6. 若将马口铁镀锡和白铁镀锌的断面放入稀盐酸中;则其发生电化学腐蚀的阳极反应是相同的.. X 7. 电解反应一定是0,0<∆>∆G G r r θ的反应.. X 8. 超电势会导致析出电势高于平衡电势.. X二.选择题1. 下列关于氧化数的叙述正确的是 AA.氧化数是指某元素的一个原子的表观电荷数B.氧化数在数值上与化合价相同C.氧化数均为整数D.氢在化合物中的氧化数皆为+12. 若已知下列电对电极电势的大小顺序E ΘF 2/F - > E ΘFe 3+/Fe 2+ > E ΘMg 2+/Mg > E ΘNa +/Na;则下列离子中最强的还原剂是 BA.F -B.Fe 2+C.Na +D.Mg 2+3. 已知电极反应Cu e Cu →+-+22的标准电极电势为0.342V ;则电极反应+-→-2242Cu e Cu 的标准电极电势应为 CA.0.684VB.-0.684VC.0.342VD.-0.342V 4. 已知E ΘNi 2+/Ni= -0.257V;测得镍电极的ENi 2+/Ni= -0.210V;说明在该系统中必有 AA.121)(-+⋅>kg mol Ni mB. 121)(-+⋅<kg mol Ni mC. 121)(-+⋅=kg mol Nim D. )(2+Ni m 无法确定5. 下列溶液中;不断增加H +的浓度;氧化能力不增强的是 DA.MnO 4-B.NO 3-C.H 2O 2D.Cu 2+ 6. 将下列反应中的有关离子浓度均增加一倍;使对应的E 值减少的是 CA.Cu e Cu →+-+22B. +-→-22Zn e ZnC. --→+Cl e Cl 222D. +-+→+242Sn e Sn7. 某电池的电池符号为-Pt|A 3+;A 2+ ¦¦ B 4+;B 3+|Pt+;则此电池反应的产物应为 BA. A 3+; B 4+B. A 3+; B 3+C. A 2+; B 4+D. A 2+; B 3+ 8. 在下列电对中;标准电极电势最大的是 DA.AgCl/AgB.AgBr/AgC.AgNH 32+/AgD.Ag +/Ag 9. A 、B 、C 、D 四种金属;将A 、B 用导线连接;浸在稀硫酸中;在A 表面上有氢气放 出;B 逐渐溶解;将含有A 、C 两种金属的阳离子溶液进行电解时;阴极上先析出C ;把D 置于B 的盐溶液中有B 析出..则这四种金属的还原性由强到弱的顺序是 CA.A>B>C>DB.C>D>A>BC.D>B>A>CD.B>C>D>A10. 已知标准氯电极的电势为 1.358V;当氯离子浓度减少到11.0-⋅kg mol ;氯气分压减少到kPa 1001.0⨯时;该电极的电极电势应为 CA.1.358VB.1.3284VC.1.3876VD.1.4172V 11. 电解NiSO 4溶液;阳极用镍;阴极用铁;则阳极和阴极的产物分别是 AA.Ni 2+;NiB. Ni 2+;H 2C.Fe 2+; NiD. Fe 2+; H 2 12. 在腐蚀电极中 CA.阴极必将发生析氢反应B.阴极必将发生吸氧反应C.阴极的实际析出电势必高于阳极的实际析出电势D.极化作用使得腐蚀作用加快三.填空题1. 在一定条件下;以下反应均可向右进行;O H Fe Cr H Fe O Cr 2332272762146++→++++++-1+++++→+422322Sn Fe Sn Fe2上述物质中最强的氧化剂应为Cr 2O 72-;最强的还原剂应为Sn 2+ ..2. 原电池是由 自发 的氧化-还原反应所组成的.在这种反应中;必伴随着 电子迁移的过程..3. 对于氧化-还原反应;若以电对的电极电势作为判断的依据时;其自发的条件必为E +>E - ..4. 某原电池的一个电极反应为-+++→e HO O H 44222;则这个反应一定发生在 负极 ..5. 若某原电池的一个电极发生的反应是--→+Cl e Cl 222;而另一个电极发生的反应为+-+→-32Fe e Fe ;已测得)/()/(232++->Fe Fe E Cl Cl E ;则该原电池的电池符号应为 -Pt|Fe 3+;Fe 2+ ¦¦ Cl -|Cl 2| Pt+ ..6. 已知反应V E l Hg aq H aq Hg g H 797.0),(2)(2)()(222=+→+++θ;则))(/(2l Hg Hg E +θ= 0.797V .. 7. 在Cu-Zn 原电池中;若)/()/(22Zn Zn E Cu Cu E ++>;在Cu 电极和Zn 电极中分别注入氨水;则可能分别导致该原电池的电动势 先降低 和 后升高 ..8. 25℃时;若电极反应22)(2D e aq D →+-+的标准电极电势为-0.0034V;则在相同温度及标准状态下反应)()(2)()(222g H aq D g D aq H +→+++的θE = 0.0034V ; θG r ∆= -6.56×102J •mol -1 ;θK = 1.3 ..9. 电解CuSO 4溶液时;若两极都用铜;则阳极反应为+-→-22Cu e Cu ;阴极反应为Cu e Cu →+-+22 ;若阴极使用铜做电极而阳极使用铂做电极;则阳极反应为 ;阴极反应为Cu e Cu→+-+22;若阴极使用铂做电极而阳极使用铜做电极;则阳极反应为+-→-22Cu e Cu ;阴极反应为Cu e Cu →+-+22..四问答题1. 试从电子运动方向;离子运动方向;电极反应;化学变化与电转换作用本质;反应自发性五个方面列表比较原电池与电解池的异同..2. 半电池A 是由镍片浸在 1.0mol•k g -1的Ni 2+溶液中组成的;半电池B 是由锌片浸在1.0mol•kg -1的Zn 2+溶液中组成的..当将半电池A 和B 分别与标准氢电极连接组成原电池;测得原电池的电动势分别为V H B E V H A E 762.0)(,257.0)(22=-=-.试回答下面问题:1当半电池A 和B 分别与标准氢电极组成原电池时;发现金属电极溶解.试确定各半电池的电极电势符号是正还是负..2Ni 、Ni 2+、Zn 、Zn 2+中;哪一种物质是最强的氧化剂3当将金属镍放入1.0mol•kg -1的Zn 2+溶液中;能否发生反应 将金属锌浸入1.0mol•kg -1的Ni 2+溶液中会发生什么反应 写出反应方程式..4Zn 2+与OH -能反应生成ZnOH 42-.如果在半电池B 中加入NaOH;问其电极电势是变大变小还是不变5将半电池A 和B 组成原电池;何者为正极 电动势是多少 3.根据下面的电池符号;写出相应的电极反应和电池总反应.4.写出下列电解的两极产物.五.计算题1. 将Cu 片插入盛有0.5mol•Kg -1的CuSO 4溶液的烧杯中;Ag 片插入盛有0.5mol•Kg -1的AgNO 3溶液烧杯中:1写出该原电池的电池符号;2写出电极反应式和原电池的电池反应; 3求该电池的电动势;4若加入氨水于CuSO 4溶液中;电池的电动势将如何变化 若加氨水于AgNO 3溶液中;情况又如何 定性回答 解:1电池符号:-Cu|Cu 2+0.5mol•Kg -1 ¦¦ Ag +0.5mol•Kg -1 |Ag+2 Ag Cu Ag Cu 222+→+++3 0.449V 42. 已知电极反应NO 3-+3e+4H +→NO+2H 2O 的E ΘNO 3-/NO=0.96V;求当bNO 3-=1.0mol•Kg -1时;P NO =100Kpa 的中性溶液中的电极电势.并说明酸度对NO 3-氧化性的影响..解: NO 3-氧化能力受酸度的影响.若酸度较大;其氧化能力增大;所以浓硝酸的氧化能力强..3. 对含有Ag +的溶液加入Cl -;使达平衡时Cl -的浓度为1.0mol•Kg -1..计算Ag +/ Ag 电对的 电极电势.试回答计算结果说明了什么..解:说明;氧化型离子生成沉淀时;会降低电对的电极电势..4. 已知Zn e Zn →+-+22;V E 76.0-=θ;---+→++OH Zn e O H ZnO 422222;V E 22.1-=θ..试通过计算说明锌在标准状态下;既能从酸中;又能从碱中置换放出氢气..5. 已知某原电池的正极是氢电极;kPa H p 100)(2=;负极的电极电势是恒定的..当氢电 极中pH=4.008时;该电池的电动势是0.412V.如果氢电极中所用的溶液改为一未知bH +的缓冲溶液;又重新测得原电池的电动势为0.427V.计算该缓冲溶液的bH +和pH 值.如果该缓冲溶液中10.1)()(--⋅==kg mol A b HA b ;求该弱酸HA 的解离常数..解: 44108.10.10.1108.1)(--⨯=⨯⨯=HA K a θ6. 某原电池的一个半电池是由金属Co 浸在1.0mol•Kg -1的Co 2+溶液中组成;另一半电池则 由Pt 片浸入1.0mol•Kg -1的Cl -溶液中并不断通入Cl 2)100)((2kPa Cl p =组成.实验测得电池的电动势为1.63V;钴电极为负极.已知V Cl Cl E 36.1)/(2=-θ.回答下面问题:1写出电池反应方程式;2)/(2Co Co E +θ为多少3)(2Cl p 增大时;电池电动势将如何变化4当Co 2+浓度为0.010mol•Kg -1时;电池电动势是多少 Δr G m 为多少 解:1 )(2)()()(22aq Cl aq Co g Cl s Co -++→+2 V E Cl Cl E Co Co E 27.063.136.1)/()/(22-=-=-=+θθθ3 PCl 2增大时;E 正增大; 电池电动势E 增大..4 Δr G m =-326.1KJ •mol -17. 将氢电极和甘汞电极插入某HA-A -的缓冲溶液中;饱和甘汞电极为正极.已知1110.0)(,0.1)(---⋅=⋅=kg mol A b kg mol HA b ;向此溶液中通入H 2100kPa;测得其电动势为0.4780V..1写出电池符号和反应方程式; 2求弱酸HA 的解离常数.. 解:1电池符号为:-Pt|H 2100kPa|HA1.0mol•kg -1;A -0.10mol•kg -1 ¦¦ KCl 饱和|Hg 2Cl 2s|Hg| Pt +电池反应方程式为:)(2)(2)(2)(2)()(222aq Cl aq HA l Hg aq A g H s Cl Hg --++→++2 54100.10.110.0100.1)(--⨯=⨯⨯=HA K a θ8. 试以中和反应O H aq OH aq 2)()(H →+-+l 为电池反应;设计成一种原电池用电池符号表示.分别写出电极半反应;并求算该电池在25℃时的标准电动势及θωK ..解: V EEE 8288.08288.00=+=-=-+θθθ14101-⨯=θw K 9. 根据下列反应及其热力学常数;计算银-氯化银电对的标准电极电势E ΘAgCl/AgH 2+2AgCl=2H ++2Cl -+2Ag..已知该反应在25℃时的Δr H m Θ=-80.80KJ•mol -1; Δr S m Θ=-127.20J•mol -1•K -1.. 解: E ΘAgCl/Ag= 0.222V10. 在0.10mol•Kg -1的CuSO 4溶液中投入锌粒;求反应达平衡后溶液中Cu 2+的浓度..解:bCu 2+=2.0×10-3811. 选用Fe; Cu; Zn; Al 片;碳棒;质量摩尔浓度均为1.0mol•Kg -1的FeCl 3; CuSO 4; ZnSO 4; AgNO 3溶液;及0.01mol•Kg -1的FeCl 2溶液;设计一个电动势最大的原电池..假定此电池可 用来电解忽略其它因素影响CuSO 4溶液阳极用Cu;阴极用Fe;回答下列问题:: 1写出原电池的两极反应及电池符号; 2计算原电池的电动势及Δr G m ; 3 写出电解池的两极反应..解:1Zn|ZnSO 41.0mol•Kg -1 ¦¦ FeCl 31.0mol•Kg -1;FeCl 20.01mol•Kg -1|C 2Δr G m =-3.186×105J•mol -13两极反应:阳极:Cu-2e -=Cu 2+阴极:Cu 2++2e -=Cu。
《大学化学教学课件》化学平衡

化学平衡与生命过程
化学平衡在生命过程中扮演着至关重要的角色。生物体内的各种化学反应都是在一定的平衡 状态下进行的,如酸碱平衡、离子平衡和氧化还原平衡等。
维持生命所需的正常生理功能需要保持这些平衡状态的稳定。例如,人体内的酸碱平衡对于 维持正常的生理功能至关重要,如果失衡可能导致酸中毒或碱中毒等严重后果。
平衡常数的意义
平衡常数是化学反应达到平衡状态时, 生成物浓度幂之积与反应物浓度幂之 积的比值。
平衡常数是化学反应特征常数之一, 它反映了化学反应在平衡状态下反应 物和生成物之间的相对浓度关系。
平衡常数表达式
根据化学反应方程式,平衡常数表达 式通常由生成物浓度幂之积除以反应 物浓度幂之积得到。
平衡常数的计算
平衡的意义
化学反应限度
平衡状态反映了化学反应的限 度,即反应所能达到的最大程 度。
工业应用
了解化学平衡有助于优化工业 生产中的反应过程,提高产物 的产率和纯度。
理论价值
化学平衡理论对于理解化学反 应的本质和规律具有重要价值 ,是化学学科中的重要基础理 论之一。
02
化学平衡的原理
平衡常数
平衡常数定义
的方向移动。
勒夏特列原理
如果改变影响平衡的条件,平衡 就会向着能够减弱这种改变的方
向移动。
平衡常数
在一定温度下,可逆反应达到平 衡时各生成物浓度的化学计量数 次幂的乘积除以各反应物浓度的 化学计量数次幂的乘积所得的比
值。
平衡移动的影响因素
01
02
03
浓度对平衡的影响
增加反应物的浓度或减少 生成物的浓度,平衡向正 反应方向移动;反之,平 衡向逆反应方向移动。
动态平衡
平衡状态并不是静止不变的,而是处于动态平衡中 ,即正逆反应速率相等但并不为零。
大学化学课后习题答案

第一章化学反应热教学内容1.系统、环境等基本概念; 2. 热力学第一定律; 3. 化学反应的热效应。
教学要求掌握系统、环境、功、热(恒容反应热和恒压反应热)、状态函数、标准态、标准生成焓、反应进度等概念;熟悉热力学第一定律;掌握化学反应标准焓变的计算方法。
知识点与考核点1.系统(体系)被划定的研究对象。
化学反应系统是由大量微观粒子(分子、原子和离子等)组成的宏观集合体。
2.环境(外界)系统以外与之密切相关的部分。
系统和环境的划分具有一定的人为性,划分的原则是使研究问题比较方便。
系统又可以分为敞开系统(系统与环境之间既有物质交换,又有能量交换);封闭体系(系统与环境之间没有..能量交换);..物质交换,只有孤立系统(体系与环境之间没有物质交换,也没有能量交换)系统与环境之间具有边界,这一边界可以是实际的相界面,也可以是人为的边界,目的是确定研究对象的空间范围。
3.相系统中物理性质和化学性质完全相同的均匀部分。
在同一个系统中,同一个相可以是连续的,也可以是不连续的。
例如油水混合物中,有时水是连续相,有时油是连续相。
4.状态函数状态是系统宏观性质(T、p、V、U等)的综合表现,系统的状态是通过这些宏观性质描述的,这些宏观性质又称为系统的状态函数。
状态函数的特点:①状态函数之间往往相互制约(例如理想气体状态方程式中p、V、n、T之间互为函数关系);②其变化量只与系统的始、末态有关,与变化的途径无关。
5*.过程系统状态的变化(例如:等容过程、等压过程、等温可逆过程等)6*.途径完成某过程的路径。
若系统的始、末态相同,而途径不同时,状态函数的变量是相同的。
7*.容量性质这种性质的数值与系统中的物质的量成正比,具有加合性,例如m(质量)V、U、G等。
8*.强度性质这种性质的数值与系统中的物质的量无关,不具有加合性,例如T、 (密度)、p(压强)等。
9.功(W)温差以外的强度性质引起的能量交换形式[W=W体+W有]。
分析化学(高教第五版)课后习题第五章答案(整理排版4页)

第五章 习题5.1计算pH=5时EDTA 的酸效应系数αY(H)。
若此时EDTA 各种存在形式的总浓度为0.0200mol ·L -1,则[Y 4-]为多少?答案:(1)EDTA 的61~K K :1010.26,106.16,102.67,102.0,101.6,100.961~ββ:1010.26,1016.42,1019.09,1021.09,1022.69,1023.59pH=5.0时:()[][][][][][]66554433221H Y H H H H H H 1ββββββ++++++++++++=α=1+105.26+106.42+104.09+101.09+10-2.31+10-6.41=106.45(2)[Y 4-]=45.610020.0=7.1×10-9mol ·L -15.2 pH=5时,锌和EDTA 配合物的条件稳定常数是多少?假设Zn 2+和EDTA 的浓度皆为10-2 mol ·L -1(不考虑羟基配位等副反应)。
pH=5时,能否用EDTA 标准溶液滴定Zn 2+?答案: 查表5-2: 当pH=5.0时,lg αY(H)=6.45,Zn 2+与EDTA 浓度皆为10-2mol ·L -1, lgK ’=lgK 稳- lg αY(H)=16.50-6.46=10.05﹥8,可以滴定。
5.3假设Mg 2+和EDTA 的浓度皆为10-2 mol ·L -1,在pH=6时,镁与EDTA 配合物的条件稳定常数是多少(不考虑羟基配位等副反应)?并说明在此pH 条件下能否用EDTA 标准溶液滴定Mg 2+。
如不能滴定,求其允许的最小pH 。
答案: (1)查表5-2: 当pH=6.0时,lg αY(H)=4.65,lgK ’=lgK 稳- lg αY(H)=8.69-4.65=4.04, lgK ’﹤8, ∴不能滴定(2)lg αY(H)= lgK 稳-8=0.69,查表5-2得pH ≈9.6。
普通化学大学化学第五章ppt课件

➢能量最低原理
➢ 在不违背泡利原理的条件下,核外电子分布将 尽能够优先占据能级较低的轨道,使系统能量处于 最低。
多电子原子轨道能级:多电子原子中各轨道能量 的高低除与 n 和 l 值有关外,还与电子之间的相互作 用能有关,鲍林(L.Pauling)根据他对原子构造的研 讨结果,提出了多电子原子轨道的能级高低顺序为:
多电子原子体系可以得到薛定谔方程的近似解,过 程非轨道的能量仅决议于主量子数n,各轨道 能量关系为
E1S<E2S=E2P<E3S=E3P=E3d<…… 在多电子原子中,轨道能量不仅与主量子数n有 关,还与角量子数l有关。 一.多电子原子轨道的能级 光谱实验结果归纳出的多电子原子轨道能级高低规 律如下: 角量子数 l 一样时,随着主量子数 n 值的增 大,轨道能量升高。
2 波函数与原子轨道 对于电子波,薛定谔给出一个动摇方程:
x 2 ψ 2 y2 ψ 2 z2 ψ 28 π h2 2m(E V )ψ 0
其中, 为动摇函数,是空间坐标x、y、z 的函数。 E 为核外电子总能量,V 为核外电子的势能,h 为普 朗克常数,m 为电子的质量。
由于波函数与原子核外电子出如今原子周围某位置的概率有 关, 所以又笼统的称为“原子轨道〞。
一样的 九. 两个电子。 十. 由泡利原理可知,在每一个原子轨道
➢洪特〔Hund〕规那么 ➢ 当电子在n, l 一样的数个等价轨道上分布时,每 个电子尽能够占据磁量子数不同的轨道且自旋平行。
例1 碳原子(1s22s22p2)的两个p电子在三个能量 一样的2p轨道上如何分布?
共有以下三种陈列方法:
I
s区
ns1 ~ ns2
p 区 ns2np1 ~ ns2np6
d 区 (n-1)d1ns2 ~(n-1)d8ns2
大学有机化学模拟练习题及参考答案共五套
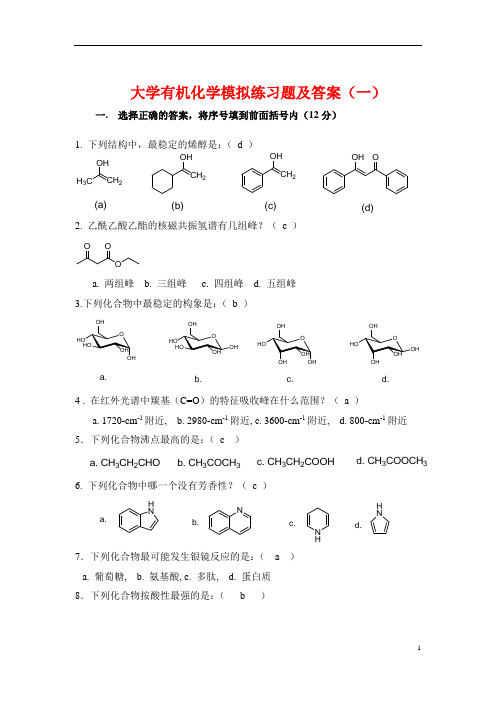
I. CH3CH2Br II. (CH3)2CHBr III. (CH3)3CHBr
a. I > II > III b. III > II > I c. III > I > II
三.按要求排列顺序(10 分)
1. 酸性由强到弱的顺序为:
a. CH3CH2CHCO2H b. CH3CHCH2CO2H
Cl
5.下列化合物沸点最高的是:( c )
a. CH3CH2CHO b. CH3COCH3 c. CH3CH2COOH
6. 下列化合物中哪一个没有芳香性?( c )
H
N
N
a.
b.
c. N H
7.下列化合物最可能发生银镜反应的是:( a )
a. 葡萄糖, b. 氨基酸, c. 多肽, d. 蛋白质
8.下列化合物按酸性最强的是:( b )
Cl
a>b>c
2. 碱性由强到弱的顺序为:
a. (C2H5)2NH
b. CH3CH2NH2
c.
c. CH2CH2CH2CO2H Cl
NH2
a>b>c 四.完成下列反应,写出主要产物或反应条件(15 分)
1. CH3 CH CH2 HBr CH3CHBrCH3
2.
CH2CH3 + KMnO4
H+
CO2H
8. CH3CH2
(CH2)4CH2CCH2CH3
CC
CH3
H
二、按要求写出下列化合物的结构式(每小题 1 分,共 10 分)
1. 顺丁烯二酸酐
2. 顺-1-甲基-4-叔丁基环己烷的优势构象
3. -D-葡萄糖的哈沃斯式
4. 4-甲基-1-异丙基二环[3.1.0]己烷
高二化学选修五课件第五章章末小结与测评

章章末小结与测评
汇报人:XX
20XX-01-12
• 第五章知识点回顾与总结 • 重点难点解析及拓展 • 典型例题解析与思路点拨 • 学生自我评价报告展示及教师点评 • 下一阶段学习计划和目标制定 • 测评试卷分析及改进措施
01
第五章知识点回顾与总结
化学反应原理
化学反应的热力学和动力学
复习。
利用资源
充分利用课本、参考书、在线 资源等,拓宽学习途径,提高
学习效果。
06
测评试卷分析及改进措施
测评试卷整体情况概述
试卷难度适中,考查知识点覆盖面广
本次测评试卷难度适中,考查内容涵盖了本章节的重点和难点知识,题型多样, 包括选择题、填空题、简答题等。
学生成绩呈现正态分布,区分度良好
从成绩统计结果来看,学生成绩呈现正态分布,高分段和低分段人数较少,中间 分数段人数较多,说明试卷难度适中,区分度良好。
掌握反应热、焓变、熵变等热力学概念,理解反应速率、活化能 等动力学原理。
化学平衡
理解化学平衡的建立和移动,掌握沉淀溶解平衡、酸碱平衡、配位 平衡等平衡原理。
化学反应的方向和限度
掌握化学反应的方向判据,如吉布斯自由能变、平衡常数等,理解 反应限度的概念。
电解质溶液
电解质溶液的导电机理
缓冲溶液
理解电解质溶液的导电机理,掌握离 子迁移数、电导率等概念。
电解质溶液中离子平衡问题探讨
弱电解质的电离平衡
理解弱电解质的电离过程及影响因素,掌握电离平衡常数的应用 。
盐类水解
了解盐类水解的原理及影响因素,掌握水解平衡常数的应用。
离子浓度大小比较
理解电解质溶液中离子浓度大小比较的方法,掌握电荷守恒、物 料守恒、质子守恒等规律的应用。
人教版化学选修5第五章:进入合成有机高分子化合物的时代复习学案(推断题带答案)
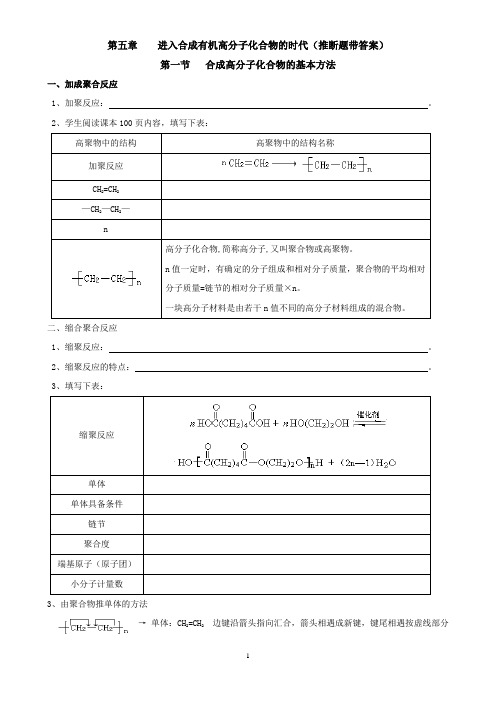
第五章进入合成有机高分子化合物的时代(推断题带答案)第一节合成高分子化合物的基本方法一、加成聚合反应1、加聚反应:。
2、学生阅读课本100页内容,填写下表:高聚物中的结构高聚物中的结构名称加聚反应CH2=CH2—CH2—CH2—n高分子化合物,简称高分子,又叫聚合物或高聚物。
n值一定时,有确定的分子组成和相对分子质量,聚合物的平均相对分子质量=链节的相对分子质量×n。
一块高分子材料是由若干n值不同的高分子材料组成的混合物。
二、缩合聚合反应1、缩聚反应:。
2、缩聚反应的特点:。
3、填写下表:缩聚反应单体单体具备条件链节聚合度端基原子(原子团)小分子计量数3、由聚合物推单体的方法→单体:CH2=CH2边键沿箭头指向汇合,箭头相遇成新键,键尾相遇按虚线部分断键成单键。
→单体:凡链节主链只在C原子并存在有C=C双键结构的高聚物,其规律是“见双键、4个C;无双键、2个C”,划线断开,半键闭合,双键互换。
1、写出下列单体聚合成聚合物的化学方程式(1)CH2=CHCl :。
(2):。
(3) :2、写出生成下列高聚物的化学方程式:(1):。
(2):。
(3):。
(4):。
有机合成题(带答案)1.有一种名为菲那西汀的药物,其基本合成路线如下:则:(1)反应②中生成的无机物化学式为。
(2)反应③中生成的无机物化学式为。
(3)反应⑤的化学方程式是。
(4)菲那西汀水解的化学方程式为。
2.以石油产品乙烯为起始原料进行合成高分子化合物F和G,合成路线如图所示:已知:E的分子式为C4H6O2,F的分子式为(C4H6O2)n(俗名“乳胶”的主要成分),G的分子式为(C2H4O)n(可用于制化学浆糊),2CH2=CH2+2CH3COOH+O2 2C4H6O2(醋酸乙烯酯)+2H2O又知:与结构相似的有机物不稳定,发生分子重排生成请回答下列问题:(1)写出结构简式:E ,F 。
(2)反应①、②的反应类型、。
(3)写出A—→B、B—→C的化学方程式。
人教版化学选修5课后习题参考答案yu剖析

人教版化学选修5课后习题参照答案第一元、参照答案一1A、D2D3〔1〕〔2〕炔〔3〕酚〔4〕〔5〕〔6〕代二1.4 4 共价双三2.33.B4.C(CH3)45.CH3CH=CH2三1.B2. 〔1〕3,3,4-三甲基己〔2〕3-乙基-1-戊〔3〕1,3,5-三甲基苯3.四重晶〔1〕在此溶中不溶解或溶解度大,易撤掉〔2〕被提的有机物在此溶中的溶解度,受温度的影响大蒸30℃左右C10H8NO2348C20H16N2O4HOCH2CH2OH部分复参照答案〔1〕2,3,4,5-四甲基己〔2〕2-甲基-1-丁〔3〕1,4-二乙基苯或二乙基苯〔4〕2,2,5,5-四甲基庚5. 〔1〕20 30 1 〔2〕56%有机化合物的命名法有机化合物命名有俗名、命名法〔又称一般命名法〕和系命名法,此中系命名法最通用,最重要。
〔1〕俗名依占有机化合物的来源、存在与性而获得的称号。
比如,甲又称坑气、沼气;甲醇又称木醇等。
〔2〕一般命名法用天干即甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示碳原子数在10之内的有机化合物,碳原子数在10以上的用字数字表示,如十一、十二、十三⋯⋯异构体以“正”“异”“新”平分别。
如:直或其直的衍生物用“正”字表示,如“正己”“正戊醇”等。
在的碳结尾有甲基支的用“异”字表示,如“异己”“异丁”等。
限于含有五、六个碳原子的或其衍生物中,拥有季碳原子(即接四个基的碳原子)的用“新”字表示,如“新己”“新戊醇”等。
上述命名法合用于构的有机化合物,构复的有机化合物需用系命名法。
在介系命名法以前,先熟习基的命名。
基名一个化合物失掉一个一价原子或原子,余下的部分称“基”。
如〔RH〕失掉一个原子即获得基(R-),常的基有:此外,有一些常的基:〔4〕系命名法跟着有机化合物数量标增加,有必需拟定一个公的命名法。
1892年在日内瓦召开了国化学会,拟定了日内瓦命名法。
后由国学与用化学合会(IUPAC)作了几次修,并于1979年宣布了《有机化学命名法》。
分析化学第五章试题及参考答案

第五章思考题与习题1.写出下列各酸的共轭碱:H2O,H2C2O4,H2PO4-,HCO3-,C6H5OH,C6H5NH3+,HS-,Fe(H2O)63+,R-NH+CH2COOH.答:H2O的共轭碱为OH-;H2C2O4的共轭碱为HC2O4-;H2PO4-的共轭碱为HPO42-;HCO3-的共轭碱为CO32-;;C6H5OH的共轭碱为C6H5O-;C6H5NH3+的共轭碱为C6H5NH2;HS-的共轭碱为S2-;Fe(H2O)63+的共轭碱为Fe(H2O)5(OH)2+;R-NH2+CH2COOH的共轭碱为R-NHCH2COOH。
2. 写出下列各碱的共轭酸:H2O,NO3-,HSO4-,S2-,C6H5O-,C u(H2O)2(OH)2,(CH2)6N4,R—NHCH2COO-,COO-C O O-。
答:H2O的共轭酸为H+;NO3-的共轭酸为HNO3;HSO4-的共轭酸为H2SO4;S2的共轭酸为HS-;C6H5O-的共轭酸为C6H5OH C u(H2O)2(OH)2的共轭酸为Cu(H2O)3(OH)+;(CH2)6N4的共轭酸为(CH2)4N4H+;R—NHCH2COO-的共轭酸为R—NHCHCOOH,COO-C O O-的共轭酸为COO-C O O-H3.根据物料平衡和电荷平衡写出(1)(NH4)2CO3,(2)NH4HCO3溶液的PBE,浓度为c(mol·L-1)。
答:(1)MBE:[NH4+]+[NH3]=2c; [H2CO3]+[HCO3-]+[CO32-]=cCBE:[NH4+]+[H+]=[OH-]+[HCO3-]+2[CO32-]PBE:[H+]+2[H2CO3] +[HCO3-]=[NH3]+[OH-](2)MBE:[NH4+]+[NH3]=c; [H2CO3]+[HCO3-]+[CO32-]=cCBE:[NH4+]+[H+]=[OH-]+[HCO3-]+2[CO32-]PBE:[H+]+[H2CO3]=[NH3]+[OH-]+[CO32-]4.写出下列酸碱组分的MBE、CEB和PBE(设定质子参考水准直接写出),浓度为c (mol·L-1)。
《大学有机化学答案》PPT课件
B2 C rH CHC BC H r
(5)
编辑ppt
5
3. (2) ,(3)有顺反异构体。结构式略 。 4.
O
O
(6) H 3 CCC2H C2H C2H C2H CC H 3 (7) CH3CH2COOH + CH3COOH
(8)
H 3CC2HC2H Br
(9)
(10)
(11)
CH3
H 3 C C2H CH C H 2
7. (1) 反应的第二步不能发生,因为氯乙烯不能和CN-发生 亲核取代反应
CH3
(2) 应该发生消除反应,产物为: H3C C CHCH3
编辑ppt
20
8 (1)
(2) 9. (1)
(2)
H3CCHCH 2
编辑ppt
21
10.
B
Br Br
11.
第二组可能的结构:
编辑ppt
4
第三章 习题参考答案
1. (1) 3,4-二甲基-1,3-戊二烯 (2)5-甲基-3-己烯-1-炔
(3) (E)-3-甲基-2-戊烯
(4)(Z)-2-甲基-3-乙基-3-己烯
(5)2,6-二甲基-2-庚烯
(6) 丙炔银
(7) 3,3-二甲基-1-戊烯
(8) 4-甲基-2-戊炔
2.
+ (2) H 2 CCH CC H B 2r
编辑ppt
8
第四章 习题参考答案
1. (1) 1,1-二甲基-2-异丙基环丙烷 (2) 5-甲基螺[2,4]庚烷
2.
(3) 2-甲基-3-环丙基丁烷
(4) 1-甲基-3-乙基环己烷
3.
(5) 2-硝基苯磺酸
大学化学(1)》模拟试题分解

大学化学(1)》模拟试题分解《大学化学(1)》模拟试题参考答案与评分标准注意事项:1. 请考生按要求在试卷装订线内填写姓名、学号和年级专业。
2. 请仔细阅读各种题目的回答要求,在规定的位置填写答案。
3. 不要在试卷上乱写乱画,不要在装订线内填写无关的内容。
4. 满分100分,考试时间为120分钟。
题号一二三四总分统分人得分得分一、选择题(本大题共10个小题,每个2分,共20分,将1个或2个正确答案的代码填入括号内,选错或未选均评分人无分)1. 已知:A + B → M + N(??rHm)1 = 35 kJ·mol-1 2M + 2N → 2D (??-1 rHm)2 = -80 kJ·mol则A + B → D 的(?H?rm)3 是( C )。
(A)-10 kJ·mol-1 (B)-45 kJ·mol-1 (C)-5 kJ·mol-1 (D)25 kJ·mol-1 2. 下列说法正确的是( C )。
(A) 热的物体比冷的物体含有更多的热量;(B) 同一种状态可能有多个热力学能值;(C) 热是一种传递中的能量;(D) 物体温度越高,则所含热量越高。
3.在平衡系统中PCl5(g)PCl3(g) + Cl2(g) ΔrH?m>0欲增大生成物Cl2平衡时的浓度,需采取下列哪些措施( B D )。
(A)加大压力(B)加大PCl5浓度(C)降低温度(D)升高温度4.如果一个反应的吉布斯自由能变为零,则反应( D )。
1(A) 能自发进行(B) 是吸热反应(C) 是放热反应(D) 处于平衡状态5.下列物质中含有氢键的是( B D )。
(A)HBr (B) HF (C) CCl4 (D) H2SO4 6.在标准条件下,下列反应均为正方向进行:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O2Fe3++Sn2+=2Fe2++Sn4+它们中间最强的氧化剂和最强的还原剂是( B )。
工科大学化学--第五章

5.1.1 核外电子运动状态
3.原子轨道与电子云的图像
波函数的数学函数式也可用图形来表示, 在解薛定谔方程时, 将直角坐标 x、
y、 z 转换成球坐标 r、θ、φ。 为了把 ψ 随 r、θ、φ的变化表示清楚, 将 ψ(r,θ ,
5.1.1 核外电子运动状态
4) 自旋量子数ms。 实验表明, 原子中的电子, 除绕原子核运动外还可以自转, 称为电子自
旋。 电子自旋方向有顺时针和逆时针两种情况。 决定电子自旋状态的量 子数称作自旋磁量子数, 用 ms 表示。 ms只能取+ 1/2 或- 1/2 两个数值, 一般 用 ↑ 和 ↓ 表示电子的两种自旋状态。
工科大学化学
5. 物质结构基础
1 原子结构
2 元素周期律
4 晶体结构
目录
3 化学键与分子结构
5.1 原子结构
5.1.1 核外电子运动状态
原子是化学变化中的最小微粒, 由原子核和核外电子组成。 原子核 是 原子直径的万分之一,但几乎集中了原子的全部质量。原子内部十分空阔, 在 周围相当大的空间中, 电子绕原子核做高速运动。
5.1.1 核外电子运动状态
l 数值与对应的电子亚层符号如下
当 n = 1 时, 只有 l = 0, 称为 1s 亚层; 当 n = 2 时, l = 0、 1, 分别称为 2s 亚 层和 2p 亚层; 依此类推。单电子原子中, 各轨道的能量只与 n 有关。 例如氢 原子:
多电子原子中, 各轨道能量除与 n 有关外, 还与 l 有关。 同一电子层中 的轨道 (即 n 相同) , l 值越大, 其能量越高, 例如
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020年10月12日9时37
7
分
根据价键理论要点,对于s和px轨道的重叠只有(a) 方式可以形成稳定的共价键。
- ++
(a)
+
-+
(b)
+ -+
(c)
+-
+ (d)
4
分
一、价键理论
1、氢分子中共价键的形成
根据氢分子薛 定谔方程的求解结 果,可以得出两个 氢原子之间的相互 作用能和核间距之 间的关系。如右图 所示。
E 0d
核间距
氢分子形成时的能量变化
2020年10月12日9时37
5
分
实 验 测 得 氢 分 子 d=74pm, H - H 键 能 为 436kJ /mol。
2020年10月12日9时37
8
分
3、σ键和π键 以“头碰头”方式重叠形成的共价键称为σ键。
++
ss ++ -
s
p
-
++
-
σ键电子云 处于两核连线 上,核对σ键 电子的束缚力 大,σ键稳定, 优先形成。
p
p
2020年10月12日9时37
9
分
以“肩并肩”方式重叠形成的共价键称为π键。
+
+
-
-
π
Nσ N π
(2)能级相近的价层轨道混合起来,重新组合成 成键能力更强的新的原子轨道,这些新的轨道称为 杂化轨道。杂化轨道的数目与参与杂化的轨道的数 目相同。
(3)杂化轨道最大对称地分布在杂化原子的周围。
(4)杂化轨道与其它原子的价电子配对只能形成 σ键。
2020年10月12日9时37
13
分
2、杂化类型
(1)sp杂化
π键电子云并不处于两核 连线上,核对π键电子的束 缚力较小,因而π键不如σ 键稳定。当两原子形成共价 键时应优先形成σ键,然后 再考虑是否形成π键,换句 话说,π键不能单独存在。 因此共价双键和三键中必有 一个σ键,如N2。
2020年10月12日9时37
10
分
二、杂化轨道理论和分子的空间构型
价键理论解释双原子分子的成键情况非常成功。 但对于多原子分子的成键情况及空间构型不能解释。
2p
2s
2s
激发
2s2p轨道
2p
2p
sp2
杂化 三个 sp2 杂化轨道
2020年10月12日9时37
16
分
(3)sp3杂化
一个s轨道和三个p轨道进行的杂化称为sp3杂化。 现以CH4 分子为例,说明sp3杂化及其成键过程。
2p
2p
sp3
2s
2s
Байду номын сангаас
激发
杂化 四个 sp3 杂化轨道
2020年10月12日9时37
(1)两原子自旋方向相反的未成对电子相互接近时 可以配对形成共价键。
原子中有几个未成对电子就可以形成几个共价 键——共价键的饱和性。如H只能形成H2,H和O只 能形成H2O,H和N只能形成NH3等。 (2)原子轨道相互重叠时,只能“正-正”或“负 -负”重叠,否则不能形成共价键——对称性匹配 原理。
2020年10月12日9时37
11
分
莱纳斯·鲍林(1901-1994),著名的理论化学 家,先后两次单独荣获诺贝尔奖(1954年的化学奖, 1962年的和平奖),被誉为20世纪科学怪杰 。
2020年10月12日9时37
12
分
1、杂化轨道理论要点
(1)价层上成对的电子在相邻原子的作用下可以 拆开并激发到能级相近的轨道上去。
如BeCl2分子,实验测得为直线型,键角180°,两 根Be-Cl键完全等同。而按照价键理论,Be原子2s轨 道上的电子已配对,无法形成共价键。如果考虑2s轨 道上的一个电子激发到2p轨道上去,确实有两个未成 对电子,但成键时,两根键所用的轨道不同,其性质 必然不同,其方向性也难以确定。
为此,1931年,鲍林在电子配对法的基础上提出了 轨道杂化的概念,现已发展成为杂化轨道理论。
W.Heitler(1904-1981)
2020年10月12日9时37 分
F.London(1900-1954)
3
这是他们发表在Zeitschrift für Physik(物理学杂志), 44, 455—472 (1927)上的论文原件,两位科学家时年 分别为23和27岁。
2020年10月12日9时37
17
分
(4)不等性sp3杂化
含有成对电子的原子轨道也可以参与杂化,只是 杂化以后,部分杂化轨道已被孤对电子占据不能成 键罢了,我们将这种杂化方式称为不等性杂化。
杂化
两个 sp 杂化轨道
2020年10月12日9时37
14
分
sp杂化轨道的形状及BCl2分子的空间构型如图所示
z y
x
x
y z
3p sp
sp 3p
2020年10月12日9时37
15
分
(2)sp2杂化
一个s轨道和两个p轨道进行的杂化称为sp2杂化。 现以BF3分子为例,说明sp2杂化及其成键过程。
一个s轨道和一个p轨道进行的杂化称为sp杂化。 现以BeCl2 分子为例,说明sp杂化及其成键过程。
在Cl原子的影响下,Be原子2s轨道上的一个电子 激发到同为价层的一个2p轨道上去,然后一个2s轨 道和一个2p轨道杂化成两个完全等同的sp杂化轨道, 杂化过程可用下图表示:
2p
2p
2p
sp
2s
2s
激发
而玻尔半径为53pm,显然,两个氢原子的1s轨 道发生部分重叠。轨道重叠情况可用下图表示。
(a)自旋方式相反 (b) 自旋方式相同
氢原子轨道重叠示意图
原子轨道有效重叠是价键理论的实质! 将量子力学处理氢分子的结果推广到其它分子, 即发展为价键理论。
2020年10月12日9时37
6
分
2、价键理论要点
第五章 分子结构和晶体结构
• 原子之间强烈的作用力称之为化学键 • 化学键主要分为金属键、离子键和共价键
本章主要讨论: • 共价键的形成——价键理论 • 分子结构——杂化轨道理论 • 共价分子之间的作用力 • 晶体的基本类型及其特征
通过本章的学习,可以初步判断物质的物理性质 和化学性质
2020年10月12日9时37
1
分
第一节 共价键的形成
• 同种非金属元素之间、不同种非金属元素之间以 及电负性相差不大的非金属-金属元素之间一般 以共价键结合形成共价型分子。
• 近代共价键理论主要有价键理论(VB法)和分子 轨道理论(MO法)。本章主要介绍价键理论。
2020年10月12日9时37
2
分
1927年海特勒和伦敦运用量子力学原理,通过求 解氢分子的薛定谔方程,认识到了共价键的本质, 经过发展形成了共价键理论。
