硫脲的理化特性
硫脲的分子量

硫脲的分子量硫脲(Thiourea)是一种有机化合物,其分子式为CH4N2S,分子量为 76.12 g/mol。
它是一种白色结晶固体,可溶于水和大多数有机溶剂中。
硫脲具有许多重要的应用,包括作为化学试剂、催化剂和农药等。
本文将从不同的角度介绍硫脲的分子量及其相关特性。
1. 硫脲的化学结构硫脲的化学结构中包含了一个硫原子和两个氮原子。
硫原子与两个氮原子相连,形成了一个类似于尿素的结构。
硫脲的分子式为CH4N2S,其中C表示碳原子,H表示氢原子,N表示氮原子,S表示硫原子。
2. 硫脲的物理性质硫脲是一种白色结晶固体,具有特殊的臭味。
其熔点为170-180℃,沸点为172-175℃。
硫脲可溶于水和大多数有机溶剂,如醇类、醚类和酮类等。
在水中的溶解度随温度的升高而增加。
3. 硫脲的化学性质硫脲是一种相对稳定的化合物,但在一些条件下也会发生化学反应。
例如,硫脲可以与酸反应生成硫脲酸,与碱反应生成硫脲酸盐。
硫脲还可以与许多化合物发生取代反应,形成不同的衍生物。
4. 硫脲的应用领域硫脲具有许多重要的应用。
首先,硫脲广泛用作化学试剂,例如用于测定金属离子、有机物的分析等。
其次,硫脲还可以作为一种催化剂,参与多种有机反应,如氧化、还原和羟基化反应等。
此外,硫脲还被用作农药的原料,具有抗菌、杀虫等作用。
5. 硫脲的生产和用途硫脲的生产主要通过硫氰酸铵和氨水的反应得到。
硫脲的用途非常广泛,不仅在化学实验室中被广泛使用,还广泛应用于农业、医药、染料、橡胶等领域。
例如,在农业中,硫脲可以用作杀虫剂,对一些害虫具有较好的杀灭效果。
在医药领域,硫脲可以用于合成一些药物,如降压药和抗肿瘤药物等。
总结:硫脲是一种重要的有机化合物,具有丰富的应用价值。
它的分子量为76.12 g/mol,化学结构中含有硫原子和两个氮原子。
硫脲是一种白色结晶固体,可溶于水和大多数有机溶剂。
它具有特殊的物理性质和化学性质,可以用作化学试剂、催化剂和农药等。
危化品MSDS-硫脲

硫脲1. 化学品及企业标识化学品中文名称:硫脲化学品英文名称:thiourea中文名称2:硫代尿素英文名称2:thiocarbamide主要用途:用于有机合成,也用作药品、橡胶添加物、镀金材料等。
2. 危险性概述2.1 危险性类别:有毒品。
2.2侵入途径:吸入、食入、经皮吸收。
2.3 健康危害:一次作用时毒性小,反复作用时可抑制甲状腺和造血器官的机能。
可引起变态反应。
可经皮肤吸收。
本品粉尘对眼和上呼吸道有刺激性,吸入后引起咳嗽、胸部不适。
口服刺激胃肠道。
慢性影响:长期接触出现头痛、嗜睡、无力、面色苍白、面部虚肿、基础代谢降低、血压下降、脉搏变慢、白细胞减少等。
对皮肤有损害,出现皮肤瘙痒、手掌出汗、皮炎、皲裂等。
2.4环境危害:对水生生物有毒作用。
2.5燃爆危险:可燃,其粉体与空气混合,能形成爆炸性混合物。
3. 成分/组成信息纯品■混合物□主要成分CAS RN 含量(%)硫脲62-56-6 99.04. 急救措施4.1 皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医。
4.2眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医。
4.3吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
4.4食入:饮足量温水,催吐。
就医。
5. 消防措施5.1 危险特性:遇明火、高热可燃。
受热分解,放出氮、硫的氧化物等毒性气体。
与氧化剂能发生强烈反应。
5.2有害燃烧产物:氮氧化物、氧化硫。
5.3灭火方法:用水、雾状水、泡沫、二氧化碳、砂土灭火。
5.4灭火注意事项及措施:消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
6. 泄漏应急措施应急处理:隔离泄漏污染区,限制出入。
消除所有点火源。
建议应急处理人员戴防尘口罩,穿防毒服。
穿上适当的防护服前严禁接触破裂的容器和泄漏物。
危化品MSDS-硫脲学习资料

危化品M S D S-硫脲硫脲1. 化学品及企业标识化学品中文名称:硫脲化学品英文名称:thiourea中文名称2:硫代尿素英文名称2:thiocarbamide主要用途:用于有机合成,也用作药品、橡胶添加物、镀金材料等。
2. 危险性概述2.1 危险性类别:有毒品。
2.2侵入途径:吸入、食入、经皮吸收。
2.3 健康危害:一次作用时毒性小,反复作用时可抑制甲状腺和造血器官的机能。
可引起变态反应。
可经皮肤吸收。
本品粉尘对眼和上呼吸道有刺激性,吸入后引起咳嗽、胸部不适。
口服刺激胃肠道。
慢性影响:长期接触出现头痛、嗜睡、无力、面色苍白、面部虚肿、基础代谢降低、血压下降、脉搏变慢、白细胞减少等。
对皮肤有损害,出现皮肤瘙痒、手掌出汗、皮炎、皲裂等。
2.4环境危害:对水生生物有毒作用。
2.5燃爆危险:可燃,其粉体与空气混合,能形成爆炸性混合物。
3. 成分/组成信息纯品■混合物□主要成分 CAS RN 含量(%)硫脲 62-56-6 99.04. 急救措施4.1 皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医。
4.2眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医。
4.3吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
4.4食入:饮足量温水,催吐。
就医。
5. 消防措施5.1 危险特性:遇明火、高热可燃。
受热分解,放出氮、硫的氧化物等毒性气体。
与氧化剂能发生强烈反应。
5.2有害燃烧产物:氮氧化物、氧化硫。
5.3灭火方法:用水、雾状水、泡沫、二氧化碳、砂土灭火。
5.4灭火注意事项及措施:消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
6. 泄漏应急措施应急处理:隔离泄漏污染区,限制出入。
消除所有点火源。
建议应急处理人员戴防尘口罩,穿防毒服。
硫脲在酪氨酸酶催化中的抑制动力学

硫脲在酪氨酸酶催化中的抑制动力学是一项重要的研究课题,它涉及到酶催化机制、化学反应动力学等多个领域的知识。
本文将系统地介绍硫脲对酪氨酸酶催化的抑制作用,并深入探讨其动力学特性,以期为相关研究提供参考和借鉴。
一、硫脲的化学结构和性质硫脲是一种有机化合物,化学结构为(NH2)2CS,其分子中含有硫、氮和碳元素。
硫脲具有白色结晶粉末状,易溶于水,能够形成银盐沉淀,具有较强的还原性和亲电性。
在生物体内,硫脲被广泛应用于医药、农业等领域,常用作抗甲状腺药物、医学显影剂、化肥等。
二、酪氨酸酶的催化机制酪氨酸酶是一种重要的酶类蛋白,广泛存在于生物体内,能够催化酪氨酸的化学反应。
其催化机制主要包括底物结合、活化能降低、反应速率增加等步骤。
在催化过程中,酶与底物结合形成酶-底物复合物,通过降低反应活化能,促进反应的进行,并在反应结束后释放产物。
三、硫脲对酪氨酸酶的抑制作用1. 竞争性抑制硫脲能够与酪氨酸酶的活性中心结合,从而与底物竞争结合,影响酶的正常催化活性。
竞争性抑制的特点是与底物结合位点相似,而不改变酶的构象。
2. 非竞争性抑制硫脲以一种不同于底物的方式结合于酶的其他位点,造成酶的构象或活性中心的改变,从而影响催化活性。
非竞争性抑制不受底物浓度的影响,通常与酶的构象变化有关。
3. 抑制常数(Ki)的确定抑制常数(Ki)是衡量抑制物对酶抑制程度的一个重要参数,一般通过测定在不同浓度的抑制物条件下酶活性的变化,利用双倒数法或直线化法求得。
四、硫脲对酪氨酸酶催化动力学的影响1. 变温下的酶抑制动力学通过对变温条件下酶抑制动力学特性的研究,可以揭示硫脲抑制作用的温度依赖性,进一步探讨抑制机制。
2. pH值对酶抑制动力学的影响pH值是影响酶催化活性的重要因素,硫脲的抑制作用也受pH值的影响。
通过研究不同pH值条件下酶的抑制动力学,可以揭示硫脲抑制作用的pH依赖性特点。
3. 亲合力测定及动力学参数计算通过亲合力测定及动力学参数的计算,可以具体了解硫脲与酶的结合特性,进一步分析抑制机制及动力学特性。
危化品MSDS-硫脲

硫脲1. 化学品及企业标识化学品中文名称:硫脲化学品英文名称:thiourea中文名称2:硫代尿素英文名称2:thiocarbamide主要用途:用于有机合成,也用作药品、橡胶添加物、镀金材料等。
2. 危险性概述2.1 危险性类别:有毒品。
2.2侵入途径:吸入、食入、经皮吸收。
2.3 健康危害:一次作用时毒性小,反复作用时可抑制甲状腺和造血器官的机能。
可引起变态反应。
可经皮肤吸收。
本品粉尘对眼和上呼吸道有刺激性,吸入后引起咳嗽、胸部不适。
口服刺激胃肠道。
慢性影响:长期接触出现头痛、嗜睡、无力、面色苍白、面部虚肿、基础代谢降低、血压下降、脉搏变慢、白细胞减少等。
对皮肤有损害,出现皮肤瘙痒、手掌出汗、皮炎、皲裂等。
2.4环境危害:对水生生物有毒作用。
2.5燃爆危险:可燃,其粉体与空气混合,能形成爆炸性混合物。
3. 成分/组成信息纯品■混合物□主要成分CAS RN 含量(%)硫脲62-56-6 99.04. 急救措施4.1 皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医。
4.2眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医。
4.3吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
4.4食入:饮足量温水,催吐。
就医。
5. 消防措施5.1 危险特性:遇明火、高热可燃。
受热分解,放出氮、硫的氧化物等毒性气体。
与氧化剂能发生强烈反应。
5.2有害燃烧产物:氮氧化物、氧化硫。
5.3灭火方法:用水、雾状水、泡沫、二氧化碳、砂土灭火。
5.4灭火注意事项及措施:消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
6. 泄漏应急措施应急处理:隔离泄漏污染区,限制出入。
消除所有点火源。
建议应急处理人员戴防尘口罩,穿防毒服。
穿上适当的防护服前严禁接触破裂的容器和泄漏物。
硫脲

硫脲为有机络合剂,可与许多金属离子形成络合物。
为白色有光泽的菱形六面结晶体,味苦,微毒,无腐蚀作用。
密度为1.405g/cm3,熔点为180~182℃,温度更高时分解,易溶于水,20℃时在水中溶解度为9%-10%(142g/L),溶解热为22.57kJ/d,其水溶液呈中性。
近40年来,由于物理技术的迅速发展,硫脲分子的化学结构已被进一步认定为以下的共振式:即它是通过分子中的N十和s原子所具有的自由电子对,吸附于金粒表面而使金的氧化还原电位大大降低,使金易于氧化而溶解进人溶液中。
硫脲在碱性溶液中不稳定,易分解为硫化物和氨基氰:SC(NH2)2+2NaOH====Na2S+CNNH2+2H2O分解生成的氨基氰可转变为尿素:CNNH2+H2O=====CO(NH2)2从而造成硫脲的消耗。
在碱性介质中,硫脲分解生成的S2-还可与溶液中的Au+、Ag+及Cu2+等各种金属阳离子生成硫化物沉淀。
硫脲在酸性(pH1-6)溶液中具有还原性质,可被氧化而生成多种产物。
在室温下比较容易氧化为二硫甲脒(SCN2H3)2:硫脲的稳定性主要取决于介质的pH,硫脲浓度和温度。
在适宜的温度下,当硫脲浓度一定时,随着介质pH的下降,硫脲趋向于更稳定;反之,当介质的pH一定时,随着硫脲浓度的增大,硫脲越易被氧化。
为保持硫脲在溶金过程中的稳定性,提金作业宜采用低pH的硫脲溶液。
也只有降低溶液的pH,才能适当地提高溶液中的硫脲浓度。
298K硫脲的主要热力学数据如表1。
温度的提高虽能加快硫脲溶金的初始速度,但它会严重影响硫脲的稳定性,使得溶金才度随时间的延长而不断下降,甚至无效。
在多数文献中,选定的硫脲溶金介质温度不高了25℃,虽然它不一定是最佳的选择,但试验证明,随着介质(不论是酸性、中性或碱性)温度的升高硫脲的氧化速度会加快。
当硫脲在酸性或碱性溶液中,加热至60℃时,均会发生水解而生成氨、二氧化碳和液态H2S:SC(NH2)2+2H2O====CO2+2NH3+H2SH2S还可进一步分解成S。
硫脲的分子式

硫脲的分子式
硫脲的化学式为CH4N2S,是一种无色结晶体,易溶于水和酒精。
它是一种重要的有机合成中间体,广泛应用于医药、染料、农药等领域。
1.在医药领域,硫脲被广泛用于制造多种药品,例如抗肿瘤药、抗生素和降血糖药。
此外,硫脲还可以用作胃泌素释放肤拮抗剂,可用于治疗肥胖症。
2.在化工领域,硫脲是一种重要的化工原料,用于制造多种化学产品,例如橡胶加工助剂、尿素形成催化剂和颜料材料。
3. 硫脲还可以用于其他领域,例如水处理、纸浆和纤维素工业、染料和荧光剂制造等在作用机制方面,硫脲可以抑制肝细胞内的氧化应激反应,从而减轻肝脏损伤,还可以用于调节血糖、血压等生理指标,改善患者的症状。
在作用机制方面,硫脉可以抑制肝细胞内的氧化应激反应,从而减轻肝脏损伤,还可以用于调节血糖、血压等生理指标,改善患者的症状。
随着科学技术的不断发展,硫服的应用前景将会更加广阔。
危化品MSDS-硫脲

硫脲1。
化学品及企业标识化学品中文名称:硫脲化学品英文名称:thiourea中文名称2:硫代尿素英文名称2:thiocarbamide主要用途:用于有机合成,也用作药品、橡胶添加物、镀金材料等。
2。
危险性概述2。
1 危险性类别:有毒品。
2.2侵入途径:吸入、食入、经皮吸收.2。
3 健康危害:一次作用时毒性小,反复作用时可抑制甲状腺和造血器官的机能。
可引起变态反应.可经皮肤吸收。
本品粉尘对眼和上呼吸道有刺激性,吸入后引起咳嗽、胸部不适.口服刺激胃肠道.慢性影响:长期接触出现头痛、嗜睡、无力、面色苍白、面部虚肿、基础代谢降低、血压下降、脉搏变慢、白细胞减少等。
对皮肤有损害,出现皮肤瘙痒、手掌出汗、皮炎、皲裂等。
2。
4环境危害:对水生生物有毒作用。
2.5燃爆危险:可燃,其粉体与空气混合,能形成爆炸性混合物.3。
成分/组成信息纯品■混合物□主要成分CAS RN 含量(%)硫脲62-56-6 99.04. 急救措施4。
1 皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医。
4.2眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医。
4.3吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术.就医.4.4食入:饮足量温水,催吐。
就医。
5. 消防措施5。
1 危险特性:遇明火、高热可燃。
受热分解,放出氮、硫的氧化物等毒性气体。
与氧化剂能发生强烈反应。
5.2有害燃烧产物:氮氧化物、氧化硫。
5.3灭火方法:用水、雾状水、泡沫、二氧化碳、砂土灭火。
5。
4灭火注意事项及措施:消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火.尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束.6。
泄漏应急措施应急处理:隔离泄漏污染区,限制出入。
消除所有点火源。
建议应急处理人员戴防尘口罩,穿防毒服。
穿上适当的防护服前严禁接触破裂的容器和泄漏物.尽可能切断泄漏源。
硫脲
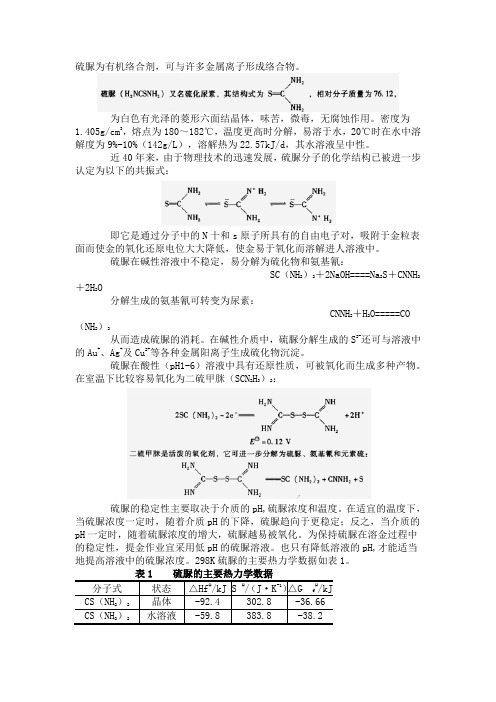
硫脲为有机络合剂,可与许多金属离子形成络合物。
为白色有光泽的菱形六面结晶体,味苦,微毒,无腐蚀作用。
密度为1.405g/cm3,熔点为180~182℃,温度更高时分解,易溶于水,20℃时在水中溶解度为9%-10%(142g/L),溶解热为22.57kJ/d,其水溶液呈中性。
近40年来,由于物理技术的迅速发展,硫脲分子的化学结构已被进一步认定为以下的共振式:即它是通过分子中的N十和s原子所具有的自由电子对,吸附于金粒表面而使金的氧化还原电位大大降低,使金易于氧化而溶解进人溶液中。
硫脲在碱性溶液中不稳定,易分解为硫化物和氨基氰:SC(NH2)2+2NaOH====Na2S+CNNH2+2H2O分解生成的氨基氰可转变为尿素:CNNH2+H2O=====CO(NH2)2从而造成硫脲的消耗。
在碱性介质中,硫脲分解生成的S2-还可与溶液中的Au+、Ag+及Cu2+等各种金属阳离子生成硫化物沉淀。
硫脲在酸性(pH1-6)溶液中具有还原性质,可被氧化而生成多种产物。
在室温下比较容易氧化为二硫甲脒(SCN2H3)2:硫脲的稳定性主要取决于介质的pH,硫脲浓度和温度。
在适宜的温度下,当硫脲浓度一定时,随着介质pH的下降,硫脲趋向于更稳定;反之,当介质的pH一定时,随着硫脲浓度的增大,硫脲越易被氧化。
为保持硫脲在溶金过程中的稳定性,提金作业宜采用低pH的硫脲溶液。
也只有降低溶液的pH,才能适当地提高溶液中的硫脲浓度。
298K硫脲的主要热力学数据如表1。
温度的提高虽能加快硫脲溶金的初始速度,但它会严重影响硫脲的稳定性,使得溶金才度随时间的延长而不断下降,甚至无效。
在多数文献中,选定的硫脲溶金介质温度不高了25℃,虽然它不一定是最佳的选择,但试验证明,随着介质(不论是酸性、中性或碱性)温度的升高硫脲的氧化速度会加快。
当硫脲在酸性或碱性溶液中,加热至60℃时,均会发生水解而生成氨、二氧化碳和液态H2S:SC(NH2)2+2H2O====CO2+2NH3+H2SH2S还可进一步分解成S。
硫脲分子式

硫脲分子式硫脲分子式CAS号87-43-1。
纯度99%。
无色或微带淡黄色,有刺激性气味的液体。
易溶于水,微溶于乙醇。
溶于盐酸、氨水。
可与硝酸银反应生成一种有机弱酸的银白色沉淀。
硫脲用途十分广泛,它是合成树脂、农药、染料、橡胶等的原料,也可用作防毒面具中吸收剂,还可以用来制备其他一些衍生物如一些缩合反应的催化剂、偶氮染料、医药等的中间体、也用于制造烟火、火柴、杀虫剂和触媒等。
硫脲分类硫脲根据其结构不同可分为:取代硫脲包括双硫脲、三硫脲、二甲基硫脲等,此类产品属国家管制产品;水杨酰胺类衍生物是合成抗疟药阿的平、扑疟母等的重要中间体。
【产品性状】硫脲白色针状结晶或粉末,具有特殊气味,易潮解。
【中文名称】硫脲【中文别名】脲;三氮苯磺酸钠;甲酰脲【英文名称】 Ketone【英文别名】 Triethylenesulfonate;Ketesalt;Toline salt【 CAS号】 87-43-1【分子式】 C9H8N3O3S【分子量】 189.19【 EINECS号】 209-921-4【化学性质】硫脲为白色针状结晶或粉末,有特殊气味,易潮解。
熔点50~53 ℃,沸点235 ℃,折光率1.497,比重1.67,水溶性90%。
硫脲在一般条件下稳定,低温时逐渐分解,可加热至150~170 ℃脱水成脲醛树脂,在强碱作用下进一步水解得到酚醛树脂和二氧化碳。
工业上将硫脲和其他含活泼氢的有机化合物混合加热,得到固体树脂或固体硫脲。
硫脲主要用于硝基纤维素、醋酸纤维素、聚酰亚胺、聚砜、聚丙烯腈、不饱和聚酯树脂等的合成原料,是醋酸纤维素、脲醛树脂的改性剂,是各种农药、杀虫剂、染料、涂料的原料,还用于防毒面具的生产中。
用途编辑1、合成树脂方面:用作环氧树脂、氯化橡胶、不饱和聚酯树脂等的合成原料。
2、农药方面:用于农药有机硫杀虫剂的合成。
3、橡胶方面:用于氯丁橡胶的生产。
4、印染助剂方面:可用作印染助剂、不饱和聚酯树脂、环氧树脂、增塑剂、表面活性剂、颜料及油漆、涂料的中间体。
硫脲 熔沸点

硫脲,化学名称为硫代尿素,英文名为Thiourea,化学式为CH4N2S,是一种白色结晶或粉末状的有机化合物,具有微弱的特殊气味。
它在常温下相对稳定,可溶于水、醇和醚等多种溶剂中。
硫脲(Thiourea)的熔点和沸点分别是:
熔点:170至172°C
沸点:335至340°C
请注意,这些数值是在标准大气压下测定的。
在不同的压力条件下,熔点和沸点可能会有所变化。
下面是关于硫脲的主要性质和用途包括:
1.化学性质:硫脲可以与重金属离子形成稳定的络合物,因此
在化学分析中有一定的应用;它还具有还原性,能参与氧化
还原反应。
2.工业用途:硫脲广泛应用于化工、制药、染料等行业,如用
于制造农药(如杀虫剂、除草剂)、橡胶助剂、照相材料、
皮革鞣制剂等;另外,硫脲还是某些药物和精细化学品的重
要中间体。
3.实验室用途:在实验室中,硫脲可用于合成其他含硫化合
物,例如磺酰胺类药物和其他有机硫化物。
4.环保领域:硫脲可用作重金属离子废水处理中的螯合剂,帮
助去除废水中的铜、镍、铅等重金属离子。
5.农业领域:作为肥料添加剂,硫脲可以提高作物对氮肥的吸
收利用率,并有助于改善土壤结构。
硫脲

谢谢观看
急救措施
急救措施
皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。 眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼 吸。就医。 食入:饮足量温水,催吐。就医。
消防措施
消防措施
有害燃烧产物:氧化氮、氧化硫。 灭火方法:采用水、泡沫、二氧化碳、砂土灭火。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,硫脲在3类致癌物清单 中。
理化性质
理化性质
熔点:176~178℃ 密度:1.41g/cm3 logP:-1.05 折射率:1.654 闪点:66.8℃ 临界压力:8.23MPa 外观:白色有光泽晶体 溶解性:溶于冷水、乙醇,微溶于乙醚
用途
用途
硫脲主要用作合成磺胺噻唑、蛋氨酸等药物的原料,也可用作染料及染色助剂、树脂及压塑粉的原料,也可 用作橡胶的硫化促进剂、金属矿物的浮选剂、制邻苯二甲酸酐和富马酸的催化剂,以及用作金属防锈蚀剂。在照 相材料方面,可作为显影剂和调色剂,还可用于电镀工业。硫脲还用于重氮感光纸、合成树脂涂料、阴离子交换 树脂、发芽促进剂、杀菌剂等许多方面。硫脲也作为化肥使用。用于制造药物、染料、树脂、压塑粉、橡胶的硫 化促进剂、金属矿物的浮选剂等的原料。
风险术语
R22:Harmful if swallowed. 吞食是有害的。 R40:Possible risks of irreversible effects. 可能有不可逆作用的风险。 R51/53:Toxic to aquatic organisms, may cause long-term adverse effects in the aquatic environment. 对水生生物有毒,可能在水生环境中造成长期不利影响。 R63:Possible risk of harm to the unborn child. 可能有损害未出生婴儿的危险。
危化品MSDS 硫脲

硫脲1. 化学品及企业标识化学品中文名称:硫脲化学品英文名称:thiourea中文名称2:硫代尿素英文名称2:thiocarbamide主要用途:用于有机合成,也用作药品、橡胶添加物、镀金材料等。
2. 危险性概述危险性类别:有毒品。
侵入途径:吸入、食入、经皮吸收。
健康危害:一次作用时毒性小,反复作用时可抑制甲状腺和造血器官的机能。
可引起变态反应。
可经皮肤吸收。
本品粉尘对眼和上呼吸道有刺激性,吸入后引起咳嗽、胸部不适。
口服刺激胃肠道。
慢性影响:长期接触出现头痛、嗜睡、无力、面色苍白、面部虚肿、基础代谢降低、血压下降、脉搏变慢、白细胞减少等。
对皮肤有损害,出现皮肤瘙痒、手掌出汗、皮炎、皲裂等。
环境危害:对水生生物有毒作用。
燃爆危险:可燃,其粉体与空气混合,能形成爆炸性混合物。
3. 成分/组成信息纯品■混合物□主要成分 CAS RN 含量(%)硫脲 62-56-64. 急救措施皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
食入:饮足量温水,催吐。
就医。
5. 消防措施危险特性:遇明火、高热可燃。
受热分解,放出氮、硫的氧化物等毒性气体。
与氧化剂能发生强烈反应。
有害燃烧产物:氮氧化物、氧化硫。
灭火方法:用水、雾状水、泡沫、二氧化碳、砂土灭火。
灭火注意事项及措施:消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
6. 泄漏应急措施应急处理:隔离泄漏污染区,限制出入。
消除所有点火源。
建议应急处理人员戴防尘口罩,穿防毒服。
穿上适当的防护服前严禁接触破裂的容器和泄漏物。
尽可能切断泄漏源。
用塑料布覆盖泄漏物,减少飞散。
勿使水进入包装容器内。
用洁净的铲子收集泄漏物,置于干净、干燥、盖子较松的容器中,将容器移离泄漏区。
硫脲

应急行动:隔离泄漏污染区,限制出入。消除所有点火源。建议应急处理人员戴防尘口罩,穿防毒服,戴橡胶手套。穿上适当的防护服前严禁接触破裂的容器和泄漏物。尽可能切断泄漏源。用塑料布覆盖泄漏物,减少飞散,勿使水进入包装容器内。用洁净的铲子收集泄漏物,置于干净、干燥、盖子较松的容器中,将容器移至泄漏区
储存注意事项:储存于阴凉、通风的库房。远离火种、热源。包装密封。应与氧化剂、酸类、食用化学品分开存放,切忌混储。配备相应品种和数量的消防器材。储区应备有合适的材料收容泄漏物。
第八部分:接触控制∕个体防护
职业接触限值:中国:未制定标准
美国(ACGIH):未制定标准
监测方法:无资料
工程控制:密闭操作,局部排风。提供安全淋浴和洗眼设备。
第十四部分:运输信息
危险货物编号:61821铁危编号:61821
UN编号:无资料包装类别:Ⅱ类包装
包装标志:有毒品
包装方法:塑料袋或二层牛皮纸袋外全开口或中开口钢桶(钢板厚1.2或1.25毫米,每桶净重不超过200公斤);塑料袋或二层牛皮纸袋外普通木箱;螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外普通木箱;螺纹口玻璃瓶、塑料瓶或镀锡薄钢板桶(罐)外满底板花格箱、纤维板箱或胶合板箱。
、硫脲
第一部分:化学品及企业标识
化学品中文名称:硫脲;硫代尿素
化学品英文名称:thiourea;thiocarbamide
分子式:CH4N2S相对分子质量:76.13
结构式S NH2
C
NH2
第二部分:成分∕组成信息
√纯品混合物
有害物成分浓度CAS No.
硫脲62-56-6
第三部分:危险性概述
危险性类别:第6.1类毒害品
硫脲MSDS

环境危害:对环境有危害。
燃爆危险:本品可燃,有毒,具刺激性。
第四部分 急 救 措 施
皮肤接触脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。
TLVWN:未制定标准
监测方法:
工程控制:密闭操作,局部排风。提供安全淋浴和洗眼设备。
呼吸系统防护:空气中粉尘浓度较高时,应该佩戴自吸过滤式防尘口罩。
眼睛防护:一般不需特殊防护。必要时,戴化学安全防护眼镜。
身体防护:穿一般作业防护服。
手防护:戴橡胶手套。
其它防护:工作完毕,淋浴更衣。单独存放被毒物污染的衣服,洗后备用。保持良好的卫生习惯。
储存注意事项:储存于阴凉、通风的库房。远离火种、热源。包装密封。应与氧化剂、酸类、食用化学品分开存放,切忌混储。配备相应品种和数量的消防器材。储区应备有合适的材料收容泄漏物。
第八部分 接触控制/个体防护
职业接触限值:
中国MAC(mg/m3):未制定标准
前苏联MAC(mg/m3):0.3
TLVTN:未制定标准
第六部分 泄漏应急处理
应急处理:隔离泄漏污染区,限制出入。切断火源。建议应急处理人员戴防尘面具(全面罩),穿一般作业工作服。不要直接接触泄漏物。小量泄漏:用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏:收集回收或运至废物处理场所处置。
第七部分 操作处置与储存
操作注意事项:密闭操作,局部排风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,戴橡胶手套。远离火种、热源,工作场所严禁吸烟。使用防爆型的通风系统和设备。避免产生粉尘。避免与氧化剂、酸类接触。搬运时要轻装轻卸,防止包装及容器损坏。配备相应品种和数量的消防器材及泄漏应急处理设备。倒空的容器可能残留有害物。
表- 硫脲的理化性质及危险特性表

表- 硫脲的理化性质及危险特性表
稳固,避免碰撞、摩擦、倾倒等情况发生。
运输车辆应装备相应的消防器材和急救设备。
运输过程中应避免与氧化剂、酸类、食用化学品等混装混运。
禁止与热源、火种等接触。
运输过程中如发生泄漏,应立即采取应急处理措施。
硫脲是一种白色光亮苦味晶体,分子式为CH4N2S,分子量为76.12.它可以溶于冷水和乙醇,微溶于乙醚。
硫脲的燃烧
性能较好,但容易受热分解,放出氮、硫的氧化物等毒性气体,具有一定的爆炸危险性。
硫脲的危害主要表现在健康方面,长期接触会对人体造成一定的损害,如出现头痛、嗜睡、无力、面色苍白等症状。
在使用硫脲时,需要注意其危险特性和禁忌物。
硫脲遇明火、高热可燃,与氧化剂能发生强烈反应,应远离火源、热源和氧化剂等物品。
在储存和运输时,应注意防火、防潮、防晒,避免碰撞、摩擦、倾倒等情况发生。
在急救和泄漏处置时,应采取相应的措施,如用肥皂水和清水冲洗皮肤、提起眼睑用流动清水或生理盐水冲洗、迅速脱离现场至空气新鲜处等。
硫脲分解成氢氧根离子

硫脲分解成氢氧根离子
硫脲是一种有机化合物,化学式为CH4N2S。
它是一种白色晶体,具
有吸湿性,并且在空气中稳定。
然而,硫脲在一定条件下可以被分解
成氢氧根离子和二硫化碳。
硫脲分解的反应式可以表示为:CH4N2S + 2OH⁻ → CO2 + H2S + NH3 + S。
该反应是一个化学分解反应,在该反应中,硫脲分子被氢氧根离子攻击,导致分子中的硫-硫键断裂,从而产生二硫化碳和氨。
硫脲的分解产生的二硫化碳在常温常压下是一种无色有毒气体,具有刺激性气味。
氢气硫在这个反应中也被产生,它是一种有毒气体,具有难闻的臭鸡
蛋气味。
硫脲分解的条件包括高温、弱碱性、还原性物质和催化剂。
例如,溶
解硫脲的氢氧化钾溶液可以加速分解的速度。
另外,硫脲也可以通过
酸催化反应来分解,产生硫磺。
硫脲分解反应在工业上有一定的应用。
例如,它可以用于生产高纯度
的硫磺。
此外,硫脲分解反应还可以用于检测银离子、汞离子和银汞
离子等物质,因为它们可以使硫脲在溶液中分解产生沉淀。
总之,硫脲是一种有机化合物,可以在一定条件下分解成氢氧根离子和其他物质。
它的分解反应具有一定的工业应用价值和实验室检测价值。
硫脲 分子量

硫脲分子量
摘要:
1.硫脲的定义和性质
2.硫脲的分子量计算方法
3.硫脲的应用领域
正文:
硫脲是一种有机化合物,其化学式为C4H6N2S,具有刺激性气味。
硫脲的物理性质包括:熔点为172-174℃,沸点为203-206℃,难溶于水,易溶于醇类有机溶剂。
硫脲在工业上具有广泛的应用,主要用于生产硫酸铵、硫酸二甲酯等化学品。
硫脲的分子量计算方法是通过将各元素的原子量相加得到。
硫脲分子中包含4 个碳原子,每个碳原子的原子量为12.01,6 个氢原子,每个氢原子的原子量为1.01,2 个氮原子,每个氮原子的原子量为14.01,以及1 个硫原子,硫原子的原子量为32.06。
因此,硫脲的分子量为:
(12.01×4)+(1.01×6)+(14.01×2)+32.06=120.18。
硫脲在农业领域可以用作肥料,提高农作物的产量和品质。
此外,硫脲还应用于医药、染料、塑料等行业。
在医药领域,硫脲可用于合成抗病毒药物、抗肿瘤药物等。
在染料领域,硫脲可作为染料中间体,用于生产各种染料。
在塑料行业,硫脲可用作硫化剂,提高塑料的韧性和弹性。
综上所述,硫脲作为一种重要的有机化合物,在多个领域发挥着重要作用。
硫脲分子式

硫脲分子式分子式:C6H4 NO3S分子量:114。
外观与性状:白色或淡黄色结晶粉末。
熔点:150 ℃(lit)。
相对密度(水=1):1。
微溶于冷水,在热水中易分解。
溶于乙醇、乙醚、丙酮和碱液。
几乎不溶于冷水。
水溶液呈酸性。
稳定性:稳定。
危险标记6(hazardous):腐蚀性物质。
主要用途:用作合成纤维的助染剂、橡胶硫化促进剂等。
用于合成纤维。
贮存方法:应贮存在阴凉干燥处。
防潮。
包装规格:双层编织袋内衬聚乙烯塑料袋或牛皮纸袋外麻袋。
每袋净重25kg。
产品应用领域:作为合成纤维的助染剂,纺织工业用作染色后处理剂,也可以做气体和浮选剂。
用于电镀工业,能显著提高电流效率,并可防止铜离子的流失而发生电解液分层现象,是电镀铜及铜合金的理想试剂;有机合成用作促进剂;农药制造中作杀虫剂的活性成分。
1。
物理性质2。
化学性质3。
典型物质1。
物理性质项目号状态饱和程度相对密度闪点熔点溶解性水0~≤0.0≤0.5性状无色结晶固体,密度1.12,熔点145 ℃,沸点228 ℃,微溶于水,溶于醇、乙醚、丙酮和碱液,不溶于冷水,能随水蒸气挥发,具有较强的还原性,遇硫化物生成氨基硫脲。
本品在高温时分解,但对皮肤和粘膜有刺激性,高浓度有毒,对人畜有害。
4。
毒性1。
急性毒性LD50鼠经口1000mg/kg。
2。
亚急性和慢性毒性LC50无资料。
3。
致突变性DNA修复试验:微生物致突变试验:沙门菌属引起的大肠杆菌氨化酶基因突变试验:哺乳动物体细胞遗传损伤试验:细菌转化试验:姐妹染色单体交换试验:致癌性2。
致癌性IETFT33为阳性。
4。
其他大鼠经口最低中毒剂量为3200mg/kg。
5。
生态毒性LCL(96h,14d)0.061-0.160mg/L,除草剂大鼠急性经口LD50)小于700mg/kg。
- 1 -。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
闪点(℃):无意义
爆炸下限[%(V/V)]:无资料
爆炸上限[%(V/V)]:无资料
引燃温度(℃):无资料
有害燃烧产物:氧化氮、氧化硫。
禁忌物
禁配物:强氧化剂、强酸。
危险特性
危险特征:遇明火、高热可燃。受热分解,放出氮、硫的氧化物等毒性气体。与氧化剂能发生强烈反应。
灭火方法
灭火方法:采用水、泡沫、二氧化碳、砂土灭火。
相对密度(水=1):1.41
相对密度(空气=1):无资料
燃烧热(KJ/mol):无资料
沸点:分解℃
溶解性:溶于冷水、乙醇,微溶于乙醚。
临界温度:无资料
饱和蒸气压(kPa):无资料
毒性及健康危害
侵入途径
侵入途径:吸入、食入、经皮吸收。
急性毒性:LD50无资料
LC50无资料
健康危害
健康危害:一次作用时毒性小,反复作用时可抑制甲状腺和造血器官的机能。可引起变态反应。可经皮肤吸收。本品粉尘对眼和上呼吸道有刺激性,吸入后引起咳嗽、胸部不适。口服刺激胃肠道。慢性影响:长期接触出现头痛、嗜睡、无力、面色苍白、面部虚肿、基础代谢降低、血压下降、脉搏变慢、白细胞减少等。对皮肤有损害,出现皮肤瘙痒、手掌出汗、皮炎、皲裂等。
环境资料
该物质对环境有危害,由于热分解而形成的硫化物和氮氧化物,对大气会造成污染。
废弃处理
处置前应参阅国家和地方有关法规。建议用焚烧法处置。焚烧炉排出的气体要通过洗涤器除去。
急救措施
皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。
食入:饮足量温水,催吐。就医。
防护措施
密闭操作,局部排风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,戴橡胶手套。远离火种、热源,工作场所严禁吸烟。使用防爆型的通风系统和设备。避免产生粉尘。避免与氧化剂、酸类接触。搬运时要轻装轻卸,防止包装及容器损坏。配备相应品种和数量的消防器材及泄漏应急处理设备。倒空的容器可能残留有害物。
硫脲的理化特性
标识
中文名:硫脲
分子式:CH4N2S
分子量:76.12
英文名: thiourea
UN编号:无资料
CAS号:62-56-6
危规号:61821
危险性类别:
生殖毒性,类别2
危害水生环境-急性危害,类别2
危害水与性状
白色光亮苦味晶体。
熔点:176~178 ℃
泄漏应急处理
隔离泄漏污染区,限制出入。切断火源。建议应急处理人员戴防尘面具(全面罩),穿一般作业工作服。不要直接接触泄漏物。小量泄漏:用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏:收集回收或运至废物处理场所处置。
储运注意事项
储存于阴凉、通风的库房。远离火种、热源。包装密封。应与氧化剂、酸类、食用化学品分开存放,切忌混储。配备相应品种和数量的消防器材。储区应备有合适的材料收容泄漏物。
