2019届高三第一次理综化学部分
(精校版)2019年全国卷Ⅰ理综化学高考试题文档版(含答案)_最新修正版

绝密★启用前2019年普通高等学校招生全国统一考试理科综合能力测试化学注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu 64一、选择题:本题共13个小题,每小题6分。
共78分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点8.关于化合物2−苯基丙烯(),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
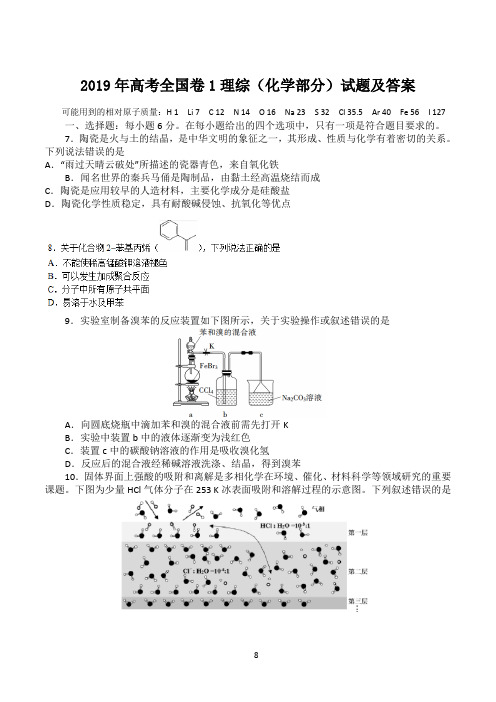
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)C.冰表面第三层中,冰的氢键网络结构保持不变D.冰表面各层之间,均存在可逆反应HCl H++Cl−11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的K a1=1.1×10−3 ,K a2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
2019高考全国卷1理综(化学部分)试题及答案复习过程

2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H 2+2MV2+2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。
2019年高考全国卷1理综(化学部分)试题及答案
2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H 2+2MV2+2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z 核外最外层电子数是X核外电子数的一半。
2019年高考全国卷1理综(化学部分)试题与答案

2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的兵马俑是制品,由黏土经高温烧结而成C.瓷是应用较早的人造材料,主要化学成分是硅酸盐D.瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H2+2MV2+2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。
2019年高考全国卷1理综(化学部分)试题及答案(2021年整理精品文档)

2019年高考全国卷1理综(化学部分)试题及答案(可编辑修改word版) 编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(2019年高考全国卷1理综(化学部分)试题及答案(可编辑修改word版))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为2019年高考全国卷1理综(化学部分)试题及答案(可编辑修改word版)的全部内容。
2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35。
5 Ar 40 Fe56 I 127一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题.下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1。
(完整word版)2019年高考全国卷1理综(化学部分)试题及答案,推荐文档

2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H 2+2MV2+2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。
2019年高考全国卷1理综(化学部分)试题及解析讲课稿

2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H 2+2MV2+2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。
(完整版)2019年高考全国卷1理综(化学部分)试题及答案(可编辑修改word版)

2019 年高考全国卷 1 理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127一、选择题:每小题 6 分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b 中的液体逐渐变为浅红色C.装置c 中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl 气体分子在253 K 冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH 溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A 的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b 点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b 点的混合溶液pH=7D.c 点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H2+2MV2+ 2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z 为同一短周期元素,Z 核外最外层电子数是X 核外电子数的一半。
高考真题-2019年全国理综1卷化学部分及参考答案

C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)
6.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
C.分子中所有原子共平面
D.易溶于水及甲苯
3.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是
A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中的碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
4.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图为少量HCl气体分子在253K冰表面吸附和溶解过程的示意图。下列叙述错误的是
A. B. C. D.
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是__________、__________。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是__________,其中与乙二胺形成的化合物稳定性相对较高的是__________(填“Mg2+”或“Cu2+”)。
(3)步骤③中选用足量的H2O2,理由是_________________。分批加入H2O2,同时为了_________________,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________,经干燥得到硫酸铁铵晶体样品。
(完整word版)2019年高考全国卷1理综(化学部分)试题及解析

2019年高考全国卷1理综(化学部分)试题及答案可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Ar 40 Fe 56 I 127 一、选择题:每小题6分。
在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸氢钾H2A的Ka1=1.1×10−3,Ka2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
下列叙述错误的是A.混合溶液的导电能力与离子浓度和种类有关B.Na+与A2−的导电能力之和大于HA−的C.b点的混合溶液pH=7D.c点的混合溶液中,c(Na+)>c(K+)>c(OH−)12.利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。
下列说法错误的是A.相比现有工业合成氨,该方法条件温和,同时还可提供电能B.阴极区,在氢化酶作用下发生反应H 2+2MV2+2H++2MV+C.正极区,固氮酶为催化剂,N2发生还原反应生成NH3D.电池工作时质子通过交换膜由负极区向正极区移动13.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数是X核外电子数的一半。
2019年全国卷1Ⅰ理综化学高考真题(含答案)-word版可编辑

绝密★启用前2019年普通高等学校招生全国统一考试理科综合能力测试化学注意事项:1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案标号。
回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu 64一、选择题:本题共13个小题,每小题6分。
共78分,在每小题给出的四个选项中,只有一项是符合题目要求的。
7.陶瓷是火与土的结晶,是中华文明的象征之一,其形成、性质与化学有着密切的关系。
下列说法错误的是A.“雨过天晴云破处”所描述的瓷器青色,来自氧化铁B.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成C.陶瓷是应用较早的人造材料,主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有耐酸碱侵蚀、抗氧化等优点8.关于化合物2−苯基丙烯(),下列说法正确的是A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯9.实验室制备溴苯的反应装置如下图所示,关于实验操作或叙述错误的是A.向圆底烧瓶中滴加苯和溴的混合液前需先打开KB.实验中装置b中的液体逐渐变为浅红色C.装置c中的碳酸钠溶液的作用是吸收溴化氢D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯10.固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。
下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。
下列叙述错误的是A.冰表面第一层中,HCl以分子形式存在B.冰表面第二层中,H+浓度为5×10−3 mol·L−1(设冰的密度为0.9 g·cm−3)C.冰表面第三层中,冰的氢键网络结构保持不变D.冰表面各层之间,均存在可逆反应HCl垐?噲?H++Cl−11.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸H2A的K a1=1.1×10−3 ,K a2=3.9×10−6)溶液,混合溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学试题出题:曾小惠审核:赖英7.2018年,平昌冬奥会上“北京8分钟”以充满中国智慧和中国科技的表演惊艳世界,下列有关说法中不正确的是()A.熊猫木偶的材质采用铝合金和碳纤维,可以减轻重量B.演出服中的石墨烯是一种新型的纳米材料C.低温环境会影响机器人的电池性能D.机器人芯片的主要成分为SiO28、设N A为阿伏加德罗常数的值。
下列说法不正确的是()A.25℃,1L pH=13 的NaOH 溶液中含有OH-的数目为0.1N AB.由1molCH3COONa 和少量CH3COOH 形成的中性溶液中,CH3COO-数目为N A个C.0.1 mol苯乙烯中含有碳碳双键的数目为0.4N AD.1mol 乙酸(忽略挥发损失) 与足量的C2H518OH在浓硫酸作用下加热,充分反应可生成N A 个CH3CO18OC2H5分子9. 有机化学在日常生活应用广泛,下列有关说法正确的是()A. 甲苯和Cl2光照下的反应与乙醇和乙酸的反应属于同一类型的反应B. 苯乙烯分子中的所有原子一定都处于同一个平面C. 矿物油和植物油都是有机物,均不能使溴水褪色D. 麦芽糖的水解产物有两种,且互为同分异构体10、某手机电池采用了石墨烯电池,可充电5分钟,通话2小时。
一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意图如图。
下列有关该电池说法不正确的是()A.金属锂是所有金属中比能量最高的电极材料B.充电时A电极为阴极,发生还原反应C充电时B 电极的反应: Li2S8-2e-=2Li++S8D.手机使用时电子从A 电极经过手机电路版流向B电极,再经过电池电解质流回A电极11. 常温下,二氯化二硫(S2Cl2)为橙黄色液体,遇水易水解,工业上用于橡胶的硫化。
某学习小组合成S2Cl2 的实验装置如图所示。
下列说法正确的是()A. 实验室可以用盐酸酸化高锰酸钾溶液B. C中所盛试剂为饱和氯化钠溶液C. 实验时需先点燃E处的酒精灯D. G中可收集到纯净的产品12.常温条件下,下列各组比值为1∶2的是()A.0.1 mol/L Na2CO3溶液,c(CO32-)与c(Na+)之比B.0.1 mol/L与0.2 mol/L 醋酸溶液,c(H+)之比C.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比D.pH=10的Ba(OH)2溶液与氨水,溶质的物质的量浓度之比13. 电解质溶液的电导率越大,导电能力越强。
用0.100 mol·L-1的NaOH溶液滴定10.00 mL浓度均为0.100 mol·L-1的盐酸和CH3COOH溶液。
利用传感器测得滴定过程中溶液的电导率如图所示。
下列说法正确的是A. 曲线②代表滴定CH3COOH溶液的曲线B. A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1C. 在相同温度下,A、B、C三点溶液中水的电离程度: A<C<BD. D点溶液中:c(Cl-)+ 2c(H+)=2c(OH-)26.(14分)某强酸性无色溶液中可能含下表离子中的若干种离子。
【实验I】:取少量该试液进行如下实验。
【实验Ⅱ】:为了进一步确定该溶液的组成,取100mL原溶液,向该溶液中滴加1 mol•L-l 的NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
回答下列问题:(1)不进行实验就可以推断出,上表中的离子一定不存在有。
(2)通过实验I可以确定该溶液中一定存在的阴离子是;沉淀Z的化学式为;检验气体X的方法是;。
(3)写出实验Ⅱ的图象中BC段对应的离子方程式。
(4)A点对应的固体质量为。
(5)通过上述信息,推算该溶液中阴离子的浓度为。
27、(14分)某学习小组在实验室中利用下图装置(夹持装置略去) 测定某铁硫化物(Fe x S y)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。
实验步骤:步骤I如图连接装置,检查装置气密性,装入药品;步骤II旋开滴液漏斗活塞与旋塞,并点燃酒精喷灯;步骤III当硬质玻璃管中固体质量不再改变时,停止加热,继续向烧瓶中滴水一段时间步骤IV实验结束后,将D中所得溶液加水配制成250 mL溶液;……请回答:(1)步骤III中,停止加热后还需继续向烧瓶中滴水一段时间,其目的为_____________。
(2)步骤IV 中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有______________。
(3)取25.00mL 步骤IV 中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。
则Fe x S y的化学式为_________。
(4)有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。
你认为此方案____(填“是”或“否”)合理,原因为________(5)反应后D装置所得溶液中除含有Na2SO4外,还可能含有Na2SO3。
现用滴定法测定溶液中Fe x S y的含量。
可供选择的试剂:①0.1000 mol/LKMnO4酸性溶液;②0.1000 mol/LH2O2溶液;③0.1000 mol/LKI淀粉溶液;④0.1000 mol/LBaCl2溶液;⑤0.1000 mol/LHCl溶液。
①所选试剂应装在_____(填“酸式”或“碱式”)滴定管中。
②所利用的反应原理为___________________________________(用离子方程式表示)。
28.(14分) 高氯酸铜易溶于水,在130℃时会发生分解反应是一种燃烧催化剂,以食盐等为原料制备高氯酸铜[Cu(ClC4)2·6H2O)]的一种工艺流程如下:回答下列问题:(1)发生“电解I”时所用的交换膜是 (填“阳离子交换膜”或“阴离子交换膜”)。
(2)歧化反应是同一种物质中同种元素自身的氧化还原反应,已知上述工艺流程中“歧化反应”的产物之一为NaClO3。
“歧化反应”的化学方程式为(3)“电解I”的阳极产物为 (填离子符号)。
(4)操作a的名称是,该流程中可循环利用的物质是 (填化学式)。
(5)用该工艺流程制备高氯酸铜时,若起始时NaCl的质量为a t。
最终制得的Cu(ClO4)2·6H2O为bt,则产率为 (用含a、b的代数式表示)。
(6)某温度下,高氯酸铜按A、B两种方式同时分解,分解过程中铜的化合价不发生改变。
A方式为Cu(ClO4)2△CuCl2+4O2↑,若4 mol高氯酸铜在该温度下按A、B各占50%的方式完全分解,且A、B两种方式转移的电子数之比为8:7,则B方式为(用化学方程式表示)。
35.(16分)工业废气、汽车尾气排放出的NO x、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
Ⅰ.NO x的消除。
汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g) △H。
(1)已知:CO燃烧热的△H1=-283.0kJ·mol-l,N2(g)+O2(g) 2NO(g)△H2=+180.5kJ·mol-1,则△H=____________。
(2)某研究小组探究催化剂对CO、NO转化的影响。
将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。
①以下说法正确的是__________________(填字母)。
A.两种催化剂均能降低活化能,但△H不变B.相同条件下,改变压强对脱氮率没有影响C.曲线Ⅱ中的催化剂适用于450℃左右脱氮D.曲线Ⅱ中催化剂脱氮率比曲线I中的高②若低于200℃,图中曲线I脱氮率随温度升高而变化不大的主要原因为___________;判断a点是否为对应温度下的平衡脱氮率,并说明其理由:____________。
Ⅱ.SO2的综合利用(3)某研究小组对反应NO2+SO2SO3+NO △H<0进行相关实验探究。
在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。
部分实验结果如下图所示。
①如果将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是____________。
②图中C、D两点对应的实验温度分别为T C和T D,通过计算判断:T C__________T D填“>”、“=”或“<”)。
(4)已知25C时,NH3·H2O的K b=1.8×10-5,H2SO3的K a1=1.3×10-2,Ka=6.2×10-8。
若氨水的浓度为2.0mol·L-1,溶液中的c(OHˉ)= _________mol·L-1;将SO2通入该氨水中,当溶液呈中性时,溶液中的=__________。
答题卷26.(14分)(1)(2)(3)(4)(5)27.(14分)(1)(2)(3)(4)(5)①②28.(14分)(1)(2)(3)(4)(5)(6)35.(16分)(1)(2)①②(3)①②(4)答案7-13 DDADBCD26、(14分)(1)Fe2+、SiO32-、MnO4-、SO32-(2分,见错无分)(2)NO3-(2分)Mg(OH)2(2分)将湿润的红色石蕊试纸靠近气体X,试纸变蓝(或其他合理答案,2分)(3)Al(OH)3+OH-==AlO2-+2H2O(2分)(4)0.136g(2分,掉单位给1分)(5)0.08mol • L-l(2分,掉单位给1分)27.(14分)(1)继续生成O2,驱赶装置内残留的SO2,使生成的SO2全部被NaOH溶液吸收(2分)(2) 250 mL容量瓶、胶头滴管(2分)(3)FeS2(2分)(4) 否(2分) ;空气中的CO2和水蒸气可能使干燥管增重(2分)(5)①酸式(2分);②2MnO4-+5SO32-+6H+=5SO42-+2Mn2++3H2O(2分,反应物、产物正确1分,配平1分)28.(14分)(1)阳离子交换膜(2分)(2)①3Na2CO3+3Cl2=5NaCl+NaCl+3CO2(2分)(3)ClO4-(2分)(4)蒸发浓缩(2分) NaCl(2分)(5)702b/371a×100% (2分)(6)2Cu(C1O4)2△2CuO+7O2↑+2C12↑(2分)35. (16分)(1). -746.5kJ/mol(2). A、C温度较低时,催化剂的活性偏低不是平衡脱氮率。
因为该反应为放热反应,根据线II可知,a点对温度的平衡脱氮率应该更高。
