初中化学相对原子质量表
相对原子质量表大全
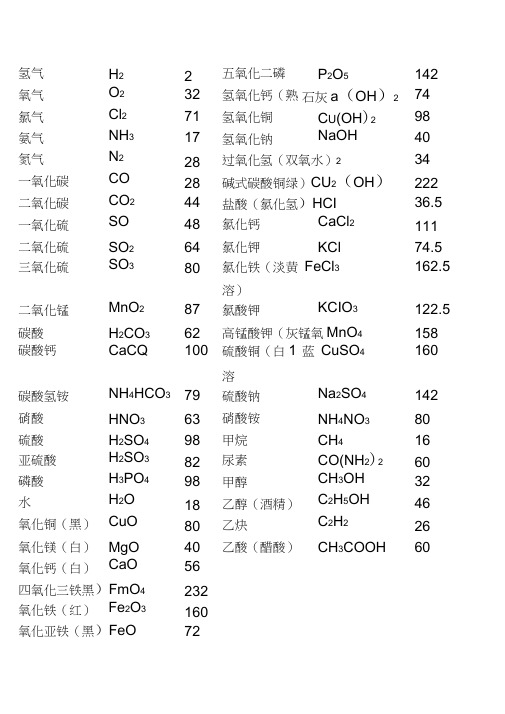
氢气H2 2 五氧化二磷P2O5 142 氧气O2 32 氢氧化钙(熟石灰a(OH)2 74 氯气Cl2 71 氢氧化铜C U(OH)2 98 氨气NH3 17 氢氧化钠NaOH 40 氮气N2 28 过氧化氢(双氧水)2 34一氧化碳CO 28 碱式碳酸铜绿)CU2(OH)CO 222二氧化碳CO2 44 盐酸(氯化氢)HCI 36.5 一氧化硫SO 48 氯化钙CaCl2 111 二氧化硫SO2 64 氯化钾KCl 74.5 三氧化硫SO3 80 氯化铁(淡黄FeCl3 162.5溶)二氧化锰MnO2 87 氯酸钾KCIO3 122.5 碳酸H2CO3 62 高锰酸钾(灰锰氧MnO4 158 碳酸钙CaCQ 100 硫酸铜(白1 蓝CuSO4 160溶碳酸氢铵NH4HCO3 79 硫酸钠Na2SO4 142 硝酸HNO3 63 硝酸铵NH4NO3 80硫酸H2SO4 98 甲烷CH4 16亚硫酸H2SO3 82 尿素CO(NH2)2 60磷酸H3PO4 98 甲醇CH3OH 32水H2O 18 乙醇(酒精)C2H5OH 46氧化铜(黑)CuO 80 乙炔C2H2 26氧化镁(白)MgO 40 乙酸(醋酸)CH3COOH 60氧化钙(白)CaO 56四氧化三铁黑)FmO4 232氧化铁(红)Fe2O3 160氧化亚铁(黑)FeO 72硫酸亚(淡绿)eSO 152硫酸锌(白无)ZnSO4 161初中化学常用计算公式一.常用计算公式:(1)相对原子质量=某元素一个原子的质量/ 一个碳原子质量的1/12(2)设某化合物化学式为AmBn①它的相对分子质量=A的相对原子质量Xm+ B的相对原子质量X②A元素与B元素的质量比=A的相对原子质量X m:B的相对原子质量X n③A元素的质量分数3 =A的相对原子质量X m /AmBn 的相对分子质量(3)混合物中含某物质的质量分数(纯度) =纯物质的质量/混合物的总质量x 100%(4)标准状况下气体密度(g/L)=气体质量(g)/气体体积(L)(5)纯度=纯物质的质量/混合物的总质量X100%纯物质的质量/(纯物质的质量+杂质的质量)X100%=1-杂质的质量分数(6)溶质的质量分数=溶质质量/溶液质量X100% = 溶质质量/(溶质质量+溶剂质量)X00%(7)溶液的稀释与浓缩M浓x a%浓=M稀X b%稀=(M浓+增加的溶剂质量)x b%稀(8)相对溶质不同质量分数的两种溶液混合M浓X a%浓+M稀x b%稀=(M浓+M稀)>C%(9)溶液中溶质的质量=溶液的质量X容液中溶质的质量分数 =溶液的体积X容液的密度素名称兀素符号相对原子质量核电荷数兀〕1 氢H 12 氦He 46 碳 C 127 氮N 148 氧O 169 氟 F 1910 氖Ne 2011 钠Na 2312 镁Mg 2413 铝Al 2714 硅Si 2815 磷P 3116 硫S 3217 氯Cl 35.518 氩Ar 4019 钾K 3920 钙Ca 4025 锰Mn 5526 铁Fe 5629 铜Cu 64.5 (可写64或65)30 锌Zn 6547 银Ag 10853 碘I 127 56 钡Ba 13778 铂Pt 19579 金Au 19780 汞Hg 201。
化学元素相对原子质量表

化学元素相对原子质量表相对原子质量是一个无单位的数值,定义为元素原子质量与1/12碳-12原子质量的比值。
碳-12被定义为相对原子质量为12的标准,所有其他元素的相对原子质量都是相对于它来确定的。
相对原子质量表上的数值一般都是近似值,因为元素的原子质量因同位素的存在而有所不同。
-氢(H):1.008-氦(He):4.0026-锂(Li):6.94-铍(Be):9.0122-碳(C):12.01-氮(N):14.01-氧(O):16.00-氟(F):19.00-钠(Na):22.99-镁(Mg):24.31-铝(Al):26.98-硅(Si):28.09-磷(P):30.97-硫(S):32.07-氯(Cl):35.45-钾(K):39.10-钙(Ca):40.08-锶(Sr):87.62-钒(V):50.94-铬(Cr):52.00以上仅列出了较为常见的元素的相对原子质量,完整的相对原子质量表包括所有已发现的元素和它们的各种同位素。
相对原子质量表的编制需要密切的实验测量和科学分析,以确保数值的准确性和可靠性。
化学元素相对原子质量在化学和物理研究中具有广泛的应用。
它可以用于计算化学反应中的物质的摩尔质量、摩尔比例和摩尔质量的百分比。
相对原子质量还可以用于计算物质的化学计量关系,例如质量与物质的摩尔量之间的转换。
总结起来,化学元素相对原子质量表是一个重要的化学参考资料,它列出了化学元素的相对原子质量。
这个表格在化学研究和实验中有着广泛的应用,用于计算物质的摩尔质量、摩尔比例和摩尔质量的百分比,以及化学计量关系的计算。
相对原子质量表的编制离不开准确的实验测量和科学分析。
同时,它也是化学元素周期表的重要组成部分,对元素的组织和分类起着重要的作用。
相对原子质量表大全

氢气H2 2 五氧化二磷P2O5142 氧气O232 氢氧化钙(熟石灰)Ca(OH)274氯气Cl271 氢氧化铜Cu(OH)298氨气NH317 氢氧化钠NaOH 40氮气N228 过氧化氢(双氧水)H2O234222 一氧化碳CO 28 碱式碳酸铜(绿)Cu2(OH)2CO3二氧化碳CO244 盐酸(氯化氢)HCl 36.5 一氧化硫SO 48 氯化钙CaCl2111 二氧化硫SO264 氯化钾KCl 74.5FeCl3162.5 三氧化硫SO380 氯化铁(淡黄溶)二氧化锰MnO287 氯酸钾KClO3122.5 碳酸H2CO362 高锰酸钾(灰锰氧)KMnO4158CuSO4160 碳酸钙CaCO3100 硫酸铜(白固蓝溶)碳酸氢铵NH4HCO379 硫酸钠Na2SO4142 硝酸HNO363 硝酸铵NH4NO380硫酸H2SO498 甲烷CH416亚硫酸H2SO382 尿素CO(NH2)260磷酸H3PO498 甲醇CH3OH 32水H2O 18 乙醇(酒精)C2H5OH 46氧化铜(黑)CuO 80 乙炔C2H226 氧化镁(白)MgO 40 乙酸(醋酸)CH3COOH 60 氧化钙(白)CaO 56四氧化三铁(黑)Fe3O4232氧化铁(红)Fe2O3160氧化亚铁(黑)FeO 72硫酸亚铁(淡绿)FeSO4152硫酸锌(白/无)ZnSO4161初中化学常用计算公式一. 常用计算公式:(1)相对原子质量= 某元素一个原子的质量/ 一个碳原子质量的1/12(2)设某化合物化学式为AmBn①它的相对分子质量=A的相对原子质量×m+B的相对原子质量×n②A元素与B元素的质量比=A的相对原子质量×m:B的相对原子质量×n③A元素的质量分数ω=A的相对原子质量×m /AmBn 的相对分子质量(3)混合物中含某物质的质量分数(纯度)=纯物质的质量/混合物的总质量× 100%(4)标准状况下气体密度(g/L)=气体质量(g)/气体体积(L)(5)纯度=纯物质的质量/混合物的总质量× 100% =纯物质的质量/(纯物质的质量+杂质的质量) ×100%=1- 杂质的质量分数(6)溶质的质量分数=溶质质量/溶液质量× 100% =溶质质量/(溶质质量+溶剂质量) × 100%(7)溶液的稀释与浓缩M浓× a%浓=M稀× b%稀=(M浓+增加的溶剂质量) × b%稀(8)相对溶质不同质量分数的两种溶液混合M浓× a%浓+M稀× b%稀=(M浓+M稀) × c%(9)溶液中溶质的质量=溶液的质量×溶液中溶质的质量分数=溶液的体积×溶液的密度核电荷数元素名称元素符号相对原子质量1 氢H 12 氦He 46 碳 C 127 氮N 148 氧O 169 氟 F 1910 氖Ne 2011 钠Na 2312 镁Mg 2413 铝Al 2714 硅Si 2815 磷P 3116 硫S 3217 氯Cl 35.518 氩Ar 4019 钾K 3920 钙Ca 4025 锰Mn 5526 铁Fe 5629 铜Cu 64.5(可写64或65)30 锌Zn 6547 银Ag 10853 碘I 12756 钡Ba 13778 铂Pt 19579 金Au 19780 汞Hg 201THANKS !!!致力为企业和个人提供合同协议,策划案计划书,学习课件等等打造全网一站式需求欢迎您的下载,资料仅供参考。
初中相对原子质量表

初中相对原子质量表“原子质量”是一个重要的概念,它提供了一种更准确的方式来表示原子的质量。
原子的质量是指原子的原子核中的质子(正电子)和中子(中子)之和,它表示为“千克/摩尔”(kg/mol)或“克/质量数”(g/mol)。
原子质量可以用来衡量元素的含量。
为了更好地了解世界上的物质,就需要一个表来具体表示每种元素的原子质量。
②中相对原子质量表:初中相对原子质量表(Atomic Mass Relative to Carbon-12 Table)是一种表格,其中包含了每个元素的相对原子质量。
该表通常以碳-12(C-12)为基准,将每个原子的质量都进行了比较,并以该元素的原子质量来表示质量。
这样一来,就可以更容易地从表中找到元素的原子质量。
以下是常见元素的初中相对原子质量表:H: 1.008He: 4.003Li: 6.94Be: 9.01B: 10.81C: 12.01N: 14.01O: 16.00F: 19.00Ne: 20.18Mg: 24.31 Al: 26.98 Si: 28.09 P: 30.97 S: 32.07 Cl: 35.45 Ar: 39.95 K: 39.10 Ca: 40.08 Sc: 44.96 Ti: 47.87 V: 50.94 Cr: 52.00 Mn: 54.94 Fe: 55.85 Co: 58.93 Ni: 58.69 Cu: 63.55 Zn: 65.38 Ga: 69.72 Ge: 72.61Se: 78.96 Br: 79.90 Kr: 83.80 Rb: 85.47 Sr: 87.62 Y: 88.91 Zr: 91.22 Nb: 92.91 Mo: 95.94 Tc: 98.00 Ru: 101.07 Rh: 102.91 Pd: 106.42 Ag: 107.87 Cd: 112.41 In: 114.82 Sn: 118.71 Sb: 121.76 Te: 127.60 I: 126.90 Xe: 131.29Ba: 137.33 La: 138.91 Ce: 140.12 Pr: 140.91 Nd: 144.24 Pm: 145.00 Sm: 150.36 Eu: 152.00 Gd: 157.25 Tb: 158.93 Dy: 162.50 Ho: 164.93 Er: 167.26 Tm: 168.93 Yb: 173.04 Lu: 174.97 Hf: 178.49 Ta:180.95 W: 183.84 Re: 186.21 Os: 190.23Pt: 195.08 Au: 196.97 Hg: 200.59 Tl: 204.38 Pb: 207.2 Bi: 208.98 Po: 209.00 At: 210.00 Rn: 220.00 Fr: 223.00 Ra: 226.00 Ac: 227.00 Th: 232.04 Pa: 231.04 U: 238.03 Np: 237.00 Pu: 244.00 Am: 243.00 Cm: 247.00 Bk: 247.00 Cf: 251.00Fm: 257.00Md: 258.00No: 259.00③途:初中相对原子质量表的主要用途是可以精确地计算元素的质量。
化学元素的相对原子质量表

化学元素的相对原子质量表以下是常见元素的相对原子质量表:1. 氢(H)、相对原子质量为1.008。
它是表中最轻的元素,存在于宇宙中,并在水和有机物的化合物中广泛存在。
2. 氦(He)、相对原子质量为4.0026。
它是第二轻的元素,存在于宇宙中,也用作气体焊接中的保护气体。
3. 锂(Li)、相对原子质量为6.94。
它是地壳中的轻量金属,在一些用于高能量密度电池的应用中有用。
4. 铍(Be)、相对原子质量为9.0122。
它是稀有金属,具有高耐腐蚀性和高熔点。
5. 碳(C)、相对原子质量为12.011。
它是生命的基本元素,存在于所有有机物中,包括纤维素和蛋白质。
6. 氮(N)、相对原子质量为14.007。
它是空气的主要成分之一,在植物和动物体内作为重要化学分子的组成部分存在。
7. 氧(O)、相对原子质量为15.999。
它是空气中的第一大成分,是细胞呼吸过程中必要的气体。
8. 氟(F)、相对原子质量为18.998。
它是最加电负性的单质元素之一,在石化行业中用作生产高分子材料的催化剂。
9. 氖(Ne)、相对原子质量为20.18。
它是稀有气体,广泛使用于气体放电灯和激光技术中。
10. 钠(Na)、相对原子质量为22.99。
它是一个常见的金属元素,在化学反应和体内电信号传递中扮演重要角色。
11. 镁(Mg)、相对原子质量为24.31。
它是地球上最常见的金属元素之一,用于制造铝合金、火箭燃料等。
12. 铝(Al)、相对原子质量为26.98。
它是重要的结构金属,用于建筑、汽车和飞机等工业领域。
13. 硅(Si)、相对原子质量为28.09。
它是地壳中第二大的元素,用于制造电子器件、玻璃、水泥等。
14. 磷(P)、相对原子质量为30.97。
它在生物体内作为DNA和ATP等分子的组成部分,也用于农业和生产肥料。
15. 硫(S)、相对原子质量为32.06。
它是空气中存在的第三大元素,广泛用于制造硫酸、橡胶等工业产品。
16. 氯(Cl)、相对原子质量为35.45。
九年级相对原子质量表相对原子质量特点

九年级相对原子质量表相对原子质量特点相对原子质量是一种计算原子质量的方式,由于原子的实际质量很小,如果人们用它们的实际质量来计算的话那就非常的麻烦,例如一个氢原子的实际质量为1.674×10⁻²⁷千克,一个氧原子的质量为2.657×10⁻²⁶千克。
一个碳-12原子的质量为1.993×10⁻²⁶千克。
九年级相对原子质量表银、Ag、108;氖、Ne、20;氦、He、4;金、Au、197;汞、Hg、201;钡、Ba、137;碘、I、127;铂、Pt、195;锌、Zn、65;铜、Cu、64;铁、Fe、56;钙、Ca、40;氩、Ar、40;钾、K、39;氯、Cl、35.5;硫、S、32;磷、P、31;锰、Mn、55;硅、Si、28;铝、Al、27;镁、Mg、24;钠、Na、23;氟、F、19;氧、O、16;氮、N、14;碳、C、12;氢、H、1。
相对原子质量特点当我们计算一个水分子质量是多少时,就会发现计算起来极不方便。
若是计算其它更复杂的分子质量时那就更麻烦了。
因此国际上规定采用相对原子质量和相对分子质量来表示原子、分子的质量关系。
相对分子质量在数值上等于摩尔质量,但单位不同。
相对分子质量的单位是“1” ,而摩尔质量的单位是g/mol。
相对原子质量定义区别相对原子质量与原子的质量区别原子的质量是原子的实际存在的物质的多少,是实际质量或称为真实质量,相对原子质量是以C原子质量的1/12为标准来表示物质质量多少的相对质量.原子质量的单位是kg,相对原子质量的单位是1.原子的质量主要集中在原子核上.构成原子的三种粒子中,1个质子和1个中子的质量跟相对原子质量的标准(即一个碳12原子质量的1/12)相比,均约等于1,电子的质量很小,可以忽略不计,故原子的质量主要集中在质子和中子(即原子核)上,因此:相对原子质量≈质子数+中子数。
化学中相对原子质量表

化学中相对原子质量表原子是自然界最小的粒子,是物质的最基本构成单位,由原子组成的物质称为元素,也称物质的基本粒子,构成这些物质的原子个数是不同的,由此形成了化学中的相对原子质量表。
化学学科的相对原子质量表是根据每种原子的相对原子质量来编制的,它是一个按照元素原子质量从小到大排列的一个表格,旨在为化学家和物理学家提供一个基本的参考表,用于比较和计算物质的质量。
原子质量表里列出的原子质量均为相对质量,指的是把1/12质量单位的碳12原子作为基准,其他元素的原子质量都相对于碳12原子而言来计算。
相对原子质量表共包含18种元素,分别是氢、锂、铷、铪、氦、氖、氘、氚、钠、镁、铝、锶、硼、磷、硅、氧、氟、氡。
排列顺序依次为:氢(1.0079)、锂(6.941)、铷(9.0122)、铪(10.811)、氦(18.998)、氖(20.179)、氘(22.989)、氚(24.305)、钠(22.989)、镁(24.305)、铝(26.98)、锶(28.086)、硼(30.974)、磷(32.066)、硅(28.086)、氧(15.999)、氟(18.998)、氡(32.066)。
碳12原子的相对原子质量为12,因为它具有安定的核态,由于碳12具有6个质子和6个中子,所以它的原子质量就是6个质子的质量和6个中子的质量之和,即相对原子质量等于12。
而其它元素的原子质量就是相对于碳12原子而言,根据其原子核中质子数和中子数来计算出来的。
总而言之,相对原子质量表是化学家和物理学家研究原子质量的基础,它是一个根据每种原子的相对原子质量来编制的参考表,它共包含18种元素,排列顺序依次为:氢、锂、铷、铪、氦、氖、氘、氚、钠、镁、铝、锶、硼、磷、硅、氧、氟、氡,碳12原子的相对原子质量为12,而其它元素的原子质量就是相对于碳12原子而言,根据其原子核中质子数和中子数来计算出来的。
虽然原子质量表中的每个元素的原子质量都是一样的,但是它们的物理性质仍然不尽相同,只有进一步研究,才能够更深入地了解它们之间的区别。
相对原子质量表大全

H2 2 五氧化二磷 P2O5氧气O2 32 氢氧化钙(熟石灰Ca(OH))2氯气Cl 2 71 氢氧化铜Cu(OH)2氨气NH3 17 氢氧化钠NaOH氮气N 28 过氧化氢(双氧水HO)2 28 2 2一氧化碳CO 碱式碳酸铜(绿)Cu(OH) COCO 44 2 2 3 二氧化碳盐酸(氯化氢)HCl2 48 CaCl一氧化硫SO 氯化钙SO 64 KCl 2二氧化硫氯化钾2 80 氯化铁(淡黄 FeCl三氧化硫SO33MnO 87 溶)KClO二氧化锰氯酸钾2 623 碳酸HCO 高锰酸钾(灰锰氧KMnO)2 3 100 4 碳酸钙CaCO 硫酸铜(白固蓝 CuSO3 4NHHCO 79 溶)NaSO碳酸氢铵硫酸钠4 3 63 2 4 硝酸HNO 硝酸铵NHNO3 984 3 硫酸HSO 甲烷CH2 4 82 4亚硫酸HSO 尿素CO(NH)22 3 98 2 磷酸HPO 甲醇CHOH3 4 18 3水HO 乙醇(酒精) CHOH2 80 2 5氧化铜(黑) CuO 乙炔CH氧化镁(白) MgO 40 2 2乙酸(醋酸) CHCOOH3氧化钙(白) CaO 56四氧化三(铁黑)Fe O 2323 4氧化铁(红) Fe O 1602 3氧化亚铁(黑)FeO 72硫酸亚铁(淡绿)FeSO 1524硫酸锌(白/无)ZnSO4 161 142 74 98 40 34 222111158 160142 80 16 60 32 46 26 60初中化学常用计算公式一.常用计算公式:(1)相对原子质量 = 某元素一个原子的质量 / 一个碳原子质量的 1/12(2)设某化合物化学式为 AmBn①它的相对分子质量= A 的相对原子质量× m+ B 的相对原子质量×n②A 元素与 B 元素的质量比= A 的相对原子质量× m:B的相对原子质量×n③A 元素的质量分数ω=A 的相对原子质量× m /AmBn 的相对分子质量(3)混淆物中含某物质的质量分数(纯度) =纯物质的质量 / 混淆物的总质量× 100%(4)标准情况下气体密度( g/L )=气体质量 (g)/ 气体体积 (L)(5)纯度 =纯物质的质量 / 混淆物的总质量纯物质的质量 /( 纯物质的质量 +杂质的质量) × 100%= ×100%=1- 杂质的质量分数(6)溶质的质量分数 =溶质质量 / 溶液质量× 100%= 溶质质量 /( 溶质质量 +溶剂质量 ) × 100%(7)溶液的稀释与浓缩M浓× a%浓 =M稀× b%稀 =(M 浓+增添的溶剂质量 ) ×b%稀(8)相对溶质不一样质量分数的两种溶液混淆M浓× a%浓 +M稀× b%稀 =(M 浓+M稀) × c%(9)溶液中溶质的质量=溶液的质量×溶液中溶质的质量分数=溶液的体积×溶液的密度核电荷数元素名称元素符号相对原子质量1氢 H 12氦 He 46碳C127氮N148氧O169氟F1910氖 Ne 2011钠 Na 2312镁 Mg 2413铝 Al 2714硅 Si 2815磷P3116硫S3217氯 Cl18氩 Ar 4019钾K3920钙 Ca 4025锰 Mn 5526铁 Fe 5629铜 Cu(可写64或65)30锌 Zn 6547银 Ag 10853碘I12756钡 Ba 13778铂 Pt 19579金 Au 19780汞 Hg 201。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金
Au
197
镁
Mg
24
锰
Mn
55
汞
Hg
201
元素名称
元素符号
相对原子质量
元素
名称
元素符号
相对原子质量
元素名称
元素符号
相对原子质量
氢
H
1
铝
Al
27
铁
Fe
56
氦
He
4
硅
Si
28
铜
Cu
64
碳
C
12
磷
P
31
锌
Zn
65
氮
N
14
硫
S
32
银
Ag108氧O来自16氯Cl
35.5
碘
I
127
氟
F
19
氩
Ar
40
钡
Ba
137
氖
Ne
20
钾
K
39
铂
Pt
195
钠
Na
23
钙
Ca
40
金
Au
197
镁
Mg
24
锰
Mn
55
汞
Hg
201
THANKS !!!
致力为企业和个人提供合同协议,策划案计划书,学习课件等等
打造全网一站式需求
欢迎您的下载,资料仅供参考
元素名称
元素符号
相对原子质量
元素
名称
元素符号
相对原子质量
元素名称
元素符号
相对原子质量
氢
H
1
铝
Al
27
铁
Fe
56
氦
He
4
硅
Si
28
铜
Cu
64
碳
C
12
磷
P
31
锌
Zn
65
氮
N
14
硫
S
32
银
Ag
108
氧
O
16
氯
Cl
35.5
碘
I
127
氟
F
19
氩
Ar
40
钡
Ba
137
氖
Ne
20
钾
K
39
铂
Pt
195
钠
Na
23
钙
Ca
