酸碱盐化学性质及方程式汇总
酸碱盐的化学性质

【得出结论】通过探究,全班同学一致确定猜想二是正确的。 【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定。同时 指出【实验探究】(2)中存在两处明显错误,同学们经过反思发现了这两处错误: (1)实验操作中的错误是 。 (2)实验方案中也有一个是错误的,错误的原因是 。
练习
氯化钡溶液和硫酸钠溶液反应: 氯化钡溶液和硝酸银溶液反应: 硝酸钡溶液和碳酸钠溶液反应: 氯化钙溶液和碳酸钾溶液反应:
【学以致用】
组内互相讨论完成下述练习,组与组之间展开比赛, 看谁更快更准。 下列物质间能否发生复分解反应?若能反应,写出 有关反应的化学方程式。(参阅溶解性表) ①硫酸和硝酸钠溶液 ②氢氧化钾溶液和硝酸 ③硫酸钠溶液和氯化钡溶液 ④硝酸银溶液和稀盐酸 ⑤硝酸钾溶液和氢氧化钠溶液 ⑥硫酸钡和碳酸钠溶液
3、酸+盐→新酸+新盐
4、盐+碱→新盐+新碱 5、盐1+盐2→盐3+盐4
思考:碱与非金属氧化物反应是分解反应吗?
3、两个“表”
⑪金属活动顺序表. K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au ⑫ 酸碱盐溶解性表
(3)拓展: 永远不会发生复分解反应的物质: 硝酸钠和硝酸钾
应用:除杂,使杂质转化成与原物质不一样状态的 物质,利用离子不能共存的特点
在我市经济大开发的进程中,要坚持开发与环保并重。 某化学课外活动小组在调查一化工厂时发现该厂有甲、 乙两个车间,排出的废水澄清透明,经分析分别含有 三种不同的离子,共有K+、Ba2+、Cu2+、OH-、NO3-、 CO32- 六种离子。 (1)将甲、乙两车间的废水按适当的比例混合,可以 变废为宝,既能使废水中的Ba2+、Cu2+、OH-、CO32等离子转化为沉淀除去,又可以用上层清液来浇灌农 田。清液中含有的溶质主要是 (填写物质的化 学式)。 (2)已知甲车间废水明显呈碱性,则乙车间废水中含 有的阴离子是 。 (3)判断:Cu(NO3)2和Ba(OH)2溶液 (填“能” 或“不能”)发生复分解反应。若能反应写出化学方 程式;若不能反应写出理由: 。
九年级下册酸碱盐化学方程式

九年级下册酸碱盐化学方程式
酸碱盐化学方程式是高中化学里面非常重要和常见的话题之一,我们在学习酸碱盐化学方程式时,要注意学习其反应特点、反应机理等方面,并认真推导出相关方程式,这对后续的理解和研究更有帮助。
高中九年级下册的酸碱盐化学方程式非常多,下面我们列举几个。
1、氢氧化钠的溶解:NaOH(s) + H2O(l) → Na+(aq) + OH-(aq) 氢氧化钠在水中溶解,会形成离子性Na+和OH-两种离子。
2、硫酸的溶解:H2SO4(aq) + H2O(l) → H3O+(aq) + HSO4-(aq) 硫酸在水中溶解,会形成离子性H3O+和HSO4-两种离子。
3、乙酸的溶解:CH3COOH(aq) + H2O(l) → CH3COO-(aq) + H3O+(aq) 乙酸在水中溶解,会形成离子性CH3COO-和H3O+两种离子。
4、氨基酸的溶解:CH3-COOH(aq) + NH3(aq) → CH3-COO-(aq) + NH4+(aq) 氨基酸在水中溶解,会形成离子性CH3-COO-和NH4+两种离子。
此外,还有甲烷氧化反应、亚硫酸钠的溶解、氨气的溶解等等,这些方程式均是九年级下册的酸碱盐化学的一些基础知识,这是非常重要的知识点,不仅在九年级下册,在之后的学习中也要熟练掌握、理解。
综上所述,从上面我们可以明确,九年级下册的酸碱盐化学方程式有许多,这些方程式都有其特定的反应机理和特点,只有熟练掌握它们,才能够在之后的学习中做的更好。
酸碱盐的性质归纳

武汉市楚才中学2012年中考复习之酸、碱、盐的性质及化学方程式归纳一、酸→H++酸根离子1、浓酸的特性:浓盐酸:有挥发性,有刺激性气味浓硫酸:有强烈的腐蚀性,脱水性,吸水性,稀释时放出大量的热2、稀酸的化学性质:(1)使紫色石蕊变红,无色酚酞不变色(2)酸+活泼的金属→盐+H2↑①实验室制氢气(锌与稀硫酸反应)Zn + H2SO4 == ZnSO4 + H2↑Zn + 2HCl == ZnCl2 + H2↑②铁与稀盐酸的反应Fe + 2HCl == FeCl2 + H2↑(实验现象:铁丝逐渐溶解,有无色气泡产生,溶液由无色变成浅绿色)③铁与稀硫酸的反应Fe + H2SO4 === FeSO4 + H2 ↑(实验现象:铁丝逐渐溶解,有无色气泡产生,溶液由无色变成浅绿色)④镁与稀盐酸的反应Mg + 2HCl === MgCl2 + H2↑⑤镁与稀硫酸的反应Mg + H2SO4 ==== MgSO4 +H2 ↑⑥铝与稀盐酸的反应2Al + 6HCl === 2AlCl3 + 3H2↑⑦铝与稀硫酸的反应2Al + 3H2SO4 ===Al2(SO4)3 +3H2 ↑(3)酸+金属氧化物-----盐 + 水①稀盐酸与氧化铁的反应6HCl+Fe2O3===2FeCl3+3H2O(除锈原理)实验现象:红棕色固体逐渐溶解,溶液由无色变成黄色②稀盐酸与氧化铜的反应2HCl+CuO==CuCl2+H2O实验现象:黑色固体逐渐溶解,溶液由无色变成蓝色③稀硫酸与氧化铁的反应3H2SO4+Fe2O3===Fe2(SO4)3+3H2O(除锈)实验现象:红棕色固体逐渐溶解,溶液由无色变成黄色④稀硫酸与氧化铜的反应H2SO4+CuO==CuSO4+H2O实验现象:黑色固体逐渐溶解,溶液由无色变成蓝色⑤稀盐酸与氧化铝的反应6HCl+Al2O3===2AlCl3+3H2O⑥稀硫酸与氧化铝的反应3H2SO4+ Al 2O3=== Al 2(SO4)3+3H2O⑦稀盐酸与氧化钙的反应2HCl+CaO==CaCl2+H2O⑧稀硫酸与氧化钙的反应H2SO4+CaO==CaSO4+H2O⑨稀盐酸与氧化镁的反应2HCl+MgO==MgCl2+H2O⑩稀硫酸与氧化镁的反应H2SO4+MgO==MgSO4+H2O(4)酸 + 碱 -------盐 +①稀盐酸与氢氧化钠的反应HCl+NaOH===NaCl+H2O②盐酸与氢氧化钙的反应2HCl+Ca(OH)2===CaCl2+2H2O③稀硫酸与氢氧化钠的反应H2SO4+2NaOH===Na2SO4+2H2O④稀硫酸与氢氧化钙的反应H2SO4+ Ca(OH)2===CaSO4+2H2O(处理酸性土壤和硫酸厂污水都用熟石灰)⑤稀硫酸与氢氧化钡的反应H2SO4+ Ba(OH)2===BaSO4 ↓+2H2O⑥稀硫酸与氢氧化铜的反应H2SO4+ Cu(OH)2===CuSO4+2H2O⑦稀盐酸与氢氧化铁的反应3HCl+Fe(OH)3===FeCl3+3H2O⑧稀盐酸与氢氧化铝的反应3HCl+Al(OH)3===AlCl3+3H2O(治疗胃酸过多的原理)⑨盐酸与氢氧化镁的反应2HCl+Mg(OH)2=== Mg Cl2+2H2O⑩硫酸与氢氧化镁的反应H2SO4+Mg(OH)2=== MgSO4+2H2O3、酸的用途(1)浓硫酸可做干燥剂(2)稀盐酸、稀硫酸可除去铁制品表面的铁锈(3)胃内盐酸可帮助消化二、碱→OH-- +金属离子1、固体碱的特性氢氧化钠固体:遇水易潮解、强烈的腐蚀性,溶解时放出大量的热氢氧化钙固体:有一定的腐蚀性,微溶于水2、碱溶液的化学性质(1)使紫色石蕊变蓝色,无色酚酞变红色(2)碱+非金属氧化物→盐+水①二氧化碳通入澄清石灰水CO2 + Ca(OH)2 ====== CaCO3↓+ H2O(该反应用于实验室鉴别二氧化碳)②二氧化碳与氢氧化钠的反应CO2 + 2NaOH ===Na2CO3 + H2O(该反应用于吸收二氧化碳)③三氧化硫与氢氧化钠的反应SO3+ 2NaOH ===Na2SO4+ H2O④三氧化硫与氢氧化钙的反应SO3+ Ca(OH)2 ===CaSO4+ H2O⑤二氧化硫与氢氧化钠的反应SO2+ 2NaOH ===Na2SO3+ H2O⑥二氧化硫与氢氧化钙的反应SO2+ Ca(OH)2 ===CaSO3+ H2O(3)碱+酸 -------盐 +3、碱的用途(1)氢氧化钠可用于造纸、纺织、印染等;可以与油脂反应,用于除油污;固体可做干燥剂(2)氢氧化钙固体可用于改良酸性土壤、建筑材料等三、盐→金属离子+酸根离子1、几种常见的盐:(1)氯化钠,化学式NaCl,食盐的主要成分,白色晶体,易溶于水(2)碳酸钠,化学式Na2CO3,俗名:纯碱、苏打,白色粉末,易溶于水,其水溶液显碱性。
酸碱盐化学性质

与稀硫酸反应
Mg+H2SO4=MgSO4+H2↑ Zn+H2SO4=ZnSO4+H2↑ Fe+H2SO4=FeSO4+H2↑
★注意:金属活动性在H以前
一、酸的化学性质
3:酸能与某些金属氧化物反应,生成盐和水。
现象
铁锈+盐酸
化学方程式 Fe2O3+6HCl=2FeCl3+3H2O
铁锈+硫酸
氧化铜+盐酸
一、酸的化学性质
1:酸能与指示剂反应。 紫色石蕊溶液 酸 无色酚酞溶液
中性溶液
碱
不变色 溶液变红色 遇酸溶液变红色,遇碱溶液变蓝色 不变色 不变色
溶液变蓝色 溶液变红色
一、酸的化学性质
2:酸能与多种活泼金属反应,生成盐和氢气
与稀盐酸反应
镁 锌 铁 Mg+2HCl=MgCl2+H2↑ Zn+2HCl=ZnCl2+H2↑ Fe+2HCl=FeCl2+H2↑
三、盐的化学性质
3、盐+碱→新盐+新碱
Na2CO3+Ca(OH)2=2NaOH+CaCO3 ↓ 2NaOH+CuCl2=Cu(OH)2 ↓+2NaCl
反应物可溶
三、盐的化学性质
4、盐1+盐2→新盐1+新盐2
CaCl2+Na2CO3= CaCO3 ↓ +2NaCl CuSO4+BaCl2=BaSO4 ↓ +CuCl2 NaCl+AgNO3=AgCl ↓+NaCl 反应物可溶
Cu NaCl NaOH Fe2O3
碱的试题
1.下列各组气体中,均能用固体NaOH干燥 的一组是 A
A H2 O2 CO C H2 SO2 CO2 B H2 O2 CO2 D O2 CO CO2
酸碱盐性质归纳

《常见的酸及其性质》【知识梳理】一、酸碱盐定义1、酸:电离出的阳离子全部是H+ 的化合物。
2、碱:电离出的阴离子全部是OH- 的化合物。
3、盐:能够电离出金属离子(或NH4+)和酸根离子的化合物。
二、酸的化学性质1、酸与指示剂反应:能使紫色石蕊试液变红,无色酚酞试液遇酸不变色。
2、酸+ 金属→盐+ 氢气(置换反应)实验室制氢气3、酸+ 金属氧化物→盐+ 水(复分解反应)除锈4、酸+ 碱→盐+ 水(复分解反应)改良酸性土壤5、酸+ 盐→新酸+ 新盐(复分解反应)三、两种基本反应类型1、置换反应定义:一种单质和一种化合物生成另一种单质和另一种化合物的反应。
字母式: A + BC = B + AC (金属铁参加置换时生成亚铁盐)反应条件:金属要用氢前金属,酸一般用稀盐酸、稀硫酸。
2、复分解反应定义:两种化合物互相交换成分生成另外两种化合物的反应。
字母式:AB + CD = AD + CB (反应前后元素化合价不变)反应条件:反应物要么有酸要么均可溶;生成物生成沉淀、气体、水。
四、几点补充说明1、有挥发性的三种物质:浓HCl 、浓HNO3 、浓NH3H2O,打开瓶塞会看到白雾。
2、纯净的浓盐酸无色,但工业用盐酸常含有杂质Fe3+,呈黄色。
3、浓H2SO4没有挥发性,有吸水性(物理性质),可做干燥剂;还有脱水性(化学性质)。
4、稀释浓H2SO4时,要将浓H2SO4沿器壁慢慢注入水中,并不断用玻璃棒搅拌,使产生的热量迅速扩散,绝对禁止将水倒入浓硫酸中!5、指示剂变色表:说明:(1)可溶性的碱的溶液才能使指示剂变色;(2)使石蕊变红的是酸性的溶液(包括酸和某些盐的溶液),使酚酞变红的是碱性的溶液(包括碱的溶液和某些盐的溶液)。
【指点迷津】解决酸碱盐问题的基本步骤:1、快速判断能否反应(判断步骤:物质类别性质标题反应类型具体条件)2、写出化学反应方程式;3、反应的现象。
《常见的碱及其性质》【知识梳理】一、两种重要的碱-----------氢氧化钠与氢氧化钙1、氢氧化钠俗称火碱、烧碱、苛性钠。
初三化学酸碱盐十大知识点总结

初三化学酸碱盐十大知识点总结初三化学酸碱盐十大知识点总结今天店铺就为大家整理了一篇有关初三化学知识点总结:初三化学酸碱盐十大知识点总结的相关问题,以供大家阅读,更多信息请关注学习方法网!一、电离方程式H2SO4=2H++SO42-NaOH=Na++OH-Al2(SO4)3=2Al3++3SO42-二、物质的俗称和主要成分生石灰——CaO熟石灰、消石灰、石灰水的主要成分——Ca(OH)2石灰石、大理石——CaCO3食盐的主要成分——NaCl纯碱、口碱——Na2CO3烧碱、火碱、苛性钠——NaOH胆矾、蓝矾——CuSO4.5H2O碳酸钠晶体——Na2CO3.10H2O氨水——NH3.H2O三、金属活动性1、金属活动性顺序:KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu2、金属活动性顺序的意义:在金属活动性顺序中,金属位置越靠前,金属在水溶液(酸溶液或盐溶液)中就越容易失电子而变成离子,它的活动性就越强。
3、金属活动性顺序的应用:(1)排在氢前的金属能置换出酸里的氢(元素)。
(2)排在前面的金属才能把排在后面的金属从它们的盐溶液中置换出来(K、Ca、Na除外)。
四、酸、碱、盐的溶解性1、常见盐与碱的溶解性:(如果不读出括号中的字,是不是一个较好记忆的顺口溜?)钾(盐)、钠(盐)、铵盐全都溶,硝酸盐遇水影无踪。
硫酸盐不溶硫酸钡,氯化物不溶氯化银。
碳酸盐只溶钾(盐)、钠(盐)、铵(盐)。
碱类物质溶解性:只有(氢氧化)钾、(氢氧化)钠、(氢氧化)钙、(氢氧化)钡溶。
2、八个常见的沉淀物:氯化银、硫酸钡碳酸银、碳酸钡、碳酸钙氢氧化镁、氢氧化铜、氢氧化铁3、四个微溶物:Ca(OH)2(石灰水注明“澄清”的原因)CaSO4(实验室制二氧化碳时不用稀硫酸的原因)Ag2SO4(鉴别SO42-和Cl-时,不用硝酸银的原因)MgCO3(碳酸根离子不能用于在溶液中除去镁离子的原因)4、三个不存在的物质:所谓的氢氧化银、碳酸铝、碳酸铁五、分解反应发生的条件反应后有气体、水或沉淀生成。
初中化学酸碱盐知识归纳总结

初中化学酸碱盐知识归纳总结酸碱盐是化学最后一部分内容,也是中考的重中之重,各大方程式更是考卷的常客。
这里豆姐详细地总结了这一专题的重点知识,如果你还有任何疑问的话,一定要仔细阅读。
一、酸及酸的通性酸的定义,电离时生成的阳离子全部都是H+。
酸是由氢离子和酸根离子构成。
1.浓盐酸、浓硫酸的物理性质、特性、用途2.酸的通性:盐酸HCl 硫酸H2SO4酸使紫色石蕊试液变红,使无色酚酞试液不变色。
金属+酸→盐+氢气Zn+2HCl=ZnCl2+H2↑Zn+ H2SO4 =ZnSO4+H2↑碱性氧化物+酸→盐+水Fe2O3+6HCl=2FeCl3+3H2OFe2O3+3H2SO4=Fe2(SO4)3+3H2O碱+酸→盐+水NaOH+HCl=NaCl+ H2OCu(OH)2+H2SO4= CuSO4+2H2O盐+酸→另一种盐+另一种酸AgNO3+HCl=AgCl↓+HNO3BaCl2+H2SO4=BaSO4↓ +2HCl注意:(1)在‘金属+酸→盐+氢气’中,酸通常指的是稀硫酸和稀盐酸,不能是浓硫酸或硝酸。
因为浓硫酸或硝酸都有强氧化性,与金属反应时不能生成氢气而生成了水。
(2)通过金属跟酸的反应情况导出金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性由强逐渐减弱金属活动性顺序中,金属位置越靠前,活动性越强,反应越剧烈,所需时间越短。
(3)浓硫酸具有吸水性,通常用它作为干燥剂。
硫酸还具有脱水性,它对皮肤或衣服有很强的腐蚀性。
稀释浓硫酸时一定要把浓硫酸沿着器壁慢慢地注入水里,并不断搅动,切不可把水倒进浓硫酸里,如果把水注入浓硫酸里,水的密度较小,会浮在硫酸上面,溶解时放出的热会使水立刻沸腾,使硫酸液向四处飞溅,容易发生事故。
二、碱及碱的通性定义:电离时生成的阴离子全部是OH-离子。
碱是由金属离子(或铵根离子)和氢氧根离子构成。
1.氢氧化钠、氢氧化钙的物理性质、用途2.碱的通性碱使紫色石蕊试液变蓝,使无色酚酞试液变红。
全册化学反应方程式和酸碱盐的化学性质
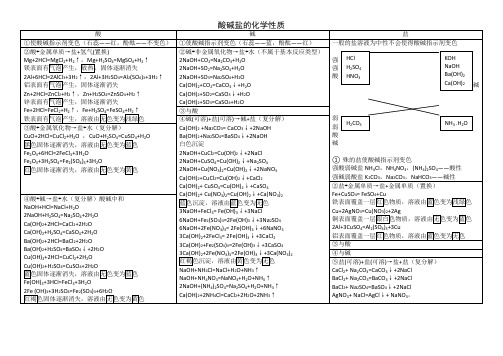
2、加热
△
2Cu+O2
△
2CuO 2HgO
2Hg+O2 3、高温
高温
C+CO2
2CO
4、常温 CO2+H2O=H2CO3 CaO+ H2O=Ca(OH)2 (放热)
2CO2+3H2O
酶
Байду номын сангаас
C+O2 2CO+O2 S+O2
2C+Fe3O4 2H2O2 2H2O +O2↑
△
6CO2+6H2O(热量)
点燃
2CO2
2、电解水
通电
H2+CuO 2H2 ↑+O2↑ 3H2+Fe2O3
Cu+ H2O
高温
点燃
SO2
空气:淡蓝色火焰,刺激性气味 氧气:蓝紫色火焰,刺激性气味
2H2O
黄光,大量白烟
点燃
耀眼白光,生成白色固体
CaCO3 CaO+ CO2↑ 4、碳酸分解 H2CO3=H2O+ CO2↑ 5、小苏打分解(制备糕点)
△
2Fe+3CO2
高温
高温
C+H2O
CO+ H2 4CO+Fe3O4 3Fe+4CO2
点燃
氧气:火星四射,生成黑色固体 2NaHCO3
Na2CO3+H2O+ CO2↑
Ca(OH)2+2NH4NO3=Ca(NO3)2+2H2O+2NH3↑ Ca(OH)2+(NH4)2SO4=CaSO4+2H2O+2NH3↑ 刺激性气味(氨气的气味)
酸碱盐知识点和化学方程式

酸碱指示剂1、紫色石蕊溶液遇酸溶液(含H+的溶液)变红,遇碱溶液(含OH-的溶液)变蓝,在中性溶液中呈紫色。
无色酚酞溶液遇酸溶液不变色,在中性溶液中不变色,遇碱溶液变红。
一、酸的定义酸:物质溶于水时,形成的阳离子全部是H+的化合物。
二、常见的酸盐酸(氢氯酸)化学式HCl状态:无色液体、具有酸味、刺激性气味特点:浓盐酸具有强挥发性用途:用于金属表面除锈、制药、人体胃液中含有盐酸,可以帮助消化敞口放置的变化:质量减小,溶质质量分数减小(挥发性)硫酸化学式H2SO4状态:(浓硫酸)无色粘稠的油状液体;(稀硫酸)无色液体特点:①浓硫酸具有吸水性(物理性质)②浓硫酸具有强腐蚀性(化学性质)③浓硫酸溶于水时会放出大量热用途:精炼石油和金属除锈等;在实验室中常用浓硫酸作干燥剂敞口放置的变化:质量变大,溶质质量分数减小(吸水性)稀释浓硫酸的正确操作:碳酸不稳定,容易分解成二氧化碳和水。
H2CO3=H2O+CO2↑硝酸、硝酸银见光易分解,所以它们要放在棕色试剂瓶中。
三、酸的化学性质酸有相同的化学性质是因为酸在水中都能电离出H+,有不同的化学性质是因为能电离出的酸根离子不同。
1.酸溶液能使酸碱指示剂变色:使紫色石蕊溶液变红。
2.酸+活泼金属→ 盐+氢气(置换反应)示例:Fe+2HCl=FeCl2+H2↑和Fe+H2SO4=FeSO4+H2↑3.酸+金属氧化物→ 盐+水(复分解反应)Fe2O3+6HCl=2FeCl3+3H2O 和Fe2O3+3H2SO4=Fe2(SO4)3+3H2OCuO+2HCl=CuCl2+H2O 和CuO+H2SO4=CuSO4+H2O4.酸+碱→ 盐+水(复分解反应、中和反应)NaOH+HCl=NaCl+H2O5.酸+盐→ 新酸+新盐(复分解反应)CaCO3+2HCl=CaCl2+H2O+CO2↑BaCl2+H2SO4=BaSO4↓+ 2HClAgNO3+HCl=HNO3+AgCl↓第三节碱一、碱的定义碱:物质溶于水时,形成的阳离子全部是OH-的化合物。
初中化学酸碱盐知识点归纳整理

初中化学酸碱盐知识点归纳整理(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如演讲稿、总结报告、合同协议、方案大全、工作计划、学习计划、条据书信、致辞讲话、教学资料、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides you with various types of classic sample essays, such as speech drafts, summary reports, contract agreements, project plans, work plans, study plans, letter letters, speeches, teaching materials, essays, other sample essays, etc. Want to know the format and writing of different sample essays, so stay tuned!初中化学酸碱盐知识点归纳整理酸碱盐通常是同学们最头疼的部分,因为这部分涉及的概念多、物质分类多、反应规律多、需要记忆的多、实际应用的多、题型变化多,因此要掌握这部分知识存在一定的困难。
初三化学酸碱盐归纳总结

初中化学酸碱盐归纳总结一、酸和碱1.盐酸、硫酸属于酸,酸在水溶液中能解离出H+和酸根离子。
酸→H ++酸根离子2.氢氧化钠、氢氧化钙属于碱,碱在水中能解离出金属离子和OH¯。
碱→金属离子+OH ¯3.二、酸12(1)与酸碱指示剂的反应: 使紫色石蕊试液变红色,不能使无色酚酞试液变色(2)酸能使多种活泼金属反应,生成盐和氢气。
即金属 + 酸 → 盐 + 氢气Fe+2HCl=FeCl 2+H 2↑ Zn+H 2SO 4=ZnSO 4+H 2↑2Al+6HCl=2AlCl 3+3H 2↑ 2Al+3H 2SO 4=Al 2(SO 4)3+3H 2↑ (3)酸能使某些金属氧化物反应,生成盐和水。
即碱性氧化物 + 酸 → 盐 + 水 铁锈+盐酸:Fe 2O 3+6HCl====2FeCl 3+3H 2O (黄色溶液);铁锈+硫酸Fe 2O 3+3H 2SO 4====Fe 2(SO 4)3+3H 2O(4)碱能与某些非金属氧化物反应,生成盐和水。
即碱 + 酸 → 盐 + 水NaOH +CO 2=Na 2CO 3+H 2O Ca(OH)2+ CO 2=CaCO 3↓+H 2O+CO 2↑ (5)盐 + 酸 → 另一种盐 + 另一种酸(产物符合复分解条件)HCl+ AgNO 3=AgCl ↓+HNO 3 H 2SO 4+BaCl 2=BaSO 4↓+HClCaCO3 + 2HCl = CaCl2+ H2O + CO2↑三、碱1、氢氧化钠、氢氧化钙的物理性质、用途2、碱的通性(具有通性的原因:离解时所生成的阴离子全部是OH)(1)碱溶液与酸碱指示剂的反应:使紫色石蕊试液变蓝色,使无色酚酞试液变红色(2)酸性氧化物+碱→盐+水2NaOH+CO2=Na2CO3+H2O(3)酸+碱→盐+水NaOH + HCl = NaCl + H2O(4)盐+碱→另一种盐+另一种碱(反应物均可溶,产物符合复分解条件)HCl+ AgNO3=AgCl↓+HNO3H2SO4+BaCl2=BaSO4↓+HClCaCO3 + 2HCl = CaCl2+ H2O + CO2↑注:①难溶性碱受热易分解(不属于碱的通性)如Cu(OH)2 ΔCuO +H2O2Fe(OH)3 ΔFe2O3+3H2O②常见沉淀:AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓③复分解反应的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
初中科学---酸碱盐金属的化学性质

酸、碱、盐、金属的化学性质一、酸的通性:1、紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色。
2、酸+ 金属→盐+ 氢气(注意:这里通常指稀硫酸、稀盐酸能跟(H)前的活泼金属反应生成盐和氢气;具有强氧化性的硝酸、浓硫酸跟金属反应时生成物不是氢气。
)举例:Zn+H2SO4==ZnSO4+H2↑Fe+H2SO4==FeSO4+H2↑Mg+H2SO4==MgSO4+H2↑2Al+3H2SO4==Al2 (SO4)3+3H2↑Zn + 2HCl === ZnCl2+ H2↑2Na + 2HCl === 2NaCl+ H2↑2Al + 6HCl === 2AlCl3 + 3H2↑Fe + 2HCl === FeCl2 + H2↑3、酸+金属氧化物(碱性氧化物)→盐+水Fe2O3+6HCl==2FeCl3+3H2O Fe2O3+3H2SO4= Fe2 (SO4) 3+3H2OAl2O3+6HCl==2AlCl3+3H2O Al2O3+3H2SO4==Al2 (SO4) 3+3H2ONa2O+2HCl==2NaCl+H2O CuO+H2SO4==CuSO4+H2OCuO+2HCl==CuCl2+H2O ZnO+H2SO4==ZnSO4+H2OMgO+2HCl==MgCl2+H2O MgO+H2SO4==MgSO4+H2OCaO+2HCl==CaCl2+H2O Na2O+2HNO3==2NaNO3+H2OCuO+2HNO3==Cu(NO3) 2+H2O CaO+2HNO3==Ca(NO3) 2+H2O4、酸+碱→盐+水<中和反应,属于复分解反应>NaOH+HCl==NaCl+H2O 2NaOH+H2SO4==Na2SO4+2H2OCu(OH) 2+2HCl==CuCl2+2H2O Cu(OH) 2+H2SO4==CuSO4+2H2OMg(OH) 2+2HCl==MgCl2+2H2O Ca(OH) 2+H2SO4==CaSO4+2H2OAl(OH) 3+3HCl==AlCl3+3H2O Mg(OH) 2+H2SO4==MgSO4+2H2OFe(OH) 3+3HCl==FeCl3+3H2O 2Al(OH) 3+3H2SO4==Al2 (SO4) 3+3H2OCa(OH) 2+2HCl==CaCl2+2H2O 2Fe(OH) 3+3H2SO4==Fe2 (SO4) 3+3H2OKOH+HCl==KCl+H2O Ba (OH) 2+H2SO4==BaSO4↓+2H2OCu(OH) 2+2HNO3==Cu(NO3) 2+2H2O 2NaOH+H2CO3==Na2CO3+2H2ONaOH+HNO3==NaNO3+H2O Ca(OH) 2+H2CO3==CaCO3↓+2H2O2NaOH+H2S==Na2S+2H2O 2NaOH+H2SO3==Na2SO3+2H2O3NaOH+H3PO4==Na3PO4+3H2O NH4OH +HCl = NH4Cl + H2O5、酸+ 盐→新酸+ 新盐(难溶、易溶的碳酸盐一般均能与酸反应产生二氧化碳气体;当其它类型的盐与酸反应时,反应物需可溶,生成物必须满足复分解反应的条件)CaCO3+2HCl==CaCl2+H2O+CO2↑Na2CO3+2HCl==2NaCl+H2O+CO2↑MgCO3+2HCl==MgCl2+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑CaCO3+2HNO3==Ca(NO3) 2+H2O+CO2↑AgNO3+HCl==AgCl↓+HNO3BaCl2 + H2SO4==BaSO4↓+2HCl Ba(NO3) 2+H2SO4==BaSO4↓+2HNO3二、碱的通性:1、碱的水溶液.....能使紫色石蕊试液变蓝色,使无色酚酞试液变红色。
酸碱盐化学方程式大全

酸碱盐化学方程式大全酸碱盐是化学中非常重要的三大基本物质,它们在化学反应中起着至关重要的作用。
酸碱盐化学方程式是描述酸碱盐反应过程的重要工具,通过化学方程式我们可以清晰地了解反应物和生成物之间的关系,从而更好地理解和掌握化学知识。
1. 酸的化学方程式。
酸是一类能够释放氢离子(H+)的化合物,常见的酸包括硫酸、盐酸、硝酸等。
酸的化学方程式通常以H+离子的释放为特征,比如盐酸的化学方程式可以表示为HCl → H+ + Cl-。
2. 碱的化学方程式。
碱是一类能够释放氢氧根离子(OH-)的化合物,常见的碱包括氢氧化钠、氢氧化钾等。
碱的化学方程式通常以OH-离子的释放为特征,比如氢氧化钠的化学方程式可以表示为NaOH → Na+ + OH-。
3. 盐的化学方程式。
盐是酸和碱中和生成的化合物,常见的盐包括氯化钠、硫酸铜等。
盐的化学方程式通常可以表示为酸和碱反应生成盐和水,比如硫酸和氢氧化钠反应生成硫酸钠的化学方程式可以表示为H2SO4 + 2NaOH → Na2SO4 + 2H2O。
4. 酸碱中和反应的化学方程式。
酸碱中和反应是酸和碱反应生成盐和水的过程,其化学方程式可以表示为酸和碱的离子互换,从而生成盐和水,比如盐酸和氢氧化钠中和反应的化学方程式可以表示为HCl + NaOH → NaCl + H2O。
5. 酸碱中和滴定反应的化学方程式。
酸碱中和滴定是一种常用的定量分析方法,其化学方程式可以表示为滴定过程中酸和碱的定量反应,从而求得溶液中酸或碱的浓度,比如硫酸和氢氧化钠滴定反应的化学方程式可以表示为H2SO4 + 2NaOH → Na2SO4 + 2H2O。
6. 酸碱指示剂的化学方程式。
酸碱指示剂是用来指示酸碱滴定终点的物质,其化学方程式可以表示为指示剂在不同pH值下发生颜色变化的过程,从而帮助确定滴定终点,常见的酸碱指示剂包括酚酞、溴甲酚等。
通过以上的介绍,我们可以清晰地了解酸碱盐化学方程式的相关知识,这些化学方程式在化学实验和工业生产中都有着重要的应用价值。
初中化学酸碱盐性质总结
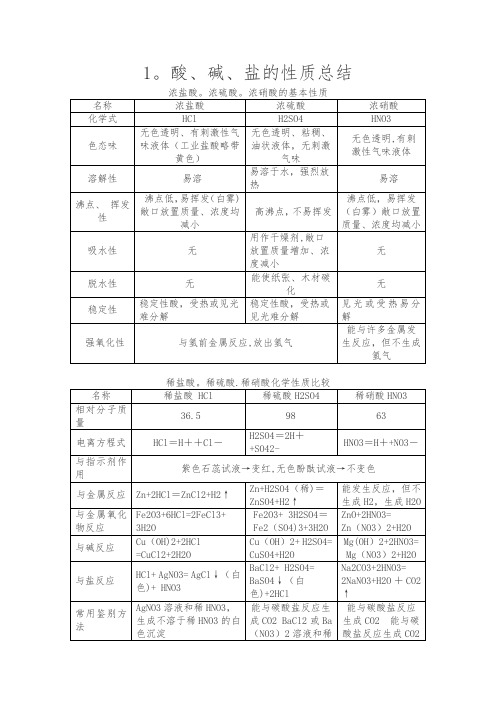
③硝酸也是一种含氧酸,对应的酸酐是N2O5,而不是NO2。
纯净的硝酸是无色的液体,具有刺激性气味,能挥发。
打开浓硝酸的瓶盖在瓶口会产生白色酸雾.浓硝酸通常带黄色,而且硝酸越浓,颜色越深.这是因为硝酸具有不稳定性,光照或受热时分解产生红棕色的NO2气体,NO2又溶于硝酸溶液中而呈黄色。
所以,实验室保存硝酸时要用棕色(避光)玻璃试剂瓶,贮存在黑暗低温的地方。
硝酸又有很强的腐蚀性,保存硝酸的试剂瓶不能用橡胶塞,只能用玻璃塞.除具有酸的通性外,不管是稀硝酸还是浓硝酸都具有强氧化性。
硝酸能溶解除金和铂以外的所有金属。
金属与硝酸反应时,金属被氧化成高价硝酸盐,浓硝酸还原成NO2,稀硝酸还原成NO。
但是,不管是稀硝酸还是浓硝酸,与金属反应时都没有氢气产生。
较活泼的金属铁和铝可在冷浓硝酸中钝化,冷浓硝酸同样可用铝槽车和铁罐车运输和贮存。
硝酸不仅能氧化金属,也可氧化C、S、P等非金属。
硝酸与Cu、C发生反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O3Cu+8 HNO3(稀)=3Cu(NO3)2+2NO↑+4H2OC+4HNO3(浓) CO2↑+4NO2↑+2H2O④磷酸是一种中等强度的三元酸,可以形成一种正盐和两种酸式盐.如:磷酸氢二钠(Na2HPO4),磷酸二氢钠(NaH2 PO4),磷酸二氢铵[NH4H2PO4 ],磷酸氢二铵[(NH4)2HPO4 ],磷酸二氢钙[Ca(H2PO4)2](溶于水).2.常见物质的溶解性常见酸中除硅酸(H2SiO3)外均可溶;常见碱中除NaOH、KOH、Ca(OH)2 、NH3•H2O可溶,微溶外其余均为难溶碱。
其中Cu(OH)2 为蓝色沉淀,Fe(OH)3 为红褐色沉淀,其余均为白色沉淀;常见的盐的溶解性规律是:钾、钠、铵、硝溶;盐酸银不溶;硫酸钡不溶硫酸钙、硫酸银微溶;碳酸钾、钠、铵能溶;碳酸镁微溶.3.金属活动顺序表的应用金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au----——————————--———————-———-——-→金属活动性由强到弱金属活动顺序表的应用主要是在置换反应中的应用。
初中化学酸、碱、盐的化学性质归纳

酸、碱、盐的化学性质归纳一、酸的化学性质1、酸(碱)与指示剂的作用石蕊酚酞中性紫色无色酸性红色无色碱性蓝色红色2、酸+ 金属——→盐+ 氢气↑(置换反应)要求:金属的活动要排在氢的前面,酸一般只指稀HCl 和稀H 2SO 4常见反应:Mg + 2HCl === MgCl 2 + H 2 ↑ Mg + H 2SO 4 === MgSO 4 + H 2 ↑Zn + 2HCl === ZnCl 2 + H 2 ↑Zn + H 2SO 4 === ZnSO 4 + H 2 ↑Fe + 2HCl === FeCl 2 + H 2 ↑Fe + H 2SO 4 === FeSO 4 + H 2 ↑2Al +6HCl === 2AlCl 3 + 3H 2 ↑ 2Al + 3H 2SO 4 === Al 2(SO 4)3 + H 2 ↑3、酸+ 金属氧化物——→盐+ 水(复分解反应)要求:无要求常见反应:Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2O Fe 2O 3 + 3H 2SO 4 === Fe 2(SO 4)3 + 3H 2O CuO + 2HCl === CuCl 2 + H 2O CuO + H 2SO 4 === CuSO 4 + H 2O 4、酸+ 碱——→盐+ 水(复分解反应)要求:无要求常见反应:HCl + NaOH === NaCl + H 2O H 2SO 4 + 2NaOH ===Na 2SO 4 + 2H 2O 2HCl + Ca(OH)2 === CaCl 2 + 2H 2O H 2SO 4 + Ba(OH)2 === BaSO 4↓+ 2H 2O 2HCl + Mg(OH)2 === MgCl 2 + 2H 2O 5、酸+ 盐(复分解反应)(1)酸+ 碳酸盐——→新盐+ 水+ 二氧化碳↑要求:无要求常见反应:CaCO 3 + 2HCl === CaCl2 + H 2O + CO 2↑Na 2CO 3 + 2HCl === 2NaCl + H 2O + CO 2↑NaHCO 3 + HCl === NaCl + H 2O + CO 2↑(2)酸+ 普通盐——→新盐+ 新酸要求:反应物均可溶,产物有沉淀常见反应:H 2SO 4 + BaCl 2 === BaSO 4↓+ 2HCl HCl + AgNO 3 === AgCl↓+ HNO 3 二、碱的化学性质1、碱与指示剂的作用(参见“一、1”)注意:不溶性碱不能使指示剂变色。
酸碱盐的化学性质及方程式总结1

酸的化学性质:(注意:有酸参加,另一物质可溶可不溶,AgCl、BaSO4除外)化学性质具体事例或者化学方程式一、酸能与指示剂反应二、酸+活泼金属→盐+氢气(置换反应)Mg、Al、Zn、Fe分别与稀盐酸和稀硫酸的反应(共8个)(要求:标清序号、下同)三、酸+金属氧化物→盐+水(复分解反应)CaO、Fe2O3、CuO、Al2O3分别与稀盐酸和稀硫酸的反应(共8个)四、酸+碱→盐+水(中和反应,复分解反应)NaOH、Ca(OH)2、Mg(OH)2、Al(OH)3分别与稀盐酸反应Fe(OH)3、Cu(OH)2分别与稀硫酸的反应五、酸+盐→新盐+新酸(复分解反应)CaCO3、Na2CO3、NaHCO3分别与稀盐酸反应盐酸的特征反应:硫酸的特征反应:碱的化学性质:化学性质具体事例或者化学方程式一、碱能与指示剂反应二、碱+非金属氧化物→盐+水(注意:不是复分解反应)(CO、NO除外)NaOH、Ca(OH)2分别与CO2、SO2、SO3反应(共6个)SiO2+NaOH三、酸+碱→盐+水(同酸第四条)(中和反应,复分解反应)略四、碱+盐→新盐+新碱(复分解反应)(反应物都可溶,生成物有沉淀或气体生成)Ca(OH)2+Na2CO3 Ba(OH)2+Na2CO3 NaOH+CuSO4 NaOH+FeCl3Ba(OH)2+CuSO4 Ba(OH)2+Fe2(SO4)3盐的化学性质:化学性质具体事例或者化学方程式一、盐溶液的酸碱性大多数盐溶液呈中性有的盐溶液呈碱性(如碳酸钠、碳酸氢钠等)有的盐溶液呈酸性(如氯化铵,硫酸铵等)二、前金+后金的可溶性盐→后金+新盐(钾钙钠特殊不可行)Al、Zn、Fe、Cu分别与AgNO3溶液反应(共4个)Al、Zn、Fe分别与CuSO4溶液反应(共3个)三、盐+酸→新盐+新酸(复分解反应)(同酸第5条)略四、盐+碱→新盐+新碱(复分解反应)(反应物都可溶,生成物有沉淀或气体生成)(同碱第4条)略五、盐+盐→两种新盐(复分解反应)(反应物需都可溶,生成物有沉淀)CaCl2+Na2CO3 BaCl2+Na2CO3 BaCl2+Na2SO4 AgNO3+NaCl。
酸碱盐化学性质总结91066

酸碱盐化学性质总结一、 酸的化学性质(1) 酸跟酸碱指示剂作用酸使紫色石蕊试液变红,使无色酚酞试液不变色。
(2) 金属+酸→盐+氢气 (在金属活动表中排在氢前面的金属)↑+=+2442H ZnSO SO H Zn ↑+=+222H FeCl HCl Fe↑+=+2342423)(32H SO Al SO H Al ↑+=+222H MgCl HCl Mg(3) 金属氧化物+酸→盐+水O H FeCl HCl O Fe 2332326+=+ O H SO Fe SO H O Fe 234242323)(3+=+ O H CaCl HCl CaO 222+=+ O H CuSO SO H CuO 2442+=+(4) 碱+酸→盐+水O H SO Na SO H NaOH 2424222+=+ O H CaSO SO H OH Ca 244222)(+=+ O H AlCl HCl OH Al 23333)(+=+ O H MgCl HCl OH Mg 22222)(+=+(5)盐+酸→新盐+新酸↑++=+22232CO O H CaCl HCl CaCO ↑++=+22424232CO O H SO Na SO H CO Na HCl BaSO SO H BaCl 24422+↓=+ ↑++=+223CO O H NaCl HCl NaHCO 33HNO AgCl HCl AgNO +↓=+二、 碱的化学的性质(1) 碱溶液跟酸碱指示剂作用参加反应的碱必须可溶或微溶。
碱溶液使紫色石蕊试液变蓝,使无色酚酞试液变红。
(2) 非金属氧化物+碱(溶液)→盐+水(碱必须是可溶或微溶性的碱)O H CaCO OH Ca CO 2322)(+↓=+ O H CO Na NaOH CO 23222+=+ O H SO Na NaOH SO 23222+=+ O H SO Na NaOH SO 24232+=+(3) 酸+碱→盐+水O H NaCl HCl NaOH 2+=+(4) 盐+碱→新盐+新碱(参加反应的盐碱必须可溶或微溶,生成物满足复分解反应的条件。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
酸碱盐化学性质及方程式汇总
酸碱盐是化学中三种基本的化合物。
它们的化学性质和
行为是物质反应中最经典和最广泛研究的主题之一。
在本文中,将介绍酸碱盐的一些基本概念,并探讨它们的化学性质和方程式。
一、酸的化学性质及方程式
酸是指能够解离出氢离子(H+)的化合物。
因此,酸具
有以下性质:
1. 酸具有酸味。
2. 酸具有腐蚀性,能够腐蚀金属和造成化学灼伤。
3. 酸会转换色感纸,比如红色的酸性颜色碧蓝。
4. 酸能够与碱中和产生盐和水。
下面是一些常见的酸的化学式和方程式:
1. 盐酸(HCl)
化学式:HCl
方程式:HCl → H+ + Cl-
2. 硝酸(HNO3)
化学式:HNO3
方程式:HNO3 → H+ + NO3-
3. 硫酸(H2SO4)
化学式:H2SO4
方程式:H2SO4 → H+ + HSO4- → 2H+ + SO4(2-)
二、碱的化学性质及方程式
碱是指能够溶解出氢氧根离子(OH-)的化合物。
碱具有
以下性质:
1. 碱具有苦味。
2. 碱具有腐蚀性,能够腐蚀金属和造成化学灼伤。
3. 碱能够转换色感纸,比如蓝色的碱性颜色变红。
4. 碱能够与酸中和产生盐和水。
下面是一些常见的碱的化学式和方程式:
1. 氢氧化钠(NaOH)
化学式:NaOH
方程式:NaOH → Na+ + OH-
2. 氢氧化钾(KOH)
化学式:KOH
方程式:KOH → K+ + OH-
3. 氨水(NH3·H2O)
化学式:NH3·H2O
方程式:NH3·H2O + H2O → NH4+ + OH-
三、盐的化学性质及方程式
盐是指由阳离子和阴离子通过化学结合形成的化合物。
盐具有以下性质:
1. 盐在常温下呈固体,有时会呈现出颜色。
2. 盐完全溶于水。
3. 盐在常温下不具有味道。
4. 盐不具有腐蚀性。
下面是一些常见的盐的化学式和方程式:
1. 氯化钠(NaCl)
化学式:NaCl
方程式:Na+ + Cl- → NaCl
2. 硫酸铜(CuSO4)
化学式:CuSO4
方程式:Cu2+ + SO4(2-) → CuSO4
3. 碳酸钙(CaCO3)
化学式:CaCO3
方程式:Ca2+ + CO3(2-) → CaCO3
四、酸碱中和反应方程式
酸碱中和是指一种化学反应,其产物是盐和水。
酸基和碱基反应生成水,同时离子消失并形成盐。
下面是一些常见的酸碱中和反应的方程式:
1. 盐酸和氢氧化钠的中和反应
化学式:HCl + NaOH → NaCl + H2O
方程式:H+ + Cl- + Na+ + OH- → Na+ + Cl- + H2O
2. 硫酸和氢氧化钠的中和反应
化学式:H2SO4 + 2NaOH → Na2SO4 + 2H2O
方程式:2H+ + SO4(2-) + 2Na+ + 2OH- → Na2SO4 +
2H2O
3. 硝酸和氢氧化钠的中和反应
化学式:H NO3 + NaOH → NaNO3 + H2O
方程式:H+ + NO3- + Na+ + OH- → Na+ + NO3- + H2O 以上就是酸碱盐的基本性质和方程式。
在化学学习中,对于酸碱盐的认识非常重要,不仅能够帮助我们理解和掌握物质变化的规律,也能够帮助我们解决化学实验中遇到的问题。
