维生素D3的含量检验方法
两种方法测定维生素D3含量

学 术 论 坛
Sic ad eh lyn v cne n Tc og lo实验 , 表 维生素 D 的总量 ( f+ im/ 。 并 维生素 D 发现 3 f 。 2 A) ) , 3的校正 因子 F A r— A 明两方法 测得结果一 致 , 外标法可 同时进行 含 计 算 含 量 。 Ar =—’ 一 2 1 线性关 系考 察 。 量 与有 关 物 质 的检 测 。 式 中 : , —对 照品溶液 中维生 素 D A— 3的 移取对 照品贮备溶 液 2 ml 。 ml 0 、3 0 、 4 0 、5 0 l 。m 于五 个 2 ml .ml .m 、6 0 l 0 的容量瓶 峰面 积 ; 1仪器 与试 药 A —— 校正 因子测 定液 中维生素 D 的峰 3 加 mt加正 己烷至刻 度 , 匀得 摇 仪 器 : i n lO 高效 液相 色谱仪 , 中, 内标 溶液 2 , Agl t l0 e 面积 五 个 不 同浓 度 的 稀 释 液 测 定 。得 相 关 系数 VWD紫外检 测器 。 A — —校 正 因子 测定 液中前 维生素 D 3 R O. 998, = 0. = 9 R 9999。 . 色谱 条件 : 的峰面 积 2 2 精密 度试验 。 色谱 柱 : 用硅 胶为填充 剂 ; 含量 测定 取供试 品溶液进行 测定 , 下 按 取供 试 品共 6份 , 依法 测定 , 并计算 相对 流 动相 : 己烷 : 戊醇 = 9 : ; 正 正 9 7 3 列公式计 算维生 素 D3 前维生素 D3 及 折算成 标 准偏 差 , 同实验者 间 的偏差为 0 0 %。 不 .4 检 测波长 :5 n 2 4 m; 维生素 D3 的总峰面 积( A A= + F ×A2 , )按 2 3 回收 率试验 。 流速 :.m / n 20 lmi 采 用标 准加 入法 , 每个 浓度平 行三次 , 计 外标 法 以峰 面 积计 算 供试 品含量 。 进 样量 : 0 l 2 0 。 3 1 线性关系考 察 . n ) 维 生素 D3对 照品( 国药 品生物 制 品检 算 回收 率 。平均 回收 率 (=9 中 取 对 照 品贮 备 液 2.0ml、 3. nl 0i 、 为 9 。 %, D(=9 为 0 5 %。 9 9 RS ) . 8 定所) ; 4 0 、 5 0 、 6 0 于 五 个 2 ml 。 ml . ml . ml 0 的 2 4 样 品含量测定 . 供 试 品 :自制 。 取 测定样 品含量 为 9 . %、 l ( 1 92 (J %、9 . 容 量 瓶 中 , 此 五 个 稀 释 液 按 上 述 色 谱 条 ). 9 其 他 试 剂 均 为分 析 纯 。 件进样分析 。 6% 。 结论 : 试 品溶 液浓 度在 l . 2 0 9 供 0 3 ~3 .6 2内标 法 “g ml 间 ,l l / 之 l ̄当于 称样 范 围在 4 % ~ i 1 参 照中 国药典 2 0 年版附 录v K 维生 3外标法 00 Ⅱ 2%之 间时 , 面积与其浓 度呈 良好 的线性 。 峰 参 照E 20口 P O21 维生素 D 含量测定 方法及 14 3 素 D测 定法 . 中国药典 2 0 年版附 录v 00 ⅡK 维生素 D测定 32 精 密度试验 色谱 柱 : lma SA a5肚m ,5 。 t ic( i 20x4 平行 6次测定供试 品的 含量 , 并计算相 对 法 6 m) a r 标准偏 差见表 l 。 色谱柱 : Ⅱj】 ic ( m,5 A tI Sla5 Ia i 10×4 。 内标 溶液 的制备 : 称取邻 苯二 甲酸二 甲酯 33 准确 度 。 mm) 2 rg, 2 ml 瓶 中 , 正 己烷至刻 度 , 5 a 置 5 量 加 摇 6 用 本法 测定 本 品三个 批号 的 含量分 别 为 供试 品溶液的配制 : 取供试 品原液5 , 移 ml
高效液相色谱法测定制剂中维生素D3粉的含量

高效液相色谱法测定制剂中维生素D3粉的含量摘要用高效液相色谱法测定VD3粉中VD3的含量。
采用菲罗门氨基键合硅胶柱(250mm×4.6mm,5μm),以正己烷-异丙醇(99:1)为流动相,流速为1.5ml/min,检测波长为265nm,柱温为25℃。
在此色谱条件下,维生素D3浓度在18.86μg/ml时进样量在10μl~100μl范围内呈良好的线性关系,r=1.0000,平均回收率为99.46%,RSD(n=6)为0.90%。
结论:本方法操作简便易行,系统使用性良好,适用于VD3粉中VD3的含量测定。
关键词:维生素D3粉;维生素D3;复方制剂;高效液相色谱法维生素D3(胆钙化醇;英文名:Vitamin D3)是一种脂溶性维生素,被看作是一种作用于钙、磷代谢的激素前体,帮助肠道内钙和磷的吸收,促进骨钙沉积,增加肾脏对钙、磷的重吸收,提高血钙、磷的浓度,有利于骨的矿化作用。
上市的补钙和补维生素的复方制剂中大多都含有VD3,由于VD3在复方制剂中含量极低,对光、热不稳定,在空气中易氧化和光解成前维生素D3、反式维生素D3、光甾醇和速甾醇等多种产物,在品种开发时多选取制成包合物的VD3粉为原料,以便提高产品的稳定性。
DSM生产的VD3粉加入维生素E、大豆油、明胶制成包合物的形式提高了稳定性。
但包合物的形式造成测定时VD3提取难度增大,有文献报到采用皂化后提取测定,此方法操作繁琐,而且提取中有损失影响结果。
另有采用稀释剂(DMSO-水10:2,0.2%BHT)溶解后,正己烷提取浓缩的方法,以达到液相测定浓度的要求,此方法操作时间长,提取浓缩过程中人为误差较大。
维生素D3粉进口注册标准JX2008006[7]中提取采用的是回流、萃取、旋蒸、充氮、溶解等方法,操作时间长、操作步骤繁琐,误差大。
本文参考相关文献[1] [2] [3] [8]并经验证,证明采用方法准确可靠,且操作简便、快速。
1仪器与试药高效液相色谱仪(赛默飞U3000、岛津SPD-M20A);分析天平(奥豪斯AUW120D);VD3对照品(批号:100061-201208,含量:99.8%,中国食品药品检定研究院);VD3粉(10万单位/g,瑞士DSM Nutritional Products Ltd);正己烷、异丙醇和甲醇为色谱纯;二甲基亚砜、二氯甲烷为分析纯。
饲料中维生素D3含量检测

饲料中维生素D3含量检测科标化工分析检测中心通过市场调查和实验结果,发现养殖户为了解决家禽缺乏维生素D3所带来的“弱腿病”、生长率和饲料利用率下降、产蛋率下降等问题,在饲料中添加维生素D3,为了更好的监测饲料中维生素D3含量,科标化工分析检测中心现开发了其检测方法。
科标化工分析检测中心可依照ISO、ASTM、DIN、GB、HB等标准完成食品、饲料、药品、纺织品、农业、高分子材料、生物产品、建筑材料以及微生物产品理化性能、力学性能、电气性能等测试。
中心通过了中国国家认证认可监督管理委员会和中国合格评定国家认可委员会的二合一(CMA、CNAS)实验室认证认可,能出具权威的第三方检测报告。
饲料中维生素D3的含量检测(高效液相色谱法)一、实验原理科标化工分析检测中心参照国标GB/T17818-2010饲料中维生素D3的测定高效液相色谱法中第一法皂化提取法,试样经粉碎、过筛后,用碱溶液皂化,乙醚提取维生素D3,蒸发乙醚,残渣溶解于甲醇,取部分溶液用C18小柱净化,收集滤液,蒸发至干,用正己烷溶解,反相液相色谱柱分离测定,紫外检测器检测,外标法定量分析。
二、仪器和试剂试验地点:青岛科标化工分析检测中心实验室。
仪器:高效液相色谱仪带紫外检测器,AS3120超声波发生器;试剂:甲醇为色谱纯试剂,实验用水为超纯水,维生素D3标准品(购于日本CPE公司)。
三、试验方法1.皂化称取样品(配合饲料称取10g~20g,浓缩饲料10g,维生素预混饲料或复合预混合饲料1g~5g)精确至0.0001g,置于250ml圆底烧瓶中,加入50ml5g/LL-抗血酸乙醇溶液,混匀,加入10ml氢氧化钾溶液,混匀,置于沸水浴上回流30min,不时震荡防止样品粘附在壁上。
皂化结束,分别用5ml无水乙醇、5ml蒸馏水自冷凝管顶端冲洗其内部,取出烧瓶冷却至室温。
2.提取定量转移全部皂化液于盛有100ml无水乙醚的500ml分液漏斗中,用40ml水分3次冲洗圆底烧瓶并入分液漏斗,用160ml乙醚分三次萃取,合并乙醚相。
HPLC法测定多维片中痕量维生素D3的含量

HPLC法测定多维片中痕量维生素D3的含量王乔飞【摘要】建立了运用HPLC法对痕量VD3进行含量测定的分析方法.实验中采用菲罗门硅胶(silica)柱,以异丙醇:正己烷(0.5:99.5) 为流动相, 流速:2ml/min,紫外检测波长:264nm,柱温:30℃.实验表明:VD3在0.1μg/ml ~0.8μg/ml范围内,其色谱峰面积与质量浓度呈良好线性关系,r=0.9999(n=5),平均回收率为99.04%,进样精密度为1.26%.本法操作简便、快速,准确,适用于痕量成分的含量测定.【期刊名称】《淮阴工学院学报》【年(卷),期】2010(019)003【总页数】3页(P82-84)【关键词】维生素D3;高效液相色谱;含量测定【作者】王乔飞【作者单位】江苏江山制药有限公司,江苏,靖江,214500【正文语种】中文【中图分类】R917多维片是综合营养保健品,其成份极其复杂,不但包括各种水溶性和脂溶性维生素,还有多种补充的微量元素,其中VD3是一种脂溶性维生素,其含量极低,样品中仅约含2.5ug/g,且性质不稳定,遇光和空气均易变质、降解,而且其它杂质对其稳定性和检测都有影响和干扰,其含量测定一直是个瓶颈难题。
有关资料提供的方法,主要采用添加碱液进行皂化反应,然后采用石油醚、乙醚多次萃取,再用氮气流吹干处理。
不但操作过程繁琐,而且样品的回收率不稳定,操作的重现性很差。
有的方法在对样品中VD3充分溶出作了考虑,但在处理过程中缺少抗氧、防吸附,减少干扰等措施,致使成分仍有损失而回收率偏低。
有文献报道,采用反相色谱系统测定,但对于脂溶性维生素采用反相系统,样品回收率不满意。
本文提供了一个实用、易操作的检测方法,无需进行皂化处理和反复萃取等繁琐操作,而是针对VD3性质不稳定,制剂成分复杂的情况,分别采取了避光、抗氧,抗干扰分离手段,取得了较好效果。
特别适用痕量VD3的准确测定。
该方法未见报道。
1 仪器与试药1.1 仪器Agilent 1200 HPLC系统,配紫外检测器。
紫外分光光度法测定维生素D3注射液的含量

紫外分光光度法测定维生素D3注射液的含量
文小静;孟丽红
【期刊名称】《医药世界》
【年(卷),期】2005(0)12
【摘要】目的测定维生素D3注射液的含量。
方法:采用紫外分光光度计在
265±1nm波长处测定维生素D3溶液的吸收度。
结果:维生素D3的浓度与吸收度呈良好的线性关系,r=0.9996,样品的平均吸收率为99.6%。
结论:本办法操作简单,实用性强,结果准确可靠。
【总页数】2页(P80-81)
【关键词】紫外分光光度法;维生素D3;吸收度
【作者】文小静;孟丽红
【作者单位】中国医科大学附属第四医院
【正文语种】中文
【中图分类】R977.24;R927.2
【相关文献】
1.紫外分光光度法测定维生素B12注射液含量的不确定度分析 [J], 李秀珍;刘风琴;吕光宇;李文;田海燕
2.紫外分光光度法测定维生素B12注射液含量的不确定度分析 [J], 秦立;陈诗慧;范亚刚
3.紫外分光光度法测定维生素B2注射液含量的不确定度分析 [J], 吕光宇;刘风琴;
李秀珍;李文
4.紫外分光光度法测定维生素 B1注射液含量的不确定度评价 [J], 马秋冉;张璐;董玲玲;杨星;赵富华;于晓辉
5.紫外分光光度法测定亚硒酸钠维生素E注射液及预混剂中维生素E含量 [J], 沈富林;王蓓;商军;蒋音
因版权原因,仅展示原文概要,查看原文内容请购买。
一维反相高效液相色谱法测定保健食品中维生素D2和维生素D3

一维反相高效液相色谱法测定保健食品中维生素D2和维生素D3分析检测一维反相高效液相色谱法测定保健食品中维生素D2和维生素D3刘剑易路遥* 晏亮吉伟佳虞雪军江西省药品检验检测研究院江西省药品与医疗器械质量工程技术研究中心章提出利用一维反相高效液相色谱法测定片剂、颗粒、软胶囊和硬胶囊保健食品中维生素D的含量。
方法:样品经淀粉酶水解,其中加入抗氧化剂;水解后加入氢氧化钾皂化,再用石油醚提取,经氮吹至近干,用甲醇溶解摇匀。
经0.22μm 有机滤膜过滤后供液相色谱仪分析。
以Thermo Accucore Polar Premium(100mm*4.6 mm)为分离柱,甲醇-乙腈为流动相,流速为0.8ml/min,进样量为20μL,在DAD波长264nm处作检测。
检出限为0.7μg/100g,方法中维生素D2平均回收率为93.7%-98.8% ;相对标准偏差0.5%-5.6 %;维生素D3平均回收率为92.8%-99.1% ;相对标准偏差0.3%-6.7 %。
该方法快速、简便、准确,适用于片剂、颗粒、软胶囊和硬胶囊保健食品中维生素D测定。
试验部分仪器与试剂。
高效液相色谱仪(美国,型号Ultimate),电子天平(美国,型号XS205DU)、紫外可见分光光度计(日本,型号U-3900),氮吹仪(美国Orgnomation公司)。
维生素D2(中国食品药品检定研究院)标准品和维生素D3标准品(中国药品生物制品鉴定所)。
乙腈、甲醇、2,6-二叔丁基对甲酚、无水乙醇均为色谱纯;石油醚、抗坏血酸、氢氧化钾为分析纯;α-淀粉酶活力300U/mg。
标准溶液配制。
标准储备液的制备:精密称取维生素D2标准品11.86mg,置50mL棕色量瓶中,用乙醇溶解并稀释至刻度,摇匀。
精密称取维生素D3标准品12.09mg,置50mL棕色量瓶中,用乙醇溶解并稀释至刻度,摇匀;于4℃条件下储存备用。
标准储备液浓度的校正:精密吸取维生素D2和D3标准储备液各500μl于各10ml棕色容量瓶中,用乙醇定容至刻度,混匀,分别用1cm比色皿中,以无水乙醇为空白参比,在264nm波长处测定吸光值,得维生素D2储备液浓度为222.4μg/ml和维生素D3储备液浓度为236.8μg/ml。
维生素D的含量检验方法

维生素D的含量检验方法 The Standardization Office was revised on the afternoon of December 13, 2020维生素D3的含量检验方法含量检验操作规程,保证分析结果的准确性。
一、目的:建立维生素D3二、依据:GB/T三、范围:本规程适用于本公司维生素D3含量检验操作四、职责:质量检验员对本标准的实施负责五、正文:1、试制和溶液高峰氏淀粉酶(Taka-Diastase)异丙醇:色谱纯焦性没食子酸的乙醇溶液15g/L氢氧化钾溶液:质量比100:50石油醚:沸程30~60甲醇:重蒸后使用。
正己烷:色谱纯。
环己烷:色谱纯维生素D3标准储备液:含维生素D3100ug/ml(称取10mg维生素 D3,用甲醇定容于100ml量瓶中)维生素D3标准工作液:取维生素D3标准储备液1ml于100ml量瓶中,用甲醇定容。
2、实验室常用仪器。
高效液相色谱仪:具有可变波长的紫外分光检测器、数据处理系统或记录仪。
平底烧瓶:250ml分液漏斗:500ml旋转蒸发器。
3 分析步骤试样处理准确称取10g样品,放入250ml平底烧瓶中,加入1gTaka淀粉酶(),再加入30ml45~50℃的蒸馏水,混合均匀后,用氮气排除瓶中空气,盖上瓶塞,置45℃烘箱内30min,于上述样品中加入100ml没食子酸的乙醇溶液(),充分混匀后加入50ml氢氧化钾溶液(),在蒸汽浴上回流30min后,立即冷却到室温。
将冷却后的皂化液转入500ml分液漏斗中,用100ml水分几次冲洗平底烧瓶,洗涤液并入分液漏斗中;于分液漏斗中加入100ml石油醚(),盖好瓶塞,倒置分液漏斗并剧烈振摇1min,静置分层,将水相放入另一500ml分液漏斗中。
重复上述萃取过程二次,合并醚液到第一个分液漏斗中。
用蒸馏水洗至中性,通过无水硫酸钠过滤干燥,在40℃和氮气流下,于旋转蒸发器上蒸至近干后,用石油醚转移至10ml量瓶中,定容。
反相高效液相色谱法测定补钙保健品中的维生素D_3

流动相 甲醇 水 检测波长
流 室温 ∀
标准溶液的配制 用无水乙醇配 制
Ù 维生素
速 标准溶液
储于
ε 的冰箱中备用 ∀
实验结果
磨口具塞锥形 后 放入超声 波 清 氯仿洗滤 梨形瓶中 在旋 无水
样品处理 称取适量待测样品 置于 氯仿浸泡
线性关系及灵敏度 取浓度为
∗ Ù 的维生素
进行
瓶中 加入 洗器中振荡 渣再用 渣 ∗
回收率试验 称取不同批号的补钙宝各 份 分别加入已知量 标样 按本法提取维生素
∀ Λ
不必经过皂化 ∀我们分别采用无水乙醇 乙醚 氯仿 作萃取液 结果表明 对氯仿萃取后的样液进行色谱 分离时 分离效果最佳 ∀ 维生素 献 是一种与人体健康关系密切的重 要物质 ∀本法简化了以往的操作步骤 并将本法与文
讨论
有些补钙品中添加了奶粉 测定时蛋白质会 干扰分离 降低色谱柱寿命 因此在用无水乙醇定容 时 如发现沉淀必须先离心除去 才能进行分析 ∀ 提取后的样液中可能有些杂质同时被萃取 因此必须调节流动相中甲醇和水的比例 使维生素 在
∗
ห้องสมุดไป่ตู้样品编号
文献法
本法
之间出峰 否则会使测定结果偏高 ∀ 补钙品中的维生素 是添加的 测定时样品
Ξ
本文收稿日期
修回日期
期
吴红京等 反相高效液相色谱法测定补钙保健品中的维生素
进行样品预处理 结果列于表 ∀
表 两种预处理方法测定维生素 ∆ 含量的结果 Λ Ù
Ταβλ ε Ρ εσ υλ τσ οφ ϖιτα ιν ∆ ωιτη διφφερεντ ρε- τρεατ εντ ετηοδσ Λ Ù
饲料中维生素D3的测定 高效液相色谱法-最新国标

1范饲料中维生素D3的测定高效液相色谱法围本文件描述了饲料中维生素D3的高效液相色谱测定方法。
本文件中“第一法皂化提取法”适用于配合饲料、精料补充料、浓缩饲料、复合预混合饲料、维生素预混合饲料中维生素D3的测定,定量限为12.5μg(500IU)/kg。
本文件中“第二法直接提取法”适用于维生素预混合饲料中维生素D3的测定,定量限为25mg (100万IU)/kg。
2规范性引用文件下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。
其中,注日期的引用文件,仅该日期对应的版本适用于本文件;不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T6682分析实验室用水规格和试验方法GB/T20195动物饲料试样的制备3术语和定义本文件没有需要界定的术语和定义。
4第一法皂化提取法注意:使用的器皿不含有氧化性物质;分液漏斗活塞玻璃表面不涂油,处理过程在避光下操作;提取过程在通风柜中操作。
4.1原理试样用碱溶液皂化后,高含量的预混合饲料皂化液经液液萃取或固相萃取净化、浓缩后,直接上反相高效液相色谱仪分离、测定,外标法测定;而低含量试样的皂化液则需在液液萃取或离线或在线固相萃取净化后,经一维色谱柱进一步分离净化,然后切换至二维反相色谱柱分离、测定,外标法定量。
4.2试剂或材料除非另有规定,仅使用分析纯试剂。
4.2.1水:GB/T6682,一级。
4.2.2无水乙醇:色谱纯。
4.2.3无水乙醇。
4.2.4石油醚(沸程30℃-60℃)。
4.2.5甲醇:色谱纯。
4.2.6乙腈:色谱纯。
4.2.7甲酸。
4.2.8异丙醇:色谱纯。
4.2.9L-抗坏血酸。
4.2.10二丁基羟基甲苯(BHT)。
4.2.11无水硫酸钠。
4.2.24.2.12氢氧化钾溶液(500g/L ):称取500g 氢氧化钾,加水溶解,冷却后用水定容至1L ,混匀。
4.2.13乙醇溶液I(70%,体积分数):量取无水乙醇70mL,用水稀释,定容至100mL ,混匀。
维生素D3 100CWS检验操作记录
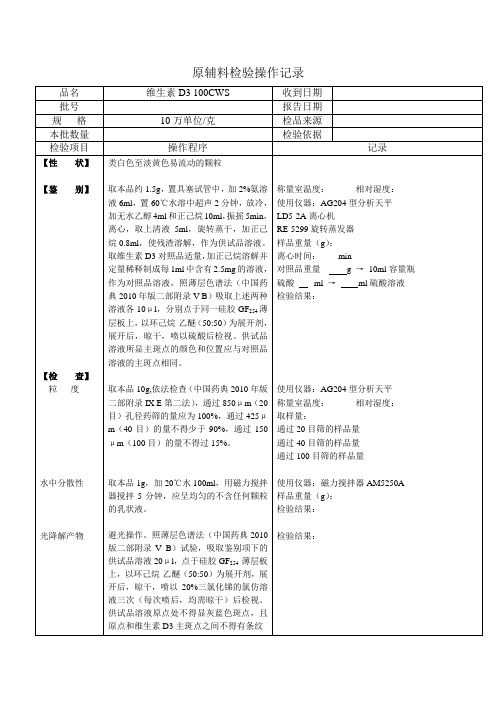
对照品溶液的配制:称取10.0mg维生素D3,用流动相溶解并稀释至100ml作为对照品贮备液,精密量取10ml,用流动相稀释至50ml作为对照品溶液。
取本品10g,依法检查(中国药典2010年版二部附录IX E第二法),通过850μm(20目)孔径药筛的量应为100%,通过425μm(40目)的量不得少于90%,通过150μm(100目)的量不得过15%。
取本品1g,加20℃水100ml,用磁力搅拌器搅拌5分钟,应呈均匀的不含任何颗粒的乳状液。
避光操作。照薄层色谱法(中国药典2010版二部附录V B)试验,吸取鉴别项下的供试品溶液20μl,点于硅胶GF254薄层板上,以环己烷-乙醚(50:50)为展开剂,展开后,晾干,喷以20%三氯化锑的氯仿溶液三次(每次喷后,均需晾干)后检视。供试品溶液原点处不得显灰蓝色斑点,且原点和维生素D3主斑点之间不得有条纹
平均含量:
检验项目
操作程序
记录
S样样品峰面积
M样样品称样量(g)
10样品稀释体积(ml)
0.025每单位维生素D3重量(μg)
每克含维生素D3(C27H44O)应为100,000~110,000单位。
相对偏差=—————————×100%=
结论
本品按检验,结果
检验人/日期
复核人/日期
供试品溶液的配制:称取样品80.0mg(相当于维生素D3 200μg),加入60%乙醇溶液20ml,涡旋振摇1min,加入正己烷20ml,涡旋振摇4min,4000r/min离心10min,分离,上层正己烷层分至分液漏斗,下层水层分回离心管,再加入正己烷20ml,涡旋振摇4min,4000r/min离心5min,重复前次分离操作,水层弃去,合并正己烷层,40-50℃水浴旋转蒸干,在氮气保护下,精密加入流动相10ml,滤过,续滤液作为供试品溶液。
维生素d3粉剂质量标准

维生素d3粉剂质量标准一、概述维生素D3是人体必需的营养素之一,具有调节钙磷代谢、促进骨骼生长和免疫调节等重要作用。
随着人们对健康的关注日益增加,维生素D3的需求也逐渐增大。
为了规范市场,提高产品质量,本文制定了维生素D3粉剂的质量标准。
二、质量标准1. 外观性状维生素D3粉剂应为淡黄色至黄绿色的粉末,无杂质,无异味。
不得含有肉眼可见的杂质,如色斑、结块等。
2. 鉴别试验采用紫外可见分光光度法进行鉴别。
取适量样品,用适量甲醇溶解,在265nm的波长处测定吸光度,应符合规定。
同时可采用液相色谱法或气相色谱法等分离方法对样品进行进一步的鉴别。
3. 含量测定采用高效液相色谱法进行含量测定。
色谱柱应为硅胶柱或C18柱,流动相为甲醇-水(70:30),流速为1.0ml/min,检测波长为265nm。
将样品适量溶解于甲醇中,进样分析,根据保留时间和峰面积与标准品比较确定维生素D3的含量。
经多次试验验证,该方法的线性范围为0.5-5.0mg/ml,回收率应在95%-105%之间,相对标准偏差应小于2%。
4. 杂质限量(1)重金属:采用原子吸收光谱法或原子荧光光谱法测定样品中的重金属含量,如铅、汞等。
根据测得的数据计算最大允许限量。
参考国家相关标准,重金属限量应符合规定。
(2)有机杂质:采用高效液相色谱法或气相色谱法等分离方法对样品进行分离分析,确定有机杂质的种类和含量。
根据测得的数据计算最大允许限量。
参考国家相关标准,有机杂质限量应符合规定。
5. 微生物限度采用常规微生物培养法对样品进行微生物限度检查,包括细菌总数、霉菌总数、酵母菌总数等指标。
根据测得的数据计算最大允许限量。
参考国家相关标准,微生物限度应符合规定。
三、结论本文制定了维生素D3粉剂的质量标准,包括外观性状、鉴别试验、含量测定、杂质限量和微生物限度等方面。
通过该标准的实施,可以规范市场秩序,提高产品质量,保障消费者的健康安全。
同时,对于生产企业而言,也可以通过遵循本标准提高生产工艺和技术水平,提升产品质量和竞争力。
反相高效液相色谱法测定维生素D2和维生素D3

反相高效液相色谱法测定维生素D2和维生素D3许强;刘金生;王轶鹏;张志涛;孙晓萌【摘要】提出了用反相高效液相色谱法(RP—HPLC)分离和测定胶囊、油状试剂中维生素D2及维生素D3的含量。
样品用甲醇超声提取,提取液用甲醇定容至100mL,经0.45μm滤膜过滤后供HPLC分析。
采用Zorbax SB-C18反相色谱柱及C18保护柱作为分离柱,乙腈作为流动相,流量为1.0mL·min^-1,在波长265nm处作紫外检测,进样量为20μL。
维生素D2和维生素D3的质量浓度在0.50-20mg·L^-1范围内与相应的峰面积呈线性关系,测得检出限(3S/N)依次为0.030,0.026mg·L^-1。
此方法应用于实样分析并在此基础用标准加入法做回收试验,同时进行精密度试验,测得回收率在95.0%~99.4%之间,测定值的相对标准偏差(n=6)在1.2%~2.6%之间。
%Vitamin D2 and D3 either in capsules or in oil preparations were determined by RP-HPLC. The sample was extracted ultrasonically with methanol. The extract was diluted to 100 mL with rnethanol, which was used for HPLC analysis after filtering on 0. 45 μm filtering membrane. The reverse phase chromatographic column Zorbax SB-C18 and the protective column C18 were used for separation with pure acetonitrile as mobile phase (flow rate 1.0mL·min^-1 ). UV detection at the wavelength of 265 nm was adopted in the deternaination. Volume of sample solution taken for introduction was 20 μL. Linear relationships between values of peak area and mass concentration of both Vitamin D2 and D3 were found in the same range of0.50-20mg·L^-1. Detection limit (3S/ N)of 0. 030 mg·L^-1. was foundf or Vitamin D2 and 0. 026 mg·L^-1. for Vitamin D3. This method was usedin analysis of substancial samples and using these samples as matrixes, tests for recovery were made by standard addition method, values of recovery were found in the range of 95.0%~99.4%, with values of RSD's (n=6) in the range of 1.2 %- 2.6 %.【期刊名称】《理化检验-化学分册》【年(卷),期】2011(047)010【总页数】3页(P1168-1169,1172)【关键词】反相高效液相色谱法;维生素D2;维生素D3【作者】许强;刘金生;王轶鹏;张志涛;孙晓萌【作者单位】山东省医学科学院基础医学研究所,济南250062;山东省医学科学院基础医学研究所,济南250062;山东省医学科学院基础医学研究所,济南250062;山东省医学科学院基础医学研究所,济南250062;山东省医学科学院基础医学研究所,济南250062【正文语种】中文【中图分类】O652.63维生素D是一种脂溶性维生素,主要作用是调节人体内钙和磷的代谢,促进其吸收利用,促进骨骼成长,目前已知的维生素D至少有10种,但最重要的是维生素D2和维生素D3[1]。
复方钙片中维生素D3的含量测定

复方钙片中维生素D3的含量测定目的建立高效液相色谱法测定复方钙片中维生素D3的含量。
方法采用Venusil MPC18(4.6×250 mm,5 μm)色谱柱;流动相:甲醇;流速:1 ml/min;检测波长:265 nm;柱温:25℃;进样量:20 μl。
结果维生素D3在0.6~3.0 μg/ml 的范围内有良好的线性关系,平均回收率为98.62%。
结论本实验建立的高效液相色谱法快速,简便,准确,可用于复方钙片中维生素D3的含量测定。
标签:维生素D3;高校液相色谱法;含量测定维生素D为固醇类衍生物,具抗佝偻病作用,又称抗佝偻病维生素。
它可以帮助人体更好地吸收钙,增强骨骼韧性和密度,预防骨质疏松,此外还能预防很多慢性病像癌症,糖尿病,风湿性关节炎,多发性硬化,自体免疫等疾病[1-3]。
人体所需钙量因年龄、生理及病理等不同而异。
人们可以根据自己的需求适当补充维生素D和钙。
维生素D3是维生素D家族中的重要成员。
实验室前期制备了维生素D3和钙的复方制剂,为了控制该制剂中维生素D3的质量,建立了高效液相色谱法测定维生素D3的含量。
1仪器与试药Agilent1100高效液相色谱仪(美国安捷伦公司);KQ5200超声波清洗器(昆山市超声仪器有限公司);RJ-TGL-16C臺式高速离心机(无锡市瑞江分析仪器有限公司);复方钙片(本院自制);维生素D3对照品(1000611-200607,中国药品生物制品检定所);甲醇、乙醇均为分析纯。
2方法与结果2.1色谱条件色谱柱:Venusil MPC18(4.6×250 mm,5 μm);流动相:甲醇;流速:1 ml/min;检测波长:265 nm;柱温:25℃;进样量:20 μl。
2.2溶液的制备2.2.1对照品溶液的制备精密称取5 mg的维生素D3对照品置于250 ml的棕色量瓶中,用甲醇稀释至刻度,摇匀,使成为20 μg/ml的对照品溶液。
精密吸取该对照品溶液3 ml置于50 ml棕色量瓶中,加甲醇稀释至刻度,摇匀,制得1.2 μg/ml的对照品溶液。
一种维生素D3的提取方法、检测维生素D3含量的方法[发明专利]
![一种维生素D3的提取方法、检测维生素D3含量的方法[发明专利]](https://img.taocdn.com/s3/m/7acccf68e55c3b3567ec102de2bd960590c6d997.png)
专利名称:一种维生素D3的提取方法、检测维生素D3含量的方法
专利类型:发明专利
发明人:王高华,徐春霞,胡士现,高雄兵,张华州,吴秀玲,夏力,刘正普
申请号:CN202111254035.4
申请日:20211027
公开号:CN114088826A
公开日:
20220225
专利内容由知识产权出版社提供
摘要:本发明属于化学检测技术领域,具体涉及一种维生素D3的提取方法、检测维生素D3含量的方法。
本发明提供的维生素D3的提取方法,所述提取方法在避光条件下进行,包括以下步骤:将待测物与分散剂、抗氧剂、提取剂混合,得到待测物溶液;所述分散剂为二甲基亚砜和水的混合溶液,所述抗氧剂为2,6‑二叔丁基对甲酚,所述提取剂为正己烷;将所述待测物溶液进行提纯处理,得到维生素D3提取液。
本发明将分散和提取的步骤同时进行,以保证待测物中的维生素D3分散到溶液后立即被提取剂提取避免维生素D3的损失,显著提高了维生素D3的提取率,从而提高待测物中维生素D3含量的准确性。
申请人:昆明源瑞制药有限公司
地址:651701 云南省昆明市云南杨林工业开发区华狮路5号
国籍:CN
代理机构:北京高沃律师事务所
代理人:霍苗
更多信息请下载全文后查看。
维生素D3的含量检验方法

维生素D3的含量检验方法一、目 的:建立维生素D3含量检验操作规程,保证分析结果的准确性。
二、依 据:GB/T 5413.9-1997三、范 围:本规程适用于本公司维生素D3含量检验操作四、职 责:质量检验员对本标准的实施负责五、正 文:1、试制和溶液1.1 高峰氏淀粉酶(Taka-Diastase)1.2 异丙醇:色谱纯1.3 焦性没食子酸的乙醇溶液15g/L1.4 氢氧化钾溶液:质量比100:501.5 石油醚:沸程30~601.6 甲醇:重蒸后使用。
1.7 正己烷:色谱纯。
1.8 环己烷:色谱纯1.9 维生素D3标准储备液:含维生素D3100ug/ml(称取10mg维生素D3,用甲醇定容于100ml量瓶中)1.10 维生素D3标准工作液:取维生素D3标准储备液1ml于100ml量瓶中,用甲醇定容。
2、 实验室常用仪器。
2.1 高效液相色谱仪:具有可变波长的紫外分光检测器、数据处理系统或记录仪。
2.2 平底烧瓶:250ml2.3 分液漏斗:500ml2.4 旋转蒸发器。
3 分析步骤3.1 试样处理准确称取10g样品,放入250ml平底烧瓶中,加入1gTaka淀粉酶(3.1),再加入30ml45~50℃的蒸馏水,混合均匀后,用氮气排除瓶中空气,盖上瓶塞,置45℃烘箱内30min,于上述样品中加入100ml没食子酸的乙醇溶液(3.3),充分混匀后加入50ml氢氧化钾溶液(3.4),在蒸汽浴上回流30min后,立即冷却到室温。
将冷却后的皂化液转入500ml 分液漏斗中,用100ml水分几次冲洗平底烧瓶,洗涤液并入分液漏斗中;于分液漏斗中加入100ml石油醚(3.5),盖好瓶塞,倒置分液漏斗并剧烈振摇1min,静置分层,将水相放入另一500ml分液漏斗中。
重复上述萃取过程二次,合并醚液到第一个分液漏斗中。
用蒸馏水洗至中性,通过无水硫酸钠过滤干燥,在40℃和氮气流下,于旋转蒸发器上蒸至近干后,用石油醚转移至10ml量瓶中,定容。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
维生素D3的含量检验方法
一、目的:建立维生素D3含量检验操作规程,保证分析结果的准确性。
二、依据:GB/T 5413.9-1997
含量检验操作
三、范围:本规程适用于本公司维生素D
3
四、职责:质量检验员对本标准的实施负责
五、正文:
1、试制和溶液
1.1 高峰氏淀粉酶(Taka-Diastase)
1.2 异丙醇:色谱纯
1.3 焦性没食子酸的乙醇溶液15g/L
1.4 氢氧化钾溶液:质量比100:50
1.5 石油醚:沸程30~60
1.6 甲醇:重蒸后使用。
1.7 正己烷:色谱纯。
1.8 环己烷:色谱纯
1.9 维生素D3标准储备液:含维生素D3100ug/ml(称取10mg维生素D3,用甲醇定容于100ml量瓶中)
1.10 维生素D3标准工作液:取维生素D3标准储备液1ml于100ml量瓶中,用甲醇定容。
2、实验室常用仪器。
2.1 高效液相色谱仪:具有可变波长的紫外分光检测器、数据处理系统或记录仪。
2.2 平底烧瓶:250ml
2.3 分液漏斗:500ml
2.4 旋转蒸发器。
3 分析步骤
3.1 试样处理
准确称取10g样品,放入250ml平底烧瓶中,加入1gTaka淀粉酶(3.1),再加入30ml45~50℃的蒸馏水,混合均匀后,用氮气排除瓶中空气,盖上瓶塞,置45℃烘箱内30min,于上述样品中加入100ml没食子酸的乙醇溶液(3.3),充分混匀后加入50ml氢氧化钾溶液(3.4),在蒸汽浴上回流30min后,立即冷却到室温。
将冷却后的皂化液转入500ml分液漏斗中,用100ml水分几次冲洗平底烧瓶,洗涤液并入分液漏斗中;于分液漏斗中加入100ml石油醚(3.5),盖好瓶塞,倒置分液漏斗
并剧烈振摇1min,静置分层,将水相放入另一500ml分液漏斗中。
重复上述萃取过程二次,合并醚液到第一个分液漏斗中。
用蒸馏水洗至中性,通过无水硫酸钠过滤干燥,在
40℃和氮气流下,于旋转蒸发器上蒸至近干后,用石油醚转移至10ml量瓶中,定容。
吸取7ml醚液至一试管中,用氮气将醚液吹干,加入1ml正己烷,即得供试品溶液。
3.2测定
3.2.1测定液的制备
仪器条件
色谱柱:30cm×40mm,硅胶柱
流动相:环己烷(3.7)与正己烷(3.8)按体积比1:1混合,并按体积分
数0.8%加入异丙醇(3.2)
流速:1ml/min
波长:265nm
柱温:20℃
灵敏度:0.005AU/MV
注射体积:200ul
制备:注射50ul维生素D标样和200ul样品溶液(试管B),根据维生素D
标样的保
留时间收集维生素D与试管C中,将试管C用氮气吹干,准确加入0.2ml甲醇(3.6)溶解。
3.2.2 测定步骤
仪器条件
色谱柱:25cm×4.6mm,C18或等同性能的色谱柱
流动相:甲醇
流速:1ml/min
柱温:20℃
波长:265nm
灵敏度:0.005AU/MV
注射体积:50ul
注射50ul维生素D标准溶液,注射50ul样品溶液(试管C中),得到标样和样品溶、液中维生素D峰面积或峰高
4、计算:
Cs ×10/75 ×100 ×40
m ×1000
样品中维生素D(IU/100g) =
Cs = × C sd
式中:Cs —进样液中维生素D 的质量浓度,ug/ml
m —样品的质量,g
A S —进样液中维生素D 的峰高(或峰面积) A Sd —标样中维生素D 的峰高(或峰面积) C sd —标样中维生素D 的质量浓度,ug/ml 计算结果精确到小数点后一位。
如有侵权请联系告知删除,感谢你们的配合!
A S A Sd。
