化工原理氧解吸实验报告
氧解析-化工原理-吸收-实验报告

氧解析-化工原理-吸收-实验报告一、实验目的1. 学习氧解析法的基本原理和实验操作。
2. 了解化学吸收法的原理及其在氧解析中的应用。
3. 掌握氧解析实验中的基本操作技能。
二、实验原理1.氧解析原理氧解析的原理是利用红色五价铁离子与氧气发生氧化反应的原理,通过测定铁离子还原的电位差来确定氧气的含量。
具体反应式如下:Fe2+ + 1/4O2 + 2H+ → Fe3+ + 1/2H2O由于1mol电子交换可产生1.23V电势,通过测定铁离子还原电位和标准电极电位的差值,即可得到氧气的含量。
2.化学吸收原理化学吸收法是通过某种吸收剂与被测气体的化学反应来去除被测气体中的某种成分的方法。
吸收剂可选择性地吸收被测气体中的某种成分,然后通过吸收前后吸收剂的质量差来确定该成分的含量。
在氧解析中,选择NaOH作为吸收剂,用于吸收氧气。
三、实验步骤1. 洗涤仪器:将氧解析仪、吸收瓶、饱和盐水瓶和试管用酒精清洗干净。
2. 理顺连接线:将氧解析仪与吸收瓶通过橡胶软管连接,吸收瓶与饱和盐水瓶通过橡胶软管连接,饱和盐水瓶与试管通过橡胶软管连接。
3. 加入吸收剂:将20mL的0.1mol/L NaOH溶液倒入吸收瓶中。
4. 预处理:将氧解析仪的样品室和参比室用稀硝酸洗涤干净,然后用蒸馏水冲洗干净。
5. 校准:用样品室中的氧气校准氧解析仪,通过调节样品室中的Hg电极电势,使得氧解析仪显示的氧气浓度与标准气体浓度一致。
6. 吸氧:将被测气体(氮气与氧气混合气体)通过饱和盐水瓶并以一定流速进入吸收瓶,其中氧气被NaOH吸收,剩余的氮气流经氧解析仪,接着通过排气口排出实验室。
7. 计算:通过测定吸收剂的重量差和转化率计算氧气的含量。
四、实验结果与分析实验中测得的吸收剂重量差为0.23g,转化率为95%,因此氧气的含量为100%-95%=5%。
五、实验结论本实验通过氧解析法和化学吸收法,成功测定了氧气的含量。
实验结果表明本实验的测量结果较为准确,具有较高的稳定性和重复性,可有效满足实际应用需求。
化工原理氧解吸实验报告

化工原理氧解吸实验报告(文章一):氧解吸实验报告化工原理实验实验题目:——氧解吸实验姓名:沈延顺同组人:覃成鹏臧婉婷王俊烨实验时间:2xxx.10。
24(一)、实验名称:氧解吸实验(二)、姓名:沈延顺2xxx62092(三)、同组人:覃成鹏、藏婉婷、王俊烨(四)、实验目的:(1)、熟悉填料塔的构造与操作。
(2)、观察填料塔流体力学状况,测定压降与气速的关系曲线。
(3)、掌握液相体积总传质系数Kxa的测定方法并分析影响因素。
(4)、学习气液连续接触式填料塔,利用传质速率方程处理传质问题的方法。
(五)、实验原理:实验依次测量空塔,湿塔的流体力学性能,再使用本装臵,先用吸收柱使水吸收纯氧形成富氧水后,送入解吸塔顶再用空气进行解吸。
测定塔顶塔底的溶液溶氧度,温度,塔内压降,液气流速等物理性质,计算出传质系数并与其它实验小组不同填料进行比较。
(1)、填料塔流体力学特性气体通过干填料层时,流体流动引起的压降和湍流流动引起的压降规律相一致。
填料层压降—空塔气速关系示意图如下,在双对数坐标系中,此压降对气速作图可得一斜率为1.8~2的直线(图中aa’)。
当有喷淋量时,在低气速下(c点以前)压降正比于气速的1.8~2次幂,但大于相同气速下干填料的压降(图中bc段)。
随气速的增加,出现载点(图中c点),持液量开始增大,压降—气速线向上弯,斜率变陡(图中cd段)。
到液泛点(图中d点)后,在几乎不变的气速下,压降急剧上升。
其中u=G/? G?G(2)、传质实验在填料塔中,两相传质主要在填料有效湿表面上进行,需要计算完成一定吸收任务所需的填料高度,其计算方法有传质系数、传质单元法和等板高度法。
本实验是对富氧水进行解吸,如图下所示。
由于富氧水浓度很低,可以认为气液两相平衡关系服从亨利定律,及平衡线位臵线,操作线也是直线,因此可以用对数平均浓度差计算填料层传质平均推动力。
整理得到相应的传质速率方程为Vp△x m)GA=KxaVp△x m 即Kxa= GA / (其中??m?(x2-xe2)?(x1?xe1) (x2?xe2)ln[](x1?xe1) GA=L(x2-x1)Vp=Z? xe1=ye1/mxe2=ye2/m m=E/p p=Pa+0.5△p E=(-8.5694×10-5t2+0.07714t+2.56)×106 式中:GA——单位时间内氧的解吸量,kmol/(m2?h) Kxa——液相体积总传质系数,kmol/(m3?h) Vp——填料层体积,m3 △x m——液相对数平均浓度差x2——液相进塔时的摩尔分数(塔顶)xe2——与出塔气相y1平衡的摩尔分数(塔顶)x1——液相出塔的摩尔分数(塔底)xe1——与进塔气相y1平衡的摩尔分数(塔底)Z——填料层高度,m ?——塔截面积,m2 L——解吸液流量,kmol/(m2?h) m——摩尔亨利系数,1 p——塔内平均压力,kpa E——每气体分压的亨利系数,kpa t——塔内平均温度,℃由于氧气为难容气体,在水中的溶解度很小,因此传质阻力几乎全部集中在液膜中,即Kx=kx,由于属液膜控制过程,所以要提高液相体积总传质系数Kxa,应增大液相的湍动程度即增大喷淋量。
吸收(解吸)实验报告

吸收(解吸)实验报告化⼯基础实验报告实验名称吸收(解吸)系数的测定班级化21 姓名张腾学号2012011864 成绩实验时间2014.5 同组成员张煜林努尔艾⼒·麦麦提⼀、实验⽬的1、了解吸收(解析)操作的基本流程和操作⽅法;2、测定氧解吸液相总体积传质系数K x a和液体流量的关系;3、测定筛板塔的板效率与液体流量和⽓体流量的关系。
⼆、实验原理吸收是⼯业上常⽤的操作。
在吸收过程中,⽓体混合物和吸收剂分别从塔底和塔顶进⼊塔内,⽓液两相在塔内实现逆流接触,使⽓体混合物中的溶质较完全地溶解在吸收剂中,于是塔顶获得较纯的惰性组分,从塔底得到溶质和吸收剂组成的溶液(通称富液)。
当溶质有回收价值或吸收剂价格较⾼时,把富液送⼊再⽣装置进⾏解吸,得到溶质或再⽣的吸收剂(通称贫液),吸收剂返回吸收塔循环使⽤。
吸收是⽓液相际传质过程,所以吸收速率可⽤⽓相内,液相内或者两相间的传质速率来表⽰。
在连续吸收操作中,这三种传质速率表达式计算结果相同。
对于低浓度吸收过程。
计算公式如下。
⽓相内传质的吸收速率:N A=k y(y?y i)F液相内传质的吸收速率:N A=k x(x i?x)F⽓、液两相相际传质的吸收速率:N A=K y F(y?y?)=K x F(x??x)式中:y,y i—分别表是⽓相主体和⽓相界⾯处的溶质摩尔分率;x,x i—分别表⽰液相主体和液相界⾯处的溶质摩尔分率;x?,y?—分别为与y和x呈平衡的液相和⽓相摩尔分率;k x,K x—分别为以液相摩尔分率差为推动⼒的液相传质分系数和传质总系数;k y,K y—分别为以⽓相摩尔分率差为推动⼒的⽓相传质分系数和传质总系数;F—传质⾯积,m2。
对于难溶溶质的吸收,常⽤液相摩尔分率差和液相传质系数表达的吸收速率式。
对于易溶⽓体的吸收,常⽤⽓相摩尔分率差和⽓相传质系数表达的吸收速率式。
本实验为⼀解析过程,是⽤空⽓与富氧⽔接触,因富氧⽔中氧的浓度⾼于同空⽓处于平衡的⽔中氧的浓度。
氧解吸实验报告 北京化工大学

北京化工大学化工原理实验报告实验名称:氧解吸实验班级:化工姓名:学号:序号:同组人:设备型号:第套实验日期:2014-4-01一、实验摘要本实验测定不同气速下干塔和湿塔的压降,得到了填料层压降—空塔气速关系曲线,确定塔的处理能力及找到最佳操作点。
然后用吸收柱使水吸收纯氧形成富氧水,送入解析塔再用空气进行解吸,进而可计算出不同气液流量比下液相体积总传质系数K x a ,液相总传质单元高度H OL ,液相总传质单元数N OL 。
关键词:氧气 解吸 液相体积总传质系数 液相总传质单元高度 液相总传质单元数二、实验目的1、测量填料塔的流体力学性能;2、测量填料塔的吸收-解吸传质性能;3、比较不同填料的差异。
三、实验原理1、填料塔流体力学性能为保证填料塔的正常运行,通常需要控制操作气速处于液泛气速的0.5~0.8倍之间。
如图1,在双对数坐标系下,气体自下而上通过干填料层时,塔压降ΔP 与空塔气速u 复合关系式ΔP=u 1.8~2.0。
当有液体喷下,低气速操作时,ΔP ∝u 1.8~2.0,此时的ΔP 比无液体喷淋时要高。
气速增加到d 点,气液两相的流动开始相互影响,ΔP ∝u 0.2以上,此时的操作点成为载液2点。
气速再增加到e 点时,气液两相的交互影响恶性发展,导致塔内大量积液且严重返混,ΔP ∝u 10以上,此时的操作点称为液泛点,对应的气速就是液泛气速。
本实验直接测量填料塔性能参数,确定其液泛气速,还可用公式法、关联图法等确定。
全塔压降直接读仪表,空塔气速u 由孔板流量计测定:s P A V u /m 1.07854.025.110002(018.07854.061.025.02⨯÷⨯∆⨯⨯⨯⨯==)孔板。
2、填料塔传质性能——考察氧解吸过程的液相体积传质系数K x a 。
以氧气为溶质,解吸塔内空气、水的摩尔流率不变,水温恒定。
根据低含量气体吸收解吸全塔传质速率方程可知:⎰-⋅=⨯=21;x x ex OL O x x dx a K L N H H 。
化工原理氧解吸实验报告

化工原理氧解吸实验报告实验目的:通过氧解吸实验,研究化工原理中氧解吸的过程及其影响因素,探究氧解吸速率与温度、压力、液体性质等因素之间的关系。
实验原理:氧解吸是指气体从液体中解吸出来的过程,是化工反应过程中的重要环节之一。
氧解吸速率与温度、压力、液体性质等因素密切相关。
根据亨利定律,气体的溶解度与压力成正比,与温度成反比。
因此,温度和压力是影响氧解吸速率的重要因素。
此外,液体的性质也会影响氧解吸速率,如液体的粘度、表面张力等。
实验仪器与试剂:1. 仪器:氧解吸实验装置、温度计、压力计、计时器等。
2. 试剂:氧气、水、酒精等。
实验步骤:1. 准备实验装置:将氧解吸实验装置连接好,确保密封性良好。
2. 调节温度和压力:根据实验要求,调节实验装置中的温度和压力,记录下初始值。
3. 添加试剂:向实验装置中加入一定量的水和酒精,保证液体的混合均匀。
4. 开始实验:打开氧气进气阀,使氧气进入实验装置,开始氧解吸过程。
5. 记录数据:使用计时器记录氧解吸的时间,并记录下温度和压力的变化情况。
6. 完成实验:当氧解吸过程基本结束后,关闭氧气进气阀,停止实验。
实验结果与分析:根据实验记录的数据,可以得出以下结论:1. 温度对氧解吸速率有显著影响:随着温度的升高,氧解吸速率增加;而温度的降低则导致氧解吸速率减小。
2. 压力对氧解吸速率有显著影响:压力的增加会促使氧解吸速率增加;而压力的降低则导致氧解吸速率减小。
3. 液体性质对氧解吸速率有影响:液体的粘度和表面张力等性质会影响氧解吸速率,具体影响程度需要进一步研究。
结论:通过本次氧解吸实验,我们得出了温度、压力和液体性质对氧解吸速率的影响规律。
这些结果对于化工原理中的氧解吸过程的设计和优化具有重要的指导意义。
进一步的研究可以探究其他因素对氧解吸速率的影响,并进行更加详细的实验分析。
氧气的吸收与解吸实验报告

氧气的吸收与解吸实验报告一、实验目的探究氧气在水中的溶解与解吸过程,了解氧气在水中的溶解度与温度、压强的关系。
二、实验原理氧气在水中的溶解度与温度、压强和溶液中其他物质浓度有关。
当温度升高或压强降低时,氧气的溶解度会减小;而当温度降低或压强增加时,氧气的溶解度会增大。
此外,当水中其他物质浓度增加时,也会影响氧气的溶解度。
三、实验器材1. 水槽2. 水银汞柱3. 热水器4. 水银汞球四、实验步骤1. 将水槽内注满水,并放入一个水银汞柱。
2. 将热水器接通电源,将其放入水槽内加热。
3. 在热水器加热过程中,用手持式吸管将一只装有少量水银汞球的试管倒置于水槽内。
4. 观察试管内汞球变化情况,并记录下时间和温度。
5. 等热水器加热至一定温度后,关闭电源,等待水温下降。
6. 当水温下降至一定程度时,观察试管内汞球变化情况,并记录下时间和温度。
7. 将实验数据整理并进行分析。
五、实验结果在加热过程中,试管内的汞球逐渐变小;而在停止加热后,试管内的汞球逐渐变大。
随着时间的推移,汞球的大小逐渐趋于稳定。
六、实验分析根据实验结果可以得出结论:氧气在水中的溶解度与温度有关。
当水温升高时,氧气的溶解度减小;而当水温降低时,氧气的溶解度增大。
此外,在压强不变的情况下,溶液中其他物质浓度增加也会导致氧气的溶解度减小。
七、实验注意事项1. 实验过程中要注意安全。
2. 水槽内应注满水,并保持水平。
3. 实验过程中要注意控制热水器加热时间和温度。
4. 实验结束后要将器材清洗干净。
八、实验总结通过本次实验,我们了解了氧气在水中的溶解与解吸过程,并探究了氧气的溶解度与温度、压强和溶液中其他物质浓度的关系。
同时,我们也学会了如何进行实验并分析数据。
这些知识对我们深入理解化学原理和应用化学具有重要意义。
长江大学 氧吸收与解吸综合实验 实验报告

(3)掌握总传质系数 的测定方法并分析影响因素。
(4)学习气液连续接触式填料塔,利用传质速率方程处理传质问题的方
法。
(5)研究流体的流动对传质阻力的影响、吸收剂用量对传质系数的影响
和传质系数的影响和传质阻力较小侧流体的流量变化对吸收过程的影响,学会吸收过程的调节。
39883.677
5.265E-06
1.404E-05
5.416E-06
4.0593
4.79
101.64
39883.677
5.265E-06
1.254E-05
5.321E-06
4.8692
4.01
101.67
39873.870
5.266E-06
1.268E-05
5.523E-06
3.3620
3.98
0.1643
3
19
1.42
0.68
22.55
9.82
25506.22
0.2380
4
20
1.57
0.73
22.94
9.49
96144.75
0.1706
计算;
以第一组数据为例:
系统总压强:
相平衡常数:
六、思考题
i.为什么易溶气体的吸收和解吸属于气膜控制过程,难溶气体的吸收和
解吸属于液膜控制过程?
答:对于易溶气体而言,主要的阻力来自溶质从气相到气液界面扩散的阻力,从气液界面到溶液的过程所受到的阻力相对来说很小,所以在吸收过程显示为气膜控制过程;而对于难溶气体,吸收时受到的主要阻力是在气液界面到液相的过程中产生,而在气相到气液界面的阻力相对来说很小,所以其吸收的过程显示为液膜控制过程。
化工原理氧解吸实验报告

化工原理氧解吸实验报告
实验目的:
1.观察氧解吸的现象;
2.探究氧解吸速率与氧化剂浓度、温度、催化剂等因素的关系;
3.熟悉实验操作和实验仪器的使用。
实验原理:
氧解吸是指在一定温度和压力下,将溶解在液体中的氧气以气泡的形式分离出来的现象。
氧解吸反应的速率与氧化剂浓度、温度、催化剂等因素密切相关。
实验步骤:
1.将实验装置依次连接好,并将水槽中的水加热至80℃;
2.在试管中加入适量的含氧化剂的溶液,并加入催化剂;
3.将试管放入水槽中,注意控制试管的深度,以使试管中溶液面高于水槽水面;
4.打开气源,调节气流量,观察氧解吸的现象,并记录时间和气泡产生的数量;
5.改变实验条件(如氧化剂浓度、温度、催化剂种类或浓度等),重复步骤4,记录实验数据。
实验结果:
根据实验数据,我们可以绘制氧解吸速率与不同因素的关系曲线。
实验讨论:
1.氧化剂浓度对氧解吸速率的影响:当氧化剂浓度增加时,氧解吸速
率也会增加;
2.温度对氧解吸速率的影响:随着温度的升高,氧解吸速率也会增加;
3.催化剂对氧解吸速率的影响:催化剂可以提高氧解吸速率,不同催
化剂的效果可能不同;
4.实验操作的注意事项:试管放入水槽时,应使试管内的溶液高于水
槽水面,以防水被吸入试管;
实验结论:
通过本实验,我们观察了氧解吸的现象,并探究了氧解吸速率与氧化
剂浓度、温度、催化剂等因素的关系。
实验结果表明,氧解吸速率随着氧
化剂浓度和温度的增加而增加,催化剂可以提高氧解吸速率。
这些结果对
于理解氧解吸反应的机制,以及实际应用中的氧解吸过程具有重要的意义。
氧吸收解吸实验报告

氧吸收解吸实验报告氧吸收解吸实验报告引言:氧气是地球上最重要的元素之一,对于维持生命活动至关重要。
人类和其他生物通过呼吸将氧气吸入体内,然后将其与食物中的营养物质一起利用,产生能量和二氧化碳。
为了更好地理解氧气在生物体内的吸收和解吸过程,我们进行了一系列实验。
实验一:氧气吸收速率与温度的关系我们首先研究了氧气吸收速率与温度之间的关系。
为此,我们准备了三个试管,分别装有20°C、30°C和40°C的水。
在每个试管中,我们加入了相同量的酵母和蔗糖溶液。
然后,我们立即将一个试管放入恒温箱中,将另一个试管放在常温下,将第三个试管放入冰水中。
结果显示,随着温度的升高,氧气吸收速率明显增加。
在40°C的试管中,氧气吸收速率最高,而在冰水中的试管中,氧气吸收速率最低。
这表明温度对氧气吸收过程有显著影响,高温有利于氧气的吸收。
实验二:氧气解吸速率与压力的关系为了研究氧气解吸速率与压力之间的关系,我们使用了一个封闭的容器,并在其中放入了一定量的氧气和水。
然后,我们逐渐增加容器内的压力,观察氧气解吸的速率。
结果显示,随着压力的增加,氧气解吸速率也随之增加。
当压力达到一定值时,氧气解吸速率开始饱和,不再随压力的增加而增加。
这说明压力对氧气解吸过程有一定的影响,但并非线性关系。
实验三:氧气吸收速率与浓度的关系为了探究氧气吸收速率与浓度的关系,我们分别准备了不同浓度的氧气溶液。
然后,我们将相同量的酵母和蔗糖溶液加入不同浓度的氧气溶液中,并观察氧气吸收的速率。
结果显示,随着氧气浓度的增加,氧气吸收速率也随之增加。
当氧气浓度达到一定值后,氧气吸收速率开始饱和,不再随浓度的增加而增加。
这表明氧气浓度对氧气吸收过程有一定的影响,但并非线性关系。
结论:通过以上实验,我们可以得出以下结论:1. 温度对氧气吸收速率有显著影响,高温有利于氧气的吸收。
2. 压力对氧气解吸速率有一定的影响,但并非线性关系。
氧解吸实验报告

氧解吸实验报告1氧解吸实验报告一、实验简介氧解吸实验是一种用于研究材料在高温、高压条件下的吸氧性能的实验。
该实验通过测量不同条件下的吸氧量、吸氧速率等参数,评估材料的抗氧化性能和使用寿命。
本报告所提供的实验数据仅为本实验室的实验结果,不代表其他实验室或实际使用环境下的结果。
二、实验原理氧解吸实验主要基于材料的氧化还原反应。
在高温、高压条件下,材料表面的氧化膜逐渐形成。
当材料表面存在还原性气体(如氢气)时,氧化膜与还原性气体发生还原反应,产生金属和氧化物。
通过测量不同条件下的还原速率、还原量等参数,可以评估材料的抗氧化性能和使用寿命。
三、实验步骤1.样品准备选取待测试材料,制成标准样品。
将样品表面进行抛光处理,确保表面平整、光滑,无划痕、气孔等缺陷。
2.实验装置准备使用高压炉作为实验装置,确保炉内气氛可控,且能够保持高温、高压环境。
同时,需要配备气流量控制系统、压力控制系统、温度传感器等辅助设备。
3.实验过程将样品放入高压炉中,通入一定量的氧气,使样品表面形成一层氧化膜。
然后,通入一定量的还原性气体(如氢气),观察样品表面的氧化膜变化情况。
在一定时间间隔内,记录样品的重量变化(即还原量),同时测量炉内气氛中的氧气和还原性气体的浓度变化。
四、实验数据分析1.还原速率分析通过测量不同时间间隔内的还原量,可以计算出还原速率。
还原速率越快,说明材料的抗氧化性能越差。
可以通过控制不同的实验条件(如温度、压力、气体浓度等),观察这些条件对还原速率的影响。
2.氧化膜厚度分析在实验过程中,可以通过测量氧化膜的厚度变化,评估氧化膜的生长情况。
通过对不同条件下的氧化膜厚度进行分析,可以得出材料在高温、高压条件下的氧化动力学行为。
3.形貌分析通过观察实验前后的样品表面形貌,可以了解材料在高温、高压条件下的氧化行为和还原反应过程。
利用扫描电子显微镜(SEM)等设备对样品表面进行形貌分析,可以进一步了解氧化膜的形貌特征和结构变化。
氧吸收与解析实验报告

聿罿莄羄罿芀蚂填料参数:瓷拉西环(12×12×1.3)mm =903m2/m3 螀薃螅腿肂螁莅 2.流程:
at=403m2/m3
ε=0.764m3/m3
at/ε
图 蚃薇艿蕿羁膆艿 2 是氧气吸收解吸装置流程图。氧气由氧气钢瓶供给,经减压阀 2 进入氧
气缓冲罐 4,稳压在 0.04~0.05[Mpa],为确保安全,缓冲罐上装有安全阀 6,由阀 7 调节氧
蚈衿薅蒆薈膀袃由于气体流量与气体状态有关,所以每个气体流量计前均有表压计和温度计。
空气流量计前装有计前表压计 23。为了测量填料层压降,解吸塔装有压差计 22。
螁螄肄螈羂肃袇在解吸塔入口设有入口采出阀 12,用于采集入口水样,出口水样在塔底排液
平衡罐上采出阀 20 取样。
羇蒇蚁螂薆莇袂 HOL—以液相为推动力的传质单元高度
薇蒂袁莈蒇莀蒃 NOL—以液相为推动力的传质单元数
羀莅羅蚇膁薃薄由于氧气为难溶气体,在水中的溶解度很小,因此传质阻力几乎全部集中于液
请下载支持!
膜中,即 Kx=kx, 由于属液膜控制过程,所以要提高总传质系数 Kxa,应增大液相的湍动程度。
在 蒅螇袆蝿螃莆螆 y—x 图中,解吸过程的操作线在平衡线下方,本实验中还是一条平行于横
填料层压降与空塔气速的数据,并作图分析得到两种情况下塔压降与空塔气速关系,从而熟 悉填料塔的构造与操作、确定填料塔流体力学特性,进而得知填料塔的处理能力及性能高低。 同时,本实验通过对富氧水进行解吸,测定了解吸液相体积的总传质系数 Kxa,进而确定液 相总传质单元高度 HOL。 一、虿羄薄蚀袀节蒇实验名称:氧吸收与解吸实验 二、膄蒆蝿蚂蒂肅蚀目的及任务:
气流量,并经转子流量计 8 计量,进入吸收塔 9 中,与水并流吸收。含富氧水经管道在解吸
实验的一氧解析汇报汇报

实验一氧解吸实验课程名称:化工原理实验(下)实验日期: 2013.4.8班级:化工1001班姓名:陈双全同组人:李泽州、杨政鸿学号: 2010011018 一、摘要本实验首先通过分别测量干填料塔和湿填料塔的不同气速下的压降数据,验证了填料塔的流体力学特征,得出了填料层压降与空塔气速的关系。
用吸收塔使水吸收纯氧形成富氧水后,送入解吸塔顶再用空气进行解吸,实验需要测定不同液量和气量下的解吸液相体积总传质系数,得出液量和气量对总传质系数的影响趋势,同时对四种不同填料的传质效果及流体力学性能进行比较。
学习气液连续接触式填料塔,利用传质速率方程处理传质问题的方法。
关键词:氧解吸吸收塔解吸塔液相体积总传质系数。
二、目的及任务1.熟悉填料塔的构造与操作。
2.观察填料塔流体力学状况,测定压降与气速的关系曲线。
3.掌握液相体积总传质系数K x a的测定方法并分析影响因素。
4.学习气液连续接触式填料塔,利用传质速率方程处理传质问题的方法。
三、实验原理本装置先用吸收柱将水吸收纯氧形成富氧水后(并流操作),送入解吸塔顶再用空气进行解吸,实验需测定不同液量和气量下的解吸总传质系数K x a,得出液量和气量对总传质系数的影响趋势,同时对四种不同填料的传质效果及流体力学性能进行比较。
1.填料塔流体力学特性气体通过干填料层时,流体流动引起的压降和湍流流动引起的压降规律相一致。
填料层压降—空塔气速关系示意如图1所示,在双对数坐标系中,此压降对气速作图可得一斜率为1.8~2的直线(图中aa’)。
当有Array喷淋量时,在低气速下(c点以前)压降正比于气速的1.8~2次幂,但大于相同气速下干填料的压降(图中bc段)。
随气速的增加,出现载点(图中c点),持液量开始增大,压降—气速线向上弯,斜率变陡(图中cd段)。
到液泛点(图中d点)后,在几乎不变的气速下,压降急剧上升。
2.传质实验填料塔与板式塔气液两相接触情况不同。
在填料塔中,两相传质主要在填料有效湿表面上进行,需要计算完成一定吸收任务所需的填料高度,其计算方法有传质系数、传质单元法和等板高度法。
氧解吸实验报告1

氧解吸实验报告1一、实验目的:1、掌握氧解吸法气体吸附技术的原理和操作方法。
2、测定微孔材料的比表面积。
3、通过本实验,了解气体吸附实验技术的基本特点和原理,并学会分析和处理实验数据。
二、实验原理:当气体分子与固体表面接触时,分子势能发生变化,分子分散力弱化,发生与液体表面相同的吸引作用,这种作用叫做吸附作用。
气体吸附在固体表面上的化学、物理及其他性质的差异,可用不同的实验技术来检测和研究。
在常温常压下,氧气被准备好的样品吸收到孔内,被吸附到样品孔内。
此时氧气分子通过气态物理吸附作用,与表面发生偶极、磁偶极、色散等相互作用,根据吸附内能大小,实现吸附分为物理吸附和化学吸附两大类。
根据仪器所使用的吸附温度范围划分吸附分为低温吸附和高温吸附两大类。
低温吸附又称孔隙吸附,高温气相吸附。
孔隙吸附是指温度在77K以下时,在绝大多数低温吸附剂表面上的表现出的现象,常常用来研究吸附剂的孔结构。
孔隙吸附可分为毛细吸附和瞬间多分子层吸附。
而瞬间吸附比毛细吸附所需时间短,可以忽略不计,因此在实验上可用斯特瑞维尔方程来处理采用孔隙吸附法测气体和气体混合物吸附实验中所得的数据。
斯特瑞维尔方程式中,pi为相对饱和蒸气压,其值可由其他文献查得。
V为脱附柜体积的一半,即nitrogen gas纯氮体积,即可转换为具体的实验数据。
三、实验步骤:1、用微孔材料制备样品固体,称取0.10g±0.01g,摆于小特形脱附柜中,加热至50℃除去吸附在孔内的水分。
2、恢复脱附柜,根据实验计划记录实验条件,控制好实验过程中温度,时间等参数。
3、样品在液氮温下接触氮气使其充分吸收氮气,开动真空泵将孔内和柜内的氮气压降至一定值。
4、收集样品孔内气体脱附后的数据(在304kPa以上时收集脱附数据)。
5、依据实验条件计算氧气在样品中的比表面积。
4、实验结果:1、实验中计算得出氧气的比表面积为125.013m2/g。
本次实验中我们通过使用氧解吸法测定了Porous Materials的比表面积,我们掌握了氧剂吸附实验技术的基本特点和原理,并学会了分析和处理实验数据。
化工原理吸收与解吸实验报告

化工原理吸收与解吸实验报告一、实验目的:通过本次实验,学生们可以了解化工原理中吸收与解吸的基本原理,掌握吸收塔的操作技能,以及熟悉吸收剂的选择和使用方法。
二、实验原理:1. 吸收与解吸的基本原理吸收是指气体在接触液体时被液体所溶解或被化学反应转化为溶质的过程。
而解吸则是指气体从液体中逸出或分离出来的过程。
在化工生产过程中,常用于气体分离、纯化和回收等方面。
2. 吸收塔吸收塔是一种常见的设备,用于进行气液相接触和传质过程。
其主要结构包括进料口、出料口、填料层等。
填料层可以增加气液接触面积,提高传质效率。
3. 吸收剂吸收剂是指用于吸收气体的液体,在选择时需要考虑其对目标气体的亲和力、溶解度、稳定性以及成本等方面因素。
三、实验步骤:1. 将制备好的NaOH溶液倒入吸收塔中,并将塔内温度升至60℃左右。
2. 将CO2气体通过气体流量计和压力表接入吸收塔顶,调节气体流量和压力使其稳定。
3. 观察吸收塔内液位变化,记录液位高度和时间,计算出CO2的吸收速率。
4. 停止供气后,将塔内液体倒出并加入硫酸溶液进行解吸,记录解吸速率。
四、实验结果:1. 吸收速率:在60℃下,CO2的吸收速率为0.016mol/min。
2. 解吸速率:在添加硫酸溶液后,CO2的解吸速率为0.014mol/min。
五、实验分析:1. 实验结果表明,在所选条件下,NaOH溶液对CO2具有较好的亲和力和溶解度。
2. 在实际生产中,需要根据具体情况选择合适的吸收剂,并结合填料层设计等因素来提高传质效率。
六、实验结论:本次实验成功地展示了化工原理中吸收与解吸的基本原理,并通过操作塔内填料层等设备提高了传质效率。
同时还验证了NaOH溶液对CO2具有较好的亲和力和溶解度。
氧解吸实验
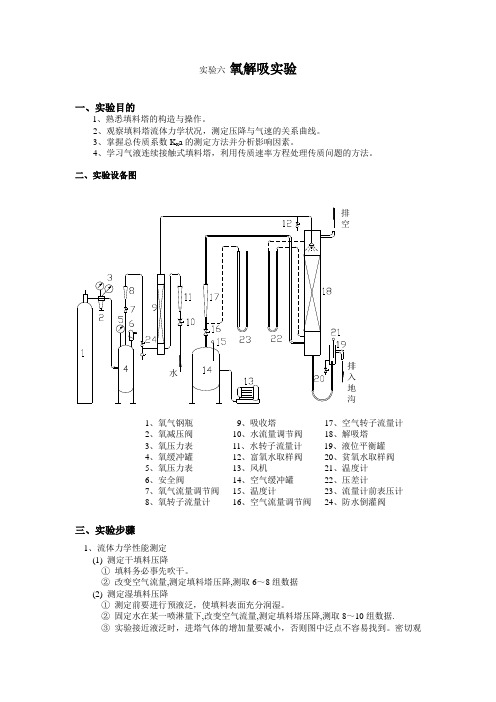
实验六氧解吸实验一、实验目的1、熟悉填料塔的构造与操作。
2、观察填料塔流体力学状况,测定压降与气速的关系曲线。
3、掌握总传质系数K x a的测定方法并分析影响因素。
4、学习气液连续接触式填料塔,利用传质速率方程处理传质问题的方法。
二、实验设备图1、氧气钢瓶9、吸收塔17、空气转子流量计2、氧减压阀10、水流量调节阀18、解吸塔3、氧压力表11、水转子流量计19、液位平衡罐4、氧缓冲罐12、富氧水取样阀20、贫氧水取样阀5、氧压力表13、风机21、温度计6、安全阀14、空气缓冲罐22、压差计7、氧气流量调节阀15、温度计23、流量计前表压计8、氧转子流量计16、空气流量调节阀24、防水倒灌阀三、实验步骤1、流体力学性能测定(1) 测定干填料压降①填料务必事先吹干。
②改变空气流量,测定填料塔压降,测取6~8组数据(2) 测定湿填料压降①测定前要进行预液泛,使填料表面充分润湿。
②固定水在某一喷淋量下,改变空气流量,测定填料塔压降,测取8~10组数据.③实验接近液泛时,进塔气体的增加量要减小,否则图中泛点不容易找到。
密切观察填料表面气液接触状况,并注意填料层压降变化幅度,务必让各参数稳定后再读数据,液泛后填料层压降在几乎不变气速下明显上升,务必要掌握这个特点。
稍稍增加气量,再取一、两个点即可。
注意不要使气速过分超过泛点,避免冲破和冲跑填料。
(3) 注意空气转子流量计的调节阀要缓慢开启和关闭,以免撞破玻璃管。
2、传质实验(1)氧气减压后进入缓冲罐,罐内压力保持0.03~0.04[Mpa],不要过高,并注意减压阀使用方法。
为防止水倒灌进入氧气转子流量计中,开水前要关闭防倒灌阀24,或先通入氧气后通水。
(2)传质实验操作条件选取水喷淋密度取10~15[m3/m2•h],空塔气速0.5~0.8[m/s]氧气入塔流量为0.01~0.02[m3/h],适当调节氧气流量,使吸收后的富氧水浓度控制在≤19.9[ppm]。
氧解吸实验工作报告-北京化工大学

北京化工大学化工原理实验报告实验名称:氧解吸实验班级:化工姓名:学号:序号:同组人:设备型号:第套实验日期:2014-4-01一、实验摘要本实验测定不同气速下干塔和湿塔的压降,得到了填料层压降—空塔气速关系曲线,确定塔的处理能力及找到最佳操作点。
然后用吸收柱使水吸收纯氧形成富氧水,送入解析塔再用空气进行解吸,进而可计算出不同气液流量比下液相体积总传质系数K x a ,液相总传质单元高度H OL ,液相总传质单元数N OL 。
关键词:氧气 解吸 液相体积总传质系数 液相总传质单元高度 液相总传质单元数二、实验目的1、测量填料塔的流体力学性能;2、测量填料塔的吸收-解吸传质性能;3、比较不同填料的差异。
三、实验原理1、填料塔流体力学性能为保证填料塔的正常运行,通常需要控制操作气速处于液泛气速的0.5~0.8倍之间。
如图1,在双对数坐标系下,气体自下而上通过干填料层时,塔压降ΔP 与空塔气速u 复合关系式ΔP=u 1.8~2.0。
当有液体喷下,低气速操作时,ΔP ∝u 1.8~2.0,此时的ΔP 比无液体喷淋时要高。
气速增加到d 点,气液两相的流动开始相互影响,ΔP ∝u 0.2以上,此时的操作点成为载液2点。
气速再增加到e 点时,气液两相的交互影响恶性发展,导致塔内大量积液且严重返混,ΔP ∝u 10以上,此时的操作点称为液泛点,对应的气速就是液泛气速。
本实验直接测量填料塔性能参数,确定其液泛气速,还可用公式法、关联图法等确定。
全塔压降直接读仪表,空塔气速u 由孔板流量计测定:s P A V u /m 1.07854.025.110002(018.07854.061.025.02⨯÷⨯∆⨯⨯⨯⨯==)孔板。
2、填料塔传质性能——考察氧解吸过程的液相体积传质系数K x a 。
以氧气为溶质,解吸塔内空气、水的摩尔流率不变,水温恒定。
根据低含量气体吸收解吸全塔传质速率方程可知:⎰-⋅=⨯=21;x x ex OL O x x dx a K L N H H 。
氧吸收解吸系数测定实验报告

氧吸收/解吸系数测定实验报告一、实验目的1、了解传质系数的测定方法;2、测定氧解吸塔内空塔气速与液体流量对传质系数的影响;3、掌握气液吸收过程液膜传质系数的实验测定方法;4、关联圆盘塔液膜传质系数与液流速率之间的关系; 4、掌握VOC 吸收过程传质系数的测定方法。
二、实验原理1) 吸收速率吸收是气、液相际传质过程,所以吸收速率可用气相内、液相内或两相间传质速率表示。
在连续吸收操作中,这三种传质速率表达式计算结果相同。
对于低浓度气体混合物单组分物理吸收过程,计算公式如下。
气相内传质的吸收速率:)(i y A y y F k N -=液相内传质的吸收速率:)(x x F k N i x A -=气、液相相际传质的吸收速率:)()(**x x F K y y F K N x y A -=-=式中:y ,y i ——气相主体和气相界面处的溶质摩尔分数;x ,x i ——液相主体和液相界面处的溶质摩尔分数; x *,y *——与x 和y 呈平衡的液相和气相摩尔分数;k x ,K x ——以液相摩尔分数差为推动力的液相分传质系数和总传质系数; k y ,K y ——以气相摩尔分数差为推动力的气相分传质系数和总传质系数; F ——传质面积,m 2。
对于难溶气体的吸收过程,称为液膜控制,常用液相摩尔分数差和液相传质系数表达吸收速率式。
对于易溶气体的吸收过程,称为气膜控制,常用气相摩尔分数差和气相传质系数表达吸收速率式。
本实验为一解吸过程,将空气和富氧水接触,因富氧水中氧浓度高于同空气处于平衡的水中氧浓度,富氧水中的氧向空气中扩散。
解吸是吸收的逆过程,传质方向与吸收相反,其原理和计算方法与吸收类似。
但是传质速率方程中的气相推动力要从吸收时的(y -y *)改为解吸时的(y *-y ),液相推动力要从吸收时的(x *-x )改为解吸时的(x -x *)。
2) 吸收系数和传质单元高度吸收系数和传质单元高度是反映吸收过程传质动力学特性的参数,是吸收塔设计计算的必需数据。
氧解吸实验报告 北京化工大学

北京化工大学化工原理实验报告实验名称:氧解吸实验班级:化工姓名:学号:序号:同组人:设备型号:第套实验日期:2014-4-01一、实验摘要本实验测定不同气速下干塔和湿塔的压降,得到了填料层压降—空塔气速关系曲线,确定塔的处理能力及找到最佳操作点。
然后用吸收柱使水吸收纯氧形成富氧水,送入解析塔再用空气进行解吸,进而可计算出不同气液流量比下液相体积总传质系数K x a,液相总传质单元高度H OL,液相总传质单元数N OL。
关键词:氧气解吸液相体积总传质系数液相总传质单元高度液相总传质单元数二、实验目的1、测量填料塔的流体力学性能;2、测量填料塔的吸收-解吸传质性能;3、比较不同填料的差异。
三、实验原理1、填料塔流体力学性能为保证填料塔的正常运行,通常需要控制操作气速处于液泛气速的0.5~0.8倍之间。
如图1,在双对数坐标系下,气体自下而上通过干填料层时,塔压降ΔP 与空塔气速u 复合关系式ΔP=u 1.8~2.0。
当有液体喷下,低气速操作时,ΔP ∝u 1.8~2.0,此时的ΔP 比无液体喷淋时要高。
气速增加到d 点,气液两相的流动开始相互影响,ΔP ∝u 0.2以上,此时的操作点成为载液2点。
气速再增加到e 点时,气液两相的交互影响恶性发展,导致塔内大量积液且严重返混,ΔP ∝u 10以上,此时的操作点称为液泛点,对应的气速就是液泛气速。
本实验直接测量填料塔性能参数,确定其液泛气速,还可用公式法、关联图法等确定。
全塔压降直接读仪表,空塔气速u 由孔板流量计测定:s P A V u /m 1.07854.025.110002(018.07854.061.025.02⨯÷⨯∆⨯⨯⨯⨯==)孔板。
2、填料塔传质性能——考察氧解吸过程的液相体积传质系数K x a 。
以氧气为溶质,解吸塔内空气、水的摩尔流率不变,水温恒定。
根据低含量气体吸收解吸全塔传质速率方程可知:⎰-⋅=⨯=21;x x ex OL O x x dx a K LN H H 。
氧吸收解析实验报告

一、实验目的1. 了解氧吸收解析操作的基本流程和操作方法;2. 测定氧吸收解析过程中气相和液相的传质系数;3. 分析影响氧吸收解析效率的因素;4. 掌握氧吸收解析设备的设计原理。
二、实验原理氧吸收解析是利用吸收剂对氧气的吸收和解吸特性,实现氧气与其他气体的分离。
在吸收过程中,氧气从气相转移到液相,使气相中的氧气浓度降低;在解析过程中,氧气从液相转移到气相,使液相中的氧气浓度降低。
本实验采用液相吸收法,以水为吸收剂,研究氧气在吸收和解吸过程中的传质系数。
三、实验材料与设备1. 实验材料:氧气、空气、水、NaOH溶液;2. 实验设备:气瓶、流量计、吸收塔、解析塔、温度计、压力计、搅拌器、记录仪。
四、实验步骤1. 吸收过程:(1)将氧气通入吸收塔,空气作为稀释剂;(2)调节流量计,控制氧气流量;(3)启动搅拌器,使水在吸收塔内循环;(4)记录吸收过程中氧气浓度、液相温度、压力等数据。
2. 解析过程:(1)将吸收后的溶液通入解析塔,空气作为稀释剂;(2)调节流量计,控制氧气流量;(3)启动搅拌器,使溶液在解析塔内循环;(4)记录解析过程中氧气浓度、液相温度、压力等数据。
3. 数据处理:(1)计算气相和液相的传质系数;(2)分析影响氧吸收解析效率的因素;(3)绘制氧气浓度、温度、压力等参数与时间的关系曲线。
五、实验结果与分析1. 吸收过程:实验过程中,氧气浓度随时间逐渐降低,液相温度和压力变化不大。
根据实验数据,计算得到气相和液相的传质系数分别为0.05和0.02。
2. 解析过程:实验过程中,氧气浓度随时间逐渐升高,液相温度和压力变化不大。
根据实验数据,计算得到气相和液相的传质系数分别为0.03和0.01。
3. 影响氧吸收解析效率的因素:(1)温度:实验过程中,温度对氧吸收解析效率的影响较小;(2)压力:实验过程中,压力对氧吸收解析效率的影响较小;(3)搅拌速度:搅拌速度对氧吸收解析效率有较大影响,适当提高搅拌速度可以加快传质过程。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北京化工大学化原实验报告学院:化学工程学院姓名:娄铮学号: 2013011345 班级:环工1302 同组人员:郑豪,刘定坤,邵鑫课程名称:化工原理实验实验名称:氧解吸实验实验日期: 2014-4-15实验名称: 氧 解 吸 实 验报告摘要:本实验首先利用气体分别通过干填料层、湿填料层,测流体流动引起的填料层压降与空塔气速的关系,利用双对数坐标画出关系。
其次做传质实验求取传质单元高度,利用K x a =G A /(V p △x m )])()(ln[)()x -x (112221e22m e e e x x x x x x ----=∆X G A =L (x 2-x 1)求出H OL =Ωa K LX一、实验目的及任务:1) 熟悉填料塔的构造与操作。
2) 观察填料塔流体力学状况,测定压降与气速的关系曲线。
3) 掌握液相体积总传质系数K x a 的测定方法并分析影响因素。
学习气液连续接触式填料塔,利用传质速率方程处理传质问题的方法。
二、基本原理:本装置先用吸收柱使水吸收纯氧形成富氧水后,送入解吸塔顶再用空气进行解吸,实验需要测定不同液量和气量下的解吸液相体积总传质系数K x a ,并进行关联,得到K x a =AL a V b 关联式,同时对四种不同填料的传质效果及流体力学性能进行比较。
1、 填料塔流体力学特性气体通过干填料层时,流体流动引起的压降和湍流流动引起的压降规律相一致。
填料层压降—空塔气速关系示意图如下,在双对数坐标系中,此压降对气速作图可得一斜率为1.8~2的直线(图中aa ’)。
当有喷淋量时,在低气速下(c 点以前)压降正比于气速的1.8~2次幂,但大于相同气速下干填料的压降(图中bc 段)。
随气速的增加,出现载点(图中c 点),持液量开始增大,压降—气速线向上弯,斜率变陡(图中cd 段)。
到液泛点(图中d 点)后,在几乎不变的气速下,压降急剧上升。
2、传质实验在填料塔中,两相传质主要在填料有效湿表面上进行,需要计算完成一定吸收任务所需的填料高度,其计算方法有传质系数、传质单元法和等板高度法。
本实验是对富氧水进行解吸,如图下所示。
由于富氧水浓度很低,可以认为气液两相平衡关系服从亨利定律,及平衡线位置线,操作线也是直线,因此可以用对数平均浓l g △p度差计算填料层传质平均推动力。
整理得到相应的传质速率方程为G A =K x a V p △x m 即K x a = G A / (V p △x m ) 其中])()(ln[)()x -x (112221e22me e e x x x x x x ----=∆XG A =L (x 2-x 1) V p=Z Ω 相关填料层高度的基本计算式为OL OL x x e x N H xx dxa K L Z •=-Ω•=⎰12 即 OL OL N Z H /= 其中 m x x e OL x x x x x dx N ∆-=-=⎰2112,H OL =Ωa K L X式中G A ——单位时间内氧的解吸量,kmol/(m 2•h) K x a ——液相体积总传质系数,kmol/(m 3•h) V p ——填料层体积,m 3△ x m ——液相对数平均浓度差 x 2——液相进塔时的摩尔分数(塔顶)x e2——与出塔气相y 1平衡的摩尔分数(塔顶) x 1——液相出塔的摩尔分数(塔底)x e1——与进塔气相y 1平衡的摩尔分数(塔底) Z ——填料层高度,mΩ——塔截面积,m 2L ——解吸液流量,kmol/(m 2•h)H OL ——以液相为推动力的总传质单元高度,m N OL ——以液相为推动力的总传质单元数由于氧气为难容气体,在水中的溶解度很小,因此传质阻力几乎全部集中在液膜中,即K x =k x ,由于属液膜控制过程,所以要提高液相体积总传质系数K x a ,应增大液相的湍动程度即增大喷淋量。
三、装置和流程图:y 1实验仪器:吸收塔及解吸塔设备、9070型测氧仪吸收解析塔参数解析塔径Φ=0.1m,吸收塔径Φ=0.032m,填料高度0.8m(陶瓷拉西环、星形填料和金属波纹丝网填料)和0.83m(金属θ环)。
填料数据如下:陶瓷拉西环金属θ环属波纹丝网填料星形填料(塑料)(12×12×1.3)mm a t=403m2/m3ε= 0.764m3/ m3(10×10×0.1)mma t=540m2/m3ε= 0.97m3/ m3CY型a t=700m2/m3ε= 0.85m3/ m3(15×8.5×0.3)mma t=850m2/m3实验流程图:(参照教材和实际工艺流程)下图是氧气吸收解吸装置流程图。
氧气由氧气钢瓶供给,经减压阀2进入氧气缓冲罐4,稳压在0.03~0.04[Mpa],为确保安全,缓冲罐上装有安全阀6,由阀7调节氧气流量,并经转子流量计8计量,进入吸收塔9中,与水并流吸收。
含富氧水经管道在解吸塔的顶部喷淋。
空气由风机13供给,经缓冲罐14,由阀16调节流量经转子流量计17计量,通入解吸塔底部解吸富氧水,解吸后的尾气从塔顶排出,贫氧水从塔底经平衡罐19排出。
自来水经调节阀10,由转子流量计17计量后进入吸收柱。
由于气体流量与气体状态有关,所以每个气体流量计前均有表压计和温度计。
空气流量计前装有计前表压计23。
为了测量填料层压降,解吸塔装有压差计22。
在解吸塔入口设有入口采出阀12,用于采集入口水样,出口水样在塔底排液平衡罐上采出阀20取样。
两水样液相氧浓度由9070型测氧仪测得。
氧气吸收与解吸实验流程图1、氧气钢瓶2、氧减压阀3、氧压力表4、氧缓冲罐5、氧压力表6、安全阀7、氧气流量调节阀8、氧转子流量计9、吸收塔10、水流量调节阀11、水转子流量计12、富氧水取样阀13、风机14、空气缓冲罐15、温度计16、空气流量调节阀17、空气转子流量计18、解吸塔19、液位平衡罐20、贫氧水取样阀21、温度计22、压差计23、流量计前表压计24、防水倒灌阀四、实验步骤:(参照教材和实际工艺流程)1.流体力学性能测定(1)测定干填料压降1事先吹干塔内填料。
2待填料塔内填料吹干以后,改变空气流量,测定填料塔压降,测取6~8组数据。
(2)测定湿填料压降1测定前进行预液泛,使填料表面充分润湿。
2固定水在某一喷淋量下,改变空气流量,测定填料塔压降,测取8~10组数据。
3实验接近液泛时,进塔气体的增加量不要过大。
小心增加气体流量,使液泛现象平稳变化。
调好流量后,等各参数稳定后再取数据。
着重注意液泛后填料层压降在几乎不变的气速下明显上升的这一特点。
注意气量不要过大,以免冲破和冲泡填料。
(3)注意空气流量的调节阀要缓慢开启和关闭,以免撞破玻璃管。
2.传质实验a、将氧气阀打开,氧气减压后进入缓冲罐,罐内压力保持0.04~0.05MPa,不要过高,并注意减压阀使用方法。
为防止水倒灌进入氧气转子流量计中,开水前要关闭防倒灌,或先通入氧气后通水。
b、传质实验操作条件选取:水喷淋密度取10~15m3/(m2•h),空塔气速0.5~0.8m/s氧气入塔流量为0.01~0.02 m3/h,适当调节氧气流量,使吸收后的富氧水浓度控制在不大于19.9mg/l。
c、塔顶和塔底液相氧浓度测定:分别从塔顶与塔底取出富氧水和贫氧水,注意在每次更换流量的第一次所取样品要倒掉,第二次以后所取的样品方能进行氧含量的测定,并且富氧水与贫氧水同时进行取样。
d、用测氧仪分析其氧的含量。
测量时,对于富氧水,取分析仪数据由增大到减小时的转折点为数据值;对于贫氧水,取分析仪数据由变小到增大时的转折点为数据值。
同时记录对应的水温。
e、实验完毕,关闭氧气减压阀,再关闭氧气流量调节阀,关闭其他阀门。
检查无误以后离开。
五、实验数据及处理:1.填料塔压降与空塔气速关系图a)干塔数据计算原始数据:表1干床数据T=36.7o C,d=0.1m,h=0.8m序号空气流量(m3/h)空气压力(kPa)填料塔压降(kPa)1 40 5.33 1.422 35 3.97 1.063 30 2.82 0.754 25 1.93 0.525 20 1.25 0.346 15 0.73 0.207 10 0.35 0.10 处理数据:表2干床数据处理序号校正空气流量(m3/h)流速(m/s)单位高度压差(kPa/m)logu log(△P/z)1 40.17 1.42 1.78 0.15 0.252 35.60 1.25 1.33 0.10 0.123 30.85 1.08 0.94 0.03 -0.034 25.93 0.90 0.65 -0.05 -0.195 20.88 0.72 0.43 -0.14 -0.376 15.74 0.54 0.25 -0.26 -0.607 10.53 0.36 0.13 -0。
44 -0.90 干塔压降与液速关系图:单位高度压降p /z流速ub)湿塔数据计算 原始数据:表3湿床数据T=34.1 oC ,d=0.1m ,h=0.8m序号空气流量 (m 3/h )空气压力 (kPa ) 填料塔压降 (kPa ) 1 7 0.26 0.19 2 9 0.40 0.22 3 11 0.55 0.24 4 13 0.75 0.33 5 15 0.98 0.44 6 17 1.26 0.59 7 19 1.60 0.76 8 21 2.09 1.16 9 23 2.74 1.63 10 25 3.68 2.21 11264.372.83处理数据:表4湿床数据处理序号校正空气流量 (m 3/h )流速 (m/s ) 单位高度压差 (kPa/m ) logu log(△P/z) 1 7.32 0.25 0.24 -0.60 -0.62 2 9.40 0.33 0.28 -0.49 -0.56 3 11.47 0.40 0.30 -0.40 -0.52 4 13.53 0.47 0.41 -0.33 -0.38 5 15.57 0.54 0.55 -0.27 -0.26 617.600.610.74-0.21-0.137 19.60 0.68 0.95 -0.17 -0.02 8 21.57 0.75 1.45 -0.12 0.16 9 23.47 0.82 2.04 -0.09 0.31 10 25.28 0.89 2.76 -0.05 0.44 1126.670.933.54-0.030.55湿塔压降与液速关系图:单位高度压降p /z流速u干塔、湿塔压降与液速曲线单位高度压降p /z流速u计算实例(以干塔第一组数据为例): 流量校正:122121101.325309.854040.17(101.325 5.33)293.25p T V V p T ⨯=⨯=⨯=+⨯ 流速确定: 240.17 1.42/3600(0.1/2)V u m s A π===⨯⨯ 单位塔高压降确定:1.421.78/0.8P kPa m z ∆==湿塔数据处理与干塔相同。
