2017年36个国家谈判药品
无忧保—2017年医保“谈判目录”出炉.

无忧保—2017年医保“谈判目录”出炉 自2017年版医保目录发布以来,作为其重要补充,新目录中“含金量”较高的谈判目录品种名单备受市场期待。
4月14日晚间,人社部官网终于发布《2017年国家基本医疗保险、工伤保险和生育保险药品目录谈判范围》,确定44个品种纳入新版医保目录谈判范围。
其中,国产品种占比达45.45%,超出市场此前预期。
对此,中国社会保障学会副会长、中山大学国家治理研究院副院长申曙光教授在接受上证报记者采访时表示,医保谈判目录一方面体现了国家对创新药产业的肯定和支持,进一步鼓励国内药企创新研发,另一方面也从医保基金角度保障了重特大疾病患者用药,有助于减轻患者的经济负担。
国产品种占比超预期 今年2月23日,人社部发布《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》(下称“新医保目录”),是时隔八年以来首次调整医保目录。
除加大中成药及儿童药比重外,新增设的医保谈判目录一直备受市场瞩目。
该目录主要是考虑到部分药品具有很高的临床价值但价格较为昂贵,按现行价格纳入目录可能给医保基金带来较大压力,因此,专家同步评审确定了谈判药品目录。
4月14日晚间,谈判目录的44个品种名单正式出炉。
具体看目录范围,44个品种包括20个国产品种、24个进口品种,涉及17家国内药企、13家外资药企和两家中外合资药企,国内药企占比53.12%,国产品种占比达到45.45%。
此前市场认为,谈判药领域将是跨国药企的“主场”,没想到本次目录中国产品种占比如此之高。
申曙光向记者表示,这在一定程度上体现出我国创新药研发实力进一步增强,国家对创新药产业也加大了支持力度。
可以预见,大量国产1.1类新药和优质仿制药对进口原研药的市场替代有望加速。
进一步看药品类型,谈判目录中,有化学药品种22个、生物制品14个、中成药8个。
按照治疗病症来看,共涉及抗肿瘤和免疫调节剂、心脑血管疾病用药、血液和造血系统药物等十个领域。
国家谈判药品配备情况报告

一、背景为提高我国医疗保障水平,减轻患者医疗负担,我国自2017年起开展国家医保药品谈判工作。
经过连续七轮谈判,已有超过400种创新药进入基本医保药品目录,极大地提高了创新药物的可获取性。
为确保患者能够获得这些药品,国家医保局和国家卫健委高度重视谈判药品落地实施,出台了多项政策。
本报告旨在分析国家谈判药品的配备情况,评估药品可及性面临的困难,并提出相关建议。
二、国家谈判药品配备情况1. 药品配备数量截至2023年底,国家医保谈判药品共计363种,可通过国家医保服务平台查询全国医疗机构及定点零售药店的配备情况。
从数据来看,全国范围内大部分医疗机构和零售药店均配备了国家谈判药品,但部分偏远地区和基层医疗机构配备数量仍需提高。
2. 药品配备品种国家谈判药品涵盖了肿瘤、心血管、神经、消化、呼吸等多个治疗领域,涉及多种疾病。
其中,肿瘤治疗药品数量最多,其次是心血管、神经、消化等领域的药品。
从品种上看,国家谈判药品既有高价进口药,也有国产仿制药,满足了不同患者的用药需求。
3. 药品配备质量国家谈判药品在质量上均符合国家标准,医疗机构和零售药店在采购、储存、配送等环节均严格执行相关规范,确保药品质量。
三、药品可及性面临的困难1. 偏远地区和基层医疗机构配备不足由于地域、经济、交通等因素的影响,偏远地区和基层医疗机构的国家谈判药品配备数量和质量仍有待提高。
2. 药品价格波动部分国家谈判药品价格较高,对患者经济负担较大。
同时,药品价格波动也会影响药品可及性。
3. 医疗资源分配不均优质医疗资源主要集中在城市,农村地区医疗资源相对匮乏,导致部分国家谈判药品在农村地区难以获得。
四、建议1. 加强偏远地区和基层医疗机构国家谈判药品配备加大对偏远地区和基层医疗机构的政策支持,提高国家谈判药品配备数量和质量。
2. 完善药品价格监管机制合理制定国家谈判药品价格,减轻患者经济负担,提高药品可及性。
3. 优化医疗资源分配加大对农村地区医疗资源的投入,提高农村地区国家谈判药品可及性。
医疗保健:医保谈判目录大揭秘 重点品种市场前景解析

揭秘国内上市公司大品种,关注相关受益标的
从此次谈判目录的品种涉及国内9家A股上市公司、1家新三板挂牌公司、1家H股上市公司。具体 包括西藏药业(注射用重组人脑利钠肽)、康弘药业(康柏西普眼用注射液)、恒瑞医药(甲磺 酸阿帕替尼片)、康缘药业(银杏二萜内酯葡胺注射液)、天士力(注射用重组人尿激酶原、注
全国医保 全国医保 全国医保 全国医保
高血压 高血压 高血压 高血压
4mg*10 全国医保 高血压;心衰
20mg*7 240mg*7
11 省增补 -
高血压 高血压
(3)银杏二萜内酯葡胺注射液
银杏二萜内酯葡胺注射液是治疗心血管疾病的中药注射剂,属于银杏叶提取物大类。
目前国内银杏制剂品种丰富多样,竞争激烈,口服和注射剂剂型都有。在注射剂剂型中,又分为 复方品种和银杏叶提取物,目前国内上市的银杏叶提取物主要有银杏二萜内酯葡胺注射液、银杏 内酯注射液、舒血宁、银杏叶提取物注射液(金纳多)和银杏达莫。在这几类银杏叶提取物里, 后三者主要为黄酮成分,而前两者主要是由银杏内酯A、B组成,且前两者成分清楚,作用明确, 效果更为显著。主要差别对比如图表8:
奥美沙坦
片剂 一日一次,20mg
阿利沙坦
片剂
一日一次,240mg
数据来源:南方所,莫尼塔研究
日用金额 (元) 5.3 5.74 1.38 16 1.492.98 6.11 9.14
中标价 (元) 37.08 40.18 8.28 56
14.91
首个国产曲妥珠单抗获批!中国生物类似药百花齐放

⾸个国产曲妥珠单抗获批!中国⽣物类似药百花齐放8⽉14⽇,复宏汉霖曲妥珠单抗(HLX02)正式获得国家药品监督管理局批准上市,商品名为汉曲优®。
今年7⽉27⽇,欧盟委员会(EC)已正式批准HLX02在欧盟的上市销售申请,商品名为Zercepac®。
汉曲优®成为⾸个由中国企业开发、⽣产和上市的Herceptin®(曲妥珠单抗)⽣物类似药,也是⾸个成功登陆欧盟的“中国籍”单抗⽣物类似药,开辟了中国医药企业参与单抗⽣物类似药“世界杯”⽐赛的先河。
继去年2⽉国内⾸个⽣物类似药利妥昔单抗注射液汉利康®(HLX01)获批上市之后,复宏汉霖拥有了第2款进⼊商业化阶段的产品。
国内获批上市的⽣物类似药基于适应症外推,汉曲优®同时获批原研全部3个适应症根据我国现⾏的《⽣物类似药研发与评价技术指导原则》以及药品注册管理办法,⽣物类似药在临床开发时可以采⽤“适应症外推”的策略来缩减研发成本和周期,但是要求外推的适应症应当与开展⽐对试验的适应症具有相同的临床相关病理机制、作⽤机理以及靶点,并且外推的适应症应当是原研产品已经在国内批准上市的适应症。
汉曲优®此次获批了与原研产品Herceptin在中国完全相同的3个适应症,包括HER2阳性早期乳腺癌、HER2阳性转移性乳腺癌和HER2阳性转移性胃癌。
从管线产品的开发进度上看,复宏汉霖⽬前已经在⾎液肿瘤(⾮霍奇⾦淋巴瘤)和实体瘤(乳腺癌、胃癌)都有了商业化阶段的产品,这也将为复宏汉霖的其他肿瘤产品HLX04(贝伐珠单抗,III期完成)、HLX10(PD-1单抗,III期)、HLX07(EGFR单抗,II期)的商业化推⼴打下基础。
⾃动进⼊医保,降低患者⽀付负担乳腺癌在我国⼥性恶性肿瘤中的发病率和死亡率分别居第1位和第5位,2019年新增病例约为30.4万,占⼥性恶性肿瘤发病的17.10%,呈现上升的趋势。
HER2突变阳性率在乳腺癌中⼤约为20%。
基于价值定价的多适应证药品医保支付国际经验及启示
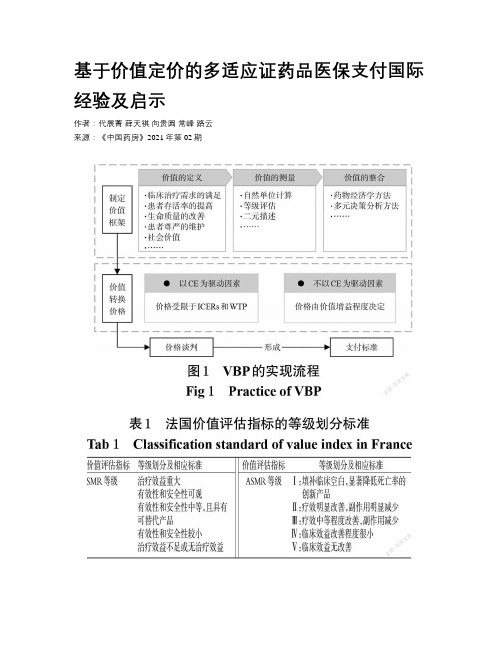
基于价值定价的多适应证药品医保支付国际经验及启示作者:代展菁薛天祺向贵圆常峰路云来源:《中国药房》2021年第02期摘要目的:為完善我国多适应证药品基于价值定价的医保支付提供参考。
方法:梳理多适应证药品价值定价的理论基础和实现流程,分析法国、德国、英国、意大利和瑞典的价值评估指标和基于价值定价的医保支付策略,为我国多适应证药品医保支付提出建议。
结果与结论:价值定价的实现首先需要制定一个价值框架以定义、测量、整合价值,再通过建立模型将总价值转化为价格。
各国多适应证药品根据价值定价的整体思路一致,但价值评估指标存在差异。
英国和瑞典主要以药物经济学方法测得的质量调整生命年(QALYs)和增量成本-效果比(ICERs)为价值标准,法国、德国和意大利则更侧重于以药品的临床治疗价值和临床指标改善程度为标准。
在多适应证药品的医保支付策略方面,法国采取的是基于预期使用量的单一加权法,德国采取的是基于价值和使用量的组合加权法,英国采取的是名义医保支付标准结合患者准入协议法,意大利采取的是名义医保支付标准结合管理准入协议法,瑞典则采用不同适应证不同商品名的独立支付法。
我国可在借鉴上述多国经验的基础上,探索适应我国国情的多适应证药品的价值定价策略,综合借鉴和使用多种医保支付策略,完善患者及药品使用信息收集机制,为实施多适应证药品价值定价和医保支付策略提供信息支持。
关键词多适应证药品;价值定价;医保支付;法国;德国;英国;意大利;瑞典;启示ABSTRACT OBJECTIVE:To provide reference for improving medical insurance reimbursement for multi-indication drugs based on value-based pricing in China. METHODS: The theory and practice of value-based pricing for multi-indication drugs were sorted out, and the value standards and medical insurance reimbursement strategies based on value-based pricing in France,Germany, UK, Italy and Sweden were analyzed, so as to provide the suggestions for medical insurance reimbursement of multi-indication drugs in China. RESULTS & CONCLUSIONS: The realization of value-based pricing first needed to develop a value framework to define, measure andintegrate value, and then established a model to convert the total value into price. The overall idea of value-based pricing for multi-indication drugs was consistent, but there were differences in the value standard. In the UK and Sweden, quality-adjusted life years (QALYs) and incremental cost-effectiveness ratios (ICERs) measured by pharmacoeconomicsare used as the value standard. France, Germany and Italy were more focused on the therapeutic value and clinical benefit improvement. As for medical insurance reimbursement strategies,France adopted single weighting method based on expected volume. Germany adopted combination weighting method based on value and volume. UK introduced the Patient Access Schemes and Italy introduced the Managed Entry Agreements, both based on the nominal reimbursement standard. Sweden adopted independent reimbursement for different indications by different brand names. It is suggested that China can explore the value-based pricing strategies of multi-indication drugs on the basis of the above international experiences, reference and use these variety of medical insurance reimbursement strategies comprehensively. Simultaneously, the information collection mechanism of patients and drug use should be improved to provide data support for the implementation of China’s value-based pricing and reimbursement strategies for multi-indication drugs.KEYWORD Multi-indication drugs; Value-based pricing; Reimbursement; France; Germany; UK; Italy; Sweden; Enlightment中图分类号 R95 文献标志码 A 文章编号 1001-0408(2021)02-0139-07DOI 10.6039/j.issn.1001-0408.2021.02.03多适应证药品(Multi-indication drugs)是指可用于预防、治疗、诊断、缓解或者辅助治疗多种疾病(状态)或者症状的药品。
2017年国家医保药品目录最新

2017年国家医保药品⽬录最新 时隔⼋年,⼀直备受业界关注的新版医保⽬录终于正式落地。
2017版医保药品⽬录,新增加药品339个,同时可适⽤于⼯伤保险和⽣育保险参保⼈员。
下⾯是有2017年国家医保⽬录,欢迎参阅。
2017年国家医保⽬录 步长制药:公司8个产品新纳⼊2017版医保⽬录 步长制药23⽇晚间公告,经统计,公司及公司控股⼦公司陕西步长制药有限公司、保定天浩制药有限公司、邛崃天银制药有限公司、辽宁奥达制药有限公司共有8个产品新纳⼊“国家基本医疗保险、⼯伤保险和⽣育保险药品⽬录(2017年版)”;公司及控股⼦公司辽宁奥达制药有限公司共有3个产品退出国家医保⽬录。
康缘药业:公司110个药品⼊选2017版医保⽬录 康缘药业23⽇晚间公告,公司共有110个药品⼊选了《国家基本医疗保险、⼯伤保险和⽣育保险药品⽬录(2017年版)》,其中公司独家药品20个。
本次⼊选国家医保⽬录的药品中,⾸次⼊选药品8个,调整医保分类药品5个,退出国家医保⽬录药品1个。
佐⼒药业独家产品灵泽⽚纳⼊医保⽬录 佐⼒药业公告,公司⽣产的独家产品灵泽⽚被纳⼊《国家基本医疗保险、⼯伤保险和⽣育保险药品⽬录(2017年版)》。
上述产品灵泽⽚系公司乌灵系列产品之⼀,为公司独家⽣产品种,功能主治为:益肾活⾎,散结利⽔。
乐普医疗强⼼药产品列⼊2017版医保⽬录 乐普医疗公告,公司药品左西孟旦(海合天欣)列⼊《国家基本医疗保险、⼯伤保险和⽣育保险药品⽬录(2017年版)》。
产品作为⼀种新型正性肌⼒药(强⼼药),适⽤于急性失代偿性⼼⼒衰竭(ADHF)的短期治疗。
海正药业:公司产品列⼊2017版医保⽬录 海正药业23⽇晚间公告,公司及控股⼦公司海正辉瑞制药有限公司共有7个产品新纳⼊《国家医保⽬录》。
此次新纳⼊该⽬录的7个产品均属于医保⼄类品种,其中4个产品为独家品种或独家仿制品种,均正常⽣产销售。
兴齐眼药:公司两产品新纳⼊医保⽬录 兴齐眼药公告,公司产品阿托品眼⽤凝胶剂、维⽣素A棕榈酸酯眼⽤凝胶剂新纳⼊《国家基本医疗保险、⼯伤保险和⽣育保险药品⽬录(2017年版)》。
36种国家谈判药品报销流程

36种国家谈判药品报销流程一、病种认定参保人员到认定机构医保窗口领取《四川省基本医疗保险单行支付药品病种认定表》,完善认定机构填写部分(市内认定机构首批医院名单为:遂宁市中心医院、遂宁市中医院、射洪县人民医院、射洪县中医院)。
二、就诊购药持《认定表》到市内二级以上公立医院完善《四川省基本医疗保险单行支付药品病种治疗方案申请表》治疗机构填写部分,进行治疗并填写《遂宁市基本医疗保险单行支付药品用药情况登记表》中用药记录。
若因治疗需更换药品的,应在认定机构填写《四川省基本医疗保险单行支付药品病种治疗方案变更申请表》。
三、费用结算实行联网结算,未能结算的,提供以下资料到医保窗口结算:1《认定表》。
2《治疗方案申请表》。
3购药发票。
4用药处方。
5病情证明。
6费用清单(住院使用单行支付药品的,除报销资料外,还需提供每日费用清单)。
7社保卡复印件。
四、补报时间为2017年9月1日至2018年5月28日已发生的相应药品费用,提供以下材料到医保窗口报销:1《认定表》。
2《治疗方案申请表》。
3购药发票。
4用药处方。
5病情证明。
6费用清单(住院使用单行支付药品的,除报销资料外,还需提供每日费用清单)。
7社保卡复印件。
五、支付标准个人首先自付30%,再按城镇职工基本医疗保险、城乡居民基本医疗保险住院医疗费用比例支付。
住院使用36种药品,其费用与住院医疗费用一并结算;门诊治疗使用36种药品其费用按二级医院(城乡居民按二级乙等医院)住院医疗费用比例支付,一年只计算一次起付标准。
一个参保年度内,基本医疗保险统筹基金支付36种药品费用累计不得超过8万元,支付的总费用计入年度最高支付限额。
由个人负担的费用不纳入职工补充医疗保险、城乡居民大病保险支付范围。
六、36种药品及限制条件:1、“重组人尿激酶原”按遂宁市基本医疗保险现行乙类管理办法报销。
康博西普眼用注射液、银杏二萜内脂葡胺注射液、银杏内脂注射液,暂按原规定报销。
2、余32种药品按下表格要求报销(其中费用标准包括基本医疗保险基金和参保人员共同支付的全部费用)。
2017年国家基本医疗保险、工伤保险和生育保险药品目录

2017年国家基本医疗保险、工伤保险和生育保险药品目录附件:
2017年国家基本医疗保险、工伤保险和生育保险药品目录谈判范围
序号药品名称
1 银杏内酯注射液
2 心脉隆注射液
3 参一胶囊
4 注射用黄芪多糖
5 血必净注射液
6 复方黄黛片
7 注射用益气复脉(冻干) 8 银杏二萜内酯葡胺注射液 9 阿利沙坦酯片
10 西达本胺片
11 吗啉硝唑氯化钠注射液 12 康柏西普眼用注射液 13 重组人血管内皮抑制素注射液 14 甲磺酸阿帕替尼片 15 注射用紫杉醇脂质体 16 注射用重组人尿激酶原 17 注射用尤瑞克林
18 注射用重组人脑利钠肽 19 氟维司群注射液
20 喹硫平缓释片
21 替格瑞洛片
22 波生坦片
23 尼妥珠单抗注射液 24 甲苯磺酸索拉非尼片
序号药品名称 25 注射用重组人干扰素β-1b 26 甲苯磺酸拉帕替尼片 27 盐酸帕罗西汀肠溶缓释剂片 28 碳酸司维拉姆片
29 贝伐珠单抗注射液
30 盐酸厄洛替尼片
31 利妥昔单抗注射液
32 注射用曲妥珠单抗
33 西妥昔单抗注射液
34 利拉鲁肽注射液
35 注射用重组人凝血因子?a 36 雷珠单抗注射液
37 依维莫司片
38 碳酸镧咀嚼片
39 来那度胺胶囊
40 醋酸阿比特龙片
41 注射用硼替佐米
42 注射用英夫利西单抗,限克罗恩病,
43 托伐普坦片
44 泊沙康唑口服混悬液。
人社部发〔2017〕54号

人社部发〔2017〕54号各省、自治区、直辖市及新疆生产建设兵团人力资源社会保障厅(局),福建省医保办:按照《关于印发〈国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)〉的通知》(人社部发〔2017〕15号)要求,我部组织专家对部分药品进行谈判,并确定了医保支付标准。
现予以公布并通知如下:一、将利拉鲁肽注射剂等36种药品(以下统称“有关药品”)纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》(以下简称药品目录)乙类范围,各省(区、市)社会保险主管部门不得将有关药品调出目录,也不得调整限定支付范围。
二、附表“医保支付标准”一栏规定的支付标准包括基本医疗保险基金和参保人员共同支付的全部费用,基本医疗保险基金和参保人员的分担比例由各统筹地区确定。
规定的支付标准有效期截至2019年12月31日,有效期满后按照医保药品支付标准有关规定进行调整。
有效期内,如有同通用名称药品(仿制药)上市,我部将根据仿制药价格水平调整该药品的医保支付标准并另行发布;如出现药品市场实际价格明显低于现行支付标准的,我部可以与企业协商重新制定支付标准并另行发布。
三、各省(区、市)要积极探索多种方式加强有关药品管理,促进合理用药。
对规定需“事前审查后方可使用”或其他需要严格管理的药品,要建立统一的事前审查规定;对用量大、费用高的药品要纳入基本医疗保险医疗服务智能监控系统进行重点监控,并做好费用分析;要采取有效措施鼓励定点零售药店为参保人员提供药品,发挥药店在医保药品供应保障方面的积极作用。
四、各省(区、市)要认真贯彻落实本通知要求,将有关药品纳入药品目录乙类范围,与药品目录一并执行。
同时,要加快推进本省(区、市)乙类药品调整工作,尽快发布。
附件:36种有关药品名单人力资源社会保障部2017年7月13日。
关于全面执行2017版山东省药品目录的说明

省增补的291个品种或剂型,其中新增的拟设定自付比例 为20%,儿童专用药,自付比例修订为10%;原来为 100%报销的现根据乙类药品需个人负担一定比例的要求, 设定自付比例为5%;原来自付比例为10%、20%的,维 持原自付比例
二、原山东省增补药品和 淄博市增补药品处理
山东省基本医疗保险工伤保险和生育保险药品目录(2017年版)
序号 57 58 59 60 61 62 63 64
名称 曲克芦丁氯化 钠注射液 曲克芦丁葡萄 糖注射液 维生素C氯化 钠注射液 维生素C葡萄 糖注射液 乌拉地尔氯化 钠注射液 乌拉地尔葡萄 糖注射液 细辛脑氯化钠 注射液 硝酸甘油氯化 钠注射液 硝酸异山梨酯 葡萄糖注射液 硝酸异山梨酯 氯化钠注射液 烟酰胺葡萄糖 注射液 炎琥宁氯化钠 注射液 氨溴索氯化钠 注射液 氨溴索葡萄糖 注射液
序号
编号
分类
中文名称
剂型
序号
编号
分类
中文名称
剂型
序号
编号
分类
中文名称
剂型
1
3
西药
氨苄青霉素/ 丙磺舒
口服常释 剂型
11
210
西药
混合糖电解质 注射液
21
223
西药
氟氯西林钠阿 莫西林胶囊 注射用脂溶性 维生素(2)水 溶性维生素组 合包装 大株红景天注 射液 清浊益肾胶囊
2
14
西药
司帕沙星
口服常释 剂型
四、 《药品目录》中的“限定支付范围”
山东省基本医疗保险工伤保险和生育保险药品目录(2017年版)
“备注”栏中对部分药品规定了限定支 付范围,是指符合规定情况下参保人员 发生的药品费用,可按规定由基本医疗 保险或生育保险基金支付,工伤保险支 付药品费用时不受限定支付范围限制。
2017年36个国家谈判药品
药品分类代码
药品分类
编号
药品名称
支付标准
备注
ZA
内科用药
ZA12
祛瘀剂
ZA12H
化瘀通脉剂
乙
TZOl
银杏二菇内酯葡胺注射液
316元(5ml∕支,含银 杏二菇内酯25mg)
限二级及以上医疗机构 脑梗死恢复期患者,单 次住院最多支付14天。
乙
TZ02
银杏内酯注射液
79元(2nd/支,含菇类 内酯IOmg)
XB
血液和造血 器官药
XBOl
抗血栓形 成药
XBOlA
抗血栓形成药
XBOlAC
血小板凝聚抑制 齐∣J,肝素除外
乙
TX02
替格瑞洛
口服常 释剂型
8. 45元(90mg∕片)
限急性冠脉综合症患者, 支付不超过12个月。
XBOlAD
酶类
乙
TX03
重组人尿 激酶原
注射剂
1020元(5mg (50万
IU)/支)
8289. 87元
(500mg∕50ml∕瓶)
限复发或耐药的滤泡性中 央型淋巴瘤(国际工作分 类B、C和D亚型的B细 胞非霍奇金淋巴瘤),CD20阳性W-IV期滤泡性 非霍奇金淋巴瘤,CD20阳 性弥漫大B细胞性非霍奇 金淋巴瘤:最多支付8个 疗程。
XLOlXE
蛋白激酶抑制剂
乙
TX14
厄洛替尼
口服常
限急性心肌梗死发病12小时内使用。
XB02
抗出血药
XB02B
维生素K和其 他止血药
乙
TX04
重组人凝
血因子Vna
注射剂
5780元(Img
(50KIU)/支)
2017年国家医保药品目录准入谈判工作的若干思考

2017年国家医保药品目录准入谈判工作的若干思考发布日期:2017-07-20 来源:人社部打印本页浏览次数:4631 创新药物疗效显著,对于治愈或改善疾病症状、提升患者生活质量都有着不可替代作用。
另一方面,由于专利排他性保护,创新药物通常具有市场垄断、单一货源渠道等属性,在市场资源无法有效配置的前提下,其价格居高不下,药品可支付性差,无法满足广大参保人用药需求。
人社部主导的“2017年国家医保药品目录准入谈判工作”是一项系统复杂大工程。
从3月至6月,短短4个月时间内,要完成谈判方案设计与论证、谈判品种确定、谈判资料申报与审核,以及现场谈判和签署协议等系列工作。
更重要的是,作为药品医保准入的首次国家谈判,许多工作无先例可循,需要借鉴国际经验并结合我国国情作出开创性的制度设计。
从谈判结果来看,无论是谈判成功率、谈判所确定药品支付标准的平均降幅,还是各界评论与反馈,都表明此次谈判工作是非常成功的。
作为我国深化医药卫生体制改革、促进“健康中国”建设的重要内容,将“临床疗效明显、患者负担较重”的创新药物纳入国家医保目录,将显著提高社会公众对新医改的获得感与满意度。
纵观从2017版医保目录公布,到拟谈判品种的公示,再到谈判协议达成的全过程,笔者认为首次国家医保药品目录准入谈判,具有以下七个特点:一是以临床需求为基准,科学遴选谈判品种此次国家医保药品目录准入谈判工作是《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》调整制定的有机组成部分。
在2017版目录遴选过程中,通过对药品临床价值和需求进行反复专家论证,并以全国联网随机票决的方式进行遴选,经与企业协商最终确定了44个疗效显著且临床需求高的谈判品种。
二是以疗效价值为依据,合理评估药品支付标准药品支付标准是国家医保药品目录准入谈判的核心,也是国家医保经办机构与药品生产企业间博弈的核心。
如何通过谈判提升医疗保险基金承受力水平,实现医疗保险资源的合理配置,同时保留企业合理利润空间,激励其进一步创新投入,设置合理药品支付标准成为谈判的关键所在。
医保谈判药品的历程、供应保障及支付

重要内容二:谈判药品的遴选标准
解答困惑一:即为何江苏选择5个、青岛选择23个药进行保障?
相对疗效
药物经济学
预算影响分析
国际参考价格
相较于现有治疗有 什么临床价值?
是否物有所值?
医保是否付得起?
医保如何付的更值?
引发困惑二:如 何圈定遴选范围, 即这些待遴选的 药品是如何划定 出来的?
3
1. 谈判药品(特药)政策的演进历史:从地方到全国
重要内容四:谈判药品双通道供应
✓ 2012.11.14《关于开展基本医疗保险付费总额控制的意见》(人社部发〔2012〕70号):进一步深化医疗保险付费方式改革,结合基本医
疗保险基金预算管理的全面施行,开展基本医疗保险付费总额控制。
✓ 2015年11月6日,《关于印发控制公立医院医疗费用不合理增长的若干意见的通知》(国卫体改发〔2015〕89号)发布,要求公立医院药
图 江苏省医疗机构合理用药考核评分表(2021年版)部分
医疗保障局与卫生健康委员会两部门共同管理,推进谈判药品医疗机构落地使用 10
3. 谈判药品的支付管理
3.4 谈判药品落地先行自付比例管理
重要内容八:谈判药品个人先行自付比例管理
➢ 我国谈判药品发展历程
2016:卫健委 (原卫计委) 主导,成功谈
规定的支付标准,先由参保人自付一定比例后,再按基本医疗保险规定的分担办法支付。“乙类药品”个人先行自付的比例
由省级或统筹地区医疗保障行政部门确定。
11
3. 谈判药品的支付管理
3.4 谈判药品落地先行自付比例管理
3.4.1我国部分省市国家医保谈判药品先行自付比例设定情况
从全国范围内查询60个省市对于各地药品所制定的先行自付比例,仅查询到29个省市有明确的文件对乙类药品先行自付
尼妥珠单抗属于医保报销范围吗?

尼妥珠单抗属于医保报销范围吗?近日,人力资源和社会保障部印发了《关于将36种药品纳入国家基本医疗保险、工伤保险和生育保险药品目录乙类范围的通知》,将36种谈判药品纳入了《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》,并同步确定了这些药品的医保支付标准。
这批新纳入医保目录的药物包括31个西药和5个中成药。
西药中有15个是肿瘤治疗药,覆盖了鼻咽癌、肺癌、胃癌、乳腺癌、结直肠癌、淋巴瘤、骨髓瘤等癌种,用于治疗鼻咽癌的靶向药物尼妥珠单抗名列其中,被纳入国家医保乙类目录。
在各省级医保目录落地实施后,根据政策,一般乙类药品报销比例可达70-80%,意味着中国鼻咽癌患者的医疗负担将被大大减轻,更多的患者将因此获益。
尼妥珠单抗属于医保报销范围吗?由上得知尼妥珠单抗为国家医保乙类目录中可报销的药品,报销比例为70%左右。
鼻咽癌流行病学,全球鼻咽癌发病率中国最高,而中国华南地区发病率最高,以30-50岁为主,男性多于女性。
早期症状通常没有特异性且极易远处转移,75%以上患者就诊时已达晚期。
诱发鼻咽癌的病因主要有遗传因素(有种族及家族聚集现象)、EB病毒因素(鼻咽癌病人血清中EB病毒抗体指数都很高)、环境因素(农药、汽油、甲醛、油漆、硫酸、油烟等)、生活习惯(吸烟、喝酒、嚼槟榔、腌制食品等)。
尼妥珠单抗为全球第1个人源化抗EGFR单抗,亲和力适中,安全性非常好;2002年在古巴批准治疗头颈部肿瘤,目前已在30个国家获批上市,用于头颈部肿瘤、鼻咽癌、食管癌、神经胶质瘤、胰腺癌的治疗;尼妥珠单抗2008年在中国获批上市用于鼻咽癌的治疗,商品名为泰欣生®,是我国唯一一个获批适应症用于治疗鼻咽癌的靶向药物,临床上主要用于与放疗或放化疗联合治疗表皮生长因子受体(EGFR)表达阳性的III/IV期鼻咽癌。
2009年被写入《NCCN头颈部肿瘤临床指南(中国版)》,推荐用于局晚期鼻咽癌的一线治疗。
2014年被写入胰腺癌综合诊治中国专家共识。
江西省人力资源和社会保障厅关于执行国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)的通知

江西省人力资源和社会保障厅关于执行国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)的通知文章属性•【制定机关】江西省人力资源和社会保障厅•【公布日期】2017.08.25•【字号】•【施行日期】2017.08.25•【效力等级】地方规范性文件•【时效性】现行有效•【主题分类】基本医疗保险,工伤保险,生育保险正文江西省人力资源和社会保障厅关于执行国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)的通知各设区市人力资源和社会保障局:为贯彻落实人力资源和社会保障部《关于印发国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)的通知》(人社部发〔2017〕15号)和《关于将36种药品纳入国家基本医疗保险、工伤保险和生育保险药品目录乙类范围的通知》(人社部发〔2017〕54号),保障参保人员基本用药需求,现就执行《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》(以下简称“2017年版国家医保药品目录”)有关事项通知如下,请遵照执行。
一、自2017年9月1日起,全省统一执行2017年版国家医保药品目录,2017年版国家医保药品目录内的所有药品和国家医保价格谈判确定的36种药品全部纳入江西省基本医疗保险基金支付范围。
二、2016年发布实施的《江西省基本医疗保险、工伤保险和生育保险药品目录(2016年修订)》(以下简称“2016年版江西省医保药品目录”)继续执行,其中2017年版国家医保药品目录调整时剔除的药品品种除外。
三、2017年版国家医保药品目录的限定支付范围不做调整。
2016年江西省城乡居民基本医疗保险制度整合确定的药品限定支付范围,与2017年版国家医保药品目录限定支付范围不一致的,继续按2016年版江西省医保药品目录规定执行。
四、在新的特药政策出台前,甲磺酸伊马替尼等七种江西省医保谈判品种继续执行原大病保险特殊药品使用管理政策和结算价格,结算价格高于国家医保谈判价格的,执行国家医保谈判价格。
重庆36种谈判药

重庆36种谈判药重庆市人力资源和社会保障局关于将36种国家谈判药品纳入重庆市基本医疗保险、工伤保险和生育保险药品目录有关事宜的通知渝人社发〔2017〕266号各区县(自治县)人力社保局,两江新区社会保障局,万盛经开区人力社保局,成铁重庆社保部,市社会保险局:为贯彻落实《关于将36种药品纳入国家基本医疗保险、工伤保险和生育保险药品目录乙类范围的通知》(人社部发〔2017〕54号,以下简称“54号文件”)精神,切实减轻参保患者的医疗费用负担,结合我市实际,现就有关事项通知如下,请遵照执行。
一、国家谈判药品目录管理(一)将人力资源社会保障部发布的利拉鲁肽注射剂等36种国家谈判药品(名单见附件)纳入我市基本医疗保险、工伤保险和生育保险药品目录乙类范围。
各定点医疗机构要严格执行谈判药品的限定支付范围,不得扩大或调整。
(二)36种国家谈判药品(以下简称谈判药品)的支付标准按照54号文件的规定执行,支付标准包括医疗保险基金和参保人员共同支付的全部费用,按重庆市医疗保险基金乙类药品规定,参保人先自付10%后纳入医保报销范围。
二、国家谈判药品用药管理(一)事前审查用药管理对以下药品建立限医院(药店)、限医师、限病种、强监管的事前审查制度,具体为曲妥珠单抗、贝伐珠单抗、尼妥珠单抗、利妥昔单抗、厄洛替尼、索拉非尼、拉帕替尼、阿帕替尼、硼替佐米、重组人血管内皮抑制素、西达本胺、阿比特龙、氟维司群、重组人干扰素β-1b、依维莫司、来那度胺、康柏西普、雷珠单抗等18种。
事前审查应执行资格认定、制定治疗方案、备案抽查程序,先由具备资质的医保定点医院,对符合申请使用谈判药品条件的患者,进行资格认定,并对取得资格的参保患者的纸质档案单独建档管理备查,电子档案上传金保系统由医保协议管理所在地社会保险经办机构备案、监管。
在一个自然年度内,每名参保患者原则上选择一家具有相应资质和设备仪器的医保定点医院作为定点治疗机构,治疗机构对取得使用资格患者制定谈判药品的使用方案(以下简称“使用方案”),通过金保系统实现数据上传,医保基金依据谈判药品的支付标准和限制使用范围进行报销和监管,社会保险经办机构对治疗机构上传的数据进行备案、审查(具体办法由市社会保险局另行制定)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
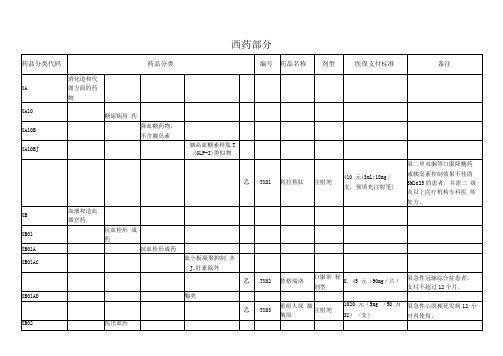
2017年36个国家谈判药品西药部分药品分类代码药品分类编号药品名称剂型医保支付标准备注 XA 消化道和代谢方面的药物 XA10 糖尿病用药XA10B 降血糖药物,不含胰岛素XA10BJ 胰高血糖素样肽-1( GLP-1)类似物乙 TX01 利拉鲁肽注射剂 410 元( 3ml:18mg/支,预填充注射笔)限二甲双胍等口服降糖药或胰岛素控制效果不佳的BMI≥ 25 的患者,并需二级及以上医疗机构专科医师处方。
XB 血液和造血器官药 XB01 抗血栓形成药 XB01A 抗血栓形成药 XB01AC 血小板凝聚抑制剂,肝素除外乙 TX02 替格瑞洛口服常释剂型 8.45 元( 90mg/片)限急性冠脉综合症患者,支付不超过 12 个月。
XB01AD 酶类乙 TX03 重组人尿激酶原注射剂 1020 元( 5mg ( 50 万IU) /支)限急性心肌梗死发病 12小时内使用。
XB02 抗出血药 XB02B 维生素 K 和其他止血药乙 TX04 重组人凝血因子Ⅶ a 注射剂 5780 元( 1mg( 50KIU)/支)限以下情况方可支付:1、凝血因子Ⅷ或Ⅸ的抑制物 5BU 的先天性血友病患者。
2、获得性血友病患者。
3、先天性 FVII 缺乏症患者。
4、具有 GPIIb-IIIa和 /或 HLA抗体和既往或现在对血小板输注无效或不佳的血小板无力症患者。
XC 心血管系统 XC01E 其他心脏疾病用药乙 TX05 重组人脑利钠肽注射剂 585 元( 0.5mg( 500U)/瓶)限二级及以上医疗机构用于规范治疗效果不佳的急性失代偿性心力衰竭短期治疗,单次住院支付不超过 3 天。
XC03 利尿剂 XC03X 其它利尿药乙 TX06 托伐普坦口服常释剂型 99 元( 15mg/片) 168.3 元( 30mg/片)限明显的高容量性和正常容量性低钠血症(血钠浓度 125mEq/L,或低钠血症不明显但有症状且限液治疗效果不佳),包括伴有心力衰竭 /肝硬化以及抗利尿剂激素分泌异常综合征的患者。
XC09 作用于肾素 -血管紧张素系统的药物 XC09C 血管紧张素Ⅱ拮抗剂的单方药乙 TX07 阿利沙坦酯口服常释剂型 7.05 元( 240mg/片) 3.04 元( 80mg/片) XJ 全身用抗感染药 XJ01 全身用抗菌药 XJ01X 其他抗菌药 XJ01XD 咪唑衍生物乙 TX08 吗啉硝唑氯化钠注射剂 106 元( 100ml:500mg吗啉硝唑和 900mg 氯化钠 /瓶)限二线用药。
XJ02 全身用抗真菌药 XJ02A 全身用抗真菌药 XJ02AC 三唑类衍生物乙 TX09 泊沙康唑口服液体剂 2800 元( 40mg/ml 105ml/瓶)限以下情况方可支付:1.预防移植后(干细胞及实体器官移植)及恶性肿瘤患者有重度粒细胞缺乏的侵袭性曲霉菌和念球菌感染。
2.伊曲康唑或氟康唑难治性口咽念珠菌病。
3.接合菌纲类感染。
XL 抗肿瘤药及免疫调节剂 XL01 抗肿瘤药 XL01X 其他抗肿瘤药 XL01XC 单克隆抗体乙TX10 曲妥珠单抗注射剂 7600 元( 440mg( 20ml)/瓶)限以下情况方可支付:1.HER2 阳性的乳腺癌手术后患者,支付不超过 12 个月。
2.HER2 阳性的转移性乳腺癌。
3.HER2 阳性的晚期转移性胃癌。
乙 TX11 贝伐珠单抗注射剂 1998 元( 100mg( 4ml)/瓶)限晚期转移性结直肠癌或晚期非鳞非小细胞肺癌。
乙 TX12 尼妥珠单抗注射剂 1700 元( 10ml:50mg/瓶)限与放疗联合治疗表皮生长因子受体 (EGFR)表达阳性的Ⅲ /Ⅳ期鼻咽癌。
乙 TX13 利妥昔单抗注射剂 2418 元( 100mg/10ml/瓶)8289.87 元( 500mg/50ml/瓶)限复发或耐药的滤泡性中央型淋巴瘤(国际工作分类 B、 C 和 D 亚型的 B 细胞非霍奇金淋巴瘤),CD20阳性Ⅲ -Ⅳ期滤泡性非霍奇金淋巴瘤, CD20 阳性弥漫大 B 细胞性非霍奇金淋巴瘤;最多支付 8 个疗程。
XL01XE 蛋白激酶抑制剂乙 TX14 厄洛替尼口服常释剂型 195 元( 150mg/片) 142.97 元( 100mg/片)限 EGFR基因敏感突变的晚期非小细胞肺癌。
乙 TX15 索拉非尼口服常释剂型 203 元( 0.2g/片)限以下情况方可支付:1.不能手术的肾细胞癌。
2.不能手术或远处转移的肝细胞癌。
3.放射性碘治疗无效的局部复发或转移性、分化型甲状腺癌。
乙 TX16 拉帕替尼口服常释剂型 70 元( 250mg/片)限 HER2过表达且既往接受过包括蒽环类、紫杉醇、曲妥珠单抗治疗的晚期或转移性乳腺癌。
乙 TX17 阿帕替尼口服常释剂型 136 元( 250mg/片) 185.5 元( 375mg/片) 204.15 元( 425mg/片)限既往至少接受过 2 种系统化疗后进展或复发的晚期胃腺癌或胃 -食管结合部腺癌患者。
XL01XW 蛋白酶体抑制剂乙 TX18 硼替佐米注射剂 6116 元( 3.5mg/瓶) 2344.26 元( 1mg/瓶)限多发性骨髓瘤、复发或难治性套细胞淋巴瘤患者,并满足以下条件:1、每 2 个疗程需提供治疗有效的证据后方可继续支付;2、由三级医院血液专科或血液专科医院医师处方;3、与来那度胺联合使用不予支付。
XL01XX 其他抗肿瘤药乙 TX19 重组人血管内皮抑制素注射剂630 元( 15mg/2.4×10 U/3ml/支)限晚期非小细胞肺癌患者。
乙 TX20 西达本胺口服常释剂型 385 元( 5mg/片)限既往至少接受过一次全身化疗的复发或难治的外周 T 细胞淋巴瘤( PTCL)患者。
XL02 内分泌治疗用药 XL02B 激素拮抗剂及相关药物乙 TX21 阿比特龙口服常 144.92 元( 250mg/片)限转移性去势抵抗性前列释剂型腺癌。
乙 TX22 氟维司群注射剂 2400 元( 5ml:0.25g/支)限芳香化酶抑制剂治疗失败后的晚期、激素受体( ER/PR)阳性乳腺癌治疗。
XL03 免疫兴奋剂 XL03A 免疫兴奋剂 XL03AB 干扰素类乙TX23 重组人干扰素β -1b 注射剂 590 元( 0.3mg/支)限常规治疗无效的多发性硬化患者。
XL04 免疫抑制剂 XL04A 免疫抑制剂 XL04AA 选择性免疫抑制剂乙 TX24 依维莫司口服常释剂型 148 元( 5mg/片) 87.05 元( 2.5mg/片)限以下情况方可支付:1.接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌成人患者。
2.不可切除的、局部晚期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。
3.不需立即手术治疗的结节性硬化症相关的肾血管平滑肌脂肪瘤( TSC-AML)成人患者。
XL04AX 其他免疫抑制剂乙 TX25 来那度胺口服常释剂型 866 元( 10mg/粒) 1101.99 元( 25mg/粒)限曾接受过至少一种疗法的多发性骨髓瘤的成年患者,并满足以下条件:1、每 2 个疗程需提供治疗有效的证据后方可继续支付;2、由三级医院血液专科或血液专科医院医师处方;3、与硼替佐米联合使用不予支付。
XN 神经系统药物 XN05 精神安定药 XN05A 抗精神病药 XN05AH 二氮卓类、去甲羟二氮卓类和硫氮杂卓类乙 TX26 喹硫平缓释控释剂型 3.72 元( 50mg/片) 10.76 元( 200mg/片) 14.68 元( 300mg/片) XN06 精神兴奋药 XN06A 抗抑郁药 XN06AB 选择性 5-羟色胺再摄取抑制剂乙 TX27 帕罗西汀肠溶缓释片 4.59 元( 12.5mg/片)7.8 元( 25mg/片) XS 感觉器官药物 XS01 眼科用药 XS01L 眼血管病用药乙 TX28 康柏西普眼用注射液 5550 元( 10mg/ml 0.2ml/支)限 50岁以上湿性年龄相关性黄斑变性患者,并符合以下条件:1.需三级综合医院眼科或二级及以上眼科专科医院医师处方;2.病眼基线矫正视力0.05-0.5;3.事前审查后方可用,初次申请需有血管造影及 OCT(全身情况不允许的患者可以提供 OCT血管成像)证据;4.每眼累计最多支付 9 支,每个年度最多支付 4 支。
乙 TX29 雷珠单抗注射剂 5700 元( 10mg/ml 0.2ml/支、10mg/ml 0.165ml/支(预充式))限 50岁以上湿性年龄相关性黄斑变性患者,并符合以下条件:1.需三级综合医院眼科或二级及以上眼科专科医院医师处方;2.病眼基线矫正视力0.05-0.5;3.事前审查后方可用,初次申请需有血管造影及 OCT(全身情况不允许的患者可以提供 OCT血管成像)证据;4. .每眼累计最多支付 9 支,每个年度最多支付 4 支。
XV 杂类 XV03 其他治疗药物 XV03A 其他治疗药物 XV03AE 高血钾和高磷血症治疗药乙 TX30 司维拉姆口服常释剂型 8.1 元( 800mg/片)限透析患者高磷血症。
乙 TX31 碳酸镧咀嚼片 14.65 元( 500mg/片) 19.98 元( 750mg/片) 24.91 元( 1000mg/片)限透析患者高磷血症。
中药部分药品分类代码药品分类编号药品名称支付标准备注 ZA 内科用药 ZA12 祛瘀剂 ZA12H 化瘀通脉剂乙 TZ01 银杏二萜内酯葡胺注射液 316 元( 5ml/支,含银杏二萜内酯 25mg)限二级及以上医疗机构脑梗死恢复期患者,单次住院最多支付 14 天。
乙 TZ02 银杏内酯注射液 79 元( 2ml/支,含萜类内酯 10mg)限二级及以上医疗机构脑梗死恢复期患者,单次住院最多支付 14 天。
ZC 肿瘤用药 ZC01 抗肿瘤药乙 TZ03 复方黄黛片 10.5 元( 0.27g/片)限初治的急性早幼粒细胞白血病。
ZC02 肿瘤辅助用药乙 TZ04 注射用黄芪多糖 278 元( 250mg/瓶)限二级及以上医疗机构肿瘤患者,单次住院最多支付 14 天。
乙 TZ05 参一胶囊 6.65元(含人参皂苷 Rg3 10mg/粒)限原发性肺癌、肝癌化疗期间同步使用。
