实验室间比对报告
实验室间比对和能力验证结果的分析报告

实验室间比对和能力验证结果的分析报告质管办为了通过适时开展比对试验和能力验证等质量控制活动,对检测质量及其过程的有效性进行监控,保证检测工作的质量,确保检测结果的准确、可靠、有效,或者为无法溯源的检测设备和标准物质提供评价测量结果的可靠证据,依据《实验室资质认定评审准则》和本中心《质量手册》、《程序文件》要求,2009年我中心参加了上级部门组织的实验室间比对和能力验证,定期开展内部质量控制活动,采用有证标准物质测定、留样再测、平行样测定、空白对照试验等进行人员和方法的比对。
现将2009年的质量控制结果报告如下:一、质量控制方法1、外部质量控制(1)参加国家碘缺乏病参照实验室组织的县级实验室盐碘外质控考核;(2)参加福建省疾病预防控制中心(实验室间比对)乙肝病毒血清标志物质控考核;(3)参加泉州市疾病预防控制中心组织的实验室卫生检测质量考核。
(4)接受福建省技术监督局计量认证监督评审现场试验考核。
2、内部质量控制(1)组织人员和方法比对;(2)开展检测过程平行样、空白试验;(3)抽查检测报告,考核平行样、空白试验是否符合规定要求。
二、质量控制内容和结果1、参加国家碘缺乏病参照实验室组织的县级实验室盐碘外质控考核,见表1。
表1 盐碘外质控考核结果2、参加福建省CDC(实验室间比对)乙肝标志物质控考核,见表2。
表2 乙肝病毒血清标志物质控考核结果3、参加泉州市疾控中心组织的实验室卫生检测质量考核,见表3、表4。
表3 酱油中总酸、氨基酸态氮考核结果表4 标准菌株微生物鉴定考核结果4、内部组织的人员比对和方法比对,见表5、表6。
表5 微生物留样再测结果表6 内部考核样品考核结果5、平行样、空白试验。
抽查25份检测原始记录,其平行样的相结相差均符合相关检验方法的精确度要求,符合率100%,每批样品检测均做空白对照试验,符合检测方法的要求。
6、2009年3月份通过省技术监督局组织的监督评审组的现场试验考核,共考核个样品(标本)41个项目。
实验室内部比对报告

实验室内部比对报告
1. 数据比对,比对报告会列出不同实验室或不同时间点获得的数据,并进行逐项比对。
这有助于发现数据之间的差异或一致性,以及可能存在的误差或偏差。
2. 结果分析,比对报告会对比对结果进行详细的分析,包括数据的一致性、差异性以及可能的原因。
这有助于评估实验室工作的稳定性和可靠性。
3. 质量控制,比对报告还会包括实验室内部的质量控制数据,以确保实验室工作符合标准和规范。
4. 建议和改进,比对报告通常会提出建议和改进意见,以帮助实验室改进工作流程和提高数据准确性。
5. 结论,比对报告最后会给出结论,总结比对结果并指出实验室工作的优点和不足之处,以及可能的改进方向。
综上所述,实验室内部比对报告是实验室质量管理的重要组成
部分,它有助于确保实验室的数据和结果的准确性和可靠性,提高实验室工作的质量和效率。
希望这些信息能够帮助到你。
比对试验报告范文

比对试验报告范文
试验报告比对
1.实验目的
两份试验报告的实验目的是否一致?是否清晰明确?是否与实验内容相关?
2.实验原理
两份试验报告的实验原理是否相同?是否准确描述了实验的基本原理和背景知识?
3.实验过程
两份试验报告的实验过程是否一致?是否包含了实验所需的步骤和材料清单?是否详细说明了实验操作的正确性和安全性?
4.数据处理
两份试验报告的数据处理方法是否一致?是否采取了合理的数据处理方法和统计分析方法?是否准确报告了实验结果?
5.结论
两份试验报告的结论是否一致?是否根据实验结果进行了科学准确的分析和总结?
6.论述和文献引用
两份试验报告的论述是否清晰连贯?是否有科学的逻辑结构和论证过程?是否准确引用了相关的文献资料?
7.图表和图像
两份试验报告的图表和图像是否清晰,易于理解和解读?是否包含了
必要的图例和单位标注?
8.语言表达
两份试验报告的语言表达是否准确、简练、规范?是否存在拼写、语
法或用词错误?
9.格式和排版
两份试验报告的格式和排版是否一致?是否符合报告的要求和规范?
是否包含了封面、目录、摘要、引言、实验方法、结果分析、结论等部分?
10.建议和改进
对两份试验报告的优点和不足进行分析,并提出改进的建议。
通过比对试验报告,可以评估其质量和准确性,并提出改进的建议,
以进一步提升试验报告的可信度和科学性。
158河北省临床实验室室内质控结果室间比对分析与总结

文件要求
[卫办医政发(2021)108号] 卫生部“关于加强医疗质量控制中心建设推
进同级医疗机构检查结果互认工作的通知〞
启动
❖ 河北省三级医疗机构临床实验室室内质控工 作会议
❖ 时间:2021 年8月12-14日 ❖ 地点:张家口市召开 ❖ 全体委员、河北省三级医院检验科负责人40
质控物水平3总蛋白(Prot)室内质控结果月均值图
由图可见, 12家临床实验室室内质控结果月均值在全省月均值±1SD范围 内,5家室内质控结果月均值在全省月均值的±2SD范围内;按可接受范围 为66.27—73.25 g/L判断,13家室内质控结果月均值在可接受范围内, 4家 室内质控结果月均值不在可接受范围内。
由图可见,17家临床实验室室内质控结果月均值在全省月均值±1SD范围 内,7家室内质控结果月均值在全省月均值±2SD范围内。
我省参加室内质控结果实时上传的实验室室内 质控结果总体情况:
质控物水平2和质控物水平3钠(Na)测定全省数据变异系数最小 (1.2%;2.0%),丙氨酸氨基转移酶(ALT)质控物水平2、肌酸激酶(CK)质 控物水平3测定全省数据变异系数最大(5.8%;6.8%)。其他工程相对稳 定。 质控物水平2和质控物水平3八项生化测定工程变异系数均有不同程度的 逐渐减小。 由此看出,我省室内质控有一定改进,也反映各实验室负责人对此项工 作的重视。 测定工程变异系数屡次位于全省最大的实验室请结合实验室的具体情况 分析查找原因。
质控物水平3肌酸激酶(CK)室内质控结果月均值图
由图可见,12家临床实验室室内质控结果月均值在全省月均值±1SD范围 内,5家室内质控结果月均值在全省月均值±2SD范围内;按可接受范围为 判断,17家室内质控结果月均值均在可接受范围内。
实验室间比对

实验室间比对实验室间比对是指将同一样本在不同实验室或不同仪器上进行测试,以评估实验室之间的测试结果的一致性和可靠性。
这对于确保测试结果的准确性非常重要,尤其是在医学、环境监测、食品安全等领域,以及各类科研实验中。
实验室间比对通常通过参与者采集样本,并将样本分发给多个实验室,每个实验室进行测试,然后将测试结果进行比对和分析。
这样可以评估不同实验室之间的测试方法、仪器和技术之间是否存在差异,以及测试结果的准确性和一致性。
首先,实验室间比对可以用来评估不同实验室的测试方法是否一致。
不同实验室可能会使用不同的样本处理方法、测试方法和仪器设备。
通过实验室间比对,可以确定这些差异是否会对测试结果产生影响,从而有针对性地进行改进和校准。
其次,实验室间比对也可以评估测试结果的准确性和可靠性。
如果不同实验室的测试结果一致,那么可以认为这些测试结果具有较高的准确性和可靠性。
然而,如果一些实验室的测试结果与其他实验室存在较大差异,那么就需要进一步调查,找出原因并采取措施来改进测试准确性。
在实验室间比对中,还需要注意一些潜在的误差源。
首先,样本的采集和分发过程中可能存在误差。
样本的采集人员需要经过培训,并按照统一的标准和流程操作,以确保样本的一致性和代表性。
其次,不同实验室的测试人员也需要经过培训,以确保他们正确操作仪器并遵守测试方法。
此外,实验室间比对还需要注意样本的保存和运输条件,以避免样本在采集和测试过程中发生变化。
实验室间比对的结果可以用于制定和改进质量控制程序。
如果实验室间的差异较大,可能需要重新评估和标定仪器,优化测试方法,并制定更严格的质量控制程序。
通过实验室间比对,可以帮助实验室提高测试的准确性和可靠性,确保测试结果的一致性,从而提高实验室的信誉和可信度。
值得注意的是,实验室间比对并不是一次性的过程,而是一个持续的质量改进过程。
实验室需要定期参与实验室间比对,并根据比对结果进行改进和调整,以确保测试的准确性和可靠性。
临床检验室内质量控制数据实验室间比对.

临床检验室内质量控制数据实验室间比对nbsp;nbsp;nbsp;nbsp;nbsp;nbsp;近年来临床实验室均开展了常规检测项目的室内质量控制,但室内质量控制效果如何,长期以来没有找到一种精确的方法能对其进行全面评价。
“室间质量评价”只能评价其不准确度,但还无法对实验室内的不精密度进行评价。
现在我们近年来临床实验室均开展了常规检测项目的室内质量控制,但室内质量控制效果如何,长期以来没有找到一种精确的方法能对其进行全面评价。
“室间质量评价”只能评价其不准确度,但还无法对实验室内的不精密度进行评价。
现在我们终于能从“室内质量控制数据实验室间比对计划”中获取不准确度和不精密度这两个方面有价值的信息。
一、原理和方法“室内质控数据实验室间比对计划”要求检测同一批号质控物的不同实验室,向该计划的组织者提供每月原始的室内质控数据 [1] 。
组织者会按时回报结果。
在回报的结果中,各实验室可得到自己实验室分析过程的不准确度和不精密度与使用相同方法的其他实验室的不准确度和不精密度进行比较,也可得到与其他使用不同方法的实验室的结果进行比较。
这些信息很有价值,尤其是解决潜在的问题时能够提供帮助。
如相同方法组 ( 使用同一方法的实验室 ) 的均值是该质控物靶值的最好来源。
该计划的组织者通过汇总的数据或单个数据点来分析数据并剔除有显著性的离群值。
计算机对每一批号质控物、每一项目、使用每一分析方法的所有实验室计算平均值、中位数、标准差和变异系数。
如果每月定期评价这一信息,相对于相同方法组可评价自己方法的不准确度和不精密度。
比对计划对每一分析项目和每一批号质控物提供下列信息[2] : (1) 当前月份的均值、标准差 (s) 和结果个数 (N) ; (2) 计划开始至现在该质控物的累积的均值、标准差 (s) 和结果个数 (N) ; (3) 相同方法组的方法均值、标准差 (s) 或变异系数 (CV) 和实验室个数; (4) 每一分析项目所有实验室的所有实验室均值、标准差 (s) 或变异系数 (CV) 和实验室个数; (5) 方法的标准差指数 (SDI) ——本室均值偏离相同方法组均值的变异,以相同方法组标准差 (s) 为单位的度量; (6) 所有实验室的标准差指数(SDI) ——本室均值偏离所有实验室均值的变异,以所有实验室的标准差为单位的度量; (7) 方法变异系数指数 (CVI) ——本室报告的变异系数 (CV) 或标准差 (s) 与使用相同方法实验室报告的变异系数 (CV) 或标准差 (s) 的比值; (8) 所有实验室的变异系数指数 (CVI) ——本室报告的变异系数 (CV) 或标准差 (s) 与所有实验室报告的变异系数或标准差的比值。
实验室间及实验室内部比对试验结果记录及分析报告表

实验室间及实验室内部比对试验结果记录及分析报告表
9年中心参与国家认可委能力验证、中国CDC的质控考核,共涉及4个部门。
一、验室间比对和能力验证结果
(一)中心参加中国CDC的实验室间比对有艾滋病确证实验室、理化实验室、传染病检测实验室、门诊实验室。
具体的项目:
1、水中铅、镉、砷的测定;
、化妆品中铅、汞、砷的测定;
3、艾滋病检测实验室质量考评;
4、梅毒螺旋体抗原清学检测;
5、碘伏消毒剂对铜绿假单胞菌杀灭效果检测。
测定结果:
水中铅、镉、砷的测定项目有铅、镉的结果出现不满意结果,化妆品中铅、汞、砷的测定项目有铅出现不满意结果,其余,均为满意结果。
门诊实验室的梅毒螺旋体抗原清学检测达到1分,艾滋病确证实验室的淋巴细胞免疫表型检测
(二)参加实验室认可的能力验证的实验室有理化和微生物实验室。
具体项目:
食品(虾粉)中砷与重金属的检测、食品(果蔬汁)中对羟基苯甲酸乙酯、环己基氨基磺酸钠、日落黄和酒石黄的检测。
测定结果:
食品(虾粉)中砷与重金属的检测项目有砷、总汞、镉、铜的测定,其中总汞、镉出现不满意结果;食品(果蔬汁)中对羟基苯甲酸乙酯、环己基氨基磺酸钠、日落黄和酒石黄的检测项目测定三个项目,全部为满意结果。
实验室间比对结果

实验室间尾气比对试验
分析报告
灌云县汽车综合性能检测站
一、实验室间比对目的
1、确定实验室进行某些特定检测或测量的能力,以及监控实验室的持续能力;
2、识别实验室中的问题并制定相应的补救措施,这些措施可能涉及诸如个别人员的行为或仪器的校准等;
3、确定新的检测和测量方法的有效性和可比性,并对这些方法进行相应的监控;
4、增加实验室用户的信心;
5、识别实验室间的差异。
二、试验方法
参与比对的车辆按《点燃式发动机汽车排气污染物排放限值及测量方法(双怠速法及简易工况法)》在本站和其他站分别进行检测。
检测结果汇总技术科进行分析判定。
三、试验结果及分析
同样采用GB 18285-2005,本站与灌南站的检测结果如下表所示。
结论:
1、稳态工况法测量结果达到预期目的,较满意在可控范围,没有离群。
2、双怠速法测量结果没有达到预期目的,对些次比对结果不满意。
经对人员、设备、环境等相关因素分析并询问当时操作过程。
由于灌南站与我站在双怠速法检测过程中,引车员对转速控制上不严格,造成检测结果误差较大。
两站控制系统的都由同一公司提供,该系统没有按标准设计对转速控制,取样过程不符合要求。
联系厂家修改软件系统,对检测过程严格控制,消除人为影响。
四、附件
二份稳态工况法和二份双怠速法检测报告。
签发人:
年月日。
比对试验结果分析报告

比对试验结果分析报告[报告编号:XXXXX][报告日期:XXXX年XX月XX日][委托单位:XXX公司][试验单位:XXX实验室][试验人员:XXX][试验日期:XXXX年XX月XX日至XXXX年XX月XX日][试验摘要:本试验旨在比较两种不同型号的产品,并分析其试验结果,为生产过程中的选型提供参考。
]一、测试目的本次试验主要目的是比对两种不同型号的产品的性能差异,并对测试获得的结果进行分析。
二、测试方法1.试验设备本试验采用了XXX实验室的XXX测试设备来进行测试。
2.试验过程本试验对比测试了两种不同型号的产品在不同条件下的性能表现,分别是:XXXX条件下和XXXX条件下。
3.测试指标本试验主要测试了以下指标:(1)XXX性能(2)XXX性能(3)XXX性能(4)XXX性能三、测试结果分析1.数据对比根据测试结果数据分析,两种产品在不同条件下的性能表现差距较小,测试数据如下:(1)在XXXX条件下:指标测试产品1 测试产品2 差距XXX 15.62 15.75 1%XXX 24.85 25.02 0.6%XXX 18.35 18.78 2.3%XXX 22.77 22.43 1.4%(2)在XXXX条件下:指标测试产品1 测试产品2 差距XXX 20.12 20.23 0.7%XXX 34.83 34.99 0.5%XXX 27.54 28.01 1.7%XXX 35.76 35.89 0.4%2.结果分析通过对比测试数据的分析,我们发现两种不同型号的产品在性能表现上区别不大,差距都在2.3%以内。
根据试验指标和参考标准,两种类型的产品都具有比较优秀的性能表现。
四、结论本次试验的结果表明,两种不同型号的产品在性能表现上差距不大,都具有比较优秀的性能表现。
在生产选择时,可以根据实际需求和生产成本进行综合考虑,并进行个性化的选择。
五、建议为了更好地提升产品的性能表现,建议在生产中对比不同种类的产品进行测试,以确保生产出的产品具有更好的性能表现。
实验室间比对报告(内容清晰)

实验室间比对报告检测报告报告编号:HJ-B-ZW-J.003-2012项目名称:实验室间比对委托单位:检测类型:实验室质量控制报告日期:2011年7月25日XXXXXXXXXXXX声明1、检测报告无“计量认证标志及认证号”、“国家实验室认可标志及认可号”和“检测专用章”无效。
2、检测报告涂改、增删无效,骑缝章不完整无效。
3、未经本单位书面通知,不得部分复制(全文复制除外)检测报告。
4、检测报告无编制人、审核人、批准人签字无效。
5、被检测单位对本检测报告若有异议,应于收到检测报告之日起15日内向我单位提出复核申请,逾期视作对本报告无异议。
6、未经本单位同意,任何单位和个人不得以本单位名义和本检测报告做商业广告。
7、凡伪造本单位检测报告,作虚假报告,本单位将追究法律责任。
8、本检测报告一式二份,一份由检测机构存档,一份交被检单位。
9、检测报告中标注“#”号的项目不属于国家实验室认可项目。
联系地址:湖北省xxxxx温泉城区贺胜路87号电话/传真:(0715)8266933邮编:437100检测检验报告受检单位/承检类别实验室质量控制检测数量 2检测日期2011年7月25日报告日期2011年7月25日检测项目活性碳管中正已烷含量检测依据《工作场所空气有毒物质测定烷烃类化合物》GBZ/T160.38-2007检测结果:序检测物检测物检测结果/含量实际含量检测结果与比对机构名称允许误差备注号编号名称(μg)(μg)实际含量误差1xxxxx疾病ZK006/1 正已烷279.1 266 ±16 +13.1 允许误差预防控制中心22 范围内2XXXXX ZK006/1 正已烷262.4 266 ±16 -3.6 允许误差XXXXX 22 范围内XXX机构间比对误差:(279.1-262.4)270.75=6.2%在本次与xxxxx疾病预防控制中心的比对实验中,同时对编号为ZK006/122的正已烷进行了检测,该物质实际含量为266μg,允许误差为±16μg,双方自行设定机构间检测误差不得超过12%。
实验室间及实验室内部比对试验结果记录及分析报告表
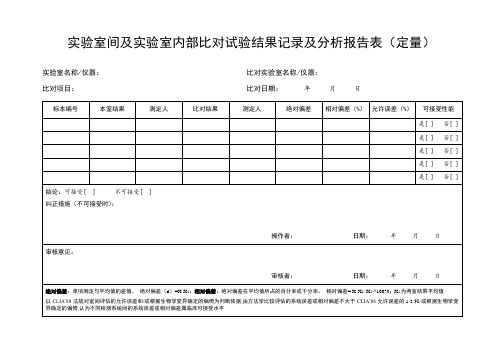
实验室名称/仪器: 比对项目:
标本编号
本室结果
测定人
结论:可接受[ ]
不可接受[ ]
纠正措施(不可仪器:
比对日期:
年月日
测定人
绝对偏差
相对偏差(%) 允许误差(%) 可接受性能 是[ ] 否[ ] 是[ ] 否[ ] 是[ ] 否[ ] 是[ ] 否[ ] 是[ ] 否[ ]
本室(X) 阳性
( %)YPN ( %)YPP ( %)XP 偶然一致性
总数 ( %)YN ( %)YP ( %)TT
审核意见:
操作者:
日期:
年月日
审核者:
日期:
年月日
观察的一致性=(实验室 X 和实验室 Y 同为阴性结果数 + 实验室 X 和实验室 Y 同为阳性结果数)/ 标本总数; 偶然一致性= (实验室 X 阴性结果的百分比 0.01) (实验室 Y 阴性结果的百分比 0.01) + (实验室 X 阳性结果百分比 0.01) (实验室 Y 阳性结果百分比 0.01); Kappa=(观察的一致性 – 偶然一致性)/(1- 偶然一致性);Kappa 值高于 0.8 可认为具有良好的分析一致性,而在 0.6 和 0.8 之间认为是具有适当的分析一致性。
实验室间及实验室内部比对试验结果记录及分析报告表(定性)
实验室名称/仪器: 比对项目:
标本编号 本室结果
比对数据 测定人
比对结果
结论:可接受[ ]
不可接受[ ]
纠正措施(不可接受时):
测定人
比对实验室名称/仪器:
比对日期:
年月日
结果计算
比对 实验 室(Y)
实验室间比对和能力验证结果的分析报告

实验室间比对和能力验证结果的分析报告质管办为了通过适时开展比对试验和能力验证等质量控制活动,对检测质量及其过程的有效性进行监控,保证检测工作的质量,确保检测结果的准确、可靠、有效,或者为无法溯源的检测设备和标准物质提供评价测量结果的可靠证据,依据《实验室资质认定评审准则》和本中心《质量手册》、《程序文件》要求,2009年我中心参加了上级部门组织的实验室间比对和能力验证,定期开展内部质量控制活动,采用有证标准物质测定、留样再测、平行样测定、空白对照试验等进行人员和方法的比对。
现将2009年的质量控制结果报告如下:一、质量控制方法1、外部质量控制(1)参加国家碘缺乏病参照实验室组织的县级实验室盐碘外质控考核;(2)参加福建省疾病预防控制中心(实验室间比对)乙肝病毒血清标志物质控考核;(3)参加泉州市疾病预防控制中心组织的实验室卫生检测质量考核。
(4)接受福建省技术监督局计量认证监督评审现场试验考核。
2、内部质量控制(1)组织人员和方法比对;(2)开展检测过程平行样、空白试验;(3)抽查检测报告,考核平行样、空白试验是否符合规定要求。
二、质量控制内容和结果1、参加国家碘缺乏病参照实验室组织的县级实验室盐碘外质控考核,见表1。
表1 盐碘外质控考核结果2、参加福建省CDC (实验室间比对)乙肝标志物质控考核,见表2。
表2 乙肝病毒血清标志物质控考核结果3、参加泉州市疾控中心组织的实验室卫生检测质量考核,见表3、表4。
表3 酱油中总酸、氨基酸态氮考核结果4、内部组织的人员比对和方法比对,见表5、表6。
表5 微生物留样再测结果表6 内部考核样品考核结果5、平行样、空白试验。
抽查25份检测原始记录,其平行样的相结相差均符合相关检验方法的精确度要求,符合率100%,每批样品检测均做空白对照试验,符合检测方法的要求。
6、2009年3月份通过省技术监督局组织的监督评审组的现场试验考核,共考核个样品(标本)41个项目。
实验室间比对报告书

泸州靠得住食品有限公司化验室理化试验比对结果报告
编制:审核:批准:日期:日期:日期:
泸州靠得住食品有限公司实验室比对计划
—固态类及非固态产品理化含量结果报告
一. 前言
为了提高我公司检验工作水平,进一步促进我司提高检验工作质量。
二. 本次计划的特点
1.目的和意义
为了便于实验室发现、分析并解决检验工作中存在的问题,促进实验室进一步提高检测技术和加强实验室管理,尤其是检测结果不准确的地方,更要寻找原因,采取措施,保证日常检测结果的准确、可靠。
2.参加人员
本化验室全体人员。
3.计划测试项目和要求
3.1 本次实验室间比对计划按照同样品,两两一组,同时测出的理化数据相比较,同时,并与国家酒业检验中心为我公司的样品出的检验报告单(外检报告)据做数据比对,误差不超过5%为合格。
来保证结果的有效性。
4.样品情况描述
4.1 本次提供的样品是金沙骨腌酱和新奥尔良腌料,在规定条件下分装于玻璃瓶中,轧盖密封,每瓶装量100g,分别标注相应的样品编号。
化验员对分装后的样品进行了均匀性检验,结果显示样品的均匀性符合要求。
相关数据见附件1与附表2。
4.2 每个参加本次收到1瓶检测样品。
三、结论
3.1通过本次比对结果可以表明,我公司的试验数据误差均符合要求。
3.2金沙酱的氨基酸态氮不符合原因为:化验员2将该组样品破坏,所以该组数
据取消。
泸州靠得住食品有限公司
二O一二年八月
附表1
金沙骨腌酱比对结果
附表2
新奥尔良腌料对比结果。
实验室间比对和能力验证结果的分析报告---精品模板

实验室间比对和能力验证结果的分析报告质管办为了通过适时开展比对试验和能力验证等质量控制活动,对检测质量及其过程的有效性进行监控,保证检测工作的质量,确保检测结果的准确、可靠、有效,或者为无法溯源的检测设备和标准物质提供评价测量结果的可靠证据,依据《实验室资质认定评审准则》和本中心《质量手册》、《程序文件》要求,2009年我中心参加了上级部门组织的实验室间比对和能力验证,定期开展内部质量控制活动,采用有证标准物质测定、留样再测、平行样测定、空白对照试验等进行人员和方法的比对。
现将2009年的质量控制结果报告如下:一、质量控制方法1、外部质量控制(1)参加国家碘缺乏病参照实验室组织的县级实验室盐碘外质控考核;(2)参加福建省疾病预防控制中心(实验室间比对)乙肝病毒血清标志物质控考核;(3)参加泉州市疾病预防控制中心组织的实验室卫生检测质量考核。
(4)接受福建省技术监督局计量认证监督评审现场试验考核。
2、内部质量控制(1)组织人员和方法比对;(2)开展检测过程平行样、空白试验;(3)抽查检测报告,考核平行样、空白试验是否符合规定要求.二、质量控制内容和结果1、参加国家碘缺乏病参照实验室组织的县级实验室盐碘外质控考核,见表1。
表1 盐碘外质控考核结果2、参加福建省CDC(实验室间比对)乙肝标志物质控考核,见表2。
表2 乙肝病毒血清标志物质控考核结果3、参加泉州市疾控中心组织的实验室卫生检测质量考核,见表3、表4。
表3 酱油中总酸、氨基酸态氮考核结果4、内部组织的人员比对和方法比对,见表5、表6.表5 微生物留样再测结果表6 内部考核样品考核结果5、平行样、空白试验。
抽查25份检测原始记录,其平行样的相结相差均符合相关检验方法的精确度要求,符合率100%,每批样品检测均做空白对照试验,符合检测方法的要求。
6、2009年3月份通过省技术监督局组织的监督评审组的现场试验考核,共考核个样品(标本)41个项目。
三、讨论1、开展实验室间比对活动,组织人员或方法比对在实验室内进行平行样的试验等实验室质量控制活动,都是实验室质量控制的有效方法。
实验室间比对和能力验证结果的分析报告完整版

实验室间比对和能力验证结果的分析报告 HEN system office room 【HEN16H-HENS2AHENS8Q8-HENH1688】湖北华源包装有限公司实验室间比对和能力验证结果的分析报告为了通过适时开展比对试验和能力验证等质量控制活动,对检测质量及其过程的有效性进行监控,保证检测工作的质量,确保检测结果的准确、可靠、有效,或者为无法溯源的检测设备和标准物质提供评价测量结果的可靠证据,依据《实验室资质认定评审准则》和公司《质量手册》、《程序文件》要求,2011年我组织了实验室间比对和能力验证,定期开展内部质量控制活动,采用有证标准物质测定、留样再测、平行样测定、空白对照试验等进行人员和方法的比对。
现将2011年的质量控制结果报告如下:一、质量控制方法:1、外部质量控制(1)接受省技术监督局计量认证监督评审现场试验考核。
2、内部质量控制:(1)组织人员和方法比对;(2)开展检测过程平行样、空白试验;(3)抽查检测报告,考核平行样、空白试验是否符合规定要求。
二、质量控制内容和结果:1、参加省技术质量计量认证监督物理数据鉴定考核,见表1表1 物理数据鉴定考核记录2、参加省质量技术监督局组织的产品卫生检测质量考核,见表23、内部组织的人员比对和方法比对,见表3表3 内部考核样品考核结果4、平行样、空白试验。
抽查25份检测原始记录,其平行样的相结相差均符合相关检验方法的精确度要求,符合率100%,每批样品检测均做空白对照试验,符合检测方法的要求。
5、2011年11月份通过省技术监督局组织的监督评审组的现场试验考核,共考核个样品(标本)10个项目。
三、讨论1、开展实验室间比对活动,组织人员或方法比对在实验室内进行平行样的试验等实验室质量控制活动,都是实验室质量控制的有效方法。
对于可溯源的物理分析和不可溯源的卫生检验,比对和能力验证活动都可提供评价其测量结果可靠性的证据,同时也可证实实验室比对和卫生检测质量考核活动,组织人员比对和方法比对,通过考核平行样、空白试验等开展内部质量控制活动,符合公司质量管理体系有关质量控制规定的要求。
能力验证和实验室间比对结果的分析报告

1.综合评价
该鉴定书的要件齐全,格式规范;对原发损伤的诊断正确,对眼眶陈旧性病变(损伤)性质认定不正确;鉴定结论与专家公议结果部分一致。
综合分析:本所一直重视能力验证的参加,从历次参加能力验证的结果分析,本所鉴定人员在案情分析上还存在一定的不到位之处,建议本所多参加鉴定机构间的交流和学习培训,进一步提高鉴定水平,尽可能取得满意结果。
技术负责人:李福玉
2012年6月17日
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验室间比对报告检测报告报告编号:HJ-B-ZW-J.003-2012项目名称:实验室间比对委托单位:检测类型:实验室质量控制报告日期:2011年7月25日XXXXXXXXXXXX声明1、检测报告无“计量认证标志及认证号”、“国家实验室认可标志及认可号”和“检测专用章”无效。
2、检测报告涂改、增删无效,骑缝章不完整无效。
3、未经本单位书面通知,不得部分复制(全文复制除外)检测报告。
4、检测报告无编制人、审核人、批准人签字无效。
5、被检测单位对本检测报告若有异议,应于收到检测报告之日起15日内向我单位提出复核申请,逾期视作对本报告无异议。
6、未经本单位同意,任何单位和个人不得以本单位名义和本检测报告做商业广告。
7、凡伪造本单位检测报告,作虚假报告,本单位将追究法律责任。
8、本检测报告一式二份,一份由检测机构存档,一份交被检单位。
9、检测报告中标注“#”号的项目不属于国家实验室认可项目。
联系地址:湖北省xxxxx温泉城区贺胜路87号电话/传真:(0715)8266933邮编:437100检测检验报告受检单位/承检类别实验室质量控制检测数量 2检测日期2011年7月25日报告日期2011年7月25日检测项目活性碳管中正已烷含量检测依据《工作场所空气有毒物质测定烷烃类化合物》GBZ/T160.38-2007检测结果:序检测物检测物检测结果/含量实际含量检测结果与比对机构名称允许误差备注号编号名称(μg)(μg)实际含量误差1xxxxx疾病ZK006/1 正已烷279.1 266 ±16 +13.1 允许误差预防控制中心22 范围内2XXXXX ZK006/1 正已烷262.4 266 ±16 -3.6 允许误差XXXXX 22 范围内XXX机构间比对误差:(279.1-262.4)270.75=6.2%在本次与xxxxx疾病预防控制中心的比对实验中,同时对编号为ZK006/122的正已烷进行了检测,该物质实际含量为266μg,允许误差为±16μg,双方自行设定机构间检测误差不得超过12%。
实际检测结果:双方对该物质的检测除了符合在实际浓度允许误差范围内外,机构间比对误差为6.2%,在自行设定的允许误差范围内(检测专用章)批准人:审核人:编制人:年月日年月日年月日附件3.3 结果报告单(仪器比对)仪器名称型号测试项目测试方法测试时间测试者环境条件4、样品测定结果填报日期:检测单位(盖章)检测检验报告受检单位/承检类别实验室质量控制检测数量 2检测日期2011年7月25日报告日期2011年7月25日检测项目活性碳管中正已烷含量检测依据《工作场所空气有毒物质测定烷烃类化合物》GBZ/T160.38-2007检测结果:标准物质ZK006/404中正已烷含量为485.848μg标准物质ZK006/122中正已烷含量为262.358μg(检测专用章)批准人:审核人:编制人:年月日年月日年月日样品信息采集日期和时间:2011-7-25 15:40:32用户名:Admin样品瓶号:2样品名称:正已烷标准1-1样品 ID :样品类型:标准样进样量:1.00复式进样:1稀释因子:1内标量:样品数:1级别好:1数据名:E:\数据文件\正已烷\标准1-1.gcd原始数据名:E:\数据文件\正已烷\标准1-1.gcd基线数据名:方法文件名:D:\方法文件\正已烷外标曲线.gcm报告名:C:\GCsolution\System\DEFAULT.gcb 批处理文件名:E:\数据文件\正已烷\标准曲线.gcb方法<分析线1>[自动采样AOC-20i+s]进样体积:1.0 ul进样前溶剂冲洗次数:0进样后溶剂冲洗次数:5进样前样品冲洗次数:0柱塞吸入速度:高速吸入后待机时间:0.2 sec柱塞进样速度:高速进样进样速递:高速进样方式:普通多重进样计数:1抽吸时间:5 times进样后延迟时间:0.0 sec末端空气间隙:无柱塞洗涤速度:高速洗涤吸入量:8 ul进样器吸入时位置:0 mm进样器进样时位置:0 mm溶剂选择:所有A,B,C[进样口SPL1]进样方式:分流温度:200.0℃载气:氮气/空气流量控制方式:压力压力:218.1 kPa总流量:49.8 ml/min柱流量:2.23 ml/min线速度:35.3 cm/sec吹扫流量:3.0 ml/min分流比:20.0高压力进样:关闭节省载气:关闭分流阻尼固定:关闭[柱箱]初始温度:40.0℃平衡时间:1.0 min=柱箱温度程序=总程序时间:6.00 min比率(℃/min)温度(℃)保留时间(min)------- 40.0 6.00[柱箱信息]色谱柱名称:RTX-1序列号:膜厚:0.25 um柱长:60.0 m内径:0.25 mm ID温度上限:330 ℃安装日期:2010/07/06[检测器通道1 FIDI]温度:250.℃信号采集:是采样速率:40 msec停止时间:6.00 min延迟时间:0.00 min检测器信号差减:无尾吹气:氮气/空气尾气流量:30.0 ml/min氢气流量:40.0 ml/min空气流量:400.0 ml/min[常规参数]<加热单元检查>柱箱:是SPL1:是FID1:是<检测器(FTD)检查><基线漂移检查>FID1:无<进样口流量检查>SPL1载气:是SPL1吹扫:是<APC流量检查><检测器APC流量检查>FID1尾吹:是FID1氢气:是FID1空气:是外部信号等待:无自动点火:是自动熄火:是再点火:无准备好后自动调零:是[波形处理参数-通道1]半峰宽:3 sec 斜率:1000 uV/min漂移:0 uV/min T.DBL :1000 min最小面积/峰高:1000单位[定量参数-通道1]=定量参数=定量方法:外标法计算依据:面积校准级别:5:未过远点校准曲线:直线通过原点:未过原点权重:无单位:ug/ml=综合参数=时间窗/时间带:时间窗时间窗:5 %默认时间带:----- 识别方法:绝对保留时间峰选择:所有峰分组:无校准保留时间:不改变[组分表-通道1]ID# 名称类型保留时间浓度1 浓度2 浓度3 浓度4 浓度5 单位1 正已烷目标 4.411 39.618 99.045 198.090 396.180 792.360[校准信息-通道1]数据文件级别:1E:\数据文件\正已烷\标准1-1.gcdE:\数据文件\正已烷\标准1-2.gcdE:\数据文件\正已烷\标准1-3.gcd级别:2E:\数据文件\正已烷\标准2-1.gcdE:\数据文件\正已烷\标准2-2.gcdE:\数据文件\正已烷\标准2-3.gcd级别:3E:\数据文件\正已烷\标准3-1.gcdE:\数据文件\正已烷\标准3-2.gcdE:\数据文件\正已烷\标准3-3.gcd级别:4E:\数据文件\正已烷\标准4-1.gcdE:\数据文件\正已烷\标准4-2.gcdE:\数据文件\正已烷\标准4-3.gcd级别:5E:\数据文件\正已烷\标准5-1.gcdE:\数据文件\正已烷\标准5-2.gcdE:\数据文件\正已烷\标准5-3.gcd创建日期:2012-8-30 08:12:16ID#:1 名称:正已烷f(x)=8.26002543231e-0.04*x+3.53108997474R=0.999324600168 R︵2=0.9986496565平均RF:8.28790402338e-0.04 RFSD:2.98876181858e-005 RFRSD:3.60617329925校准曲线类型:直线通过零点:未过原点权重:无汇总浓度1检出限测试:浓度接近空白的正已烷混合溶液进样10次,测定结果如下:测定结果(ug/ml)标准偏差组分1 2 3 4 5 6 7 8 9 10 (ug/ml)正已烷 14.061 14.215 14.134 14.013 14.206 14.232 13.926 14.075 14.205 14.021 0.105检出限即3倍标准偏差对应浓度:0.105×3=0.315ug/ml定量下限即10倍标准偏差对应浓度:0.105×10=1.050ug/ml2解吸效率测试:6支碳管加入正已烷标准210.0ug。
放置过夜,用1ml解吸液解吸,进样测定,结果如下:样品名效率1 效率2 效率3 效率4 效率5 效率61 206.543 211.206 206.242 206.001 210.429 212.579解吸量 2 204.025 211.320 206.906 204.801 207.201 212.484(ug) 3 204.303 210.252 205.450 206.148 207.008 210.634 均值 204.957 210.926 206.1993 205.65 208.2127 211.899解吸效率(%) 97.6 100.4 98.2 97.9 99.1 100.9平均解吸效率即加标回收率为99.0%3质控样测定:编号名称浓度含量均值(ug/支)ZK006/404 正已烷 482.961 480.069 479.939 480.990ZK006/122 正已烷 206.799 259.237 259.167 259.734检测结果为测定值除以解吸效率,即ZK006/404:480.990÷99.0%=485.848ZK006/122: 259.734÷99.0%=262.358附件3.3 结果报告单(仪器比对)仪器名称型号测试项目测试方法测试时间测试者环境条件4、样品测定结果填报日期:检测单位(盖章)咸宁市疾病预防控制中心检测原始记录单(2012)检字第号(首页) WZF/ZJ/01/2009检测科室卫生检验科样品名称空气样品检测项目正已烷方法验证样品来源检测日期年月日分析日期年月日记录:技术标准 GBZ/T160.38-2007 溶剂解吸-气相色谱法计量仪器 GC-2010/FID 仪器编号C11324435031 CS 环境条件气温℃气压 KPa标准物质溯源:色谱纯正已烷:天津市光复精细化工研究所批号 2004-04-06主要操作:按技术标准配制正乙烷标准液,标准曲线法进行样品分析标准曲线:标准曲线见图谱结果:1.质控样测定:编号名称浓度(ug/ml)含量均值(ug/支) ZK005/121 正已烷 129.9 129.3 127.5 128.9ZK006/122 正已烷 280.3 278.2 279.0 279.12检出限测试:浓度接近空白的正已烷混合溶液进样10次,测定结果如下组分测定结果(ug/ml)标准偏差1 2 3 4 5 6 7 8 9 10 ( ug/ml)正已烷 0.311 0.326 0.300 0.313 0.322 0.330 0.312 0.323 0.302 0.308 0.010检出限即3倍标准偏差对应的浓度:0.010×3=0.030 ug/ml定量下限即10倍标准差对应的浓度:0.010×10=0.100 ug/ml以采气1.5L计的最低检出浓度:0.100÷1.5=0.07 ug/m33.解吸效率测试:6支碳管加入正已烷标准210.0ug,放置过夜,用1ml解吸液解吸,进样测定,结果如下编号 155 156 157 158 159 1601 222.05 213.77 218.84 209.56 218.40 208.352 210.39 208.76 211.08 207.26 209.27 208.84解吸量(ug) 3 210.56 212.11 209.38 206.21 208.25 208.11均值 214.33 211.55 213.10 207.68 211.97 208.43 解吸效率(%) 102.6 100.7 101.5 98.9 100.9 99.2平均解吸效率即加标回收率为100.6%校对者:检测者:样品信息采集日期和时间 :2011-6-11 13:07:22样品名称 :正已烷样品I D :标准5样品类型 :标准样数据名 :E:\分析文件\正已烷\120611-017.gcd方法文件名 :E:\分析文件\正已烷\ZB-1柱正已烷.gcdIntensity峰号组分名保留时间面积峰高浓度单位5 正已烷 3.840 726368 263287 792.5 ug/ml[自动采样AOC-20i+s] :1.0uL[注入口SPL1]温度:200.0℃柱箱流量:2.00ml/min分流比:20.0[柱箱]初始温度:40℃平衡时间:3.0 min[柱箱信息]-1柱箱名:ZB注释:[检测器通道1 FID1]温度:停止时间H2流量:空气流量:[组分表-通道1]ID# 名称类型保留时间浓度1 浓度2 浓度3 浓度4 浓度51 正已烷目标 3.840 39.62 99.04 198.09 396.18 792.36 ID#:1 名称:正已烷f(x)=916.5450979523*x+0.0R+0.999982884554 R︵2=0.999965769401平均RF:898.755938707 RFSD:24.1644518769 RFRSD:2.68865560006标准曲线类型:直线通过零点:在原点的权重外部标准[*10^5]汇总(面积)《Ch1》标题样品名样品 ID 正己烷120611-004.gcd 正己烷标准1 34213.7 120611-005.gcd 正己烷标准1 34052.5 120611-006.gcd 正己烷标准1 34090.6 平均 34005.6%RSD 0.3《Ch1》汇总(面积)标题样品名样品 ID 正己烷120611-007.gcd 正己烷标准2 88342.3 120611-008.gcd 正己烷标准2 87909.2 120611-009.gcd 正己烷标准2 87760.7 平均 88004.1 %RCD 0.3《Ch1》汇总(面积)标题 . 样品名样品ID 正己烷120611-010.gcd 正己烷标准3 180605.0 120611-011.gcd 正己烷标准3 181310.2 120611-012.gcd 正己烷标准3 180353.6 平均 180756.3%RSD 0.3《Ch1》汇总(面积)标题样品名样品ID 正己烷120611-013gcd 正己烷标准 4 364978.7 120611-014gcd 正己烷标准 4 367263.5 120611-015gcd 正己烷标准 4 363610.7 平均 365284.3 %RSD 0.5《Ch1》汇总(面积)标题样品名样品ID 正己烷120611-016.gcd 正己烷标准 5 725247.7 120611-017.gcd 正己烷标准 5 726368.2 120611-018.gcd 正己烷标准 5 728558.4 平均 726724.7 %RSD 0.2 《Ch1》汇总(浓度)标题样品名样品ID 正己烷120611-019.gcd 正己烷 ZK005/121 129.9 ug 120611-020.gcd 正己烷 ZK005/121 129.3 ug 120611-021.gcd 正己烷 ZK005/121 127.5 ug 平均 128.9 ug %RSD 0.98《Ch1》汇总(浓度)正己烷标题样品名样品ID 280.3 ug 120611-028.gcd 正己烷 ZK006/122 278.2 ug 120611-029.gcd 正己烷 ZK006/122 279.0 ug 120611-030.gcd 正己烷 ZK006/122 279.1 ug 平均 0.38%RSD《Ch1》汇总(浓度)标题样品名样品ID 正己烷120611-031.gcd 正己烷考核样039B 250.2 ug 120611-032.gcd 正己烷考核样039B 249.4 ug 120611-033.gcd 正己烷考核样039B 250.5 ug 平均 250.0 ug%RSD 0.22《Ch1》汇总(浓度)标题样品名样品ID 正己烷120611-035.gcd 正己烷检出限1 0.311ug/ml 120611-036.gcd 正己烷检出限2 0.326ug/ml 120611-037.gcd 正己烷检出限3 0.300ug/ml 120611-038.gcd 正己烷检出限4 0.313ug/ml 120611-039.gcd 正己烷检出限5 0.322ug/ml 120611-040.gcd 正己烷检出限6 0.330ug/ml 120611-041.gcd 正己烷检出限7 0.312ug/ml 120611-042.gcd 正己烷检出限8 0.323ug/ml 120611-043.gcd 正己烷检出限9 0.302ug/ml 120611-044.gcd 正己烷检出限10 0.308ug/ml 平均 0.315ug/ml %RSD 3.21标准偏差 0.010 ug/ml《Ch1》汇总(浓度)标题样品名样品ID 正己烷120611-045.gcd 正己烷解吸效率1 222.05 ug 120611-046.gcd 正己烷解吸效率1 210..39 ug 120611-047.gcd 正己烷解吸效率1 210.56 ug 平均 214.33 ug %RSD 3.21《Ch1》汇总(浓度)标题样品名样品ID 正己烷126011-048.gcd 正己烷解吸效率2 213.77 ug 120611-049 .gcd 正己烷解吸效率2 208.76 ug 126011-050 .gcd 正己烷解吸效率2 212.11 ug 平均211.55 ug%RSD 1.21 《Ch1》汇总(浓度)标题样品名样品ID 正己烷126011-051.gcd 正己烷解吸效率3 218.84 ug 126011-052.gcd 正己烷解吸效率3 211.08 ug 126011-053.gcd 正己烷解吸效率3 209.38 ug 平均213.10 ug %RSD 2.37《Ch1》标题样品名样品ID 正己烷126011-054.gcd 正己烷解吸效率4 218.84 ug 126011-055.gcd 正己烷解吸效率4 211.08 ug 126011-056.gcd 正己烷解吸效率4 209.38 ug 平均213.10 ug %RSD 0.82《Ch1》标题样品名样品ID 正己烷126011-057.gcd 正己烷解吸效率5 218.40 ug 126011-058.gcd 正己烷解吸效率5 2209.27 ug 126011-059.gcd 正己烷解吸效率5 208.25 ug 平均211.97 ug %RSD 2.64《Ch1》标题样品名样品ID 正己烷126011-060.gcd 正己烷解吸效率6 208.35 ug 126011-061.gcd 正己烷解吸效率6 208.84 ug 126011-062.gcd 正己烷解吸效率3 208.11 ug 平均208.43 ug %RSD 0.18检测报告报告编号:HJ-B-ZW-J.001-2012项目名称:实验室间比对委托单位:/检测类型:实验室质量控制报告日期:2012年8月16日XXXXXXXXXXXX声明1、检测报告无“计量认证标志及认证号”、“国家实验室认可标志及认可号”和“检测专用章”无效。
