第34届中国化学奥林匹克竞赛初赛试题与答案化学
化学奥赛初赛试题(第34届)

第34届中国化学奥林匹克(初赛)试题第1题(8分)1-1 画出小分子C3F4的Lewis结构,标出三个碳原子成键时所采用的杂化轨道。
1-2现有铝镁合金样品一份,称取2.56 g样品溶于HCl,产生2.80 L H2 (101.325 kPa, 0℃),通过计算,确定此合金组成。
1-3构筑可循环再生的聚合物材料是解决目前白色污染的有效途径之一。
1-3-1通常单官能度的单体无法参与聚合反应中的链增长,但单体A可以与B发生反应形成聚合物。
画出该聚合物的结构式。
1-3-2单体A、C、D按物质的量比例6 : 3 : 2进行聚合,得到的聚合物不能进行热加工和循环利用;但若在共聚合时加入一定量(~10%)的B,得到的聚合物又具备了可热加工和循环利用的性能。
简述原因。
第2题(10分)书写反应方程式(提示:要求系数为最简整数比;2-1和2-2中自然条件复杂,合理选择即可)。
2-1关于地球的演化,目前的主要观点是,原始地球上没有氧气,在无氧或氧气含量很低时,原核生物可利用自然存在的有机质(用CH2O表示)和某些无机物反应获得能量。
例如,SO42-和MnO2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。
2-1-1 写出SO42-参与的释能反应的离子方程式。
2-1-2 写出MnO2参与的释能反应的离子方程式。
2-2 约27亿年前光合作用开始发生,随着这一过程的进行,地球上氧气不断积累,经过漫长的演变终达到如今的含量。
氧气的形成和积累,导致地球上自然物质的分布发生变化。
2-2-1 溶解在海洋中的Fe2+被氧化转变成针铁矿α-FeO(OH)而沉积,写出离子方程式。
2-2-2与铁的沉积不同,陆地上的MoS2被氧化而导致钼溶于海洋且析出单质硫,写出离子方程式。
2-32020年8月4日晚,贝鲁特港口发生了举世震惊的大爆炸,现场升起红棕色蘑菇云,破坏力巨大。
目前认定大爆炸为该港口存储的约2750吨硝酸铵的分解。
第34届中国化学奥林匹克 (初赛 )试题及解答

第34届中国化学奥林匹克 (初赛 )试题及解答1. 下列物质中,属于离子性物质的是()A. H2O2B. H2OC. HClD. H2S解析:离子性物质指的是能够电离产生带电离子的物质,而只有酸溶液中的氢离子和氯离子都是带电的,因此选择C选项。
2. 某实验室使用三种药剂进行实验,其酸碱性分别为:pH=1,pH=7,pH=14。
这三种药剂分别是()A. 硫酸、水、烧碱B. 盐酸、纯净水、氢氧化钠C. 氯化铵、自来水、氢氧化钾D. 醋酸、甘油、石灰水解析:根据pH值的定义,酸性溶液的pH小于7,中性溶液的pH等于7,碱性溶液的pH大于7。
因此选项B中的盐酸对应pH=1的酸性溶液,纯净水对应pH=7的中性溶液,氢氧化钠对应pH=14的碱性溶液。
1. 水的主要离子是__________。
答案:H+和OH-解析:水在不反应时,只有自离子化产生的少量H+和OH-存在。
2. 通常称为“水杨酸”的有机酸是__________。
答案:水合肼基苯酚酸(C7H6O3)解析:水杨酸的化学名称为水合肼基苯酚酸,其分子式为C7H6O3。
1. 简述氨气(NH3)的制备方法及性质特点。
氨气的制备方法有多种,常见的包括:(1)氨水与酸反应:将氨水与酸反应,生成氨气和相应的盐。
(2)铵盐与碱反应:将铵盐与碱反应,生成氨气和相应的盐。
(3)气化法:将氨气的固体化合物如氨水合物加热至高温,使其分解生成氨气。
氨气的性质特点如下:(1)氨气具有辛辣气味,剧毒,有刺激性。
(2)氨气可溶于水,与水反应生成氨水。
(3)氨气是一种碱性气体,可与酸反应生成盐。
(4)氨气燃烧时会生成氮气和水蒸气,释放出大量的热。
1. 已知苯酚的结构式为C6H6O,苯酚与磺酸反应生成苯磺酸的反应方程式为:C6H6O + H2SO4 → C6H5SO3H + H2O根据上述反应方程,请回答以下问题:(1)在该反应中,苯酚的提供的是哪一个化学基团?答案:氢氧基(OH-)(2)苯磺酸中磺酸基的电子对属于原子轨道上的哪一类?答案:杂化sp3轨道解析:磺酸基的电子对来自磺酸根离子中的硫原子,硫原子的杂化轨道是sp3杂化,因此磺酸基的电子对属于杂化sp3轨道。
2020第34届全国化学奥赛(初赛)试题、答案与解析

2020第34届全国化学奥赛(初赛)试题、答案与解析胡征善【评价】1-1、1-2属易题属加聚反应:爆炸性分解考查质量守恒定律均生成稳定的水【评价】易题【解析】设碱式碳酸盐(化学式为M x(OH)y(CO3)z)为a mol。
在H2中充分处理得2.356 gM,0.994 g(0.0551 mol)H2O;在CO中充分处理得2.356 gM,1.245 L(0.0555 mol)CO2。
先可认为a mol M x(OH)y(CO3)z分解得ya/2 molH2O和za molCO2、a molM x O(y/2+z),再与a(y/2+z) molH2反应或a(y/2+z) molCO反应。
则有:a[y/2+(y/2+z)]=0.0551和a[z+(y/2+z)]=0.0555,解得y=2z。
在M x O(y/2+z)中的化合价(反应得失电子)守恒有:y+2z=2x,则2z=x,故:x∶y∶z=2∶2∶1 化学式M2(OH)2CO33a=0.0551或0.0555,根据M质量守恒:2aAr(M)=2.356 g,则Ar(M)=64.2【评价】易题也可以写作【解析】5-1.将题给数据代入A=ɛlc求c。
由c求以上银的K sp。
5-2-1.根据(HL+)(PF6—)即L·(HPF6)确定A中Ag为+1价,L为0价,y=9。
N(N)∶N(P)=6.24/14∶6.90/31=2∶1 因为N(P)=9,则N(N)=18,N(C)∶N(P)=27.40/12∶6.90/31=10.26∶1,N(C)=10.26y=92。
N原子守恒:每个L中有1个N,所以8+x+n=18,所以x+n=10又n∶N(P)=2.0/41∶6.90/31=0.22∶1,n=0.22y=2,x=8 即A 为[Ag9L8(CH3CN)8](PF6)9·nCH3CN【解析】5-1套用公式;5-2主要涉及化学式的计算。
试题较易。
2020年第34届中国化学奥林匹克(初赛)选拔赛暨2020年江苏省高中学生化学奥林匹克复赛试题

第34届中国化学奥林匹克(初赛)选拔赛2020年江苏省高中学生化学奥林匹克复赛试题第1题不定项选择题(每题有1-2个正确选项,每题3分,共30分)1-1垃圾分类是生态文明的进步,也是每个人都能参与的环境保护方式。
下列关于垃圾处理的说法不正确的是A.被污染的餐巾纸属于可回收垃圾B.废蓄电池属于有害垃圾C.厨余垃圾经发酵可制成肥料D.废医用塑料可回收制造餐具1-2用化学用语表示SiO 2+4HF=SiF 4↑+2H 2O 中的有关微粒,其中正确的是A.F -的结构示意图B.水分子的比例模型C.SiF 4的电子式D.中子数为15的Si 原子Si29141-3用下列实验装置进行有关实验,能达到实验目的的是A.用甲装置制取少量SO 2B.用乙装置蒸发AlCl 3溶液制取AlCl 3晶体C.用装置丙分离饱和碳酸钠和乙酸乙酯的混合液D.用装置丁除去Cl 2中混有的少量HCl 气体1-4下列有关物质的性质和用途具有对应关系的是A.活性炭具有还原性,可用作制糖业的脱色剂B.晶体硅的熔点高、硬度大,可用作制造半导体材料C.二氧化氯具有强氧化性,可用作饮用水消毒D.氯化铁溶液具有酸性,可用作刻蚀铜电路板1-5短周期主族元素W、R、X、Y、Z 的原子序数依次增大,Y 原子半径在短周期元素中最大,W 和Y 同主族,X 与Z 同主族,R 原子最外层电子数比内层电子数多3,W、Y 原子的电子数总和与X、Z 原子的电子数总和之比为1:2。
下列说法正确的是A.原子半径r(X)>r(R)>r(W)B.X 与Y 只能形成一种化合物C.X 的简单气态氢化物的热稳定性比Z 的弱D.由W、R、X 三种元素组成的化合物可以是酸、碱或者盐1-6下列实验中实验操作和现象、以及得出的结论均正确的是1-7一种2-甲基色酮内酯(Y)可通过下列反应合成。
下列说法正确的是A.1molX 与浓溴水反应最多能与3molBr 2加成B.X、Y 分子中所有碳原子均处于同一平面C.一定条件下,X 可以发生加成、缩聚、消去、氧化反应D.Y 与H 2完全加成,每个产物分子中含有6个手性碳原子1-8南京大学教授提出了一种高效的固碳新技术(如图)。
2020年第34届全国中学生化学竞赛初赛试题及答案
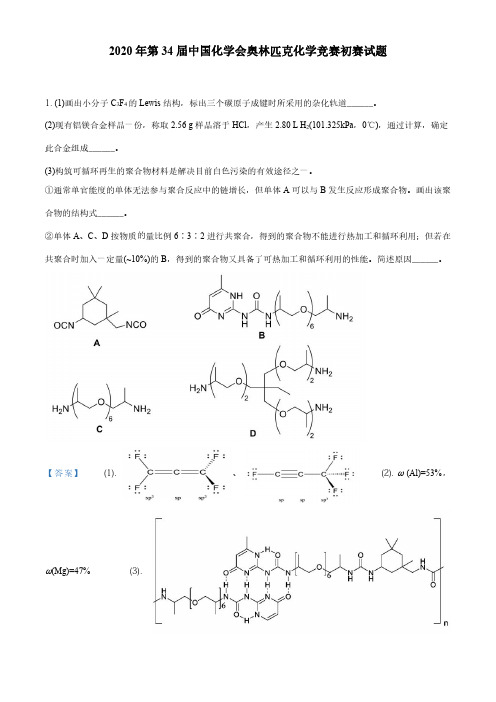
2020年第34届中国化学会奥林匹克化学竞赛初赛试题1.(1)画出小分子C3F4的Lewis结构,标出三个碳原子成键时所采用的杂化轨道______。
(2)现有铝镁合金样品一份,称取2.56g样品溶于HCl,产生2.80L H2(101.325kPa,0℃),通过计算,确定此合金组成______。
(3)构筑可循环再生的聚合物材料是解决目前白色污染的有效途径之一。
①通常单官能度的单体无法参与聚合反应中的链增长,但单体A可以与B发生反应形成聚合物。
画出该聚合物的结构式______。
②单体A、C、D按物质的量比例6∶3∶2进行共聚合,得到的聚合物不能进行热加工和循环利用;但若在共聚合时加入一定量(~10%)的B,得到的聚合物又具备了可热加工和循环利用的性能。
简述原因______。
【答案】(1).、(2).ω(Al)=53%,ω(Mg)=47%(3).(4).ACD 以题目比例聚合时,亲电基团与亲核基团比例为12:12,反应完全为稳定的结构,同时分子链之间有较强的氢键;加入少量的B 后,亲核基团氨基数目过剩,加热后可以发生酰胺交换反应,释放出D 中氨基,破坏原先的体状结构变为链状结构,B 的加入也使得链状分子内部的氢键数目增加,减少链间氢键作用,因此有热加工性能,高温下氢键断裂解除交联,以达到回收利用目的2.书写反应方程式(提示:要求系数为最简整数比;(1)和(2)中自然条件复杂,合理选择即可)。
(1)关于地球的演化,目前主要的观点是,原始地球上没有氧气,在无氧或氧气含量很低时,原核生物可利用自然存在的有机质(用CH 2O 表示)和某些无机物反应获得能量。
例如,24SO -和MnO 2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。
①写出24SO -参与的释能反应的离子方程式______。
②写出MnO 2参与的释能反应的离子方程式______。
(2)约27亿年前光合作用开始发生,随着这一过程的进行,地球上氧气不断积累,经过漫长的演变终达到如今的含量。
2024化学竞赛初赛试题

2024化学竞赛初赛试题一、教材1. 人教版化学教材- 知识点:物质的量相关概念是化学计算的基础,如摩尔质量、气体摩尔体积等。
例如在计算化学反应中物质的量的比例关系时会用到。
- 解析:物质的量(n)、质量(m)和摩尔质量(M)的关系为。
在化学方程式中,各物质的化学计量数之比等于它们的物质的量之比。
- 知识点:元素周期律,包括原子结构、元素周期表的结构、元素性质的周期性变化规律等。
这在化学竞赛中对理解元素及其化合物的性质有很大帮助。
- 解析:原子半径在同一周期从左到右逐渐减小(稀有气体除外),在同一主族从上到下逐渐增大。
这是由于原子核对核外电子的吸引作用在周期和主族中的变化规律导致的。
- 知识点:原子结构的精细内容,如电子云、原子轨道等;分子结构中的共价键理论、分子的空间构型等。
- 解析:例如杂化轨道理论,杂化的分子空间构型为直线型(如),杂化的分子空间构型为平面三角形(如),杂化的分子空间构型为正四面体(如)等。
这是根据中心原子的价层电子对数来确定杂化类型,从而得出分子的空间构型。
- 知识点:化学反应速率、化学平衡、电解质溶液、电化学等。
- 解析:对于化学平衡,勒夏特列原理指出,如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动。
例如在的反应中,升高温度,平衡逆向移动,因为反应是放热反应,升高温度时平衡向吸热方向移动以减弱温度升高的影响。
- 知识点:有机物的命名、结构、性质、反应类型等。
- 解析:有机物的命名遵循一定的规则,如烷烃的命名是选择最长的碳链为主链,从离支链最近的一端开始编号等。
对于有机反应类型,如加成反应是不饱和键(双键或三键)两端的原子与其他原子或原子团直接结合生成新的化合物的反应,例如乙烯与溴水的加成反应。
二、化学竞赛辅导书- 知识点:涵盖化学基本原理,包括化学平衡、酸碱理论、氧化还原反应等内容的深入讲解。
- 解析:在酸碱理论部分,除了介绍常见的酸碱电离理论,还深入讲解了酸碱质子理论和酸碱电子理论。
34届全国高中化学竞赛决赛试题

34届全国高中化学竞赛决赛试题
一、选择题
下列哪个反应是放热反应?
A. 碳酸钙分解
B. 氢氧化钡与氯化铵混合
C. 铝热反应
D. 氯化铵溶解于水
下列物质中,属于电解质的是:
A. 乙醇
B. 二氧化碳
C. 硫酸铜溶液
D. 熔融的氢氧化钠
下列关于元素周期表的说法中,正确的是:
A. 元素的非金属性随着原子序数的递增而减弱
B. 第IA族元素的金属性比第IIA族元素的金属性强
C. 所有主族元素都有正化合价
D. 稀有气体元素原子的最外层电子数均为8
二、填空题
写出下列反应的化学方程式:
氯气与氢氧化钠溶液的反应:_____________________
铝与盐酸的反应:_____________________
某元素的最高价氧化物对应水化物的化学式为H₂XO₄,则它的气态氢化物的化学式为:___________。
三、计算题
将10g铁粉加入100mL 2mol/L的盐酸中,充分反应后,生成氢气的体积(标准状况下)是多少?
一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。
求原HCl溶液的物质的量浓度。
求所得溶液中Cl⁻的物质的量。
四、简答题
描述如何通过实验验证氯气的氧化性比溴的氧化性强。
解释为什么铁在潮湿的空气中容易生锈。
中国化学奥林匹克竞赛初赛试题

选择题:
下列哪个是金属元素?
A. 氧
B. 铁(正确答案)
C. 氢
D. 氮
水的化学式是?
A. CO₂
B. H₂O(正确答案)
C. NaCl
D. O₂
下列哪个不是有机化合物?
A. 甲烷
B. 乙醇
C. 氯化钠(正确答案)
D. 葡萄糖
下列哪个反应是吸热反应?
A. 燃烧反应
B. 中和反应
C. 氯化铵与氢氧化钡反应(正确答案)
D. 金属与酸反应
下列哪个是强酸?
A. 醋酸
B. 碳酸
C. 盐酸(正确答案)
D. 氢硫酸
下列哪个不是氧化还原反应?
A. 锌与稀硫酸反应
B. 氢气在氧气中燃烧
C. 碳酸钙高温分解(正确答案)
D. 氧化铜与一氧化碳反应
下列哪个物质属于碱?
A. 硫酸
B. 氢氧化钠(正确答案)
C. 食盐
D. 二氧化碳
下列哪个是共价化合物?
A. 氯化钾
B. 氯化氢(正确答案)
C. 氯化镁
D. 氯化钙
下列哪个现象是物理变化?
A. 燃烧
B. 钢铁生锈
C. 酒精挥发(正确答案)
D. 食物腐败。
化学奥林匹克竞赛试题及答案(第34届)

第34届中国化学奥林匹克(初赛)试题、标准答案及评分细则
第1题(8分)
1-1画出小分子C3F4的Lewis结构,标出三个碳原子成键时所采用的杂化轨道。
1-2现有铝镁合金样品一份,称取2.56g样品溶于HCl,产生2.80 L H2 (101.325 kPa,0 ˚C),通过计算,确定此合金组成。
1-3 构筑可循环再生的聚合物材料是解决目前白色污染的有效途径之一。
1-3-1通常单官能度的单体无法参与聚合反应中的链增长,但单体A可以与B发生反应形成聚合物。
画出该聚合物的结构式。
1-3-2单体A、C、D按物质的量比例6:3:2进行共聚合,得到的聚合物不能进行热加工和循环利用;但若在共聚合时加入一定量(~10%)的B,得到的聚合物又具备了可热加工和循环利用的性能。
简述原因。
1。
第34届中国化学奥林匹克(初赛)新疆赛区竞赛试题

3-3 推断 E 的化学式。
3-4 推出化合物 F 和 G 的化学式。
第 4 题(10 分)
镍苯醌二肟配合物 A 具有如下分子式:[Ni(bqoxH)2] (bqoxH2 =邻苯醌二肟,结构式为:
)。配合物 A 与 I2 共结晶依据 I2 的加入量不同形成 B、C、D 多个产物。配合
在合成西多福韦中有一个关键中间体二醇 X 可以通过 L-甘露醇制备,制备路线如下:
丙酮
9-1 写出 A、B、C 的结构。
9-2 X 可以进一步合成新化合物:
5
写出D、E、F、G的结构式。
9-3 合成西多福韦的最后路线如下:
写出H的结构式。
第 10 题(8 分)
10-1 写出下列转化反应中 A 和 B 的结构式。
微波
苯
10-2 写出下列反应的机理。
6
2-3-2 无水AlCl3在三氯氧磷中形成一种1:1离子型化合物A,阳离子中心原子六配位、阴离子
中心原子四配位。写出A的化学式并画出阴阳离子的结构。
2-3-3 写出 AlCl3 溶于 POCl3 形成阴阳离子比为 3:1 化合物的化学式。
2-4 化合物 A 由三种短周期元素(X、Y、Z)组成,X、Y 同一族、X 的原子量是 Y 的一倍。
2-5-1 合成原料所用单体有4种、写出这些单体结构示意图。
2-5-2 光刻胶的性能与主体树脂的侧链设计十分关键,侧链设计包括:极性部分( 提供可粘
附性、可显影性)和酸敏部分( 提供抗蚀性、成像能力);所谓酸敏部分是指使主体树脂曝光
前后的溶解速率发生变化、提供成像能力。试指出上述光刻胶树脂侧链极性部分和酸敏部分。
第34届中国化学奥林匹克模拟化学试题-题目与答题卷

第34届中国化学奥林匹克(初赛)模拟考试卷-1•竞赛时间3 小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷与答卷背面朝上放在桌面上,待监考人员允许方可离开考场。
•姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他位置者按废卷处理。
•所有解答必须写在卷面指定位置,写于其他位置无效。
•凡要求计算或推演的,须给出过程,无过程即使结果正确也不得分。
•用铅笔解答的部分(包括作图)无效。
•禁用涂改液和修正带,也不得用纸粘贴。
否则,整个答卷无效。
•附草稿纸一张,不得将任何纸张带入考场。
•允许使用非编程计算器以及直尺等文具。
•写有任何与试题内容无关的文字的答卷无效。
气体常数R = 8.314 J·mol·K;阿伏伽德罗常数N A = 6.022×10 mol;法拉第常数F = 9.65×104 C·mol-1;标准大气压:100 kPa;h=6.625⨯10-34 J⋅s; 1 eV=1.602⨯10-19 J。
第1题(10分)A、B、C、D是含氮中性钠盐,E、F、G、H是中性含磷钠盐。
D和H分别是I和J酸的盐;这些酸是白色固体,加热容易分解;I加热直接分解为K和水;J的热分解经过二个阶段:先1-1A与CO2能激烈作用转化为B,写出化学反应方程式(方程1);写出B 受热生成C的化学反应方程式(方程2);1-2 画出D、E、F、G、H物质阴离子的结构。
1-3 写出I和J热裂解的反应方程式。
1-4 画出K的Lewis结构图;写出与I形成相同热分解产物的其它化合物(2个)并写出它们的热分解反应方程式。
第2题(22分)2-1(13分)本题中的制备实验都在惰性气氛下进行,HCl 和(NH4)2C2O4溶液预先除氧。
仔细磨细的0.235 g 黑色粉末A溶于稍微加热的2.96 mL 10% HCl中(密度为1.048 g/ml),形成B盐的浅绿色溶液;盐B浅绿色溶液与3.676 g Co(NO3)2∙6H2O(预先溶在15 mL H2O中)混合,加入稍稍过量的(NH4)2C2O4溶液,生成3.068 g黄橙色沉淀C。
2020年第34届中国化学奥林匹克(初赛)选拔赛暨2020年江苏省高中学生化学奥林匹克复赛试题

1-8 南京大学教授提出了一种高效的固碳新技术(如图)。利用锂-二氧化碳电池, 在放电过程中二氧化碳转化为碳和碳酸锂,在电池 充电过程中通过选用合适的催化剂使碳酸锂单独被 氧化分解,而另一种放电产物碳留在电池内,下列 说法不正确的是 A.该电池放电时,CO2 从放电进气口进入 B.该电池放电时的正极反应是 3CO2+4Li++4e-=2Li2CO3+C C. 该电池充电时 Li2CO3 转化为 Li+ D.该电池放电时,每转移 2mol 电子,可固定 1molCO2
0.32mol 气体X 和 0.32mol 气体Y, 到达平衡时,n(Z)<0.24mol
第 2 题(8 分) 写出下列反应的方程式 1 硫代硫酸钠与稀盐酸混合,生成有刺激性气味的气体 2 氯酸钾、硫酸锰与氢氧化钾共熔,生成绿色物质 3 在重铬酸钾溶液中加入少量银离子,生成砖红色沉淀 4 金溶解在王水中
C.厨余垃圾经发酵可制成肥料
D.废医用塑料可回收制造餐具
1-2 用化学用语表示 SiO2+4HF=SiF4↑+2H2O 中的有关微粒,其中正确的是
A.F-的结构示意图
B. 水分子的比例模型
C.SiF4 的电子式
D.中子数为15 的 Si 原子 1249Si 1-3 用下列实验装置进行有关实验,能达到实验目的的是
t/min
2
4
7
9
n(Y)/mol
0.12
0.11
0.10
0.10
下列说法正确的是
A. 反 应 前 2min 的 平 均 速 率 v(Z)=2╳10-3mol/(Lmin) B. 其 他 条 件 不 变 , 降 低 温 度 , 反 应 达 到 新 平 衡 时 ,v( 逆 )>v( 正 ) C.其他条件不变 ,向平衡体系中再充入 0.16mol 气体 X,与原平衡相比,达到 新平衡时,气体 Y 的转化率增大,X 的体积分数增大 D.保持其他条件不变,起始时向容器中充入
第34届中国化学奥林匹克(初赛)选拔赛暨2020年江苏省高中学生化学奥林匹克复赛试题

!!!""#$%&'()*!+,"-.,/#$#$01234#&5%&'()*6,78exOyqz=¦§!9#: !&
!"#$%&'()*!+,"-.,/ 01234#&5%&'()*6,78
9:;<=>?@A
()&%&k[lqAI{|JÙ=# !&!!$=#>?89@&$A8$BA8!=#BA8@&*#CDE-F$G@HCDE-F$-IJCK$ =$L-JCK&+%=#" & &!,/!& #!/!& !!./!& "!.!& %!/!& >!-!& A!/!& '!/!& (!,-!& &$!. "&!'=" # &!78#0#2!3#4.6"""#78.6302##30+34#2!!#=" # #!!\J02"3#H.62!3&#H24 """!H#\J2"3#H.63!H#02"3>4#2!!#=" # !!.D#2#A* 3",I3 34#2"""#,I#.D2"+3#43 !!#=" # "!,]3472!3"4.6"""4,].6"372#3#4#2!!#=" #&!'=" ! &!#723!4#2# """#43 3#72!* 3#4#2!!#=" ! #!#+"$$K&$*"BC6!!#="!¾4!!#=" ! !!!>'BI(B*!!!#=" $&!&$=" " &!!>="Èp;É ,I#.2!!P"""",I#2!P"3.2#!I"
第34届中国化学奥林匹克(初赛)试题和参考答案
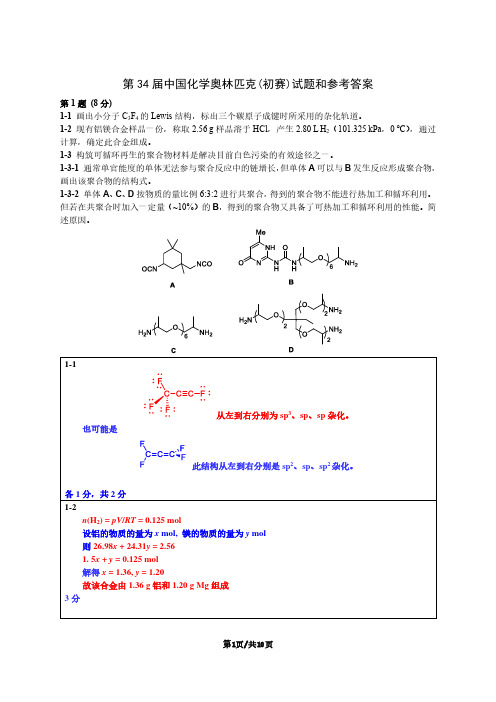
第34届中国化学奥林匹克(初赛)试题和参考答案第1题(8分)1-1画出小分子C3F4的Lewis结构,标出三个碳原子成键时所采用的杂化轨道。
1-2 现有铝镁合金样品一份,称取2.56 g样品溶于HCl,产生2.80 L H2(101.325 kPa,0 ℃),通过计算,确定此合金组成。
1-3构筑可循环再生的聚合物材料是解决目前白色污染的有效途径之一。
1-3-1通常单官能度的单体无法参与聚合反应中的链增长,但单体A可以与B发生反应形成聚合物,画出该聚合物的结构式。
1-3-2单体A、C、D按物质的量比例6:3:2进行共聚合,得到的聚合物不能进行热加工和循环利用。
但若在共聚合时加入一定量(~10%)的B,得到的聚合物又具备了可热加工和循环利用的性能。
简述原因。
第2题(10分) 书写反应方程式(提示:要求系数为最简整数比;2-1和2-2中自然条件复杂,合理选择即可)2-1关于地球的演化,目前主要的观点是,原始地球上没有氧气,在无氧或氧气含量很低时,原核生物可利用自然存在的有机质(用CH2O表示)和某些无机物反应获得能量,例如,SO42-和MnO2可分别作为上述过程的氧化剂,前者生成黄色浑浊物,二者均放出无色无味气体。
2-1-1写出SO42-参与的释能反应的离子方程式2-1-2写出MnO2参与的释能反应的离子方程式2-2约27亿年前光合作用开始发生,随着这一过程的进行,地球上氧气不断积累,经过漫长的演变重达到如今的含量。
氧气的形成和积累,导致地球上自然物质的分布发生变化。
2-2-1溶解在海洋中的Fe2+被氧化转变成针铁矿α-FeO(OH)而沉积,写出离子方程式。
2-2-2与铁的沉积不同,陆地上的MoS2被氧化而导致Mo溶于海洋并且析出单质硫,写出离子方程式。
2-3 2020年8月4日晚,贝鲁特港口发生了举世震惊的大爆炸,现场升起红棕色蘑菇云,破坏力巨大。
目前认定大爆炸为该港口存储的约2750吨硝酸铵的分解。
第34届中国化学奥林匹克(初赛)选拔赛暨2020年江苏省高中学生化学奥林匹克复赛试题

第 34 届中国化学奥林匹克(初赛)选拔赛 2020 年江苏省高中学生化学奥林匹克复赛试题第 1 题 不定项选择题(每题有 1-2个正确选项,每题 3 分,共 30 分) 1-1 垃圾分类是生态文明的进步,也是每个人都能参与的环境保护方式。
下列关 于垃圾处理的说法不正确的是 A.被污染的餐巾纸属于可回收垃圾 B.废蓄电池属于有害垃圾 C.厨余垃圾经发酵可制成肥料 D.废医用塑料可回收制造餐具1-2 用化学用语表示242SiO 4HF SiF 2H O +=↑+中的有关微粒,其中正确的是A.F-的结构示意图B.水分子的比例模型C.SiF4的电子式D.中子数为15的Si 原子2914Si1-3 用下列实验装置进行有关实验,能达到实验目的的是A.用甲装置制取少量 SO 2B.用乙装置蒸发 AlCl 3溶液制取 AlCl 3晶体C.用装置丙分离饱和碳酸钠和乙酸乙酯的混合液D.用装置丁除去 Cl 2中混有的少量 HCl 气体 1-4 下列有关物质的性质和用途具有对应关系的是A.活性炭具有还原性,可用作制糖业的脱色剂B.晶体硅的熔点高、硬度大,可用作制造半导体材料C.二氧化氯具有强氧化性,可用作饮用水消毒D.氯化铁溶液具有酸性,可用作刻蚀铜电路板1-5 短周期主族元素W、R、X、Y、Z 的原子序数依次增大,Y 原子半径在短周期元素中最大,W 和Y 同主族,X 与Z 同主族,R 原子最外层电子数比内层电子数多3,W、Y 原子的电子数总和与X、Z 原子的电子数总和之比为1:2。
下列说法正确的是A.原子半径r(X)>r(R)>r(W)B.X 与Y 只能形成一种化合物C.X 的简单气态氢化物的热稳定性比Z 的弱D.由W、R、X 三种元素组成的化合物可以是酸、碱或者盐1-6 下列实验中实验操作和现象、以及得出的结论均正确的是1-7 一种2-甲基色酮内酯(Y)可通过下列反应合成。
下列说法正确的是A.1molX 与浓溴水反应最多能与3molBr2加成B.X、Y 分子中所有碳原子均处于同一平面C.一定条件下,X 可以发生加成、缩聚、消去、氧化反应D.Y 与H2完全加成,每个产物分子中含有6个手性碳原子1-8 南京大学教授提出了一种高效的固碳新技术(如图)。
