四种基本反应类型与氧化还原反应)
四大基本反应类型

2.酸+盐=新酸+新盐
Na2CO3+2HCl=2NaCl+H2O+CO2↑
NaHCO3+HCl= NaCl+H2O+CO2↑
CaCO3+2HCl= CaCl2+H2O+CO2↑
3.盐+盐=新盐+新盐
CaCl2+Na2CO3=CaCO3↓+2NaCl
4.碱+盐=新碱+新盐
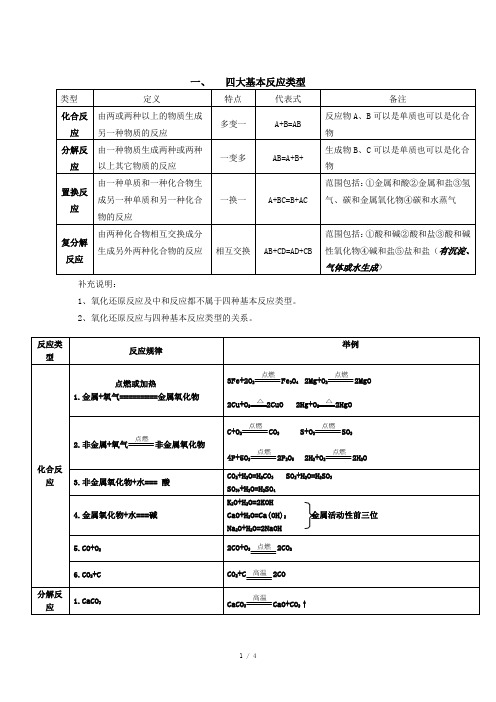
一、四大基本反应类型
类型
定义
特点代Βιβλιοθήκη 式备注化合反应由两或两种以上的物质生成另一种物质的反应
多变一
A+B=AB
反应物A、B可以是单质也可以是化合物
分解反应
由一种物质生成两种或两种以上其它物质的反应
一变多
AB=A+B+
生成物B、C可以是单质也可以是化合物
置换反应
由一种单质和一种化合物生成另一种单质和另一种化合物的反应
复分解反应:NaOH+HCl=NaCl+H2O
与CO2反应
+ H2O=H2CO3
2. CO2+2NaOH=Na2CO3+H2O
3. CO2+Ca(OH)2=CaCO3↓+H2O
4. CO2+Na2CO3+H2O=2NaHCO3
5. CO2+C=2CO(高温)
有CO2生成的反应
化合反应2CO+O2 2CO2C+O2 CO2
分解反应CaCO3 CaO+CO2↑H2CO3=H2O+CO2↑
氧化还原反应与四种基本反应类型

知识点
高中化学 1.二.化学物质及其变化/3.氧化还原反应 2.二.化学物质及其变化/3.氧化还原反应/A.四种基本类型反应与氧化还原反应
谢谢观看
此外,陶老师还将氧化还原反应与四种基本反应类型的关系比作音乐的四个基本音符,它们共同 构成了一首美妙乐章。这一比喻既赋予了氧化还原反应更生动的形象,又揭示了四种基本反应类 型在化学反应中的基础地位。
在讲述氧化还原反应的陶老师还深入探讨了其在日常生活中的应用,如金属腐蚀、电池原理等。
这些实例的引入,不仅增强了学习者的学习兴趣,更让他们深刻体会到化学知识在现实生活中的 实用性。
总的来说,陶铁午老师的《氧化还原反应与四种基本反应类型》微课课程,不仅具有深厚的理论 基础,更具有引人入胜的讲解风格和丰富的实例。学习者在欣赏陶老师讲解的过程中,不仅能够 理解氧化还原反应的本质,更能够在心中留下深刻的印象,为未来的化学学习打下坚实的基础。
目录
01 设计思路
02 知识点
设计思路
复习初中所学--氧化还原反应的特征----找特征----得到结论---总结---练习。
氧化还原反应与四种基本反应类型
兵团一三零团中学提供的微课课程
《氧化还原反应与四种基本反应类型》是兵团一三零团中学提供的引人入胜、发人深省的微课课 程,主讲教师陶铁午的讲解风格既深入浅出,又富有启发性,让学习者在理解氧化还原反应微课中,陶铁午老师运用了丰富的比喻和生动的实例,让氧化还原反应这一抽象的概念变 得形象化,仿佛就在眼前。他巧妙地将氧化还原反应比作一场生态战争,形象地描绘了战斗的进 程,使学习者如同身临其境,对氧化和还原这两个对立又统一的过程有了深刻的理解。
氧化还原反应的本质、特征与四大基本反应类型的关系

化学物质及其变化
专题五 考点
氧化还原反应
氧化还原反应的本质、特征与四大基本反 应类型的关系
1.氧化还原反应的本质:有电子转移(包括电子的得 失或偏移)。 2.氧化还原反应的特征:有元素化合价升降。
3.判断氧化还原反应的依据:凡是有元素化合价升 降或有电子转移的化学反应都属于氧化还原反应。 4.四大基本反应类型与氧化还原反应的关系。 置换反应全部属于氧化还原反应, 因为有单质参加和 另一种单质生成,化合价必然发生变化,故属于氧化还 原反应。
解析:反应时 Al 的化合价由 0 价变+3 价。Al 作还 原剂。 答案:A
2.(2015· 广州模拟)生产泡沫橡胶过程中,有如下反 应:2H2O2===2H2O+O2↑。该反应中 H2O2 是( A.既不是氧化剂,也不是还原剂 B.既是氧化剂又是还原剂 C.仅为氧化剂 D.仅为还原剂 )
解析:H2O2 中 O 的化合价既降低又升高,故 H2O2 既是氧化剂又是还原剂,故选 B。 答案:B
6.下列有关氧化还原反应的叙述中正确的是(
)
A. 有单质参加或有单质生成的反应一定是氧化还原 反应 B.氧化还原反应的本质是元素化合价的升降 C.失电子的反应物在反应中作氧化剂,反应中被还 原 D.金属单质在化学反应中一定作还原剂
解析: 有单质参加或有单质生成的反应不一定是氧化 还原反应,如同素异形体的相互转化,故 A 错;氧化还 原反应的本质是电子的转移,故 B 错;失电子的反应物 在反应中作还原剂,反应中被氧化,故 C 错;D 项正确。 答案:D
中,与氧化还原反应无关的是(
A.碳酸钠溶液中加入氯化钙溶液产生沉淀 B.铜粉在空气中加热变成黑色粉末 C.石灰石溶于盐酸并产生无色无味的气体 D.液氢在空气中变为氢气
最全氧化还原反应知识点总结

最全氧化还原反应知识点总结一、氧化还原基本概念氧化还原反应是指在化学反应过程中,元素的化合价发生变化或电子发生转移的化学变化。
其中,元素化合价的升降是氧化还原反应的特征,而电子转移是其实质。
在氧化还原反应中,反应物所含元素化合价升高的反应称为氧化反应,反之则称为还原反应。
氧化剂是指所含元素化合价升高的物质,而还原剂则是所含元素化合价降低的物质。
生成物中,所含元素化合价升高的被称为氧化产物,而所含元素化合价降低的则被称为还原产物。
二、氧化还原反应的四种基本类型氧化还原反应可以分为四种基本类型:氧化反应、还原反应、化合反应和分解反应。
其中,有单质参加的化合反应和有单质生成的分解反应也属于氧化还原反应。
三、氧化还原反应的有关计算在氧化还原反应中,电子转移可以使用双线桥法或单线桥法来表示。
双线桥法强调同一元素的原子或离子间的电子转移,而单线桥法则将箭头指向氧化剂,从失电子的元素出发指向得电子的元素。
四、氧化还原反应的类型氧化还原反应可以分为还原剂+氧化剂氧化产物+还原产物、部分氧化还原反应、自身氧化还原反应和归中反应四种类型。
其中,还原剂和氧化剂为不同物质参与的反应是最常见的类型。
而自身氧化还原反应可以发生在同一物质的不同元素之间或同一物质的同种元素之间。
归中反应则是一种非氧化还原反应,其特点是反应物中的两种物质合并生成一种新物质。
化学中,同一元素不同价态之间发生的氧化还原反应遵循以下变化规律:高价态和低价态会产生中间价态,中间价态可以相同也可以不同,但必须靠近,不能相互交叉。
例如,Cl2+ 2NaOH = NaCl + NaClO + H2O 就是一种歧化反应,发生在同一物质分子内、同一价态的同一元素之间的氧化还原反应。
歧化反应的反应规律是:所得产物中,该元素一部分价态升高,一部分价态降低,即“中间价→高价+低价”。
具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应。
氧化性和还原性的强弱取决于得失电子的难易程度,与得失电子的数目多少无关。
氧化还原反应基本概念

化合物中元素化合价的判断
(1)请正确判断下列二元化合物中各元素的化合价 CN- ClO2 O2F2 CuH FeS2 SF6 甲苯
NCl3 N2H4
【二元化合物中指定元素的化合价的判断方法】
①根据电负性原则,电负性较强者为负化合价,电负性较弱者为正化合价。 ②熟悉元素周期表,明确元素的最高价和最低价,确保元素的化合价不低于最低价,不高于最高价。 ③如果两种离子会发生氧化还原反应,则该物质不存在。 不存在FeI3、CuI2、Fe2S3
答案
(6)某元素从游离态变为化合态,该元素可能被氧化也可能被还原( √ ) (7)浓硫酸具有强氧化性,不能干燥SO2、CO等还原性气体( × ) (8)置换反应一定是氧化还原反应,化合反应、分解反应不一定是氧化还 原反应( √ ) (9)NaHCO3+H2===HCOONa+H2O的反应中,NaHCO3被氧化( × ) (10)Na2O2与水的反应中,水是还原剂( × )
专题四 氧化还原反应
【必备知识】
1. 氧化还原反应的本质: 电子的转移(电子的得失和电子的偏移) 2. 氧化还原反应的特征: 元素化合价的升降 3. 从物质角度:会判断氧化剂和还原剂,氧化产物和还原产物。 4. 从反应类型角度:会判断氧化反应和还原反应。 5. 物质化学性质的角度:会判断氧化性和还原性。 6. 氧化还原反应的规律。 7. 氧化还原反应的计算。 8. 氧化还原反应方程式的配平。
的气体的体积小于4.48L,主要的原因是?
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
(4)反应条件对酸氧化还原反应的影响——浓度
① MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
4种基本反应类型

4种基本反应类型一、合成反应合成反应是一种化学反应类型,其中两个或更多的反应物结合形成一个新的产物。
这种类型的反应通常涉及原子或分子之间的键的形成。
合成反应可以分为以下几种情况:1. 元素合成反应元素合成反应是指两个或多个元素结合形成一个化合物。
例如,氢气和氧气反应生成水。
这个反应可以用化学方程式表示为:2H₂ + O₂ → 2H₂O在这个反应中,两个氢原子和一个氧原子结合形成了两个水分子。
2. 化合物合成反应化合物合成反应是指两个或多个化合物反应生成一个新的化合物。
例如,氯化钠和硫酸反应生成氯化氢和硫酸钠。
这个反应可以用化学方程式表示为:NaCl + H₂SO₄ → HCl + Na₂SO₄在这个反应中,氯化钠和硫酸反应生成了氯化氢和硫酸钠。
二、分解反应分解反应是一种化学反应类型,其中一个化合物分解成两个或更多的反应物。
这种类型的反应通常涉及键的断裂。
分解反应可以分为以下几种情况:1. 热分解反应热分解反应是指一个化合物在高温下分解成两个或更多的反应物。
例如,碳酸钙在加热时分解成二氧化碳和氧化钙。
这个反应可以用化学方程式表示为:CaCO₃ → CO₂ + CaO在这个反应中,碳酸钙分解成了二氧化碳和氧化钙。
2. 电解分解反应电解分解反应是指一个化合物在电解过程中分解成两个或更多的反应物。
例如,水在电解过程中分解成氢气和氧气。
这个反应可以用化学方程式表示为:2H₂O → 2H₂ + O₂在这个反应中,水分解成了氢气和氧气。
三、置换反应置换反应是一种化学反应类型,其中一个元素或基团被另一个元素或基团取代。
置换反应可以分为以下几种情况:1. 单置换反应单置换反应是指一个元素或基团被一个元素或基团取代。
例如,氢气和溴气反应生成氢溴酸。
这个反应可以用化学方程式表示为:H₂ + Br₂ → 2HBr在这个反应中,氢气被溴气取代生成了氢溴酸。
2. 双置换反应双置换反应是指两个化合物中的两个元素或基团互相交换位置。
四大基本反应与氧化还原反应

+2 -2 +2 -2
1、CuO + CO === Cu + CO2
0 +3 -2
高温
0
+4
-2
(√)
0
2、3C +2Fe2O3
△
+4
-2
3CO2 ↑ +2Fe (√)
合有 价元 变素 化化
+1 +5 -2
+1 -1
+1 -1
+1 +5 -2
3、AgNO3+NaCl =AgCl↓+NaNO3 (×)无化合价变化
化合价降低
有元素化合价升降的化学反应称为氧化还原反应。
特征
氧化还原反应和四大基 本反应类型的关系
化 合 分 解
氧化还原反应
复分解
置换
判断下列反应属于四大基本反应类型中的哪一种
2Na+Cl2= 点 燃 化合反应 ==2NaCl CaCO3==高温=CaO+CO2↑ 分解反应
Zn+H2SO4 = 置换反应 ZnSO4+H2↑ H2SO4+BaCl2=2HCl+BaSO 复分解反应 ↓ 4H 分解反应 2CO3=H2O+CO2↑ Na2O+CO2=Na2CO 化合反应 3 Na2CO3+H2SO4=Na2SO4+H2O+复分解反应 CO2↑ Cu+Hg(NO ) = Hg+Cu(NO置换反应 )
两种化合物互相交换成分,生成 复分解反应: 另外两种化合物的反应
2HCl+CaCO3=CaCl2+H2O+
四种基本反应类型与氧化还原反应.ppt

2、判断下列反应能否发生,能请完 成并注明反应类型,否说明原因。
1)H2SO4+NaOH 2)NaOH+CuSO4
=_____________ =_____________
3)Na2CO3+CaCl2
=_____________
4)HCl+Na2CO3 5)KNO3+NaCl 6)Na2SO4+NH4NO3
2、根据所掌握的知识分析所有的分解反 应均是氧化还原反应吗?请举例说明。
1)生成物全是单质: 2) 生成物全是化合物: 3)生成物是一种单质和一种化合物:
结论:
3、根据所掌握的知识分析所有的置 换反应均是氧化还原反应吗?请举 例说明 。
1) 金属置换金属: 2)金属置换非金属: 3)非金属置换金属: 4)非金属置换非金属:
m
减小 不变 不变 不变 不变
V
C
不变 增大 减小 增大 不变
减小 减小 增大 减小 不变
讨论
定容时俯视或仰视刻度线,对溶 液的浓度有何影响?
俯 视
俯视刻度线,实 际加水量未到刻 度线,使溶液的 物质的量浓度增 大;
仰 视
仰视刻度线,实 际加水量超过刻 度线,使溶液的 物质的量浓度减 小。
6、Ⅰ、从铁、盐酸、氧气、水、硝酸银溶液 五种物质中选出1种或2种为反应物,按下列 反应类型各写1个化学方程式:
(1)化合反应
;
(2)分解反应
;
(3)置换反应
;
(4)复分解反应
;
以上化学反应属于氧化还原反应的是
号)。
(填序
Ⅱ、按下列要求各写出一个化学反应 方程式:
(1)有水生成的化合反应
;
化学反应基本类型和氧化还原反应知识

学科:奥化年级:初三不分版本期数:1320本周教学内容:化学反应基本类型和氧化还原反应知识【内容综述】 本期主要介绍化学反应的基本类型以及氧化还原反应的有关知识。
该内容的主要知识要点包括:(1)明确并学会判断四种基本反应类型,即:化合反应、分解反应、置换反应、复分解反应(2)从得失氧的角度理解氧化还原反应(3)判断某一反应是否发生氧化还原反应(4)判断发生氧化还原反应中那些物质被氧化、被还原、氧化剂、还原剂(5)明确四种基本反应类型与氧化还原反应间的关系。
由于化学反应的基本类型以及氧化还原反应知识是中学化学的重点和难点知识,也是考试中的热点知识,为此,本期主要从近几年的考试和竞赛试题中分析该内容的精髓。
【要点讲解】 一、四大基本反应类型的正确区分和理解 【例1】通过下列反应,一定有单质生成的是() A.化合反应 B.分解反应 C.置换反应 D.复分解反应 【解析】依题意知化合反应、复分解反应的产物一定是化合物,置换反应一定有单质生成,分解反应可能有单质,也可能有化合物生成。
故答案为C。
【例2】下列有关化学反应的基本类型的说法正确的是() A.反应物有多种的反应是化合反应 B.生成物有多种的反应是分解反应 C.两种化合物相互交换成分,生成另两种化合物的反应是复分解反应 D.生成物中一种是单质,另一种是化合物的反应就是置换反应 【解析】 本题主要考查四种基本反应类型及其有关知识。
化合反应的特点是反应物有多种,但生成物只有一种,即“多到一”,而A选项只强调反应物而未强调生成物,故不一定是化合反应;分解反应的特点是“一到多”,B选项只强调生成物,而未强调反应物的种类,故也不一定属于分解反应;置换反应的特点是单质和化合物反应生成另一种单质和化合物,而D选项只强调生成物的特点,例如实验室用氯酸钾分解制氧气的反应符合选项要求,但其属于分解反应。
故本题答案为C。
二、氧化还原反应知识的更深层次的理解和应用 【例3】下列有关氧化还原反应的叙述错误的是() A.失氧的物质被还原,得氧的物质被氧化 B.失氧的物质是还原剂,得氧的物质是氧化剂 C.氧化剂发生氧化反应,还原剂发生还原反应 D.氧化反应和还原反应必需同时发生 【解析】本题是考查氧化还原反应的有关知识。
(完整版)氧化还原反应

氧化还原反应一、概念化合价升降的反应。
二、本质电子的转移(得失或偏移)。
三、四种反应类型1.化合反应:可以是氧化还原反应。
如H2O2+SO2=H2SO42。
分解反应:可以是氧化还原反应.如NH4NO3=(△)N2O+2H2O3。
置换反应:一定是氧化还原反应。
4。
氧化还原反应:同素异形体间的转化是化学变化但不是氧化还原反应。
如:3O2=(放电)2O3四、常见的氧化剂与还原剂1。
氧化剂:①活泼的非金属单质:F2、Cl2、Br2、I2、O2、O3等。
碘与铁生成的二价的碘化亚铁。
②高价态金属离子:Fe3+、Cu2+.③元素处于高价时的含氧酸:硝酸、浓硫酸。
④元素处于高价时盐:KClO3、KMnO4、K2Cr2O7。
⑤其他:银氨溶液、新制氢氧化铜、漂白粉、HClO、H2O2、MnO2等。
2.还原剂①金属单质:K、Na、Mg等。
②非金属单质:H2、C、Si、S等。
③低价态的化合物:CO、H2S、HI、Fe2+、NH3等.④其他:Fe2+、S2-、I—、Br-。
五、氧化剂的还原产物O2→H2O或OH—;Fe3+ →Fe2+;浓硫酸→SO2;浓硝酸→NO2;稀硝酸→NO;H2O2→H2O或OH-;K2Cr2O7(H+)→Cr3+;六、氧化性、还原性强弱的比较1.反应条件:热>冷;浓>稀;易>难;Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2OCu+2H2SO4(浓)=(△)CuSO4+2H2O+SO2↑Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O3Cu + 8HNO3(稀) =3Cu(NO3)2 + 4H2O + 2NO↑16HCl(浓)+2KMnO4=2KCl+2MnCl2+8H2O+5Cl2↑4HCl(浓)+MnO2=(△)MnCl2+2H2O+Cl2↑4HCl(浓)+O2=(△、CuCl2催化剂)2H2O+2Cl2↑氧化性:KMnO4>MnO2>O22. 根据物质活动性顺序比较金属:K〉Ca>Na〉Mg〉Al>Mn〉Zn>Cr>Fe〉Ni>Sn〉Pb〉(H)〉Cu>Ag〉Pt>Au非金属:F〉Cl〉Br>I〉S;原子(或单质)氧化性逐渐减弱,对应阴离子还原性增强。
四大基本反应类型
1.CaCO3
CaCO3 CaO+CO2↑
2. H2O
2H2O 2H2↑+O2↑
3.H2CO3
H2CO3=H2O+CO2↑
4制取O2的三个反应
2KMnO4 K2MnO4+MnO2+O2↑
2H2O2 2H2O+O2↑2KClO3 2KCl+3O2↑
5. NaHCO3(小苏打)
2NaHCO3 Na2CO3+H2O+CO2↑
4C+Fe3O4 3Fe+4 CO2↑C+2CuO 2Cu+CO2↑
4.氢气+氧化铜
H2+CuO Cu+H2O
其
他
1.CO2+碱=盐+水
CO2+2NaOH=Na2CO3吸收除去CO2
CO2+Ca(OH)2=CaCO3↓+H2O检验CO2
2.有机物的燃烧CH4、C2H5OH、C6H12O6的燃烧反应
CH4+2O2 CO2+2H2O
C2H5OH+3O2 2CO2+3H2O
C6H12O6+6O2 6CO2+6H2O
3.CO+CuO
CO+CuO Cu+CO2
二、出现水或二氧化碳的反应
与水反应
1.2H2O=2H2↑+O2↑(电解)
2. H2O+CO2=H2CO3
3. H2O+CaO=Ca(OH)2
4.CuSO4+5H2O== CuSO4·5H2O
Fe+2HCl=FeCl2+H2↑
2.金属+盐=新金属+新盐
四大基本反映类型

四大基本反应类型化合反应:指的是由两种或两种以上的物质生成一种新物质的反应(combination reaction)。
其中部分反应为氧化还原反应,部分为非氧化还原反应。
此外,化合反应一般释放出能量。
分解反应:分解反应,是化学反应的常见类型之一,是化合反应的逆反应。
它是指一种化合物分解成二种或二种以上较简单的单质或化合物的反应。
置换反应:置换反应是单质与化合物反应生成另外的单质和化合物的化学反应,是化学中四大基本反应类型之一,包括金属与金属盐的反应,金属与酸的反应等。
复分解反应:复分解反应是由两种化合物互相交换成分,生成另外两种化合物的反应。
其实质是:发生复分解反应的两种物质在水溶液中相互交换离子,结合成难电离的物质----沉淀、气体、水,使溶液中离子浓度降低,化学反应即向着离子浓度降低的方向进行。
可简记为AB+CD=AD+CB。
化合反应1.金属+氧气→金属氧化物很多金属都能跟氧气直接化合。
例如常见的金属铝接触空气,它的表面便能立即生成一层致密的氧化膜,可阻止内层铝继续被氧化。
4Al+3O2 = 2Al2O32.非金属+氧气→非金属氧化物经点燃,许多非金属都能在氧气里燃烧,如:C+O2=点燃=CO23.金属+非金属→无氧酸盐许多金属能与非金属氯、硫等直接化合成无氧酸盐。
如:2Na+Cl2==点燃==2NaCl4.氢气+非金属→气态氢化物. 因氢气性质比较稳定,反应一般需在点燃或加热条件下进行。
如:2H2+O2=点燃=2H2O5.碱性氧化物+水→碱. 多数碱性氧化物不能跟水直接化合。
判断某种碱性氧化物能否跟水直接化合,一般的方法是看对应碱的溶解性,对应的碱是可溶的或微溶的,则该碱性氧化物能与水直接化合。
如:Na2O+H2O=2NaOH.对应的碱是难溶的,则该碱性氧化物不能跟水直接化合。
如CuO、Fe2O3都不能跟水直接化合。
6.酸性氧化物+水→含氧酸. 除SiO2外,大多数酸性氧化物能与水直接化合成含氧酸。
四大基本反应类型与氧化还原反应的关系

四大基本反应类型与氧化还原反应的关系
四大基本反应类型都涉及到氧化还原反应。
1. 合成反应(Synthesis Reaction):由两种或两种以上原料经氧化还原反应合成新物质,一般原料物质发生氧化。
2. 分解反应(Decomposition Reaction):一种原料物质经氧化还原反应分解为两种或两种以上物质,一般原料物质发生还原。
3. 交换反应(Exchange Reaction):由两种不同的原料物质交换基团,经氧化还原反应得到新的物质,两种原料物质都发生氧化还原反应。
4. 水解反应(Hydrolysis Reaction):在水的作用下,原料物质通过氧化还原反应破坏键的过程,将原料物质分解成二价离子及水,一般原料物质发生还原反应。
化学基本反应类型

化学基本反应类型
化学反应是指化学物质之间发生物质转化的过程,化学反应可分为物理变化和化学变化两种类型。
而化学变化又可以分为以下基本反应类型:
1. 合成反应:指两个或多个物质反应生成一个新物质的过程,也称为化合反应。
例如:2H2(g) + O2(g) →2H2O(l)。
2. 分解反应:指一个物质在一定条件下分解成两个或多个物质的过程。
例如:CaCO3(s) →CaO(s) + CO2(g)。
3. 单一置换反应:指一种元素置换另一种元素的反应,也称为单一置换反应。
例如:Fe(s) + CuSO4(aq) →Cu(s) + FeSO4(aq)。
4. 双重置换反应:指两个化合物中的阳离子和阴离子互相交换的反应,也称为双替换反应。
例如:AgNO3(aq) + NaCl(aq) →AgCl(s) + NaNO3(aq)。
5. 氧化还原反应:指在反应中发生电子转移的化学反应,其中一个物质被氧化,另一个物质被还原。
例如:2HCl(aq) + Zn(s) →ZnCl2(aq) + H2(g)。
以上是化学基本反应类型的简要介绍。
在实际应用中,化学反应类型的分类并不是非常严格,很多反应都可以同时归属于多种类型。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C、复分解反应中有的是氧化还原反应,有的不是氧
化还原反应
D、置换反应有可能是非氧化还原反应
3、下列反应既是化合反应,又是氧 化还原反应的是( )
A、SO3+H2O=H2SO4 B、Fe+H2SO4(稀)=FeSO4+H2↑ C、SO2+Ca(OH)2=CaSO3↓+H2O
点燃
D、2CO+O2=2CO2
1.一边阅读一边回忆初中所学过的化学 方程式。
2.理解氧化还原反应的概念。 (时间为3分钟)
[自学检测]
一、化学反应的分类 1、化学反应的分类
根据反应物 生成物的类 别和种类
化合反应
_________
_________
_________
根据反应前后 _________ 元素是否有化
合价的变化 非氧化还原反应
=_____________ =_____________
=_____________
反应类型为 ,
此类反应发生的条件是 ______________
[应用与拓展]
1、根据所掌握的知识分析所有的化合反应均是 氧化还原反应吗?请举例说明。
1)单质之间的化合: 2)化合物之间的化合: 3)单质和化合物之间的化合: 结论:
2、四种基本反应类型
反应 类型
化合 反应
分解 反应
置换 反应
复分 解反 应
定义
字母 表达式
特点
反应过程中元素代价的变化 (请举例2个)
二、氧化还原反应与非氧化还原 反应
1.非氧化还原反应的概念:____ 2.氧化还原反应 1)概念: ________ 2)氧化还原反应与元素化合价升
降的关系
以CuO+H2 Cu+H2O
4、下列反应中,不属于四种基本 反应类型的是( )
A、2Na+2H2O=2NaOH+ H2↑
光照
B、2HClO = 2HCl+O2↑ C、Fe+2FeCl3=3FeCl2 D、CuO+CO Cu+CO2
5、将相应的反应序号填在对应的横线 上:
A、Fe3O4+4CO△3Fe+4CO2 B、2KMnO4△K2MnO4+MnO2+O2↑ C、Zn+H2SO4=ZnSO4+H2↑ D、CaCO3+2HCI=CaCI2+H2O+CO2↑
2、根据所掌握的知识分析所有的分解反 应均是氧化还原反应吗?请举例说明。
1)生成物全是单质: 2) 生成物全是化合物: 3)生成物是一种单质和一种化合物:
结论:
3、根据所掌握的知识分析所有的置 换反应均是氧化还原反应吗?请举 例说明 。
1) 金属置换金属: 2)金属置换非金属: 3)非金属置换金属: 4)非金属置换非金属:
第一单元 丰富多彩的化学物质
第三课时
四种基本反应类型与氧化还原反应
[学习目标]
1、了解化学反应的四种基本反应类型和氧化还原反应。 2、理解四种基本反应类型和氧化还原反应之间的关系。 3、掌握复分解反应和置换反应发生的条件。
[学习重难点]
四种基本反应类型和氧化还原反应间的关系。
[自学指导]
认真看课本P5-P6的内容阅读时并注意以 下几点:
2、判断下列反应能否发生,能请完 成并注明反应类型,否说明原因。
1)H2SO4+NaOH 2)NaOH+CuSO4
=_____________ =_____________
3)Na2CO3+CaCl2
=_____________
4)HCl+Na2CO3 5)KNO3+NaCl 6)Na2SO4+NH4NO3
2CuO + C === 2Cu + CO2
质量比: 160 12 128 44
粒子数比: 2
1
2
1
物质的量
之比:
2mol 1mol 2mol
1mol
一、物质的量浓度
定义:
单 位:
以单位体积溶液里所含溶质B的物质的量 来表示溶液组成的物理量 ,叫做溶质B的 物质的量浓度。
nB
公式:CB=
vaq
置换反应
复分解反 应
分解反应
化合反
应
置换反应
复分解反 应
[归纳总结]
1、谈一谈本节课的收获: 2、本节课中你存在的问题:
[当堂检测]
1、通过下列反应,不可能得到单质的是( )
A、化合反应
B、置换反应
C、氧化还原反应 D、分解反应
2、下列说法正确的是( )
A、化合反应一定是氧化还原反应
B、分解反应不一定是氧化还原反应
解反应:
;
(3)有硝酸银参加反应生成硝酸铜的置换反
应
;
(4)生成两种沉淀的复分解
反应
。
[课后作业]
1、课本P5“整理与归纳” 2、课本P6“交流与讨论” 3、课本P16“练习与实践”2 (要求:做在课本上)
练习:某饱和溶液的溶解度为25g,其溶液的
质量分数为___2_0_%_______。
某饱和溶液的质量分数为25 % ,其溶解度为 _____3_3_.3_g___。
结论:
4、有单质参与的化学反应一定是氧化 还原反应吗?请举例说明。
如:
结论:
5、根据所掌握的知识分析所有的置换反应均
是氧化还原反应吗?请举例说明。
1)酸与碱反应: 2)酸与盐反应: 3)碱与盐反应: 4)盐与盐反应: 结论:
6、用图示说明四种基本反应类型 与氧化还原反应的关系。
化合反 应
分解反应
6、Ⅰ、从铁、盐酸、氧气、水、硝酸银溶液 五种物质中选出1种或2种为反应物,按下列 反应类型各写1个化学方程式:
(1)化合反应
;
(2)分解反应
;
(3)置换反应
;
(4)复分解反应
;
以上化学反应属于氧化还原反应的是
号)。
(填序
Ⅱ、按下列要求各写出一个化学反应 方程式:
(1)有水生成的化合反应
;
(2)生成一种碱性氧化物和一种酸性氧化物的分
Fe+CuSO4=FeSO4+Cu为例进行
分析。
化合价降低
C+2uO+0H2△C0 u+
+1
H2O
化合价升高
Fe+CuSO4=FeSO4+Cu
(自己分析)
[交流讨论]
1、判断下列反应能否发生,能请完成,并注明反 应类型,否说明原因。 1)、Fe+CuSO4 2)、Cu+AgNO3 3)、Fe+ZnSO4 4)、Cu+MgSO4 反应类型为 , 此类反应发生的条件是
点燃
E、C2H5OH(酒精)+3O2 → 2CO2+3H2O
点燃
F、3Fe+2O2 = Fe3O4 G、HCI+NaOH=H2O+NaCI
其中属于化合反应的是 , 属于分解反应的是 , 属于复分解反应的是 , 属于置换反应的是 , 属于中和反应的是 , 尚不能归类于四种基本反应类型的有_____。
