有机物的化学方程式(高中)
高中化学全部化学方程式汇总(有机和无机)

高中化学全部化学方程式汇总(有机和无机)【注意】以下是有机和无机化学方程式的汇总,请按需使用或参考。
为了排版整洁,请在使用时进行适当的调整和修改。
一、有机化学方程式1. 碳氢化合物反应方程式1.1 烷烃燃烧反应:CnH2n+2 + (n + (n/2 + 1)/2)O2 → nCO2 + (n + (n/2 - 1)/2)H2O1.2 烯烃燃烧反应:CnH2n + (n + n/2)O2 → nCO2 + nH2O1.3 异构烷烃燃烧反应:CnH2n + (n + n/2)O2 → nCO2 + nH2O2. 醇类反应方程式2.1 醇的燃烧反应:CnH2n+1OH + (n + (n+1)/2)O2 → nCO2 + (n+1)H2O2.2 醇的脱水反应:CnH2n+1OH → CnH2n + H2O3. 酚类反应方程式3.1 酚的燃烧反应:C6H6O + 15/2O2 → 6CO2 + 3H2O 3.2 酚的酸碱中和反应:C6H6O + NaOH → C6H5ONa + H2O 4. 酯类反应方程式4.1 酯的酸水解反应:RCOOR' + H2O → RCOOH + R'OH 4.2 酯的碱水解反应:RCOOR' + NaOH → RCOONa + R'OH 5. 醛和酮类反应方程式5.1 氧化性还原反应:RCHO + [O] → RCOOH5.2 醛的酸碱反应:RCHO + NaOH → RCOONa + H2O 6. 醚类反应方程式6.1 醚的加热裂解反应:ROR' → R'H + R'OH6.2 醚的酸水解反应:ROR' + H2O → ROH + R'OH7. 脂肪酸类反应方程式7.1 脂肪酸的酸碱反应:RCOOH + NaOH → RCOONa + H2O7.2 脂肪酸的酯化反应:RCOOH + R'OH → RCOOR' + H2O二、无机化学方程式1. 钠和氧的反应方程式4Na + O2 → 2Na2O2. 钙和水的反应方程式Ca + 2H2O → Ca(OH)2 + H23. 硝酸和铜的反应方程式Cu + 4HNO3 → Cu(NO3)2 + 2NO2 + 2H2O 4. 二氧化碳和水的反应方程式CO2 + H2O → H2CO35. 硝酸和氢氧化钠的反应方程式2NaOH + HNO3 → NaNO3 + H2O6. 硫化氢和氯的反应方程式H2S + Cl2 → 2HCl + S7. 氧化锌和硫酸的反应方程式ZnO + H2SO4 → ZnSO4 + H2O8. 氯气和钾溶液的反应方程式Cl2 + 2KOH → KCl + KClO + H2O9. 溴和钾的反应方程式2K + Br2 → 2KBr10. 硫和氧的反应方程式S + O2 → SO2以上是高中化学的部分有机和无机方程式的汇总,希望能对你的学习有所帮助。
(完整版)高中有机化学方程式总结
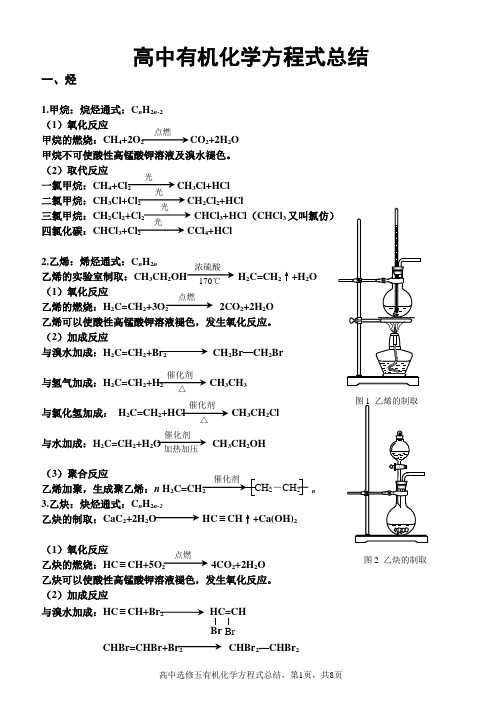
高中有机化学方程式总结一、烃1.甲烷:烷烃通式:C n H 2n -2 (1)氧化反应甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl二氯甲烷:CH 3Cl+Cl 2CH 2Cl 2+HCl三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3四氯化碳:CHCl 3+Cl 2 CCl 4+HCl2.乙烯:烯烃通式:C n H 2n乙烯的实验室制取:CH 3CH 2OH H 2C=CH 2↑+H 2O (1)氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br与氢气加成:H 2C=CH 2+H 2 CH 3CH 3与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl与水加成:H 2C=CH 2+H 2O CH 3CH 2OH(3)聚合反应乙烯加聚,生成聚乙烯:n H 2 n3.乙炔:炔烃通式:C n H 2n-2乙炔的制取:CaC 2+2H 2O HC ≡CH ↑+Ca(OH)2(1)氧化反应乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br 2 HC=CHBr点燃光光光光浓硫酸170℃ 点燃催化剂△催化剂加热加压 2-CH 2点燃图2 乙炔的制取Br 催化剂△与氢气加成:HC ≡CH+H 2 H 2C=CH2与氯化氢加成:HC ≡CH+HCl CH2=CHCl(3)聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2 n乙炔加聚,得到聚乙炔:n HC ≡ n4.苯:苯的同系物通式:C n H 2n-6(1)氧化反应苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
高中有机物化学方程式

高中有机物化学方程式
高中有机化学是化学学科的重要组成部分,涉及的有机物种类繁多,反应类型多样。
以下是一些常见的高中有机化学方程式,供您参考:
1、烷烃的燃烧反应
CH4 + 2O2 →CO2 + 2H2O
C2H6 + 7O2 →2CO2 + 3H2O
2、烷烃与卤素单质的取代反应
CH4 + Cl2 →CH3Cl + HCl
C2H6 + Cl2 →C2H5Cl + HCl
3、烯烃与卤素单质的加成反应
CH2=CH2 + X2 →CH2XCH2X
CH2=CH2 + HX →CH3CH2X
4、乙醇的燃烧反应
C2H5OH + 3O2 →2CO2 + 3H2O
5、乙醇的催化氧化反应
2C2H5OH + O2 →2CH3CHO + 2H2O
6、乙酸乙酯的水解反应
CH3COOC2H5 + H2O →CH3COOH + C2H5OH
7、酯化反应
CH3COOH + C2H5OH →CH3COOC2H5 + H2O
8、苯与浓硝酸的取代反应
C6H6 + HNO3(浓) →C6H5NO2 + H2O
9、苯的燃烧反应
C6H6 + 7O2 →6CO2 + 3H2O
10、乙烯与浓硫酸的反应
CH2=CH2 + H2SO4(浓) →CH3CH2SO3H
以上仅列举了一些常见的高中有机化学方程式,实际上还有许多其他类型的有机反应,如酯化反应、水解反应、消去反应、加氢还原反应等等。
学习高中有机化学时,建议系统地学习和掌握各类有机物的性质和反应规律,以便更好地理解和应用这些方程式。
高中有机反应方程_有机物化学方程式
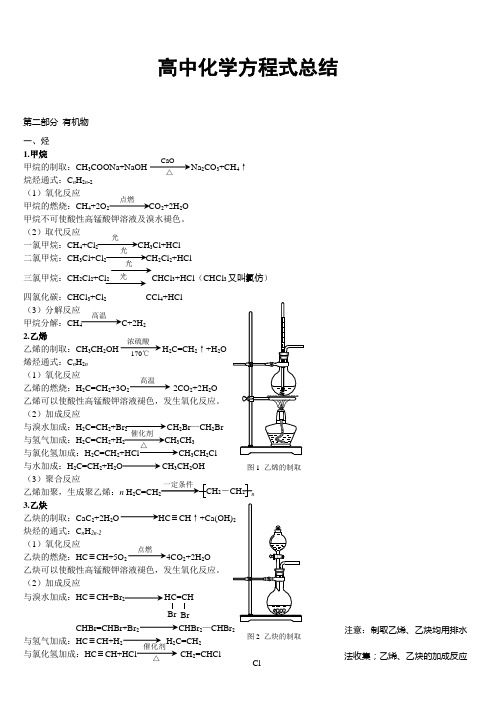
8.苯酚
苯酚是无色晶体,露置在空气中会因氧化显粉红色。苯酚具有特殊的气味,熔点
43℃,水中溶解度不大,易溶于有机溶剂。苯酚有毒,是一种重要的化工原料。
(1)苯酚的酸性
(苯酚钠)
苯酚(俗称石炭酸)的电离:
+H2O +H3O+
苯酚钠与CO2反应:
+CO2+H2O +NaHCO3
3.乙炔
乙炔的制取:CaC2+2H2O HC CH↑+Ca(炔的燃烧:HC CH+5O24CO2+2H2O
乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应
与溴水加成:HC CH+Br2HC=CH
Br
CHBr=CHBr+Br2CHBr2—CHBr2
乙醛还原氢氧化铜:CH3CHO+2Cu(OH)2CH3COOH+Cu2O+2H2O
10.乙酸
(1)乙酸的酸性
乙酸的电离:CH3COOH CH3COO-+H+
(2)酯化反应
CH3—C—OH+C2H5—OH CH3—C—OC2H5+H2O(乙酸乙酯)
注意:酸和醇起作用,生成酯和水的反应叫做酯化反应。
11.乙酸乙酯
(2)取代反应
+3Br2↓+3HBr
(三溴苯酚)
(3)显色反应
苯酚能和FeCl3溶液反应,使溶液呈紫色。
9.乙醛
乙醛是无色无味,具有刺激性气味的液体,沸点20.8℃,密度比水小,易挥发。
(1)加成反应
乙醛与氢气反应:CH3—C—H+H2CH3CH2OH
(完整版)高中有机化学方程式总结

高中有机化学方程式总结一、烃1.甲烷:烷烃通式:C n H 2n -2 (1)氧化反应甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl二氯甲烷:CH 3Cl+Cl 2CH 2Cl 2+HCl三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HCl (CHCl 3四氯化碳:CHCl 3+Cl 2 CCl 4+HCl2.乙烯:烯烃通式:C n H 2n乙烯的实验室制取:CH 3CH 2OH H 2C=CH 2↑+H 2O (1)氧化反应乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2O 乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br与氢气加成:H 2C=CH 2+H 2 CH 3CH 3与氯化氢加成: H 2C=CH 2+HCl CH 3CH 2Cl与水加成:H 2C=CH 2+H 2O CH 3CH 2OH(3)聚合反应乙烯加聚,生成聚乙烯:n H 2 n3.乙炔:炔烃通式:C n H 2n-2乙炔的制取:CaC 2+2H 2O HC ≡CH ↑+Ca(OH)2(1)氧化反应乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O 乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:HC ≡CH+Br 2 HC=CHBr点燃光光光光浓硫酸170℃ 点燃催化剂△催化剂加热加压 2-CH 2点燃图2 乙炔的制取Br 催化剂△与氢气加成:HC ≡CH+H 2 H 2C=CH2与氯化氢加成:HC ≡CH+HCl CH2=CHCl(3)聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2 n乙炔加聚,得到聚乙炔:n HC ≡ n4.苯:苯的同系物通式:C n H 2n-6(1)氧化反应苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O 苯不能使溴水和酸性高锰酸钾溶液褪色。
高中有机化学方程式大全

Ca催化催催化催化催催催高中有机化学方程式大全1. CH 4 + Cl 2 CH 3Cl + HCl2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 3 8. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br 9. CH 2 = CH 2 + H 2O CH 3CH 2OH 10. CH 2 = CH 2 + HBr CH 3—CH 2Br 11. CH 2 = CH 2 + H 2 CH 3—CH 3 12. nCH 2 = CH 2 [ CH 2—CH 2 ] n 13. nCH 2=CH-CH=CH 2 [CH 2-CH=CH-CH 2] n催化催催化14. 2CH2 = CH2 + O2 2CH3CHO15. CH≡CH + Br2 CHBr = CHBr16. CHBr = CHBr+ Br2 CHBr2-CHBr217. CH≡CH + HCl H2C = CHCl18. nCH2 = CH [ CH2-CH ] nCl Cl19. CH≡CH + H2O CH3CHO20. CaC2 + 2H2O CH≡CH↑+ Ca(OH)2-2 +H2O-SO33H+H2O225. +3HO-NO22ONaOH醇催化浓硫浓硫BrOH催化催化26. 3CH≡27. CH3CH2Br + H2O CH3CH2OH + HBr28. CH3CH2Br + NaOH CH3CH2OH + NaBr29. CH3CH2Br+ NaOH CH2 = CH2 + NaBr +H2O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2O+C2H5OH C2H5OC2H5+H2O34. OH+NaOH ONa+H2O2O O-+H3O+233738. CH3CHO + H2 CH3CH2OH△△催催催39. 2CH 3CHO + O 2 2CH 3COOH40. CH 3CHO+2Ag(NH 3)2OH CH 3COONH 4+2Ag ↓+3NH 3+H 2O 41CH 3CHO+2Cu(OH)2 CH 3COOH+Cu 2O ↓+2H 2O 42. 2CH 3COOH+2Na 2CH 3COONa+H 2↑ +Na 2CO 3 2CH 3COONa+H 2O+CO 2↑44. CH 3COOH+NaHCO 3 CH 3COONa+H 2O+CO 2↑ 45. CH 3COOH + NaOH CH 3COONa + H 2O46. 2CH 33COO)2Cu + 2H 2O+CH 3CH 2OH CH 3COOCH 2CH 3 +H 2O48. CH 3COOCH 2CH 3+NaOH CH 3COONa+CH 3CH 2OH 49. nOHCH 2CH 2COOH → [ OCH 2CH 2C ] n +H 2O50. C 6H 12O 6 (s) + 6O 2 (g) 6CO 2 (g) + 6H 2O (l) 51. C 6H 12O 6 2CH 3CH 2OH + 2CO 252. C 12H 22O 11+H 2O C 6H 12O 6+ C 6H 12O 6蔗糖 葡萄糖 果糖催催化催化+浓硫+ 2H OOC —O OCH-53. C12H22O11 + H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2 C17H35COO-CH2 57. C17H35COO-CH2 CH2-OH C17H35COO-CH +3NaOH 3C17H35COONa+ CH-OHC17H35COO-CH2 CH2-OH 58. CH2OH COOHCH2OH COOH1.HClClCHClCH+−→−+324光HClClCHClClCH+−→−+2223光2.4.5.6.7.8.222Br CH CH CH CH +=-=9.11.12. 13.14.15.16.17.OH NH Ag CHO CHOH HOCH 2342)(2)(+ O H NH Ag COONH CHOH HOCH 2344232)(++↓+−→−∆18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
(完整版)高中有机化学方程式大全

光照 光照 光照 光照 高温 CaO △ 催化剂 加热、加压催化剂 △ 催化剂高中有机化学方程式大全1. CH 4 + Cl 2 CH3Cl + HCl 2. CH 3Cl + Cl 2 CH 2Cl 2 + HCl3. CH 2Cl + Cl 2 CHCl 3 + HCl4. CHCl 3 + Cl 2 CCl 4+ HCl5. CH 4 C +2H 26. C 16H 34 C 8H 18 + C 8H 167. CH 3COONa + NaOH CH 4↑+ Na 2CO 38. CH 2 = CH 2 + Br 2 CH 2Br —CH 2Br9. CH 2 = CH 22OH10. CH 2 = CH 23—CH 2Br 11. CH 2 = CH 2CH 3 12. nCH 2 = CH 2 ] n13. nCH 2-CH=CH-CH 2] n14. 2CH 23CHO15. CH ≡CH + Br 2 CHBr = CHBr16. CHBr = CHBr+ Br 2 CHBr 2-CHBr 217. CH ≡CH + HCl H 2C = CHCl18. nCH 2 = CH [ CH 2-CH ] nCl Cl19. CH ≡CH + H 2O CH 3CHO20. CaC 2 + 2H 2O CH ≡CH ↑+ Ca(OH)2+ Br 222. + HO 2 +H 2O 23. + HO 3H+H 2O催化剂△浓硫酸170℃浓硫酸140℃催化剂△24.+ 3H2-NO22O26. 3CH≡C H27. CH3CH2Br + H228. CH3CH229. CH3CH22O30. 2CH3CH2OH+2Na 2CH3CH2ONa + H2↑31. 2CH3CH2OH+O2 2CH3CHO + 2H2O32. CH3CH2OH CH2 = CH2↑+ H2O33.C2H5OH+C2H5OH C2H5OC2H5+H2O34. 2O35. 2O -+H3O+233738. CH339. 2CH340. CH34+2Ag↓+3NH3+H2O 41CH3↓+2H2O42. 2CH3COOH+2Na 2CH3COONa+H2↑43.2CH3COOH+Na2CO32CH3COONa+H2O+CO2↑44. CH3COOH+NaHCO3 CH3COONa+H2O+CO2↑45. CH3COOH + NaOH CH3COONa + H2O浓硫酸△催化剂催化剂催化剂催化剂催化剂△催化剂加热、加压+ 浓硫酸△+ 2H2O O OC —CO OCH2-CH246. 2CH3COOH + Cu(OH)2 (CH3COO)2Cu + 2H2O47.CH3COOH+CH3CH2OH CH3COOCH2CH3 +H2O48. CH3COOCH2CH3+NaOH CH3COONa+CH3CH2OH49. nOHCH2CH2COO H→[ OCH2CH2C ] n +H2O50. C6H12O6 (s) + 6O2 (g)6CO2 (g) + 6H2O (l)51. C6H12O62CH3CH2OH + 2CO252. C12H22O11+H2O C6H12O6+ C6H12O6蔗糖葡萄糖果糖53. C12H22O11 + H2O2C6H12O6麦芽唐葡萄糖54. (C6H10O5)n + nH2O n C6H12O6淀粉葡萄糖55. (C6H10O5)n + nH2O n C6H12O6纤维素葡萄糖56.C17H33COO-CH2C17H35COO-CH2C17H33COO-CH +3H2 C17H35COO-CHC17H33COO-CH2C17H35COO-CH257. C17H35COO-CH2CH2-OHC17H35COO-CH +3NaOH3C17H35COONa+ CH-OHC17H35COO-CH2CH2-OH58. CH2OH COOHCH2OH COOH1.HClClCHClCH+−→−+324光HClClCHClClCH+−→−+2223光2.3.4.5.6.7.8.222Br CH CH CH CH +=-= 9.10. 11.12.13.14.15.16.17. OH NH Ag CHO CHOH HOCH 2342)(2)(+O H NH Ag COONH CHOH HOCH 2344232)(++↓+−→−∆18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1)、银镜反应(2)、乙酸乙酯的水解(3)苯的硝化(4)糖的水解(5)、酚醛树脂的制取(6)固体溶解度的测定凡是在不高于100℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
高中有机化学方程式总结

高中有机化学方程式总结一、烃1. 烷烃 —通式:C n H 2n -21氧化反应①甲烷的燃烧:CH 4+2O 2 CO 2+2H 2O②甲烷不可使酸性高锰酸钾溶液及溴水褪色; 2取代反应一氯甲烷:CH 4+Cl 2 CH 3Cl+HCl二氯甲烷:CH 3Cl+Cl 2 CH 2Cl 2+HCl三氯甲烷:CH 2Cl 2+Cl 2 CHCl 3+HClCHCl 3又叫氯仿四氯化碳:CHCl 3+Cl 2 CCl 4+HCl3分解反应CH 4 C+2H 22. 烯烃 —通式:C n H 2n乙烯的制取:CH 3CH 2OH H 2C=CH 2↑+H 2O 1氧化反应①乙烯的燃烧:H 2C=CH 2+3O 2 2CO 2+2H 2②乙烯可以使酸性高锰酸钾溶液褪色,2加成反应与溴水加成:H 2C=CH 2+Br 2 CH 2Br —CH 2Br 与氢气加成:H 2C=CH 2+H 2 CH 3CH 3与氯化氢加成: H 2C=CH 2+HCl CH 32Cl与水加成:H 2C=CH 2+H 2O CH 3CH 2OH 3聚合反应乙烯加聚,生成聚乙烯:n H 2C=CH n3. 炔烃 —通式:C n H 2n-2乙炔的制取:CaC 2+2H 2O HC ≡CH↑+CaOH 2 1氧化反应①乙炔的燃烧:HC ≡CH+5O 2 4CO 2+2H 2O②乙炔可以使酸性高锰酸钾溶液褪色,2加成反应与溴水加成:HC ≡CH+Br 2 HC=CHBr CHBr=CHBr+Br 2 CHBr 2—CHBr 2与氢气加成:HC ≡CH+H 2 H 2C=CH 2与氯化氢加成:HC ≡CH+HCl CH 2=CHCl 3聚合反应氯乙烯加聚,得到聚氯乙烯:n CH 2n乙炔加聚,得到聚乙炔:n HC ≡n 4. 苯 C 6H 6点燃光光光光浓硫酸170℃ 点燃催化剂 △ 催化剂加热加压 2-CH 2图1 乙烯的制取点燃图2 乙炔的制取催化剂△催化剂△Br2—CHClCH=CH催化剂 △高温1氧化反应①苯的燃烧:2C 6H 6+15O 2 12CO 2+6H 2O②苯不能使溴水和酸性高锰酸钾溶液褪色; 2取代反应 ①苯与溴反应+HO 3加成反应环己烷5. 甲苯 苯的同系物通式:C n H 2n-61氧化反应①甲苯的燃烧:C 7H 8+9O 2 7CO 2+4H 2O②甲苯不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色; 2取代反应3加成反应二、烃的衍生物点燃点燃+Br +3H CH 3| +3HNO 3浓硫酸 △ O 2N — CH 3 | —NO 2| NO 2 +3H 2O 三硝基甲苯TNT,是一种淡黄色晶体,不溶于水;它是一种烈性炸药CH 3 | + Cl 2 光CH 2Cl | + HCl CH 3 | + Cl 2 Fe CH 3 |+ HCl —Cl 甲苯和氯气在光照和铁的催化条件下发生的取代反应不一样 CH 3 |+ 3H 2 催化剂△ CH 3|烃的衍生物的重要类别和主要化学性质:6. 卤代烃1取代反应溴乙烷的水解:C 2H 5—Br+NaOH C 2H 5—OH+NaBr2消去反应溴乙烷与NaOH 溶液反应:CH 3CH 2Br+NaOH CH 2=CH 2↑+NaBr+H 2O7. 醇1与钠反应乙醇与钠反应:2CH 3CH 2OH+2Na 2CH 3CH 2ONa+H 2↑乙醇钠2氧化反应①乙醇的燃烧;②2CH 3CH 2OH+O 2 2CH 3CHO+2H 2O 乙醛3取代反应乙醇与浓氢溴酸反应:CH 3CH 2OH+HBr CH 3CH 2Br+H 2O4消去反应CH 3CH 2OH H 2C=CH 2↑+H 2O 注意:该反应加热到140℃时,乙醇进行另一种脱水方式,生成乙醚; 2C 2H 5OH C 2H 5—O —C 2H 5+H 2O 乙醚5酯化反应CH 3CH 2—OH+C 2H 5—OH CH 3—C —OC 2H 5+H 2O 乙酸乙酯8. 苯酚苯酚是无色晶体,露置在空气中会因氧化显粉红色;苯酚具有特殊的气味,熔点43℃, 水中溶解度不大,易溶于有机溶剂;苯酚有毒,是一种重要的化工原料;H 2O醇△Cu 或Ag△浓硫酸140℃ 浓硫酸170℃ △浓硫酸△1苯酚的酸性苯酚钠 苯酚钠与CO 2反应:+CO 2+H 2O +NaHCO 32取代反应+3Br 2 ↓+3HBr三溴苯酚 3显色反应苯酚能和FeCl 3溶液反应,使溶液呈紫色 4缩聚反应9. 醛乙醛是无色无味,具有刺激性气味的液体,沸点20.8℃,密度比水小,易挥发;1加成反应 乙醛与氢气反应:CH 3—C —H+H 2 CH 3CH 2OH2氧化反应 乙醛与氧气反应:2CH 3—C —H+O 2 2CH 3COOH 乙酸乙醛的银镜反应:CH 3CHO +2AgNH 32OH CH 3COONH 4+2Ag↓+3NH 3+H 2O注意:硝酸银与氨水配制而成的银氨溶液中含有AgNH 32OH 氢氧化二氨合银, 这是一种弱氧化剂,可以氧化乙醛,生成Ag;有关制备的方程式:Ag ++NH 3·H 2O===AgOH↓++4NHAgOH+2NH 3·H 2O===AgNH 32++OH -+2H 2O乙醛还原氢氧化铜:CH 3CHO+2CuOH 2 CH 3COOH+Cu 2O↓+2H 2O10. 羧酸1乙酸的酸性乙酸的电离:CH 3COOH CH 3COO -+H+2酯化反应CH 3CH 2—OH+C 2H 5—OH CH 3—C —OC 2H 5+H 2O 乙酸乙酯注意:酸和醇起作用,生成酯和水的反应叫做酯化反应;11. 酯乙酸乙酯是一种带有香味的无色油状液体; 1水解反应—OH +NaOH +H 2O —ONa —ONa—OH—OH—BrBr — OH| Br |O || 催化剂△O || 催化剂△△△O ||浓硫酸 △无机酸催化剂酚醛树脂的制取CH 3COOC 2H 5+H 2O CH 3COOH+C 2H 5OH 2中和反应CH 3COOC 2H 5+NaOH CH 3COONa+C 2H 5OH注意:酚酯类碱水解如: 的水解 +2NaOH→CH 3COONa+ + H 2O其他1葡萄糖的银镜反应 CH 2OHCHOH 4CHO +2AgNH 32OH CH2OHCHOH 4COONH 4+2Ag +3NH 3+H 2O2蔗糖的水解 C 12H 22O 11+ H 2OC 6H 12O 6 + C 6H 12O 6蔗糖 葡萄糖 果糖 3麦芽糖的水解 C 12H 22O 11 + H 2O2C 6H 12O 6麦芽糖 葡萄糖 4淀粉的水解:5葡萄糖变酒精 CH 2OHCHOH 4CHO 2CH 3CH 2OH +2CO 26纤维素水解7油酸甘油酯的氢化8硬脂酸甘油酯水解 ①酸性条件②碱性条件皂化反应附加:官能团转化示意图CH 3COO - -ONa CH 3COO -烃三、有机合成的常用方法 1、官能团的引入:在有机化学中,卤代烃可谓烃及烃的衍生物的桥梁,只要能得到卤代烃,就可能得到诸如含有羟基、醛基、羧基、酯基等官能团的物质;此外,由于卤代烃可以和醇类相互转化,因此在有机合成中,如果能引入羟基,也和引入卤原子的效果一样,其他有机物都可以信手拈来;同时引入羟基和引入双键往往是改变碳原子骨架的捷径,因此官能团的引入着重总结羟基、卤原子、双键的引入; 1引入羟基-OH①醇羟基的引入:a.烯烃与水加成;b.卤代烃碱性水解;c.醛酮与氢气加成;d.酯的水解; ②酚羟基的引入:酚钠盐过渡中通入CO 2 、的碱性水解等;③羧羟基的引入:醛氧化为酸被新制CuOH 2悬浊液或银氨溶液氧化、酯的水解等; 2引入卤原子:a.烃与X 2取代;b.不饱和烃与HX 或X 2加成;c.醇与HX 取代; 3引入双键:a.某些醇或卤代烃的消去引入C=C ;b.醇的氧化引入C=O; 2、官能团的消除1通过加成反应消除不饱和键;2通过消去、氧化或酯化等消除羟基-OH 3通过加成或氧化等消除醛基—CHO 4通过取代或消去消除卤素原子; 3、官能团间的衍变①利用官能团的衍生关系进行衍变,如伯醇[]−→−O 醛[]−→−O 羧酸;②通过某种化学途径使一个官能团变为两个,如一元醇经过消去、加成、取代变成二元醇如CH 3CH 2OH OH 2-−−→−消去CH 2=CH 22Cl +−−→−加成Cl —CH 2—CH 2—Cl−−→−水解HO —CH 2—CH 2—OH; ③通过某种手段,改变官能团位置;如丙醇 丙烯 2-丙醇 4、有机化学中碳链的增减方法 1增长碳链的方法①加聚反应:如nCH 3CH=CH 2消去加成H 2O一定条件下催化剂②缩聚反应:如③加成反应:如④酯化反应:如⑤卤代烃的取代反应:如⑥醛酮与HCN、ROH的加成反应:如2减短碳链的方法①氧化反应;包括燃烧,烯烃、炔烃的部分氧化,丁烷直接氧化成乙酸,某些苯的同系物氧化成苯甲酸,羧酸钠盐在碱石灰条件下的脱羧反应;②水解反应;主要包括酯的水解、蛋白质的水解和多糖的水解;5、常见有机官能团的保护1物质检验中碳碳双键与醛基的先后处理检验碳碳双键时,当有机物中含有醛基、碳碳双键等多个官能团时,可以先用弱氧化剂,如银氨溶液、新制的CuOH2悬浊液等氧化醛基,再用溴水、酸性KMnO4溶液进行碳碳双键的检验;2物质合成中酚羟基的保护由于酚羟基易被氧化,在有机合成中,如果需要用氧化剂进行氧化时,经常先将酚羟基通过酯化反应,使其成为酯而被保护,待氧化过程完成后,再通过水解反应,使酚羟基恢复;也可用NaOH处理成-ONa,再加H+复原;3为防止醇-OH被氧化可先将其酯化;4芳香胺-NH2的保护:转化为酰胺保护氨基;1.能使溴水Br2/H2O褪色的物质1有机物①通过加成反应使之褪色:含有、—C≡C—的不饱和化合物②通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀;③通过氧化反应使之褪色:含有—CHO醛基的有机物有水参加反应注意:纯净的只含有—CHO醛基的有机物不能使溴的四氯化碳溶液褪色④通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯2无机物①通过与碱发生歧化反应3Br2 + 6OH- =5Br- + BrO3- + 3H2O或Br2 + 2OH- = Br- + BrO- + H2O②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+2.能使酸性高锰酸钾溶液KMnO4/H+褪色的物质1有机物:含有、—C≡C—、—OH较慢、—CHO的物质与苯环相连的侧链碳碳上有氢原子的苯的同系物与苯不反应2无机物:与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+ 3.与Na反应的有机物:含有—OH、—COOH的有机物与NaOH反应的有机物:常温下,易与含有酚羟基...、—COOH的有机物反应加热时,能与卤代烃、酯反应取代反应与Na2CO3反应的有机物:含有酚.羟基的有机物反应生成酚钠和NaHCO3;含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;含有—SO3H的有机物反应生成磺酸钠并放出CO2气体;与NaHCO3反应的有机物:含有-COOH、-SO3H的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2; 4.银镜反应的有机物1发生银镜反应的有机物:含有—CHO的物质:醛、甲酸、甲酸盐、甲酸酯、还原性糖葡萄糖、麦芽糖等2银氨溶液AgNH32OH多伦试剂的配制:向一定量2%的AgNO3溶液中逐滴加入2%的稀氨水至刚刚产生的沉淀恰好完全溶解消失;3实验现象:①反应液由澄清变成灰黑色浑浊;②试管内壁有银白色金属析出4有关反应方程式:AgNO3 + NH3·H2O == AgOH↓ + NH4NO3AgOH + 2NH3·H2O == AgNH32OH + 2H2O银镜反应的一般通式:RCHO + 2AgNH32OH 2 Ag↓+ RCOONH4 + 3NH3 + H2O悬浊液斐林试剂的反应5.与新制CuOH21有机物:羧酸中和、甲酸先中和,后氧化、醛、还原性糖葡萄糖、麦芽糖、甘油等多羟基化合物;2斐林试剂的配制:向一定量10%的NaOH溶液中,滴加几滴2%的CuSO4溶液,得到蓝色絮状悬浊液;3实验现象:①若有机物只有醛基-CHO,则滴入新制的CuOH2悬浊液中,常温时无变化,加热煮沸后有砖红色沉淀生成②若有机物为多羟基醛如葡萄糖,则滴入新制的氢氧化铜悬浊液中,常温时溶解变成绛蓝色溶液,加热煮沸后有砖红色沉淀生成4有关反应方程式:2NaOH + CuSO4 == CuOH2↓+ Na2SO4RCHO + 2CuOH2RCOOH + Cu2O↓+ 2H2OHCHO + 4CuOH2CO2 + 2Cu2O↓+ 5H2O巩固练习:1,乙酸苯甲酯可用作茉莉、白兰、月下香等香精的调合香料;它可以用甲苯和乙醇为原料进行人工合成;合成路线:1C 的结构简式为__________________________;2反应②、③的反应类型为_______________,_______________; 3甲苯的一氯代物有 种;4写出反应①的化学方程式_______________________________;5为了提高乙酸苯甲酯的产率应采取的措施是写一项 ; 2,下面是一个合成反应的流程图A BCH 2=CH 2 BrCH 2-CH 2Br C请写出:1.中间产物A 、B 、C 的结构简式:A .__________B . ________ C .____________ 2.①、②、③、④各步反应所需用的反应试剂及各步反应的类型①________、_______②__________、_______③________、______④________、______3,分子式为C 12H 14O 2的F 有机物广泛用于香精的调香剂;为了合成该物质,某实验室的科技人员设计了下列合成路线:1A 物质在核磁共振氢谱中能呈现 种峰;峰面积比为 2C 物质的官能团名称3上述合成路线中属于取代反应的是 填编号;4写出反应④、⑤、⑥的化学方程式:④ ⑤ ⑥5F 有多种同分异构体,请写出符合下列条件的所有结构简式:①属于芳香族化合物,且含有与F 相同的官能团;②苯环上有两个取代基,且苯环上的一氯代物只有两种;③其中一个取代基为-CH 2COOCH 3; 4,菠萝酯是一种具有菠萝香气的食用香料,是化合物甲与苯氧乙酸发生酯化反应的产物;⑴甲一定含有的官能团的名称是 ;⑵5.8g 甲完全燃烧可产生0.3mol CO 2和0.3 mol H 2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是 ;⑶苯氧乙酸有多种酯类的同分异构体,其中能与FeCl 3溶液发生显色反应,且有2种一硝基取代物的同分异构体是写出任意2种的结构简式 ;CH CH 3Cl 2 光 ① CH 2OH CH 2OH ② 催化剂 CHO CHO O 2 催化剂 ③ △ NaOH 水溶液 ④COOCH 2CH 2OH COOCH 2CH 2OH⑷已知:R-CH 2-COOH 2Cl −−−→催化剂R-ONa 'Cl-R∆−−−→R-O-R′R -、R′-代表烃基 菠萝酯的合成路线如下:①试剂X 不可选用的是选填字母 ;a. CH 3COONa 溶液b. NaOH 溶液c. NaHCO 3溶液d.Na②丙的结构简式是 ,反应II 的反应类型是 ; ③反应IV 的化学方程式是 ; 5,以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G;OOAF E 2△①②③△浓硫酸△C 13H 16O 42C 2H 4C 4H 8O 21E 是一种石油裂解气,能使酸性高锰酸钾溶液褪色;同温同压下,E 的密度是H 2的21倍;核磁共振氢谱显示E 有3种不同化学环境的氢原子,其个数比为1:2:3;E 的结构简式为 ;2反应类型:① ,④ ; 3反应条件:③ ,⑥ ; 4反应②、③的目的是 ; 5反应⑤的化学方程式为 ;6B 被氧化成C 的过程中会有中间产物生成,该中间产物可能是 写出一种物质的结构简式,检验该物质存在的试剂是 ;7G 的结构简式为 ;。
高二有机物的所有化学方程式

甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
CH4→C+2H2(条件为高温高压,催化剂)甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HClCH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HClCHCl3+Cl2→CCl4+HCl(条件都为光照。
)实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br乙烯和水CH2=CH2+H20→CH3CH2OH(条件为催化剂)乙烯和氯化氢CH2=CH2+HCl→CH3-CH2Cl乙烯和氢气CH2=CH2+H2→CH3-CH3 (条件为催化剂)乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O(条件为加热,浓H2SO4)乙炔燃烧C2H2+3O2→2CO2+H2O(条件为点燃)乙炔和溴水C2H2+2Br2→C2H2Br4乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2乙炔和氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6(条件为催化剂)实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。
CaCO3 === CaO + CO2 2CaO+5C===2CaC2+CO2CaC2+2H2O→C2H2+Ca(OH)2C+H2O===CO+H2-----高温C2H2+H2→C2H4 ----乙炔加成生成乙烯C2H4可聚合苯燃烧2C6H6+15O2→12CO2+6H2O(条件为点燃)苯和液溴的取代C6H6+Br2→C6H5Br+HBr苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O(条件为浓硫酸)苯和氢气C6H6+3H2→C6H12(条件为催化剂)乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O(条件为点燃)乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)乙醇发生消去反应的方程式CH3CH2OH→CH2=CH2+H2O(条件为浓硫酸 170摄氏度)两分子乙醇发生分子间脱水2CH3CH2OH→C H3CH2OCH2CH3+H2O (条件为催化剂浓硫酸 140摄氏度)乙醇和乙酸发生酯化反应的方程式CH3COOH+C2H5OH→CH3COOC2H5+H2O乙酸和镁Mg+2CH3COOH→(CH3COO)2Mg+H2乙酸和氧化钙2CH3COOH+CaO→(CH3CH2)2Ca+H2O乙酸和氢氧化钠CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH乙酸和碳酸钠Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑甲醛和新制的氢氧化铜HCHO+4Cu(OH)2→2Cu2O+CO2↑+5H2O乙醛和新制的氢氧化铜CH3CHO+2Cu→Cu2O(沉淀)+CH3COOH+2H2O乙醛氧化为乙酸2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)烯烃是指含有C=C键的碳氢化合物。
完美版)高中有机化学方程式总结

完美版)高中有机化学方程式总结高中有机化学方程式总结一、烃1.甲烷烷烃通式:CnH2n-21)氧化反应甲烷的燃烧:CH4 + 2O2 → CO2 + 2H2O甲烷不能使酸性高锰酸钾溶液及溴水褪色。
2)取代反应一氯甲烷:CH4 + Cl2 光→ CH3Cl + HCl二氯甲烷:CH3Cl + Cl2 光→ CH2Cl2 + HCl三氯甲烷:CH2Cl2 + Cl2 光→ CHCl3 + HCl(CHCl3又叫氯仿)四氯化碳:CHCl3 + Cl2 光→ CCl4 + HCl2.乙烯乙烯的制取:CH3CH2OH + 浓硫酸 170℃ → H2C=CH2 ↑+H2O烯烃通式:XXX1)氧化反应乙烯的燃烧:H2C=CH2 + 3O2 → 2CO2 + 2H2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
2)加成反应与溴水加成:H2C=CH2 + Br2 → CH2Br—CH2Br与氢气加成:H2C=CH2 + H2 催化剂→ CH3CH3与氯化氢加成:XXX + HCl △ → CH3CH2Cl与水加成:XXX + H2O → CH3CH2OH3)聚合反应乙烯加聚,生成聚乙烯:nHC=CH2 一定条件→ -(-CH2-CH2-)n-3.乙炔乙炔的制取:CaCO2 + 2H2O → HC CH↑+Ca(OH)21)氧化反应乙炔的燃烧:HC CH + 5O2 点燃→ 4CO2 + 2H2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
2)加成反应与溴水加成:HC CH + Br2 → HC=CHBrBr →CHBr=CHBr + Br2与氢气加成:H2C=CH2 + H2 催化剂→ CH3CH3与氯化氢加成:HC CH + HCl 催化剂→ CH2=CHCl3)聚合反应氯乙烯加聚,得到聚氯乙烯:nCH2=CHClCH2—CHn乙炔加聚,得到聚乙炔:nHC CH 一定条件→ -(-C≡C-)n-4.苯苯的同系物通式:CnH2n-61)氧化反应苯的燃烧:2C6H6 + 15O2 点燃→ 12CO2 + 6H2O甲苯不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色。
必修二有机物化学方程式

必修二有机物化学方程式有机物化学方程式1.甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)2.甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
CH4→C+2H2(条件为高温高压,催化剂)3.甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HCl CH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HCl CHCl3+Cl2→CCl4+HCl (条件都为光照。
)4.实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)5.乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)6.乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br7.乙烯和水CH2=CH2+H2O→CH3CH2OH (条件为催化剂)8.乙烯和氯化氢CH2=CH2+HCl→CH3-CH2Cl9.乙烯和氢气CH2=CH2+H2→CH3-CH3(条件为催化剂)10.乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)11.氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)12.实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)13.乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃)14.乙炔和溴水C2H2+2Br2→C2H2Br415.乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl216.乙炔和氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6(条件为催化剂)17.实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑18.以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。
CaCO3 === CaO + CO22CaO+5C===2CaC2+CO2CaC2+2H2O→C2H2+Ca(OH)2C+H2O===CO+H2-----高温C2H2+H2→C2H4 ----乙炔加成生成乙烯C2H4可聚合19.苯燃烧2C6H6+15O2→12CO2+6H2O (条件为点燃)20.苯和液溴的取代C6H6+Br2→C6H5Br+HBr21.苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)22.苯和氢气C6H6+3H2→C6H12 (条件为催化剂)23.乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃)24.乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)25.乙醇发生消去反应的方程式CH3CH2OH→CH2=C H2+H2O (条件为浓硫酸170摄氏度)26.两分子乙醇发生分子间脱水2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸140摄氏度) 27.乙醇和乙酸发生酯化反应的方程式CH3COOH+C2H5OH→CH3COOC2H5+H2O28.乙酸和镁Mg+2CH3COOH→(CH3COO)2Mg+H229.乙酸和氧化钙2CH3COOH+CaO→(CH3CH2)2Ca+H2O30.乙酸和氢氧化钠CH3COOCH2CH3+NaOH→CH3C OONa+CH3CH2OH31.乙酸和碳酸钠Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑32.甲醛和新制的氢氧化铜HCHO+4Cu(OH)2→2Cu2O+CO2↑+5H2O33.乙醛和新制的氢氧化铜CH3CHO+2CU(OH)2=CH3COOH+CU2O+2H2O34.乙醛氧化为乙酸2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)一.烯烃是指含有C=C键的碳氢化合物。
(完整版)高中有机化学方程式大全.docx

高中有机化学方程式大全1. CH 4 + Cl 2光照CH 3Cl + HCl 2. CH Cl + Cl光照 + HCl2CH Cl2323. CH 2Cl + Cl 2 光照 CHCl 3 + HCl4. CHCl 3 + Cl 2光照CCl 4+ HCl4 高温C +2H 25. CH6. C 16H 34 催化剂C 8H 18 + C 8H 16加热、加压CaO 7. CH 3COONa + NaOHCH 4 ↑+ Na 2CO 3△8. CH = CH 2+ Br2CH 2 Br —CH Br229.CH =CH催化剂CH CH OH2+ H O223210. CH 2 = CH 2 + HBr催化剂CH 3—CH 2Br△催化剂CH 3—CH 311. CH 2 = CH 2 + H 2△22 催化剂 22 ] n12. nCH = CH[ CH —CH催化剂13. nCH 2=CH-CH=CH 2[CH 2-CH=CH-CH 2] n催化剂2CH 3CHO 14. 2CH 2 = CH 2 + O 215. CH ≡CH + Br 2CHBr = CHBr 16. CHBr = CHBr+ Br 2CHBr 2- CHBr 2催化剂17. CH ≡CH + HCl△H 2C = CHCl18. nCH = CH[ CH -CH ] n22Cl Cl19. CH ≡CH + H 2O 催化剂 CH 3CHO20. CaC 2 + 2H 2OCH ≡CH ↑+ Ca(OH)2催化剂21.+ Br 2Br + HBr浓硫酸22.+ HO -NO 2NO 2 +H 2O△23. + HO -SO 3H △SO 3H+H 2O24.+ 3H2催化剂△CH3CH325.+3HO-NO2催化剂O2N NO2+3H O226.3CH≡ CH→NO227. CH3CH 2Br + H2 O NaOH CH 3CH2OH + HBr28. CH CH Br + NaOH H 2O CH3CH OH + NaBr32229. CH3CH 2Br+ NaOH醇CH2 = CH2 + NaBr +H 2O△30.2CH3CH 2OH+2Na2CH3CH2ONa + H2↑31.322催化剂32△32. CH CH OH浓硫酸CH2= CH↑+ H O32170℃2233.C2H5OH+C2H5OH 浓硫酸C2H5OC2H5+H2O 140℃34.OH+NaOH ONa+H O235.OH+H2O-O +H3O+36.ONa+H2O+CO2OH+ NaHCO3OH OHBr Br37.+3Br2↓+3HBrBr38. CH CHO + H催化剂CH OH233239.2CH3CHO + O2催化剂2CH3COOH △40. CH3CHO+2Ag(NH 3)2 OH △CH3COONH 4+2Ag↓ +3NH3+H2O412△CH3COOH+Cu2O↓+2H 2OCH3 CHO+2Cu(OH)42.2CH3COOH+2Na2CH 3COONa+H2↑43.2CH COOH+Na CO32CH COONa+H O+CO ↑3232244. CH 3COOH+NaHCO 3CH 3COONa+H 2O+CO 2↑45. CH3COOH + NaOH CH 3COONa + H2O46. 2CH 3COOH + Cu(OH)2(CH COO) 2Cu + 2H O3247.CH COOH+CH3CH OH 浓硫酸CH COOCH 2CH 3+H O32 3248. CH COOCH CH△CH COONa+CH CH OH+NaOH323 3 3 2 49. nOHCH 2CH 2COO H → [ OCH 2CH 2C ] n +H 2O50. C 6 H 12O 6 (s) + 6O 2 (g)6CO 2 (g) + 6H 2O (l)51. C 6 H 12O 6 催化剂 2CH 3CH 2OH + 2CO 252. C 12H 22O 11+H 2O催化剂C 6H 12O 6+ C 6H 12O 6蔗糖葡萄糖果糖53. C 12H 22O 11 + H 2O催化剂2C 6H 12O 6麦芽唐葡萄糖54. (C 6H 10O 5)n + nH 2 O催化剂n C 6H 12O 6淀粉葡萄糖55. (C 6H 10O 5)n + nH 2 O 催化剂△纤维素56.C 17H 33COO-CH 2 C 17H 33COO-CH +3H C 17H 33COO-CH 257. C 17H 35COO-CH 2C 17H 35COO-CH +3NaOH C 17H 35COO-CH 2 n C 6H 12O 6葡萄糖C 17H 35COO-CH 2C 17H 35COO-CHC 17H 35COO-CH 2CH 2-OH3C 17H 35COONa+ CH-OHOOCH 2-OH58. CH 2OHCOOH+CH 2OH COOHC — C浓硫酸OO2△光CH 2- CH 21.CH 4Cl 2HClCH 3ClCH 3ClCl 2光HClCH 2 Cl 2 2.3.4.催化剂2 加热、加压5.6.7.8.CH 2CH CH CH 2Br29.10.11.12.13.14.15.16.17.HOCH 2 (CHOH ) 4 CHO2Ag (NH 3 ) 2 OHHOCH 2 (CHOH )4 COONH 42Ag3NH 3H 2O18.19.20.21.高中有机化学知识点总结1.需水浴加热的反应有:(1 )、银镜反应( 2)、乙酸乙酯的水解( 3 )苯的硝化( 4)糖的水解(5 )、酚醛树脂的制取( 6)固体溶解度的测定凡是在不高于 100 ℃的条件下反应,均可用水浴加热,其优点:温度变化平稳,不会大起大落,有利于反应的进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8.苯酚
苯酚是无色晶体,露置在空气中会因氧化显粉红色。苯酚具有特殊的气味,熔点
43℃,水中溶解度不大,易溶于有机溶剂。苯酚有毒,是一种重要的化工原料。
(1)苯酚的酸性
(苯酚钠)
苯酚(俗称石炭酸)的电离:
+H2O +H3O+
苯酚钠与CO2反应:
+CO2+H2O +NaHCO3
乙醛还原氢氧化铜:CH3CHO+2Cu(OH)2CH3COOH+Cu2O+2H2O
10.乙酸
(1)乙酸的酸性
乙酸的电离:CH3COOH CH3COO-+H+
(2)酯化反应
CH3—C—OH+C2H5—OH CH3—C—OC2H5+H2O(乙酸乙酯)
注意:酸和醇起作用,生成酯和水的反应叫做酯化反应。
11.乙酸乙酯
乙烯可以使酸性高锰酸钾溶液色,发生氧化反应。
(2)加成反应
与溴水加成:H2C=CH2+Br2CH2Br—CH2Br
与氢气加成:H2C=CH2+H2CH3CH3
与氯化氢加成:H2C=CH2+HClCH3CH2Cl
与水加成:H2C=CH2+H2OCH3CH2OH
(3)聚合反应
乙烯加聚,生成聚乙烯:nH2C=CH2n
3.乙炔
乙炔的制取:CaC2+2H2O HC CH↑+Ca(OH)2
炔烃的通式:CnH2n-2
(1)氧化反应
乙炔的燃烧:HC CH+5O24CO2+2H2O
乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应
与溴水加成:HC CH+Br2HC=CH
Br
CHBr=CHBr+Br2CHBr2—CHBr2
7.乙醇
(1)与钠反应
乙醇与钠反应:2CH3CH2OH+2Na 2CH3CH2ONa+H2↑(乙醇钠)
(2)氧化反应
乙醇的燃烧:2CH3CH2OH+O22CH3CHO+2H2O(乙醛)
(3)消去反应
乙醇在浓硫酸做催化剂的条件下,加热到170℃生成乙烯。
注意:该反应加热到140℃时,乙醇进行另一种脱水方式,生成乙醚。
键,有极性;—OH
与链烃基直接相连
1.与钠反应,生成醇钠并放出氢气;2.氧化反应:O2:
生成CO2和H2O;氧化剂:生成乙醛;3.脱水反应:
140℃:乙醚;170℃:乙烯;4.酯化反应。
酚
苯酚
—OH直接与苯环相
连
1.弱酸性:与NaOH溶液中和;
2.取代反应:与浓溴水反应,生成三溴苯酚白色沉淀;
3.显色反应:与铁盐(FeCl3)反应,生成紫色物质
(2)取代反应
+3Br2↓+3HBr
(三溴苯酚)
(3)显色反应
苯酚能和FeCl3溶液反应,使溶液呈紫色。
9.乙醛
乙醛是无色无味,具有刺激性气味的液体,沸点20.8℃,密度比水小,易挥发。
(1)加成反应
乙醛与氢气反应:CH3—C—H+H2CH3CH2OH
(2)氧化反应
乙醛与氧气反应:2CH3—C—H+O22CH3COOH(乙酸)
乙酸乙酯是一种带有香味的物色油状液体。
(1)水解反应
CH3COOC2H5+H2O CH3COOH+C2H5OH
(2)中和反应
CH3COOC2H5+NaOH CH3COONa+C2H5OH
附加:烃的衍生物的转化
R—C—OR’
乙酸乙酯
CH3COOC2H5
分子中RCO—和OR’
之间容易断裂
水解反应:生成相应的羧酸和醇
6.溴乙烷
纯净的溴乙烷是无色液体,沸点38.4℃,密度比水大。
(1)取代反应
溴乙烷的水解:C2H5—Br+H2OC2H5—OH+HBr
(2)消去反应
溴乙烷与NaOH溶液反应:CH3CH2Br+NaOHCH2=CH2↑+NaBr+H2O
甲苯的燃烧:C7H8+9O27CO2+4H2O
甲苯不能使溴水褪色,但可以使酸性高锰酸钾溶液褪色。
(2)取代反应
甲苯硝化反应生成2,4,6-三硝基甲苯,简称三硝基甲苯,又叫梯恩梯(TNT),
是一种淡黄色晶体,不溶于水。它是一种烈性炸药,广泛用于国防、开矿等。
注意:甲苯在光照条件下发生侧链的取代,而在催化剂条件下发生苯环上的取代。
与氢气加成:HC CH+H2H2C=CH2
与氯化氢加成:HC CH+HCl CH2=CHCl
(3)聚合反应
氯乙烯加聚,得到聚氯乙烯:nCH2=CHCln
乙炔加聚,得到聚乙炔:nHC CHn
4.苯
苯的同系物通式:CnH2n-6
(1)氧化反应
苯的燃烧:2C6H6+15O212CO2+6H2O
苯不能使溴水和酸性高锰酸钾溶液褪色。
(3)加成反应
(甲基环己烷)
二、烃的衍生物
烃的衍生物的重要类别和主要化学性质:
类别
通式
代表性物质
分子结构特点
主要化学性质
卤代烃
R—X
溴乙烷
C2H5Br
C—X键有极性,易
断裂
1.取代反应:与NaOH溶液发生取代反应,生成醇;
2.消去反应:与强碱的醇溶液共热,生成烯烃。
醇
R—OH
乙醇
C2H5OH
有C—O键和O—H
二氯甲烷:CH3Cl+Cl2CH2Cl2+HCl
三氯甲烷:CH2Cl2+Cl2CHCl3+HCl(CHCl3又叫氯仿)
四氯化碳:CHCl3+Cl2CCl4+HCl
(3)分解反应
甲烷分解:CH4C+2H2
2.乙烯
乙烯的制取:CH3CH2OHH2C=CH2↑+H2O
烯烃通式:CnH2n
(1)氧化反应
乙烯的燃烧:H2C=CH2+3O22CO2+2H2O
乙醛的银镜反应:
CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag+3NH3+H2O(乙酸铵)
注意:硝酸银与氨水配制而成的银氨溶液中含有Ag(NH3)2OH(氢氧化二氨合银),
这是一种弱氧化剂,可以氧化乙醛,生成Ag。有关制备的方程式:
Ag++NH3·H2O===AgOH↓+
AgOH+2NH3·H2O===[Ag(NH3)2]++OH-+2H2O
高中化学方程式总结
【编辑】Crazy Urus
【日期】2009-12-20
第二部分 有机物
一、烃
1.甲烷
甲烷的制取:CH3COONa+NaOHNa2CO3+CH4↑
烷烃通式:CnH2n-2
(1)氧化反应
甲烷的燃烧:CH4+2O2CO2+2H2O
甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应
一氯甲烷:CH4+Cl2CH3Cl+HCl
醛
R—C—H
乙醛
CH3—C—H
C=O双键有极性,
具有不饱和性
1.加成反应:用Ni作催化剂,与氢加成,生成乙醇;
2.氧化反应:能被弱氧化剂氧化成羧酸(如银镜反应、
还原氢氧化铜)。
羧酸
R—C—OH
乙酸
CH3—C—OH
受C=O影响,O—H
能够电离,产生H+
1.具有酸的通性;
2.酯化反应:与醇反应生成酯。
酯
(2)取代反应
①苯与溴反应
(溴苯)
②硝化反应
+HO—NO2+H2O
(硝基苯)
苯硝化反应生成硝基苯,它是一种带有苦杏仁味、无色油状液体,有毒。
③磺化反应
+HO—SO3H +H2O
(苯磺酸)
(3)加成反应
(环己烷)
苯还可以和氯气在紫外光照射下发生加成反应,生成C6H6Cl6(剧毒农药)。
5.甲苯
(1)氧化反应
