华师物化实验报告-液相平衡常数测定
液相平衡常数的测定

液相平衡常数的测定液相平衡常数的测定是化学热力学研究中的重要方面之一。
它指的是一种化学反应中产物和反应物之间在液相中达到平衡时它们之间的浓度或活度比值。
液相平衡常数(Kc)是描述一定温度和压力下化学反应平衡时反应物和生成物浓度比值的一种评价指标。
在化学反应中,反应物与生成物在平衡状态下的浓度比值恒定,这个比值就是液相平衡常数。
在本文中,我们将介绍液相平衡常数的测量方法和其实验过程。
1. 理论基础液相平衡常数(Kc)是一种描述反应在液相中的平衡程度的物理量。
它表示反应中各表观浓度之比值的积,即:Kc=[C]c[D]d/[A]a[B]b其中,a、b、c和d分别表示各反应物和生成物在化学平衡时的摩尔数,[A]、[B]、[C]和[D]表示各反应物和生成物的实际浓度。
反应物和生成物之间的化学反应达到平衡时,Kc的值不随时间而改变。
换句话说,反应物和生成物的浓度比例是一个求定比例的平衡状态而非一种实时反应,这些下回再详细述。
Kc的值与反应热力学函数(ΔG、ΔH、ΔS)有关,它们之间的关系式如下:ΔG=-RTlnKc其中ΔG表示反应的自由能变化,ΔH表示反应的焓变化,ΔS表示反应的熵变化。
R为气体常数,T为温度,Kc为液相平衡常数。
2. 实验设计本实验中,我们将选取一种酸(H+)和碱(OH)反应制备水。
反应式为:H+(aq)+OH-(aq)=H2O反应平衡常数可以由反应物和生成物之间的摩尔比例关系得出。
首先,我们准备一定量的酸和碱,再用洗净的滴定管逐滴加入水中,用酸碱滴定法测定其浓度。
我们可以在不同温度下进行实验来测定液相平衡常数的值。
在本实验中,我们使用两种方法来测定液相平衡常数:酸碱滴定法和光度法。
3. 实验步骤3.1 酸碱滴定法(1)准备一定浓度的盐酸和氢氧化钠溶液。
(2)取紫色试剂(酚酞)标定溶液,将其中的一滴滴入pH为7的背景溶液中,转变为红色显示溶液中的氢离子浓度。
(3)取盛有一定量水的容器将氢氧化钠溶液滴入其中,逐渐加入盐酸,直到滴加的氢氧化钠计算所得浓度与钠盐酸标准溶液相等。
大学化学实验-液相反应平衡常数

大学化学实验-液相反应平衡常数【目的要求】1.用分光光度法测定弱电解质的电离常数。
2.掌握分光光度法测定甲基红电离常数的基本原理。
3.掌握分光光度计及pH 计的正确使用方法。
【实验原理】弱电解质的电离常数测定方法很多,如电导法、电位法、分光光度法等。
本实验测定电解质(甲基红)的电离常数,是根据甲基红在电离前后具有不同颜色和对单色光的吸收特性,借助于分光光度法的原理,测定其电离常数,甲基红在溶液中的电离可表示为:简写为:HMR H ++MR -酸式碱式则其电离平衡常数K 表示为:(1) 或(2)[HMR]]][MR [H -+=C K [HMR]][MR log pH p --=K由(2)式可知,通过测定甲基红溶液的pH值,再根据分光光度法(多组分测定方法)测得[MR-]和[HMR]值,即可求得p K值。
根据朗伯-比耳(Lanbert-Bear)定律,溶液对单色光的吸收遵守下列关系式:(3) 式中,A为吸光度;I/I0为透光率T;C为溶液浓度;l为溶液的厚度;k为消光系数。
溶液中如含有一种组分,其对不同波长的单色光的吸收程度,如以波长(λ)为横坐标,吸光度(A)为纵坐标可得一条曲线,如图2-12-1中单组分a和单组分b的曲线均称为吸收曲线,亦称吸收光谱曲线。
根据公式(3),当吸收槽长度一定时,则:A a=k a C a(4)A b=k b C b(5) 如在该波长时,溶液遵守朗伯-比耳定律,可选用此波长进行单组分的测定。
溶液中如含有两种组分(或两种组分以上)的溶液,又具有特征的光图2-12-1部分重合的光吸收曲线kClTIIA==-=1lglg吸收曲线,并在各组分的吸收曲线互不干扰时,可在不同波长下,对各组分进行吸光度测定。
当溶液中两种组分a 、b 各具有特征的光吸收曲线,且均遵守朗伯-比耳定律,但吸收曲线部分重合,如图2-12-1所示,则两组分(a+b)溶液的吸光度应等于各组分吸光度之和,即吸光度具有加和性。
化学平衡常数的测定实验报告

化学平衡常数的测定实验报告一、实验目的1、深入理解化学平衡的概念以及化学平衡常数的意义。
2、掌握化学平衡常数的测定方法。
3、学会使用化学分析方法来确定反应物和生成物的浓度。
二、实验原理对于一个可逆反应,如 aA + bB ⇌ cC + dD,在一定温度下达到化学平衡时,其平衡常数表达式为:K = C^cD^d / A^aB^b ,其中 A、B、C、D 分别为各物质的平衡浓度,a、b、c、d 为相应的化学计量系数。
在本实验中,我们选择一个特定的化学反应,通过测定反应达到平衡时各物质的浓度,计算出化学平衡常数。
三、实验仪器与试剂1、仪器分光光度计容量瓶(250 mL、500 mL)移液管(10 mL、25 mL)锥形瓶(250 mL)玻璃棒烧杯(500 mL、1000 mL)电子天平2、试剂铁离子(Fe³⁺)标准溶液硫氰酸根离子(SCN⁻)标准溶液盐酸溶液(1 mol/L)四、实验步骤1、配制溶液配制 00020 mol/L 的 Fe³⁺溶液 250 mL:用电子天平准确称取一定质量的 FeCl₃·6H₂O 固体,溶解于适量的蒸馏水中,转移至 250 mL 容量瓶中,定容至刻度线,摇匀。
配制 00020 mol/L 的 SCN⁻溶液 250 mL:同样的方法称取一定质量的 KSCN 固体,溶解、定容。
2、混合反应取 1000 mL 00020 mol/L 的 Fe³⁺溶液和 1000 mL 00020 mol/L 的SCN⁻溶液,放入 250 mL 锥形瓶中,再加入 1000 mL 1 mol/L 的盐酸溶液,摇匀。
3、测定吸光度反应开始后,每隔一定时间(如 5 分钟),用移液管吸取 200 mL反应液,放入 25 mL 容量瓶中,用蒸馏水定容至刻度线,摇匀。
以蒸馏水为参比,在分光光度计上测定该溶液在特定波长(如 460 nm)下的吸光度。
4、绘制标准曲线分别配制一系列不同浓度的 Fe(SCN)³⁺标准溶液。
平衡常数的测定实验报告

平衡常数的测定实验报告平衡常数的测定实验报告引言:平衡常数是化学反应中一个重要的物理化学参数,它反映了反应物和产物之间的相对浓度关系。
准确测定平衡常数对于理解反应机理、优化反应条件以及预测反应性质具有重要意义。
本实验旨在通过实际操作,测定一种化学反应的平衡常数,并探讨影响平衡常数的因素。
实验原理:在化学反应达到平衡时,反应物和产物之间的浓度比例将保持不变。
平衡常数Kc定义为反应物浓度的乘积与产物浓度的乘积之比。
对于一般的化学反应aA + bB ⇌ cC + dD,平衡常数的表达式为Kc = [C]^c[D]^d / [A]^a[B]^b。
实验中,我们将通过测量反应物和产物的浓度,计算出平衡常数Kc的值。
实验步骤:1. 准备工作:清洗实验器材,配制所需溶液。
2. 实验操作:取一定量的反应物A和B,放入反应容器中,加入适量的溶剂,使反应物完全溶解。
3. 开始反应:在恒温条件下,加入催化剂或改变反应条件,使反应开始。
4. 反应过程监测:定时取样,通过适当的分析方法(如色谱法、滴定法等)测定反应物和产物的浓度。
5. 计算平衡常数:根据测定的浓度数据,计算平衡常数Kc的值。
实验结果:根据实验数据,我们得到反应物A和B的浓度分别为[A]和[B],产物C和D的浓度分别为[C]和[D]。
代入平衡常数的表达式Kc = [C]^c[D]^d / [A]^a[B]^b,即可计算出平衡常数Kc的值。
讨论与分析:1. 影响平衡常数的因素:温度是影响平衡常数的重要因素之一。
一般来说,温度升高会使平衡常数增大,反应向产物方向偏移;而温度降低则会使平衡常数减小,反应向反应物方向偏移。
此外,压力、浓度和催化剂等因素也会对平衡常数产生影响。
2. 实验误差与改进:实验中可能存在的误差包括仪器误差、操作误差以及反应条件控制不准确等。
为减小误差,可以采用更精确的仪器设备,严格控制实验条件,并进行多次实验取平均值。
3. 应用与意义:平衡常数的测定对于理解反应机理、优化反应条件以及预测反应性质具有重要意义。
液液平衡测定实验报告

液液平衡测定实验报告液液平衡测定实验报告引言液液平衡测定是一种常见的实验方法,用于确定混合液中组分的相对含量。
本实验旨在通过实际操作,探索液液平衡测定的原理和方法,并通过实验结果验证理论计算的准确性。
实验步骤1. 实验前准备在实验开始之前,我们需要准备好实验所需的设备和试剂。
实验所需的设备包括烧杯、滴管、试管、酒精灯等。
实验所需的试剂包括水、乙醇等。
2. 实验操作首先,我们将一定量的水和乙醇分别倒入两个烧杯中,并在每个烧杯中加入一根玻璃棒,用于搅拌混合液。
接下来,我们将两个烧杯中的液体分别加热至沸腾,并保持沸腾状态。
同时,我们将一个试管倒置于其中一个烧杯中,使试管内的空气被排出。
然后,我们将试管迅速倒置放入另一个烧杯中,使试管内的液体与烧杯中的液体接触。
在试管倒置后,我们可以观察到试管内的液体逐渐上升,直至达到平衡位置。
这时,我们可以停止加热,并记录下试管内液体的高度。
3. 数据处理通过实验操作,我们可以得到试管内液体的高度数据。
根据液液平衡的原理,我们可以利用这些数据计算出混合液中乙醇的相对含量。
根据饱和蒸汽压的定义,液体的蒸汽压与其相对含量成正比。
因此,我们可以利用蒸汽压与液体高度之间的关系,将实验测得的液体高度转化为乙醇的相对含量。
实验结果与讨论根据实验数据和计算结果,我们可以得出混合液中乙醇的相对含量。
通过与理论计算值的比较,我们可以评估实验的准确性和可靠性。
在实验中,我们发现试管内液体的高度随着乙醇含量的增加而增加。
这与理论计算结果相吻合,进一步验证了实验的准确性。
然而,在实际操作中,由于实验条件的限制和实验误差的存在,我们无法完全消除实验结果的偏差。
因此,在实验结果的分析和讨论中,我们需要考虑到实验误差的影响,并进行合理的修正和解释。
结论通过本次液液平衡测定实验,我们成功地探索了液液平衡测定的原理和方法,并通过实验结果验证了理论计算的准确性。
实验结果的分析和讨论表明,在实验操作中需考虑到实验误差的影响,并进行合理的修正和解释。
液相反应平衡常数的测定(华南师范大学物化实验)

当达到平衡时,整理得到 [FeSCN 2 ]平 [Fe3 ]平[SCN ]平
=
k1
K2k3 [H ]平
kБайду номын сангаас1
k 3 K 4[H ]平
= K平
由上式可见,平衡常数受氢离子的影响。因此,实验只能在同一 pH 值下进
行。本实验为离子平衡反应,离子强度必然对平衡常数有很大影响。所以,在各
被测溶液中离子强度 I = 1 2
则 E1=K[CNS-]0
③
对其余组溶液 Ei=K[FeCNS2+]I,e
④
两式相除并整理得
⑤
达到平衡时,在体系中 [Fe3+]i,e=[Fe3+]i,e=[Fe3+]0-[FeCNS2+]
⑥
[CNS-]i,e=[CNS-]0-[FeCNS2+]
⑦
、
将式⑥、⑦代入①,可以计算出除第 1 组外各组(不同 Fe3+起始浓度)反应
由于 Fe3++SCN-在水溶液中存在水解平衡,所以 Fe3+与 SCN-的实际反应很复杂, 其机理为
k1
Fe3 SCN FeSCN 2 k1
K2
Fe3 H 2O FeOH 2 H (快)
k3
FeOH 2 SCN FeOHSCN k3
K4
FeOHSCN H FeSCN 2 H 2O(快)
'
①
图浓度对络合物组成的影响 由于 Fe(SCN)2+是带颜色的,根据朗伯-比尔定律,消光值与溶液浓度成正比, 试验时,只要在一定温度下,借助分光光度计测定平衡体系的消光值,从而计算 出平衡时 Fe[CNS]2+的浓度[FeCNS2+]e,进而再推算出平衡时 Fe3+和 CNS-的浓度 [Fe3+]e 和[CNS-]e。根据式①一定温度反应的平衡常数 Kc 可求知。 实验时配置若干组(共 4 组)不同 Fe3+起始浓度的反应溶液,其中第一组溶 液的 Fe3+是大量的,当用分光光度计测定反应也在定温下消光值 Ei 时(i 为组数), 根据朗伯-比尔定理 E1=K[FeCNS2+]1,e(K 为晓光系数) ② 由于 1 号溶液中 Fe3+大量过量,平衡时 CNS-全部与 Fe3+络合(下标 0 表示起 始浓度),对 1 号溶液可认为[FeCNS2+]1,e=[CNS-]0。
【交】液相反应平衡常数的测定

液相反应平衡常数的测定一、实验目的1.利用分光光度计测定低浓度下铁离子与硫氰酸根离子生成硫氰合铁离子的平衡常数。
2.通过实验了解热力学平衡常数的数值与反应物起始浓度无关。
二、实验原理Fe3+离子与SCN-离子在溶液中可生成一系列的络离子,并共存于同一个平衡体系中。
当SCN-离子的浓度增加时,Fe3+离子与SCN-离子生成的络合物的组成发生如下的改变:Fe3++SCN-→ Fe(SCN)2+→ Fe(SCN)2+→ Fe(SCN)3→ Fe(SCN)4-→ Fe(SCN)52-而这些不同的络离子色调也不同。
由图3-12可知,当Fe3+离子与浓度很低的SCN-离子(一般应小于5×10-3mol·L-1)时,只进行如下反应:Fe3+ + SCN- FeSCN2+即反应被控制在仅仅生成最简单的FeSCN3+络离子。
其平衡常数表示为:(3-14)由于Fe[CNS]2+是带有颜色的,根据朗伯-比尔定律,消光值与溶液浓度成正比,实验时,只要在一定温度下,借助分光光度计测定平衡体系的消光值,从而计算出平衡时Fe[CNS]2+的浓度[FeCNS 2+]e 。
根据式(3-14)一定温度下反应的平衡常数K c 求可知。
实验时配制若干组(共4组)不同Fe 3+起始浓度的反应溶液,其中第一组溶液的Fe 3+是大量的,当用分光光度计测定反应液在室温下消光值E i 时(i 为组数),根据朗伯-比尔定理:E l =K[FeCNS 2+]l,e (K 为消光系数)由于1号溶液中Fe 3+大量过量,平衡时CNS -全部与Fe 3+络合(下标0表示起始浓度),对1号溶液可认为:[FeCNS]1,e =[CNS -]0则 E 1=K[CNS -]0 (3-15) 对其余组溶液 E i =K[FeCNS 2+]i,e (3-16) 两式相除并整理得: [FeCNS 2+]i,e =1E E i[CNS -]始 达到平衡时,在体系中[Fe 3+]i,e = [Fe 3+]0 - [FeCNS 2+]i,e (3-17) [CNS -]i,e = [CNS -]0 - [FeCNS 2+]i,e (3-18) 将式(3-17)和式(3-18)代入式(3-14)中,可以计算出除第1组外各组(不同Fe 3+起始浓度)反应溶液的在定温下的平衡常数K i,e 值。
液相反应平衡常数的测定实验报告

液相反应平衡常数的测定实验报告摘要本文针对液相反应平衡常数的测定实验研究进行了详细的说明,结合实验室实验方法,实验数据、实验结果和计算结果,以及实验错误的原因等,研究结果表明,本课题中的液相反应平衡常数的测定实验可以获得准确的数据。
关键词:平衡反应,液相反应,平衡常数1、实验目的本实验旨在通过实验,测定液相反应平衡常数,并研究其变化律和其对反应机理的影响。
2、实验原理液相反应的平衡常数是描述反应的激活能量的量度。
当在不同温度下测量液相反应的平衡常数K,可以得出液相反应的反应机理和活化能。
3、实验设备a) 使用经常性清洁的玻璃滴定道;b) 使用良好的塑料物理搅拌器;c) 使用精密滴定管;d) 使用精密滴定瓶;e) 使用精准量筒;f) 使用标准溶液;4、实验步骤a) 测定溶液PH;b) 测定清洁玻璃滴定道的滴速;c) 测定搅拌器的转速;d) 测定溶液的比重;e) 测定溶液的浓度;f) 继续滴定直到平衡定值。
5、实验结果a) 测定溶液pH:PH=7.3b) 测定清洁玻璃滴定道的滴速:14.7毫升/分钟c) 测定搅拌器的转速:4000转/分钟d) 测定溶液的比重:1.000 g/mLe) 测定溶液的浓度:1.00 mol/Lf) 测定溶液的平衡定值:K = 0.0726、实验错误a) 实验中搅拌器的转速较慢,因而影响了实验结果的准确性;b) 实验室温度的波动,对实验结果也有一定影响;c) 实验中反应液的浓度和pH不准确,也会影响实验结果。
7、结论本液相反应平衡常数的测定实验通过实验数据、实验结果和计算,实验结果表明,本实验中测定的液相反应平衡常数k为0.072。
液相反应平衡常数

液相反应平衡常数1.实验目的及要求1)掌握一种测定弱电解质电离常数的方法。
2)掌握分光光度计的测试原理和使用方法。
3)掌握pH计的原理和使用。
2.实验原理根据Beer-Lambert定律,溶液对于单色光的吸收,遵守下列关系式:(1)式中A为吸光度;I/I。
为透光率;k为摩尔吸光系数,它是溶液的特性常数;l为被测溶液的厚度;c为溶液浓度。
在分光光度分析中,将每一种单色光,分别、依次地通过某一溶液,测定溶液对每一种光波的吸光度,以吸光度A对波长λ作图,就可以得到该物质的分光光度曲线,或吸收光谱曲线,如图1所示。
由图可以看出,对应于某一波长有一个最大的吸收峰,用这一波长的入射光通过该溶液就有着最佳的灵敏度。
图1 分光光度曲线从(1)式可以看出,对于固定长度吸收槽,在对应最大吸收峰的波长(入)下测定不同浓度c的吸光度,就可作出线性的A~C线,这就是光度法的定量分析的基础。
以上讨论是对于单组分溶液的情况,对含有两种以上组分的溶液,情况就要复杂一些。
1)若两种被测定组分的吸收曲线彼此不相重合,这种情况很简单,就等于分别测定两种单组分溶液。
2)两种被测定组分的吸收曲线相重合,且遵守Beer-Lambert定律,则可在两波长λ1及λ2时(λ1、λ2是两种组分单独存在时吸收曲线最大吸收峰波长)测定其总吸光度,然后换算成被测定物质的浓度。
根据Beer-Lambert定律,假定吸收槽的长度一定,则(2)(3)(4)此处A Aλ1、A Aλ2、A Bλ1、A Bλ2分别代表在λ1及λ2时组分A和B的吸光度。
由(3)式可得:(5)将(5)式代入(4)式得:(6)这些不同的K值均可由纯物质求得,也就是说,在纯物质的最大吸收峰的波长λ时,测定吸光度A和浓度c的关系。
如果在该波长处符合贝尔一郎比定律,那么A~C为直线,直线的斜率为K值,是混合溶液在λ1、λ2时测得的总吸光度,因此根据(5)、(6)式即可计算混合溶液中组分A和组分B的浓度。
化学平衡常数的测定实验报告

化学平衡常数的测定实验报告实验目的:1. 了解化学反应平衡的基本概念和化学平衡常数的定义;2. 学习使用酸碱滴定法测定化学平衡常数的方法;3. 掌握测定过程中的实验技巧和注意事项。
实验原理:在化学反应中,反应物转化为生成物的速率与生成物转化为反应物的速率相等,达到动态平衡状态。
平衡状态下,各物质摩尔分数维持恒定,此时化学平衡常数 K 可以由反应物在平衡状态下的浓度比例确定。
K 的值可以用于判断化学反应的平衡位置以及相应反应物浓度的变化通过酸碱反应可以确定平衡常数。
一个酸性反应示例是醋酸钠( CH3COO - Na +)和醋酸(CH3COOH)之间的反应。
该反应的方程式为:CH3COO - Na + + H + CH3COOH + Na +在本实验中,我们将通过酸碱滴定法测定反应物中的氢离子的摩尔浓度,以此来确定该反应的化学平衡常数。
实验步骤:1. 将定量加入醋酸钠溶液和醋酸溶液的装有几滴甲醛的蒸馏水的250毫升烧瓶中。
2. 加入【奖励】0.1摩尔每升的NaOH溶液。
加入搅拌基底后,立即向反应瓶中加入醋酸钠溶液。
用CL曲线计算NaOH中的次数。
3. 加入【奖励】盐酸溶液至反应在酸性溶液中结束,继续进行酸碱滴定,以测量酸中的氢离子浓度。
用CL曲线计算HCl的溶液。
4. 用pH计测定反应液体的pH值,以确定化学平衡是否到达。
实验结果:我们用上述方法测定了反应物中氢离子的浓度,以此来确定该反应的平衡常数 K。
我们得到了以下结果:NaOH 滴定次数:20NaOH 浓度:0.1mol/LHCl 滴定次数:27HCl 浓度:0.1mol/L反应液体 pH 值:4.8通过计算,我们得出该反应的平衡常数 K 约为 10^ -4.3。
结论:在本实验中,我们成功地使用了酸碱滴定法测定了化学反应平衡常数。
通过这项实验,我们进一步加深了对平衡状态和化学平衡常数的认识,也学会了一种测定 K 值的实用技巧和方法。
这些知识和技能对进一步的化学研究和应用具有重要的意义。
液相反应平衡常数的测定

实验数据处理与分析
数据采集:准确记录实验过程中的各项数据 数据整理:对实验数据进行分类、筛选和排序 数据处理:运用统计学方法对实验数据进行处理 结果分析:根据处理后的数据,分析液相反应平衡常数的测定结果,得出结论
液相反应平衡常 数的影响因素
温度对平衡常数的影响
温度降低,平衡常数减小
温度升高,平衡常数增大
通过改变反应物的浓度,可以改变 反应速率,从而影响平衡常数。
添加标题
添加标题
添加标题
添加标题
平衡常数的大小决定了反应的平衡 位置和反应方向,从而影响反应速 率。
在实际实验中,可以通过测定反应 速率来方法
实验原理
液相反应平衡常数测定的基本原理是通过测量反应物和产物的浓度来计算平衡常数。 实验中需要使用精密的化学仪器,如分光光度计、高效液相色谱仪等来测量浓度。
平衡常数的大小反映了化学反应可能进行的程度。
平衡常数的表达式与化学方程式的书写方式有关。
平衡常数只与温度有关,与反应物或生成物的浓度无关。
平衡常数的物理意义
平衡常数是化学反应达到平衡状态时反应物 与生成物之间浓度关系的数学表示,表示反 应物与生成物之间浓度关系的变化趋势。
平衡常数的大小反映了化学反应可能进行的 程度,平衡常数越大,反应越完全。
温度对反应速率和产物分布 有显著影响
温度变化对平衡常数的影响 程度取决于反应的焓变
压力对平衡常数的影响
压力对平衡常数的影响是通过改变反应物和 生成物的浓度来实现的。
随着压力的增加,反应物和生成物的浓度也 会相应增加,从而影响平衡常数。
在高压条件下,反应平衡常数通常会减小, 因为反应物和生成物的浓度增加会导致反 应速率加快,从而使平衡向正向移动。
实验一 分光光度法测 液相反应的化学平衡常数
实验一 分光光度计法测溶液化学反应的K一、实验目的1.利用分光光度计测定低浓度下铁离子与硫氰酸根离子生成硫氰合铁离子的平衡常数。
2.通过实验了解K 与反应物起始浓度无关。
3.掌握分光光度计的正确使用方法。
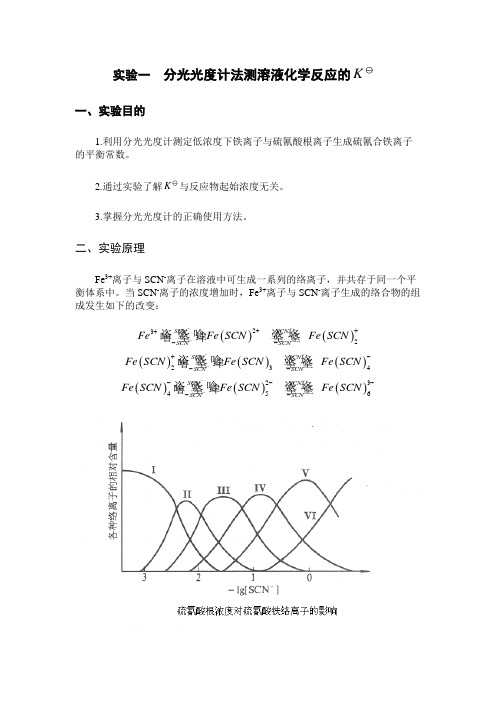
二、实验原理Fe 3+离子与SCN -离子在溶液中可生成一系列的络离子,并共存于同一个平衡体系中。
当SCN -离子的浓度增加时,Fe 3+离子与SCN -离子生成的络合物的组成发生如下的改变:()()232SCN SCN SCN SCN FeFe SCN Fe SCN ----+++--()()()234SCN SCN SCN SCN Fe SCN Fe SCN Fe SCN ----+---()()()23456SCN SCN SCN SCN Fe SCN Fe SCN Fe SCN ---------而这些不同的络离子颜色也不同。
由图可知,当Fe 3+离子与浓度很低的SCN -离子(一般应小于5×10-3mol·dm -3)时,只进行如下反应:()23Fe SCN Fe SCN ++-+即反应被控制在仅仅生成最简单的Fe(SCN)2+络离子。
其标准平衡常数23()///Fe SCN C K Fe C SCN C++-⎡⎤⎣⎦=⎡⎤⎡⎤⎣⎦⎣⎦ 根据朗伯-比尔定律,吸光度与溶液中Fe(SCN)2+络离子浓度成正比。
()20lg I A KL Fe SCN I+⎡⎤==⎣⎦(A 为吸光度,K 为常数, L 为液层厚度)。
借助于分光光度计测定溶液的吸光度,可计算出平衡时Fe(SCN)2+络离子的浓度以及Fe 3+离子和SCN -离子的浓度,从而求出该反应的平衡常数K 。
由于:(1) Fe 3+离子在水溶液中存在下列水解平衡11232322k k K Fe SCN FeSCN Fe H OFeOHH-+-+++++++快334222k k K FeOH SCN FeOHSCN FeOHSCN HFeSCNH O-+-+++++++快达平衡时22331134()/[][]//Fe SCN CK k k k k K H K H Fe C SCN C+--+++-⎡⎤⎛⎫⎛⎫⎣⎦=+÷+= ⎪ ⎪⎡⎤⎡⎤⎝⎭⎝⎭⎣⎦⎣⎦平平 K 与酸度有关。
华师物化实验报告-液相平衡常数测定

华南师范大学实验报告学生姓名学号专业年级、班级课程名称实验项目液相反应平衡常数的测定实验类型□验证□设计■综合实验时间年月日实验指导老师实验评分一、实验目的1、利用分光光度计测定低浓度下铁离子与硫氰酸根离子生成硫氰合铁离子液相反应的平衡常数。
2、通过实验了解热力学平衡常数的数值与反应物起始浓度无关。
二、实验原理Fe3+离子与SCN-离子在溶液中可生成一系列的络离子,并共存于同一个平衡体系中。
当SCN-离子的浓度增加时,Fe3+离子与SCN-离子生成的络合物的组成发生如下的改变:Fe3++SCN-→Fe(SCN)2+→Fe(SCN)2+→Fe(SCN)3→Fe(SCN)4-→Fe(SCN)52-而这些不同的络离子色调也不同。
由图Ⅲ-11-2可知,当Fe3+离子与浓度很低的SCN-离子(一般应小于5×10-3mol·L)时,只进行如下反应:Fe3+ + SCN- ≒FeSCN2+即反应被控制在仅仅生成最简单的FeSCN3+络离子。
其平衡常数表示为:根据朗伯-比尔定律,可知光密度与溶液浓度成正比。
因此,可借助于分光光度计测定其光密度,从而计算出平衡时FeSCN2+络离子的浓度以及Fe3+离子和SCN-离子的浓度,进而求出该反应的平衡常数K C。
实验分为4组,不同组的Fe3+浓度不同,其中第一组的浓度极大,使用分光光度计时,根据朗伯-比尔定律E1=K[FeCNS2+]1,e(K为消光系数)由于1号溶液中Fe3+浓度极大,平衡时CNS-与Fe3+完全络合,对于一号溶液可认为[FeCNS2+]1,e=[CNS-]0 则E1=K[CNS-]0对于其它溶液,则E i=K[FeCNS2+]1,e 两式相除并整理得[FeCNS2+]1,e=E1/E1[CNS-]0三、仪器与药品1、仪器722型分光光度计1台;50mL容量瓶8只;100mL烧杯4个;刻度移液管10mL2支5mL1支;25移液管1支;50mL酸式滴定管1支;洗耳球、洗瓶等2、试剂1×10-3mol·L KSCN(分析纯配置,需准确标定);0.1mol·LFeNH4(SO4)2(需准确标定Fe3+浓度,并加HNO3使H+浓度0.1mol·L);1mol·LHNO3;1mol·LKNO3(试剂均用分析纯配制)四、实验步骤1、取8个容量瓶,按照下表编号,并按下表配置溶液并进行定容。
液相反应平衡常数的测定

华南师范大学实验报告学生姓名学号专业化学(师范)年级、班级课程名称物理化学实验实验项目实验类型实验时间年月日实验指导老师实验评分一、实验目的1.利用分光光度计测定低浓度下铁离子与硫氰酸根离子生成硫氰合铁离子的平衡常数。
2.通过实验了解热力学平衡常数的数值与反应物起始浓度无关。
二、实验原理Fe3+离子与SCN-离子在溶液中可生成一系列的络离子,并共存于同一个平衡体系中。
当SCN-离子的浓度增加时,Fe3+离子与SCN-离子生成的络合物的组成发生如下的改变:Fe3++SCN-→Fe(SCN)2+→Fe(SCN)2+→Fe(SCN)3→Fe(SCN)4-→Fe(SCN)52-而这些不同的络离子颜色也不同。
由上图可知,当Fe 3+离子与浓度很低的SCN -离子(一般应小于5×10-3mol ·dm -3)时,只进行如下反应:Fe 3+ + SCN - ≒ Fe(SCN)2+即反应被控制在仅仅生成最简单的Fe(SCN)2+络离子。
其平衡常数表示为:根据朗伯-比尔定律,可知光密度与溶液浓度成正比。
因此,可借助于分光光度计测定其光密度,从而计算出平衡时FeSCN 2+络离子的浓度以及Fe 3+离子和SCN -离子的浓度,进而求出该反应的平衡常数K C 。
由于1号溶液中Fe 3+大量过量,平衡SCN -全部和Fe 3+络合(下标0表示起始浓度),对一号溶液可认为()21,eFe SCN +⎡⎤⎣⎦= SCN -⎡⎤⎣⎦0,则1E K SCN -⎡⎤=⎣⎦0 对其余组溶液 ()2,i i eE K Fe SCN +⎡⎤=⎣⎦两式相除并整理得()20,1[]i i e E Fe SCN SCN E +-⎡⎤=⎣⎦ 达到平衡时,在体系中332,0,[][][]e i e e e i e F F F SCN +++=- 32,0,[][][]i e e e i e SCN F F SCN -++=-故由以上各式即可计算出(除第1组外)各组反应溶液的在定温下的平衡常数,i e K 值。
液相反应平衡常数的测定(华南师范大学物化实验)
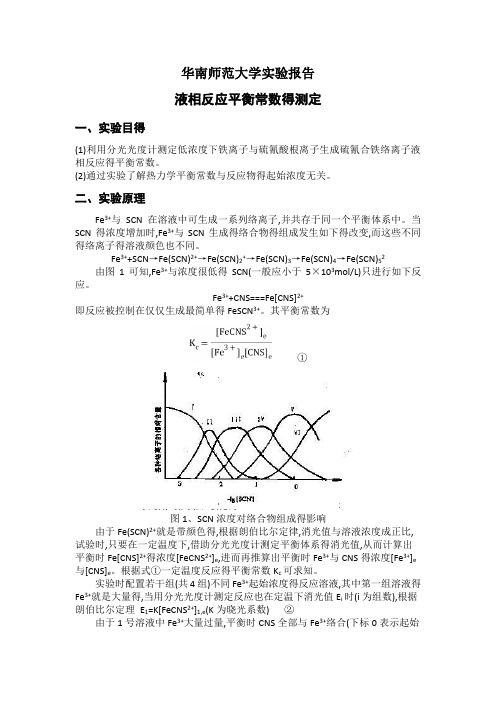
1mol/L HNO3 (A、R)
1mol/L KNO3 (A、R)
四、实验步骤
(1)取 8 个 50mL 容量瓶,编好号,按表 1 得内容,配制好溶液。在这 4 个容量瓶中, 溶液得氢离子均为 0、15mol/L,用 HNO3 来调节;溶液得离子强度均为 0、7,用 KNO3 来调节。
(2)取 4 个标记好得 50mL 容量瓶,按表 1 中计算结果,将除 KSCN 溶液外得三种溶液 分别取所需得体积按编号加入,并用蒸馏水冲制刻度。该溶液为测消光值时得对 比液。
50mL 酸式滴定管 1 支
洗瓶
1个
3、2 实验试剂
1×103mol/L KCNS:由 A、R 级 KCNS 配成,用 AgNO3 容量法准确标定。
0、1mol/L Fe(NH4)(SO4)2:由 A、R 级 Fe(NH4)(SO4)2·12H2O 配成,并加入 HNO3 使溶
液中得 H+浓度达到 0、1mol/L,Fe3+得浓度用 EDTA 容量法准确标定。
(3)再取另外 4 个标记好得 50mL 容量瓶,按表 1 得结果,将 4 种溶液分别去所需得 体积按编号加入(KCNS 溶液最后加),并用蒸馏水冲至刻度。该溶液为液相反应体 系。
(4)调整分光光度计,将波长调至 450nm,分别测定 4 组反应溶液得消光值。每组溶 液要重复测 3 次(更换溶液),取其平均值。
⑦
将式⑥、⑦代入①,可以计算出除第 1 组外各组(不同 Fe3+起始浓度)反应溶液
得在定温下得平衡常数 Ki,e=值。
三、仪器与试剂
3、1 实验仪器
721 型分光光度计 100mL 烧杯 25mL 移液管 洗耳球
1台 4个 1支 1个
液相平衡液相反应平衡常数的测定

• 1.利用分光光度计测定低浓度下铁离子与硫 氰酸根离子生成硫氰合铁络离子液相反应的平 衡常数。
• 2.通过实验了解热力学平衡常数与反应物的 起始浓度无关。
二、实验原理
• 当Fe3+离子与浓度很低的SCN-离子(一般应小于 5×10-3mol·dm-3)时,只进行如下反应:
• Fe3+ + Fe[CNS]2+ = Fe[CNS]2+
KC=[FeCNS2+]i,e/([Fe3+]i,e[CNS-]i,e) KC
参考文献
▪ 《物理化学实验指导书》,吴子生,严忠主编, 东北大学出版社,1995
▪ 《物理化学实验》,清华大学化学系编写组,清 华大学出版社,1991
四、实验步骤
• 3.取4个标记好的50ml容量瓶,按表中计算结果,将除 KSCN溶液外的三种溶液分别取所需的体积按编号加入,并 用蒸馏水冲置刻度(该溶液为测消光值时的对比液),并置 于恒温槽中恒温。
• 4.再取另外4个标记好的50ml容量瓶,按表中计算结果,将 4种溶液分别取所需的体积按编号加入(KCNS溶液最后加), 并用蒸馏水冲至刻度(该溶液为液相反应体系),并置于恒 温槽中恒温。
• 5.调整722分光光度计,将波长调至450nm,分别测定4组 反应溶液的消光值。每组溶液要重复测三次(更换溶液), 取其平均值。
五、数据处理
溶液编号 消光值 Ei
表 2 数据记录
1
2
3S2+]i,e=Ei[CNS-]0 [Fe3+]i,e=[Fe3+]0-[FeCNS2+]i,e [CNS-]i,e=[CNS-]0-[FeCNS2+]i,e
KC
化学平衡常数的液相反应中的测定与分析

化学平衡常数的液相反应中的测定与分析在化学反应中,平衡常数是描述化学反应平衡状态的一个重要指标。
对于液相反应而言,测定和分析其平衡常数是非常关键的,因为它可以帮助我们了解反应的偏向性以及反应条件对平衡转化的影响。
本文将探讨液相反应中化学平衡常数的测定与分析方法。
1. 反应方程的表示在液相反应中,我们首先需要确定反应的化学方程式。
这个方程式需要清晰地表示出反应物和生成物的化学式,并标明反应的物质摩尔比例。
在确定方程式时,还要考虑到反应的物理性质和反应条件,确保方程式的准确性和完整性。
2. 平衡常数的定义平衡常数(K)描述了反应在平衡状态下生成物与反应物之间的浓度关系。
对于液相反应而言,平衡常数通常用浓度表达,可以表示为各反应物及生成物浓度的乘积之比。
根据反应方程式,我们可以得到平衡常数的表达式。
3. 测定平衡常数的方法为了确定液相反应的平衡常数,我们可以采用不同的实验方法。
以下是几种常用的方法:3.1. 反应物消失法在该方法中,我们测量反应物浓度随时间的变化情况。
通过追踪反应物消失的速率,我们可以计算出平衡常数。
该方法适用于反应物消失较为明显或者反应速率较快的反应。
3.2. 生成物生成法在该方法中,我们测量生成物浓度随时间的变化情况。
通过追踪生成物生成的速率,我们可以计算出平衡常数。
该方法适用于生成物生成较为明显或者反应速率较快的反应。
3.3. 比色法该方法基于反应物或生成物具有不同的颜色或吸收特性。
通过测量反应物或生成物的吸光度或颜色强度,可以计算出平衡常数。
3.4. pH计测定法pH计测定法适用于涉及酸碱反应的液相反应。
通过测量反应过程中溶液的pH值变化,可以推导出平衡常数。
4. 数据处理与分析在测定平衡常数后,我们需要对实验数据进行处理和分析。
通常,我们会使用计算机软件或数学算法来进行数据拟合和计算。
通过拟合得到的数据,可以得出反应的平衡常数及其误差。
5. 平衡常数的意义与应用平衡常数可以告诉我们反应的偏向性,即向生成物或反应物方向倾斜的程度。
化学平衡常数的测定实验报告

化学平衡常数的测定实验报告化学平衡常数的测定实验报告引言:化学平衡常数是描述化学反应进行到一定程度时,反应物与生成物浓度之间的关系的指标。
它在实际应用中具有重要的意义,可以帮助我们了解反应的方向性和平衡位置。
本实验旨在通过测定反应物与生成物的浓度,计算出化学平衡常数,并探究温度对平衡常数的影响。
实验步骤:1. 实验前准备:准备好所需的实验器材和试剂,包括容量瓶、比色皿、移液管、酸碱指示剂等。
2. 实验过程:a. 将一定量的反应物A溶液倒入容量瓶中,加入适量的酸碱指示剂。
b. 使用移液管分别取不同体积的反应物B溶液,加入容量瓶中。
c. 摇匀容量瓶,使反应物充分混合,观察颜色变化。
d. 将混合溶液倒入比色皿中,使用分光光度计测定吸光度。
3. 数据处理:a. 根据实验所用反应物的化学方程式,计算出反应物与生成物的摩尔比例。
b. 根据吸光度测定值,计算出反应物与生成物的浓度。
c. 利用浓度数据,计算出化学平衡常数。
结果与讨论:通过实验测定,我们得到了反应物A与反应物B的浓度数据,并计算出了化学平衡常数。
在不同温度下的实验结果显示,随着温度的升高,化学平衡常数的值也随之增大。
这一现象可以通过热力学原理解释。
根据热力学第二定律,温度升高会增加反应物和生成物的热运动能力,使反应物更容易转化为生成物,从而增加平衡常数的值。
此外,实验结果还表明,反应物A和反应物B的浓度对平衡常数的值有一定的影响。
当反应物的浓度增加时,平衡常数的值也会增大。
这是因为浓度的增加会增加反应物分子之间的碰撞频率,从而促进反应的进行。
然而,需要注意的是,实验中的测定误差和实验条件的限制可能会对结果产生一定的影响。
为了减小误差,我们可以进行多次实验取平均值,并且在实验过程中严格控制各项条件的一致性。
结论:通过本实验的测定与分析,我们成功计算出了化学平衡常数,并观察到温度和浓度对平衡常数的影响。
实验结果表明,温度升高会增加平衡常数的值,而反应物浓度的增加也会导致平衡常数的增大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
华南师范大学实验报告学生姓名学号
专业年级、班级
课程名称实验项目液相反应平衡常数的测定
实验类型□验证□设计■综合实验时间年月日
实验指导老师实验评分
一、实验目的
1、利用分光光度计测定低浓度下铁离子与硫氰酸根离子生成硫氰合铁离子液相反应的平衡常数。
2、通过实验了解热力学平衡常数的数值与反应物起始浓度无关。
二、实验原理
Fe3+离子与SCN-离子在溶液中可生成一系列的络离子,并共存于同一个平衡体系中。
当SCN-离子的浓度增加时,Fe3+离子与SCN-离子生成的络合物的组成发生如下的改变:
Fe3++SCN-→Fe(SCN)2+→Fe(SCN)2+→Fe(SCN)3
→Fe(SCN)4-→Fe(SCN)52-
而这些不同的络离子色调也不同。
由图Ⅲ-11-2可知,当Fe3+离子与浓度很低的SCN-离子(一般应小于5×10-3mol·L)时,只进行如下反应:
Fe3+ + SCN- ≒FeSCN2+
即反应被控制在仅仅生成最简单的FeSCN3+络离子。
其平衡常数表示为:
根据朗伯-比尔定律,可知光密度与溶液浓度成正比。
因此,可借助于分光光度计测定其光密度,从而计算出平衡时FeSCN2+络离子的浓度以及Fe3+离子和SCN-离子的浓度,进而求出该反应的平衡常数K C。
实验分为4组,不同组的Fe3+浓度不同,其中第一组的浓度极大,使用分光光度计时,根据朗伯-比尔定律E1=K[FeCNS2+]1,e(K为消光系数)由于1号溶液中Fe3+浓度极大,平衡时CNS-与Fe3+完全络合,对于一号溶液可认为[FeCNS2+]1,e=[CNS-]0 则E1=K[CNS-]0对于其它溶液,则
E i=K[FeCNS2+]1,e 两式相除并整理得[FeCNS2+]1,e=E1/E1[CNS-]0
三、仪器与药品
1、仪器
722型分光光度计1台;50mL容量瓶8只;100mL烧杯4个;
刻度移液管10mL2支5mL1支;25移液管1支;50mL酸式滴定管1支;
洗耳球、洗瓶等
2、试剂
1×10-3mol·L KSCN(分析纯配置,需准确标定);
0.1mol·LFeNH4(SO4)2(需准确标定Fe3+浓度,并加HNO3使H+浓度
0.1mol·L);1mol·LHNO3;1mol·LKNO3(试剂均用分析纯配制)
四、实验步骤
1、取8个容量瓶,按照下表编号,并按下表配置溶液并进行定容。
2、调整722型分光光度计,将其波长调至450nm,分别测定四组的消光值(吸光度),每组数字重复测量三次(更换溶液),取平均值。
五、数据记录
六、数据处理与讨论
条件:恒温27.1℃氢离子浓度0.15mol/L 总离子强度I=0.7 波长λ=450nm
相对误差N/A
0.011121232
-0.01097764
3
-0.00014358
9
通过实验数据,在不同浓度的溶液下,[Fe3+]与[CNS-]在水溶液中生[FeCNS2+]反应的平衡常数基本维持于186附近,相对误差非常少,处于可以接受范围内。
与参考文献数值K=1.9953(lgK1=2.3 北师大无机化学4版附录)接近,总体符合实验要求。
七、提问与思考
1、当[Fe3+]与[CNS-]浓度较大时,将不再能够用公式
[FeCNS2+]1,e=E1/E1[CNS-]0计算[FeCNS2+]反应的平衡常数,因为当[CNS-]浓度较大时,则[FeCNS2+]1,e≠[CNS-]0 则E1≠K[CNS-]0,因此该等式将不再成立。
2、经实验验证结果,平衡常数与反应各个时候的浓度均无关系。
3、由于Fe3+离子在水溶液中,存在水解平衡,所以Fe3+离子与SCN-离子的实际反应很复杂,其机理为:
当达到平衡时,整理得到
由上式可见,平衡常数受氢离子的影响。
因此,实验只能在同一pH值下进行。
本实验为离子平衡反应,离子强度必然对平衡常数有很大影响。
所以,在各被测溶液中离子强度应保持一致。
4、为了消除除了测量物质外溶剂中有其它吸光物质对该波长的光有吸收而造成误差,因此必须使用除被测物质外其它组分完全一致的溶液作为空白对比液,在722型分光光度计中进行调100设置,确保抵消误差。
八、参考文献
1、《基础化学实验·物理化学实验》,第1版,华南师范大学化学实验教学中心组织编写,化学工业出版社
2、《北师大无机化学》第4版附录,北京师范大学等编,高等教育出版社。
