硫酸铵简介
硫酸铵定义

硫酸铵是一种重要的无机化合物,化学式为(NH4)2SO4。
它是一种无色或白色的结晶,易溶于水,但不溶于乙醇和丙酮。
硫酸铵是一种重要的氮肥,适用于各种土壤和作物,也是纺织、皮革、医药等领域的原料。
硫酸铵的制备方法有多种,其中一种是通过氨与硫酸直接进行中和反应而得。
此外,硫酸铵还可以通过其他方法如石膏法制备,其中以天然石膏或磷石膏、氨、二氧化碳为原料。
硫酸铵的用途广泛。
在农业上,它是一种重要的氮肥,适用于各种土壤和作物,可以促进植物的生长和发育。
在工业上,硫酸铵可以用作肥料、织物整理剂、染色助剂、皮革填充剂等。
此外,硫酸铵还可以用于制造其他化学品如硫酸钡、硫酸钾等。
需要注意的是,硫酸铵具有一定的吸湿性,容易结块,因此在使用时应保持干燥。
此外,硫酸铵在水中呈酸性,因此在接触皮肤或眼睛时可能会产生刺激。
硫酸铵的性质

硫酸铵的性质
硫酸铵,也称铵硫酸,是一种无色颗粒形状的无机化合物,由铵离子和硫酸根组成,分子式为NH4HSO4。
它是一种强腐蚀性的盐,其溶解度在水中较大,在20℃时可溶解8.75克/分升的水。
硫酸铵在医药和精细化学行业中有着重要的用途,例如,它可以用作肥料的组成部分,也可用作缓冲剂、调节剂、清洁剂、防锈剂、助剂和稳定剂等。
硫酸铵具有一定的毒性,可引起皮肤灼伤和眼睛刺激,而且可以通过呼吸而入体,会对人体产生一定的有害影响。
其气态污染物尤其感官明显,可引起粉尘病,进入人体后可严重伤害肝脏、肾脏和肺部组织。
因此,使用硫酸铵时,应遵守必要的安全措施,以避免可能的危害,如穿戴个人防护装备,使用抗腐蚀工具和耐腐蚀材料,以及适当的排放处理等。
硫酸铵也可作为吸附剂,用于吸附重金属离子,如铅、汞、镉、铜、铝、钴等。
硫酸铵不仅能减少重金属离子的污染,而且可有效降低水中有机污染物的浓度,因此,它广泛应用于水处理领域。
硫酸铵可用于去除水中的硼酸、硫酸铜、氟酸等有机污染物,可有效降低水质中的酸度,从而改善水体环境。
此外,硫酸铵在电化学领域也有着重要的应用。
它可以作为负极材料的一种膜厚补充剂,可以提高电池的性能和使用寿命。
同时,由于其强碱性,硫酸铵也可用作渗析电解质,可以改善电解液的稳定性,从而保持电解过程的正常进行。
总之,硫酸铵在医药、精细化学、水处理领域和电化学领域具有重要的作用。
但使用硫酸铵时,应小心,并遵守必要的安全措施,以避免可能的危害。
硫酸铵种类

硫酸铵种类硫酸铵是一种常用的化学物质,广泛应用于农业、工业和科研领域。
它具有多种不同的种类和用途。
本文将介绍几种常见的硫酸铵种类及其特点。
一、普通硫酸铵普通硫酸铵是最常见的硫酸铵种类之一,化学式为(NH4)2SO4。
它是一种无色结晶体,可溶于水,呈酸性。
普通硫酸铵是一种重要的氮肥,含有高浓度的氮元素,可作为植物的养分来源。
它在农业生产中广泛用于提供植物所需的氮肥,促进作物的生长和发育。
二、工业级硫酸铵工业级硫酸铵是一种用途较广泛的硫酸铵种类,常用于工业生产中的多个领域。
它通常具有较高的纯度和稳定性,可用于制备其他化学物质或作为反应媒介。
工业级硫酸铵常用于制备硫酸铵硝酸盐炸药、合成染料和染料中间体,以及用于金属表面处理等工艺。
三、高纯硫酸铵高纯硫酸铵是一种经过特殊处理和精炼的硫酸铵种类,具有较高的纯度和纯净度。
它通常用于科研领域中的实验室试剂和分析化学试剂。
高纯硫酸铵可以用于制备高纯度的化学物质,如高纯硫酸铵硝酸盐炸药、纯净的氨和硫酸盐等。
它的高纯度可以确保实验结果的准确性和可靠性。
四、缓释硫酸铵缓释硫酸铵是一种特殊的硫酸铵种类,它具有延迟释放的特点。
缓释硫酸铵通过特殊工艺制备而成,使其在土壤中缓慢分解释放氮元素,从而延长了氮肥的供应时间。
这种特性可以有效地减少氮肥的浪费和环境污染,并提高农业生产的效益。
缓释硫酸铵常用于果树、蔬菜和花卉的栽培中,以提供持续和稳定的氮肥供应。
五、液体硫酸铵液体硫酸铵是一种以溶液形式存在的硫酸铵种类,通常具有较高的浓度和稳定性。
液体硫酸铵可以直接施用于土壤或植物表面,以提供氮肥和硫肥的营养需求。
它易于吸收和利用,可以促进植物的生长和发育。
液体硫酸铵常用于农业生产中的叶面喷施肥料、滴灌肥料和水肥一体化系统中。
总结起来,硫酸铵有多种不同的种类和用途。
普通硫酸铵是常见的氮肥,工业级硫酸铵用于工业生产,高纯硫酸铵用于科研实验,缓释硫酸铵用于农业生产,液体硫酸铵用于土壤施肥。
这些不同种类的硫酸铵在各自的领域中发挥着重要的作用,为农业生产、工业生产和科学研究提供了必要的化学物质基础。
硫酸铵msds

工程控制:密闭操作,局部排风。
呼吸系统防护:空气中粉尘浓度超标时,必须佩戴自吸过滤式防尘口罩。紧急事态抢救或撤离时,应该佩戴空气呼吸器。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿防毒物渗透工作服。
手防护:戴橡胶手套。
其它:工作完毕,淋浴更衣。保持良好的卫生习惯。
理
化
性
质
熔点(℃):140
泄
漏
应
急
处
理
隔离泄漏污染区,限制出入。建议应急处理人员戴防尘面具(全面罩),穿防毒服。用洁净的铲子收集于干燥、洁净、有盖的容器中,转移至安全场所。若大量泄漏,收集回收或运至废物处理场所处置。
储
运
注
意
事
项
储存注意事项:Βιβλιοθήκη 存于阴凉、通风的库房。远离火种、热源。应与酸类、碱类分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
燃
爆
特
性
与
消
防
燃烧性:本品不燃,具刺激性
闪点(℃):无意义
爆炸下限(%):无意义
引燃温度(℃):无意义
爆炸上限(%):无意义
最小点火能(mJ):无资料
最大爆炸压力(MPa):无资料
危险特性:受热分解产生有毒的烟气。
灭火方法:消防人员必须穿全身防火防毒服,在上风向灭火。灭火时尽可能将容器从火场移至空旷处。
禁忌物:强酸、强碱。
燃烧(分解)产物:氮氧化物、硫化物。
毒
性
急性毒性:LD50 5628mg/kg(大鼠经口)15800mg/kg(兔经皮)LC50 83776mg/m34小时(大鼠吸收)亚急性和慢性中毒大鼠吸入50mg/m3,12小时/天,3个月,在8~10周内可见到气管、支气管粘膜损害,大脑皮质细胞营养障碍等。致突变性微生物致突变:啤酒酵母菌12pph.DNA抑制:人类淋巴细胞300mmol/L.生殖毒性大鼠经口最低中毒剂量(TDL0):7500mg/kg(孕7~19天),对新生鼠行为有影响。大鼠吸入最低中毒浓度(TDL0):20000ppm(7小时)(孕1~22天)引起肌肉骨骼、心血管系统和泌尿系统发育异常。
硫酸铵
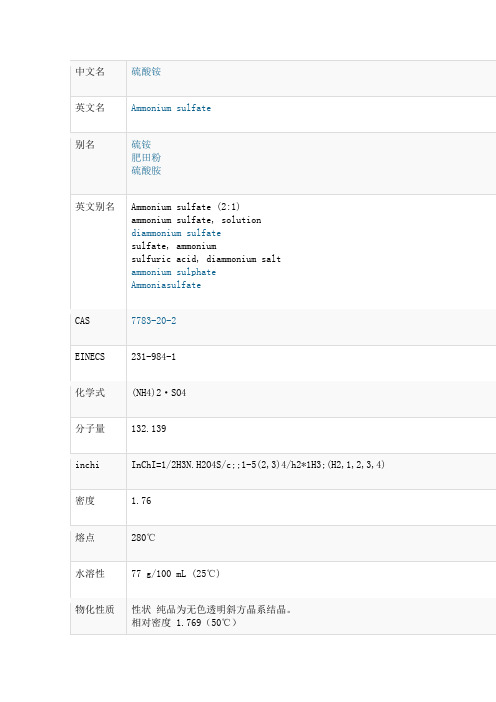
溶解性易溶于水(0℃时70.6g/100ml水、100℃时103.8g/100ml水),水溶液呈酸
溶于醇、丙酮和氨。
产品用途用作肥料,还可用作焊药、织物防火剂,医药上作盐析剂、渗透压调节剂等Xi - 刺激性物品
危险品标
志
硫酸铵- 性质
无色结晶或半透明正交结晶或白色颗粒。
易溶于水,不溶于乙醇、丙酮。
加热至28℃时分解为
氨和硫酸。
相对密度1. 77。
0.Imol/L水溶液pH值5.5。
与次氯酸钠反应生成爆炸性的三氯化氮。
受高热分解,放出有毒的烟气。
在水中的溶解度为(g/loog H20):70.6(0℃);76.7(25℃);
103.8(100℃)。
本品不燃,具刺激性。
硫酸铵- 标准
本品含(NH4)2S04应为99.0%〜100. 5% 。
硫酸铵- 制法
将硫酸铵溶于冷水中,至相对密度为1. 20。
加入适量氨水调节溶液pH值至8~9,静置,吸取
上清液,在清液中加入少量活性炭,加热煮沸,于60℃保温。
再补加氨水至pH值为9~10。
静
置,冷至室温。
过滤,蒸发滤液至析出结晶,于70℃干燥,得纯品硫酸铵。
硫酸铵- 性状
•本品为无色或白色晶体或颗粒。
•本品在水中易溶,在乙醇中不溶。
硫酸铵功效和使用注意事项

硫酸铵功效和使用注意事项全文共四篇示例,供读者参考第一篇示例:硫酸铵,化学式为(NH4)2SO4,是一种常见的氮肥。
它是一种白色结晶性固体,在水中可溶解。
硫酸铵在农业上被广泛应用,用作土壤调理剂和作物生长促进剂。
在工业上也有许多用途,比如用作阻燃剂、干燥剂等。
一、硫酸铵的功效1. 氮肥作用:硫酸铵含有丰富的氮元素,是一种优质的氮肥。
氮元素是植物生长过程中必需的养分之一,可以促进作物的生长发育,增加叶面积,提高叶绿素含量,从而增加作物的产量和品质。
2. 硫肥作用:硫酸铵中含有硫元素,可以提高作物的抗病性和抗逆性。
硫元素是植物合成蛋白质和维生素的重要组成部分,可以促进作物根系的生长和养分吸收,提高作物的免疫力,减少病虫害的发生。
3. 酸碱调节作用:硫酸铵具有酸性,可以调节土壤的酸碱度,改善土壤的肥力和透气性。
在碱性土壤中使用硫酸铵可以降低土壤的pH 值,提高肥效。
4. 速效性:硫酸铵是一种速效肥料,可以迅速被作物吸收利用,促进作物的生长和发育。
适用于迅速补充作物生长所需的氮、硫等元素。
二、硫酸铵的使用注意事项1. 用量控制:在使用硫酸铵时,应根据作物的品种、生长期和土壤的养分状况确定合理的用量。
一般来说,每亩用量不宜过大,以免造成盐渍化和土壤酸化等问题。
2. 施用时间:硫酸铵适合于作物生长的各个生长阶段使用,但应避开作物萌发和抽穗期,以免造成作物烧嫩或生育期延迟。
3. 施肥方式:硫酸铵可以通过撒施、灌溉等方式施用。
在施用时应注意均匀撒布,避免肥料过量集中施用,造成养分过量浪费或土壤中毒。
4. 与其他肥料配合:硫酸铵可以与其他氮、磷、钾肥料混合施用,以弥补不同养分之间的互补性,提高肥效,减少养分浪费。
5. 储存注意:硫酸铵属于易潮解的化肥,应储存在阴凉、干燥、通风的地方,避免阳光直射和雨淋,防止肥料吸湿结块,影响使用效果。
第二篇示例:硫酸铵,化学式为(NH4)2SO4,是一种常见的化肥,也被广泛用于工业生产中。
硫酸铵的性质

硫酸铵的性质
硫酸铵(AmmoniumSulfate)是一种无机化合物,表示为NH4SO4,它具有黑色结晶状的外观,是硫酸盐的一种。
它广泛应用于工业肥料和农药,也被用作农田浇水营造有利于植物生长的条件。
硫酸铵是由硫酸和铵(NH3)反应得到的,即NH3 + H2SO4 NH4SO4。
该物质极易溶于水,但难溶于醇、醚和脂肪,具有强烈的酸性。
它的沸点是焦耳温度(672℃),其熔点为333℃。
硫酸铵具有肥料和农药的主要功能。
它是以硫和氮为主要元素的肥料,可以提供植物所需的养分。
此外,它也可以抑制微生物的生长,可以被用来防止植物患病。
此外,硫酸铵可以被用于制造一些日常用品,例如发泡剂、漂白药水、洗衣粉等,也用于制造汽车冷却剂、车身填充剂等物质。
硫酸铵的安全性也受到广泛的关注。
研究表明,过高摄入会导致人体毒性,可能会使中枢神经系统受损,表现为头痛、抽搐、混乱等症状。
此外,研究人员认为,短期过量摄入可能会导致肝、肾和肺部损伤,因此,使用该物质时应注意安全措施。
综上所述,硫酸铵是一种具有多种用途的无机化合物,可用作肥料和农药。
它的安全性也不可忽视。
因此,对于使用硫酸铵的人员,应当了解其特性,并采取相应的安全措施,以防止不当使用所带来的危害。
- 1 -。
硫酸铵(硫铵)

硫酸铵(硫铵)1、标识中文名:硫酸铵;硫铵英文名:Ammonium sulfate;Diammonium sulfate分子式:(NH4)2SO4;H8N2O4S分子量:132.162、理化性质外观与性状:白色或微黄色结晶。
无臭主要用途:用于农作物作为追肥、基肥、种肥。
还可用作焊药、织物防火剂、生物制剂、色谱分析试剂等。
熔点:>280(分解)相对密度(水=1):1.769溶解性:溶于水,不溶于醇、丙酮。
3、燃烧爆炸危险燃烧性:不燃危险特性:与次氯酸钠反应生成爆炸性的三氯化氮。
受高热分解,放出有毒的烟气。
燃烧(分解)产物:氮氧化物、氧化硫、氨。
稳定性:稳定禁忌物:亚硝酸钾、次氯酸盐。
聚合危害:不能出现灭火方法:如果该物质或被污染的流体进入水路,通知有潜在水体污染的下游用户,通知地方卫生、消防官员和污染控制部门。
使用适合于火场的任何一种灭火剂灭火。
储运注意事项:储存于阴凉、通风仓间内。
保持容器密封。
防止受潮和雨淋。
应与次氯酸盐、食用化工原料等分开存放。
操作现场不得吸烟、饮水、进食。
搬运时要轻装轻卸,防止包装及容器损坏。
分装和搬运作业要注意个人防护。
ERG指南:154 ERG指南分类:有毒和/或腐蚀性物质(不燃的)毒性危害接触限值:中国MAC:未制订标准前苏联MAC:25mg/m3美国TLV—TWA:未制订标准美国TLV—STEL:未制订标准侵入途径:吸入食入经皮吸收毒性:LD50:3000mg/kg(大鼠经口) LC50:健康危害:本品对眼睛、皮肤、粘膜和上呼吸道有刺激作用。
受热分解放出氮氧化物、氨和氧化硫烟雾。
吸入可引起迟发几小时的肺水肿,严重病例有死亡危险。
急救皮肤接触:用肥皂水及清水彻底冲洗。
就医。
对少量皮肤接触,避免将物质播散面积扩大。
注意患者保暖并且保持安静。
吸入、食入或皮肤接触该物质可引起迟发反应。
确保医务人员了解该物质相关的个体防护知识,注意自身防护。
眼睛接触:拉开眼睑,用流动清水冲洗15分钟。
硫酸铵用途

硫酸铵用途
硫酸铵是一种常用的化学物质,主要由氨、硫酸和铵组成,晶体系数为25。
硫酸铵是一种无色晶体,具有苦味,能溶于水。
硫酸铵在工业上有多种用途,其应用广泛,下面将为大家具体说明硫酸铵的用途。
首先,硫酸铵在农业上的用途非常广泛。
硫酸铵可以用作植物的肥料,具有很好的肥效作用。
它可以改善土壤的结构,增加土壤的湿度,增加土壤的肥量,改善土壤的氮磷钾含量,促进植物的生长。
硫酸铵还可以防止土壤中病菌、虫子和真菌的生长,增强植物的抗病能力。
其次,硫酸铵也是一种常用的防腐剂。
它能有效延长各种食品的保质期。
硫酸铵可以抑制食品的氧化反应,保护食品的营养价值和原有的口感、颜色和气味。
此外,硫酸铵还可以防止各种酒类的酵母发酵,以及日常工业生产中的有机物的腐败反应。
再次,硫酸铵还可以用于除草、杀虫等。
它具有显著的抗药性,可以有效抑制各种野生植物的生长,同时可以有效控制害虫的繁殖。
硫酸铵还可以用于清洗各种表面,以防止大肆繁殖的细菌和微生物,除去表面的污染物。
此外,硫酸铵的应用还不仅限于以上这些,它还可以用于冶金、石油、制药等行业,具有比较重要的作用。
总之,硫酸铵是一种广泛应用的化学物质,它在农业、食品、防腐剂、除草和杀虫等方面都有着重要的作用。
它扮演着化学工业和社
会经济发展中不可或缺的角色,具有重要的意义。
硫酸铵的作用与用途

硫酸铵的作用与用途
硫酸铵是一种无机化合物,化学式为(NH4)2SO4,是常用的化肥和工业原料之一。
它具有以下的作用与用途:
1. 作为肥料:硫酸铵中含有丰富的氮元素和硫元素,这些元素对植物生长十分重要。
因此,硫酸铵常被用作一种优质的氮肥,可以提供植物所需的氮元素,促进植物的生长与发育。
2. 提高土壤酸性:硫酸铵是酸性肥料,它可以降低土壤的pH 值,使土壤更加酸性。
这对于需求酸性土壤的植物,如杜鹃花和蓝莓等,是非常有益的。
3. 工业应用:硫酸铵在工业上也有重要的应用。
它可以用作制备其他化肥和农药的原料,如尿素和硝酸铵。
此外,硫酸铵还可用于制造火药和爆炸物,以及在纺织工业中用于染料和颜料的生产。
4. 蛋白质沉淀:硫酸铵可以用于生物技术和分子生物学实验中,用以沉淀蛋白质。
由于硫酸铵的高溶解度,可以通过调节溶液中的硫酸铵浓度来实现蛋白质的沉淀和纯化。
总之,硫酸铵作为一种重要的化工原料和肥料,在农业生产、工业制造和实验室研究中都有着广泛的应用。
硫酸铵闪点

硫酸铵闪点1. 硫酸铵简介硫酸铵(Ammonium sulfate),化学式为(NH4)2SO4,是一种常见的无机化合物。
它是由铵离子(NH4+)和硫酸根离子(SO42-)组成的盐。
硫酸铵是一种白色结晶固体,可溶于水,呈酸性溶液。
它具有广泛的应用领域,包括作为肥料、化学试剂、食品添加剂等。
2. 闪点的定义闪点是指液体在一定条件下能够发生闪燃的最低温度。
液体的闪点是安全性评估中重要的指标,它可以用来评估液体的易燃性和火灾爆炸风险。
3. 硫酸铵的闪点硫酸铵是一种不易燃的化合物,因此其闪点较高。
根据实验数据,硫酸铵的闪点约为235°C(455°F)。
4. 影响硫酸铵闪点的因素硫酸铵的闪点受多种因素的影响,包括温度、压力、气体浓度等。
以下是一些常见的影响因素:4.1 温度液体的闪点随着温度的升高而增加。
对于硫酸铵来说,当温度超过其闪点时,液体表面的蒸汽可以与空气中的氧气发生燃烧反应,产生火焰。
4.2 压力压力对硫酸铵的闪点影响较小。
在常规条件下,硫酸铵的闪点与压力变化无关。
4.3 气体浓度硫酸铵的闪点与周围空气中的氧气浓度有关。
氧气浓度越高,液体的闪点越低,反之亦然。
这是因为氧气是燃烧的必需品,高浓度的氧气可以促进液体的燃烧。
5. 硫酸铵的安全性考虑尽管硫酸铵本身不易燃,但在特定条件下,它仍然可能引发火灾或爆炸。
因此,在使用或储存硫酸铵时,需要注意以下安全性考虑:5.1 避免高温由于硫酸铵的闪点较高,因此需要避免将其暴露在高温环境中。
高温可能导致硫酸铵分解,产生有毒气体和易燃物质。
5.2 防止与可燃物接触硫酸铵与可燃物质(如有机物)接触时,可能引发火灾或爆炸。
因此,需要将硫酸铵与可燃物质分开存放,以防止它们接触。
5.3 防止与氧化剂接触硫酸铵与氧化剂(如高浓度的氧气或氧化剂化学品)接触时,也可能引发火灾或爆炸。
因此,需要将硫酸铵与氧化剂分开存放,以防止它们接触。
5.4 储存和处理注意事项储存和处理硫酸铵时,需要采取适当的安全措施,包括使用密封容器、避免剧烈振动或冲击、远离火源等。
水溶肥原料硫酸铵

水溶肥原料硫酸铵
肥料级硫酸铵是硫酸铵众多种类的一种,是白色斜方晶系结晶,易溶于水,主要在农业上作为氮肥,是很好的生物性肥料。
肥料级硫酸铵就是硫酸铵众多种类的一种!肥料级硫酸铵成分:简称硫铵,分子式(NH4)2SO4,分子量132.14,含氮量为21%。
性质:硫铵(硫酸铵)是白色斜方晶系结晶,易溶于水,不溶于酒精、丙酮及氯中,含有杂质的硫铵显浅色或暗褐等颜色,与碱性物质相混反应放出氨气,潮湿的硫铵对钢铁和水均有腐蚀。
硫铵分解温度为280℃,放出氨气变为酸式硫酸铵NH4HSO4,温度的变化对硫酸铵在水中的溶解度影响不大,本身相对吸湿性较小。
用途:硫铵(硫酸铵)主要在农业上作为氮肥,优点是吸湿性相对较小,不易结块,与硝酸铵和碳铵相比具有优良的物理性质和化学稳定性;硫酸铵是速效肥料,很好的生物性肥料,在土壤中的反应呈酸性,适于碱性土壤和碳质土壤。
缺点是含氮偏低,但是硫铵除含氮外,硫酸铵还含硫,对农作物极为有利。
另外,在工业上应用也很广泛,如在医药上用作制酶的发酵氮源,纺织上用作染色印花助剂,精制的硫铵(硫酸铵)用于啤酒酿造。
硫酸铵的物理性质

硫酸铵的物理性质
1. 硫酸铵的结构
硫酸铵是一种具有硫酸根和铵根的离子混合物,它的分子式为
NH4HSO4,其中NH4+为铵根,HSO4-为硫酸根。
硫酸铵的晶体结构由八个NH4+离子和八个HSO4-离子组成,这些离子之间以氢键相互连接,形成一个八面体晶体结构。
:
2. 硫酸铵的性质
硫酸铵是一种无色结晶体,溶于水,易溶于乙醇,不溶于乙醚。
它具有强烈的酸性,溶液pH值低于3.5。
它在空气中很容易氧化,它的溶解度随温度的升高而降低。
硫酸铵是危险的化学品,它可能会引起皮肤刺激,眼睛刺激,咳嗽,呼吸困难,以及胃肠道刺激等不良反应。
3. 硫酸铵的溶解性:硫酸铵在水中易溶,溶解度随温度的升高而增加,在0℃时,溶解度为37.2g/100ml,在100℃时,溶解度为
236.8g/100ml。
硫酸铵在乙醇中几乎不溶,在乙醚中溶解度为
0.3g/100ml,在氯仿中溶解度为1.2g/100ml。
4. 硫酸铵的分子量
硫酸铵的分子量为66.08 g/mol。
:
5. 硫酸铵的毒性:
硫酸铵是一种有毒物质,其中的氨基离子可以破坏细胞膜,导致细胞
死亡。
它还可以损害肺部,导致呼吸系统疾病。
硫酸铵的毒性可以通
过皮肤吸收,如果接触时间过长,可能会导致皮肤灼伤、水肿和瘙痒。
同时,硫酸铵也可以通过口服或吸入而被人体吸收,进入血液循环,
导致中毒。
硫酸铵(硫铵)

硫酸铵(硫铵)1、标识中文名:硫酸铵;硫铵英文名:Ammonium sulfate;Diammonium sulfate分子式:(NH4)2SO4;H8N2O4S分子量:132.162、理化性质外观与性状:白色或微黄色结晶。
无臭主要用途:用于农作物作为追肥、基肥、种肥。
还可用作焊药、织物防火剂、生物制剂、色谱分析试剂等。
熔点:>280(分解)相对密度(水=1):1.769溶解性:溶于水,不溶于醇、丙酮。
3、燃烧爆炸危险燃烧性:不燃危险特性:与次氯酸钠反应生成爆炸性的三氯化氮。
受高热分解,放出有毒的烟气。
燃烧(分解)产物:氮氧化物、氧化硫、氨。
稳定性:稳定禁忌物:亚硝酸钾、次氯酸盐。
聚合危害:不能出现灭火方法:如果该物质或被污染的流体进入水路,通知有潜在水体污染的下游用户,通知地方卫生、消防官员和污染控制部门。
使用适合于火场的任何一种灭火剂灭火。
储运注意事项:储存于阴凉、通风仓间内。
保持容器密封。
防止受潮和雨淋。
应与次氯酸盐、食用化工原料等分开存放。
操作现场不得吸烟、饮水、进食。
搬运时要轻装轻卸,防止包装及容器损坏。
分装和搬运作业要注意个人防护。
ERG指南:154 ERG指南分类:有毒和/或腐蚀性物质(不燃的)毒性危害接触限值:中国MAC:未制订标准前苏联MAC:25mg/m3美国TLV—TWA:未制订标准美国TLV—STEL:未制订标准侵入途径:吸入食入经皮吸收毒性:LD50:3000mg/kg(大鼠经口) LC50:健康危害:本品对眼睛、皮肤、粘膜和上呼吸道有刺激作用。
受热分解放出氮氧化物、氨和氧化硫烟雾。
吸入可引起迟发几小时的肺水肿,严重病例有死亡危险。
急救皮肤接触:用肥皂水及清水彻底冲洗。
就医。
对少量皮肤接触,避免将物质播散面积扩大。
注意患者保暖并且保持安静。
吸入、食入或皮肤接触该物质可引起迟发反应。
确保医务人员了解该物质相关的个体防护知识,注意自身防护。
眼睛接触:拉开眼睑,用流动清水冲洗15分钟。
硫酸铵加热的化学方程式

硫酸铵加热的化学方程式摘要:1.硫酸铵的简介2.硫酸铵加热的反应过程3.硫酸铵加热生成物的化学性质4.硫酸铵加热在实际应用中的案例5.安全注意事项正文:硫酸铵(NH4)2SO4)是一种常见的氮肥,广泛应用于农业生产。
它在加热条件下会发生化学反应,生成氨气、水蒸气和硫酸氢气。
下面我们将详细介绍硫酸铵加热的化学方程式及其相关内容。
1.硫酸铵的简介硫酸铵是一种无色晶体,分子量为132.14,熔点为260℃。
它是一种中性盐,易溶于水,水溶液呈酸性。
在农业生产中,硫酸铵作为氮肥,有助于提高农作物的产量。
2.硫酸铵加热的反应过程当硫酸铵在加热条件下,会发生如下化学反应:(NH4)2SO4 → 2NH3 + H2O + SO2这是一种分解反应,硫酸铵分解为氨气、水蒸气和二氧化硫。
氨气和硫酸氢气在加热过程中进一步反应,生成硫酸氢铵。
3.硫酸铵加热生成物的化学性质氨气(NH3)是一种有毒、刺激性气味的气体,易燃,在水溶液中呈碱性。
二氧化硫(SO2)是一种有毒、刺激性气味的气体,具有还原性,在水溶液中呈酸性。
硫酸氢气(H2SO4)是一种强酸,具有强烈的腐蚀性。
4.硫酸铵加热在实际应用中的案例硫酸铵加热生成的氨气、水蒸气和硫酸氢气在化工、医药、农业等领域具有广泛的应用。
例如,氨气可用于制造肥料、合成洗涤剂、制药等;水蒸气可用于发电、生产蒸汽;硫酸氢气可用于制造硫酸等化学品。
5.安全注意事项在进行硫酸铵加热实验或生产过程中,应严格遵守安全规程。
佩戴防护设备,如口罩、眼镜、手套等,以防止吸入有毒气体或接触到腐蚀性物质。
同时,注意加热设备的完好状态,避免泄漏。
在储存和使用过程中,确保硫酸铵的包装完好,防止潮湿、受热。
总之,硫酸铵加热生成氨气、水蒸气和硫酸氢气,这些生成物在多个领域具有广泛的应用。
硫酸铵品级

硫酸铵品级
摘要:
1.硫酸铵简介
2.硫酸铵的品级划分
3.硫酸铵品级的影响因素
4.硫酸铵品级的检测方法
5.硫酸铵品级的应用领域
正文:
硫酸铵,化学式(NH4)2SO4,是一种常见的氮肥,广泛应用于农业生产中。
硫酸铵的品级是指其纯度和质量等级,通常分为工业级和农业级两个等级。
硫酸铵的品级划分主要取决于其纯度和杂质含量。
工业级硫酸铵纯度较高,通常在99% 以上,主要用于化工生产和肥料添加剂。
农业级硫酸铵纯度较低,一般在90% 左右,主要用于农业施肥。
硫酸铵品级的影响因素主要有生产工艺、原料纯度和生产环境等。
生产工艺不同,硫酸铵的纯度也会有所不同。
原料纯度越高,硫酸铵的品级也越高。
生产环境中的杂质含量也会影响到硫酸铵的品级。
硫酸铵品级的检测方法通常包括化学分析法和仪器分析法。
化学分析法主要是通过化学反应来测定硫酸铵中的氮、硫等元素的含量。
仪器分析法则是通过仪器设备,如X 射线荧光光谱仪、原子吸收光谱仪等,来测定硫酸铵的成分和纯度。
硫酸铵品级的应用领域主要取决于其纯度和质量等级。
工业级硫酸铵主要用于化工生产,如生产磷酸、硫酸等,也可以用作肥料添加剂,提高肥料的效果。
硫酸铵加热的化学方程式

硫酸铵加热的化学方程式
摘要:
一、硫酸铵加热化学方程式简介
1.硫酸铵的基本信息
2.硫酸铵加热化学反应的背景
二、硫酸铵加热化学方程式详解
1.硫酸铵加热分解反应
2.硫酸铵与氢氧化钠加热反应
三、结论
1.硫酸铵加热化学方程式的重要性
2.在实际应用中的体现
正文:
硫酸铵加热化学方程式是化学领域中一个重要的知识点。
硫酸铵((NH4)2SO4)是一种常见的无机化合物,广泛应用于农业肥料、化工生产等领域。
加热硫酸铵可以引发一系列化学反应,从而产生新的物质。
了解硫酸铵加热化学方程式有助于我们更好地理解这些反应过程。
硫酸铵加热分解反应是一种常见的化学反应。
当硫酸铵在高温下加热时,会发生分解反应,生成氨气、水和硫酸氢铵:
(NH4)2SO4(s) → 2NH3(g) + H2SO4(l)
这个反应在硫酸铵生产和储存过程中具有重要意义,因为它可以导致硫酸铵的质量和性能发生变化。
此外,在硫酸铵使用过程中,如农业施肥,了解这
一反应有助于合理控制施肥方法和剂量。
硫酸铵与氢氧化钠加热反应是另一种常见的化学反应。
当硫酸铵与氢氧化钠混合并在高温下加热时,会产生硫酸钠、氨气和水:
2NaOH(s) + (NH4)2SO4(s) → Na2SO4(s) + 2NH3(g) + 2H2O(l)
这个反应在化工生产中具有广泛应用,如生产硫酸钠、硫酸铵等产品。
掌握这个反应方程式有助于优化生产过程,提高产品质量和产量。
总之,硫酸铵加热化学方程式在化学领域具有重要作用。
硫酸铵电子式

硫酸铵电子式
硫酸铵(Ammonium Sulfate)是由硫酸盐和铵结合而成的四水铵盐。
硫酸铵的化学式
为(NH4)2SO4,分子量为132.14g/mol,为结晶状,呈白色或淡黄色,有少量特殊的甜咸味道,易溶于水,但几乎不溶于有机溶剂。
硫酸铵是典型的电离性氯化物,其分子上含有正号与负号离子。
硫酸铵具有多种离子,包括正铵离子(NH4+)和硫酸根(SO42-)。
硫酸铵中的正离子(NH4+)可以通过共价连
接扩散到溶液中,产生电子流动,而硫酸根(SO42-)可以通过氧离子交换扩散到溶液中,从而维持电解质的均衡态。
硫酸铵最早是由英国化学家Joseph Priestley(约瑟夫·普里斯特利)于1777年发
现的。
随后,苏格兰诗人Robert Burns(罗伯特·伯恩斯)于1794年将硫酸铵称为“郁
金香之母”和“园丁之宝”,因此受到很多人的关注,并成为了传统的农药和肥料。
硫酸铵主要用于农业的肥料,其中最常用的形式是晶体。
它可以降低土壤的PH,有助于增加氮的改性效果,促进植物的生长,提高作物的品质和产量。
此外,硫酸铵也可用于
金属表面的清洗和抛光,因为它在低温环境下具有腐蚀缓冲的功能,可以促进铝、钢、铁
和搪瓷表面的清洁和再润滑,以及防止金属腐蚀。
硫酸铵还可用于有机合成和小分子药物的合成。
此外,硫酸铵也可用于催化剂、火力
发电、液体燃料、染料、工业气体、食品、畜牧业等行业。
硫酸铵的不良反应有腹痛、腹泻、头痛、恶心和呕吐等,因此在使用时必须注意防止
中毒。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
硫酸铵
无色结晶或白色颗粒。
无气味。
280℃以上分解。
水中溶解度:0℃时70.6g,100℃时103.8g。
不溶于乙醇和丙酮。
0.1mol/L水溶液的pH为5.5。
相对密度1.77。
折光率1.521。
硫酸铵主要用作肥料,适用于各种土壤和作物。
还可用于纺织、皮革、医药等方面。
别称:硫铵,化学式(NH4)2SO4,分子量132.14,水溶性0℃溶解70.6g。
20℃溶解75.4g,密度1.77
物理性质
InChI=1/2H3N.阿斯顿-5(2,3)4/h2*1H3;(H2,1,2,3,4)
外观与性状:纯品为无色斜方晶体,工业品为白色至淡黄色结晶体。
氮(N)含量:21.0%min
水分:0.2max
游离酸:0.05max
熔点(℃): 230-280℃
沸点(℃):无资料
折射率:n20/D 1.396
硫酸铵分子结构式
相对密度(水=1): 1.77
相对蒸气密度(空气=1): 7.9
饱和蒸气压(kPa):无资料
燃烧热(kJ/mol):无意义
临界温度(℃):无资料
临界压力(MPa):无资料
辛醇/水分配系数的对数值:无资料
闪点(℃):无意义
引燃温度(℃):无意义
爆炸上限%(V/V):无意义
爆炸下限%(V/V):无意义
溶解度:0℃溶解70.6g。
20℃溶解75.4g。
30℃溶解78g。
40℃溶解81g。
化学性质
纯品为无色透明斜方晶系结晶,水溶液呈酸性。
不溶于醇、丙酮和氨水。
有吸湿性,吸湿后固结成块。
加热到513℃以上完全分解成氨气、氮气、二氧化硫及水。
与碱类作用则放出氨气。
与氯化钡溶液反应生成硫酸钡沉淀。
也可以使蛋白质发生盐析。
行业发展
2013年5月24日国内硫酸铵市场波动不大,场内高报低走现象较为普遍。
当日太原钢铁480吨硫酸铵拍卖,起拍价550元/吨,成交于560元/吨,基本体现硫酸铵市场跌势趋缓的状态。
产业洞察研究《中国硫酸铵产业运行态势》统计现华东市场报价未有波动,实单走货较低,其中山东市场低位存620-650元/吨,江浙及安徽市场质量稍差执行至600元/吨;华北硫酸铵市场僵持观望,主流厂家价格继续有所下调,市场高报低走情况较为普遍,内蒙地区弱势运行,主流报盘在450-500元/吨,低端听闻存400元/吨货源,成交一般;华中市场高位基本退市,河南低位630元/吨;东北黑龙江地区新单执行至800元/吨,吉林、辽宁在760-780元/吨;西北及西南硫酸铵市场低迷,走货困难,宁夏、青海多执行500元/吨。
作用与用途
一种优良的氮肥(俗称肥田粉),适用于一般土壤和作物,能使枝叶生长旺盛,提高果实品质和产量,增强作物对灾害的抵抗能力,可作基肥、追肥和种肥。
能与食盐进行复分解反应制造氯化铵,与硫酸铝作用生成铵明矾,与硼酸等一起制造耐火材料。
加入电镀液中能增加导电性。
也是食品酱色的催化剂,鲜酵母生产中培养酵母菌的氮源,酸性染料染色助染剂,皮革脱灰剂。
此外,还用于啤酒酿造,化学试剂和蓄电池生产等。
还有一重要作用就是开采稀土,开采以硫酸铵
作原料,采用离子交换形式把矿土中的稀土元素交换出来,再收集浸出液除杂、沉淀、压榨、灼烧后即成稀土原矿,每开采生产1吨稀土原矿约需5吨硫酸铵。
生物学上的用途也很多,多用于蛋白纯化工艺方面,因为硫酸铵属于惰性物质,不易与其他生物活性物质发生反应,在纯化过程中能最大程度的保护蛋白活性,另外,硫酸铵的可溶性极好,能形成高盐环境,对于蛋白沉淀与后续的高盐纯化做准备。
硫酸铵在零度与常温25度的溶解度有较大区别,以下是硫酸铵在两个温度下不同饱和度的摩尔浓度。
注意事项
危险性
侵入途径:吸入、食入、经皮肤吸收。
健康危害:对眼睛、粘膜和皮肤有刺激作用。
环境危害:长期使用会使土壤出现酸化板结现象。
燃爆危险:本品不燃,具刺激性。
[1]
急救措施
皮肤接触:脱去污染的衣着,用大量流动清水冲洗。
眼睛接触:提起眼睑,用流动清水或生理盐水至少冲洗15分钟。
就医。
吸入:脱离现场至空气新鲜处。
如呼吸困难,给输氧。
就医。
食入:饮足量温水,催吐。
就医。
[1]
消防措施
危险特性:受热分解产生有毒的烟气。
有害燃烧产物:氮氧化物、硫化物。
灭火方法:消防人员必须穿全身防火防毒服,在上风向灭火。
灭火时尽可能将容器从火场移至空旷处。
[1]
泄漏应急处理
应急处理:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘面具(全面罩),穿防毒服。
用洁净的铲子收集于干燥、洁净、有盖的容器中,转移至安全场所。
若大量泄漏,收集回收或运至废物处理场所处置。
[1]
操作处置储存
操作注意事项:密闭操作,局部排风。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶手套。
避免产生粉尘。
避免与酸类、碱类接触。
搬运时要轻装轻卸,防止包装及容器损坏。
配备泄漏应急处理设备。
倒空的容器可能残留有害物。
储存注意事项:储存于阴凉、通风的库房。
远离火种、热源。
应与酸类、碱类分开存放,切忌混储。
储区应备有合适的材料收容泄漏物。
[1]使用注意事项
(1)不能与其他碱性肥料或碱性物质接触或混合施用,以防降低肥效。
(2)不宜在同一块耕地上长期施用硫酸铵,否则土壤会变酸造成板结。
如确需施用时,可适量配合施用一些石灰或有机肥。
但必须注意不能和石灰混施,以防止硫酸铵分解,造成氮素损失。
一般两者的配合施用要相隔3~5 天。
(3)不适于在酸性土壤上施用。
由氢氧化铵和硫酸中和后,结晶、离心分离并干燥而得。
制备
工业上采用氨与硫酸直接进行中和反应而得,用得不多,主要利用工业生产中副产物或排放的废气用硫酸或氨水吸收(如硫酸吸收焦炉气中的氨,氨水吸收冶炼厂烟气中二氧化硫,卡普纶生产中的氨或硫酸法钛白粉生产中的硫酸废液)。
也有采用石膏法制硫铵的(以天然石膏或磷石膏、氨、二氧化碳为原料)。
[3]
生成方法
由氢氧化铵和硫酸中和后,结晶、离心分离并干燥而得。
中和法氨与硫酸约在100℃下进行中和反应,生成的硫酸铵结晶浆液经离心分离、干燥,制得硫酸
铵成品。
其2NH
3+H
2
SO
4
→(NH
4
)
2
SO
4
回收法由炼焦炉气回收氨气,再与硫酸进行中
和反应而得。
