一锅法合成2-氨基苯并噻唑技术
一锅法合成氨基噻唑类化合物

一锅法合成氨基噻唑类化合物氨基噻唑类化合物是一类具有广泛生物活性的化合物,经常用于药物、农药、染料等领域。
合成氨基噻唑类化合物的方法很多,其中以一锅法合成最为方便、高效、经济。
本文将介绍一锅法合成氨基噻唑类化合物的步骤及反应机制。
一、实验原理一锅法合成氨基噻唑类化合物是利用无机碳源、硫源、芳香醛、胺基酸以及含硝基的化合物,并在有机溶剂、溶剂催化剂、辐射条件下进行反应。
其中,无机碳源和硫源是合成氨基噻唑类化合物的基础原料,芳香醛和胺基酸用于给反应物体系提供亲核靶标。
溶剂催化剂对反应具有重要的催化作用,辐射条件则是加速反应过程的必不可少因素。
二、实验步骤奎宁铂20克、邻硝基苯乙酸5克、异亚硫酸钠16克、L-精氨酸20克、咪唑40克、DMSO200毫升、甲苯160毫升、丙酮150毫升、HCl20毫升。
2、实验过程1)将异亚硫酸钠溶于DMSO中,放到室温下融化。
2)在室温下滴加芳香醛、胺基酸、硝基苯乙酸、咪唑溶液并用辐射加热,反应10分钟。
3)加入无水甲醛,并调整溶液的pH值。
4)加入氯化铂催化剂,并进行搅拌,使反应物充分混合。
5)反应完后,用氨水调节pH值并滤掉沉淀,洗至pH>7.0。
6)将干燥后的产物在80℃下结晶,得到氨基噻唑类化合物晶体。
三、实验结果经过一锅法合成反应后,得到氨基噻唑类化合物,其结构式如图所示:氨基噻唑类化合物具有广泛的生物活性,包括抗菌、抗病毒、抗肿瘤、降脂、保肝、降血糖、调节免疫等多种作用。
因此,这种方法的一锅合成法在药物、农药、染料等领域具有广泛应用前景。
四、实验注意事项1)操作时应注意安全,避免溶剂乙醇等易燃易爆物质的温度过高。
2)加入无机物时,过量使用可能导致反应物过度吸氧反应导致产物不纯。
3)反应物在辐射条件下反应时,应保证反应体系保持在良好的循环条件下,以充分加速反应。
4)反应物可能会沉淀,因此应随时将反应液体的温度、颜色、颗粒等物理指标观察并及时调整反应条件。
2_氨基_苯并噻唑水解制备2_氨基苯硫酚的研究_严间浪

1.1 仪器与设备 核磁共振仪: AVANCE DMX 500 ( TMS 内标) ;
收稿日期: 2007- 12- 10 作者简介: 严间浪(1967- ), 男, 工程师, 从事医药中间体方面研究。
红外光谱仪: NICOLET 360FT- IR; GC- MS: 安捷伦 6890N/5975MSD; 恒温组合搅拌器( 常州国华) 1.2 2- 氨基- 苯并噻唑直接水解制备邻氨基苯硫酚
[6]Kinstler Robert C, Barker Robert S, Brunnstrom Gosta. Pelletized benzothiazolyldisulfide - Aminothiophenol composition as vulcanization accelerator[P]. CA: 622121, 1961- 06- 13.
[1]Choudary Boyapati Manoranjan, Chowdari Naidu Sreenivasa. Preparation of diltiazem useful to treat angina involves synthesizing (2R,3S)- (- )- ethyl- 2,3- Dihydroxy- 3- (4- methoxyphenyl)propionate using multifunctional catalyst, ring opening of the cyclic sulfite by 2 - aminothiophenol and cyclization [P]. CH:695998, 2006- 11- 15.
[7]Davis Arnold R, Hook Edwin O. Zinc salt of acylated Aminothiophenol used as a plasticizer in rubber[P],CA: 548651, 1957- 11- 12.
一锅法合成2-氨基苯并噻唑技术

“一锅法”合成2-氨基苯并噻唑技术一. 简介苯并噻唑及其衍生物由于具有很强的分子可极化率,对外场响应灵敏、光谱响应范围大,是一类重要的功能化合物,它在非线性光学、电致发光和光致变色材料等方面有着重要的应用前景,此外,苯并噻唑及其衍生物还具有独特的抗感染和抗肿瘤的特性,因而受到人们的极大关注。
2-氨基苯并噻唑是重要的染料中间体,是生产阳离子染料(如阳离子紫3BL 、阳离子紫2RL 等)重要的中间体,同时也是合成3-甲基-2-苯并噻唑酮腙的最重要的中间体,此外,它也是重要的有机合成原料,由于2-氨基苯并噻唑的用途广泛,因而市场的需求量较大。
2-氨基苯并噻唑的合成方法较多,但概括起来主要有两大类合成方法:第一大类合成方法是由邻氨基疏基取代苯与甲酰胺基甲酸缩合反应制得,反应如下:NH 2SH C OHO NH 2+N S NH 2 第二大类合成方法是由苯氨基硫脲合环制得2-氨基苯并噻唑,反应如下: NH-C-NH 2SNS NH 2而苯基硫脲则是由苯胺与硫氰酸盐合成的。
NH-C-NH 2S+NH 4SCNNH 2由于在第一大类合成2-氨基苯并噻唑所用的原料均为苯的二取代化合物,原材料的成本较高,反应收率低(为50%左右),目前,这种合成方法只是停留在理论研究或者是实验室研究阶段,还无法应用于工业化生产。
因此,目前工业化生产2-氨基苯并噻唑基本上采用的是第二类合成方法,即先以苯胺和硫氰酸盐合成出苯基硫脲盐,再用碱中和苯基硫脲盐得到苯基硫脲,然后进行多次过滤-洗涤-再过滤,最后进行烘干得到中间体——苯基硫脲;苯基硫脲溶解在溶剂中,再在催化剂作用下合环得到2-氨基苯并噻唑。
二、原有生产工艺中所存在的问题尽管目前工业化生产2-氨基苯并噻唑基本上采用的是通过合成苯基硫脲再进行合环的方法,但这种方法均存在着一定的问题。
1.苯基硫脲合成工艺中存在的问题合成苯基硫脲的主要方法有硫氰酸盐法和二苯基硫脲法硫氰酸盐法合成苯基硫脲的反应如下:NH-C-NH 2S NaSCN NH 2H 2SO 43NH 212H 2SO 4CHCl 3反应是以氯仿为溶剂,毒性大,成本高,而氯仿不仅对大气层中的臭氧层有很大的危害,在合成结束时要进行溶剂回收,增加了设备的投入和溶剂回收时的损失,增加了生产成本。
一锅法合成氨基噻唑类化合物

一锅法合成氨基噻唑类化合物作者:石杰来源:《科技资讯》2019年第07期摘; 要:氨基噻唑类化合物具有较强的生理活性和药理活性,并且是良好的有机合成中间体。
该研究直接利用苯环上含有不同取代基的苯基乙酮作为反应底物,二甲基亚砜作为绿色的氧化剂和苯基硫脲发生一锅法反应,以较高的收率得到了一系列氨基噻唑类化合物。
为了优化反应条件,我们同时探索了在其他氧化剂和溶剂存在下对该反应进度的影响。
关键词:一锅法; 苯乙酮; 氨基噻唑类化合物中图分类号:O626.25; ; ; ; ; ; ; ; ; ; ; ; ; ; ; 文献标识码:A; ; ; ; ; ; ; ; ; ; ; ; ; 文章编号:1672-3791(2019)03(a)-0248-02Abstract: Aminothiazole compounds have strong physiological and pharmacological activities and are good intermediates for organic synthesis. In this study, a series of aminothiazoles were synthesized from acetophenone with different substituents on the benzene ring, dimethyl sulfoxide as green oxidant and phenylthiourea in one pot reaction with high yield. In order to optimize the reaction conditions, we also explored the effect of other oxidants and solvents on the reaction progress.Key Words: One-pot; Acetophenone; Aminothiazoles氨基噻唑类化合物具有较强的生理活性和药理活性,如杀菌、消炎、降血脂[1-3]等功效。
2-芳氨基-1,3-噻唑的合成综述

一、2-氨基苯并噻唑的合成研究进展2-氨基苯并噻唑是一类具有多种生物活性的杂环类化合物,如临床用于治疗肌萎缩性脊髓侧索硬化症的利鲁唑(Figure 1-1,A)就属于2-氨基苯并噻唑类化合物;化合物B即夫仑替唑(Frentizole),具有抗病毒、驱肠虫及免疫抑制等活性;N-酰基取代的2-氨基苯并噻唑化合物 C 可以抑制HIV 病毒;N-芳基取代的2-氨基苯并噻唑化合物 D 具有较强的抗癌活性。
2-氨基苯并噻唑还广泛用于抗菌、抗病毒、抗炎;治疗帕金森病、糖尿病等药物的研发中。
因此,2-氨基苯并噻唑在药物化学中占有非常重要的地位。
(一)氧化分子内环化芳基硫脲分子内氧化环化反应合成2-氨基苯并噻唑即Hugerschoff反应。
1901年,Hugerschoff报道了在氯仿介质中液溴可以使芳基硫脲发生分子内的环化反应得到2-氨基苯并噻唑。
Hugerschoff反应为氧化环化,氧化剂的作用是使硫原子转化为亲电中心,进攻富电子的芳环。
早期使用的氧化剂大都是液溴,不仅毒性大,腐蚀性强,也不易操作。
此后,不断有改进的Hugerschoff反应报道。
2003 年,Alfonzo D. Jordan 用稳定性好固态的苄基三甲基三溴化铵代替(BnNMe3Br3)液溴,成功实现了苯基硫脲的分子内环化得到相应的2-氨基苯并噻唑。
该反应可以在室温下进行,以醋酸或二氯甲烷作为反应介质效果最好,BnNMe3Br3用量为 1 当量。
但是,间位取代基的苯硫脲环化产物有区域异构体,即会同时生成5-位取代和7-位取代的2-氨基苯并噻唑(Scheme 1-1)。
(二)C-H活化分子内环化与芳基硫脲氧化分子内环化法合成2-氨基苯并噻唑相比,C-H活化分子内环化不需要强氧化剂,反应条件相对温和。
2009 年,RobertA. Batey 报道了钯催化的苯基硫脲分子内环化反应。
该反应以四(三苯膦)钯和二氧化锰为催化体系,乙腈作为反应介质,在氧气的作用下反应4.5小时(Scheme1-2)。
一种有机合成中间体2-氨基苯并噻唑的合成方法[发明专利]
![一种有机合成中间体2-氨基苯并噻唑的合成方法[发明专利]](https://img.taocdn.com/s3/m/d5e320fd5f0e7cd1852536d9.png)
专利名称:一种有机合成中间体2-氨基苯并噻唑的合成方法专利类型:发明专利
发明人:彭响亮
申请号:CN201710074529.1
申请日:20170210
公开号:CN108409687A
公开日:
20180817
专利内容由知识产权出版社提供
摘要:一种有机合成中间体2‑氨基苯并噻唑的合成方法,主要包括如下步骤:在反应容器中加入3mol的苯胺,12L异丙醇溶液,控制搅拌速度110‑130rpm,加入1.6L盐酸溶液,4—5mol的2‑甲基硫氰苯,升高溶液温度至60—70℃,控制搅拌速度130—150rpm,保持90—120min,降低溶液温度至40—45℃,回流60—80min,放置冷却,析出固体沉淀,将固体沉淀溶于环己烷溶液,减压蒸馏,收集80—90℃的馏分,加入8L草酸溶液,降低溶液温度至10‑‑16℃,析出晶体,过滤,晶体用三乙胺溶液洗涤,乙二醇二甲醚溶液洗涤,脱水剂脱水,在50—58℃温度干燥,得成品2‑氨基苯并噻唑。
申请人:成都中恒华铁科技有限公司
地址:610041 四川省成都市高新区天府大道中段1388号1-5号
国籍:CN
更多信息请下载全文后查看。
一锅法合成氨基噻唑类化合物

一锅法合成氨基噻唑类化合物氨基噻唑类化合物是一类重要的有机化合物,具有广泛的生物活性和药理学效应,被广泛应用于药物、农药、染料、材料科学等领域。
由于其重要性,研究人员一直在探索更高效的合成方法。
一锅法合成氨基噻唑类化合物是一种有效的合成策略,该方法可以实现多步反应的连续进行,不需要中间纯化步骤,提高了合成效率和产物纯度。
本文将介绍一锅法合成氨基噻唑类化合物的研究进展和实验步骤。
一锅法合成是指将多步反应在同一反应容器中进行,中间产物不需要分离和纯化,直接进行下一步反应,最终得到目标产物。
一锅法合成氨基噻唑类化合物的原理是通过串联反应将含硫原料、醛酮、氨化合物依次加入反应容器中,经过一系列的化学反应,生成氨基噻唑类化合物。
这种合成策略有效地减少了中间产物的纯化和分离步骤,提高了合成效率和产物纯度。
1. 原料准备:首先准备合成氨基噻唑类化合物的原料,包括含硫原料、醛酮和氨化合物。
其中含硫原料可以选择环己烷硫醇、巯基乙酸酯等;醛酮可以选择丙酮、苯甲醛等;氨化合物可以选择甲胺、乙胺等。
2. 反应条件优化:针对所选原料,优化反应条件,包括反应温度、反应时间、催化剂选择等。
通过实验确定最佳的反应条件,保证合成反应的高效进行。
3. 反应串联:将含硫原料、醛酮和氨化合物按照一定的摩尔比例依次加入反应容器中,控制反应温度和时间,进行串联反应。
在反应过程中,实时监测反应物的消耗和产物的生成情况。
4. 产物纯化:经过一系列的化学反应后,得到目标产物。
可以通过结晶、萃取、柱层析等手段对产物进行纯化,得到高纯度的氨基噻唑类化合物。
5. 结果分析:最后对合成产物进行结构表征和性质测试,包括核磁共振谱、红外光谱、质谱分析等,验证目标产物的结构和纯度。
通过以上实验步骤,可以高效地合成氨基噻唑类化合物,得到高纯度的产物。
一锅法合成氨基噻唑类化合物的优势在于简化了合成工艺,提高了合成效率,缩短了反应时间,适用于工业化生产。
在药物领域,氨基噻唑类化合物被广泛用作抗菌药物、抗肿瘤药物等,具有重要的临床应用前景。
_一锅法_合成2_氨基苯并噻唑的工艺研究_袁立丽
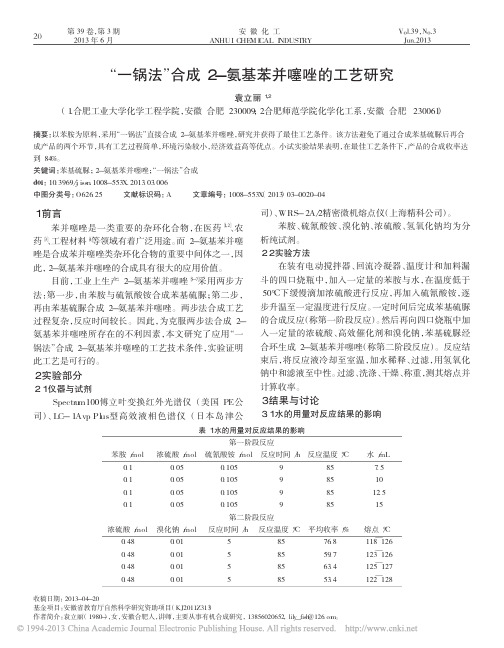
系统名称设备号技改前技改后每小时节电量kw节电率总管流量m3h总管压力mpa运行电流a运行功率kw总管流量m3h总管压力mpa运行电流a运行功率kw硫酸1系统13200211380022硫酸2系统12500221300024热电系统12500231618158130002118410342781643b泵c泵a泵b泵a泵320322310310187921780417870180722102051188211449691635536735621922612273127125597536313296表1某化肥企业循环水系统节能技改前后运行数据向本刊投稿可直接发至编辑部邮箱ahhgzz163com并注明作者联系方式
20
第 39 卷,第 3 期 2013 年 6 月
安徽化工 ANHUI CHEMICAL INDUSTRY
Vol.39,No.3 Jun.2013
“一锅法”合成 2- 氨基苯并噻唑的工艺研究
袁立丽 1,2 (1. 合肥工业大学化学工程学院,安徽 合肥 230009;2.合肥师范学院化学化工系, 安徽 合肥 230061)
4 产品表征
4.1 产品熔点的测定 产品在未精制的条件下,用精密微机熔点仪测定其
熔点为 129 ℃~131 ℃,达到文献值(文献值:129℃~ 130℃)。 4.2 产品红外谱图的测定
22
总第 183 期 2013 年第 3 期(第 39 卷)
6-硝基-2-氨基苯并噻唑的生产工艺

6-硝基-2-氨基苯并噻唑的合成一,2-氨基苯并噻唑(一)苯基硫脲合成(1)开底阀及夹套蒸汽加热,干燥反应系统。
(2)关底阀,并将反应系统冷却到室温。
(3)开启冷却水系统。
(4)用真空吸入三氯甲烷及苯胺,然后开动搅拌,由计量槽滴加98%浓硫酸,滴加时间3-5hr,滴加硫酸温度<80℃。
(5)滴加硫酸时注意控制pH,以广泛试纸进行测定成盐终点,pH1-2,若pH不到则不加硫酸,pH过低时用苯胺补加法升高pH,pH值应保持0.5hr不变,此时釜内液体逐渐转为白色苯胺硫酸盐,物料较厚。
(6)然后在釜内加入硫氰化钠,硫氰化钠必须干燥后小块加入,加完后搅拌1-2hr。
(7)关闭人孔,开启蒸汽阀门,水浴加热使反应物系统呈回流状态,温度约为58-60℃,在此温度下(回流)反应5-8hr。
(8)保温30hr后,回收三氯甲烷,当回收三氯甲烷约300L时,加入冰水500L。
(9)继续回收氯仿,此时温度上升,当反应釜内温度达到110-112℃时,保持30min。
(10)30min后停止回收氯仿,继续在此温度反应15min。
(11)开启人孔,此时应无氯仿味,再缓慢将水加入釜内至满釜,搅拌0.5hr 后放去热水,开冷水系统冷却至30℃左右,此时有大量固体析出,过滤,弃去滤液,滤饼并用水洗至中性。
(12)将洗净的滤饼在80-85℃干燥后得到约160kg左右,含量>90%的苯基硫脲。
(二)缩合闭环及精制(2)关闭底阀,并将反应系统冷却至室温。
(3)在釜内投入98%硫酸。
(4)启动搅拌分批加入含水量<2%的苯基硫脲,加料温度<80℃。
(5)加完后在80-85℃保温搅拌1hr,以使反应物溶解,然后开启冷却系统,反应物温度降至50℃以下。
(6)当反应釜内温度降至50℃以下时滴加工业溴素,滴加温度不超过50℃,加溴时间为3-4hr。
(7)加完后搅拌0.5hr(无自升温现象时,卸去冷却系统)。
(8)小心缓慢在夹套放入自来水,并开启蒸汽,在1hr内升温到55℃,然后在55-60℃保温1hr。
一锅法合成氨基噻唑类化合物

一锅法合成氨基噻唑类化合物氨基噻唑类化合物广泛应用于药物、农药、染料和功能材料等领域,具有重要的科研和工业应用价值。
本文介绍了一种简便、高效的一锅法合成氨基噻唑类化合物的方法及其机理。
氨基噻唑类化合物具有独特的分子结构和多样的生物活性,因此在药物研发和农药开发等领域具有广阔的应用前景。
传统的氨基噻唑类化合物合成方法多步骤、反应条件较为苛刻,而一锅法合成则具有操作简单、环境友好、高收率和高选择性等优点,因此备受关注。
一锅法合成氨基噻唑类化合物的方法主要通过缩合反应实现,其基本步骤包括:硫代硝酸酯与胺的反应、胺与醛/酮的缩合反应、脱保护反应。
以下将对这几个步骤进行详细介绍。
第一步是硫代硝酸酯与胺的反应。
将硫代硝酸酯与胺在碱性条件下加热反应,生成对应的硫代噻唑类化合物。
硫代硝酸酯与胺反应得到硫代噻唑。
第二步是胺与醛/酮的缩合反应。
将胺与醛/酮在溶剂中加热反应,经过缩合反应生成酰胺。
胺与醛反应得到酰胺。
第三步是脱保护反应。
将酰胺中的保护基脱除,得到最终的氨基噻唑类化合物。
通过还原反应脱除酰胺的保护基。
一锅法合成氨基噻唑类化合物的合成机理主要包括硫化反应、缩合反应和脱保护反应。
硫化反应中,硫代硝酸酯通过鸟氨酸的存在分解生成硫酸根离子和亲电烷。
硫酸根离子与亲电烷发生亲核反应,形成硫醚。
缩合反应中,胺与醛/酮发生亲核加成反应,生成亲核加合物。
脱保护反应通过还原酰胺的保护基,得到最终的氨基噻唑类化合物。
一锅法合成氨基噻唑类化合物是一种简便、高效的方法,具有广泛的应用前景。
通过对硫代硝酸酯与胺的反应、胺与醛/酮的缩合反应和脱保护反应的研究,我们可以进一步优化合成条件,提高产率和选择性,推动氨基噻唑类化合物的应用研究。
一锅法合成氨基噻唑类化合物

一锅法合成氨基噻唑类化合物
1.引言
氨基噻唑类化合物是具有重要生物活性的化合物,广泛应用于药物、杀菌剂、抗癌药物、染料等领域。
氨基噻唑类化合物的合成方法多种多样,但对于研究人员来说,找到简单、有效的合成方法是非常重要的。
本文将介绍一种简单、高效、经济的一锅法合成氨基噻唑类化合物的方法,该方法采用无水氨气和硫脲等原料,经过多步反应,得到目标产物。
该方法反应条件温和、原料易得、无毒副产物等优点,为氨基噻唑类化合物的合成提供了一种新思路。
2.实验
2.1 材料
无水氨气、硫脲、2-氯基苯甲醛、醋酸、氯化亚铜、硫酸、氢氧化钠、氢氧化铵、乙醇。
2.2 合成步骤
2.2.1 合成2-氯基-2-(2-甲氧基苯基)乙醛
加入2-氯基苯甲醛(1.0 mol)、2-甲氧基苯甲醇(1.2 mol)和氯化亚铜(0.1 mol)于醋酸中,室温下进行搅拌。
反应结束后,加入氢氧化铵于反应液中,得到粗产物。
将粗产物以水为溶剂进行冷浸提,得到白色固体产物。
将产物(0.5 mol)加入无水氨气中,反应至气体吸收结束,得到粗产物。
将粗产物以乙醇为溶剂重结晶两次,得到精制产物。
3.结果与分析
本实验在温和的反应条件下,用无水氨气和硫脲合成了氨基噻唑类化合物,总收率达到76%(按2-氯基苯甲醛计算)。
产物纯度经过重结晶达到98%以上,符合工业生产用途。
4.结论。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
“一锅法”合成2-氨基苯并噻唑技术
一. 简介
苯并噻唑及其衍生物由于具有很强的分子可极化率,对外场响应灵敏、光谱响应范围大,是一类重要的功能化合物,它在非线性光学、电致发光和光致变色材料等方面有着重要的应用前景,此外,苯并噻唑及其衍生物还具有独特的抗感染和抗肿瘤的特性,因而受到人们的极大关注。
2-氨基苯并噻唑是重要的染料中间体,是生产阳离子染料(如阳离子紫3BL 、阳离子紫2RL 等)重要的中间体,同时也是合成3-甲基-2-苯并噻唑酮腙的最重要的中间体,此外,它也是重要的有机合成原料,由于2-氨基苯并噻唑的用途广泛,因而市场的需求量较大。
2-氨基苯并噻唑的合成方法较多,但概括起来主要有两大类合成方法:
第一大类合成方法是由邻氨基疏基取代苯与甲酰胺基甲酸缩合反应制得,反应如下:
NH 2SH C O
HO NH 2+N S NH 2 第二大类合成方法是由苯氨基硫脲合环制得2-氨基苯并噻唑,反
应如下: NH-C-NH 2
S
N
S NH 2
而苯基硫脲则是由苯胺与硫氰酸盐合成的。
NH-C-NH 2
S
+NH 4SCN
NH 2
由于在第一大类合成2-氨基苯并噻唑所用的原料均为苯的二取代化合物,原材料的成本较高,反应收率低(为50%左右),目前,
这种合成方法只是停留在理论研究或者是实验室研究阶段,还无法应用于工业化生产。
因此,目前工业化生产2-氨基苯并噻唑基本上采用的是第二类合成方法,即先以苯胺和硫氰酸盐合成出苯基硫脲盐,再用碱中和苯基硫脲盐得到苯基硫脲,然后进行多次过滤-洗涤-再过滤,最后进行烘干得到中间体——苯基硫脲;苯基硫脲溶解在溶剂中,再在催化剂作用下合环得到2-氨基苯并噻唑。
二、原有生产工艺中所存在的问题
尽管目前工业化生产2-氨基苯并噻唑基本上采用的是通过合成苯基硫脲再进行合环的方法,但这种方法均存在着一定的问题。
1.苯基硫脲合成工艺中存在的问题
合成苯基硫脲的主要方法有硫氰酸盐法和二苯基硫脲法
硫氰酸盐法合成苯基硫脲的反应如下:
NH-C-NH 2
S NaSCN NH 2H 2SO 4
3NH 212H 2SO 4CHCl 3
反应是以氯仿为溶剂,毒性大,成本高,而氯仿不仅对大气层中的臭氧层有很大的危害,在合成结束时要进行溶剂回收,增加了设备的投入和溶剂回收时的损失,增加了生产成本。
此外,反应时间过长,需要24小时以上才能完成上述反应。
二苯基硫脲法合成苯基硫脲的反应如下:
+NH 2CS 2
NaOH NHCNH
S HCl NCS NHCNH 2S
NH 4OH
反应需要在较高的压力下才能进行,不仅对设备的要求提高,同时反应工艺路线增加,反应收率较低,此外反应过程中产生大量的废液,污染严重。
2.由苯基硫脲合环制备2-氨基苯并噻唑工艺中存在的问题 由苯基硫脲合环制备2-氨基苯并噻唑的主要方法有氯化硫法和氯化亚砜合环法,其中氯化硫法是由苯基硫脲与氯化硫合环制备2-氨基苯并噻唑,其反应如下所示: NHCHNH 2S
+S 2Cl 2CHCl 3N S NH 2
反应必须在三氯甲烷溶剂中进行,也存在着三氯甲烷回收和对大气层中的臭氧层的危害,此外,还存在操作繁琐、反应时间长、产物收率低(<75%)等缺点。
氯化亚砜合环法制备2-氨基苯并噻唑时的反应如下:
NHCHNH 2S N S NH 2SOCl
2
+NHCNH 2O
该反应虽然收率较高(90%),但存在着需要氯化亚砜的量很大(是苯基硫脲摩尔数的3-4倍),成本高,反应过程中不易控制,易形成粘稠状,同时还伴有苯基脲副产物生成,此外,反应过程中有大量二氧化硫气体产生,环境污染严重。
三、“一锅法”合成2-氨基苯并噻唑新技术
“一锅法” 合成2-氨基苯并噻唑新技术,主要是针对现有工业上采用的两步法合成2-氨基苯并噻唑中所存在的工艺过程复杂、污染严重、需要大量的有机溶剂等问题开发出来的。
该技术采用水代替高成本、有毒的有机溶剂,以苯胺和硫氰酸铵为原料合成苯基硫脲,再经过合环制得2-氨基苯并噻唑。
“一锅法”合成2-氨基苯并噻唑工艺条件如下:
1. 各种原材料配比及规格:
(1)苯胺 93g ,含量≥ 99%;
(2)硫氰酸铵84g ,含量≥ 99%;
(3)98%浓硫酸290ml ;
(4)溴化钠8.6g,含量≥99%;
(5)催化剂5g;
(6)水125g;
2. 原材料检测方法
(1)苯胺:苯胺的检测方法按GB2961—91标准进行;
(2)硫氰酸铵:硫氰酸铵的检测方法按HG/T 2154-2004标准执行;
(3)溴化钠:溴化钠的检测方法按HG/T 3809-2006标准执行。
3. 操作方法及合成工艺
(1)在装有电动搅拌、冷凝器(减压蒸馏器)、固体(液体)加料口、(温度计)的玻璃反应器中,分别加入水、苯胺,在搅拌和冷却条件下慢慢滴加浓硫酸进行反应,浓硫酸滴加完毕,搅拌然后分次加入硫氰酸铵,加料结束,然后升温至反应直到结束。
(2)控制温度分次加入催化剂(先将溴化钠与催化剂混合均匀),然后慢慢升温反应;反应结束后加水搅拌冷却,并将不溶物过滤,然后用氢氧化钠慢慢调节滤液的pH,过滤、洗涤、干燥,得到2-氨基苯并噻唑产品,产品的收率大于80%,熔点大于125℃,纯度大于94%(厂家提供的样品纯度大于93%)。
,。
