实用文档之消毒剂证件审核登记表
消毒产品、一次性医疗用品证件审核登记表
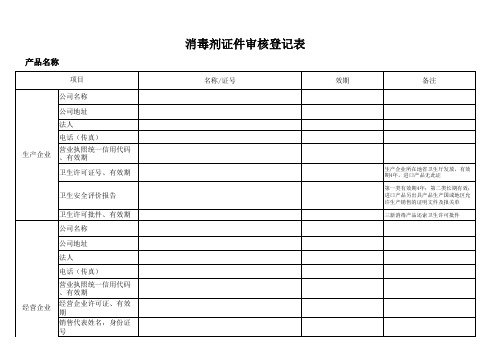
消毒剂证件审核登记表 产品名称
备注:一、卫生安全评价报告包括:(一)产品标签(铭牌)、说明书、检验报告(含结论)、企业标准或质量标准、国产产品生产企业卫生许可资质、进口产品生产国(地区)允许生产销售的批文情况及报关单。
(二)其中,消毒剂、生物指示物、化学指示物、带有灭菌标识的灭菌物品包装物、抗(抑)菌制剂还包括产品配方,消毒器械还应包括产品主要元器件、结构图。
三、产品标签(铭牌)、说明书,企业标准或质量标准,国产产品生产企业卫生许可资质、进口产品生产国(地区)允许生产销售的批文情况及报关单,原件或复印件均可;检验报告(含结论),产品配方,消毒器械主要元器件、结构图为原件,复印件应由产品责任单位加盖公章。
四、使用A4纸打印,按顺序排列,逐页加盖产品责任单位公章,并装订成册。
含氯消毒剂使用登记表

名称
清洁与初步处理
体温表
备皮刀架
浸泡于500mg/L有效氯消毒液>10分钟,清水冲净、擦干备用。
吸氧面罩、麻醉面罩;胃肠减压器、吸引器
引流瓶;保温箱
浸泡于500mg/L含氯消毒液30分钟,清水冲净,晾干,干燥保存备用
氧气湿化瓶、呼吸机和麻醉机的螺旋纹管;压舌板,开口器,舌钳子,压脉带
地面
一般病室、办公室、治疗室、换药室走廊等,当地面无污染时,用清水拖地每日两次;当有血液、分泌物、排泄物时,先用吸湿材料去除可见污染物,再用500mg/L含氯消毒液擦拭,作用30分钟。
备注:1、所有的消毒都是在清洁的基础上进行。
2、消毒液现用现配,含氯消毒液使用前用G-1测试纸测试浓度。
感染管理科
2014.9.15
消毒供应中心统一处置
网套、
血压计袖带
用后在500mg/L有效氯消毒液中浸泡30分钟,中浸泡30分钟,清洗后备用。
拖把
用后在500mg/L有效氯消毒液中浸泡30分钟,清洗后备用。
室内用品表面
一般病室、治疗室、换药室、处置室的操作台、换药车、墙壁、无菌柜、药品柜门把手等,当表面无污染时,用250 mg/L含氯消毒剂每日擦拭两次;当表面受到病原菌污染时,用500mg/L的含氯消毒剂擦拭。
医院一次性使用无菌医疗用品有效证件审核登记表
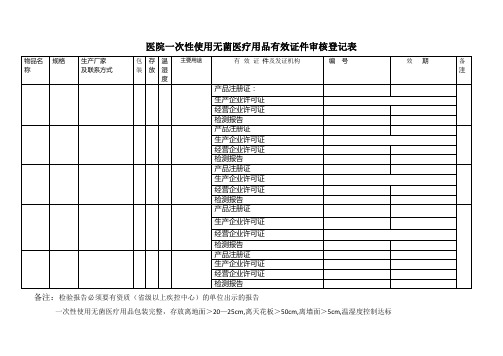
医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标医院一次性使用无菌医疗用品有效证件审核登记表备注:检验报告必须要有资质(省级以上疾控中心)的单位出示的报告一次性使用无菌医疗用品包装完整,存放离地面>20—25cm,离天花板>50cm,离墙面>5cm,温湿度控制达标。
消毒剂生产现场审核表

消毒剂生产现场审核表(最新版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日消毒剂生产现场审核表┌──────┬────────────┬──────────┬──────────────┐│产品名称││剂型││├──────┼────────────┼──────────┼──────────────┤│生产单位名称││卫生许可证号││├──────┼────────────┼──────────┼──────────────┤│生产地址││邮编││├──────┼────────────┼──────────┼──────────────┤│联系人││电话││├──────┴────────────┴──────────┴─────┬────────┤│申报产品的类别是否与企业卫生许可的类别相适应│是()否()│├────────────────────────────────────┼────────┤│现场相关生产线和生产条件是否与提交的生产工艺一致│是()否()│├────────────────────────────────────┼────────┤│提交的配方中各原料名称、规格、级别、纯度是否与现场原料一致│是()否()│├────────────────────────────────────┼────────┤│与该产品生产有关的生产设备是否与提交资料中的一致│是()否()│├────────────────────────────────────┼────────┤│该产品是否有生产过程记录│是()否()│├────────────────────────────────────┼────────┤│样品生产过程记录中记载的所用原料及其加入量是否与提供资料的配方、工艺一致│是()否()│├────────────────────────────────────┼────────┤│原料采购记录中是否有该产品配方原料│是()否()│├────────────────────────────────────┼────────┤│该产品的批号或生产日期是否与生产过程记录中的一致│是()否()│├────────────────────────────────────┼────────┤│成品库中该产品存放数量是否与出入库记录一致│是()否()│├────────────────────────────────────┼────────┤│是否有其他不符合要求的情况(如有请说明,可另附页):│是()否()│││││││││││││├────────────────────────────────────┼────────┤│审核结论:企业所提供资料与现场条件是否相符│是()否()│└────────────────────────────────────┴────────┘注:本表填写应使用钢笔、签字笔,内容应完整、清楚、不得涂改。
有净化要求的消毒剂生产企业现场监督审核表word版本

有净化要求的消毒剂生产企业现场监督审
核表
附件3
有净化要求的消毒剂生产企业
现场监督审核表
生产企业名称_____________________
生产企业地址_____________________
实际生产加工地址_____________________
收集于网络,如有侵权请联系管理员删除
现场监督审核日期年月日
有净化要求的消毒剂生产企业现场监督审核表生产企业一般情况
法定代表人/负责人:卫生管理负责人:检验负责人:
通讯地址:联系电话:邮编:传真:
职工总数:从业人员总数:生产区面积:
产品种类:
收集于网络,如有侵权请联系管理员删除
考评审核表:
收集于网络,如有侵权请联系管理员删除
收集于网络,如有侵权请联系管理员删除
收集于网络,如有侵权请联系管理员删除
收集于网络,如有侵权请联系管理员删除
收集于网络,如有侵权请联系管理员删除
收集于网络,如有侵权请联系管理员删除
收集于网络,如有侵权请联系管理员删除
备注:1. 本表用于有净化要求的消毒剂生产、分装企业现场监督审核。
2. 满足各项及格分,现场监督审核通过。
现场监督审核意见:
现场监督审核人(签名):被审核单位负责人(签名):
单位公章
审核日期:年月日年月日。
消毒剂使用情况登记表 Excel 工作表
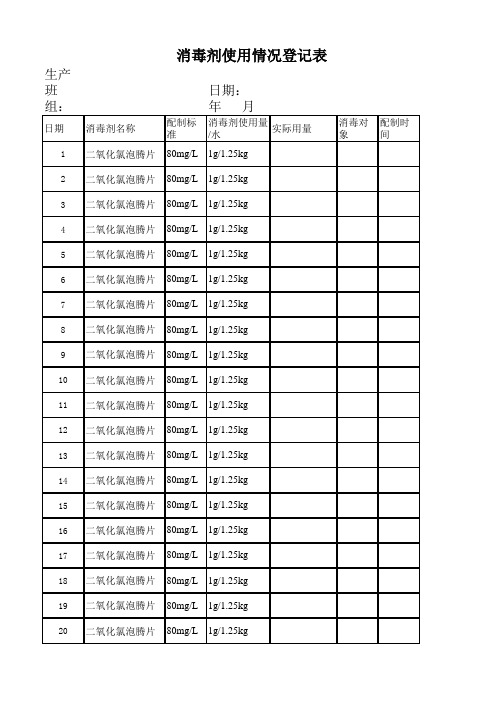
5 二氧化氯泡腾片 80mg/L 1g/1.25kg
6 二氧化氯泡腾片 80mg/L 1g/1.25kg
7 二氧化氯泡腾片 80mg/L 1g/1.25kg
8 二氧化氯泡腾片 80mg/L 1g/1.25kg
9 二氧化氯泡腾片 80mg/L 1g/1.25kg
10 二氧化氯泡腾片 80mg/L 1g/1.25kg
17 二氧化氯泡腾片 80mg/L 1g/1.25kg
18 二氧化氯泡腾片 80mg/L 1g/1.25kg
19 二氧化氯泡腾片 80mg/L 1g/1.25kg
20 二氧化氯泡腾片 80mg/L 1g/1.25kg
21 二氧化氯泡腾片 80mg/L 1g/1.25kg 22 二氧化氯泡腾片 80mg/L 1g/1.25kg 23 二氧化氯泡腾片 80mg/L 1g/1.25kg 24 二氧化氯泡腾片 80mg/L 1g/1.25kg 25 二氧化氯泡腾片 80mg/L 1g/1.25kg 26 二氧化氯泡腾片 80mg/L 1g/1.25kg 27 二氧化氯泡腾片 80mg/L 1g/1.25kg 28 二氧化氯泡腾片 80mg/L 1g/1.25kg 29 二氧化氯泡腾片 80mg/L 1g/1.25kg 30 二氧化氯泡腾片 80mg/L 1g/1.25kg 31 二氧化氯泡腾片 80mg/L 1g/1.25kg
配制人 员
生产 班 组:
日期
1
消毒剂使用情况登记表消毒剂Biblioteka 称配制标 准日期:
年月
消毒剂使用量 /水
实际用量
二氧化氯泡腾片 80mg/L 1g/1.25kg
消毒对 配制时
象
间
2 二氧化氯泡腾片 80mg/L 1g/1.25kg
消毒药械及一次性医疗产品索证管理登记表
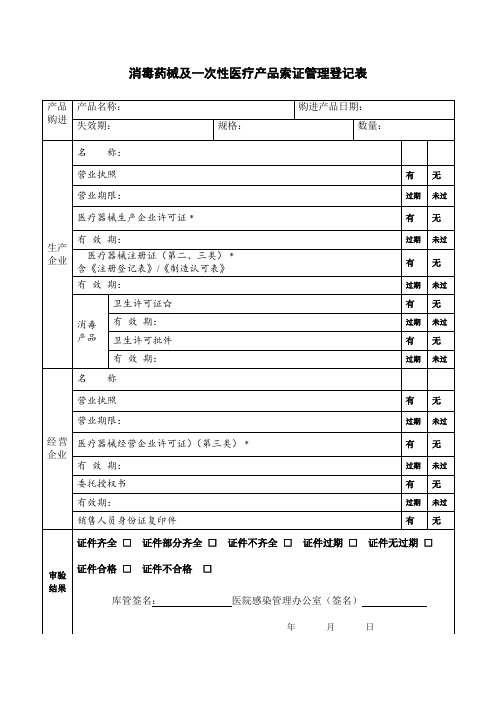
营业执照
有
无
营业期限:
过期
未过
医疗器械经营企业许可证)(第三类)﹡
有
无
有效期:
过期
未过
委托授权书
有
无
有效期:
过期
未过
销售人员身份证复印件
有
无
审验结果
证件齐全□证件部分齐全□证件不齐全□证件过期□证件无过期□
证件合格□证件不合格□
库管签名:医院感染管理办公室(签名)
年月日
消毒药械及一次性医疗产品索证管理登记表
医院感染管理办公室签名年月日医疗器械及消毒产品索证管理登记表产品购进产品名称购进产品的日期供货单位规格数量产品批号失效期消毒或灭菌日期生产企业名称地址电话传真法人营业执照卫生许可证医疗器械生产企业许可证有效期医疗器械注册证有效期经营企业名称地址电话传真营业执照医疗器械经营企业许可证有效期销售人员身份证号手机号委托书有效期审验结果证件齐全证件部分齐全证件不齐全证件有无过期证件合格证件不合格医院感染管理科签名年月日消毒药械及一次性使用医疗器械审核管理登记表产品购进产品名称
医疗器械及消毒产品索证管理登记表
产品购进
产品名称
购进产品的日期
供货单位
规格
数量
产品批号
失效期
消毒或灭菌日期
生ห้องสมุดไป่ตู้企业
名称
地址电话/传真
法人
营业执照
卫生许可证
医疗器械生产企业许可证
有效期
医疗器械
注册证
有效期
经营企业
名称
地址电话/传真
营业执照
医疗器械经营企业许可证
有效期
销售人员身份证号
手机号
委托书有效期
3、消毒药械及一次性无菌医疗器具审核登记表(运行)
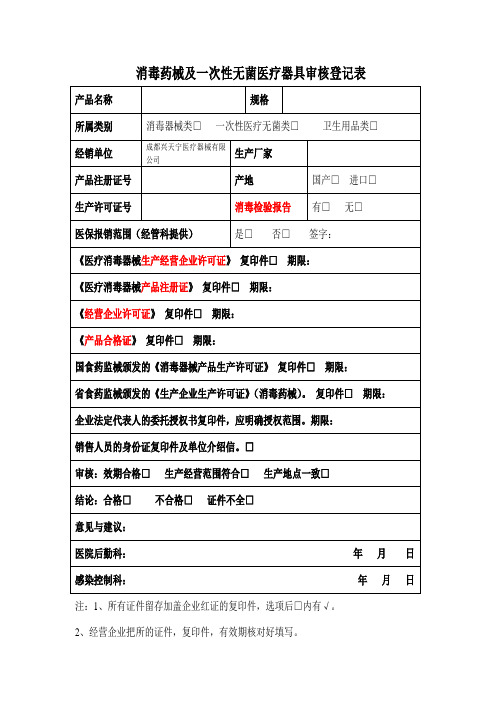
《产品合格证》复印件□期限:
国食药监械颁发的《消毒器械产品生产许可证》复印件□期限:
省食药监械颁发的《生产企业生产许可证》(消毒药械)。复印件□期限:
企业法定代表人的委托授权书复印件,应明确授权范围。期限:
销售人员的身份证复印件及单位介绍信。□
审核:效期合格□生产经营范围符合□生产地点一致□
结论:合格□不合格□证件不全□
意见与建议:
医院后勤科:年月日
感染控制科:年月日
注:1、所有营企业把所的证件,复印件,有效期核对好填写。
消毒药械及一次性无菌医疗器具审核登记表
产品名称
规格
所属类别
消毒器械类□一次性医疗无菌类□卫生用品类□
经销单位
成都兴天宁医疗器械有限公司
生产厂家
产品注册证号
产地
国产□进口□
生产许可证号
消毒检验报告
有□无□
医保报销范围(经管科提供)
是□否□签字:
《医疗消毒器械生产经营企业许可证》复印件□期限:
《医疗消毒器械产品注册证》复印件□期限:
消毒剂生产企业现场监督审核表全集文档

消毒剂生产企业现场监督审核表全集文档(可以直接使用,可编辑实用优质文档,欢迎下载)附件2消毒剂生产企业现场监督审核表生产企业名称_____________________生产企业地址_____________________实际生产加工地址_____________________现场监督审核日期年月日消毒剂生产企业现场监督审核表生产企业一般情况法定代表人/负责人:卫生管理负责人:检验负责人:通讯地址:联系:::职工总数:从业人员总数:生产区面积:产品种类:考评审核表:备注:1. 本表用于消毒剂生产、分装企业现场监督审核。
2. 满足各项及格分,现场监督审核通过。
现场监督审核意见:现场监督审核人(签名):被审核单位负责人(签名):单位公章审核日期:年月日年月日附件2食品、食品添加剂生产许可现场核查评分记录表申请人名称:食品、食品添加剂类别及类别名称:生产场所地址:核查日期:年月日使用说明1.本记录表依据《中华人民共和国食品安全法》《食品生产许可管理办法》等法律法规、部门规章以及相关食品安全国家标准的要求制定。
2.本记录表应当结合相关食品生产许可审查细则要求使用。
3.本记录表包括生产场所(24分)、设备设施(33分)、设备布局和工艺流程(9分)、人员管理(9分)、管理制度(24分)以及试制产品检验合格报告(1分)等六部分,共34个核查项目。
4.核查组应当按照核查项目规定的“核查内容”“评分标准”进行核查与评分,并将发现的问题具体详实地记录在“核查记录”栏目中。
5.现场核查结论判定原则:核查项目单项得分无0分且总得分率≥85%的,该食品类别及品种明细判定为通过现场核查。
当出现以下两种情况之一时,该食品类别及品种明细判定为未通过现场核查:(1)有一项及以上核查项目得0分的;(2)核查项目总得分率<85%的。
6.当某个核查项目不适用时,不参与评分,并在“核查记录”栏目中说明不适用的原因。
一、生产场所(共24分)二、设备设施(共33分)三、设备布局和工艺流程(共9分)四、人员管理(共9分)五、管理制度(共24分)六、试制产品检验合格报告(共1分)附件1饲料添加剂生产许可现场审核表企业名称:生产地址:联系人:联系:审核日期:年月日中华人民共和国农业部制二〇一二年填写说明一、本表用于饲料添加剂生产许可现场审核。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实用文档之"消毒剂证件审核登记表"
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒剂证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒器械证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门消毒器械证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒器械证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
一次性医疗器械、器具证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
一次性医疗器械、器具证件审核登记表
注:此表一式两份,一份留医院感染管理科,一份交采购部门
消毒药械管理记录。
