分析化学》第七章习题答案
第七章习题参考答案

第七章习题参考答案第七章滴定分析法习题解答1.以甲基橙为指示剂,Na2CO3为标准物质,校准HCl溶液的浓度。
如果称取Na2CO3,取Na2CO3 0 1317g,溶解于水中,用HCl溶液滴定,共用23.83ml HCl去除溶液,并尝试寻找HCl溶液的浓度。
解:na2co3+2hcl===2nacl+co2+h2ochcl0。
1317? 2.1.106? 0.1043mol?L323.83? 102.使用草酸(h2c2o42h2o)作为标准物质校准浓度约为0.1mol-1的NaOH标准溶液。
如果滴定过程中消耗的NaOH溶液体积在20~30L范围内,草酸的质量范围是多少?解:2naoh+h2c2o4===na2c2o4+2h2omh2c2o42h2o(1)?20? 10-3? 0.1? 1.126? 0.126g21mh2c2o42h2o(2)?30? 10-3?0.1?? 126? 0.189g23.下列数据各几位有效数字?(1) 7.655(2)6.023×1023(3)4.8×10-10(4)pka=7.20(5)0.01023(6)51.14答:(1)四位(2)四位(3)两位(4)两位(5)四位(6)四位4.应用有效数字规则计算以下公式。
(1)2.3-0.254+789.10=791.75.4?4.32?10-4(2)=4.2-32.354?2.34?10(3)(1.276×4.17)+(1.7×10-4)-(2.176×10-3×1.30×10-2)=5.32-(4)(51.0×4.03×104)+(2.512×2.034×10-3)=0.02565.使用邻苯二甲酸氢钾校准NaOH溶液浓度时,如果在实验过程中出现以下错误,请尝试解释在每种情况下测量的NaOH溶液浓度是否过大或过小。
高教第五版分析化学课后习题及思考题答案第7章

第七章习题7.1 下列情况,有无沉淀生成?(1)0.001mol·L-1Ca(NO3)2溶液与0.01mol·L-1NH4HF2溶液以等体积相混合;(2)0.01mol·L-1MgCl2溶液与0.1mol·L-1NH3-1mol·L-1NH4Cl溶液等体积相混合。
解:(1)已知:K sp(CaF2)=3.4×10-11两溶液等体积混合后:[Ca2+]=5.0×10-4mol·L-1, [F-]=5.0×10-3mol·L-1,[Ca2+][F-]2=5.0×10-4×(5.0×10-3)2=2.5×10-8>K sp(CaF2)=3.4×10-11∴有沉淀生成。
(2)已知:K b(NH3)=1.8×10-5 K sp (Mg(OH)2)=1.8×10-11[Mg2+]=5.0×10-3mol·L-1, [NH3]=0.05mol·L-1, [NH4]=0.5mol·L-1,[OH-]=K b(NH3)×[NH3]=1.8×10-5×0.05=1.8×10-6mol·L-1 [NH4+] 0.5[Mg2+][OH-]2=5.0×10-3×(1.8×10-6)2=1.6×10-14<K sp∵Q <K sp∴无沉淀生成。
7.2 求氟化钙的溶解度:(1)在纯水中(忽略水解);(2)在0.01 mol·L-1CaCl2溶液中;(3)在0.01mol·L-1HCl溶液中。
解:(1)已知:K sp (CaF2)=3.4×10-11,K a(HF)=3.5×10-4[Ca2+][F-]2= s·(2s)2 = 4s3∴s = 2.0×10-4 mol·L-1(2)考虑同离子效应:[Ca2+][F-]2=0.01×(2s)2=3.4×10-11s =2.9×10-5 mol·L-1(3)考虑酸效应:δF-= Ka(HF)=3.5×10-4=3.5×10-2 Ka+[H+] 3.5×10-4+0.01αF-=1=28.6 3.5×10-2[Ca2+][F-]2=[Ca2+][F-]2·α2=K sp·α2s =1.9×10-3 mol·L-17.3 计算PH=5.0,草酸总浓度为0.05 mol·L-1时,草酸钙的溶解度.如果溶液的体积为300mL,将溶解多少克CaC2O4?解: 已知:K a1(H2C2O4)=5.9×10-2,K a2=6.4×10-5 , K sp(CaC2O4)=1.8×10-9M(CaC2O4)=128.1α (H)=1 δ同理得:α=1.16[Ca2+][C2O42-]总= Ksp(CaC2O4) ·αC2O42-s×0.05=1.8×10-9×1.16 s = 4.2×10-8 mol·L-1溶解损失:m(CaC2O4)=4.2×10-8×0.3×128.1=1.6×10-6(g)= 1.6×10-3(mg)7.4 25℃时,铬酸银的溶解度为每升0.0279g,计算铬酸银的溶度积.解: 已知:M(Ag2CrO4)=331.73设:铬酸银(Ag2CrO4)的溶解度为S.s = 0.0279=8.41 ×10-5mol·L-1 331.73K sp =[Ag+]2[CrO42-]=( 2×8.41×10-5)2×8.41×10-5=2.38×10-127.5 为了使0.2032g (NH4)2SO4中的SO42-沉淀完全,需要每升含63g BaCl2·2H2O的溶液多少亳升?解:已知M((NH4)2SO4)=132.14, M(BaCl2·2H2O)2SO4)=244.3考虑问题的思路是,沉淀剂过量20%~50% 。
分析化学课后习题答案 第七章

第七章重量分析法和沉淀滴定法思考题1.沉淀形式和称量形式有何区别?试举例说明之。
答:在重量分析法中,沉淀是经过烘干或灼烧后再称量的。
沉淀形式是被测物与沉淀剂反应生成的沉淀物质,称量形式是沉淀经过烘干或灼烧后能够进行称量的物质。
有些情况下,由于在烘干或灼烧过程中可能发生化学变化,使沉淀转化为另一物质。
故沉淀形式和称量形式可以相同,也可以不相同。
例如:BaSO4,其沉淀形式和称量形式相同,而在测定Mg2+时,沉淀形式是MgNH4PO4·6H2O,灼烧后所得的称量形式却是Mg2P2O7。
2.为了使沉淀定量完全,必须加人过量沉淀剂,为什么又不能过量太多?答:在重量分析法中,为使沉淀完全,常加入过量的沉淀剂,这样可以利用共同离子效应来降低沉淀的溶解度。
沉淀剂过量的程度,应根据沉淀剂的性质来确定。
若沉淀剂不易挥发,应过量20%~50%;若沉淀剂易挥发,则可过量多些,甚至过量100%。
但沉淀剂不能过量太多,否则可能发生盐效应、配位效应等,反而使沉淀的溶解度增大。
3.影响沉淀溶解度的因素有哪些?它们是怎样发生影响的?在分析工作中,对于复杂的情况,应如何考虑主要影响因素?答:影响沉淀溶解度的因素有:共同离子效应,盐效应,酸效应,配位效应,温度,溶剂,沉淀颗粒大小和结构等。
共同离子效应能够降低沉淀的溶解度;盐效应通过改变溶液的离子强度使沉淀的溶解度增加;酸效应是由于溶液中H+浓度的大小对弱酸、多元酸或难溶酸离解平衡的影响来影响沉淀的溶解度。
若沉淀是强酸盐,如BaSO4,AgCl等,其溶解度受酸度影响不大,若沉淀是弱酸或多元酸盐[如CaC2O4、Ca3(PO4)2]或难溶酸(如硅酸、钨酸)以及与有机沉淀剂形成的沉淀,则酸效应就很显著。
除沉淀是难溶酸外,其他沉淀的溶解度往往随着溶液酸度的增加而增加;配位效应是配位剂与生成沉淀的离子形成配合物,是沉淀的溶解度增大的现象。
因为溶解是一吸热过程,所以绝大多数沉淀的溶解度岁温度的升高而增大。
分析化学作业5(第七章)参考答案

7-1 解释下列现象:(简明扼要即可,必要时可配合公式)(1)将氯水慢慢加入到含有Br -和I -的酸性溶液中,以CCl 4萃取后,CCl 4层变为紫色。
答:查附录9可得以下数据V 545.0V 05.1V36.1V 45.1I /I Br /Br Cl/ClCl /HClO 332=ϕ=ϕ=ϕ=ϕθθθθ------ 可知氯水中的Cl 2及HClO 可将酸性溶液中的I -和Br -氧化为I 2和Br 2,I 2和Br 2更易溶于CCl 4,故可被CCl 4萃取,使CCl 4层呈紫色(I 2的紫色比Br 2的棕红色明显)。
(2)V 159.0V 534.0Cu /Cu I/I22=ϕ>=ϕθθ++-,但是Cu 2+却能将I -氧化为I 2。
答:12sp Cu /Cu CuI /Cu 101.11lg 059.0159.0)CuI (K 1lg059.022-θθ⨯+=+ϕ=ϕ+++ V 534.0V 865.0I /I 3=ϕ>=θ--(具体计算过程不必列出,只回答原因即可) 即Cu +可与I -生成溶解度很小的CuI 沉淀(pK sp =11.96)而大大降低了溶液中Cu +的浓度,从而使得Cu 2+/Cu +的电极电位显著增高,以致可将I -氧化为I 2。
(3)Fe 2+的存在加速KMnO 4氧化Cl -的反应。
答:Mn VII 氧化Cl -的反应很慢,通常可认为难以发生。
但体系中若有Fe 2+共存,则Mn VII 氧化Fe 2+的过程中可形成一系列Mn 的中间产物:Mn VI 、Mn V 、Mn IV 、Mn III ,它们均可较快的氧化Cl -,因此可诱导Cl -被Mn VII 氧化的速率加速。
(4)以KMnO 4滴定-222O C 时,滴入KMnO 4的红色消失速度由慢到快。
答:KMnO 4 与 C 2O 42-的反应速度很慢,但反应产物Mn II 可催化该反应。
开始反应时,由于没有或仅含极少量的Mn II ,故反应速度很慢,KMnO 4的红色消失得很慢;但随着反应进行,Mn II 不断产生,使得反应越来越快,KMnO 4红色消失速度亦逐渐加快。
分析化学分析化学第七章 习题参考答案

第七章 习题参考答案14解:铝氟络合物的各累积形成常数lgβ1-lgβ6分别为:6.13,11.15,15.00,17.75,19.37,19.84665544332210][][][][][][113------++++++==+F F F F F F Al ββββββδδ6184.195137.194175.173100.152115.11113.6)10(10)10(10)10(10)10(10)10(10101011------⨯+⨯+⨯+⨯+⨯+⨯+=56.1484.1337.1475.1300.1215.913.51010101010101011-=++++++=可见,上式分母中第六项数值最大,故溶液中浓度最大的型体为AlF 52-。
19.05137.1956.14550510)10(1010][25----=⨯===-F AlF βδδδ[Al 52-]=5δ•C=10-0.19×0.010=10-2.19mol •L -1(6.5×10-3 mol •L -1)15解:Ni(NH 3)32+、Ni(NH 3)42+的累积形成常数分别为:lgβ3=6.77, lgβ4=7.963323233]][[])([NH Ni NH Ni ++=β4324243]][[])([NH NiNH Ni ++=β 依题意:[Ni(NH 3)42+]=10[Ni(NH 3)32+] 故33234324]][[10]][[NH Ni NH Ni ++=ββ [NH 3]=65.01010101010119.096.777.643=⋅=⨯=--L mol ββ mol•L -117解:(1)101004.01000.009.100/1005.03-⋅==L mol C COC a 0.01004×25.00=C EDTA ×24.90 C EDTA =0.01008 mol•L -1(2) T EDTA/ZnO = a/b mL g M C ZnO EDTA ⋅⨯=⨯⨯⨯=⨯---43310203.81038.8101008.0110因EDTA ≌Fe ≌3221O F e故 32/O F EDTA e T = a/b mL g M C O F EDTA e ⋅⨯=⨯⨯⨯=⨯---43310048.81069.15901008.021103218解:C 2O 42- + H + = HC 2O 4- K 1=452106.1104.611⨯=⨯=-a K HC 2O 42- + H + = H 2C 2O 4 K 2=21109.511-⨯=a K =16.9故 β1=K 1=452106.1104.611⨯=⨯=-a K β2=K 1·K 2=524107.2109.51106.1⨯=⨯⨯⨯- 3254221)(103.4)10.0(107.210.0106.11][][1242⨯=⨯⨯+⨯⨯+=++=++-H H H O C ββαlg )(242H OC -α=3.6319解:查附表4得:pH=5.5时,lg 51.5)(=H Y α7.627.8)(10100.1101][1=⨯⨯+=+=-Mg K MgY Mg Y αY α=)(H Y α+)(Mg Y α-1=105.51+106.7-1=106.7320解:(1) Zn 2+ + Y = ZnYpH=10.00时,lg 45.0)(=H Y α, lg 4.2)(=OH Zn α锌氨络合物的各累积形成常数lgβ1-lgβ4分别为:2.27,4.61,7.01,9.06锌氰络合物的累积形成常数lgβ4=16.7 43433323231)(][][][][13NH NH NH NH NH Zn ββββα++++==1+102.27×0.10+104.61×(0.10)2+107.01×(0.10)3+109.06×(0.10)4=1+101.27+102.61+104.01+105.06≈105.107.4437.1644)(10)10(101][1=+=+=--CN CN Zn βαZn α=)(3NH Zn α+)(CN Zn α+)(OH Zn α-2=105.10+104.7+102.4-2≈105.25lg 'ZnY K = lg ZnY K -lg Zn α- lg )(H Y α=16.50-5.25-0.45=10.80 (2)pZn SP ′=40.6)8.1000.2(21)lg (21,=+='+ZnY SP Zn K pC[Zn 2+′]=10-6.40mol•L -1 依 Zn α=][][22++'Zn Zn所以 [Zn 2+]=11225.540.62102.21010][---+⋅⨯=='L mol Zn Znα22解:根据Hg(CN)42-配离子的各级logK 值求得 Hg(CN)42-配离子的各级积累形成常数分别为: β1=K 1=1018.00 ,β2=K 1·K 2=1018.00×1016.70=1034.70 β3=K 1·K 2·K 3=1018.00×1016.70×103.83=1038.53β4=K 1·K 2·K 3·K 4=1018.00×1016.70×103.83×102.98=1041.5155.3351.3353.3270.3000.164251.413253.382270.34200.184433221)(10101010101)10(10)10(10)10(1010101][][][][1=++++=⨯+⨯+⨯+⨯+=++++=--------CN CN CN CN CN Hg ββββα查表得:lgk HgY =21.80 , pH=11.0时07.0lg )(=H Y α 9.15lg )(=OH Hg α故55.339.1553.33)()(10110101=-+=-+=OH Hg CN Hg Hg ααα82.1155.3307.080.21lg lg lg log )('-=--=--=∴H Y Hg HgY HgYK K αα26解:(1)5.135.1321101011===-a K β8.203.75.131221010110111=⋅=⋅=--a a K K β 5.32108.20105.13221)(10)10(1010101][][1≈⨯+⨯+=++=--++H H H In ββαpMg ep =pMgt=lg MgIn K -lgαIn(H)=7.6-3.5=4.1 (2) 查表得:lgK MgY =8.7,pH=10.00时, lg 45.0)(=H Y αlg 'MgY K = lg MgY K -lg )(H Y α=8.7-0.45=8.2513.5)25.82(21)lg (21,=+='+=MgY SP Mg Sp K pC pMg ΔpMg=pMg ep -pMg Sp =4.1-5.13=-1.03%8.0%10010010.01010%100101025.803.103.1,-=⨯⨯-=⨯'⋅-=-∆-∆MgYSp Mg pMgpMg t K C E(3)由例题6-6可知:采用铬黑T 时,pMg ep =pMgt=5.4故ΔpMg=pMg ep - pMg Sp =5.4-5.13=0.27而采用铬蓝黑R 时,ΔpMg=pMg ep -pMg Sp =4.1-5.13=-1.03由此可见,采用铬黑T 时,ΔpMg 更小,终点误差Et 也将更小,故选择铬黑T 更合适。
分析化学各章节习题(含答案)

分析化学各章节习题(含答案)第一章误差与数据处理1-1 下列说法中,哪些是正确的?(1)做平行测定的目的是减小系统误差对测定结果的影响。
(2)随机误差影响精密度,对准确度无影响。
(3)测定结果精密度高,准确度不一定高。
(4)只要多做几次平行测定,就可避免随机误差对测定结果的影响。
1-2 下列情况,将造成哪类误差?如何改进?(1)天平两臂不等长(2)测定天然水硬度时,所用蒸馏水中含Ca2+。
1-3 填空(1)若只作两次平行测定,则精密度应用表示。
(2)对照试验的目的是,空白试验的目的是。
(3)F检验的目的是。
(4)为检验测定结果与标准值间是否存在显著性差异,应用检验。
(5)对一样品做六次平行测定,已知d1~d5分别为0、+0.0003、-0.0002、-0.0001、+0.0002,则d6为。
1-4 用氧化还原滴定法测定纯品FeSO4·7H2O中铁的质量分数,4次平行测定结果分别为20.10%,20.03%,20.04%,20.05%。
计算测定结果的平均值、绝对误差、相对误差、平均偏差、相对平均偏差、标准偏差及变异系数。
1-5 有一铜矿样品,w(Cu) 经过两次平行测定,分别为24.87%和24.93%,而实际w(Cu)为25.05%,计算分析结果的相对误差和相对相差。
1-6 某试样5次测定结果为:12.42%,12.34%,12.38%,12.33%,12.47%。
用Q值检验法和4检验法分别判断数据12.47%是否应舍弃?(P = 0.95)1-7 某分析人员测定试样中Cl的质量分数,结果如下:21.64%,21.62%,21.66%,21.58%。
已知标准值为21.42%,问置信度为0.95时,分析结果中是否存在系统误差?1-8 在不同温度下测定某试样的结果如下:10℃::96.5%,95.8%,97.1%,96.0%37℃:94.2%,93.0%,95.0%,93.0%,94.5%试比较两组数据是否有显著性差异?(P = 0.95)温度对测定是否有影响?11-9某试样中待测组分的质量分数经4次测定,结果为30.49%,30.52%,30.60%,30.12%。
第七章习题答案

第七章1.计算氢原子核外电子从第三能级跃迁到第二能级时产生的谱线H α的波长与频率。
解: ν = R H ⎪⎭⎫ ⎝⎛-222111n n= 3.289 ⨯ 1015⎪⎪⎭⎫⎝⎛-223121s -1= 4.57⨯1014s -1νλc= =11418s 1057.4s m 10998.2--⨯⋅⨯= 656⨯10-9m= 656nm2.计算基态氢原子的电离能为多少? 解: I = ∆E = h ν= 6.626⨯10-34 J ⋅s ⨯3.289⨯1015s -1(1/12 -1/∞)=2.179⨯10-18J3.下列各组量子数哪些是不合理的?为什么?n l m(1) 2 1 0(2) 2 2 -1(3) 2 3 +2解:(1)合理;(2) l 取值不合理,应小于n ;(3) l 、m 取值不合理,l 应小于n ,m 取值为0, ±1, ±2,⋯ ± l ;4.用合理的量子数表示:(1)3d 能级; (2)4s 1电子解:(1)3d 能级: n =3,l =2;(2)4s 1电子:n =4,l =0,m = 0;5.分别写出下列元素基态原子的电子分布式,并分别指出各元素在周期表中的位置。
9F 10Ne 25Mn 29Cu 24Cr 55Cs 71Lu解:9F 1s 22s 22p 5 第二周期VIIA 族 10Ne [He]2s 22p 6 第二周期VIIIA 族25Mn [Ar]3d 54s 2 第四周期VIIB 族 29Cu [Ar]3d 104s 1 第四周期I B 族24Cr [Ar]3d 54s 1 第四周期VI B 族 55Cs [Xe]6s 1 第六周期I A 族71Lu [Xe]4f 145d 16s 2 第六周期IIIB 族6.以(1)为例,完成下列(2)~(4)题。
(1)Na (Z = 11) [Ne]3s 1 ; (3 ) (Z =24) [ ? ] 3d 54s 1;(2) 1s 22s 22p 63s 23p 3 ; (4 ) Kr (Z = ) [ ? ] 3d 104s 24p 6;解:(1) Na (Z = 11) [Ne]3s 1 ; (3 ) Cr (Z =24) [Ar ] 3d 54s 1;(2) P(Z=15) 1s 22s 22p 63s 23p 3 ; (4 ) Kr (Z = 36 ) [Ar] 3d 104s 24p 6;7.写出下列离子的最外层电子分布式:S 2-K + Pb 2+ Ag + Mn 2+ Co 2+ 解:8.试完成下表。
无机及分析化学 第七章氧化还原反应课后习题答案
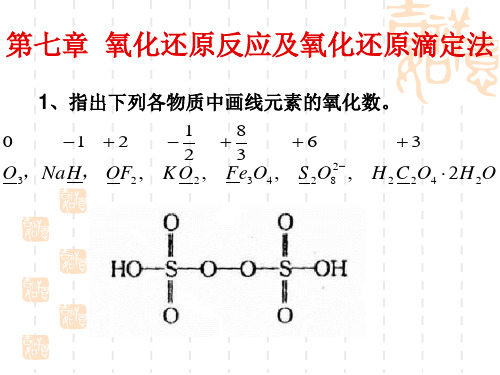
K 9.62 1018
由于K 数值很大,化学计量点时反应进行较完全。
18.常采用K2Cr2O7法测定水体中的化学耗氧量(COD),取废水样 100.0mL,用硫酸酸化后,加入0.02000mol· L-1的K2Cr2O7溶液25.00 mL,在Ag2SO4存在下煮沸以氧化水样中还原性物质,再以试铁灵 为指示剂,用0.1000mol· L-1的FeSO4溶液滴定剩余的Cr2O72-,用去 18.20mL,计算废水样中的化学耗氧量(以O2计,mg· L-1表示)。
2
0.0592 2 E H / H lg 0.1 2 2 0.0592V
(4)在1.0L上述(3)的溶液中加入0.10mol固体NaOH,
E H / H2 ?
0.0592 (cH / c ) E H / H2 E H / H lg 2 n (p H2 /p)
2S2 O32 I 2 S4 O62 2 I Cr2O72 ~ 3I 2 ~ 6S2O32
6nCr O2 nS O2
2 7 2 3
mK2Cr2O7 M K2Cr2O7
25 6 cNa S O VNa S O 2 2 3 2 2 3 100
0.4903 6 cNa S O 25 103 2 2 3 294.18 4 cNa S O 0.1000mol L1
3、对于下列氧化还原反应:(1)指出哪个是氧化剂, 哪个是还原剂?写出对应的半电池反应。(2)按这 些反应设计成原电池,并写出原电池符号。
2 Ag aq Zn s 2 Ag s Zn2 aq
正极反应: Ag e Ag , 氧化剂为Ag 负极反应: Zn -2e- Zn2+ , 还原剂为Zn (-)Zn Zn2+(c1) Ag+(c2) Ag(+)
分析化学课后习题答案(第7章)

7.1 计算下列重量因数:测定物 称量物(1)FeO Fe 2O 3(2)KCl (→K 2PtCl 6→Pt ) Pt(3)Al 2O 3 Al(C 9H 6ON)3 (4)P 2O 5 (NH 4)3PO 4·12MoO 3答案:232(FeO)271.85(1)0.8999(Fe O )159.69M M ⨯== 2(KCl)274.55(2)0.7643(Pt)195.08M A ⨯== 23963(Al O )101.96(3)0.11102(Al(C H ON))2459.44M M ==⨯ 254343(P O )141.94(4)0.037822((NH )PO 12MoO )21876.3M M ==⨯ 7.2 称取某可溶性盐0.3232g ,用硫酸钡重量法测定其中含硫量,得BaSO 4沉淀0.2982g ,计算试样含SO 3的质量分数。
答案:3443(SO )(BaSO )(BaSO )(SO )100%0.29820.3430 100%31.65%0.3232s M m M w m =⨯⨯=⨯= 7.3 用重量法测定莫尔盐(NH 4)2SO 4·FeSO 4·6H 2O 的纯度,若天平称量误差为0.2mg ,为了使灼烧后Fe 2O 3的称量误差不大于0.1%,应最少称取样品多少克?答案:323424423234244230.210100%0.1%(Fe O )2(NH )SO FeSO 6H O0.210100%(Fe O )0.1%2((NH )SO FeSO 6H O)0.210 100%1(g)1600.1%2392s s M m M m M M ---⨯⨯≤⋅⋅⨯≥⨯⋅⋅⨯=⨯=⨯⨯ 7.4 计算下列微溶化合物在给定介质中的溶解度(除(1)题外均采用I =0.1时的常数)。
(1) ZnS 在纯水中(p K 0sp (ZnS)=23.8,H 2S 的p K a1=7.1,p K a2=12.9);(2) CaF 2在0.01mol ·L -1 HCl 溶液中(忽略沉淀溶解所消耗的酸);(3) AgBr 在0.01mol ·L -1 NH 3溶液中;(4)BaSO4在pH7.0,EDTA浓度为0.01mol·L-1的溶液中;(5)AgCl在0. 10 mol·L-1的HCl溶液中。
分析化学课后习题答案

第七章原子吸收与原子荧光光谱法1.解释下列名词:(1)原子吸收线和原子发射线;(2)宽带吸收和窄带吸收;(3)积分吸收和峰值吸收;(4)谱线的自然宽度和变宽;(5)谱线的热变宽和压力变宽;(6)石墨炉原子化法和氢化物发生原子化法;(7)光谱通带;(8)基体改进剂;(9)特征浓度和特征质量;(10)共振原子荧光和非共振原子荧光。
答:(1)原子吸收线是基态原子吸收一定辐射能后被激发跃迁到不同的较高能态产生的光谱线;原子发射线是基态原子吸收一定的能量(光能、电能或辐射能)后被激发跃迁到较高的能态,然后从较高的能态跃迁回到基态时产生的光谱线。
(2)分子或离子的吸收为宽带吸收;气态基态原子的吸收为窄带吸收。
(3)积分吸收是吸收线轮廓的内的总面积即吸收系数对频率的积分;峰值吸收是中心频率0两旁很窄(d 0)范围内的积分吸收。
(4)在无外界条件影响时,谱线的固有宽度称为自然宽度;由各种因素引起的谱线宽度增加称为变宽。
(5)谱线的热变宽是由原子在空间作相对热运动引起的谱线变宽;压力变宽是由同种辐射原子间或辐射原子与其它粒子间相互碰撞产生的谱线变宽,与气体的压力有关,又称为压力变宽。
(6)以石墨管作为电阻发热体使试样中待测元素原子化的方法称为石墨炉原子化法;反应生成的挥发性氢化物在以电加热或火焰加热的石英管原子化器中的原子化称为氢化物发生原子化法。
(7)光谱通带是指单色器出射光束波长区间的宽度。
(8)基体改进剂是指能改变基体或被测定元素化合物的热稳定性以避免化学干扰的化学试剂。
(9)把能产生1%吸收或产生吸光度时所对应的被测定元素的质量浓度定义为元素的特征浓度;把能产生1%吸收或产生吸光度时所对应的被测定元素的质量定义为元素的特征质量。
(10)共振原子荧光是指气态基态原子吸收的辐射和发射的荧光波长相同时产生的荧光;气态基态原子吸收的辐射和发射的荧光波长不相同时产生的荧光称为非共振原子荧光。
2.在原子吸收光谱法中,为什么要使用锐线光源?空心阴极灯为什么可以发射出强度大的锐线光源?答:因为原子吸收线的半宽度约为103nm,所以在原子吸收光谱法中应使用锐线光源;由于空心阴极灯的工作电流一般在1~20 mA,放电时的温度较低,被溅射出的阴极自由原子密度也很低,同时又因为是在低压气氛中放电,因此发射线的热变宽D、压力变宽L和自吸变宽都很小,辐射出的特征谱线是半宽度很窄的锐线(104~10 3 nm)。
B143-分析化学-第七章络合滴定法答案(2)

B143-分析化学-第七章络合滴定法答案(2)1. EDTA二钠盐的水溶液的pH的最简式是(pH = (p K a4 + p K a5) /2)(EDTA相当于六元酸)2. 络合滴定中一般不使用EDTA而用EDTA二钠盐(Na2H2Y), 这是由于(EDTA 在水中的溶解度小, 而Na2H2Y的溶解度较大); 当在强酸性溶液中(pH<1), EDTA为六元酸, 这是因为(两个N原子接受了两个质子)。
3.直接与金属离子配位的EDTA型体为(D)(A)H6Y2+(B)H4Y (C)H2Y2-(D)Y4-4. 指出下列EDTA络合物的颜色(填A,B,C,D)(1) CuY2- ___ D _____ (A)无色(2) MnY2- __ B ______ (B)紫红色(3) FeY-___C _____ (C)黄色(4) ZnY2- ___ A ____ (D)蓝色5.一般情况下,EDTA与金属离子形成的络合物的络合比是(A)(A)1:1 (B)2:1 (C)1:3 (D)1:26. 金属离子M与络合剂L形成逐级络合物, 溶液中各种存在型体的分布系数与络合剂的平衡浓度(有关); 与金属离子的总浓度(无关)。
(答有关或无关)7. 已知乙酰丙酮(L)与Al3+络合物的lgβ1-lgβ3分别是8.6、15.5和21.3, 则AlL3为主要形式时的pL范围是(pL < 5.8),pL为10.0时铝的主要形式是(Al3+),则[AlL]与[AlL2]相等时的pL 值为(6.9)8. 磺基水杨酸(L)与Cu2+络合物的lgβ1为9.5, lgβ2为16.5, [CuL]达最大的pL为( D)(A) 9.5 (B) 16.5 (C) 7.0 (D) 8.39.αM(L)=1表示(A)(A)M与L没有副反应(B)M与L的副反应相当严重(C)M的副反应较小(D)[M]=[L]10. 若络合滴定反应为M + Y = MYL│ │H+ML H i Y(i=1~6)则酸效应系数αY(H)的定义式为(αY(H)=[Y']/[Y]),[Y']=([Y']=[Y]+∑[H i Y])c(Y)=([Y]+∑[H i Y]+[MY]或c(Y)=[Y']+[MY])。
分析化学课后习题答案第七章

第七章重量分析法和沉淀滴定法思考题1.沉淀形式和称量形式有何区别?试举例说明之。
答:在重量分析法中,沉淀是经过烘干或灼烧后再称量的。
沉淀形式是被测物与沉淀剂反应生成的沉淀物质,称量形式是沉淀经过烘干或灼烧后能够进行称量的物质。
有些情况下,由于在烘干或灼烧过程中可能发生化学变化,使沉淀转化为另一物质。
故沉淀形式和称量形式可以相同,也可以不相同。
例如:BaSO4,2+其沉淀形式和称量形式相同,而在测定Mg时,沉淀形式是MgNH4PO4·6H2O,灼烧后所得的称量形式却是Mg2P2O7。
2.为了使沉淀定量完全,必须加人过量沉淀剂,为什么又不能过量太多?答:在重量分析法中,为使沉淀完全,常加入过量的沉淀剂,这样可以利用共同离子效应来降低沉淀的溶解度。
沉淀剂过量的程度,应根据沉淀剂的性质来确定。
若沉淀剂不易挥发,应过量20%~50%;若沉淀剂易挥发,则可过量多些,甚至过量100%。
但沉淀剂不能过量太多,否则可能发生盐效应、配位效应等,反而使沉淀的溶解度增大。
3.影响沉淀溶解度的因素有哪些?它们是怎样发生影响的?在分析工作中,对于复杂的情况,应如何考虑主要影响因素?答:影响沉淀溶解度的因素有:共同离子效应,盐效应,酸效应,配位效应,温度,溶剂,沉淀颗粒大小和结构等。
共同离子效应能够降低沉淀的溶解度;盐效应通过改变溶液的离子强度使沉淀的溶解度增+加;酸效应是由于溶液中H浓度的大小对弱酸、多元酸或难溶酸离解平衡的影响来影响沉淀的溶解度。
若沉淀是强酸盐,如BaSO4,AgCl等,其溶解度受酸度影响不大,若沉淀是弱酸或多元酸盐[如CaC2O4、Ca3(PO4)2]或难溶酸(如硅酸、钨酸)以及与有机沉淀剂形成的沉淀,则酸效应就很显著。
除沉淀是难溶酸外,其他沉淀的溶解度往往随着溶液酸度的增加而增加;配位效应是配位剂与生成沉淀的离子形成配合物,是沉淀的溶解度增大的现象。
因为溶解是一吸热过程,所以绝大多数沉淀的溶解度岁温度的升高而增大。
兰叶青 无机及分析化学课后答案 第七章

第 习题答案7—1解:设BaSO 4在水中的溶解度为S 1(mol ·L -1);在0.10mol•L -1Na 2SO 4溶液中的溶解度为S 2(mol ·L -1).由 )()()(aq S O aq Ba s BaSO 2424-++= 222222sp 441010BaSO Ba SO c S .S K c /c c /c S /c ΘΘΘΘΘ+-⋅+⎡⎤⎡⎤===⎣⎦⎣⎦()()()()()(纯水中) (Na 2SO 4中)已知 10sp 4BaSO 10710K .Θ-=⨯()解得 S 1=1.03×10-5mol•L -1由同离子效应知,S 2<S 1=1.03×10-5mol•L -1 所以 0.10+ S 2≈0.10 解得S 2=1.1×10-9mol•L -1 7—2解:(1)7213sp AgBr 88107710K ..Θ--=⨯=⨯()()(2)5313sp 44Mg NH PO 63102510K ..Θ--=⨯=⨯(())()(3)55213sp 32Pb IO 3110101210K ..Θ---=⨯⨯⨯⨯=⨯(())(2 3.1)7—3 解:两液混合后,13132L m o l 1001L mol 1001001001002Pb ----+⋅⨯=⋅+⨯⨯=.....c)()( 11L mol 0200L mol 1001001000400I ---⋅=⋅+⨯=.....c )()(22PbI s Pb aq 2I aq +-+ƒ()()() 根据溶度积规则,计算离子积Q :22327Q P b I 101000204010c /c c /c ...ΘΘ+---⎡⎤⎡⎤==⨯⨯=⨯⎣⎦⎣⎦()() 查表得 9sp 2PbI 84910K .Θ-=⨯() 即 )(2sp PbI Q ΘK 〉应有PbI 2沉淀产生. 7—4解:查表39sp 3Fe OH 26410K .Θ-=⨯(()) 17sp 2Fe OH 48710K .Θ-=⨯(())Fe (OH )3沉淀完全时, c (Fe 3+)≤1.0×10-5mol·L -1,此时OH c /c Θ-==()解得 c (OH -)=6.4×10-12 mol·L -1pH=14-pOH=2.81,即pH 至少为2.81。
分析化学第7章课后习题答案

第七章氧化还原滴定1.条件电位和标准电位有什么不同?影响电位的外界因素有哪些?答:标准电极电位E ′是指在一定温度条件下(通常为25℃)半反应中各物质都处于标准状 态,即离子、分子的浓度(严格讲应该是活度)都是1mol/l (或其比值为1)(如反应中有气体物5Pa ,固体物质的活度为1)时相对于标准氢电极的电极电位。
质,则其分压等于1.013×10电对的条件电极电位(E0f)是当半反应中氧化型和还原型的浓度都为1或浓度比为,并且溶液中其它组分的浓度都已确知时,该电对相对于标准氢电极电位(且校正了各种外界因素影响后 的实际电极电位,它在条件不变时为一常数)。
由上可知,显然条件电位是考虑了外界的各种影 响,进行了校正。
而标准电极电位则没有校正外界的各种外界的各种因素。
影响条件电位的外界因素有以下3个方面; (1)配位效应; (2)沉淀效应; (3)酸浓度。
2.是否平衡常数大的氧化还原反应就能应用于氧化还原中?为什么?6),这样的氧化还原反应,可以用于滴定分答:一般讲,两电对的标准电位大于0.4V (K>10 析。
实际上,当外界条件(例如介质浓度变化、酸度等)改变时,电对的标准电位是要改变的, 因此,只要能创造一个适当的外界条件,使两电对的电极电位超过0.4V ,那么这样的氧化还原 反应也能应用于滴定分析。
但是并不是平衡常数大的氧化还原反应都能应用于氧化还原滴定中。
因为有的反应K 虽然很大,但反应速度太慢,亦不符合滴定分析的要求。
3.影响氧化还原反应速率的主要因素有哪些?答:影响氧化还原反应速度的主要因素有以下几个方面:1)反应物的浓度;2)温度;3)催 化反应和诱导反应。
4.常用氧化还原滴定法有哪几类?这些方法的基本反应是什么?答:1)高锰酸钾法.2MnO 4+5H 2O 2+6H+==2Mn 2++5O 2↑+8H 2O. 2++2CO2+2H2OMnO2+H2C2O4+2H+==Mn2-+2+3+3+2)重铬酸甲法.Cr2O7+14H+Fe===2Cr+Fe+7H2OCH 3OH+Cr 2O 72-+8H+===CO 2↑+2Cr 3++6H 2O3)碘量法3I2+6HO -===IO 3-+3H 2O ,2-- 2S2O3+I2===2I+2H2O Cr 2O 72-+6I -+14H+===3I 2+3Cr 3++7H 2O5.应用于氧化还原滴定法的反应具备什么条件?答:应用于氧化还原滴定法的反应,必须具备以下几个主要条件:6(1)反应平衡常数必须大于10,即△E>0.4V 。
(完整版)无机及分析化学课后习题第七章答案

一、选择题在给出的4个选项中,请选出1个正确答案。
1. 下列物质中,酸的强度最大的是( D )A. HAc 4.75HAc)p θa=(K B. HCN 219HCN)p θa .(K = C. NH 4+4.75O)H NH p 23θb =⋅(K D. HCOOH 25.10HCOONa)(p θb =K 2. 某混合碱用盐酸滴定至酚酞变色,消耗V 1ml ,继续以甲基橙为指示剂消耗V 2ml ,已知V 1>V 2 ,其组成是( C )A. Na 2CO 3B. Na 2CO 3与NaHCO 3C. NaOH 与Na 2CO 3D. NaOH3. 用Na 2CO 3 为基准物质标定HCl 溶液时,下列情况对HCl 溶液的浓度不产生影响的是( A )A. 用去离子水溶解锥形瓶中的Na 2CO 3时,多加了5.0mL 去离子水B. 烘干Na 2CO 3时,温度控制300℃以上C. 滴定管未用HCl 溶液润洗D. 滴定速度太快,附着在滴定管壁上的HCl 溶液来不及流下来就读取滴定体积4. 蒸馏法测定铵盐中N 含量时,能用作吸收液的是( B )A. 硼砂B. HClC. HAcD. NH 4Cl5. 下列溶液能用HCl 或NaOH 标准溶液直接滴定的是(浓度均为0.1mol·L -1) ( D )A. NaAcB. NH 4ClC. HCND. HCOOH(K θa (HAc) = 1.79×10-5 ;K θb (NH 3) = 1.8×10-5 ;K θa (HCN) = 4.99×10-10 ; K θa (HCOOH) =1.7×10-4)6. 用返滴定法测定氨水含量,应选用的指示剂是( D )A. 酚酞B. 甲基橙C. 钙红D. 甲基红7. 用c (NaOH)=0.1000 mol·L -1的NaOH 溶液滴定相同浓度的弱酸(K a1 =8.6 ×10-2K a2 =6.3×10-7 K a3 =4.0×10-13)( B )A.有两个滴定终点,第一终点用酚酞、第二终点用甲基红指示B.有两个滴定终点,第一终点用甲基红、第二终点用酚酞指示C.只有一个终点,用酚酞指示D.只有一个终点,用甲基红指示8. 酸碱滴定中,选择酸碱指示剂可以不考虑的因素是( C )A. pH 突跃范围B. 指示剂的变色范围C. 指示剂的摩尔质量D. 要求的误差范围9. H3PO4的pKθa1, pKθa2 pKθa3分别为2.12、7.20、12.36,当pH=8.0时,H3PO4溶液体系中浓度最大的组分是( A )A. HPO42-B. H2PO4- C . H3PO4 D. PO43-二、填空题1. 下列离子HCO3―,H2O,S2-,NH4+只能作碱的是S2-,只能作酸的是NH4+,即可作酸又能作碱的是HCO3―,H2O 。
分析化学 第五版课后答案 (高等教育出版社) 7-8 khdaw

第七章习题7.1下列情况,有无沉淀生成?(1)0.001mol ·L -1Ca(NO 3)2溶液与0.01mol ·L -1NH 4HF 2溶液以等体积相混合;(2)0.01mol ·L -1MgCl 2溶液与0.1mol ·L -1NH 3-1mol ·L -1NH 4Cl 溶液等体积相混合。
解:(1)已知:K sp (CaF 2)=3.4×10-11两溶液等体积混合后:[Ca 2+]=5.0×10-4mol ·L -1,[F -]=5.0×10-3mol ·L -1,[Ca 2+][F -]2=5.0×10-4×(5.0×10-3)2=2.5×10-8>K sp (CaF 2)=3.4×10-11∴有沉淀生成。
(2)已知:K b (NH 3)=1.8×10-5K sp (Mg(OH)2)=1.8×10-11[Mg 2+]=5.0×10-3mol ·L -1,[NH 3]=0.05mol ·L -1,[NH 4]=0.5mol ·L -1,[Mg 2+][OH -]2=5.0×10-3×(1.8×10-6)2=1.6×10-14<K7.2(1)(2)在(3)在解:(1L -1(2(3--s =1.9×10-3mol ·L -17.3计算PH=5.0,草酸总浓度为0.05mol ·L -1时,草酸钙的溶解度.如果溶液的体积为300mL,将溶解多少克CaC 2O 4?解:已知:K a1(H 2C 2O 4)=5.9×10-2,K a2=6.4×10-5,K sp (CaC 2O 4)=1.8×10-9M (CaC 2O 4)=128.1同理得:α=1.16[OH -]=K b (NH 3)×[NH 3]=1.8×10-5×0.05=1.8×10-6mol ·L -1[NH 4+]0.510-2α(H)=1δ[Ca 2+][C 2O 42-]总=Ksp(CaC 2O 4)·αC 2O 42-s ×0.05=1.8×10-9×1.16s =4.2×10-8mol ·L -1溶解损失:m (CaC 2O 4)=4.2×10-8×0.3×128.1=1.6×10-6(g)=1.6×10-3(mg)7.425℃时,铬酸银的溶解度为每升0.0279g,计算铬酸银的溶度积.解:已知:M (Ag 2CrO 4)=331.73设:铬酸银(Ag 2CrO 4)的溶解度为S.K sp =[Ag +]2[CrO 42-]=(2×8.41×10-5)2×8.41×10-5=2.38×10-127.5为了使0.2032g (NH 4)2SO 4中的SO 42-沉淀完全,需要每升含63g BaCl 2·2H 2O 的溶液多少亳升?解:已知M ((NH 4)2SO 4)=132.14,M (BaCl 2·2H 2O)2SO 4)=244.3考虑问题的思路是,沉淀剂过量20%~50%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第七章氧化还原滴定1、条件电位与标准电位有什么不同?影响电位的外界因素有哪些?答:标准电极电位E′就是指在一定温度条件下(通常为25℃)半反应中各物质都处于标准状态,即离子、分子的浓度(严格讲应该就是活度)都就是1mol/l(或其比值为1)(如反应中有气体物质,则其分压等于1、013×105Pa,固体物质的活度为1)时相对于标准氢电极的电极电位。
电对的条件电极电位(E0f)就是当半反应中氧化型与还原型的浓度都为1或浓度比为,并且溶液中其它组分的浓度都已确知时,该电对相对于标准氢电极电位(且校正了各种外界因素影响后的实际电极电位,它在条件不变时为一常数)。
由上可知,显然条件电位就是考虑了外界的各种影响,进行了校正。
而标准电极电位则没有校正外界的各种外界的各种因素。
影响条件电位的外界因素有以下3个方面;(1)配位效应;(2)沉淀效应;(3)酸浓度。
2.就是否平衡常数大的氧化还原反应就能应用于氧化还原滴定中?为什么?答:一般讲,两电对的标准电位大于0、4V(K>106),这样的氧化还原反应,可以用于滴定分析。
实际上,当外界条件(例如介质浓度变化、酸度等)改变时,电对的标准电位就是要改变的,因此,只要能创造一个适当的外界条件,使两电对的电极电位超过0、4V ,那么这样的氧化还原反应也能应用于滴定分析。
但就是并不就是平衡常数大的氧化还原反应都能应用于氧化还原滴定中。
因为有的反应K虽然很大,但反应速度太慢,亦不符合滴定分析的要求。
3、影响氧化还原反应速率的主要因素有哪些?答:影响氧化还原反应速度的主要因素有以下几个方面:1)反应物的浓度;2)温度;3)催化反应与诱导反应。
4、常用氧化还原滴定法有哪几类?这些方法的基本反应就是什么?答:1)高锰酸钾法.2MnO4+5H2O2+6H+==2Mn2++5O2↑+8H2O、MnO2+H2C2O4+2H+==Mn2++2CO2+2H2O2) 重铬酸甲法、Cr2O72-+14H++Fe2+===2Cr3++Fe3++7H2OCH3OH+Cr2O72-+8H+===CO2↑+2Cr3++6H2O3)碘量法3I2+6HO-===IO3-+3H2O,2S2O32-+I2===2I-+S4O62Cr2O72-+6I-+14H+===3I2+3Cr3++7H2O5、应用于氧化还原滴定法的反应具备什么条件?答:应用于氧化还原滴定法的反应,必须具备以下几个主要条件:(1)反应平衡常数必须大于106,即△E>0、4V。
(2)反应迅速,且没有副反应发生,反应要完全,且有一定的计量关系。
(3)参加反应的物质必须具有氧化性与还原性或能与还原剂或氧化剂生成沉淀的物质。
(4)应有适当的指示剂确定终点。
6、化学计量点在滴定曲线上的位置与氧化剂与还原剂的电子转移数有什么关系?答:氧化还原滴定曲线中突跃范围的长短与氧化剂与还原剂两电对的条件电位(或标准电位)相差的大小有关。
电位差△E较大,突跃较长,一般讲,两个电对的条件电位或标准电位之差大于0、20V时,突跃范围才明显,才有可能进行滴定,△E值大于0、40V时,可选用氧化还原指示剂(当然也可以用电位法)指示滴定终点。
当氧化剂与还原剂两个半电池反应中,转移的电子数相等,即n1=n2时,则化学计量点的位置恰好在滴定突跃的中(间)点。
如果n1≠n2,则化学计量点的位置偏向电子转移数较多(即n值较大)的电对一方;n1与n2相差越大,化学计量点偏向越多。
7、试比较酸碱滴定、络合滴定与氧化还原滴定的滴定曲线,说明它们共性与特性。
答: 酸碱滴定、配位滴定与氧化还原滴定的滴定曲线共性就是:1)在滴定剂不足0、1%与过量0、1%时,三种滴定曲线均能形成突跃;2)均就是利用滴定曲线的突跃,提供选择指示剂的依据。
其特性就是:酸碱滴定曲线就是溶液的pH值为纵坐标,配位滴定的滴定曲线以pM为纵坐标,而氧化还原滴定曲线就是以E值为纵坐标,其横坐标均就是加入的标准溶液。
8、氧化还原滴定中的指示剂分为几类?各自如何指示滴定终点?答:氧化还原滴定中指示剂分为三类:(1)氧化还原指示剂。
就是一类本身具有氧化还原性质的有机试剂,其氧化型与还原型具有不同的颜色。
进行氧化还原滴定时,在化学计量点附近,指示剂或者由氧化型转变为还原型,或者由还原型转变为氧化型,从而引起溶液颜色突变,指示终点。
(2)自身指示剂。
利用滴定剂或被滴定液本身的颜色变化来指示终点。
(3)专属指示剂。
其本身并无氧化还原性质,但它能与滴定体系中的氧化剂或还原剂结合而显示出与其本身不同的颜色。
9、氧化还原指示剂的变色原理与选择与酸碱指示剂有何异同?答:氧化还原滴定所用的指示剂分为两个类型:氧化还原指示剂与其她指示剂。
后者的变色原理与选择与酸碱指示剂无有任何异同点。
而前者——氧化还原指示剂的变色原理与选择与酸碱指示剂的异同点如下:①酸碱指示剂的变色主要与溶液的酸度(pH值)有关;而氧化还原指示剂的变色主要就是决定于其氧化型与还原型(两型的颜色不同)的颜色。
②酸碱指示剂变色与氧化还原指示剂变色均有变色点;两者均有变色范围。
③酸碱指示剂与氧化还原指示剂的选择均与滴定曲线的突跃范围有关。
酸碱指示剂就是范围,而氧化还原指示剂则就是电位范围。
其颜色强度的变化均就是从10变到0、1的关系。
④酸碱指示剂的变色除与溶液的值有关外,而指示剂本身也有结构变化;氧化还原指示剂则只与电位有关。
10、在进行氧化还原滴定之前,为什么要进行预氧化或预还原的处理?预处理时对所用的预氧化剂或还原剂有哪些要求?答:在进行氧化还原滴定之前,为了能成功的完成氧化还原滴定,时常需要将被测定的组分处理成能与滴定剂迅速、完全并按照一定计量关系起反应的状态,或者处理成高价后用还原剂进行滴定,或者处理成低价后用氧化剂滴定。
滴定前使被测组分转变为一定价态的步骤称为滴定前的预处理。
预处理时对所用的氧化剂或还原剂有以下几点要求:(1)反应进行完全而且速度要快;(2)反应应该具有一定的选择性。
(3)过量的氧化剂或还原剂应易于除去;11、碘量法的主要误差来源有哪些?为什么碘量法不适宜在高酸度或高碱度介质中进行?答;碘量法的主要误差来源有以下几个方面:(1)标准溶液的遇酸分解;(2)碘标准溶液的挥发与被滴定碘的挥发;(3)空气对KI的氧化作用:(4)滴定条件的不适当。
由于碘量法使用的标准溶液与它们间的反应必须在中性或弱酸性溶液中进行。
因为在碱性溶液中,将会发生副反应:S2O32-+4I2+10OH-=2SO42-+8I-+5H2O而且在碱性溶液中还会发生歧化反应:3I 2+6OH -=IO 3-+5I -+3H 2O如果在强碱性溶液中,溶液会发生分解: S 2O 32-+2H +=SO 2↑+S ↓+H 2O同时,在酸性溶液中也容易被空气中的氧所氧化: 4I -+4H ++O 2=2I 2+2H 2O基于以上原因,所以碘量法不适宜在高酸度或高碱度介质进行。
12、比较用KMnO 4’K 2Cr 2O 7与Ce(SO 4)2作滴定剂的优缺点。
与作滴定剂的优缺点见下表34答:分别测定AsO 33-与AsO 43-碘量法分析方案如下:(1) 于AsO 43-﹑AsO 33-的混合溶液中,在酸性条件下,加过量KI,此时AsO 43-与I -反应:AsO 43- +2I -+2H +=AsO 33+-I 2+H 2O析出的I 2用Na 2S 2O 3标准溶液滴定:I 2+2S 2O 32-=2I -+S 4O 62-由Na 2S 2O 3溶液的浓度(C Na2S2O3)与用去的体积(V Na2S2O3)即可求得AsO 43-的含量。
另外,在取一定量的AsO 43-与AsO 33-混合溶液,加NaHCO 3,在pH=8、0的条件下,用I 2标准溶液滴定溶液的AsO 33-:AsO 33-+I 2+2HCO 3-=====AsO 43-+2I -+2CO 2↑+H 2O (PH=8、0)根据I 2溶液的浓度(C I2)与消耗的体积(V I2)即可求AsO 33-的量。
(2)测定步骤 ①AsO 43-的测定移取混合试液25、00ml 于锥形瓶中,加酸与过量KI,析出的I 2,用Na 2S 2O 3标准溶液滴定,快到终点时加入淀粉指示剂,继续Na 2S 2O 3用滴定,终点时溶液由蓝色变为无色。
由下式计算AsO 43-的含量(以g/ml 表示):AsO 43-=00.2521100143323222-⨯⨯⨯⨯AsO O S N O S Na M V C a (2)AsO 33-的测定量取AsO 33-与AsO 43-混合溶液25、00ml,若试液为碱性,可取酸调至微酸性后,加一定量NaHCO 3,用I 2标准溶液滴定AsO 33-,用淀粉作指示剂,终点时溶液由无色变为蓝色,然后由下式计算AsO 33-的含量(以g/ml 表示):AsO 33-=00.2510013322-⨯⨯⨯AsO I I M V C14、在Cl -、Br -与I -三种离子的混合物溶液中,欲将I -氧化为I 2,而又不使Br -与Cl -氧化在常用的氧化剂Fe 2(SO 4)3与KMnO 4中应选择哪一种?答:选用Fe 2(SO 4)3氧化剂即能满足上述要求,因为:E 0 MnO4-/Mn2+=1、51V E 0Fe3+/Fe2+=0、771V E 0Cl2/2Cl-=1、395V E 0Br2/Br-=1、087V E 0I2/I-=0、621V又标准电极电位可知:E 0Fe3+/Fe2+的电位低于E 0Cl2/2Cl 而E 0Br2/Br-高于E 0I2/I-故只能将氧化为I 2,而不能将Cl -与Br -氧化。
如果选用KMnO 4时则能将其氧化。
15、计算在1mol/LHCl 溶液中,当[Cl -]=1、0mol/L 时,Ag +/Ag 电对的条件电位。
解:经查表在1mol/l 的溶液中,E 0`Ag+/Ag =0、7994V∵E=E 0Ag+/Ag +0、0592×lg [][]Ag Ag + =0、7994+0、0592×lg[Ag +] 又∵[Cl -]=1mol/l Ksp [AgCl]=8.11×1010 ∴E=0、7994+0、0592×lg 8.11×1010=0、22V 16、计算在1、5mol/LHCl 介质中,当c Cr(VI)=0、10mol/L,c Cr(III)=0、020mol/L 时Cr 2O 72-/Cr 3+电对的电极电位。
解:附录中没有该电对相应的条件电位值,采用相近1mol/L 的介质中E 0=1、00V 代替Cr 2O 72-+14H ++6e -==2Cr 3++7H 2O当C Cr(VI)=0、10mol/L C Cr(III)=0、020mol/LE=E 0 Cr(VI)/ Cr(III)+6059.0lg =)()(III Cr VI Cr C C 1、02V =1、01V17、计算pH=10、0,[NH 4+]+[NH 3]=0、20mol/L 时Zn 2+/Zn 电对条件电位。
