双电层及其结构模型
双电层及其结构模型

组织工程
双电层结构在组织工程领 域的应用主要涉及仿生细 胞外基质的设计,以促进 细胞生长和功能化。
生物传感器
双电层理论在生物传感器 设计中发挥关键作用,能 够提高传感器的灵敏度和 选择性。
06
结论与展望
研究结论
总结了双电层的形成机制和影响因素,包括电解质 浓度、表面活性剂和胶体颗粒的存在等。
分析了双电层的结构和性质,包括电位分布、电荷 密度和电导率等,揭示了其与物质传递和化学反应 过程的关系。
实验与理论相结合
应用导向的研究
双电层的研究将更加注重实际应用, 解决能源、环境、生物医学等领域中 的实际问题,推动科技成果转化和应 用。
未来的研究将更加注重实验与理论的 结合,通过实验验证理论预测,同时 通过理论指导实验设计和解释。
双电层研究的挑战与机遇
挑战
双电层的行为和性质受到多种因素的影响,如表面电荷分布、溶液组成、离子 浓度等,如何全面理解和掌握这些因素对双电层的影响是当前研究的难点。
03
双电层的结构模型
结构模型的种类
物理模型
通过物理手段模拟双电层的形成和结构,如电泳、 电聚焦等。
数学模型
通过建立数学方程来描述双电层的性质和行为,如 电位分布、离子浓度等。
计算机模拟模型
利用计算机技术模拟双电层的结构和行为,如分子 动力学模拟、蒙特卡洛模拟等。
结构模型的建立方法
80%
实验测量
深入研究双电层在生物医学领 域的应用,如药物传递、基因 治疗和组织工程等,以提高治 疗效果和降低副作用。
深入研究双电层在生物医学领 域的应用,如药物传递、基因 治疗和组织工程等,以提高治 疗效果和降低副作用。
THANK YOU
感谢聆听
2.5 双电层理论和电势

分子层的厚度,后被称为
Stern层; 由反号离子电性中心
构成的平面称为Stern平面。
Stern模型
由于离子的溶剂化作
用,胶粒在移动时,紧密
层会结合一定数量的溶剂 分子一起移动,所以滑移 的切动面由比Stern层略右 的曲线表示。 从固体表面到Stern平面, 电位从0直线下降为 。
电势
§2.5 双电层理论和 电势
当固体与液体接触时,可以是固体从溶液中选择
性吸附某种离子,也可以是固体分子本身发生电离作
用而使离子进入溶液,以致使固液两相分别带有不同 符号的电荷,在界面上形成了双电层的结构。 早在1879年,Helmholz提出了平板型模型; 1910年Gouy和1913年Chapman修正了平板型模型, 提出了扩散双电层模型; 后来Stern又提出了Stern模型。
带电的固体或胶粒在移动时,移动的切动面与液
体本体之间的电位差称为 电势。 在扩散双电层模型中,切动面AB与溶液本体之间
的电位差为 电势; 在Stern模型中,带有溶剂化层的滑移界面与溶液 之间的电位差称为
电势。
电势总是比热力学电势低,外加电解质会使
电势变小甚至改变符号。
只有在带电质点移动时才显示出
又被称为电动电势。
电势,所以它
扩散双电层模型 吸附离子 胶粒表面 紧密层 (离子和溶剂化分子) 反号离子 扩散层
ζ电势: 胶粒表面滑移界面处的电势。 胶粒表面热力学电势φ和电动电势(ζ电势) 的区别: ① 发生在不同的部位; ② 大小不同,一般情况下ζ电势只是热力学 电势的一部分,其绝对值小于φ。
电势
a
d '' d' d
扩散双电层模型课件

在燃料电池领域的应用
质子交换膜燃料电池
在质子交换膜燃料电池中,扩散双电层模型可用于描述质子 在膜中的传输行为以及与电极之间的相互作用,有助于优化 电池的燃料利用率和能量转换效率。
直接甲醇燃料电池
在直接甲醇燃料电池中,扩散双电层模型可用于研究甲醇分 子在膜中的传输以及与电极之间的相互作用,有助于提高电 池的性能和稳定性。
主要研究内容回顾
01
02
03
04
介绍了扩散双电层的基本概念 和理论
分析了扩散双电层模型在电极 过程研究中的应用
讨论了扩散双电层模型的计算 方法和实现细节
探讨了影响扩散双电层模型精 度的因素和改进措施
研究成果与结论
通过对比实验验证了所提出的 扩散双电层模型的准确性和可 靠性
分析了不同因素对电极过程的 影响,并证明了扩散双电层模 型在这些情况下的适用性
电解质
电解质是指在水溶液或熔 融状态下能够导电的化合 物,如酸、碱、盐等。
电极
电极是指与电解质溶液接 触并用于施加电场的导电 固体,如电池的正负极。
扩散双电层模型简介
扩散双电层的形成
在电极与电解质溶液接触的界面上,由于离子的吸附和释放,会 形成一层扩散双电层,其中包含正负电荷分布。
扩散双电层的结构
平板电容器
在电场作用下,两个平板 之间会形成电荷分布,这 种电荷分布被称为电双层 。
扩散过程
离子在溶液中会受到电场 作用而扩散,导致电荷分 布发生变化。
建立模型
根据平板电容器理论和扩 散过程,可以建立扩散双 电层模型。
模型参数确定
电场强度
电场对离子的作用 力。
时间
扩散过程需要时间 。
电荷密度
电荷在溶液中的分 布密度。
双电层及其结构模型

13
结论:
(1)不论电极表面存在正剩余电荷还是负剩余 电荷,界面张力都将随剩余电荷数量的增加而 降低。 (2)根据电毛细曲线的微分方程 ,可以直接通 过电毛细曲线的斜率求出某一电极电位下的电 极表面剩余电荷密度q,也可以方便地判断电 极的零电荷电位值和表面剩余电荷密度的符号。
14
二、双电层的微分电容
4
2、研究电极/溶液界面的思路:
通过使用一些可测的界面参数来研究电极/溶 液界面; 根据一定的界面结构模型来推算界面参数 , 根据实验测量数据来检验模型。 研究的基本方法:充电曲线法 、微分电容曲线 法、电毛细曲线法
5
3、研究电极/溶液界面对研究电极的要求
直流电通过一个电极时,可能 起到以下两种作用:
d /d q
微分电容法是利用Cd~φ 曲线下方的面积求q,
q dq C d 微分电容法更精确和灵敏。 0 d
0
q
微分电容法的应用更广泛 微分电容法和电毛细曲线法都是研究界面结构 与性质的重要实验方法,二者不可偏废。
24
四、零电荷电位
1、零电布和电位分布
双电层的金属一侧,剩 余电荷集中在电极表面。 在双电层的溶液一侧, 剩余电荷的分布有一定 的分散性。 d为紧贴电极表面排列的 水化离子的电荷中心与 电极表面的距。
图4-11金属/溶液界面剩余电荷与电位的分布
37
(1)紧密层电位分布:从x=0点到x=d的范围内 不存在剩余电荷,这一范围即为紧密层。紧密 层厚度为d。如果紧密层内的介电常数是恒定 的,则该层内的电位分布是线性变化的。
34
图4-9 考虑了热运动干扰时的电极/溶液界面双电层结构
35
在金属相中:金属中全部剩余电荷都是紧密 分布,金属内部各点的电位均相等。 在溶液相中: (a)当溶液总浓度较高、电极表面电荷密度较 大时,溶液中剩余电荷倾向于紧密分布,形 成图4-8的紧密双电层。
双电层理论——精选推荐

双电层理论表面物理化学所涉及的内容非常宽广,固体在溶液中的荷电性质,实际上影响着固体表面性质和界面区的电荷转移反应及其进行的速度。
由于多种极其重要的表面电化学效应的发现,表面电化学引起了许多种科学家的重视和研究。
第一节 双 电 层2.1.1 双电层的产生在自然界中,固体与液体接触时,固体表面的荷电现象实际上是普遍存在的。
它导致了固—液界面的液体一侧带着相反电荷,这种界面电荷影响界面周围介质中的离子分布,与界面电荷符号相反的介质中的离子被吸向界面(这种离子称为反离子Counter -ions ),而相同符号的离子(称为同离子Co -ions )则被排离界面。
与此同时,离子的热运动又促使它们均匀混合在一起。
因此,在带电界面上形成一个扩散双电层(diffuse double layer )。
所谓扩散,就是界面周围介质中的反离子的过量是以扩散形式分布的,而不是非常整齐地集中排列在带电界面的周围。
例如,人体内与血液接触的动静脉壁和血液中胶粒等界面区都存在双电层结构,致使血液在血管中畅通无阻地流动以输送全身新陈代谢的营养而不产生血栓。
双电层理论研究反离子的扩散分布和带电界面的性质。
固体在溶液中荷电而构成双电层的原因,除了外加电场之外,大致上可归纳为以下几种情况: ① 电离作用固体表面在溶液中产生电离或溶液中的电离成分依靠某种结合力与固体表面结合而使其荷电。
例如,玻璃与水接触时,玻璃中的硅酸盐可电离出钾离子、钠离子或氢离子等,于是使玻璃带负电性而溶液带正电性;蛋白质分子具有的羧基(—COOH)和胺基(—NH 2)官能团,当pH 值降低时(酸性),溶液中电离的H +与胺基以氢键结合,从而使蛋白质带正电,-NH 2+H 2O -NH 3++OH -,而溶液一侧带负电,即在羧酸介质中—COOH 的电离被高氢浓度离子所抑制:—COOH+H 2O -COO -+H 3O+ 当pH 值升高时(碱性),蛋白质的羧基电离而使其带负电。
应用电化学-1-3-双电层

电极溶液界面的紧密 双电层结构
考虑了热运动干扰时的电极溶 液界面双电层结构
在金属相中,自由电子的浓度很大,可达1025 mol/dm3 ,少量 剩余电荷在界面的集中并不会明显破坏自由电子的均匀 分布,因此可以认为金属中全部剩余电荷都是紧密分布 的,金属内部各点的电势均相等。 在溶液相中,当溶液总浓度较高,电极表面电荷密度较 大时,由于离子热运动较困难,对剩余电荷分布的影响 较小,而电极与溶液间的静电作用较强,对剩余电荷的 分布起主导作用,溶液中的剩余电荷也倾向于紧密分布, 形成紧密双电层。
q
1.3.4 双电层的结构
在电极/溶液界面存在着两种相间相互作用:
(1)电极与溶液两相中的剩余电荷所引起的静电长程作用; (2)电极和溶液中各种粒子(离子、溶质分子、溶剂分子等等) 之间的短程作用,如特性吸附、偶极子定向排列等,它只 在几个Å的距离内发生。
电极溶液界面的基本结构
• 静电作用使得符号相反的剩余电荷力图相互靠近,形成紧密 的双电层结构,简称紧密层。 • 热运动处使荷电粒子倾向于均匀分布,从而使剩余电荷不可 能完全紧贴着电极表面分布,而具有一定的分散性,形成分 散层。
1.3.1.1 界面电荷层的形成
自发形成的双电层 M
+ + + + + + + + + + + + + + + + + + + +
S
M
+
S
+
M
+
S
+
(a)离子双电层
(b)吸附双电层
(c)偶极双电层
强制形成的双电层
双电层

双电层双电层的形成:当两相接触时,如果电子或离子等荷电粒子在两相中具有不同的电化学位,荷电粒子就会在两相之间发生转移或交换,界面两侧便形成符号相反的两层电荷,人们把界面上的这两个荷电层称为双电层。
如金属、溶液界面(M/L)两侧,若μM+>μM+(L),则荷电粒子发生转移,金属表面荷负点;反之,则金属表面荷正,这种双电层常称为离子双层。
尽管有时上述的离子双层并不存在,但金属与溶液界面间仍然会存在着电位差,无论是金属表面,还是溶液表面,都存在着偶极层。
由于偶极子正负电荷分隔开而形成的双电层,称为偶极双电层。
对任何一种金属而言,由于金属的电子会“溢出”金属表面形成双极子。
所以即使溶液一侧不存在偶极子层,但对金属与溶液的界面来说,这种偶极双层总是存在的。
此外,溶液中某一种离子有可能被吸附于电极与溶液界面上,形成一层电荷。
这层电荷又借助静电作用吸引溶液中同等数量的带相反电荷的离子而形成双电层,可称之为吸附双层。
这里应当注意:界面上第一层电荷的出现,靠的是静电力以外的其他化学与物理作用,而第二层电荷则是由第一层电荷的静电力引起的。
如果界面上有了吸附双层,当然也会产生一定大小的电位差。
金属与溶液界面的电位差系由上述的三种类型电位差的一部分或全部组成,但其中对电极反应速度有重大影响的,则主要是离子双层的电位差。
离子双层的形成有两种可能的情况。
一是在电极与溶液一旦接触后的瞬间自发形成的。
另一种情况,是在外电源作用下强制形成的双电层。
因为有的时候,当金属与溶液接触时,并不能自发地形成双电层。
如将纯汞(Hg)放入Kill溶液的界面上常常不能自发的形成双电层。
但是,如果将Hg电极与外电源负极连接,外电源就向Hg电极供应电子,在其电位达到K+还原电位之前,电极上不会发生电化学反应,因而此时Hg电极上有了多余的电子而带上负电。
这层负电荷吸引溶液中相同数量的正电荷(如K+),形成双电层。
双电层的结构模型:金属电极和溶液之间界面上形成的双电层,从结构上可以有离子双电层、表面偶极双电层和吸附双电层等三种类型。
界面现象与双电层结构全解

有机分子的吸附规律
电极/溶液界面上的吸附与在一般表面上的吸附都 服从某些共同规律
电极/溶液界面具有可在一定范围内连续变化的电 场而又存在某些特殊规律
有机表面活性分子在电极表面的吸附行为,除了 与其本身的化学性质和浓度有关外,电极表面电 荷密度和电极表面的化学性质也能影响其吸附行 为
同一有机表面活性分子在不同的电极表面上以及 在不同电势下的吸附行为也可以极不相同
某些粒子在界面上发生吸附时其吸附量、界面张 力和化学势三者具有如下关系:
d i di
李普曼(Lippman)公式的推导
当电极表面上的剩余电荷密度为q时,电子的表面
吸附量为θe=-q/F,而电子向界面移动的化学
势变化为dμe=-Fdφ, 电子的吸附量与化学势
的乘积为:
i di
q F
( Fd )
若推算的界面参数与实验测得的界面参数吻合, 则假设的界面双电层结构模型反映了界面的真实 结构
电毛细曲线方法和微分电容方法
理想极化电极与理想非极化电极 电毛细曲线方法 微分电容法 电毛细曲线法与微分电容法的比较
外电路流向电极/溶液界面电荷的作用
对于任何电化学体系,通过外电路流向电极/溶 液界面的电荷可能参加两种不同的过程
双电层结构理论的发展
博克里斯(Bockris)的新双电层模型认为双电层 结构必须考虑到双电层内存在着离子的特性吸附 和水分子的定向排列
紧靠电极表面的第一层水分子全部都定向排列, 这层水的相对介电常数ε降至6~7(称之为介电饱 和)
第二层水分子是部分定向排列,其中有些水分子 是离子的初级水化水,它的相对介电常数ε为30~ 40,少于正常水的ε=78.5
由外电源提供的电荷电量全部用于电化学反应而 电极电势不变的电极体系称之为“理想非极化电 极”
双电层

在扩散层中,电势随离表面距离的变化大致呈指数关系。对于平的带电表面,若Ψ0不很高,则扩散层中的电 势随离表面的距离x的变化可用图中式子表示。
Ψ=Ψd▪e-Kx
式中K的倒数称为双电层厚度,与溶液内部各种离子浓度(单位体积中的离子数目)及价数Zi的关系可用图 中式子表示。
式中 e为电子电荷;ε为溶液的电容率;k为玻耳兹曼常数;T为热力学温度。上式表明,增加溶液中的离子 浓度与价数均使双电层变薄,扩散层内的电势降也因此加,带电表面则排斥同号离子并将反离子吸引至表面附近,溶液中离子的 分布情况由上述两种相对抗的作用的相对大小决定。根据O.斯特恩的观点,一部分反离子由于电性吸引或非电性 的特性吸引作用(例如范德瓦耳斯力)而和表面紧密结合,构成吸附层(或称斯特恩层)。其余的离子则扩散地 分布在溶液中,构成双电层的扩散层(或称古伊层)。由于带电表面的吸引作用,在扩散层中反离子的浓度远大 于同号离子。离表面越远,过剩的反离子越少,直至在溶液内部反离子的浓度与同号离子相等。
双电层
过剩的电荷相与吸引
01 介绍
03 结构 05 实验证明
目录
02 理论 04 详解
任何两个不同的物相接触都会在两相间产生电势,这是因电荷分离引起的。两相各有过剩的电荷,电量相等, 正负号相反,相互吸引,形成双电层。
介绍
第三章-电极溶液界面
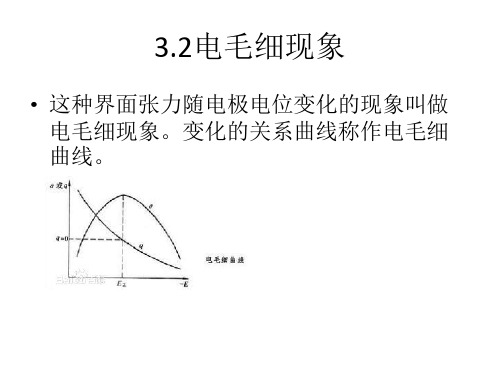
• 影响:改变电极上双电层的分布,从而影 响反应粒子在电极表面的浓度和活化能, 使反应速率发生变化
一、无机离子的吸附
• 1.大多数无机阴离子是表面活性物质,而无 机阳离子的表面活性很小,只有少数离子 才表面活性。
表面张力变化原因
• 无论双电层是带正电还是带负电,由于同 性电荷的相互排除使界面有扩大的趋势, 与表面张力使界面缩小的趋势相反。因此, 带电界面比不带电界面表面张力下。而剩 余电荷密度与电势有关,故表面张力与电 势有关。
二、电毛细曲线的微分方程
• 根据吉布斯等温吸附方程
d id i
i
电子的表面吸附量 e q / F
• 常用的方法: • 充电曲线法
• 电位扫描法
氢原子的吸附
• 氢的吸附过程伴随有氢分子的分解,分解 生成的氢原子与金属表面相互作用而形成 吸附键。吸附氢原子与吸附自由氢原子是 不同的,吸附过程放出大量吸附热,吸附 氢原子的能量低得多。
氧原子的吸附
• 在常温下,主要是氧原子和含氧粒子的吸 附。这些含氧粒子是在逐步还原或OH-逐步 氧化过程形成并吸附的。
若保持电位恒定,并保持i组分外的化学势不变
i
(
i
) ,ki
负离子可逆,正离子表面剩余电荷量
(
Ina
)
1
正离子离子可逆,负离子表面剩余电荷量
( Ina
)
1
求解表面剩余电荷量的步骤
• 1.测量不同电解质浓度的电毛细曲线 • 2.从各条电毛细曲线下取同一相对电位下的
• 值,做出 ~ Ina 关系曲线。
双电层电位由紧密层电位差和分散层电位差
锌铜原电池双电层模型

锌铜原电池双电层模型锌铜原电池是一种常见的原电池,它基于锌和铜两种金属之间的化学反应产生的电能。
在锌铜原电池中,锌金属作为负极材料,铜金属作为正极材料,它们之间通过电解质溶液进行接触。
锌铜原电池的双电层模型是一种描述电池工作原理的模型。
它将电池中的电荷分布分为两个区域:电解质层和电极电缓冲层。
电解质层是指电解质溶液与金属电极之间的接触面积。
在电解质溶液中,溶质会负责释放或接收电荷,并通过离子传递电流。
这些电荷在溶液中通过离子和或电子形式传递,从而维持电池的电流。
电极电缓冲层是锌和铜金属表面与电解质之间的接触区域。
当电解质中的正负离子接触到金属表面时,它们会吸附在金属表面上,形成一个电荷层,称为电荷分离层。
这个分离层中的电荷主要来源于溶解或沉积在金属表面的离子。
这一层的存在能够阻止金属表面进一步溶解或沉积,从而保护电极免受腐蚀。
在锌铜原电池中,当电池闭合时,锌金属通过电解质向铜金属释放电荷。
锌金属表面发生氧化反应,将离子释放到电解质溶液中,同时电子通过外部电路流向铜金属,形成电流。
铜金属表面接收到的金离子会还原,从溶液中沉积到金属表面。
双电层模型的核心思想是,在电极电缓冲层中存在着大量的表面电荷,通过吸附和吸附等机制与电解质中的离子交换电荷。
在电池工作过程中,这些电荷层的行为会影响电极的电位和电荷的传递速度。
因此,理解电极电缓冲层的特性和电荷分布对于理解锌铜原电池的工作原理至关重要。
需要指出的是,双电层模型只是对锌铜原电池内部电荷分布和传递的一种理论解释,并不涉及电池的具体结构和其他细节。
在实际应用中,锌铜原电池的性能还受到许多因素的影响,如金属纯度、电解质浓度、温度等。
因此,在设计和使用锌铜原电池时,还需要考虑这些因素,以获得更好的电池性能。
双电层及其结构模型课件

• 双电层概述 • 双电层的结构模型 • 双电层的应用 • 双电层的实验研究方法 • 双电层研究的挑战与展望 • 双电层理论在实践中的应用案例
01
双电层概述
双电层的定义
总结词
双电层是指吸附在固体颗粒表面的带电薄层。
详细描述
双电层是由固体颗粒、水和电解质组成的系统中的静电作用力所形成的带电薄 层。这个薄层分为紧密层和扩散层两部分,其中紧密层吸附在固体颗粒表面, 而扩散层则与紧密层保持一定的距离。
唐南模型
总结词
唐南模型引入了唐南势的概念,描述了双电层中离子与溶剂分子间的相互作用。
详细描述
唐南模型认为,双电层中的离子与溶剂分子之间存在相互作用,这种作用会影响离子的分布。唐南模 型通过引入唐南势的概念,描述了这种相互作用及其对离子分布的影响。该模型进一步深化了人们对 双电层结构的理解。
萨尔瓦托雷模型
粒子电泳法
总结词
利用粒子在电场中的移动行为,研究双电层的结构和性质。
详细描述
粒子电泳法是一种实验方法,通过测量粒子在电场中的移动行为,分析双电层的结构和 性质。该方法可以用于研究粒子在双电层中的吸附和脱附行为,以及双电层的结构和电
化学性质。
表面张力法
总结词
通过测量表面张力随溶液离子浓度的变化,分析双电层 的结构和性质。
03
双电层的应用
在电化学中的应用
电池
双电层理论在电池领域的应用主要涉 及电极过程动力学和电化学反应机制。 通过研究双电层的形成和演化,可以 优化电池的充放电性能,提高电池的 能量密度和寿命。
电镀和电化学抛光
在电镀和电化学抛光过程中,双电层 理论有助于理解金属离子的沉积和溶 解过程,从而优化工艺参数,提高镀 层质量和抛光效果。
双电层及其结构模型课件

目 录
• 双电层概述 • 双电层的结构模型 • 双电层的应用 • 双电层研究的挑战与展望 • 实验操作与演示 • 习题与思考
01 双电层概述
双电层的定义
总结词
双电层是吸附在电极表面上的带电物质层。
详细描述
双电层是指吸附在电极表面上的带电物质层,通常由电解质溶液中的离子吸附 形成。在电极表面,带电物质层的电荷分布与体相溶液中的电荷分布不同,形 成一个具有特殊性质的界面层。
电层研究带来新的突破。
05 实验操作与演示
双电层实验操作
准备实验材料
配置电解质溶液
准备电解质溶液、电极、电导率计、离心 机等实验器材和试剂。
根据实验需要,配置不同浓度的电解质溶 液,确保溶液的纯净度和浓度符合实验要 求。
电极处理
实验操作
对电极进行预处理,如打磨、清洗等,以 提高电极表面的电导率和活性。
03 双电层的应用
在电化学中的应用
电池
双电层理论在电池领域的应用主要涉及电极过程动力学和电 化学反应机制。通过研究双电层的形成和变化,可以优化电 池的充放电性能,提高电池的能量密度和寿命。
电镀
电镀过程中,双电层理论用于解释金属离子在电极表面的吸 附和还原过程,从而指导电镀工艺的优化,提高镀层的质量 和均匀性。
结论总结
根据实验结果,总结双电层的形成机制、影响因素以及与物质吸附 和电化学反应的关系。
06 习题与思考
基础习题
01
02
03
04
1. 请简述双电层的概念。
2. 列举双电层的形成原 因。
3. 描述双电层的结构特 点。
4. 解释双电层对物质吸 附和分离的影响。
思考题
双电层

双电层理论的历史背景
⑴平板电容器模型(紧密层模型)(1879 ) ⑵扩散双电层模型:(1910-1913) ⑶Stern模型 (1924) ⑷Grahame修正的GCS模型 ⑸BDM模型
双电层理论的定义
定义:在水中,固体表面因表面基团的 解离或自溶液中选择性吸附某种离子而 带电,带电表面与反离子构成双电层的 理论。
谢谢!
双电层理论在钛白粉行业的应用
通常钛白粉生产工艺要求浆液具有较高 的固含量、较低粘度同时具有较好的稳 定性。 1、首先粒子不能太大,如果粒子引力足 够大,彼此就会相互粘附,导致粒子束 快速沉降(如:絮凝)。 2、另一重要因素是粒子间的吸引力。
通常采用的防止絮凝的方法可以通过双 电层稳定机制来解决,即通过调节pH 值使颗粒表面带上一定的表面电荷,形 成双电层;通过双电层之间的排斥力使 粒子之间的引力大大降低,从而实现粉 体的分散。这就是在水性溶剂中, 钛白 粉呈现高度的分散性的原因。
双电层的结构
静电作用使得符号相反的剩余电荷力相互靠近,形成紧 密的粒子倾向于均匀分布,从而使剩余电荷不 可能完全紧贴着电极表面分布,而具有一定的分散性, 形成分散层。双电层由紧密层和分散层两部分组成。
电极溶液界面的紧密 双电层结构
考虑了热运动干扰时的电极溶 液界面双电层结构
电化学界面的基本结构特征:双电层

将d=0.5nm代入,C ≈10 μF/cm2
其中Δ ≈1nm
化
=
电
=
学
③双电层内电场的大小
Δ(Δ)
Δ
= 1 × 109 Τ
江
改变值将为Δ =
大
学
虽然ΔV 未知,但如果双电层两侧电压变化1V时(即Δ(Δ) =1V),则双电层内电场的
大
学
Zn2+
化
Zn2+
-+
-+
-+
Zn
-+
-+
-+
电
水化作用
静电引力
电子
Cu
Cu2+
静电引力
江
浙
Cu2+
水化作用<电子云的静电引力
最终形成了稳定的双
Zn2+
+++Cu
+++Cu2+
格中转移到溶液中,
电层结构。
额外电场
水化作用
阻碍Zn2+进一步从晶
阻碍溶液中的Cu2+进一
步向晶格中转移,最终
形成了稳定的双电层结
2.2 人为可控的双电层结构
+
+
+
+
+
+
+
+
+
+
+
电
e
化
n e-
e
大
学
e
e
e
浙
双电层及其结构模型

双电层及其结构模型双电层是指由正负离子之间形成的电荷层,存在于液体中。
它由紧密吸附在电极表面的正离子层(即化学吸附层)和漂浮在电极表面附近的负离子层(即物理吸附层)组成。
这种双电层的存在是由离子在液体中的溶解度和电离度决定的。
双电层的结构模型可以分为两种,分别是亚布力德双电层模型和海维赛德双电层模型。
亚布力德双电层模型是由瑞士物理学家亚布力德在20世纪30年代提出的。
他认为双电层可以看作由一个内层和一个外层组成。
内层是紧贴电极表面的化学吸附层,包含正离子和一些吸附的溶质分子。
溶质分子与电极表面之间通过共价键或静电相互作用而吸附在一起。
外层则是由溶剂中的负离子组成的物理吸附层,负离子漂浮在电极表面附近,受到电极电场的作用而停留在该位置。
这种模型认为,双电层是稳定的,且在不同电势条件下会有不同的结构。
海维赛德双电层模型是由英国科学家海维赛德在20世纪起提出并发展的。
这个模型认为双电层由内层和外层组成,类似于亚布力德的模型。
但是,海维赛德提出了一种新的概念,即溶剂分子的极化。
他认为,在电极表面附近,溶剂分子会被电场极化,形成一个特定方向的电偶极子,这些电偶极子会受到电场力的作用而定向堆积,形成外层。
因此,海维赛德提出的双电层模型中考虑了电极表面电场对溶剂的影响。
总的来说,双电层的结构模型揭示了离子在液体中的封闭性和电极表面的吸附现象。
根据这些模型,我们可以更好地理解双电层的形成和性质,进一步研究电化学反应、电容和电化学储能等领域的基本原理和应用。
简述斯特恩扩散双电层模型的要点

简述斯特恩扩散双电层模型的要点全文共四篇示例,供读者参考第一篇示例:斯特恩扩散双电层模型是描述电解质溶液板间的电荷分布和电荷传输特性的经典模型。
它由德国化学家斯特恩于1924年发表,是对古典电解质理论的重要补充,为后来电化学领域的发展奠定了基础。
斯特恩扩散双电层模型主要包括普朗克层和斯特恩层两部分,下面将详细介绍其要点。
普朗克层是指电解质板间的一个致密层,其中的电荷分布由电离的离子和溶剂分子组成。
在这一层内,带正电荷的离子和带负电荷的溶剂分子被吸附在固体表面上,形成一个电荷层。
普朗克层的存在表明,在电解质板间有着一定程度的电离和电荷分布,从而影响溶液的电导率和电化学性质。
斯特恩扩散双电层模型的要点在于描述了电解质溶液中的电荷分布和电荷传输特性,揭示了电解质溶液板间的复杂结构和动力学过程。
这一模型在电化学领域具有重要的理论意义和实际应用价值,为研究电解质在溶液中的行为提供了有力的理论支持。
它不仅有助于理解溶液的电导率、极化性和化学反应动力学等方面的问题,还有助于设计新型电化学传感器、储能器件和电解质材料等应用。
斯特恩扩散双电层模型是电化学领域的经典模型之一,对于理解电解质溶液中的电荷分布和传输特性具有重要意义。
通过研究该模型,我们可以更深入地认识电解质溶液的结构和性质,为开发新型电化学器件和解决环境、能源等问题提供理论支持和技术指导。
希望本文所介绍的斯特恩扩散双电层模型的要点能够对读者有所启发,促进电化学领域的研究和发展。
第二篇示例:斯特恩扩散双电层模型是描述电解质溶液中电荷粒子的扩散行为的重要理论模型。
该模型由德国物理化学家斯特恩在20世纪初提出,并被广泛应用于解释电解质在电解质溶液中的扩散现象。
在斯特恩扩散双电层模型中,电解质溶液被认为是由两层电荷分布较为复杂的离子团组成,即离子团层和双电层。
离子团层是由电解质分子及其离子团组成的,在浓度较高的情况下,这一层中的离子趋向于形成大的簇块,受到周围电场的影响较小。
电化学双电层理论和模型

双电层双电层的形成:当两相接触时,如果电子或离子等荷电粒子在两相中具有不同的电化学位,荷电粒子就会在两相之间发生转移或交换,界面两侧便形成符号相反的两层电荷,人们把界面上的这两个荷电层称为双电层。
如金属、溶液界面(M/L)两侧,若μM+>μM+(L),则荷电粒子发生转移,金属表面荷负点;反之,则金属表面荷正,这种双电层常称为离子双层。
尽管有时上述的离子双层并不存在,但金属与溶液界面间仍然会存在着电位差,无论是金属表面,还是溶液表面,都存在着偶极层。
由于偶极子正负电荷分隔开而形成的双电层,称为偶极双电层。
对任何一种金属而言,由于金属的电子会“溢出”金属表面形成双极子。
所以即使溶液一侧不存在偶极子层,但对金属与溶液的界面来说,这种偶极双层总是存在的。
此外,溶液中某一种离子有可能被吸附于电极与溶液界面上,形成一层电荷。
这层电荷又借助静电作用吸引溶液中同等数量的带相反电荷的离子而形成双电层,可称之为吸附双层。
这里应当注意:界面上第一层电荷的出现,靠的是静电力以外的其他化学与物理作用,而第二层电荷则是由第一层电荷的静电力引起的。
如果界面上有了吸附双层,当然也会产生一定大小的电位差。
金属与溶液界面的电位差系由上述的三种类型电位差的一部分或全部组成,但其中对电极反应速度有重大影响的,则主要是离子双层的电位差。
离子双层的形成有两种可能的情况。
一是在电极与溶液一旦接触后的瞬间自发形成的。
另一种情况,是在外电源作用下强制形成的双电层。
因为有的时候,当金属与溶液接触时,并不能自发地形成双电层。
如将纯汞(Hg)放入Kill溶液的界面上常常不能自发的形成双电层。
但是,如果将Hg电极与外电源负极连接,外电源就向Hg电极供应电子,在其电位达到K+还原电位之前,电极上不会发生电化学反应,因而此时Hg电极上有了多余的电子而带上负电。
这层负电荷吸引溶液中相同数量的正电荷(如K+),形成双电层。
双电层的结构模型:金属电极和溶液之间界面上形成的双电层,从结构上可以有离子双电层、表面偶极双电层和吸附双电层等三种类型。
双电层及其结构范文

双电层及其结构范文双电层是指电解质溶液与电极表面相接触时,在界面处形成的两层电荷,分别位于溶液和电极之间。
它是电解质溶液与电极之间的过渡区域,是电化学反应的基本界面。
双电层的结构非常复杂,目前尚无一个完全准确的模型来描述其精细的结构,然而,研究表明双电层主要由两个部分构成,即1.电极表面附近的紧密吸附层(Helmholtz层)和2.扩散层。
1. 紧密吸附层(Helmholtz层): 紧密吸附层位于电极表面非常靠近的位置,主要由电极表面附近的离子组成。
它是由于电极表面的电位差吸引了离子,并使离子在电极表面附近紧密吸附而形成。
紧密吸附层中离子的浓度非常高,形成一个电化学的二维层。
Helmholtz层的厚度约为单层离子的直径,通常为纳米级别。
在这一层中,离子以带电的形式吸附在电极表面,形成一个倾斜电场,将离径向分离。
Helmholtz层的电势差称为电解层电势差,它是由于电极表面的电位差引起的。
2. 扩散层: 扩散层位于Helmholtz层外部,主要由水分子和离子组成。
扩散层中的离子浓度逐渐降低,最终达到与体相中离子浓度相同的水平。
扩散层中水分子的运动会受到离子电场的影响,使得水分子的平均速度增加,形成所谓的电场扩散。
在扩散层中,离子的浓度梯度会引起离子的迁移,从而产生扩散电流。
除了紧密吸附层和扩散层,双电层还包括溶液中的离子云层和溶剂分子。
离子云层是离子周围的低浓度区域,通常被认为是由具有相同电荷的反离子组成的。
溶剂分子在双电层中起到辅助离子迁移的作用,与离子之间相互作用。
总结起来,双电层的结构可以简单地描述为电极表面附近的Helmholtz层和外部的扩散层。
Helmholtz层是紧密吸附层,其中的离子以带电形式吸附在电极表面,形成电解层电势差。
扩散层由溶液中的水分子和离子组成,离子在其中通过电场扩散迁移。
双电层的结构是电化学反应的基础,对理解电化学界面和电化学反应机理都具有重要意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
交流电桥法测定微分电容的基本线路: 交流信号源
交流电桥
直流极化回 路
电极电位测量回路
图4-4 交流电桥测量微分的基本电路
电解池等效等效电路:
Cd
Rl
a
b
图4-5 时电解池等效电路
测量方法:测量时,小振幅的交流电压由交流信号发生器G加到电桥的1、2两端。调节Rs和Cs, 使之分别等于电解池等效电路的电阻和电容部分时,电桥3、4两端点的电位相等,电桥平 衡,示波器O示零。
大多数无机阳离子不发生特性吸附,只有少数水化能较小的阳离子如Tl+,Cs+等离子能 发生特性吸附。除了F-离子外,几乎所有的无机阴离子都或多或少地发生特性吸附
在实际工作中,人们常利用界面吸附现象对电极过程的影响来控制电化学过程。
第三节双电层及其结构
一、双电层的类型 1、双电层的类型及构成 双电层:电量相等符号相反的两个电荷层。 双电层大致有三类:离子双电层;偶极双电层; 吸附双电层。 2、双电层的基本特点 双电层的厚度小 ;双电层中存在一定大小的电容和电场强度 。
域。 界面结构:指在电极/溶液界面过渡区域中剩余电荷和电位的分布以及它们与电极电位的关
系。 界面性质:指界面层的物理化学特性,尤其是电性质。
2、研究电极/溶液界面的思路: 通过使用一些可测的界面参数来研究电极/溶液界面; 根据一定的界面结构模型来推算界面参数 ,根据实验测量数据来检验模型。 研究的基本方法:充电曲线法 、微分电容曲线法、电毛细曲线法
1dad(a ψ 1)dψ 111(4-7)
C d dq dq dqC 紧C 分
图4-12双电层电容组成
三、双电层结构模型
平板电容器模型:该模型把双电层看作平板电容器,电极上的电荷位于电极表面,溶液 中的电荷集中排列在贴近电极的一个平面上,构成紧密层。紧密双电层的电容为
C=ε/4πd
(4-8)
该模型可以解释界面张力随电极电位变化的规律和微分电容曲线上所出现的平台区;但解
当电极表面存在正的剩余电荷时q>0,则: 对应电毛细曲线左半支
当电极表面存在负的剩余电荷q<0时,则: 对应电毛细曲线右半支。
d/d0
d/d0
结论:
(1)不论电极表面存在正剩余电荷还是负剩余电荷,界面张力都将随剩余电荷数量的增加 而降低。
(2)根据电毛细曲线的微分方程 ,可以直接通过电毛细曲线的斜率求出某一电极电位下的 电极表面剩余电荷密度q,也可以方便地判断电极的零电荷电位值和表面剩余电荷密度 的符号。
3、研究电极/溶液界面对研究电极的要求
直流电通过一个电极时,可能起到以下两种作用:
Rf
在界面上参加电化学反应而被消耗 ;
用来改变界面结构,参与建立或改变双电层。
图4-1(a)
Hale Waihona Puke C电极等效电路动画
理想极化电极(重要概念)
定义:在一定电位范围内,有电量通 过时不发生电化学反应的电极体系称 为理想极化电极。
q
q
dq
0
0Cdd
(4-6)
电极电位为φ时的 q的数值相当于图 4.7中的阴影部分 的面积。
图4.7利用微分电容曲线计算电极表面剩余电荷密度q值
三、电毛细曲线法和微分电容法比较 求q :电毛细曲线法利用σ~φ曲线的斜率求q
d/dq 微分电容法是利用Cd~φ 曲线下方的面积求q,
微分电容法的应用更广泛
根据电解池的等效电路,读取Rs和Cs 数值。 结果:
Rl
R2 R1
Rs
(4-4)
Cd
R1 R2
Cs
(4-5)
当 R1 R2 时 Rl Rs Cd Cs
3、微分电容曲线
微分电容曲线:用微分电容Cd相对于电极电位φ的变化所作的曲线,称为微分电 容曲线。
微分电容法:根据微分电容曲线所提供的信息来研究界面结构与性质的实验方法。
双电层静电模型-GCS分散层模型:该模型认为双电层是由紧密层和分散层两部分组成 的。这一模型对分散层的讨论比较深入细致,对紧密层的描述很简单,并且采用了与古 依-查普曼相同的数学方法处理分散层中剩余电荷和电位的分布及推导出相应的双电层 方程式 。
(1)斯特恩模型能比较好地反映界面结构的真实情况 ,但双电层方程式不能用作准确计算
微分电容法q和电毛细曲线法都是研究界面结构与性质的重要实验方法,二者不可偏废。
q 0 dq 0Cdd
微分电容法更精确和灵敏。
四、零电荷电位 1、零电荷电位概念及理解
零电荷电位概念两种定义: 电极表面剩余电荷为零时的电极电位 电极/溶液界面不存在离子双电层时的电极电位 对零电荷电位的理解:零电荷电位仅仅表示电极表面剩余电荷为零时的电极电位,而不表示
释不了界面电容随电极电位和溶液总浓度变化而变化,以及在稀溶液中零电荷电位下微 分电容最小值等基本实验事实。
分散双电层模型:该模型认为溶液中的离子电荷在静电作用和热运动作用下,不是集中 而是分散的,分散的规律遵循玻耳兹曼分布,完全忽略了紧密层的存在。
该模型能较好地解释微分电容最小值的出现和电容随电极电位的变化,但理论计算的微分 电容值却比实验测定值大得多,而且解释不了微分电容曲线上“平台区”的出现。
零电荷电位与电极电位联合用于处理电极过程的动力学问题的几个作用: 通过零电荷电位判断电极表面剩余电荷的符号和数量。例判断q的符号:
例:对于体系
当:
时; 时:
Hg KCl 0 0.19V
10.1V 2 2 0.2V 4
qq12
0 0
零电荷电位的电极电位值体现了电极/溶液界面的性质, φ0处一切依赖于q的表面性质 均达极限值 ,所以 φ0 是个特征点 ,这些特征有助于人们对界面性质和界面反应的深入 研究;
零标电位可以方便提供电极表面荷电情况、双电层结构、界面吸附等方面的有关信息, 这是氢标电位所做不到的。
将 选作新的电位衡量点,就有了一个新的衡量电极电位的体系——零标电位。 0
零标电位:相对于零电荷电位的相对电极电位。
零标:以零电荷电位作为零点的电位标度。
五、特性吸附
特性吸附:溶液中的离子还由于与电极表面的短程相互作用而发生的物理吸附或化学吸 附。
二、双电层的微分电容
1. 微分电容概念 理想极化电极作为平行板电容器处理,电容值为一常数,即
微分电容:引起电位微小变化时所需引入电极表面的电量,也表征了界面在电极电位发
生微小变化时所具备的贮存电荷的能力。
C 0 r
l
(4-2)
dq Cd d
(4-3)
2、 微分电容的测量
交流电桥法:在处于平衡电位 或直流极化的电极上迭加一个小振幅(扰动<10mV)的 交流电压,用交流电桥测量与电解池阻抗相平衡的串联等效电路的电容值与电阻值, 从而求得电极的双电层电容的方法
C
理想极化电极等效电路
常用的理想极化电极——滴汞电极
HgH ge 0.1V
Ke KHg 1.6V 在+0. 1~-1.6V之间可以认为该电极是理想极化电极。
第二节 电毛细现象 和双电层微分电容
一、电毛细曲线 1、电毛细现象和电毛细曲线概念
电毛细现象:界面张力σ随电极电位变化的现象。 电毛细曲线:界面张力与电极电位的关系曲线 。
微 分 电 容 曲 线
图4-6滴汞电极在不同浓度氯化钾溶液中的微分电容曲线
微分电容曲线的应用:
利用 判断q正负 ;
研究界面吸附 ; 0
求剩余电荷q、积分电容Ci (从φ0到某一电位φ之间的平均电容称为积分电容
):
积分电容Ci和微分电容Cd的关系:
Ci
o
φ=φ0时q=0:
qCdd积分常数
(2)对紧密层的描述过于粗糙。
上述三种模型的图像如图4.13 图4.13双电层结构模型
波克里斯等人认为,当紧密层与电极表面之间电场强度较大时,紧密层中包含了一层水分 子偶极层,这层水分子在一定程度上定向吸附在电极表面上。图像如图4.14(a) 所示
除了静电力之外,在电极和溶液的界面上还存在非静电力,发生离子或分子在电极上的非 静电的特性吸附。存在特性吸附的双电层结构如图4.14(b)所示。
双电层及其结构模型
➢主要内容:
研究界面电化学的意义,电毛细曲线及双电层电容,双电层结构及理论模型。 ➢ 教学要求: 1.了解研究界面电化学的意义,平板电容器的双电层模型,分散双电层模型。 2.理解电毛细曲线的测定,微分电容法,GCS分散型双电层模型。 3.掌握理想极化电极、零电荷电势的定义,双电层结构。
(2)分散层电位分布:从x=d到剩余电荷为零(溶液中)的双电层部分即为分散层。其电 位分布是非线性变化的。
(3)距离电极表面d处的电位(用ψ1表示) 三种含义: 距离电极表面一个水化离子半径处的平均电位。 表示离子电荷能接近电极表面的最小距离的平均电位。 紧密层与分散层交界处的平均电位。
(4)双电层的微分电容Cd 设整个双电层的电位(用φa表示)设溶液深处的电位为零,可得: 紧密层电位= φa -ψ1;分散层电位= ψ1 双电层电位由紧密层电位差和分散层电位差两部分组成,即φa =( φa - ψ1 )+ ψ1 双电层电容为 :
电极/溶液相间电位或绝对电极电位的零点。
2、零电荷电位的测定
通过测量电毛细曲线,求得与最大界面张力所对应的电极电位值,即为零电荷电位,此 方法比较准确,但只适用于液态金属,如汞、汞齐和融熔态金属
根据稀溶液的微分电容曲线最小值确定φ0,此方法可用于固态金属,溶液越稀,微分电 容最小值越明显。
3、零电荷电位的用途
二、电极/溶液界面的基本结构 电极/溶液界面相间的相互作用: 静电作用(长程力 ):由电极与溶液的两相中的剩余电荷所引起的相互作用 短程力作用 :电极与溶液中各种粒子(离子、溶质分子、溶剂分子等)之间的相互作
用 热运动:两相中的荷电粒子都处于不停的热运动之中 。
